Establecimiento del sistema de generación in vitro de callos de Lupinus mutabilis sweet (tarwi) a partir de hipocótilos
MAMANI, IRMA1 AVERANGA, KATTIA1 ESPINOZA, BORIS1 TERRAZAS, ENRIQUE1✞
1 Instituto de Investigaciones Fármaco-Bioquímicas, Facultad de Ciencias Farmacéuticas y Bioquímicas. Universidad Mayor de San Andrés. Av. Saavedra 2224. La Paz-Bolivia
CORRESPONDENCIA: BORIS ESPINOZA AEDOSP58@HOTMAIL.COM
FECHA DE RECEPCIÓN: 16 DE ABRIL DE 201
FECHA DE ACEPTACIÓN 30 DE JULIO DE 2014
La búsqueda de caminos para el mejoramiento en la producción de leguminosas, nos llevó al estudio de las condiciones optimas para el establecimiento del cultivo in vitro de Lupinus mutabilis Sweet (tarwi), leguminosa cultivada milenariamente en el altiplano boliviano, cuya utilización es mermada por las pobres condiciones tecnológicas existentes para su cultivo, siendo esta planta poco aprovechada, siendo una fuente rica en proteínas para la alimentación humana y animal.
Para tal efecto se trabajo realizando la generación de callos a partir de segmentos de hipocótilos de L. mutabilis Sw. obtenidos asépticamente utilizando combinaciones hormonales de auxinas/citocininas como mediadores de la transformación. El uso de las combinaciones ANA/BAP y 2,4D/ KIN demostraron ser las adecuadas con porcentajes de transformación mayores al 60% en casi todas las concentraciones ensayadas. Nosotros seleccionamos la concentración ANA/BAP a 5/0,25 mg/L para le generación de callos con un rendimiento del 80%. Pero con presencia de oscurecimiento prematuro de los callos generados. El oscurecimiento y envejecimiento se enfrentó con suplementación de antioxidantes (ácido ascórbico, cisteína y AgNO3) y un adsorbente (carbón activado) al medio, siendo el uso de la cisteína a 200 mg/L y el carbón activado 10 g/L los que evitaron notablemente el oscurecimiento de los callos con porcentajes de 24,9%±8,35 y 5,7%±7,19 respectivamente. El uso de antioxidantes en general no afectó el proceso de transformación pero si demostró influir en el desarrollo de los callos.
PALABRAS CLAVE Lupinus, Lupinus mutabilis Sw., hipocótilos, callos, leguminosas, ANA/BAP, 2,4D/ KIN, antioxidantes, adsorbente
Abstract
The research for ways to improve the production of legumes, led us to study the optimum conditions for the establishment of in vitro cultivation of Lupinus mutabilis Sweet (tarwi), ancient grain legume in the Bolivian highlands, whose use is reduced by the poor technological conditions for cultivation, this plant being underutilized, be-ing a rich source of protein for human and animal.
For this, we worked by the genera-tion of callus from hypocotyl segments of L. mutabilis Sw. obtained aseptically using hormonal combinations of auxin/cytoki-nin to mediating the biotransformation. The use of combinations ANA/BAP and 2,4D/ KIN proved adequate transformation with percentages greater than 60% in almost all concentrations tested. We selected the concentration of ANA/BAP 5/0,1 mg/L for the generation of callus with a yield of 80%. But there are premature browning callus generated.
The browning and aging faced with an-tioxidant supplementation (ascorbic acid, cysteine and AgNO3) and an adsorbent (ac-tivated charcoal) in the medium, with the use of cysteine at 200 mg/L and activated charcoal at 10 g/L that prevented notably the browning of callus with percentages of 24,9% ±8,35 and 5,7±7,19 respectively. The use of antioxidants in general did not affect the transformation process but appeared to influence the development of callus.
KEYWORDS Lupinus, Lupinus mutabilis Sw., hipocotyls, callus, legumes, ANA/BAP, 2,4D/KIN, antioxidants, adsorbents.
El consumo de leguminosas es un complemento valioso para las dietas, en regiones donde se tiene un limitado acceso a la proteína animal. Son pocas las poblaciones humanas en cuya dieta no estén presentes (García, 2009). Lupinus mutabilis Sweet llamado tarwi o chocho en la región andina, es una leguminosa que crece en el altiplano boliviano, no necesita mucha agua creciendo bien en clima seco. En Bolivia su producción está en manos de pequeños y medianos productores, con poca tecnificación y desconocimiento de la existencia de variedades mejoradas (Tapia, 2000).
Posee un gran valor nutritivo, con proteínas y aceites que constituyen la mitad de su peso, el tarwi es utilizado para la alimentación humana, como fruto seco o en forma de harinas, sus tallos como combustible por su gran valor calórico (Ortega, et al, 2010),aunque solo es consumido por un área reducida de la población en general (Jacobsen, 2006). Las plantas del género Lupinus son fertilizantes del suelo; al ser plantas que fijan el nitrógeno atmosférico y mejoran su porosidad. Su uso es ideal para el cultivo rotatorio junto al cultivo de cereales (Mullin, et al, 2000).
Gracias a las investigaciones desarrolladas; en nuestros días existen diferentes tecnologías y sistemas, que logran: crecimiento y propagación de plantas con mejoras genéticas, un mejor entendimiento de la mecánica metabóli-ca y hormonal, así como la manipulación y el estudio de las interacciones de las plantas y su ambiente en condiciones controladas (Stewart, 2008).
Varios estudios acerca de la producción de cultivos in vitro y generación de plantas, sobre el género Lupinus se encuentran descritos, desde la inducción de tallos a partir de callos derivados de hipocótilos y embriogénesis somática a partir de cotiledones inmaduros. Junto a la implementación de técnicas de biotransformación mediada por Agrobacterium en busca de sistemas sustentables para la producción de plantas enteras (Ewa, 1987) (Ba-baoglu, et al, 2000); muchas de las especies de leguminosas son difíciles de manipular en cultivo in vitro por ser recalcitrantes, con dificultades para la generación de callos (Bahgat, et al, 2009) y con la liberación de compuestos fe-nólicos que provocan la muerte y el envejecimiento prematuro de los cultivos (Babaoglu, 2000).
El establecimiento de nuevas técnicas y procedimientos para el mejoramiento de la producción de leguminosas tomando como base al Lupinus mu-tabilis Sweet (tarwi), nos llevó a implementar y optimizar un sistema para la generación de callos in vitro a partir de hipocótilos utilizando diferentes combinaciones hormonales de auxinas/citocininas. Establecer el sistema de mantenimiento y desarrollo suplementando los cultivos con agentes adsorbentes (carbón activado) y agentes antioxidantes (ácido ascórbico, cisteína, AgNO3) como coadyuvantes del oscurecimiento y así evitar el envejecimiento prematuro.
Material vegetal
Las Semillas de Lupinus mutabilis Sweet (tarwi) fueron colectadas de la localidad de Carabuco, provincia Camacho del departamento de La Paz, Bo-livia. Semillas sanas y uniformes fueron superficialmente desinfectadas con una solución de etanol al 70% v/v durante 30 segundos, seguido de una inmersión en solución de hipoclorito de sodio al 2,5% v/v con gotas de Tween 20 (2 gotas/1 00mL) por 10 min y luego enjuagados 3 veces con agua destilada estéril. Las semillas fueron secadas sobre papel filtro estéril antes de ser sembrados.
Cultivo de callos
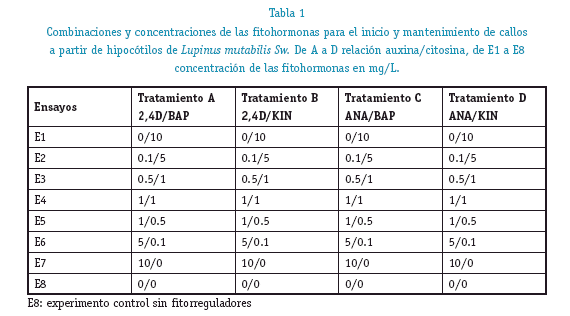
]]> Las semillas esterilizadas son germinadas en frascos de vidrio conteniendo una base de algodón envuelto en gasa y embebidas en 20 mL de agua potable estéril, según protocolo establecido en laboratorios del IIFB (Averanga, 2011). Los segmentos de hipocótilos de 2 a 4 mm de tamaño fueron diseccionados de plántulas estériles in vitro de 2 semanas de edad y utilizados como material inicial para la biotransformación y generación de callos por variación de concentraciones hormonales auxina/citocinina.Los hipocótilos se transfirieron a tubos de ensayo con tapa rosca (30 tubos/concentración/tratamiento) solución inorgánica M&S suplementado con mio-inositol 100 mg/L (Sigma), sacarosa 3% p/v. A este medio se le adicionaron las combinaciones hormonales descritas en la tabla 1. El pH de los medios fue ajustado a 5,8 y se le adicionó agar 0,8 % p/v (Sigma), la esterilización de los medios se realizó en un autoclave (All American 25X) por 15 min a una temperatura de 121 °C. Los tubos se incubaron en una cámara climática a una temperatura de 28 ± 2°C en condiciones de oscuridad completa. El proceso de transformación fue controlado durante 8 semanas de cultivo. Los resultados se expresaron como porcentaje de biotransformación, determinado como el número de tubos que forman callo sobre el número de tubos totales por experimento.
Los experimentos que obtuvieron mayores porcentajes de biotransformación y buenas características morfológicas fueron seleccionados para una segunda prueba, colocando de 10 a 15 segmentos de hipocótilos esta vez en cajas Petri de 12 cm de diámetro, utilizando como medio nutriente el descrito en el screening inicial; suplementado con las combinaciones de auxinas/ citocininas descritas en la Tabla 2. Los experimentos se dejaron crecer en una cámara climática a 28°C ±2 durante 5 semanas. Las pruebas se realizaron por triplicado, los resultados se expresaron en porcentaje de biotransformación.
Hipocótilos de 2 a 5 mm de tamaño se colocaron en cajas Petri con medio M&S suplementado con mio-inositol 100 mg/L, sacarosa 3% p/v y con ácido naftalenacético (ANA) 5 mg/L y 6-bencilaminopurina (BAP) 0,5 mg/ml (combinación hormonal óptima, determinada en los experimentos desarrollados previamente), llevado a pH de 5,8 y agar 0,8% p/v (Sigma). Los medios fueron suplementados con antioxidantes (ácido ascórbico 1 mg/L, cisteína 100 mg/L, nitrato de plata 20 mg/L) y un adsorbente (carbón activado 10 g/L). Para incrementar la firmeza del medio suplementado con carbón activado se incrementó la concentración de agar a 1% p/v con el carbón activado (Abdelwahd, et al, 2008). Los medios fueron llevados a un pH de 5,8 ± 0,1 y esterilizados en una autoclave (ALL AMERICAN).
Todos los experimentos se colocaron en una cámara climática a 28°C ±2 a oscuridad completa, por un periodo de 8 semanas. Las pruebas se realizaron por triplicado, los resultados encontrados se encuentran expresados en términos de porcentaje de transformación y porcentaje de oscurecimiento de los callos.
Características morfológicas
La estructura morfológica, el color y textura de los callos se observó y analizó con ayuda de un estéreo-microscopio NIKON NM30 con 20 aumentos, con lámpara de tungsteno.
Análisis estadístico
]]> Nosotros replicamos los experimentos por tres veces cultivando por placa petri con 10 a 15 segmentos de hipocótilos. Los resultados fueron analizados usando el programa SPSS 15.0 usando como herramientas el análisis de varianza unifactorial (ANOVA) con una significancia del 95%, test de Duncan para la formación de subgrupos homogéneos. Análisis no paramétrico para K muestras independientes (Kruskar Wallis) con una significancia del 95 %.
RESULTADOS Y DISCUSIÓN
Screening inicial
El screening inicial demostró que después de 5 semanas de crecimiento las combinaciones hormonales de auxina/citocinina de ANA/BAPy 2,4D/KIN generaron mejor transformación de los hipocótilos a callos, en todas las combinaciones de concentraciones auxina/citocinina. Un cociente alto de auxinas frente a las citocininas favoreció a la formación de callos con concentraciones de auxinas ANA y 2,4D de 1 y 5 mg/L frente a la de citocininas BAP, KIN de 1, 0,5 y 0,1 mg/L con porcentajes de transformación sobre 60% para ANA/BAP y de 57% para 2,4D/KIN. Ver figura 1.
La morfología de los callos generados en los medios suplementados con ANA/BAP y 2,4D/KIN vistas en el estéreo-microscopio, tuvieron una estructura compacta con crecimiento de las células en forma de racimo. Los callos tuvieron una coloración amarilla a amarillo verdosa hasta la tercera semana, oscureciéndose paulatinamente desde la tercera semana hasta tener una coloración pardo-negruzca a la séptima semana. Ver figura 3.
Diferentes autores han descrito métodos para la generación de cultivos celulares in vitro en diferentes especies de Lupinus (Mullin, 2000) (Nadolska, 1992), en nuestro estudio no todas las combinaciones de fitorreguladores generaron transformación de los hipocótilos de L. mutabilis Sw. Solo la combinaciones de ANA/BAP y 2,4D/KIN con un cociente de auxinas mayor que de las citocininas produjeron la transformación de los hipocótilos a callos; semejante a los estudios de biotransformación y organogénesis realizados sobre cuatro especies de Lupinus: L. albus, L. luteus, L. angustifolius y L mutabi-lis (Pniewski, 2002), y semejante también el uso del 2,4D/KIN a 1/1 mg/L en la embriogénesis a partir de anteras en L. albus (Simioniuc, 2010).
Segunda fase, generación de callos
]]> La generación de callos en las combinaciones hormonales seleccionadas (ANA/BAP 5/0,1 mg/L, 1/0,5 mg/y 2,4D/KIN 1/1 mg/L, 1/0,5 mg/L) no presentaron diferencias durante todo el proceso de crecimiento, teniendo un perfil semejante de desarrollo durante las ocho semanas de seguimiento, llegando a un porcentaje de transformación superior al 60% para la cuarta semana. Los segmentos cultivados en medio control (sin hormonas) generaron callos, más lentamente que los medio suplementados con ANA/BAP y 2,4D/KIN, llegando a igualar los porcentajes de transformación a la octava semana de cultivo (ANOVA; p 0,820) Ver figura 2.La generación de los callos en placas petri (« 75%) produjo rendimientos superiores a los del screening inicial (« 55%) realizado en tubos de ensayo, lo cual demostró la influencia existente del soporte sobre la transformación de los callos. No existieron diferencias significativas en el porcentaje de generación de callos usando ANA/BAP y 2,4D/KIN durante el tiempo de cultivo (ANOVA; p 0,820), pero si se observaron diferencias observables de coloración de los callos generados, siendo los cultivados en medio con ANA/BAP más compactos, de mejor aspecto, coloración amarillenta. Los callos generados en 2,4D/KIN fueron más friables, de coloración amarillenta a amarillento parduzco, con ennegrecimiento prematuro de la superficie en contacto con el medio desde la cuarta semana de cultivo. Ver figura 3.
Los callos generados en el medio control son de coloración blanquecina, crecimiento en forma de roseta, compactos y con la capacidad de capturar agua en su superficie. Estos llegan a generar organogénesis de raíces y tallos cuando se mantienen en el medio durante más de 7 semanas, sin oscurecimiento ni envejecimiento. Ver figura 3.
Seguimiento de la generación de callos de L mutabilis Sw. de cuatro combinaciones hormonales de ANA/BAP y 2,4D/KIN durante 8 semanas de cultivo.
Fue interesante encontrar que los cortes sin exposición a auxinas/citocini-nas generaron callos, lo cual fue reportado también en trabajos previos realizados sobre biotransformación a partir de meristemos apicales, la generación espontánea de callos y posterior organogénesis (Nadolska,1992). Esto demuestra que esta especie tiene este sistema de respuesta frente a daños ocurridos sobre la planta. El oscurecimiento prematuro de los callos fue evidente en todas las concentraciones ensayadas, según otros estudios, esto se atribuye a la presencia de compuestos que promueven la oxidación celular (Zechmann, 2008).
Adsorbente y antioxidantes
La utilización de antioxidantes (ácido ascórbico, cisteína y AgNO3) y un adsorbente (carbón activado) no afectó el proceso de biotransformación para la generación de callos no existiendo diferencias significativas entre los medios con antioxidantes, adsorbente y el medio control (M&S con hormonas) (X2 9,236; p 0,055).Ver tabla 3. Obteniéndose rendimientos semejantes al control después de 4 semanas de cultivo, demostrándonos que estos compuestos no intervienen en el proceso de biotransformación de los cortes.
El oscurecimiento de los callos, en cambio fue significativamente menor (X2 13,90; p 0,08) en el medio suplementado con carbón activado a 10g/L (5,7% ± 7,19) y con cisteína a 100 mg/L (24,9% ± 8,35), pero con un crecimiento reducido de los callos, con diámetros menores a los 10 mm. En cambio los callos generados en los medios suplementados con ácido ascórbico 1 mg/L y en AgNO3 a 20 mg/L tuvieron un oscurecimiento semejante al control (75,60%±1,10), aunque con mayor crecimiento, con diámetros que llegan a los 20 mm después de 4 semanas. Ver tabla 3. La disminución del oscurecimiento de los callos y diferencias en su desarrollo posterior a su biotransformación, demuestran que el carbón activado y la cisteína actúan paralelamente al metabolismo celular, disminuyendo el envejecimiento prematuro en los callos.
]]> Porcentaje de biotransformación de callos de L. mutabilis Sw. en medio M&S suplementado con antioxidantes y adsorbentes.El carbón activado es muy utilizado en cultivo in vitro, dependiendo del tipo de planta pueden tener una actividad inhibitoria o estimulante, y como tal es un gran adsorbente de metabolitos que pueden provocar oxidación en los cultivos (Thomas, 2008). La cisteína en cambio tiende a ser precursor de un agente antioxidante como ser el glutatión, el cual actúa evitando el envejecimiento celular provocado por la presencia de especies reactivas de oxígeno, siendo parte importante en el sistema de protección ascorbato/gluta-tión (Zechmann, 2008).
El uso de antioxidantes y adsorbentes durante la transformación y mantenimiento del cultivo de L. mutabilis Sw, fue estudiado porque su uso mejora la calidad de los cultivos y evita el envejecimiento prematuro in vitro en otras especies de leguminosas (Abdelwald 2008). Su principal utilización es disminuir la mortalidad de los cultivos, evitar el oscurecimiento de los agregados celulares y reducir la probabilidad de alteraciones genéticas causadas por el subcultivo continuo y el estrés durante el proceso de adaptación (Yinghui, 2008).
Siendo muchas especies de leguminosas de difícil cultivo en sistemas in vitro, debido a la generación de compuesto que promueven procesos oxidativos así como productos fenólicos, o especies reactivas de oxigeno (H2O2). Queda comprobado con el presente estudio que el uso de antioxidantes como la cisteína y/o adsorbentes como el carbón activado pueden mejorar el proceso de biotransformación y ayudar en gran medida al mantenimiento de los cultivos en leguminosas tomando como referencia la generación de los cultivos de Lupinus mutabilis (Tarwi) y abriendo así paso a trabajos con otras leguminosas que se cultivan en gran medida en Bolivia.

AGRADECIMIENTOS
Al IRD-Francia por la beca otorgada en la gestión 2008-2009, para la realización de la maestría de Ciencias biológicas y Biomédicas de la UMSA. Al PhD. Enrique Terrazas por el apoyo para realizar esta investigación en el área de Biotecnología Vegetal del Instituto de Investigaciones Fármaco-Bioquímicas de la UMSA.
REFERENCIAS
]]>García, O., Infante, R., Rivera, C. (2009). Las leguminosas, una fuente importante de fibra alimentaria: Una visión en Venezuela. INHRR, 40(1), 57-63. [ Links ]
Tapia, S. (2000). Cultivos andinos subexplo-tados y su aporte en la alimentación. Colombia, FAO. [ Links ]
Ortega, David, E., Rodríguez, A., David, A., Zamora, A. (2010). A characterization properties of lupin (Lupinus mutabilis) seeds grown in the Colombian andean region. Acta Agronómica, 59(1), 111-118. [ Links ]
Jacobsen, S.E., Mujica, A. (2006). Botánica económica de los Andes Centrales: el tarwi (Lupinus mutabilis Sweet.) y sus parientes silvestres. La Paz, Moraes L.P., 458-482. [ Links ]
Mullin, M., Bellio, Spataru, A. (2000). Organogenesis from hypocotyl thin cell layers of Lupinus mutabilis and Lupinus albus. PlantGrowth Regulation, 30,177-83. [ Links ]
Stewart, N. (2008). Plant biotechnology and ge-netics: Principles, Techniques, and Applications. New Jersey, John Wiley & Sons. [ Links ]
Ewa, Sroga, G. (1987). Plant regeneration of two Lupinus spp. from callus cultures via organogenesis. Plant Science, 51, 245-249. [ Links ]
Babaoglu, M., McCabe, M., Power, B., Da-vey, M. (2000). Agrobacterium-media-ted transformation of Lupinus mutabilis L. using shoot apical explants. Acta Phy-siology Plants, 22(2), 111-119. [ Links ]
Bahgat, S., Shabban, O., El-Shihy, O., Light-foot, D., El-Shemy, H. (2009). Establis-hment of the regeneration system for Vicia faba L. Current Issues Molecular Biology, 11(1), 47-54. [ Links ]
Babaoglu, M. (2000). Protoplast isolation in Lupin (Lupinus mutabilis Sweet): deter-mination of optimum explants sources and isolation conditions. Turkish Journal of Botany, 24,177-185. [ Links ]
Averanga, K. (2011). Producción de callos de Lupinus mutabilis Sweet. [Tesina de licenciatura], La Paz, UMSA.
Abdelwahd, R., Hakam, N., Labhilili, M., Udupa, S.M. (2008). Use of an adsorbent and antioxidants to reduce the effects of leached phenolics in in vitro plantlet regeneration of faba bean. African Journal of Biotechnology, 7(8), 997-1002.
Nadolska-Orksyk, A. (1992). Somatic embr-yogenesis of agriculturally important lupin species (Lupinus angustifolius, L. albus and L. mutabilis). Plant Cell, Tissue and Organ Culture, 28,19-25.
Pniewski, T., Kapusta, J., Legocki, A.B. (2002). In vitro micropropagation of four lupin species. Acta Physiologiae Plantarum, 24(4), 417-424.
Simioniuc, D., Burlacu-Arsene, M.C., Mora-riu, A., Lipsa, F. (2010). Induction of the embryogenesis process in anther and microspores cultures at the Lupinus albus species. Lucräri stiintifice, 53, 60-63.
Zechmann, B., Muller, M., Zellnig, G. (2008). Sulfur assimilation and abiotic stress in plants: modified levels of cysteine affect glutathione metabolism in plant cells. Berlin, Springer, 193-206.
Thomas, D. (2008). The role of activated charcoal in plant tissue culture. Biotechnology Advan ces, 26(6), 618-63.
Yinghui, D. (2008). Biological functions of antioxidants in plant transformation. In-Vitro Cellular & Developmental Biology Plant, 44, 149-161.
Czura, A., Pindel, A. (2007). Limitation of callus browning during its development in in vitro cultures of yellow lupin. Zeszyty Problemowe Postepow Nauk Rolni-czych, 522, 449-455.
]]>