MECANISMO MOLECULAR DE LAS ESTATINAS EN EL TRATAMIENTO DE LA ERITROCITOSIS PATOLÓGICA DE ALTURA
MOLECULAR MECHANISM OF STATINS IN THE TREATMENT OF HIGH ALTITUDE PATHOLOGICAL ERYTHROCYTOSIS
Amaru Ricardo, Vera Oscar, Miguez Hortencia, Peñaloza Rosario, Torres Gina, Jeaneth Velarde, Helly Huarachi, Reyna Mamani, Cuevas Heriberto*.
* Unidad de Biología Celular, Departamento de Ciencias Funcionales, Facultad de Medicina, Universidad Mayor de San Andrés, La Paz, Bolivia.
Correspondencia a Ricardo Amaru MD, PD, ACAD: amaru.ricardo@icloud.com
RESUMEN
Introducción
La Eritrocitosis Patológica de Altura es la manifestación hematológica de la Enfermedad Crónica de Altura, por adaptación inadecuada a grandes alturas de genes reguladores de la eritropoyesis. Las estatinas son inhibidores de la vía del mevalonato involucrado en la regulación de la eritropoyesis. El presente trabajo describe los mecanismos moleculares de la inhibición de la eritropoyesis en pacientes con eritrocitosis patológicas.
Material y métodos
Se estudiaron 35 pacientes con eritrocitosis patológicas con radicatorias en las ciudades de La Paz y El Alto (3600 y 4000 msnm respectivamente). Se realizaron Cultivo de células progenitoras hematopoyéticas y Western Blot.
Resultados
]]> Statins induce apoptosis of erythroid progenitors in the cell culture medium. Without the supplement of simvastatin the apoptosis was 12.3% and With simvastatin the apoptosis was 38.4% (p = 0.001). Furthermore statins inhibit the proliferation and differentiation of erythroid progenitors.Conclusiones
Los mecanismos moleculares involucrados en la inhibición de la eritropoyesis son: a) Bloqueo de la isoprenilación de Rho y Ras, b) Inhibición de la fosforilación de Jak-2 y Stat-5, c) inhibición de la glicosilación del EpoR, d) Disminución de colesterol en microdominios de la membrana celular (raft lipid), e) Inducción de apoptosis a través de BCLxL y caspasa 9.
Palabras claves:
Eritrocitosis patológica de altura, enfermedad crónica de altura, estatinas
ABSTRACT
Introduction
The High altitude Pathological Erythrocytosis is the chronic mountain sickness hematologic manifestation by inadequate adaptation to high altitudes of genes regulating erythropoiesis. Statins are inhibitors of the mevalonate pathway involved in the regulation of erythropoiesis. This paper describes the molecular mechanisms of erythropoiesis inhibitionin patients with pathological erythrocytosis.
Material and methods
We studied 35 patients with pathological erythrocytosis from La Paz and El Alto city (3600 and 4000 masl respectively). Were performed hematopoietic progenitor cell culture and Western blotting.
]]> ResultsStatins induce apoptosis in liquid culture medium. without simvastatin erythroid progenitors from apoptosis presentarón and 12.3% in the group supplemented with simvastatin 38.4% apoptosis (p = 0.001), statins also inhibit the proliferation and differentiation of erythroid progenitors, and inhibit transcription of STAT-5.
Conclusions
The molecular mechanisms involved in the erythropoiesis inhibition are: a) Inhibition of Ras and Rho isoprenylation, b) Inhibition of Jak-2 and Stat-5 phosphorylation, c) inhibition of EpoR glycosylation, d) Statins reduce lipid rafts cholesterol and reduce JAK2 localization to lipid rafts, e) Induction of apoptosis through caspase 9 and BclxL.
Keywords:
Pathological Erythrocytosis, Chronic mountain sickness, statins
INTRODUCCIÓN
La Eritrocitosis Patológica de Altura (EPA) es la manifestación hematológica de la Enfermedad Crónica de Altura (enfermedad de Monge), caracterizado por el aumento de número de eritrocitos, hemoglobina y hematocrito, de etiología genética por adaptación inadecuada a grandes alturas de un grupo de genes comprometidos en la eritropoyesis 1,2.
]]> La Hidroxi-Metil-Glutaril-Coenzima-A (HMG-CoA) se forma a partir de 3 moléculas de acetil-CoA del citoplasma celular, y se reduce a Mevalonato gracias a la enzima HMG-CoA reductasa. El mevalonato es el precursor clave de la vía metabólica cuyos productos finales son el colesterol, dolicol, ubiquinona e isoprenoides. La HMG-CoA reductasa es una de las enzimas más regulables y determinantes de la velocidad de la biosíntesis de la vía del mevalonato, ubicada en el reticulo endoplásmico 3,4. Las estatinas son inhibidores de la enzima HMG-CoA reductasa que bloquean o disminución la velocidad de la vía del mevalonato y sus productos finales. Existen evidencias experimentales que sugieren que los productos finales de la vía del mevalonato están involucrados en la regulación de la proliferación celular, apoptosis celular 5 y la diferenciación de la eritropoyesis 6.Estudios clínicos en el tratamiento de la EPA con atorvastatina mostraron eficacia en la disminución de la hemoglobina, en el control del síndrome de hiperviscosidad sanguínea y probablemente las complicaciones que producen las eritrocitosis patológicas.
El presente trabajo intenta explicar los mecanismos moleculares de las estatinas en la inhibición de la eritropoyesis, útil en el tratamiento de la eritrocitosis patológica.
MATERIAL Y MÉTODOS
Pacientes
Se estudiaron 10 sujetos varones como Controles Normales (CN) y 10 varones con Eritrocitosis Patológica de Altura (EPA), 10 varones con Eritrocitosis Secundaria (ES) y 5 pacientes con Polictemia Vera (PV), todos con radicatorias en las ciudades de La Paz y El Alto a 3600 y 4000 msnm respectivamente. Las muestras de aspirado de médula ósea y sangre venosa periférica fueron tomadas previo consentimiento informado.
Cultivo de células progenitoras hematopoyéticas (CPH) en medio líquido
Las CPH se obtuvieron a partir del aspirado de médula ósea con centrifugación y gradiente de densidad, fueron identificaron en citometría de flujo con anti-CD34 y la viabilidad celular se determinó con azul de cresilo. Fueron cuantificados con método manual y automatizado. Se cultivaron 1x106 cel/ml a 37°C al 5% de CO2 durante 72 horas en una estufa de CO2 (Binder GMBH, Germany). Los cultivos se realizaron en placas de poliestireno de 24 pocillos (Cellstar greiner Bio-one USA) en RPMI 1640 con suero fetal bovino 10%, L-glutamina 2mM, estreptomicina 50Ug/ml, penicilina 50UI/ml y neomicina 1000Ug/ml. Los cultivos fueron suplementados unos con rHuEpo 2 UI/ml (Hemax, SIDUS) y otros con rHuEPO 2 UI/ml asociado a simvastatina 300 ng/ml (Merk Sharp Dohm, France). La apoptosis celular se determinó mediante el Kit de Apoptosis (Becton Dickinson, Pharmigen, USA) con anti-CD235a, Anexina V-PE y 7AAD. La evaluación se realizó por citometría de flujo con FACScan (Becton Dickinson, USA) y el software Cell Quest Pro 4.0 (Becton Dickinson, USA).
Cultivo de células progenitoras hematopoyéticas en medio semisólido
]]> Fueron cultivados 2x105cel/ml de CPH en cajas petri de 33 mm con grilla de acuerdo al siguiente protocolo: 1 ml de Metilcelulosa(Metho Cult H4230Without Epo, stemCell Technologies, Canada), penicilina 250 UI/ml y estreptomicina 50ug/ml. Fueron suplementados unos con rHuEpo 2 UI/ml (Hemax, SIDUS) y otros con rHuEPO 2 UI/ml asociado a simvastatina 300 ng/ml (Merk Sharp Dohm, France). El cultivo fue realizado a 37°C y 5% CO2. La lectura de las colonias BFU-E se realizó de acuerdo a criterios estandarizados a los 14 días de cultivoWestern Blot
Fueron cultivadas 1x106 células mononucleadas en RPMI1640, con L-Glutamina, penicilina, Estreptomicina, Neomicina, Suero Fetal Bovino, hrEpo 2 UI y simvastatina 0, 5, 50 y 250 μM. El cultivo se realizó en duplicado en placas CCW (Corning Cell Well) a 37°C y 5% de CO2 por 48 y 72 horas. Las células fueron lavadas en PBS y centrifugandas a 4500 rpm 10 min; se agregó 100 ml de M-PERM (Mammalian Protein Extraction Reagent) con 1 ul de HPPI (Halt Protease and Phosphatase Inhibitor Cocktail, EDTA free) por cada 1x106 células; se mezcló y centrifugó a 13000 rpm por 15 min a 4°C, el sobrenadante se transfirió a otro tubo y conservada a -80°. La concentración de proteínas se realizó con el método Bradford de Bio-Rad y leidas a 595 nm en un equipo TECAN, y separadas por electroforesis en gel de poliacrilamida con tampón Tris-Glicina-SDS, y electrotransferidas a la membrana PVDF (Polyvinylidene difluoride) con tampón Tris-Glicina-SDS-Metanol en BIO RAD Mini-PROTEAN Tetra System; luego la membrana fue bloqueada e incubada por 24 h a 4 °C con Anticuerpos primarios Actin (C-11) Goat Polyclonal IgG 200 ug/ul, Stat 5 Fosforilado (c-17) rabbit policlonal Ig G 200 Ug/ml y Jak 2 Fosforilado Rabbit mAb. Se lavó la membrana con tampón TBST y se incubó por 2 h con los Anticuerpos secundarios Bovine anti-goat IgG-HRP 200 ug/05 ml y Bovine anti-rabbit IgG-HRP 200ug/05ml. Se lavó la membrana con tampón TBST y se incubó con el sustrato Super Signal West pico Luminol Enhancer Solution y Super Signal West pico-Stable peroxide solution. Finalmente las fracciones se hicieron visibles por Autoradiografía, utilizado Film KODAK Biomax XAR, revelador y fijador KODAK GBX.
RESULTADOS
Las estatinas inducen la apoptosis de CPH
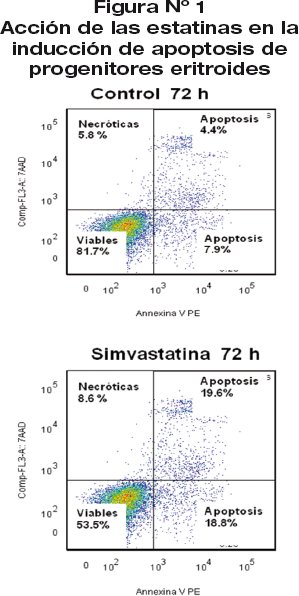
Para evaluar la acción de la estatinas en la inducción de la apoptosis de CPH, que proliferan y diferencian en presencia de eritropoyetina, los medios de cultivo celular líquido y semisólido fueron suplementadas a diferentes concentraciones de simvastatina, como inhibidor de la HMG-CoA-reductasa, en presencia de suero fetal bobino y eritropoyetina como factores de supervivencia. En medio de cultivo líquido los progenitores eritroides sin simvastatina presentarón 12.3% de apoptosis y el grupo suplementado con simvastina 38.4% de apoptosis, estadísticamente diferente (p:0.001) figura 1.

Las células progenitoras hematopoyéticas (CPH) de médula ósea de 10 pacientes con EPA fueron cultivadas en medio líquido con suplementos de Eritropoyetina y eritropoyetina más simvastatina. La valoración de células se realizó a las 72 horas. Las diferencias de apoptosis con y sin simvastatina son estadísticamente diferentes (p=0.0001).
]]> Las estatinas inhiben la proliferación de progenitores eritroidesLos progenitores eritroides suplementados con simvastatina en medio de metilcelulosa inhibe la proliferación de BFU-E en CN 51.2% (de 213 a 104 BFU-E), EPA 47.3% (de 334 a 176 BFU-E), ES 33.2% (de 368 a 246 BFU-E) y PV 62.1% (de 367 a 139 BFU-E) figura 2.
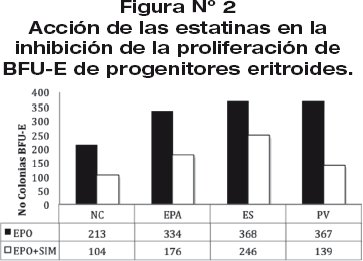
Las CPH de médula ósea fueron cultivadas en medio semisólidos con suplementos de Eritropoyetina y eritropoyetina más simvastatina. La valoración de los BFU-E se realizó al día 14. El estudio se realizó en 10 casos de control normal (NC), 10 Eritrocitosis Patológica de Altura (EPA), 510 Eritrositosis Secundaria (ES) y 5 casos de Policitemia Vera (PV).
Las estatinas inhiben la diferenciación de progenitores eritroides
Los progenitores eritroides suplementados con simvastatina en medio de metilcelulosa presentan colonias BFU-E de características pequeñas y disminución de hemoglobinización. Figura 3.

Colonias de BFU-E observadas a los 14 días de cultivo con y sin simvastatina. La colonia BFU-E presenta hemoglobinización y tamaño de acuerdo a lo esperado; mientras, que la colonia con simvastatina no presenta hemoglobinización y el tamaño de la colonia esta disminuida.
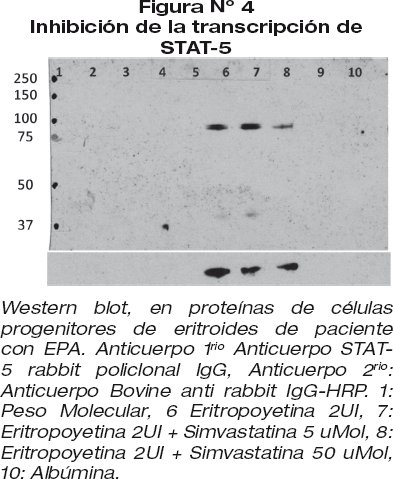
]]> Las estatinas inhiben la transcripción de STAT-5Las simvastina disminuye la transcripción de STAT-5 en medio de cultivo suplementado con 5, 50 y 250 uMol de simvastatina. Figura 4.
DISCUSIÓN
El tejido hematopoyético requiere la presencia de células progenitoras hematopoyéticas (CPH) pluripotentes con capacidad de autorenovación y diferenciación para asegurar una producción continua de nuevas células necesarias para reemplazar elementos sanguíneos maduros. En la eritropoyesis las CPH presentan diferenciación progresiva hasta eritrocitos maduros. Los pasos implicados en este proceso de diferenciación son complejos, desde CFU-Mix (Colony-Forming Unit-Mix), luego BFU-E (Burst-Forming Unit- Erythroid) y CFU-E (Colony-Forming Unit- Erythroid) y finalmente las células eritroides morfológicamente reconocibles en la médula ósea (proeritroblastos, eritroblastos, reticulocitos y eritrocitos). Durante la diferenciación las células presentan receptores de la eritropoyetina (EpoR) y se hacen sensibles a la eritropoyetina (Epo) 6,7.
Las estatinas son inhibidores de la HMG-CoA reductasa, cuyo objetivo es la inhibición de la síntesis endógena del Colesterol; pero, además tiene acciones pleiotropicas que intervienen en la proliferación, diferenciación y apoptosis de las células 19. Varios autores han demostrado que las estatinas inhiben la eritropoyesis en modelos celulares 8,9, y las principales vías moleculares comprometidas de acuerdo a nuestro trabajo y otras publicaciones son las siguientes:
a) Bloqueo de la isoprenilación de las proteínas Rho y Ras.
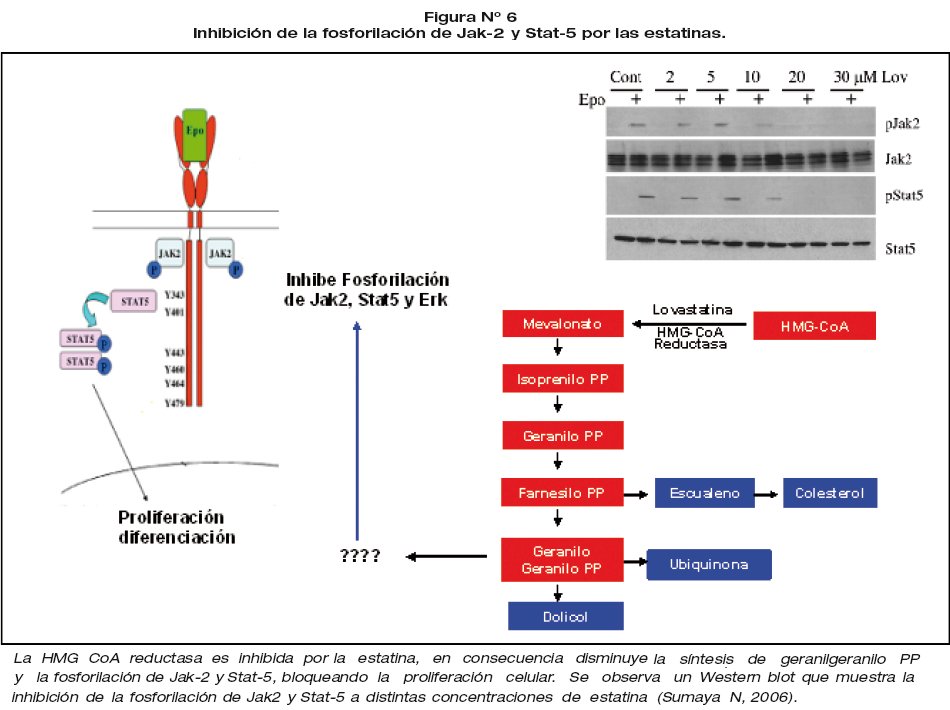
b) Inhibición de la fosforilación de Jak-2 y Stat-5.
]]> c) Inhibición de la glicosilación de la EpoR.d) Disminución de la concentración del colesterol en microdominios de la membrana celular (raft lipid).
e) Inducción de apoptosis a través de BCLxL y caspasa 9.
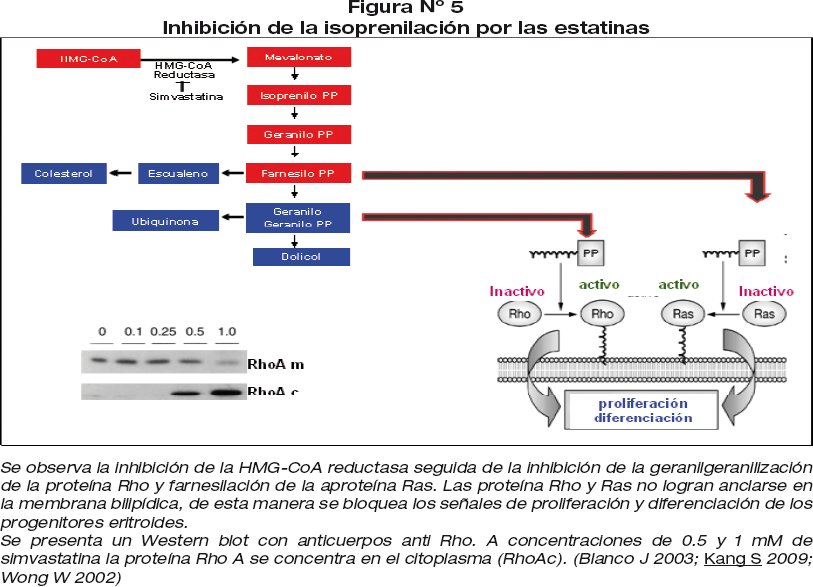
a) Las estatinas al inhibir la enzima HMG-CoA reductasa bloquean la vía del mevalonato y de este modo evitan la isoprenilación de las proteínas Rho y Ras. La proteína Rho se isoprenila con el geranilgeranilo y la proteína Ras con el farnesilo. La proteína Rho sin geranilgeranilo y la proteína Ras sin farnesilo se inactivan y no logran anclarse en la membrana bilipídica y se acumulan en el citosol, de esta manera se bloquean los señales de proliferación y diferenciación de los progenitores eritroides, seguido de la disminución de la eritropoyesis10,11. Geranilgeranilación juega un papel importante en la modificación de proteínas G de la familia Rho, que completan un ciclo entre un estado activo unido a GTP y un estado inactivo unida a GDP. La unión del geranilgeranilo al motivo CAAX en el extremo carboxilo terminal de la pequeña proteína G es importante para la localización de la membrana y por lo tanto, la función biológica. La inhibición de las estatinas en la geranilgeranilización de las proteínas induce la apoptosis en varios tipos de células e inhibe la transducción de señales de la Epo, podría explicar en parte el efecto apoptótico de los progenitores eritroides 9,12,13, también la inhibición de la farnesilación de la protetína Ras bloquea la sobrevivencia de las células 5,14-16. Figura 5.
b) Las estatinas disminuyen la fosforilación de JAK2 y Stat5 seguido del bloqueo de la señal de la eritropoyetina para la proliferación y supervivencia de la serie eritroide. El Stat-5 en ratones knockout sugiere fuertemente que el efecto antiapoptótico de este factor de transcripción en las células eritroides se ejerce a nivel de las células eritroides inmaduras y está mediada principalmente a través de la modulación de Bcl-xL. El Stat5a y Bcl-xL presentan aumento progresivo de la expresión durante la diferenciación de BFU-E de CFU-E, y disminución rápida y marcada en etapas posteriores de la maduración. Es de interés señalar que la deficiencia Stat-5 también induce una muerte prematura de los precursores mieloides, que parece estar relacionado con una disminución de Bcl-2 y Bcl-XL 9,11. Figura 6.
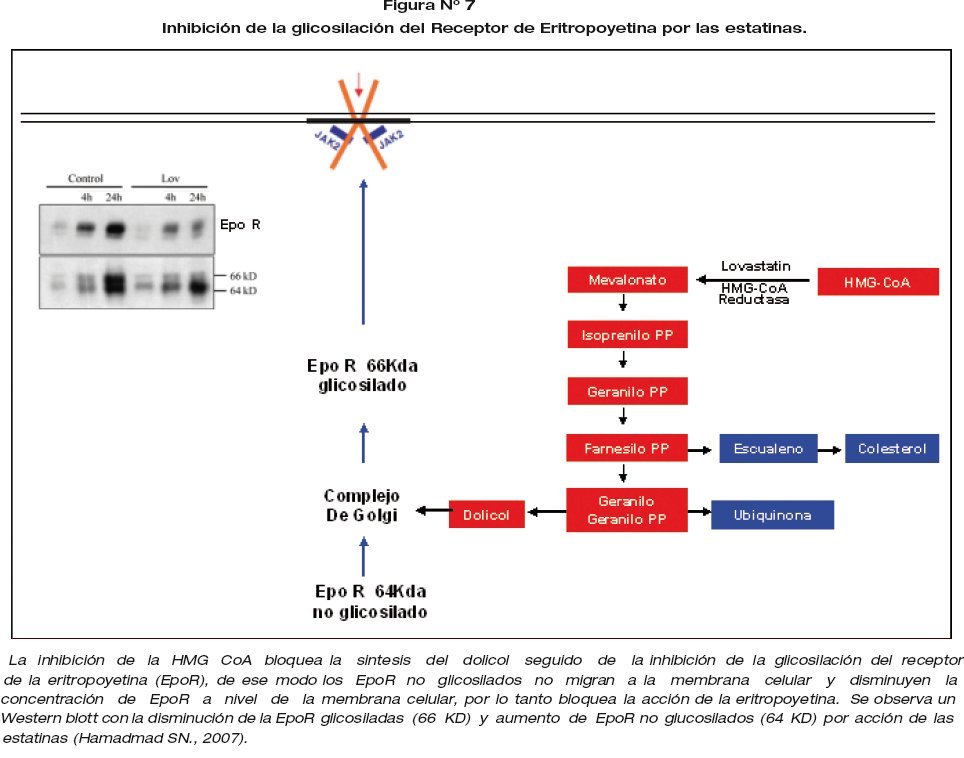
c) La inhibición de la HMG-CoA bloquea la sintesis del dolicol, y sin el dolicol no es posible la glicosilación del receptor de la eritropoyetina (EpoR) y en EpoR no glicosilado no migran a la membrana celular y disminuyen la concentración de EpoR a nivel de la membrana celular, por lo tanto bloquea la acción de la eritropoyetina. La tunicamicina, un inhibidor de glicosilación también suprime parcialmente la expresión de la Epo R en la superficie de la membrana celular de la linea eritroide 17. Figura 7.
]]>
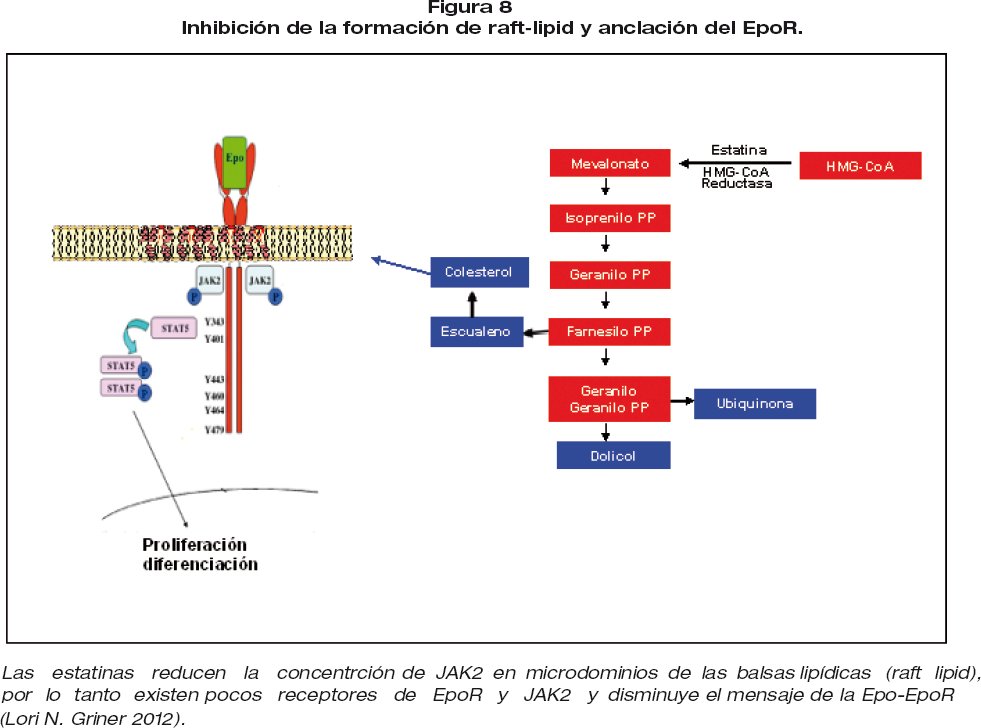
d) Las estatinas inhiben la velocidad de la enzima, HMG-CoA reductasa, en la vía del mevalonato, reduciendo la biosíntesis de colesterol intracitoplasmático seguido de la alteración de las balsas de lípidos (raft lipid) alterando de este modo el anclamiento de EpoR. El EpoR esta en microdominios de membrana celular rica en colesterol y efingolípidos (raft lipid), lo que también podría afectar a la señalización dependiente de JAK2 en las balsas de lípidos y la localización de Jak2. Recientemente han demostrado que la señalización de EpoR/ JAK2 requiere el anclamiento en microdominios 8,17,18. Figura 8.
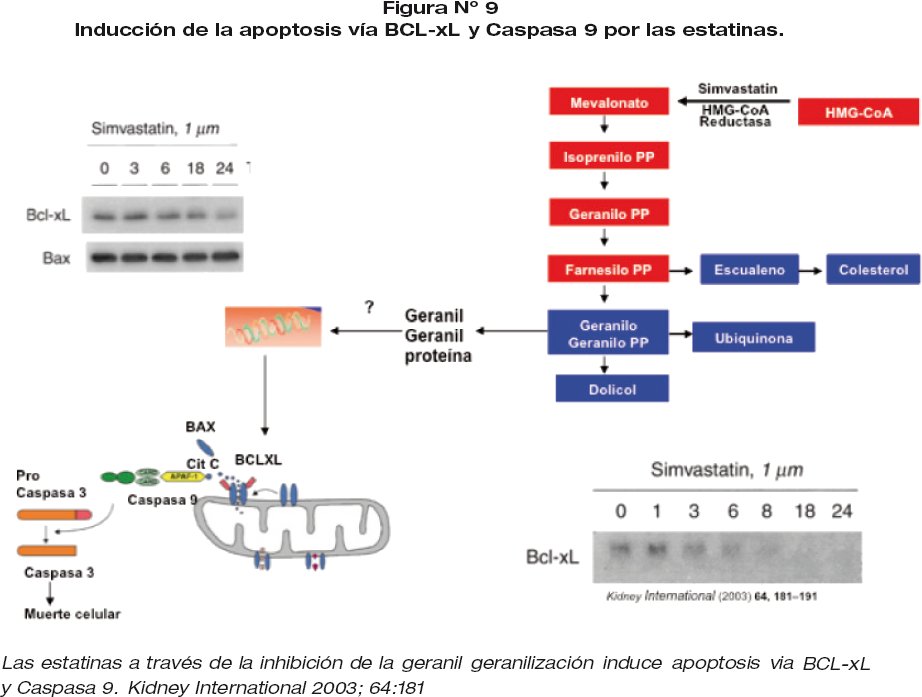
e) Esta demostrada la implicación potencial de Bcl-xL en la apoptosis inducida por inhibidores de la HMG-CoA . Estos resultados pueden estar relacionados con los efectos apoptoticos producidos por la simvastatina en nuestros modelos celulares 9. Figura 9.
Ademas de las vías metabolicas descritas, las estatinas inhiben la eritropoyesis y la maduración de células eritroides a través del sistema Fas/FasL19 y el compromiso de los factores de transcripción TAL1 y GATA1, ambas esenciales para la diferenciación y la supervivencia de la linea eritroide 20. En el futuro nos concentraremos en el gen HIF-1α (hipoxia-inducible factor-1α) un factor clave en la vía de señalización de que media una gama compleja y pleiotrópicos de las respuestas de adaptación a la hipoxia, la eritropoyesis, la supervivencia celular y la apoptosis21.
]]>REFERENCIAS
1. Amaru R. Eritrocitosis Patológica de Altura: Caracterización, diagnóstico y tratamiento. Revista Cuadernos. 2013;1-12. [ Links ]
2. TS S, Y Y, CD H, et al. Genetic Evidence for High-Altitude Adaptation in Tibet. Science. 2010 Jul 2; 329(5987):72-5. 2010;1-4. [ Links ]
3. Murray R BDBK. Bioquímica de Harper. 28 edición. McGraw-Hill Interamericana. 2010;224-233. [ Links ]
4. The 3-hydroxy-3-methylglutaryl coenzyme-A (HMG-CoA) reductases. 2004;1-7.
5. Wong WWL, Dimitroulakos J, Minden MD, Penn LZ. HMG-CoA reductase inhibitors and the malignant cell: the statin family of drugs as triggers of tumor-specific apoptosis. Leukemia. 2002;16(4):508-519. [ Links ]
6. Dzierzak E, Philipsen S. Erythropoiesis: development and differentiation. Cold Spring Harb Perspect Med. 2013;3(4):1-17. [ Links ]
7. Rossert J, Eckardt KU. Erythropoietin receptors: their role beyond erythropoiesis. Nephrology Dialysis Transplantation. 2005;20(6):1025-1028. [ Links ]
8. Griner LN, McGraw KL, Johnson JO, List AF, Reuther GW. JAK2-V617F-mediated signalling is dependent on lipid rafts and statins inhibit JAK2-V617F-dependent cell growth. Br J Haematol. 2012;160(2):177-187. [ Links ]
9. LM B, P J, I D, J LCE. Bcl-xL overexpression protects from apoptosis induced by HMG-CoA reductase inhibitors in murine tubular cells. Kidney International. 2003;1-11.
10. Weber MS, Prod'homme T, Steinman L, Zamvil SS. Drug Insight: using statins to treat neuroinflammatory disease. Nat Clin Pract Neurol. 2005;1(2):106-112. [ Links ]
11. Hamadmad SN, Henry MK, Hohl RJ. Erythropoietin receptor signal transduction requires protein geranylgeranylation. J. Pharmacol. Exp. Ther. 2006;316(1):403-409. [ Links ]
12. WiemerAJ, Hohl RJ, Wiemer DF. The intermediate enzymes ofisoprenoid metabolism as anticancer targets. Anticancer Agents Med Chem. 2009;9(5):526-542. [ Links ]
13. Wiemer AJ, Wiemer DF, Hohl RJ. Geranylgeranyl diphosphate synthase: an emerging therapeutic target. Clin. Pharmacol. Ther. 2011 ;90(6):804-812. [ Links ]
14. Clinical cancer research: an official journal of the American Association for Cancer Research.
15. Kang S, Kim E-S, Moon A. Simvastatin and lovastatin inhibit breast cell invasion induced by H-Ras. Oncol. Rep. 2009;21(5):1317-1322. [ Links ]
16. Ghittoni R, Patrussi L, Pirozzi K, et al. Simvastatin inhibits T-cell activation by selectively impairing the function of Ras superfamily GTPases. FASEB J. 2005;19(6):605-607. [ Links ]
17. Hamadmad SN, Hohl RJ. Lovastatin suppresses erythropoietin receptorsurface expression through dual inhibition of glycosylation and geranylgeranylation. Biochem. Pharmacol. 2007;74(4):590-600. [ Links ]
18. Allen JAJ, Halverson-Tamboli RAR, Rasenick MMM. Lipid raft microdomains and neurotransmitter signalling. Nat Rev Neurosci. 2007;8(2):128-140. [ Links ]
19. Testa U. Apoptotic mechanisms in the control of erythropoiesis. Leukemia. 2004;18(7):1176-1199. [ Links ]
20. Coletti D, Yang E, Marazzi G, Sassoon D. TNFalpha inhibits skeletal myogenesis through a PW1-dependent pathway by recruitment of caspase pathways. EMBO J. 2002;21(4):631-642. [ Links ]
21. Ben Lassoued A, Beaufils N, Dales J-P, Gabert J. Hypoxia-inducible factor-1α as prognostic marker. Expert Opin Med Diagn. 2013;7(1):53-70. [ Links ]
]]>