Electrochemical behaviour of anti-cancer drug carboplatin and interactions with nitrogenous bases on gold electrode
Comportamiento electroquímico de la droga anticancer carboplatin y sus interacciones con las bases nitrogenadas sobre el electrodo de oro en condiciones fisiológicas.
Blas P. Puma-Caparó*1,
Carmen A. Vega-Olivencia2
1 Departamento de Química, Laboratorio de Bioquímica, Universidad Nacional de San Antonio Abad del Cusco, Apartado postal Ne 921, Tel. 5184-224831 anexo1220, Cusco-Perú. quimblas@hotmail.com ]]>
Abstract
The electrochemical behavior results of anticancer Carboplatin (CBDCA) and interactions with adenine, guanine, cytosine and thymine (BASES), allowed knowing the formation of strong bonds between CBDCA, adenine and guanine. These bonds stop DNA replication in cancer cells. The study was carried out by cyclic voltammetry BAS 50W model on a gold electrode at pH = 7,4 and Proton Nuclear Magnetic Resonance 1H-NMR. The Free CBDCA voltammogram showed an oxidation signal on + 685,5 mV and CBDCA-BASES adducts showed a displacement and disappearance of the CBDCA oxidation signal.
Keywords: Carboplatin, Nitrogenous bases, Gold electrode, Adducts.
Resumen
Los resultados del comportamiento electroquímico del anticáncer carboplatino (CBDCA) e interacciones con adenina, guanina, citosina y timina (BASES), permitieron conocer la formación de enlaces fuertes entre CBDCA, adenina y guanina. Estos enlaces detienen la replicación del DNA en células cancerosas. El estudio se llevó a cabo con voltametría cíclica modelo BAS 50W sobre el electrodo de oro a un pH=7,4 y Resonancia Magnética Nuclear de Protón,1H-NMR. El voltamograma de CBDCA libre mostró una señal de oxidación en + 685,5 mV y los aductos CBDCA-BASES mostraron desplazamiento y desaparición de la señal de oxidación del CBDCA.
]]>
INTRODUCCION
Muchos estudios demostraron el interés en la síntesis de los medicamentos anticáncer en cuyas estructuras está presente el platino, el cisplatino, Cis-diaminodicloro platino (II), y carboplatino, Cis-diamino (1,1-ciclobutanodicarboxilato) platino (II), abreviado como CBDCA, ambos utilizados para aliviar ciertos tipos de cáncer [1-4]. Estos medicamentos en los pacientes interaccionan con las bases nitrogenadas del ácido desoxirribonucleico (DNA) [5,6]. Después del descubrimiento de la actividad biológica de los complejos de platino por Rosenberg en 1969, se han realizado muchas investigaciones con diferentes complejos de platino para el tratamiento del cáncer [7,13]. El cisplatino es el más utilizado en el tratamiento contra el cáncer en los ovarios, testículos, seno, colon, etc. pero genera ciertas limitaciones en su actividad [7-10].
El carboplatino CBCCA ha demostrado detener el crecimiento de las células infectadas eficientemente, con menos efectos secundarios que el cisplatino [11-14]. En la célula el cisplatino se hidroliza fácilmente perdiendo sus dos iones de cloro y luego interacciona inmediatamente con el DNA. Mientras el Carboplatino demora en hidrolizarse aproximadamente 14 días para interaccionar con las bases del DNA. [13,15]. En 1982 muchos investigadores manifestaron que los complejos de platino tienen mayor preferencia de formar aductos con guanina
mediante el N-7 [2,4]. El CBCCA tiene mayor importancia porque produce menos efectos adversos, por su fácil administración por vía oral y bajo costo [2,8,15]. Un experimento in vivo demostró la reducción de los complejos del platino (IV) en platino (II), el cual interacciona con las bases del DNA, ya que en el análisis de plasma y orina de pacientes que estaban bajo tratamiento con los medicamentos del platino (IV) se ha encontrado pequeñas cantidades de compuestos de Platino (II) [9,10].
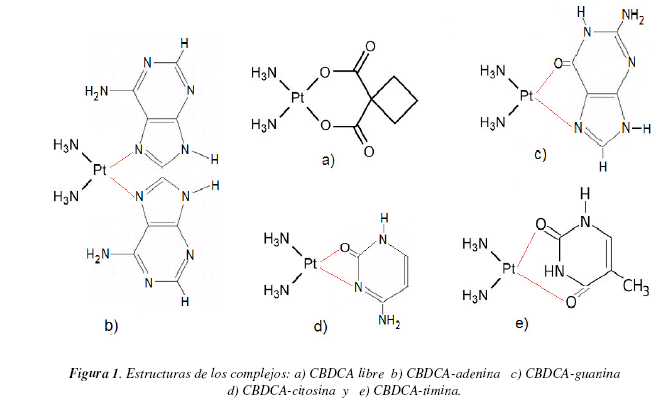
En este trabajo se estudió el comportamiento electroquímico del carboplatino e interacciones con bases nitrogenadas sobre electrodo de oro en condiciones fisiológicas a pH 7.4, utilizando voltametría cíclica modelo BAS 50W y 1HNMR [3,7,9,13]. Ver Figura 1.
RESULTADOS Y DISCUSION
Resultados de voltametría cíclica
]]> Los resultados de voltametría cíclica para la solución de CBDCA en solución amortiguadora muestran una señal de oxidación en 685,5 (±2,5) mV, con una corriente de 8,94 (±0,06)Interacciones de CBDCA y las bases nitrogenadas a una razón de 1:1
Como se muestra los resultados en la tabla 1 y los voltamogramas en la figura 2, la interacción de CBDCA con adenina muestra un cambio en potencial de 110,7 mV y en corriente de 7,51![]() comparando con CBDCA libre, estos cambios son muy significativos e indican una interacción muy fuerte. En este proceso el CBDCA ha perdido sus electrones en una solución homogénea de manera que no le quedan más electrones para ceder al electrodo. La interacción de CBDCA con guanina muestra un cambio en potencial de 62,8 mV y en corriente de 3,97
comparando con CBDCA libre, estos cambios son muy significativos e indican una interacción muy fuerte. En este proceso el CBDCA ha perdido sus electrones en una solución homogénea de manera que no le quedan más electrones para ceder al electrodo. La interacción de CBDCA con guanina muestra un cambio en potencial de 62,8 mV y en corriente de 3,97 ![]() , los cuales indican que existe una interacción fuerte, transfiriéndose los electrones en una solución heterogénea [3, 8, 14]. La interacción con citosina muestra un cambio en potencial de 35,7 mV y en corriente de 2,45 uA, y con timina un cambio en potencial de 4,5 mV y en corriente de 3,41
, los cuales indican que existe una interacción fuerte, transfiriéndose los electrones en una solución heterogénea [3, 8, 14]. La interacción con citosina muestra un cambio en potencial de 35,7 mV y en corriente de 2,45 uA, y con timina un cambio en potencial de 4,5 mV y en corriente de 3,41![]() estos resultados indican una interacción muy débil o no se forma nada. El porcentaje de interacción confirma que la interacción de CBDCA-ADENINA fue de 16% es decir 1,77 veces más fuerte que guanina, 3,2 veces más fuerte que citosina y 22,8 veces más fuerte que timina lo que indica que la droga tiene mayor afinidad por la adenina seguida de guanina [3, 8, 14].
estos resultados indican una interacción muy débil o no se forma nada. El porcentaje de interacción confirma que la interacción de CBDCA-ADENINA fue de 16% es decir 1,77 veces más fuerte que guanina, 3,2 veces más fuerte que citosina y 22,8 veces más fuerte que timina lo que indica que la droga tiene mayor afinidad por la adenina seguida de guanina [3, 8, 14].
Interacciones de CBDCA y bases nitrogenadas a una razón de 2:1
Según los resultados en la tabla 2 y los voltamogramas de la figura 3, la interacción entre CBDCA 4,0 x 10-3 M y adenina 2,0 x 10-3 M muestra un cambio en potencial en 73,5 mV y en corriente de 7.88![]() , lo que indica la formación de un enlace muy fuerte entre CBDCA y ADENINA. En la interacción con guanina también se manifiesta un cambio en potencial en 77,1 mV y en corriente de 0,66
, lo que indica la formación de un enlace muy fuerte entre CBDCA y ADENINA. En la interacción con guanina también se manifiesta un cambio en potencial en 77,1 mV y en corriente de 0,66![]() los cuales revelan la formación de un enlace fuerte.
los cuales revelan la formación de un enlace fuerte.
Interacciones de CBDCA y bases nitrogenadas a una razón de 1:2
]]> Los resultados de estas interacciones se muestran en la tabla 3 y en la figura 4. Los voltamogramas de la interacción de CBDCA 2,0 x 10-3 M con adenina 4,0 x 10-3 M exhiben un incremento de potencial en 65,2 mV en dirección de oxidación y una disminución en corriente en 7,8Resultados de Resonancia Magnética Nuclear de Protón (1H-NMR).
Los resultados de la Resonancia Magnética Nuclear de Protón ('H NMR) confirmaron las interacciones de CBDCA-Adenina, CBDCA-guanina, CBDCA-citosina, y CBDCA-timina [3, 5, 13]
Al comparar los espectros de adenina libre 1,0 x 10-2M con el aducto CBDCA-adenina 1.0 x 10-2 M se observaron deplazamientos químicos de protón hacia campos altos de H(8) y H(2) en ![]() = 0,3836 y 0,3710 ppm respectivamente. Estos desplazamientos indican una hay una interacción muy fuerte entre el CBDCA y adenina.
= 0,3836 y 0,3710 ppm respectivamente. Estos desplazamientos indican una hay una interacción muy fuerte entre el CBDCA y adenina.
El espectro de CBDCA-guanina 1,0 x 10-2 M mostró un desplazamiento químico para el H(8) en ![]() = 0,3276 ppm con respecto a guanina libre 1,0 x 10-2 M lo cual significa una interacción fuerte entre estas especies.
= 0,3276 ppm con respecto a guanina libre 1,0 x 10-2 M lo cual significa una interacción fuerte entre estas especies.
Finalmente, los espectros CBDCA-citosina y CBDCA-timina comparados con espectros de citosina y timina respectivamente no mostraron ningún desplazamiento, lo que indica que la interacción entre estas especies es débil o no existe.
]]> EXPERIMENTAL
El carboplatino (CBDCA) fue adquirido de la industria farmacéutica Brystol-Myers Squibb, en Puerto Rico. Las bases nitrogenadas y el Tris-(hidroximetil) aminometanohidroclorhídrico (Tris-HCl) fueron comprados de Sigma Aldrich Co. El cloruro de sodio (NaCl) de la compañía EM Science. El instrumento utilizado para este estudio fue analizador voltamétrico, modelo BAS 50W de Bioanalytical Systems, Inc. con una celda que contiene tres electrodos: electrodo de trabajo (oro), referencia Ag/AgCl/NaCl (3M), y auxiliar alambre de platino. Todos los potenciales han sido comparados versus Ag/AgCl. El electrodo de trabajo fue pulido con pasta de alúmina 0,05 Lim por 1-2 minutos y enjuagado con agua desionizada antes de cada experimento [3, 8, 9, 14]. El barrido de potenciales para la oxidación del CBDCA fue de +200 mV a +800 mV. Los experimentos en blanco fueron llevados a cabo con soluciones buffer recientemente preparadas los mismos han demostrado su inactividad en esos intervalos de potenciales permitiendo detectar el comportamiento rédox del CBDCA. Para experimentos de Resonancia Magnética Nuclear de protón (1H-NMR) se ha utilizado el espectrómetro modelo BruckerAdvance DRX 500 MHz. Las muestras se disolvieron en solución amortiguadora NaCl10 mM y Tris-HCl 100 mM a pH de 7,4 (ajustadas con NaOH de 3 M) y las medidas se llevaron a cabo por tres veces [6, 7, 15].
Voltametría Cíclica
El comportamiento electroquímico de la solución amortiguadora, bases nitrogenadas, CBDCA libre y complejos CBDCA-BASES se realizaron por voltametría cíclica sobre el electrodo de oro, en condiciones fisiológicas, en un intervalo de potenciales de + 200 mV hasta + 800 mV y a una velocidad de barrido de 100 mV/s. Antes de aplicar potenciales, las soluciones se han purgado con nitrógeno gaseoso de alta pureza (99.99%) por 120 segundos para eliminar el oxígeno presente en la solución. El comportamiento electroquímico de las sustancias se estudiaron en el siguiente orden: Primero, 4,00 mL de la solución amortiguadora 2,0 x 10-3 M a pH fisiológico. Segundo, mezclando 2,00 mL de la solución CBDCA libre 2,0 x 10-3 M con 2,00 mL de la solución amortiguadora 2,0 x 10-3 M, resultando una solución de concentración final de 2,0 x 10-3 M de CBDCA. Tercero, mezclando 2,00 mL de la soluciones bases nitrogenadas 2,0 x 10-3 M con 2,00 mL de la solución amortiguadora 2,0 x 10-3 M. Cuarto, CBDCA interaccionado con las bases nitrogenadas en diferentes proporciones 1:1, 2:1y 1:2CBDCA-BASES.
Espectroscopia de Resonancia Magnética Nuclear de Protón (>H RMN)
Análisis de la solución amortiguadora, carboplatino y las bases nitrogenadas sin inter accionar.
Los resultados electroquímicos de las interacciones del CBDCA y bases nitrogenadas se han confirmado por Resonancia Magnética Nuclear de Protón ('H NMR) modelo Bruker Advance-500 MHz (DRX). Para esta confirmación todas las soluciones se han preparado en agua deuterada (D2O) y se procedió de la siguiente manera: Primero, en un tubo de resonancia se colocó 0,60 mL de la solución amortiguadora a pH 7,4. Segundo, en otro tubo se colocó 0,60 mL de la solución carboplatino 1,0 x 10-2M. Tercero, en cuatro tubos se colocaron 0,60 mL de cada una de las soluciones de bases nitrogenadas.
Análisis de las interacciones de carboplatino con las bases nitrogenadas CBDCA-BASES
Las mezclas de 0,60 mL de carboplatino 1,0 x 10-2 M con 0,60 mL de cada base nitrogenada 1,0 x 10-2 M se han hecho interaccionar por 24 horas. Luego se colocaron en el campo magnético del 'H NMR para irradiar con ondas de radiofrecuencia (RF) de 500 MHz por un segundo.
]]> CONCLUSIONES
Para el Carboplatino libre (CBDCA) se determinó una señal de oxidación en + 685,5 (±2,5) mV y una corriente de 8,94 (±0,06)![]()
Al aplicar potenciales positivos a los aductos CBDCA-ADENINA en diferentes proporciones 1:1, 2:1, 1:2, éstos mostraron un cambio significativo en el potencial y corriente con respecto al CBDCA libre, los cuales indican una interacción muy fuerte entre el CBDCA y dos moléculas de adenina ya que el potencial aplicado fue insuficiente para romper.
Los aductos CBDCA-GUANINA en proporciones 1:1, 2:1 y 1:2 mostraron un cambio en la señal de oxidación y corriente indicando una interacción fuerte entre CBDCA y una molécula de guanina. Los aductos CBDCA-CITOSINA y CBDCA-TIMINA mostraron un cambio no significativo en potencial y corriente lo cual indica una interacción muy débil.
Los resultados de voltametría cíclica se comprobaron con 1H NMR el cual demostró desplazamiento químico hacia los campos altos solo para H(8), ![]() = 0,38 ppm y H(2),
= 0,38 ppm y H(2), ![]() = 0,37 ppm para CBDCA-ADENINA y H(8),
= 0,37 ppm para CBDCA-ADENINA y H(8), ![]() = 0,33 ppm para CBDCA-GUANINA.
= 0,33 ppm para CBDCA-GUANINA.
REFERENCIAS
1. P. Pil, S. J. Lippard, In Encyclopedia of Cancer, Ed. Academic Press: San Diego, CA. 1997,1, 392. [ Links ]
2. J. F. Hartwing, S. J. Lippard, J. Am. Chem. Soc. 1992,114, 5646. [ Links ]
3. V. López, C. A. Vega, M.Cádiz, E. Meléndez, Journal of Electroanalytical Chemistry, 2004, 565, 77. [ Links ]
4. B. R. Martin, Acc. Chem. Res., 1985,18, 32. [ Links ]
5. O. Vrana, V. Brabec, Bioelectrochemistry and Bioenergetics, 1988,19, 145. [ Links ]
6. L.T. Ellis, M. Erhui, T.W. Hambley, Aust. J. Chem., 1995, 48, 793. [ Links ]
7. A. J. Rodríguez, Estudios Electroquímicos de la interacción del Complejo cis- diamino (1,1-ciclobutanodicarboxilato) platino (II) con Bases Nitrogenadas. Tesis para optar el título de Magíster en química, Universidad de Puerto Rico- Recinto Universitario de Mayagüez, 2001. [ Links ]
8. A.J. Bard,L.R. Faulkner. "Electrochemical Methods Fundamentals and Applications". Second Edition. John Willey & Sons, New York, USA, 2001. [ Links ]
9. S.K. Carter. Cisplatin past, present and future. Platinum Coordination Complexes in Cancer Chemotherapy, 1984,17, 359. [ Links ]
10. N. Goswami, L.L. Bennett- Slavin, N. Rathindra. Journal of the Chemical Society, Chemical Engineering Comunication. 1989, 7, 432. [ Links ]
11. G. M. Schmidt, D.R. Atherton, Anal. Chem. 1986. 58, 1956. [ Links ]
12. J. Reedijk,. Why Does Cisplatin Reach Guanine-N7 with Completing S-Donor Ligands Available in the Cell? Chem. Rev. 1999, 2499. [ Links ]
13. N. Chevere,"Estudios Electroquímicos de la interacción del Complejo cis- diamino (1,1-ciclobutanodicarboxilato)-trans-dihidroxoplatino (IV) (CBDCA-OX) con Bases Nitrogenadas". Tesis para optar el título de Magister en Química, Universidad de Puerto Rico-Recinto Universitario de Mayagüez. 2001. [ Links ]
14. S. Choi, C. Filotto, M. Bisanzo, S. Delaney, D. Legasse, A. J. Whitworth et.al. Inorg. Chem. 1998, 37, 2500. [ Links ]
15. M. Becker, R. E. Port, H. J. Zabel, W.J. Zeller, P. Bachert, J. of Magnetic Resonance. 1998,133, 115. [ Links ]
]]>