Economía circular en minería: procesamiento de desmontes como alternativa de remediación ambiental
Circular economy in mining: waste processing as an environmental remediation alternative
*Dr.- Ing. Gerardo Zamora E. **Ing. Walter Blanco Vino - *** Octavio Hinojosa Carrasco
*Docente Carrera de Metalurgia y Ciencia de Materiales Universidad Técnica de Oruro gerardozamoraechenique@yahoo.es
** Investigador de la Carrera de Metalurgia - Walter_blanco_0000@hotmail.com ]]>
*** Director Laboratorio Concentración de Minerales Universidad Técnica de Oruro Ciudad Universitaria Zona Sud Oruro Bolivia octahinojosa@hotmail.com
Artículo recibido en: 21.10.2019 Artículo aceptado: 18.11.2019
Manejado por: Elvis Trujillo
Actualmente, muchas operaciones mineras, en el marco de la economía lineal, han generado grandes volúmenes de desmontes o estériles con bajos contenidos de los metales de interés económico a partir de los yacimientos mineros explotados ya sea a cielo abierto o por explotación subterránea. En el contexto de la economía circular, los sitios de almacenamiento de desmontes generadores de drenaje ácido de roca, pueden ser objeto de tratamiento metalúrgico, con el propósito de recuperar dichos metales de interés económico por procesos hidrometalúrgicos, como una alternativa al cierre ambiental de los mismos; tratando además que, los relaves generados en éstos procesos, sean reutilizados en el cierre de los mismos, permitiendo así, un claro beneficio económico, social y ambiental para la industria minera.
En ese contexto, el presente trabajo de investigación, presenta un estudio de las alternativas de tratamiento de muestras de desmontes de complejos de Pb-Ag-Zn por: Lixiviación cianurante directa por agitación; pretratamiento en medio ácido y en presencia de H2O2 como agente oxidante, y luego del lavado y neutralización, la respectiva cianuración de los residuos; y finalmente, el retratamiento de los mismos mediante oxidación acuosa en medio relativamente ácido y presencia de H2O2 como agente oxidante y NaCl como agente acomplejante; todos ellos con el objetivo de obtener las mayores extracciones de Ag en la lixiviación, pero además, obtener los menores contenidos de sulfuro en los relaves ya sea para su disposición sin medidas ambientales y/o su uso como coberturas secas en la etapa de cierre de los mismos.
Muestras de desmontes con diferentes contenidos de sulfuros, que varían entre 1.0 a 3.4 % de Azufre Total, y con concentraciones de entre 68 a 53 g/t de Ag, fueron sometidos a condiciones normales de cianuración por agitación, obteniéndose extracciones que variaron entre 74 % a 31 %, respectivamente. Sin embargo, después del pretratamiento ácido-oxidante, las extracciones en la etapa posterior de cianuración, subieron de entre 81% y 63%, respectivamente. Finalmente, mediante la lixiviación ácido-clorurante, se lograron extracciones de entre 58 a 98%, respectivamente; obteniéndose además, para muestras con contenidos medios de sulfuros, colas no generadoras de DAR; que en base a su caracterización geotécnica, son también aptas para su uso en forma de coberturas secas en la etapa de cierre ambiental.
Palabras Clave: Economía Circular en Minería Retratamiento Cianuración de desmontes Pretratamiento hidrometalúrgico de desmontes Cianuración de desmontes Lixiviación clorurante
Abstract
]]> Currently, many mining operations, within the framework of the linear economy, have generated large volumes of waste or sterile with low contents of the metals of economic interest from the exploited mining deposits either open pit or underground. In the context of the circular economy, storage sites for rock acid drainage generators can be metallurgically treated, with the purpose of recovering said metals of economic interest by hydrometallurgical processes, as an alternative to the environmental closure of themselves; trying also that, the tailings generated in these processes, be reused in the closing of the same, allowing a clear economic, social and environmental benefit for the mining industry.In this context, the present research paper presents a study of the alternatives of treatment of samples of dismantling of Pb-Ag-Zn complexes by: Direct cyanurant leaching by agitation; pretreatment in acidic medium and in the presence of H2O2 as oxidizing agent, and after washing and neutralization, the respective cyanidation of the residues; and finally, the retreatment thereof by aqueous oxidation in relatively acidic medium and presence of H2O2 as oxidizing agent and NaCl as complexing agent; all of them with the objective of obtaining the greatest extractions of Ag in the leaching, but also, obtaining the lowest sulfur contents in the tailings either for its disposal without environmental measures and / or its use as dry coverings in the closing stage of the same.
Samples of clearings with different sulphide contents, which vary between 1.0 to 3.4% of Total Sulfur, and with concentrations between 68 to 53 g / t of Ag, were subjected to normal conditions of cyanidation by agitation, obtaining extractions that varied between 74 % to 31%, respectively. However, after the acid-oxidant pretreatment, the extractions at the later stage of cyanidation rose from 81% to 63%, respectively. Finally, by acid-chlorurant leaching, extractions of between 58 and 98%, respectively, were achieved; also obtaining, for samples with average sulphide contents, non-DAR tails; which, based on their geotechnical characterization, are also "suitable for use in the form of dry coverings" in the environmental closure stage.
Keywords: Circular Economy in Mining - Retreatment - Cyanuration of waste - Hydrometallurgical pretreatment of waste - Cyanuration of clearings - Chlorident leaching
1. Introducción
Desde décadas anteriores, bajo el sistema de la economía lineal, la minería de complejos Pb-Ag-Zn en el mundo, ha generado y genera grandes volúmenes tanto de desmontes como de relaves que, por su bajo contenido en los metales de interés económico, han sido o van siendo almacenados en el primer caso en botaderos, y en el segundo caso, almacenados en diques de colas, después de haber sido sometidos normalmente a los procesos de beneficio mineral por flotación.
Los sitios de almacenamiento de los residuos mineros arriba señalados, a la conclusión de las operaciones mineras, deben ser objeto de un adecuado cierre ambiental; en especial, si éstos no son estables químicamente; es decir, cuando son generadores de drenajes ácido de roca. Es importante mencionar que, el balance entre el contenido de minerales sulfurosos o acido génicos y los minerales carbonáceos o acidívoros presentes en los residuos mineros generados en la operación minera, permite establecer si éstos en contacto con el agua de las lluvias y el oxígeno del aire, serán o no estables químicamente [1]; y a partir de éste dictamen, en la misma etapa de operación o al finalizar la explotación minera, encaminar las medidas de cierre ambiental respectivas de dichos sitios de disposición final de residuos mineros [2, 3].
]]> Desde la óptica de la aplicación de la filosofía de la economía circular [4], se debería empezar a considerar que, los residuos mineros generados en el sistema de la economía lineal de explotación minera, se pueden hoy en día, constituir en nuevas fuentes de explotación mediante procesos menos costosos y que permitan recuperar los valores metálicos presentes en los mismos, a lo que se converge en designar como revalorización de pasivos mineros.Es además importante señalar que, para que una propuesta de procesamiento metalúrgico tanto de desmontes o colas sea interesante para las empresas mineras, su costo deberá ser menor que el que se va a requerir en su respectivo cierre ambiental. Así, y sólo así, recién se podría hacer entender al sector minero la filosofía de la economía circular y su aplicación, puesto que se enmarca en un claro beneficio económico, social y ambiental.
Los desmontes y las colas, generados en la explotación de las reservas de complejos sulfurados de Pb-Ag-Zn y en el procesamiento mineral por flotación, respectivamente, pueden ser objeto de retratamiento mediante algunas alternativas hidrometalúrgicas; dentro de ellas, la lixiviación por cianuración, a objeto de disolver la plata presente y luego ser recuperada por cementación con Zinc; ésta podría ser una alternativa interesante, siempre y cuando, la presencia de sulfuros en los residuos mineros tratados, no genere consumos excesivos de cianuro. Para el caso de residuos con contenidos mayores de sulfuros, que son conocidos como cianicidas en la cianuración, puede considerarse un proceso de pretratamiento en medio ácido y en presencia de un agente oxidante fuerte, a objeto de primeramente oxidar y disolver los sulfuros; para posteriormente, realizar una lixiviación por cianuración bajo condiciones normales, para disolver los contenidos de Ag presentes y su recuperación también por cementación con Zn. Finalmente, la otra alternativa es que, estos residuos mineros pueden ser sometidos a un proceso de lixiviación por cloruración, utilizando el hipoclorito de sodio como agente oxidante, en presencia de un medio ácido, generado por la misma oxidación de los sulfuros, y de cloruro de sodio, a objeto de que la Ag forme un complejo clorurado estable en el medio acuoso; y finalmente, la Ag pueda ser recuperada por cementación con Fe.
El proceso de cianuración ha sido ampliamente estudiado en las décadas pasadas y su aplicación industrial ha sido y será todavía de gran relevancia en la producción de metales preciosos [5].
El pretramiento de menas refractarias de Au y Ag en medios ácidos y oxidantes, como etapa previa a la cianuración, ha sido también objeto de investigación amplia, y con aplicaciones a nivel industrial [6].
El retratamiento de menas sulfuradas en medio ácido y con el uso del hipoclorito de sodio (NaOCl) como agente oxidante y en presencia de sal (NaCl) como agente acomplejante, ha sido poco estudiado y basa su principio teórico en el hecho de que el NaOCl, mejor conocido como lejía, al hidrolizarse genera dos substancias: El ácido hipocloroso (HOCl) y el hidróxido de sodio (NaOH), mediante un balance dinámico, representado por la reacción siguiente:
![]() (1)
(1)
El ácido hipocloroso formado es un ácido débil.
![]() (2)
(2)
Su estabilidad se presenta a valores de pH inferiores a 7.5, como se muestra en el diagrama de distribución para las especies de cloro en solución acuosa (Figura 11).
]]>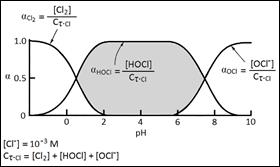
Figura 1. Diagrama de distribución para las especies de cloro en el agua a 25℃. [5]
La tabla siguiente, muestra que tanto de la especie hipoclorosa ![]() como el cloro acuoso
como el cloro acuoso ![]() , son agentes oxidantes fuertes, siendo
, son agentes oxidantes fuertes, siendo ![]() la especie preferida para la oxidación de sulfuros en ambientes no básicos.
la especie preferida para la oxidación de sulfuros en ambientes no básicos.

Tabla 1.- Datos termodinámicos para el cloro a 25℃. [7]
El agente oxidante inicialmente será el ion hipoclorito, que a pesar de ser estable en solución de pH ![]() 10, altamente básico, puede reaccionar con los sulfuros presentes en el medio acuoso:
10, altamente básico, puede reaccionar con los sulfuros presentes en el medio acuoso:
![]()
![]()
De manera que la solución comienza a acidificarse y el ion hipoclorito da lugar a la formación del ácido hipocloroso: ![]()
![]()
Luego continúa reaccionando el ion hipoclorito y da lugar a cloro gaseoso:
![]()
Por lo que mientras transcurre la reacción, ésta se hace más vigorosa y el pH llega a ser lo suficientemente ácido para que puedan lixiviarse los metales de interés económico presentes en los desmontes y relaves:
![]()
![]()
El complejo de Ag formado, es estable de acuerdo al diagrama Eh pH que se presenta a continuación:
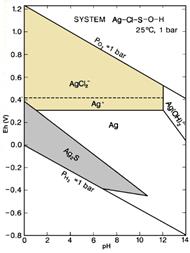
Finalmente, la oxidación especialmente de la pirita presente en los residuos mineros, y bajo las condiciones relativamente ácidas y la presencia del HOCl, permite la formación de ![]() que, por su poder oxidante, también contribuye a la oxidación de los sulfuros.
que, por su poder oxidante, también contribuye a la oxidación de los sulfuros.
2. Materiales y métodos
Cuatro muestras de desmontes, con diferentes contenidos de sulfuros, han sido preparadas de acuerdo al flujograma 1. Las condiciones bajo las cuales se lixiviaron las muestras, se detallan a continuación:
a) Lixiviación por cianuración directa y pretratamiento ácido-oxidante con posterior cianuración
Las muestras preparadas de acuerdo al flujograma 1, fueron sometidas a las siguientes condiciones de lixiviación cianurante directa: pH = 10.5; granulometría 200 # Tyler; 45 % sólidos; 2 g/L de cianuro constante, agitación a 350 rpm y un tiempo de lixiviación de 4 horas.
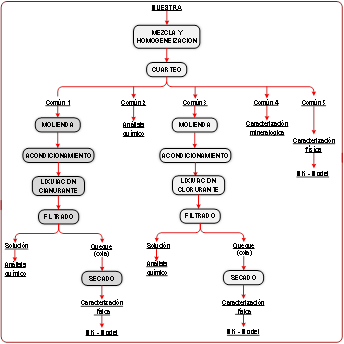
Figura 3. Flujograma de procesamiento de las muestras de desmontes
]]> Por otra parte, las condiciones del pretratamiento ácido-oxidante fueron las siguientes: pH = 1.5; granulometría 200 # Tyler; 45 % sólidos; H2O2 mantenido constante en 1.5 veces el estequiométricamente requerido, calculado con respecto al contenido de S total de la muestra; agitación a 350 rpm y un tiempo de lixiviación de 4 horas. Con la muestra de mayor contenido de sulfuro en su composición química, se estudió además el efecto de las variables granulometría, porcentaje de sólidos y temperatura. La cianuración de los residuos obtenidos en la etapa de pretratamiento, se realizó bajo las condiciones de cianuración arriba señaladas, previa etapa de lavado con agua y neutralización con cal.b) Lixiviación ácida clorurante
Las muestras fueron sometidas a las siguientes condiciones de lixiviación cloruante en medio ácido - oxidante: 6 mL de HCl por cada 100 g de muestra lixiviada (pH entre 3 y 4); Cloro activo 15 g/L (31.5 g/L de NaOCl); cloruro de sodio 200 g/L; granulometría 200 # Tyler; 45 % sólidos; temperatura de 60 °C, agitación a 350 rpm y un tiempo de lixiviación de 2 horas. Con la muestra de mayor contenido de sulfuro en su composición química, se estudió también el efecto de las variables granulometría, porcentaje de sólidos y temperatura.
3. Resultados y discusiones
3.1 Caracterización química y mineralógica de las muestras estudiadas
Se han preparado cuatro muestras de desmontes, cuyo análisis químico se muestra en la tabla siguiente:
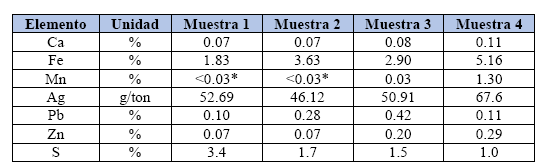
Tabla 2. Análisis químico de las muestras sometidas a las diferentes pruebas de lixiviación
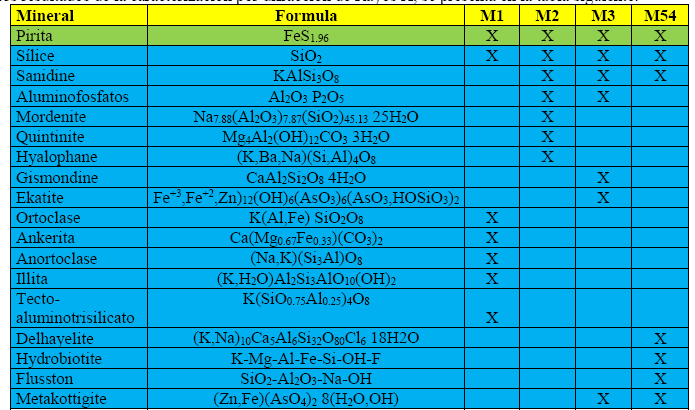
Tabla 3.- Resultado del análisis de difracción de rayos X de las muestras estudiadas
En base a los resultados de la determinación del Potencial Ácido y Potencial Neutro; y a partir de la determinación del Potencial Neto de Neutralización, los residuos mineros estudiados se clasifican en:
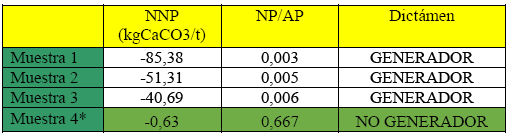
Tabla 4.- Resultado de las pruebas geoquímicas de las muestras estudiadas
* Corroborada mediante prueba geoquímica dinámica
Es decir que, en base a los criterios ABA [1, 8], tres de los sitios donde se han dispuesto los desmontes, requieren de un cierre ambiental, considerando que son generadoras de DAR (no estables químicamente).
3.2 Resultados de la lixiviación cianurante
a) Lixiviación de la muestra M1 con variación de parámetros
]]> Las gráficas siguientes, muestran los resultados obtenidos en la lixiviación por cianuración de la muestra M 1, variando la granulometría de las mismas (- 100, -200 y - 400 mallas Tyler); además de la variación de la concentración de cianuro y el porcentaje de sólidos de lixiviación, denotando también el número de las pruebas ejecutadas:
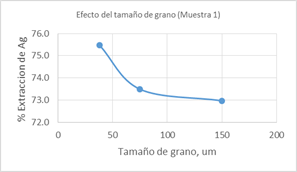
Figura 4.- Efecto del tamaño de grano en la extracción de Ag en la muestra M 1 – P1 a P3
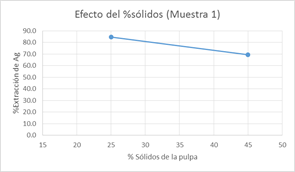
Figura 5.- Efecto del % sólidos en la extracción de Ag en la muestra M 1 P2 y P4
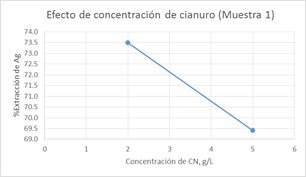
Figura 6.- Efecto del porcentaje de sólidos en la extracción de Ag en la muestra M 1 P2 y P5
b) Lixiviación de las muestras M 2 y M 3
Las condiciones de cianuración para una posible aplicación industrial encontradas en el tratamiento de la muestra M 1, fueron aplicadas a las muestras M 2 y M 3. Las extracciones de Ag que se alcanzaron fueron de 56.59 % (M 3 P6) y de 58.84 % (M 2 P7), respectivamente.
]]> c) Lixiviación de la muestra M 4La gráfica siguiente muestra los resultados obtenidos en la lixiviación cianurante de la Muestra 4, a diferentes granulometrías y bajo las condiciones de cianuración similares a las que se señalaron para la muestra M 3 y M 4:
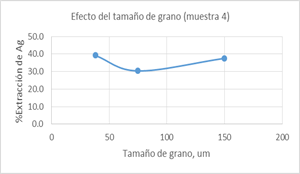
Figura 7. Efecto del tamaño de grano en la extracción de Ag en la muestra M 4 - P8 a P10
3.3 Lixiviación cianurante, con previa etapa de preoxidación en medio ácido-oxidante
a) Pretratamiento y posterior cianuración de la muestra 1
Los resultados obtenidos en la etapa de cianuración, después del pretratamiento respectivo de la muestra 1, permitieron demostrar que la extracción de Ag fue posible de incrementar de 73.49 % (sin pretratamiento P2) a 80.83 % (P 1) con la etapa de pretratamiento, considerando las mismas condiciones de cianuración.
Incrementando el % sólidos en la etapa de pretratamiento de 30 a 45% (P12), se disminuye la extracción de Ag en la etapa de posterior de cianuración de 83.91 % a 80.83 %.
b) Pretratamiento y posterior cianuración de la muestra 4
]]> Los resultados obtenidos en la etapa de cianuración, después del pretratamiento respectivo de la muestra M4, permitieron demostrar que la extracción de Ag fue posible de incrementar significativamente de 39.20 % (sin pretratamiento) a 77.03 % (P 13) con la etapa de pretratamiento, considerando las mismas condiciones de cianuración.Así mismo, incrementando el % sólidos en la etapa de pretratamiento de 30 a 45% (P 14), se disminuye de 77.03 % a 62.37 % la extracción de Ag en la etapa de cianuración.
3.4 Lixiviación de las muestras con Hipoclorito de Sodio
a) Lixiviación de la muestra 1 variando parámetros
La cantidad de sulfuros de la muestra 1, no fue suficiente para generar la suficiente acidez para que el HOCl sea la especie estable en solución; por lo que, fue necesario la adición solución de ácido clorhídrico. Los resultados obtenidos de la variación de la temperatura y del tamaño de grano en la lixiviación de la muestra 1 se presentan a continuación:
![]()
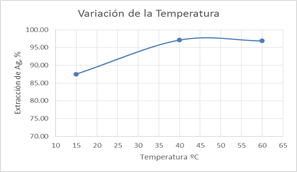
Figura 8. Efecto de la temperatura en la extracción de Ag en la muestra 1 (PC1 a PC3)
![]()
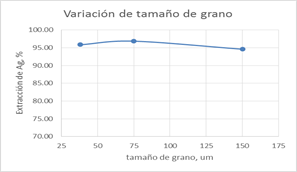
Figura 9. Efecto del tamaño de grano en la extracción de Ag en la muestra (PC4 PC5)
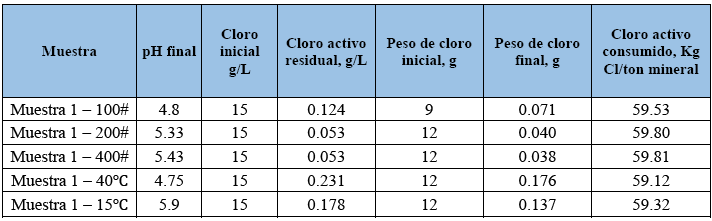
Es decir, a 60 °C, - 200# Tyler y 45% sólidos, consideradas como los mejores parámetros de operación, es posible alcanzar extracciones de Ag de hasta 96.85% de Ag (PC2). Algunos datos adicionales de las pruebas se presentan en la tabla siguiente:
]]>
b) Lixiviación de las muestras 2 y 3 bajo las mejores condiciones obtenidas en la lixiviación de la muestra 1.
Las mejores condiciones encontradas en la lixiviación de la muestra 1 fueron aplicadas a las muestras 2 y 3 para su lixiviación. La extracción de la plata de estas muestras es muy efectiva, alcanzando extracciones de Ag de hasta 83.68% (Muestra 3 PC6) y de 83.35 % (Muestra 2 PC7), respectivamente. Además, en la tabla siguiente, se presentan datos adicionales de las pruebas realizadas:
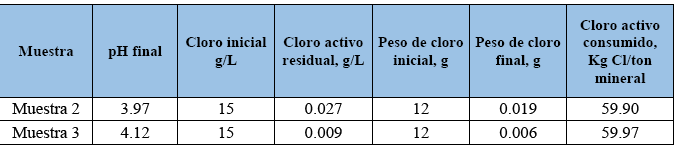
Tabla 6.- pH al final de la lixiviación y cloro activo residual luego de la lixiviación
c) Lixiviación de la muestra 4 con variación de tamaño de grano
Los resultados obtenidos en la lixiviación con Hipoclorito de Sodio de la Muestra 4, con los mejores parámetros obtenidos en la lixiviación de la muestra 1, y variando la granulometría en -100#, -200# y -400# se presenta en la gráfica siguiente:
![]()
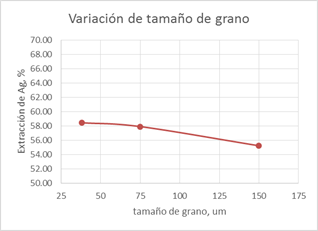
Figura 10. Efecto del tamaño de grano en la extracción de Ag en la muestra 4 (PC8 a PC10).
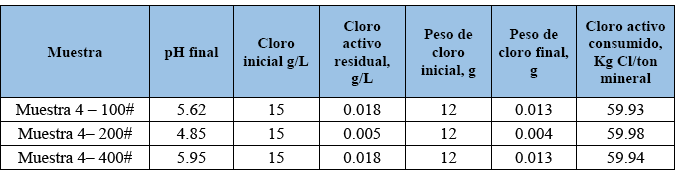
Tabla 7.- pH al final de la lixiviación y cloro activo residual luego de la lixiviación
En resumen, y después de un análisis de los aspectos teóricos de la lixiviación clorurante, se pudo concluir que la lixiviación de plata como sulfuro, que puedan contener las colas, puede ser representada como sigue:
![]()
3.5 Pruebas geoqu ímicas estáticas y aptitud de uso de los residuos generados en la lixiviación en coberturas secas para el futuro cierre
A partir de los análisis químicos reportados por azufre total y sulfato (para determinar el Potencial Ácido) y la determinación del potencial Neutro por el método de titulación inversa; además de la caracterización geotécnica de los residuos obtenidos después del proceso de lixiviación (determinación de los parámetros de granulometría, pesos específicos, densidades aparentes y coeficiente de uniformidad), tanto de la cianuración directa; pretratamiento y cianuración; y finalmente, como de cloruración, se elaboraron las tablas siguientes que resumen si dichos residuos obtenidos por una parte son o no generadores de DAR y por otra, si son o no aptos para su uso como coberturas secas.
a) Predicción del comportamiento geoquímico de los residuos obtenidos en la cloruración y cianuración
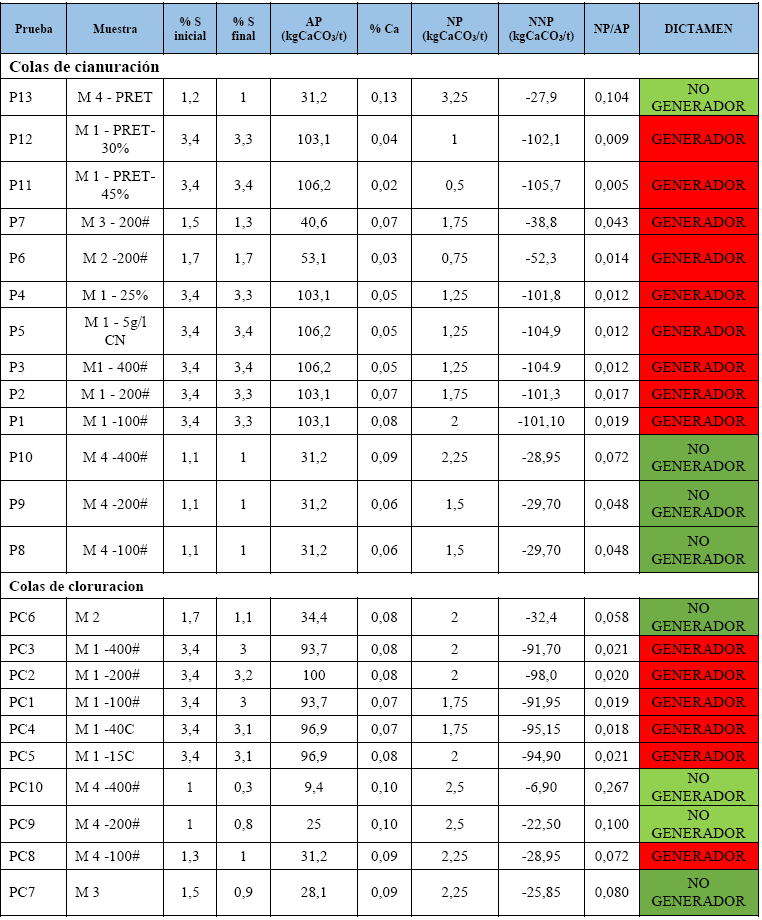
Tabla 8.- Resultados del comportamiento geoquímico estático y dinámico de los residuos obtenidos en las pruebas de cianuración (sin y con pretatamiento) y cloruración
b) Aptitud de uso de los residuos obtenidos en la cianuración y cloruración
De los resultados para establecer la aptitud de uso, basados en sus propiedades geotécnicas de los residuos obtenidos en las pruebas de lixiviación realizadas, es posible establecer que:
La lixiviación de la muestra de desmonte M1, por cualquiera de las alternativas propuestas, genera residuos con valores de AEV (capacidad de almacenamiento de agua) mayores a 1000 cm y conductividades hidráulicas pequeñas; es decir, se establece que dichos residuos pueden ser utilizados como coberturas secas en zonas semiáridas para el cierre ambiental de los mismos; sin embargo, como son residuos generadores de DAR, esta posibilidad queda descartada.La lixiviación de las muestras de desmontes M 2 y M 3, permite obtener residuos, por cualquiera de las alternativas de lixiviación estudiadas, que pueden ser utilizados como cobertura seca en la etapa de cierre.
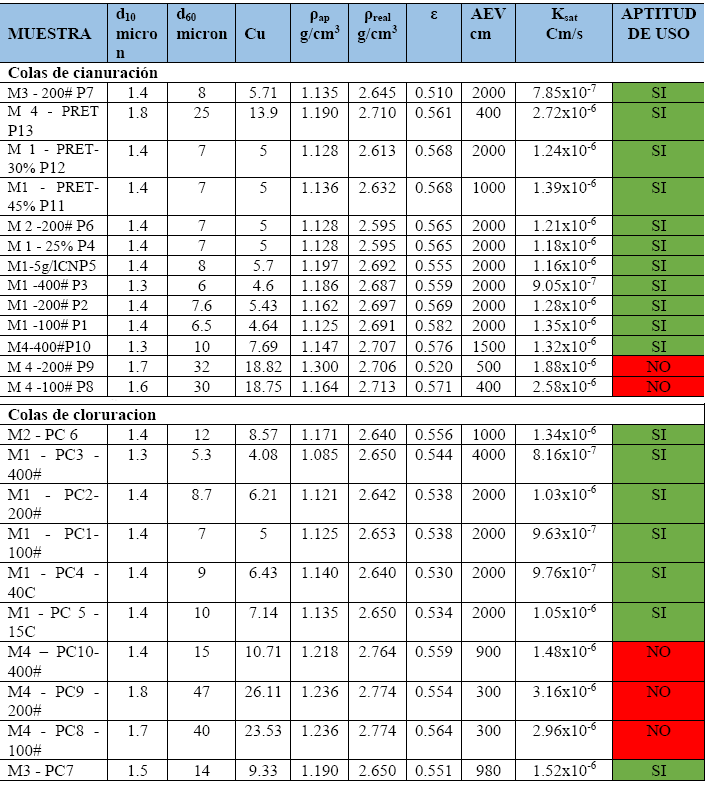
Tabla 9.- Resultados de aptitud de uso de los residuos obtenidos en las pruebas de cianuración (sin y con pretatamiento) y cloruración para su uso como coberturas secas.
4. Conclusiones
Del presente trabajo de investigación se establecen las siguientes conclusiones:
Las muestras de desmontes de complejos sulfurados de Pb-Ag-Zn, con diferentes contenidos de sulfuros (entre 1.0 a 3.4 % de Azufre Total), y con concentraciones de Ag (entre 68 a 53 g/t de Ag), al ser sometidas a condiciones normales de cianuración por agitación, permiten obtener extracciones de Ag que varían entre 74 % a 31 %, respectivamente.
Después del pretratamiento ácido-oxidante, las extracciones de Ag en la etapa posterior de cianuración, subieron de entre 81% y 63%, respectivamente.
Los desmontes de complejos sulfurados de Pb-Ag-Zn con contenidos de azufre por encima de 1.7 %, no permiten obtener residuos no generadores de DAR por ninguno de los métodos de lixiviación estudiados. Cuando los desmontes presentan contenidos de azufre menores, la lixiviación clorurante permite obtener no sólo residuos no generadores de DAR, sino aptos para su uso como coberturas secas en el cierre ambiental en zonas de poca precipitación fluvial por generar valores de AEV (capacidad de almacenamiento de agua) mayores a 1000 cm y conductividades hidráulicas pequeñas.
Finalmente, la recomendación que emerge del estudio del tratamiento de los desmontes como alternativa a su cierre ambiental, es que se debe realizar un estudio económico de la propuesta técnica generada a objeto evaluar si los costos de cierre ambiental son o no mayores a la alternativa de retratamiento propuesta.
5. Bibliografía
1. Benzaazoua, M., & Zamora, G. Predicciones de drenaje ácido de roca mediante tests geoquímicos estáticos y dinámicos. Revista Metalúrgica UTO. 2003. ISSN 2078-5593. [ Links ]
2. Zamora E. G. Hinojosa C. O. Salas C. A. Estudio de desulfurización de relaves generadores de DAR, antes de su disposición de final, como alternativa de manejo y mitigación de impacto ambiental. Revista de Medio Ambiente y Minería. 2017. N°3, 44 52 p. ISSN 2519-5352. [ Links ]
3. Zamora E. G.; Lanza F. J. y Arranz G.J. Metodología para la identificación y evaluación de riesgos de pasivos ambientales mineros con fines de priorización para su remediación. Revista de Medio Ambiente y Minería. 2018, N° 5, pp 31-43. ISSN 2519-5352. [ Links ]
4. Zamora E. G. & Hinojosa C. O. Economía circular en minería - Caso de Estudio: Producción minera de Concentrados de Pb-Ag-Zn en Bolivia. Revista de Medio Ambiente y Minería. 2019. Vol 4 (1), p 3 17. ISSN 2519-5352. [ Links ]
5. John O. Marsden and C. Alain House. The Chemistry of Gold Extraction (second edition). Society for Mining, Metallurgy and Exploration, 2006. Inc. (SME). [ Links ]
6. Cruz J. L Zamora E.G. Lixiviación de concentrados de flotación bulk de Zn-Ag en medio ácido y presencia de H2O2 y NaCl. Revista Metalúrgica UTO. N° 41, 14 -25. ISSN 2078-5593. [ Links ]
7. Blanco W. Estudio del comportamiento en la lixiviación de relaves de Poopó, Japo y san Cristóbal con hipoclorito de sodio como agente oxidante y en presencia de cloruro de sodio como agente acomplejante. 2018. Carrera de Ingeniería Metalúrgica y Ciencia de Materiales, Universidad Técnica de Oruro. Bolivia. [ Links ]
8. Price, W.A, 2010. Acid Base Accounting Criteria Used in Prediction of Drainage Chemistry. International Mine Water Association (IMWA) 2010 Symposium, Sydney, Nova Scotia, September 5-9, pp. 55-58. [ Links ]
9. Zamora E. G. Salas C.A. Hinojosa C. O. Restauración de Sitios Mineros Mediante Coberturas de Efecto SDR. Revista Metalúrgica UTO. ISSN 2078-5593 [ Links ]
]]>