
Innovaciones técnicas en el tratamiento de aguas acidas de mina con recuperación de subproductos con valor económico
Osvaldo Aduvire
Doctor Ingeniero de Minas Consultor Principal y Practice Leader de Unidad Geoambiente SRK Consulting (Peru) S.A. e-mail: oaduvire@srk.com.pe
Profesor de la Sección Minas de la Pontificia Universidad Católica del Perú (PUCP)
Recibido: 06-05-2019 Aceptado: 25-05-2019
]]>
Resumen
La actividad minería genera un gran volumen de materiales y residuos que deben almacenarse adecuadamente en depósitos de desmontes y relaves denominados botaderos o escombreras y relaveras o presas de relaves, por lo general, estos residuos mineros suelen contener sulfuros que en contacto con la atmósfera y agua inician unos complejos procesos de transformaciones físicas, químicas y biológicas, que dan origen a la generación de drenajes ácidos de mina.
En los últimos años se han desarrollado metodologías de caracterización más efectiva de las ácidas de mina en el que se incluye además de la acidez protónica la acidez mineral, aspecto que por lo general no se considera en los métodos clásicos de caracterización. También se han potenciado la aplicación de tecnologías emergentes en el control y tratamiento de efluentes como la recuperación de metales de aguas ácidas, tanto si las instalaciones se encuentran en operación o en abandono, mediante el desarrollo de procesos físicos y químicos que modifican las condiciones de Eh y pH de las descargas, de forma que se favorezca la formación de especies insolubles y la retención de la carga metálica disuelta en las aguas.
En este trabajo se describen las mejores técnicas disponibles en la caracterización hidrogeoquímica de aguas de mina, junto con procesos innovadores desarrollados para la recuperación de metales y/o subproductos con valor económico de las aguas ácidas de mina. Esta metodología de recuperación de subproductos, además de las mediciones directas en campo de parámetros como: pH, redox, conductividad, oxígeno disuelto, acidez y caudal; se toma muestras representativas para su respectivo análisis en concentraciones totales y disueltas, con esta información se selecciona los reactivos y los tipos de ensayos de neutralización y precipitación para determinar las zonas de hidrólisis de cada elemento presente en el agua y que son objeto de eliminación. A partir de las zonas de hidrólisis o tamponamiento del sistema, identificamos los rangos de pH y redox de los elementos con mayor concentración y elegimos los cortes de las distintas etapas que conformaría el sistema de tratamiento. A partir de los resultados obtenidos en la caracterización de los efluentes se procede a elegir los sistemas de tratamiento mediante ensayos experimentales a nivel de laboratorio para obtener el tamaño de las variables de diseño de la planta de tratamiento de las aguas de mina, que permita la recuperación u obtención de subproductos con posibilidades de aprovechamiento económico.
Esta metodología permite dimensionar sistemas de tratamiento de aguas de mina más eficientes, con un menor consumo de reactivos y mejor control ambiental, además, de considerar a los efluentes de mina como fuentes de donde es posible recuperar la carga metálica y obtener un subproducto con aprovechamiento económico. El estudio también incluye casos comparativos del rendimiento económico que se pueden obtener y las recomendaciones para que esta metodología sea viable técnica, ambiental y económica.
Palabras clave. Tratamiento de aguas ácidas, Recuperación de metales
Abstract
Mining activity generates a large volume of materials and waste that must be stored properly in deposits of tailings and tailings called dumps or tailings or tailings dams, usually, these mining waste usually contain sulfides that in contact with the atmosphere and water they initiate complex processes of physical, chemical and biological transformations that give rise to the generation of acid mine drainages.
In recent years, methodologies have been developed for more effective characterization of mine acid, in which mineral acidity is included in addition to protonic acidity, an aspect that is not usually considered in classical characterization methods. The application of emerging technologies in the control and treatment of effluents such as the recovery of acidic water metals has also been strengthened, whether the facilities are in operation or abandoned, through the development of physical and chemical processes that modify the conditions of Eh and pH of the discharges, so as to favor the formation of insoluble species and the retention of the dissolved metal load in the waters.
]]> This paper describes the best techniques available in the hydrogeochemical characterization of mine waters, together with innovative processes developed for the recovery of metals and / or by-products with economic value from mine acid waters. This method of recovering by-products, in addition to direct measurements in the field of parameters such as: pH, redox, conductivity, dissolved oxygen, acidity and flow rate; representative samples are taken for their respective analysis in total and dissolved concentrations, with this information the reagents and the types of neutralization and precipitation tests are selectedto determine the hydrolysis zones of eachelement present inthe water and that are subject to elimination. From the zones of hydrolysis or buffering of the system, we identify the pH and redox ranges of the elements with the highest concentration and we choose the cuts of the different stages that would form the treatment system.Based on the results obtained in the characterization of the effluents, we proceed to choose the treatment systems through experimental tests atthe laboratory levelto obtainthe size of the design variables ofthe mine water treatment plant, which allows the recovery or obtaining by-products with possibilities of economic use.
This methodology allows the sizing of more efficient mine water treatment systems, with a lower consumption of reagents and better environmental control, in addition to considering mine effluents as sources from where it is possible to recover the metallic load and obtain a by-product with use economic. The study also includes comparative cases of economic performance that can be obtained and recommendations for this methodology to be technically, environmentally and economically feasible.
Keywords. Acid water treatment, Metal recovery
1. INTRODUCCION.
La aplicación de técnicas innovadoras permiten consideran a los residuos generados en la operación minera como recursos de segunda generación con posibilidades de aprovechamiento y recuperación para obtener subproductos con valor económico. Esta metodología integral permite aprovechar mejor los recursos naturales, alargar la vida de los depósitos de residuos y reducir la descarga de residuos sólidos y líquidos al ambiente.
Para ello, nuestro grupo de trabajo ha venido desarrollando una serie de proyectos de investigación aplicada en donde se han ido poniendo a punto y/o convalidando innovadoras técnicas y procesos encaminados a la búsqueda de nuevas aplicaciones y aprovechamiento de los residuos para nuevos usos, así como a la recuperación de metales y/o subproductos de los efluentes de mina
]]>2. OBJETIVOS
Describir técnicas de caracterización y diagnóstico de la calidad de los efluentes de mina basado en el contenido de acidez y las concentraciones de metales presentes en el agua, cuyo objetivo es que los sistemas de remediación de efluentes de mina requieran menor cantidad de reactivos en los procesos de tratamiento y por otro, permita en lo posible la recuperación de metales como subproductos con valor económico.
3. METODOLOGIA
Para desarrollar una metodología que permita aprovechar y recuperar subproductos de los residuos mineros ya sean sólidos o líquidos, se ha revisado las normas ambientales de control y gestión de residuos en el sector minero de Perú, además de revisar el estado del arte a nivel mundial sobre las últimas innovaciones tecnológicas en control, tratamiento y recuperación de subproductos con valor económico obtenidos de las aguas ácidas de mina. La parte experimental ha incluido la caracterización de efluentes mediante mediciones directas de parámetros fisicoquímicos y la determinación del contenido de metales totales y disueltos. Seguidamente se han realizado una serie de ensayos de neutralización y precipitación a nivel laboratorio aplicando procesos de neutralización directa y secuencial o por etapas. Para ello, se tomaron muestras de 50 litros para realizar ensayos de neutralización y precipitación (Fig. 1) con mediciones directas de pH, Eh, Conductividad eléctrica y Sólidos totales durante los ensayos complementado con análisis químico de las alícuotas resultantes.
4. TRATAMIENTO Y RECUPERACIÓN DE METALES DE LAS AGUAS ACIDAS DE MINA
Una vez caracterizado el agua de mina se procede a dimensionar su sistema de tratamiento y a estudiar la posibilidad de recuperar metales y/o subproductos con valor económico durante el tratamiento.
]]> Una variable importante en el diseño de los sistemas de tratamiento de aguas de mina es el consumo de material reactivo necesario para alcanzar la neutralización de los efluentes. Esta tasa de consumo experimental junto con las características hidráulicas y geoquímicas ayuda a determinar el tamaño de los dispositivos de tratamiento. La dosis de consumo de material reactivo obtenido, también determina la secuencia de la operación, los tiempos de tratamiento y el volumen de lodos a generarse durante el tratamiento.En los ensayos experimentales también se tiene en cuenta los caudales a tratar y las concentraciones presentes en los efluentes, estos últimos determinan si se realizará solo tratamiento o se realizará tratamiento con recuperación de metales. Si se elige solo tratamiento el proceso será en una sola etapa (Proceso Directo), pero, si se opta por la recuperación de subproductos con valor económico el tratamiento será por etapas con separación de fases sólidas (Proceso por Etapas). Los equipos utilizados en laboratorio incluyen pHmetro, vaso de precipitados, agitador magnético, balanza de precisión, medidor del potencial redox, test de jarras, conos imhof, etc.
4.1. Diseño del sistema de tratamiento de aguas ácidas mediante Proceso Directo.
Las curvas experimentales del consumo de reactivo requerido para abatir la acidez de las aguas de mina hasta su neutralización y eliminación de la carga contaminante, se realizaron mediante ensayos de neutralización y precipitación en donde se emplearon cal, NaOH como reactivo, floculantes y otros.
Para el diseño, por lo general se realizan un gran número de ensayos, considerando muestras independientes y mezclas representativas en las mismas proporciones de los drenajes de mina, por tanto se obtienen numerosas Curvas de Neutralización en donde se detectan las zonas de hidrólisis y/o de tamponamiento principalmente de los elementos Fe, Al y otros con presencia significativa, identificando los tramos de las curvas en donde se formarían las fases sólidas (hidróxidos, hidroxisulfatos y otros), condición básica en donde se puede realizar la separación sólido-líquida.
Los ensayos de neutralización y precipitación se realizan cumpliendo parámetros de calidad que cuiden la originalidad y representatividad de las muestras de agua de mina recolectadas en campo y en una sola etapa van a alcanzar valores de pH de 8 o 9, en donde, después de un tiempo de decantación se produce la separación sólido-líquido. Este proceso funciona de forma similar a las plantas de tratamiento de aguas acidas en operación en las distintas explotaciones mineras. Las aguas tratadas deben cumplir con los Límites Máximos Permisibles (LMP) contemplados en la legislación vigente, entendiendo LMP como la concentración o contenido de elementos, sustancias o parámetros físicos, químicos y biológicos, que caracterizan a un efluente, que al ser excedido causa o puede causar daños a la salud, al bienestar humano y al ambiente. Su cumplimiento es exigible legalmente por la respectiva autoridad competente.
En el caso de Perú, estos LMP para efluentes líquidos a descargar hacia el ambiente por las instalaciones minero-metalúrgicas nuevas o en operación están contemplados en el D.S. 010-2010-MINAM, y deben medirse en los puntos de descarga a fin de determinar la concentración de cada uno de los parámetros regulados y el volumen de descarga en metros cúbicos por día. Finalmente, el volumen de los efluentes determinará la frecuencia del monitoreo, así como la periodicidad del monitoreo que se suele reportar a la autoridad correspondiente.
4.1.1. Comparación de proceso Directo y por Etapas. Caso 1.
En la Tabla1 se presenta la calidad de un drenaje de mina cuyo pH<3 con contenidos de Fe, Mn, Zn entre otros, para tratar esta agua se han realizado una serie de ensayos exprimentales orientados a obtener unas concentraciones finales que cumplan con los LMP de la legislación vigente para el sector minero-metalúrgico. A continuación se presenta el estimado del consumo de cal para los tratamientos mediante ensayo directo y por etapas.
]]> La primera alternativa es realizar ensayos de neutralización mediante proceso directo, en donde se incrementan el pH de 2.3 hasta llegar a pH 10, en la Tabla 2 se puede ver las concentraciones al final del proceso de neutralización, en donde aun se evidencia contenidos de Mn. Lo que indicaría que para seguir retirando Mn de agua se debería continuar con el proceso y añadir floculantes u otros reactivos para hacer que el Mn pase a fase sólida. El consumo de cal en la alternativa del Caso 1 (Ensayo Directo) para obtener lo resultados de la Tabla 2 alcanzo los 620 mg/l.La segunda alternativa de tratamiento del agua de mina y teniendo en cuenta las concentraciones presentes en la muestra (Tabla 1) se ha diseñado un tratamiento en dos (2) etapas, en la primera etapa se alcanzó pH 5.5 y se retiraron los lodos principalmente de Fe y en menor cantidad de Al, en la segunda etapa el tratamiento alcanzo el pH 10 en donde se obtuvo un sedimento con importante contenido de Zn y Mn con posibilidades de recuperación del primero.
En las Figuras 2 se pueden observar las curvas de consumo de cal y de la evolución del redox durante el proceso de neutralización. Evidenciandose las zonas de formación de fases sólidas o tamponamiento debido a la hidrólisis de Fe, Al, Zn y Mn principalmente, estas zonas corresponden con los rangos de pH en donde se forman fases sólidas de estos elementos. Según se incrementa el pH en el tratamiento del drenaje de mina, los valores de Eh descienden hasta valores menores a 80 mV que corresponden a aguas naturales sin afección.
En estos ensayos, las zonas de hidrólisis en rango ácido correspondiente al Hierro (pH 2.5 - 3,7) y al Aluminio (pH 4,5 - 5,5), representa el retiro de carga metálica del agua que a su vez genera acidez, dando como resultado el tamponamiento temporal del sistema.
A partir del pH 6.5 hasta pH 8 y pH 10 también se ve un tamponamiento del sistema en este caso inducido por el contenido de Zn y Mn presentes en el efluente, éste último presenta pendiente menos pronunciada asociada a la menores velocidades de reacción correspondientes a la formación de oxihidróxidos de Mn. A diferencia del tratamiento directo en donde se obtiene un solo lodo, en el tratameitno por etapas se obtiene dos a más lodos, por tanto, una vez finalizada la primera etapa se retira el lodo, luego se continúa con el proceso con adición de reactivo neutralizante hasta llegar al pH final donde concluye la segunda etapa de neutralización, luego de la cual también se requeriran los sólidos formados.
Los resultados obtenidos en el ensayo por etapas son bastante claros en cuanto a la efectividad del retiro de carga metálica del agua. La Tabla 3 muestra las concentraciones de metales en el agua después de las 2 etapas de tratamiento, consiguiendo la remoción efectiva de Zn y Mn, resultado que no se logro con el esnayo directo.
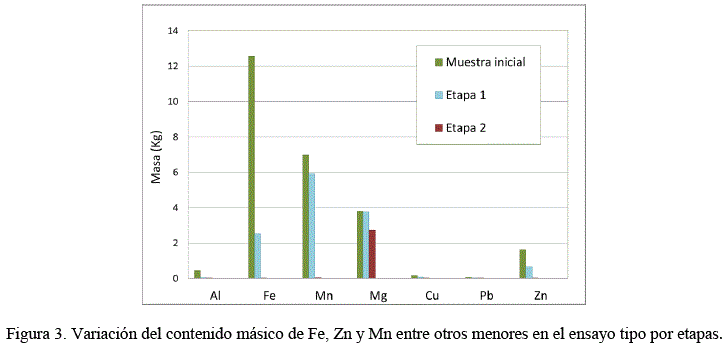
El balance de masas realizado como parte del seguimiento de las reacciones involucradas en el proceso, tal como lo muestra la Fig. 3, evidencian también la remoción de los metales de interés en cada etapa de la prueba.
]]>
El consumo de cal en la alternativa del Caso 1 (Ensayo por Etapas) para obtener los resultados de la Tabla 4, es el siguiente: 260 mg/l en la Primera Etapa y 240 mg/l en la Segunda Etapa, alcanzando un consumo total de cal de 500 mg/l. Como resultado de la comparación de los tratamientos directo y por etapas, en este último se logra mejores resultados en la remoción de carga metálica, además de consumir 120 mg/l menos de cal.
4.1.2. Comparación de proceso Directo y por Etapas. Caso 2.
Para esta comparación se ha elegido un efluente de mina denominado Nv 2 que tiene un pH de 3.5, la conductividad eléctrica supera los 4170 (µS/cm y algunos valores de los elementos mayoritarios medidos en concentraciones totales y disueltas (mg/l) superan los LMP de referencia según la legislación peruana vigente (D.S. N°010-2010-MINAM) para la descarga de efluentes líquidos procedentes de instalaciones minero-metalúrgicas. Los resultados obtenidos en los ensayos para determinar el consumo de reactivo de neutralización dan los siguientes resultados: en el caso del ensayo directo o neutralización directa, se ha estimado un consumo de cal de 1080 mg/l para alcanzar un pH de 8.5, mientras que para el ensayo por etapas el consumo de cal para alcanzar un pH=8.5 fue de 820 mg/l (Fig. 4).
Comparando los consumos de cal obtenidos en proceso de neutralización directa y el de neutralización por etapas, se deduce que para efluentes con carga metálica significativa resulta que la neutralización por etapas consume 260 mg/l menos de reactivo, lo que representa un ahorro apreciable en el consumo de cal, cuando se trata de importantes volúmenes de agua de mina a tratar. Por ejemplo, si consideramos implementar una planta de neutralización por etapas de 500l/s y que el costo de cal es de 0.5 US$/kg, al año se obtiene un ahorro de 4'043,520 kg de cal, lo que equivalente a un ahorro de2'021,760 US$/año.
Esto redundará en tener un proceso de menor costo de tratamiento del agua de mina, pero, además hay mejoras añadidas como la obtención de subproductos con posibilidades de aprovechamiento económico, menor requerimiento en el manejo de lodos, ente otras ventajas secundarias.
4.2. Recuperación de metales de aguas ácidas mediante Proceso por Etapas. Cuando las concentraciones de metales (Al, Cu y Zn) presentes en el agua de mina tienen valores significativos (superior a 300 o 500 mg/l), es viable estudiar la recuperación de estos elementos como subproductos, los ensayos experimentales deben ser por etapas a objeto de obtener en cada etapa un lodo con elevado contenido metálico, que podía enviarse a la planta concentradora o a un proceso similar para su recuperación, y en algunos casos destinarlos auna nueva aplicación como los lodos con elevada contenido de aluminio que puede enviarse a mina para la mejora del Anfo como explosivo y obtener anfo aluminizado.
]]> 4.2.1. Ensayos de neutralización y recuperación en tres etapas.En la Tabla 5 se muestra la carga metálica mayoritaria y el pH de un drenaje de mina, al que se le ha realizado ensayos de neutralización en tres etapas a fin de obtener tres subproductos con altos contenidos de Fe, Al y Zn.
La zona de tamponamiento e hidrólisis se pueden observar en las curvas de consumo de cal tanto en función al pH como del potencial redox. La Figura 5 muestra la evolución del redox durante el proceso de neutralización, en donde los valores de Eh descienden hasta valores de 50 mV que corresponden a aguas naturales sin afección.
En la Foto 1 se muestra los lodos obtenidos en un ensayo de neutralización de tres etapas: en la primera etapa se alcanzo el pH 4 y se retiraron lodos de color ocre naranja (M-1) que corresponderían a hidróxidos de Fe principalmente, en la segunda etapa se continuo con el proceso de neutralización hasta alcanzar el pH 5,5 en donde se obtuvieron lodos de color blanquecino (M-2) correspondiente a los hidróxidos de Al mayoritariamente, y finalmente en la tercera etapa de tratamiento el pH alcanzo valores superiores a 8,5 en donde se recupero un lodo marrón oscuro a negro (M-3) que correspondería a las fase sólidas de Zn como compuesto mayoritario y en menor proporción al resto de elementos como Mn, Mg, Pb presentes en el agua de mina que pasaron a fase sólida a pH superiores al neutro.
Si no se retiran los lodos de Fe y Al del proceso de tratamiento, a pH superiores al rango de movilización de estos elementos 4 y 5,5 respectivamente, estas fases sólidas formadas se redisuelven y pasan nuevamente al agua, por lo que se requeriría añadir mayor cantidad de material alcalino (cal) para hacer que formen nuevamente fases sólidas (pH 8) y poder retirarlos del agua, lo que hace que en el proceso incremente el consumo de cal, además de requerir en algunos casos añadidos de floculantes, coagulantes y secuestrantes, por tanto, el costo de tratamiento de las aguas ácidas de mina sea más elevado.
Los lodos obtenidos en el tratamiento del agua de mina mediante un sistema de 3 etapas, podrían tener las siguientes aplicaciones: el lodo con contenido de Fe (M-1) se podría aprovechar como pigmento de cerámicas, el lodo con aluminio (M-2) se emplearía en los trabajos de voladura mejorando los explosivos, y el lodo al alto contenido de Zn (M-3) serviría para obtener un concentrado de zinc.
4.3. Operaciones unitarias que conforman un sistema de tratamiento por Etapas.
Las principales Operaciones Unitarias involucradas en un sistema de tratamiento por etapas son: Disolución (de reactivos de proceso), Agitación y Decantación (Fig. 6) en cada etapa y están complementadas por operaciones secundarias que permiten controlar el proceso.
]]> Al aplicar sistema de tratamiento de aguas ácidas por etapas, permite obtener lodos con características bien definidas y de iguales particularidades, con posibilidades de recuperar metales de los lodos de proceso.El agua del proceso de tratamiento se puede descargar a un curso de agua natural del lugar (cuerpo receptor), previo control de su calidad a fin de causar el mínimo impacto ambiental, mientras que los lodos que no tengan interés de recuperación se almacenarán en depósitos adecuados para ello o enviados generalmente al depósito de relaves u otro depósito preparado para este cometido. Luego de la etapa experimental se debe llevar un pilotaje que permita dimensionar adecuadamente el sistema de tratamiento para cada tipo de agua de mina.
5. CONCLUSIONES
Caracterizar las aguas ácidas de mina en función a la acidez ayuda a estudiar las posibilidades de recuperación de subproductos con valor económico y a elegir el sistema de tratamiento más idóneo y eficiente, ya sea mediante sistemas activos o pasivos, porque además de la acidez protónica se incluye la acidez mineral, aspecto que por lo general no se considera en los métodos clásicos de caracterización.
El dimensionado del sistema de tratamiento para aguas ácidas basado en el contenido de acidez y por etapas, por un lado, permite aprovechar mejor los recursos gastando menos cal en el proceso de neutralización, y por otro, permite recuperar metales de los lodos del proceso. Esto hace que los tratamientos de aguas ácidas sean más eficientes, de menor costo y de mayor control ambiental.
La obtención de subproductos con valor económico puede tener una recursión económica directa al consumir menor cantidad de cal, pero, también conlleva otros beneficios añadidos como: se reduce el volumen de lodos a trasladar a los depósitos para su almacenamiento, por tanto, aumenta la vida de estos depósitos y se reduce los costos de operación, entre otros.
REFERENCIAS.
]]>1. Aduvire, O. y Aduvire, H. 2005. Aguas ácidas de mina: caracterización, mineralogía y microbiología. Ingeopres 141, pp. 52-62. [ Links ]
2. Aduvire, O. 2005. Drenaje Acido de Mina: Generación y Tratamiento. Madrid: Instituto Geológico y Minero de España. Edición IGME. Código: SID-63187. Publicación Electrónica 136pp. [ Links ]
3. Aduvire, O., Escribano, M., García-Bermúdez, P., López-Jimeno, C., Mataix, C. y Vaquero, I. 2006. Manual de Construcción y Restauración de Escombreras. Ed. ETSIM-UPM. 633pp. ISBN: 84-96140-20-2. [ Links ]
4. Aduvire, O., Vadillo, L., Moreno, C., Alberuche, Monteserín, V., Lacal, M., Arranz, J.C. y Martínez, B. 2007 Evolución de las descargas ácidas en arroyo la silva (Bierzo). International Congress Energy and Environmental Engineering and Management. Badajoz (España), 06-08 Junio 2007. [ Links ]
5. Aduvire, O., Moreno, C., Alberruche, E., Lacal, M. y Vadillo, L. 2007. Effects of precipitation of secondary Fe (III) minerals and dilution on the attenuation of acid drainages; mining area of Spain. MineClosure 07. Santiago (Chile), 16-19 October 2007. [ Links ]
6. Bigham, J.M., Schwertmann, U., Carlson, L. and Murad, E. 1990. A poorly crystalized oxyhydroxysulfate of iron formed by bacterial oxidation of Fe (II) in AMD. Geochimica Cosmochimica Acta, 54, 2743-2754. [ Links ]
7. Bigham, J.M. and Nordstrom, D.K. 2000. Iron and aluminum hydroxysulfates from acid sulfate waters. En: Alpers, C.N., Jambor, J.L. y Nordstrom, D.K. (eds), Sulfate minerals: crystallography, geochemistry and environmental significance. Reviews in Mineralogy & Geochemistry, MSA, Virginia. USA. (40), 350-403. [ Links ]
8. Hammarstrom, J.M., Seal II, R., Meier, A. and Kornfeld, J. 2005. Secondary sulfate minerals associated with acid drainage in the Eastern US: recycling of metals and acidity in surficial environments. Chemical Geology 215, pp. 407-431. [ Links ]
9. Jönsson, J., Jönsson, J. and Lövgren, L. 2006. Precipitation of secondary Fe (III) minerals from acid mine drainage. Applied Geochemistry 21, pp. 437-445. [ Links ]
10. Michalkova E., Schwarz, M., Pulisova, P., Masa, B., Sudovsky, P. (2013) Metals Recovery from Acid Mine Drainage and Possibilities for their Utilization. Polish Journal of Environmental Studies. Vol. 22, No. 4, 1111-1118. [ Links ]
11. Macingova, E and Luptakova, A. (2012). Recovery of Metals from Acid Mine Drainage. Chemical Engineering Transactions. Vol. 28, 109-114. [ Links ]
12. Swedlund, P. and Webster, J. 2001. Cu and Zn ternary surface complex formation with SO4 on ferrihydrite and schwertmannite. Applied Geochemistry 16, pp. 503-511. [ Links ]
13. Stumm, W. and Morgan, J. 1981. Aquatic chemistry. Wiley Iterscience. 470pp. [ Links ]
14. Walton, K. 1992. Microbiological and chemical characteristics of an stream draining a disused copper mine. Environmental Pollution, 76, 169-175. [ Links ]
15. Williams, T. and Smith, B. 2000. Hydrochemical characterization of acute acid mine drainage. Environmental Geology, 39 (4-5), 272-278. [ Links ]
]]>