Dimensionado de sistemas de tratamiento de aguas acidas de mina
Osvaldo Aduvire Dr. Ing. de Minas
e-mail : oaduvire@srk.com.pe
Practice Leader de Unidad Geoambiente. SRK Consulting (Peru) S.A
Los drenajes de mina por lo general son ácidos y contienen elevadas concentraciones de Fe, Al, SO4, además de Zn, Mn, Mg, Cu, Cd, Pb y As, son la principal fuente de biodisponibilidad de elementos contaminantes que degradan la calidad de los ecosistemas acuáticos. Esta problemática puede persistir durante décadas e incluso cientos de años una vez concluida la actividad minera.
Para revertir esta problemática, en los últimos años en el sector minero de Perú, se han venido implementando una serie normas y referencias para el control ambiental como los Estándares de Calidad Ambiental (ECA) y los Límites Máximos Permitidos (LMP), que junto con otros dispositivos legales forman parte obligada de la gestión ambiental en minería, y hacen posible el desarrollo de proyectos mineros sostenibles. Para que las descargas de mina cumplan con estas exigencias es necesario que las empresas mineras implementen una nueva planta de tratamiento o acometan la optimización del proceso de las actuales plantas de neutralización existentes.
En este trabajo se describen los resultados de un gran número de ensayos de laboratorio y mediciones en campo orientados a determinar la acidez total de las aguas de mina, en donde se incluya la acidez protónica debida al pH y la acidez mineral correspondiente a la carga metálica presente en cada efluente, esta información es base en los ensayos de neutralización porque lo que hay que abatir es la acidez presente en las aguas de mina. También se describe el dimensionado de los dispositivos de tratamiento activo o químico con cal, basados en ensayos experimentales de neutralización, floculación, coagulación y secuestro de fases sólidas y la obtención de subproductos de donde se pueden recuperar o reciclar metales, lo que permite reducir los costos de tratamiento y el desarrollo de una minería sostenida que respeta el medioambiente.
Palabras clave: Aguas ácida de mina - Dimensionamiento
Abstract:
Mine drainages are usually acidic and contain high concentrations of Fe, Al, SO4, in addition to Zn, Mn, Mg, Cu, Cd, Pb and As, are the main source of bioavailability of contaminants that degrade the quality of aquatic ecosystems. This problem can persist for decades and even hundreds of years once the mining activity is concluded.
To reverse this problem, in recent years in the mining sector in Peru, a series of standards and references for environmental control have been implemented, such as the Environmental Quality Standards (ECA) and the Maximum Permitted Limits (LMP), which together with Other legal devices are an obligatory part of the environmental management in mining, and make possible the development of sustainable mining projects. In order for the mine discharges to comply with these requirements, it is necessary for the mining companies to implement a new treatment plant or undertake the process optimization of the existing existing neutralization plants.
This paper describes the results of a large number of laboratory tests and field measurements aimed at determining the total acidity of mine waters, including the protonic acidity due to pH and the mineral acidity corresponding to the metallic load. present in each effluent, this information is based on the neutralization tests because what must be killed is the acidity present in the mine waters. It also describes the dimensioning of active or chemical treatment devices with lime, based on experimental tests of neutralization, flocculation, coagulation and sequestration of solid phases and the obtaining of by-products from where metals can be recovered or recycled, which reduces the treatment costs and the development of a sustainable mining that respects the environment.
Keywords: Acid mine waters.
1. INTRODUCCION.
La normativa ambiental relacionada con la gestión del recurso hídrico para el sector minero aprobada en los últimos años en Perú, contempla el cumplimiento de unos Límites Máximos y/o Estándares de Calidad, tanto en efluentes procedentes de las instalaciones mineras como en aguas de cursos circundantes denominados cuerpos receptores, además de contar con un plan de gestión ambiental en que se incluye un programa de monitoreo de estas aguas.
Las aguas ácidas de mina (AMD) llevarán mayor o menor carga contaminante según una serie de factores, como: la velocidad de reacción de los materiales excavados, capacidad ácido/base de los minerales y residuos mineros, tamaño y solubilidad de los materiales, capacidad de neutralización de las aguas, transporte de oxígeno, movilidad del agua intersticial, permeabilidad del medio, clima y temperatura, evaporación e infiltración, acción catalizadora de las bacterias, adsorción microbiana de metales, precipitación y disolución de los metales durante el transporte, etc., por lo que, es importante realizar una caracterización adecuada de los residuos mineros y de efluentes que se generan en los procesos mineros, a fin de elegir el sistema de control y tratamiento más eficiente y específico a cada drenaje de mina.
2. OBJETIVOS.
Dar una introducción a la gestión ambiental del agua en minería y determinar una metodología de caracterización más efectiva de las ácidas de mina en el que se incluya además de la acidez protónica la acidez mineral, aspecto que por lo general no se considera en los métodos clásicos de caracterización.
Describir la aplicación de tecnologías emergentes en el control y tratamiento de aguas ácidas como la recuperación de metales de aguas ácidas, tanto si las instalaciones se encuentran en operación o en abandono, mediante el desarrollo de procesos físicos y químicos que modifican las condiciones de Eh y pH de los drenajes de mina, de forma que se favorezca la formación de especies insolubles y la retención de la carga metálica disuelta en las aguas.
]]>3. METODOLOGIA.
Para llevar adelante el estudio se han analizado las normas ambientales de gestión de agua en el sector minero de Perú y se ha recopilado información a nivel mundial sobre las últimas innovaciones tecnológicas en control y tratamiento de generación ácida, para ello es indispensable disponer de técnicas de caracterización más eficaces que ayuden a formular sistemas de prevención, control, recuperación y tratamiento más sencillos y de menor costo.
Para el levantamiento de data de campo se ha empleado equipos portátiles para realizar medidas in situ de pH, Eh, oxígeno disuelto, conductividad, temperatura, caudal, turbidez, acidez, alcalinidad, Fe2+, Fe3+ y Fe total. Estos equipos pueden ser: conductivímetro, pHmetro, oxímetro, equipo portátil de filtrado (Millipore), sonda multiparamétrica, toma muestras de sedimentos en superficie y en profundidad, botellas alfa y beta. La acidez se valora con NaOH 0,16 N y en la determinación del hierro se emplea como indicador ácido sulfosalicílico. La recogida de muestras de agua para análisis químicos en laboratorio se realiza en frascos de HDPE de 125ml, previo lavado con ácido nítrico al 10% y enjuagado con agua del punto de muestreo. Para análisis de concentraciones totales y disueltas, se toman muestras de agua sin filtrar y filtradas a 0,45 micras, conservadas con HNO3 hasta pH<2 y refrigeradas hasta 4 Cº para su transporte, según estándares de muestreo de laboratorios reconocidos.
Para realizar los ensayos experimentales de laboratorio y obtener las curvas de neutralización y sedimentación, se han empleado los siguientes reactivos y equipos:
Muestras de agua ácidas de mina
Reactivos de neutralización: Cal
Reactivos para floculación-sedimentación
Vaso de Precipitados
]]> Agitador magnético y balanza pH-metro y medidor de Potencial Redox
4. CARACTERIZACION DE AGUAS DE MINA
La formación de aguas ácidas tiene lugar a partir de la oxidación química de los sulfuros, acelerada en muchos casos por la acción bacteriana. Los principales elementos que intervienen son: los sulfuros reactivos, el oxígeno y el agua (vapor o líquida), y como elemento catalizador las bacterias.
La velocidad de reacción es una variable muy importante, pues si el proceso ocurre muy lentamente el efecto sobre el medio puede ser despreciable. Sin embargo, si la generación de aguas ácidas es rápida el problema se agrava, ya que se producirá la contaminación del entorno.
Aunque la velocidad de reacción depende de numerosos factores como temperatura, cantidad de sulfuros, granulometría, presencia de agua, aire y bacterias. Ciertas especies mineralógicas son más reactivas que otras; por ejemplo, la marcasita, que tiene la misma fórmula química que la pirita, es muy inestable y puede generar rápidamente aguas ácidas. Los sulfuros de otros metales (plomo, zinc o cobre) son generalmente menos reactivos que los de hierro. En parte, debido a la mayor estabilidad de su estructura cristalina y también porque forman minerales menos solubles que recubren la superficie de los propios sulfuros impidiendo que progrese su oxidación.
La cantidad y el tamaño de los granos del mineral influyen en la velocidad de reacción. Las texturas finas con variedades mal cristalizadas se oxidan más rápidamente que los granos cristalinos gruesos. Por ejemplo, una forma de pirita desarrollada en condiciones de baja temperatura puede producir mucho más rápidamente acidez que una gran masa de sulfuros formada a alta temperatura, debido a la menor relación de superficie/volumen.
Existen varias propuestas de clasificación de las aguas ácidas, la mayoría en función al pH como parámetro principal, en lo últimos años se han incorporado al pH las concentraciones, el contenido de oxígeno, el potencial redox, la acidez metálica, la conductividad y otros.
En general, las aguas ácidas de mina (AMD) tienen pH entre 2 a 6, contienen cationes y aniones en disolución, predominando SO4, Fe, Mn, Al, Cu, Pb, Zn, además de Cd, Ca, Na, K, Mg y otros. Por lo general, los AMD pueden degradar hábitats acuáticos y cambiar la calidad de las aguas debido a su toxicidad, corrosión y otros efectos producidos por la disolución de sus constituyentes.
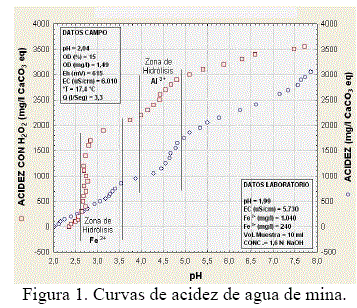
]]> Desde el punto de vista de su tratamiento, es recomendable que el agua ácida de mina a tratar esté tipificada según el contenido de acidez, mejor aún si se hace a través de una curva de acidez (Fig. 1) en donde se puede determinar las zonas de tamponamiento o hidrólisis de los elementos presentes.Esta caracterización hidrogeoquímica de los drenajes de mina, incluye la acidez protónica debida a los hidrogeniones libres (H+) más la acidez mineral debido a la disolución de Fe, Al y Mn (Fig. 1). Estos metales son considerados ácidos generadores porque mediante oxidación e hidrólisis pueden generar H+, según las siguientes reacciones:
Fe2+ + ¼O2 +3/2 H2O ® FeOOH + 2H+ Ec.1
Fe3+ + 2 H2O ® FeOOH + 3 H+ Ec. 2
Al3+ + 3 H2O ® Al (OH)3 + 3 H+ Ec. 3
Mn2+ +¼O2 +3/2H2O® MnOOH + 2H+ Ec.4
Caracterizar las aguas ácidas de mina en función a la acidez ayuda a elegir el sistema de tratamiento más idóneo y eficiente, porque además de la acidez protónica se incluye la acidez mineral, aspecto que por lo general no se considera en los métodos clásicos de caracterización. Un agua de mina, se puede considerar como agua netamente ácida cuando tiene pH menor a 4,5 y elevados contenidos de carga metálica.
]]> Para ajustar la eficiencia del sistema de tratamiento, es recomendable determinar curvas de acidez del agua a tratar, que se elaboran por adición de iones OH- provenientes de una base o álcali (solución de NaOH al 0,02N), los contenidos de acidez suelen cambiar en época seca y húmeda del ciclo hidrológico.
Otro aspecto a tener en cuenta en la elección del sistema de tratamiento, son los rangos de movilización de las especies minerales presentes y/o compuestos que se formarán en el proceso de neutralización (hidróxidos, carbonatos, sulfuros), a fin de evitar la redisolución de las fases sólidas formadas y el consumo innecesario de material o reactivo de neutralización (ver Figura 2).
Por lo general, el Fe3+ disuelto presente en aguas ácidas forman fases sólidas a pH menor a 4,5 y si no se les retira del proceso de tratamiento a pH mayor a 5 se redisuelven y pasan nuevamente a la fase líquida. De igual forma la movilización y redisolución de las fases sólidas del Aluminio (hidróxidos de aluminio) formadas en los procesos de neutralización se produce generalmente en rangos de pH de 3,7 y 5 y si no se les retira del tratamiento a pH mayor a 6 se redisuelven y pasan nuevamente a la fase líquida (Fig. 2), en ambos casos esto incrementa los costos de tratamiento y el volumen de lodos, además de reducir la efectividad del tratamiento.
5. GESTION DEL AGUA EN ZONAS MINERAS
La legislación sobre aguas en el sector minero de Perú contempla dos tipos de Aguas principalmente: las relacionadas a cursos de aguas naturales ubicadas aguas arriba del área minera o aguas que discurren en áreas cercanas al proyecto, que representan la base hidrológica de la zona y pueden recibir descargas de mina y que corresponden a lagunas, quebradas y ríos generalmente, denominadas Cuerpos Receptores cuya concentración se mide en concentraciones totales, y los Efluentes de Mina que son las descargas que se producen desde el interior de las labores mineras, que están reguladas por la R.M. 011-96-EM y el D.S. 010-2010-MINAM de descarga de efluentes líquidos procedentes de actividades minero-metalúrgicas.
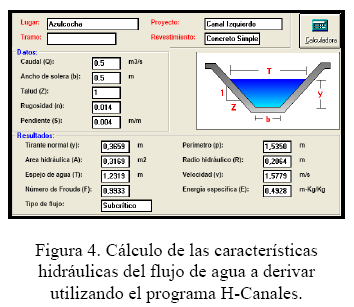
]]> La gestión del recurso hídrico se inicia con la delimitación de la cuenca o subcuenta en donde se emplazan las instalaciones mineras, y se identifican las aguas con y sin afección, es decir, si son efluentes o cuerpos receptores, tal como se puede ver en la Figura 3. Además esto permite ubicar los puntos de monitoreo y control de la aguas superficiales del lugar (cuerpos receptores y efluentes).Por otro lado, para evitar el ingreso de las aguas superficiales a las labores mineras y reducir el volumen de agua a tratar como efluente, es necesario conducir las aguas por separado. Por lo general las aguas limpias sin afección son conducidas a través de los canales de derivación o coronación hacia aguas abajo de las instalaciones mineras (cuerpos receptores), y las aguas de mina denominas efluentes conducirlas mediante un canal colector o una red de tuberías a la planta de tratamiento (Fig. 3) y finalmente el agua tratada descargarla a un curso receptor si cumple con los estándares ECAs vigentes.
A partir de la data obtenida de las estaciones meteorológicas más cercana a la zona del proyecto, se toma la información de la precipitación del lugar y las características de la cuenca aportante, se determina el caudal de diseño para dimensionar la sección de los canales de coronación que evitan el ingreso de de las aguas superficiales hacia los Depósitos e instalaciones mineras a proteger.
Estándares de Calidad Ambiental (ECA´s): Son medidas que establecen el nivel de concentración de elementos, sustancias o parámetros físicos, químicos y biológicos, presentes en el agua, en su condición de cuerpo receptor, que no representa riesgo significativo para la salud de las personas ni al ambiente. Son un referente obligatorio en el diseño de las normas legales, las políticas públicas y el diseño y aplicación de todos los instrumentos de gestión ambiental. La Ley establece que los ECAs de Agua son referentes obligados en la certificación ambiental. Estos ECAs reemplazan a los Límites establecidos en la Ley General de Aguas (actualmente derogada por la Ley de Recursos Hídricos), y han sido promulgados mediante D.S. 002-2008-MINAM (ECA de Agua) y D.S. 023-2009-MINAM que se aplican en la determinación de la calidad de las aguas de los cuerpos receptores.
Límites Máximos Permisibles (LMP´s): Son medidas de la concentración o del grado de elementos, sustancias o parámetros físicos, químicos y biológicos, que caracterizan a un efluente o una emisión, que al ser excedida causa o puede causar daños a la salud, al bienestar humano y al ambiente. Su cumplimiento es exigible legalmente por la respectiva autoridad competente.
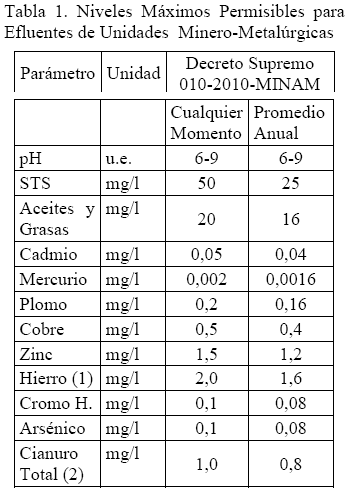
Nota:
]]> (1) Concentraciones de metales disueltos.(2) 1,0 mg/l de cianuro total es equivalente a 0,1 mg/l CN libre y 0,2 mg/l CN wad.
Estos límites máximos permisibles para efluentes líquidos descargados hacia el ambiente por las unidades minero-metalúrgicas nuevas o en operación están contemplados en el D.S. 010-2010-MINAM, y deben medirse en los puntos de descarga a fin de determinar la concentración de cada uno de los parámetros regulados y el volumen de descarga en metros cúbicos por día. Finalmente, el volumen de los efluentes determinará la frecuencia del monitoreo, así como la periodicidad del reporte a remitir a la autoridad correspondiente.
6. DIMENSIONADO DE PLANTAS DE NEUTRALIZACION
Una de las variables para el diseño de la planta de tratamiento es el consumo de material reactivo necesario para alcanzar la neutralización de los efluentes. Esta tasa de consumo experimental junto con las características hidráulicas y geoquímicas ayuda a determinar el tamaño de los dispositivos de tratamiento.
Para determinar el consumo de material reactivo necesario para neutralizar los efluentes de mina, se realizan una serie de ensayos en laboratorio, con el fin de determinar experimentalmente el tamaño de los dispositivos de tratamiento, la secuencia de la operación y los tiempos de tratamiento en cada etapa y/o dispositivo.
Para ello, se toman muestras de agua en los puntos de descargas de aguas ácidas y en laboratorio se realizan una serie de ensayos de neutralización por etapas con separación de sólidas formados en el proceso y ensayos directos de neutralización de una sola etapa. El equipo utilizado en laboratorio incluye pHmetro, vaso de precipitados, agitador magnético, balanza de precisión, medidor del potencial redox, tal como se puede observar en la siguiente Foto.

6.1. Ensayos experimentales
Las curvas experimentales del consumo de reactivo requerido para abatir la acidez de las aguas de mina hasta su neutralización y eliminación de carga contaminante, se realizaron mediante valoradores empleando NaOH y ensayos de neutralización en donde se emplearon cal como reactivo.
La muestra procedente de las labores mineras que drenan aguas acidas se subdividen con la finalidad de obtener la mayor cantidad de ensayos y obtener un gran número de Curvas de Neutralización y detectar las zonas de hidrólisis y/o de tamponamiento de los elementos Fe, Al, Zn principalmente, en donde se forman las fases sólidas en forma de hidróxidos, mediante el cual la carga metálica pasa de fase disuelta a fase sólida, condición en donde se puede realizar la separación sólido-líquida.
Estos ensayos de Neutralización se realizan cumpliendo parámetros de calidad que cuiden la originalidad y representatividad de las muestras de agua de mina recolectadas en campo. A continuación se presentan algunos ensayos realizados:
6.1.1. Ensayos Directos.
Los ensayos directos de una sola etapa se realizaron a efluentes ácidos con contenidos de Fe, AL, Cu, Zn, Mn inferiores a 200 mg/l y consiste en realizar el proceso de neutralización en una sola etapa hasta alcanzar el pH de 8 o 9, en donde, después de un tiempo de decantación se obtenía una separación sólido líquida como la que se observa en la Foto 2. Este proceso funciona de forma similar a las plantas de tratamiento de aguas acidas en operación en las distintas explotaciones mineras.
6.1.2. Ensayos por Etapas.
]]> Se suele realizar ensayos por etapas cuando los contenidos de AL y Zn en las aguas de mina son significativos (superior a 1000 mg/l), el objetivo era obtener en cada etapa un lodo con elevado contenido metálico que podía enviarse a la planta concentradora o a un proceso similar para su recuperación, y en algunos casos destinarlos a una nueva aplicación como los lodos con elevada contenido de aluminio a la mejora del Anfo como explosivo y obtener anfo aluminizado.En la Foto 3 se muestra los lodos obtenidos en un ensayo de neutralización de tres etapas: en la primera etapa se alcanzo el pH 4 y se retiraron lodos de color ocre naranja (M-1) que corresponden a hidróxidos de Fe principalmente, en la segunda etapa se continuo con el proceso de neutralización hasta alcanzar el pH 5,5 en donde se obtuvieron lodos de color blanquecino (M-2) correspondiente a los hidróxidos de Al mayoritariamente, y finalmente en la tercera etapa de tratamiento el pH alcanzo valores superiores a 8,5 en donde se recupero un lodo marrón oscuro a negro (M-3) que corresponde a las fase sólidas de Zn como compuesto mayoritario y en menor proporción al resto de elementos como Mn, Mg, Pb presentes en el agua de mina que pasaron a fase sólida a pH superiores al neutro.
Si no se retiran los lodos de Fe y Al del proceso de tratamiento, a pH superiores al rango de movilización de estos elementos 4 y 5,5 respectivamente, estas fases sólidas formadas se redisuelven y pasan nuevamente al agua, por lo que se requeriría añadir mayor cantidad de material alcalino (cal) para hacer que formen nuevamente fases sólidas (pH 8) y poder retirarlos del agua, lo que hace que en el proceso se incremente el consumo de cal, por tanto, el costo de tratamiento de las aguas ácidas de mina sea más elevado.
6.2. Procedimiento típico de neutralización por etapas.
Después de realizar un gran número de ensayos de neutralización en laboratorio, para determinar los rangos de movilización de los elementos mayoritarios presentes en las aguas ácidas de mina y el consumo de cal en el tratamiento, se ha elegido un drenaje tipo presentado en la Tabla 2, que tiene pH<3 y concentraciones de Fe, Al, Mn, Zn y otros, y cuyos resultados se presentan a continuación.
Este ensayo se realizó con una muestra de 500 ml y por los contenidos metálicos en el agua se ha diseñado un tratamiento en dos (2) etapas, en la primera etapa se alcanzó pH 6 y se retiraron los lodos con Fe y Al, en la segunda etapa el tratamiento alcanzo pH 9 que es el pH límite que contemplan las normas vigentes en el sector minero de Perú, y en donde se obtuvo un sedimento con elevado contenido de Zn con posibilidades de recuperación.
En las Figuras 4 y 5 se pueden observar las curvas de consumo de cal y de la evolución del redox durante el proceso de neutralización. La Figura 4 muestra las zonas de formación de fases sólidas o tamponamiento debido a la hidrólisis de Fe, Al y Zn principalmente, estas zonas corresponden con los rangos de pH en donde se forman fases sólidas de estos elementos. Según se incrementa el pH en el tratamiento del drenaje de mina, los valores de Eh descienden hasta valores de 50 mV que corresponden a aguas naturales sin afección, por lo general el rango de Eh de las aguas ácidas de mina esta entre 400 a 850 mV.
]]>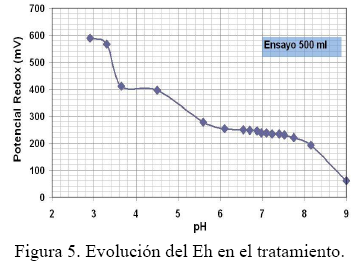
Por la forma de las curvas y los resultados en el ensayo de laboratorio, es acertado proponer que el tratamiento de este efluente debe realizarse en dos (2) etapas: la primera etapa abarcaría hasta alcanzar el pH = 6 en donde se retirarían las fases sólidas de Fe, Al y Mn (parcialmente), luego se continuaría con el proceso añadiendo cal hasta alcanzar el pH 9, en esta segunda etapa se retiraría los lodos formados mayoritariamente por hidróxidos de Zn y otros elementos en menor cantidad como Pb, Mn. Los lodos obtenidos en la segunda etapa se podrían enviar a planta concentradora para su recuperación junto con el concentrado de Zn principalmente.
En la Figura 4 se han marcado 3 zonas de tamponamiento sobre la curva de consumo de cal (acidez equivalente), indicada por el pH y los cambios de la pendiente de la curva, de donde se deduce la cantidad de cal que se necesita para retirar del agua los contenidos de Fe, Al y Zn en forma de fases sólidas.
Las zonas de hidrólisis en rango ácido correspondiente al Hierro (pH 3 - 3,7) y al Aluminio (pH 4,5 5-8), representa el retiro de carga metálica del agua que a su vez genera acidez, dando como resultado el tamponamiento temporal del sistema, manifestada en las siguientes reacciones:
Fe3+ + 3 H2O ® Fe(OH)3 + 3 H+ Ec. 5
Al3+ + 3 H2O ® Al (OH)3 + 3 H+ Ec. 6
A partir del pH 6 hasta pH 8 también se ve un tamponamiento del sistema en este caso inducido por el elevado contenido de Zn en este efluente.
En la Foto 4 se observan las fases sólidas obtenidas en el ensayo: en la 1ª etapa los sólidos tienen una coloración marrón-naranja en donde las fases mayoritarias son los hidróxidos de hierro y aluminio, en la 2ª etapa los sólidos obtenidos al final del ensayo a pH 9,0 tiene una coloración marrón oscura que correspondería mayoritariamente a las fases sólidas de Zn (hidróxidos de Zinc).
]]> El tiempo de duración de este ensayo es algo mayor a los ensayos directos de una sola etapa, debido a que se hace una parada para que decanten y precipiten las fases sólidas formadas y poder retirarlas del sistema, después del tiempo de reposo se continúa con el ensayo añadiendo cal para seguir con el proceso de neutralización.6.3. Diseño de la planta de neutralización.
Con los resultados obtenidos en los ensayos se procede al dimensionado del sistema de tratamiento para cada tipo de agua de mina, cuidando que el pH final y la carga metálica del agua tratada (neutralizada) cumpla con los límites máximos y estándares referenciales contemplados en la legislación minero-ambiental vigentes en el sector minero de Perú, como: los Límites Máximos Permisibles del D.S. 010-2010-MINAM, así como en los ECA de Agua (D.S. 002-2008-MINAM y D.S. 023-2009-MINAM).
Consumo de Cal en la planta diseñada
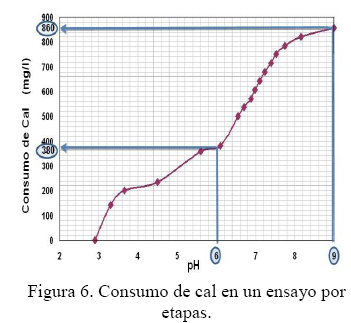
En el tratamiento por etapas, para pasar a fase sólida los contenidos de Fe y Al se requiere alcanzar el pH 6 y para ello se gastarán 380 g/l de Cal, y para pasar todo el Zn contenido en el agua a fase sólida se debe añadir Cal hasta llegar a pH 8 o 9 en donde el consumo de cal alcanza los 860 mg/l (Fig. 6). Si no se retira los lodos de la primera etapa, estos pueden redisolverse y pasar nuevamente al agua del sistema, por lo que habrá que añadir más cal para precipitarlos por sobresaturación, haciendo más costo el tratamiento de las aguas ácidas.
Comparando este consumo de Cal en una planta de 2 etapas con un tratamiento directo en 1 sola etapa el ahorro de Cal representa entre 15 a 20 %, además de que en el proceso por etapas es posible recuperar Zn de los lodos de la segunda etapa.
En general los procesos de neutralización con cal permiten cumplir con los límites de descarga para metales pesados e incluyen básicamente 4 actuaciones o pasos:
La aplicación de un tratamiento de aguas ácidas por etapas, permite obtener lodos con características bien definidas y de similares características, con posibilidades de recuperar metales de los lodos de proceso.
El agua del proceso de tratamiento se puede descargar a un curso de agua natural del lugar, previo control de su calidad a fin de causar el mínimo impacto ambiental.
Los lodos que no tengan interés de recuperación se almacenarán en depósitos adecuados para ello o se envian al depósito de relaves.
Ensayos de Floculación
Para mejorar la eficiencia en la separación de sólidos, se suelen realizar ensayos de floculación o coagulación con el objeto de determinar la dosis y el tipo de floculante mediante el Test de Jarras.
Respecto al floculante elegido (FeSO4, FeCl3 u otro), el procedimiento que se sigue, consiste en adicionar Cal hasta alcanzar el pH de tratamiento (pH=8,5-9), luego dividir el agua del proceso de neutralización en 6 volumen iguales (1 litro), posteriormente y con la debida agitación adicionar simultáneamente a cada muestra diferentes dosis de floculante y seguir un programa de agitación, iniciando con agitación rápida para seguir por agitación media y luego dejar sedimentar los lodos formados en el proceso de neutralización.
]]>7. CONCLUSIONES.
La caracterizar las aguas ácidas de mina en función a la acidez ayuda a elegir el sistema de tratamiento más idóneo y eficiente, ya sea mediante sistemas activos o semi-pasivos, porque además de la acidez protónica se incluye la acidez mineral, aspecto que por lo general no se considera en los métodos clásicos de caracterización.
El dimensionado del sistema de tratamiento para aguas ácidas basado en el contenido de acidez y por etapas, por un lado, permite aprovechar mejor los recursos gastando menos cal en el proceso de neutralización, y por otro, permite recuperar metales de los lodos del proceso. Esto hace que los tratamientos de aguas ácidas sean más eficientes, de menor costo y de mayor control ambiental.
REFERENCIAS.
1. Aduvire, O. and Aduvire, H. (2005) Aguas ácidas de mina: caracterización, mineralogía y microbiología. Ingeopres 141, pp. 52-62. [ Links ]
2. Aduvire, O., Escribano, M., García-Bermudez, P., López-Jimeno, C., Mataix, C. y Vaquero, I. (2006). Manual de construcción y restauración de escombreras. Ed. U. D. Proyectos (ETSIM-UPM). 633pp. ISBN: 84-96140-20-2. [ Links ]
3.Alpers, C. y Blowes, D. (1992). Environmental geochemistry of sulfide oxidation. National Meeting of the American Chemical Society. Washington, DC. 325-342. [ Links ]
4. Bigham, J.M., Schwertmann, U., Carlson, L. y Murad, E. (1990). A poorly crystalized oxyhydroxysulfate of iron formed by bacterial oxidation of Fe(II) in AMD. Geochimica Cosmochimica Acta, 54, 2743-2754. [ Links ]
5.Bigham, J.M. y Nordstrom, D.K. (2000). Iron and aluminum hydroxysulfates from acid sulfate waters. En: Alpers, C.N., Jambor, J.L. y Nordstrom, D.K. (eds), Sulfate minerals: crystallography, geochemistry and environmental significance. Reviews in Mineralogy & Geochemistry, MSA, Virginia. USA. (40), 350-403. [ Links ]
6.Hammarstrom, J.M., Seal II, R., Meier, A. and Kornfeld, J. (2005) Secondary sulfate minerals associated with acid drainage in the Eastern US: recycling of metals and acidity in surficial environments. Chemical Geology 215, pp. 407-431. [ Links ]
7.Jönsson, J., Jönsson, J. and Lövgren, L. (2006) Precipitation of secondary Fe(III) minerals from acid mine drainage. Applied Geochemistry 21, pp. 437-445. [ Links ]
8. MEND. Mine Environment Neutral Drainage. (2005). List of Potential Information Requirements in Metal Leaching/Acid Rock Drainage Assessment and Mitigation Work. MEND Report 5.10E. [ Links ]
9.Swedlund, P. and Webster, J. (2001). Cu and Zn ternary surface complex formation with SO4 on ferrihydrite and schwertmannite. Applied Geochemistry 16, pp. 503-511. [ Links ]
10. Stumm, W. y Morgan, J. (1981). Aquatic chemistry. Wiley Iterscience. 470pp. [ Links ]
11. Walton, K. (1992). Microbiological and chemical characteristics of an stream draining a disused copper mine. Environmental Pollution, 76, 169-175. [ Links ]
12. Williams, T. y Smith, B. (2000). Hydrochemical characterization of acute acid mine drainage. Environmental Geology, 39 (4-5), 272-278. [ Links ]
]]>