

Micropropagación de dos variedades de frutilla (Fragaria Ananassa Duch.) En diferentes medios de cultivo
Micropropagation of two varieties of strawberry (Fragaria ananassa Duch.) in different culture media
Mamani-Sánchez Beatriz1, Murillo-García Rafael Adolfo2
1Departamento de Investigación y Proyectos, Unidad Académica Campesina Carmen Pampa, Universidad Católica Boliviana San Pablo, Bolivia. beita.mamani@gmail.com
2Docente, Facultad de Agronomía, Universidad Mayor de San Andrés, Bolivia. rafomurillo@gmail.com
Artículo recibido en: 17 de marzo 2020 Aceptado en: 20 de junio 2020
Resumen
Las frutillas se propagan de forma asexual, lo que ocasiona una disminución del rendimiento, pérdida de la calidad del fruto y degeneración por acumulación de enfermedades. Una alternativa para obtener material vegetal de alta calidad fitossanitária es a traves de la micropropagación. El objetivo del presente trabajo fue determinar un protocolo de micropropagación de dos variedades de frutilla (Oso grande y Sweet charlie). Se emplearon dos tipos de explantes (yemas de estolones y corona) y fueron sometidos a diferentes tratamientos de desinfección variando concentraciones de NaClO y tiempos de inmersión. En las fases de mulitiplicación y enraizamento in vitro las dos variedades fueron sembradas el medio MS con 0.5, 1 y 1.5 mg L-1 de BAP (se adicionó 0.5 mg L-1 AIB a los medios de cultivo) y al 25, 50 y 75% de MS respectivamente. La sala de crecimiento se registró una temperatura promedio de 24ºC con un fotoperíodo de 16/8 horas de luz/oscuridad y una intensidad lumínica de 1800 lux. La desinfección fue adecuada para los explantes de corona con NaClO al 2% por 25 minutos y para estolones con NaClO al 0.8% por 13 minutos. Este último regenero en menor tiempo (13 días) en comparación a las de corona que requirieron 28 días. En la multiplicación, en el primer subcultivo ambas variedades llegaron a obtener mayor cantidad de brotes en el medio MS+0.5 mg L-1 de BAP+0,5 mg L-1 de AIB. Sin embargo, en el segundo y tercer subcultivo Sweet Charlie generó mayor número de brotes en el medio MS+1 mg L-1 de BAP+0.5 mg L-1 de AIB y Oso Grande en el médio MS+0.5 mg L-1 de BAP+0.5 mg L-1 de AIB. Para el enraizamiento los medios al 50 y 75% de concentración de MS fueron los más adecuados en ambas variedades, por el contrario al 25% de concentración de MS mostraron síntomas de deficiencia de fósforo y nitrógeno.
Palabras clave: Fragaria ananassa Duch, in vitro, micropropagación, explante, medio de cultivo
Abstract
Strawberries spread asexually, causing a decrease in yield, loss of fruit quality and degeneration due to the accumulation of diseases. An alternative to obtain high-quality plant material for plant protection is through micropropagation. The objective of the present work was to determine a micropropagation protocol of two strawberry varieties (Big Bear and Sweet Charlie). Two types of explants (stolon buds and crown) were used and they were subjected to different disinfection treatments, varying NaClO concentrations and immersion times. In the multiplication and rooting phases in vitro, the two varieties were seeded with MS medium with 0.5, 1 and 1.5 mg L-1 of BAP (0.5 mg L-1 AIB was added to the culture media) and at 25, 50 and 75% DM respectively. The growth room registered an average temperature of 24ºC with a photoperiod of 16/8 hours of light / dark and a light intensity of 1800 lux. Disinfection was adequate for crown explants with 2% NaClO for 25 minutes and for stolons with 0.8% NaClO for 13 minutes. The latter regenerated in less time (13 days) compared to those of the crown that required 28 days. In the multiplication, in the first subculture both varieties managed to obtain more shoots in the medium MS+0.5 mg L-1 of BAP+0.5 mg L-1 of AIB. However, in the second and third subcultures Sweet Charlie generated a greater number of outbreaks in the MS medium+1 mg L-1 of BAP+0.5 mg L-1 of AIB and Big Bear in the medium MS+0.5 mg L-1 of BAP+0.5 mg L-1 of AIB. For rooting, the media at 50 and 75% DM concentration were the most adequate in both varieties, on the contrary, at 25% DM concentration, they showed symptoms of phosphorus and nitrogen deficiency.
Keywords: Fragaria ananassa Duch, in vitro, micropropagation, explant, culture medium.
]]> INTRODUCCIÓN
En el departamento de La Paz se tienen muchas variedades cultivadas de frutilla (Fragaria ananassa Duch), siendo las variedades Oso Grande y Sweet Charlie las que presentan mayores rendimientos con respecto a las demás (Ticona, 2000). Los frutos de ambas variedades presentan buena calidad organoléptica, buen sabor, consistencia firme, bajo contenido de acidez y son resistentes durante el transporte (Poma, 2004).
El cultivo de frutilla se propaga en forma asexual, a través de estolones donde cada planta madre genera entre 10 a 12 estolones y cada uno de ellos entre 4 a 6 nuevas plantas; la otra forma de reproducción consiste en el deshijamiento de las plantas madres del mismo cultivar (por división de la corona); aunque, esta última no es muy utilizada por los viveristas (Montecinos, 1993). Ambas formas de reproducción presentan año tras año disminución del potencial de rendimiento, al igual que la pérdida de la calidad del fruto, así como la degeneración del cultivo debido a una infestación acumulada de enfermedades. Otro aspecto importante, es que el ciclo de vida útil del cultivo de frutilla es corto (dos años); transcurrido este tiempo es necesario realizar cambios en los campos de producción para mantener los niveles de productividad (Holmes et al., 2003). De esta manera estos campos requieren refrescar su material vegetal, utilizando para ello plantas madres provenientes de cultivo in vitro para garantizar una producción estable.
Una alternativa para satisfacer la demanda de este tipo de material vegetal, presenta la biotecnología vegetal a través de la micropropagación, la cual consiste en cultivar un explante con potencialidad de diferenciación bajo condiciones asépticas, proporcionándole artificialmente condiciones físicas y químicas para su crecimiento y desarrollo. Esta técnica permite obtener plantas rejuvenecidas con el fin de obtener material vegetal de alta calidad, libre de enfermedades fúngicas y bacterianas; al mismo tiempo permite obtener altas tasas de multiplicación en superficies reducidas, en corto tiempo y en cualquier época del año.
Las plantas obtenidas mediante la técnica de cultivo de tejidos vegetales facilita la posibilidad de obtener plantas madres, que es lo que interesa al productor, ya que a partir de ellas puede desarrollar la primera generación mediante la formación de estolones, la cual estará destinada a la producción. En este sentido, en el presente trabajo de investigación se planteó evaluar el comportamiento in vitro de las variedades de frutilla de Oso Grande y Sweet Charlie para su micropropagación en diferentes medios de cultivo. Al mismo tiempo: a) estandarizar el proceso de desinfección en dos tipos de explantes de frutilla para su introducción a condiciones in vitro, b) identificar el mejor explante de frutilla para su introducción a condiciones in vitro y c) determinar el medio de cultivo óptimo para la multiplicación y enraizamento in vitro de dos variedades de frutilla.
MATERIALES Y MÉTODOS
Ubicación de la zona de estudio
La variedad Sweet Charlie se obtuvo de la carpa solar de la Empresa Agrícola Cabaña La Esperanza ubicada en el municipio de Laja. Mientras, la variedad Oso Grande se consiguió de la carpa solar ubicada en el Campus Universitario de la Facultad de Agronomía dependiente de la Universidad Mayor de San Andrés. En ambos lugares se multiplicaron los estolones y las yemas de corona de ambas variedades.
]]> Metodología
Para la selección de plantas donadoras se tomó en cuenta que estas no muestren síntomas de enfermedades y que presenten características fenotípicas propias de las mismas variedades, en función a ello se realizó la colecta del material vegetal. En el caso, de las yemas de corona se colecto toda la planta y para yemas de estolones se seleccionó los tallos de estolones de aproximadamente unos 20 cm.


Figura 1. Colecta de material vegetal para la extracción de explantes corona (Izq.) y estolón de la variedad Sweet Charlie (Der.).
Las actividades correspondientes al laboratorio se realizaron en la Unidad de Biotecnología Vegetal, dependiente de la Facultad de Ciencias Puras y Naturales de la Universidad Mayor de San Andrés, situada en el Campus Universitario de Cota Cota en la ciudad de La Paz. Todo el experimento de laboratorio se dividió en el establecimiento a condiciones in vitro, multiplicación y enraizamiento.
Establecimiento a condiciones in vitro: El material colectado (yemas de estolones y corona) fue lavado en una solución de agua con detergente y seis enjuagues sucesivos. Posteriormente, ambos tipos de yemas fueron cortadas y colocadas en una solución de ácido cítrico al 0.5%, y luego, sumergidas en alcohol al 70% por 1 minuto y posteriormente fueron sometidas a los tratamientos desinfectantes que consistieron en: hipoclorito de sodio (NaClO) al 2% a diferentes tiempos: T1: 25 minutos y T2: 30 minutos.
Otro grupo de yemas de estolones fueron desinfectadas en ocho tratamientos: A1 (1.5% NaClO 30 minutos), A2 (1.5% NaClO 25 minutos), A3 (1% NaClO 30 minutos), A4 (1% NaClO 25 minutos), A5 (1% NaClO 20 minutos), A6 (1% NaClO 15 minutos), A7 (0.8% NaClO 15 minutos), A8 (0.8% NaClO 13 minutos).
Una vez desinfectadas los explantes dentro de la cámara de flujo laminar se realizaron tres enjuagues con agua destilada estéril, para después colocar las yemas en ácido cítrico al 1% durante tres minutos y finalmente se realizó la siembra en tubos de ensayo con medio de cultivo Murashige Skoog (MS) + 0.1 mg L-1 de AIB + 0.5 mg L-1 de BAP.
Multiplicación: Dentro la cámara de flujo laminar los explantes de ambas variedades fueron transferidos a diferentes medios de multiplicación que consistieron en el medio M.S. suplementado con 0.5 mg L-1 de AIB con variaciones de: 0.5, 1 y 1.5 mg L-1 de BAP respectivamente. Posteriormente, fueron transferidos a la sala de crecimiento por un lapso de 28 días. Durante esta fase se continuó con el repique por dos subcultivos adicionales.
]]> Enraizamiento: Los brotes obtenidos de las dos variedades de la anterior fase fueron sembrados dentro de la cámara de flujo laminar a diferentes medios de enraizamiento MS diluido al 25, 50 y 75% respectivamente suplementados con 1 mg L-1 de carbón activado.Los medios de cultivo empleados fueron ajustados con un pHmetro a 5.6 y para ello se empleó las soluciones de NaOH a 0.1N y ácido clorhídrico al 0.1N. Por otra parte, los materiales de disección (pinzas y mangos de bisturíes), cajas Petri, los medios de cultivo fueron esterilizados en la autoclave a vapor húmedo a 15 PSI durante 15 minutos.
Durante todo el proceso experimental en la sala de crecimiento se reportó una temperatura promedio de 24ºC, fotoperíodo de 16/8 horas de luz/oscuridad, y una intensidad lumínica de 1800 lux. Las variables evaluadas fueron: a) en el establecimiento (porcentaje yemas no desinfectadas, porcentaje de explantes muertos, días a la formación de una hoja in vitro); a) en la multiplicación (número de brotes); c) en el enraizamiento (número y longitud de raíces).
Para la evaluación de los tratamientos de la multiplicación y enraizamiento se utilizó un diseño experimental completamente al azar con arreglo bifactorial, con 15 repeticiones por tratamiento (Calzada, 1970). Los factores de variación fueron la concentración del medio de cultivo con sus respectivos niveles y las dos variedades de frutilla.
Sin embargo, para el análisis de tipo de explante y tratamientos de desinfección se analizó a través del diseño de bloques al azar. Cada experimento con sus respectivos análisis de varianza (ANVA) y cuando se encontraron diferencias significativas entre los tratamientos se aplicó una prueba Duncan (α=0.05) para realizar comparaciones múltiples. La información se analizó empleando el programa estadístico (Sas System versión 8, 1998).
RESULTADOS Y DISCUSIÓN
Establecimiento a condiciones in vitro
Efecto de la desinfección en dos tipos de explantes en dos concentraciones de hipoclorito de sodio
El ANVA denota diferencias significativas (F=4.50; GL1.36; P<0.05) entre explantes en el porcentaje de individuos no desinfectados. No obstante, no se presentó diferencias significativas en tiempo de inmersión al desinfectante (F=0.00; GL1.36; P>0.05). A través de la Figura 2 se evidencia, que el 100% de los explantes de yemas de estolones no presentaron contaminación, pero las yemas de corona solo un 20% no se contaminaron.
]]> Según el ANVA en el porcentaje de explantes muertos mostró diferencias significativas (F=32.40; GL1.36; P<0.05) como efecto de la desinfección entre explantes y no para el tiempo de inmersión (F=3.60; GL1.36; P>0.05). En la Figura 2 se evidencia que los tratamientos desinfectantes dañaron al 100% a las yemas de estolones, las cuales mostraron ser más sensibles y no regeneraron posteriormente en relación con las yemas de corona, probablemente debido a las características propias y al tamaño del explante. Entre tanto, las yemas de corona presentaron un 20 y 60% de explantes muertos al exponerlos a 25 y 30 minutos respectivamente.
Figura 2. Efecto de dos tipos de explantes en el porcentaje de individuos no contaminados y muertos.
Las diferencias reportadas, entre la desinfección de yemas de corona y estolones en cuanto al porcentaje de explantes no contaminados (Figura 2) probablemente se deba a que las yemas de corona, al encontrarse en contacto directo con el suelo sus tejidos fueron más expuestos a agentes contaminantes, dificultando de esta manera la total eliminación de los microorganismos presentes en la superficie del explante, que conlleva a una mayor concentración para su desinfección a diferencia de los estolones. Al respecto, Villalobos y Pérez (1979) citado por Sánchez y Salaverría (2004) mencionan que la alta pubescencia de los tejidos y su contacto directo con el suelo inducen una alta contaminación de los explantes de frutilla, especialmente cuando estos son extraídos de plantas provenientes de campo.
Al reportarse mayor incidencia de mortalidad en yemas de estolones, una de las razones podría ser, que los explantes de las yemas de estolones tenían un menor tamaño (5 a 7 mm) y presentaban tejidos herbáceos, que probablemente de características más sensibles a la desinfección a esa concentración (2% NaClO) y tiempo de inmersión (T1: 25 minutos y T2: 30 minutos).
Mientras, que los explantes provenientes de corona presentaban mayor tamaño (10 a 12 mm) y con tejidos lignificados, razón por lo que estaban más protegidas impidiendo así que el desinfectante ingrese en forma directa hacia los tejidos meristemáticos. Al respecto, Villalobos y García (1982), citado por Jiménez (1999), indican que el tamaño del explante es un factor que influye en la desinfección y regeneración de plantas, a medida que el explante es más pequeño es menor el riesgo de contaminación y más difícil su regeneración. Por su parte, Gómez (1999) menciona que la concentración y el tiempo de exposición necesaria para una desinfección adecuada, varían considerablemente en función al tipo de explante utilizado.
Además, es importante mencionar que las yemas de estolones presentaron mayor grado de oxidación en comparación con las coronas. Esto podría deberse, a que si bien ambos explantes fueron sumergidos en ácido cítrico al 1% (antioxidante) durante tres minutos previo a la siembra al medio de cultivo este hecho solo favoreció a los explantes de corona. Siendo esta práctica utilizada para contrarrestar el efecto de la oxidación fenólica de los explantes (Jiménez, 1999). Por otro lado, es probable que la alta concentración de NaClO y las características de los estolones, el enjuague de estos explantes no haya sido suficiente para eliminar los restos de NaClO, ya que este último además de ser un desinfectante, también es un agente oxidante (Roca y Mroginski, 1991).
Efecto de la desinfección de yemas de estolones en diferentes tratamientos desinfectantes
La variable porcentaje de explantes muertos, el ANVA presentó diferencias estadísticas (F=9.60; GL7.63; P<0.05) para los tratamientos de desinfección de yemas de estolones. Mediante la prueba de Duncan (a=0.05) en la Figura 3, se evidencia que el mejor tratamiento desinfectante en yemas de estolones fue el A8 (0.8% NaClO*13 minutos), es decir, cuando la concentración del hipoclorito de sodio fue baja y tiempo de exposición reducido.
]]>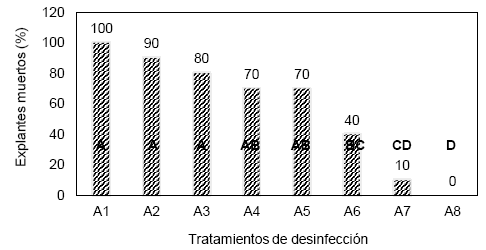
Figura 3. Efecto de los tratamientos desinfectantes en explantes provenientes de estolones en el porcentaje de explantes muertos. A1 (1.5% NaClO 30 min), A2 (1.5% NaClO 25 min), A3 (1% NaClO 30 min), A4 (1% NaClO 25 min), A5 (1% NaClO 20 min), A6 (1% NaClO 15 min), A7 (0.8% NaClO 15 min), A8 (0.8% NaClO 13 min). Letras iguales no son estadísticamente diferentes.
Al registrarse mayor mortalidad entre 100 a 40% en las yemas de estolones en los tratamientos: A1 (1.5% NaClO 30 minutos), A2 (1.5% NaClO 25 minutos), A3 (1% NaClO 30 minutos), A4 (1% NaClO 25 minutos), A5 (1% NaClO 20 minutos), A6 (1% NaClO 15 minutos) (Figura 3) y con ello se constata que concentraciones de NaClO comprendidas entre 1.5 a 1.0% en tiempos comprendidos entre 30 a 15 minutos no son adecuadas para la sobrevivencia de este tipo de explantes (estolones). Este patrón de resultados concuerda con Sánchez y Salvatierra (2004) quienes señalan que en frutilla a medida que se aumenta la concentración de hipoclorito y tiempo de inmersión causan la muerte a los explantes, a pesar que la contaminación de los explantes disminuye.
No obstante, los tratamientos A7 (0.8% NaClO 15 minutos), A8 (0.8% NaClO 13 minutos) donde la concentración de NaClO es de 0.8% y tiempos de inmersión relativamente corto para yemas de estolones es más exitoso la sobrevivencia. Bhojwani y Razdan (1983) señalaron que la concentración de 0.3 y 0.6% de hipoclorito de sodio durante 15 a 30 minutos es suficiente para descontaminar la mayoría de los tejidos y por ello recomiendan tener cuidado con las dosis del desinfectante y el tiempo de inmersión seleccionado, ya que todos los desinfectantes son dañinos para los tejidos.
Además de considerar la selección de las plantas madres con respecto a su estado sanitario y juvenil. Según Boxus (1999) indica que también, la estación juega un rol importante en la reducción de desinfección en frutilla. En el presente estudio las yemas de estolones fueron colectadas en verano finalizando la época de lluvias, probablemente sea esta una de las explicaciones de no requerir altas concentraciones de NaClO para la desinfección como emplearon Moradi et al (2011) 4% de hipoclorito de sodio por 20 minutos con una gota de Tween 20. De acuerdo al protocolo de desinfección usado por ElKichaou (2014) el método de esterilización empleado fue sumergiendo los explantes a una solución de hipoclorito al 1.5% con 2 a 3 gotas de Tween 20/100 ml durante 20 minutos y 0.1% HgCL2 por 10 minutes donde se obtuvo una asepsia adecuada de los explantes colectados en agosto que de octubre.
Tipo de explante
Para comparar el tiempo que transcurre en formar una hoja in vitro se utilizó el mejor tratamiento desinfectante de yemas de estolones (0.8% NaClO*13 minutos) y corona (2% NaClO*25 minutos). El estadístico mostró diferencias significativas existentes entre explantes (F=1045926; GL1.9; P<0.05). Las yemas procedentes de estolones en un lapso de 13 días llegaron a desarrollar una hoja, mientras que las yemas de corona requirieron 28 días es decir dos veces más que los estolones. El hecho que los explantes de estolones desarrollen menos tiempo (13 días) que las procedentes de corona de 28 días. Estos resultados se atribuyen al estado fisiológico del explante; en razón de que las yemas de estolones se encuentran en estado de crecimiento activo debido a que en condiciones naturales este material vegetal se encuentra en proceso de multiplicación vegetativa, característica que favoreció en una mejor respuesta in vitro. Al respecto, Jiménez (1999) indica que a medida que el tejido sea más joven y menos diferenciado mejor será su respuesta in vitro.

Figura 4. Explante procedente de yema de estolón de la variedad Sweet Charlie, que regenera en un tiempo promedio de 13 días desde la introducción.
La regeneración de los explantes de frutilla está comprendida entre los 3, 8 y 12 días después de la siembra en segmentos nodales y el porcentaje de explantes regenerados varía, en función a los medios de cultivo, es así que Moradi et al (2011) reporto un 100% de regeneración de explantes de frutilla con MS+0.2 mg L-1 KIN+0.5 mg L-1 BAP. Por lo que, se podría señalar que en el presente estudio está enmarcado dentro del tiempo de regeneración y que el medio empleado de MS+0.1 mg L-1 IBA+0.5 mg L-1 BAP fue propicio para su regeneración de una hoja en condiciones in vitro, ya que la presencia de citocininas como BAP, KIN son promotores de crecimiento.
]]> MultiplicaciónEn el primer subcutivo, el ANVA detectó diferencias significativas entre variedades y medios de cultivo para el número de brotes (F=4.46; GL1.84; P<0.05) y (F=3.73; GL2.84; P<0.05) respectivamente. Sin embargo, la interacción del factor variedad y medios de cultivo no presentaron diferencias significativas (F=1.10; GL2.84; P>0.05). En relación al efecto de las variedades, Oso Grande generó mayor número de brotes que Sweet Charlie de 6 y 5 brotes respectivamente. Los medios suplementados con MS+0.5 mg L-1 de BAP+0.5 mg L-1 de AIB y MS+1 mg L-1 de BAP+0.5 mg L-1 de AIB fueron estadísticamente similares y en las que obtuvieron mayor cantidad de brotes (6.1 y 5.9) con relación al medio con 1.5 mg L-1 de BAP+0.5 mg L-1 de AIB (4.6 brotes).
En el segundo subcultivo el ANVA indica diferencias altamente significativas entre variedades, medios de cultivo y la interacción de los factores (F=23.08; GL1.84; P<0.05); (F=6.29; GL2.84; P<0.05) y (F=8.98; GL2.84; P<0.05). Donde, Oso Grande fue la que obtuvo mayor número de brotes (10.6) que Sweet Charlie llegó a formar 7.4 brotes por explante. Con respecto a los medios de cultivo, los que estaban suplementados con MS+0.5 mg L-1 de BAP + 0.5 mg L-1 de AIB y MS+1 mg L-1 de BAP + 0.5 mg L-1 de AIB fueron estadísticamente similares y en los que promovieron mayor número de brotes de 10.4 y 9.3 respectivamente. En cambio, el medio con MS + 1.5 mg L-1 de BAP + 0.5 mg L-1 de AIB fue estadísticamente diferente a los anteriores medios y el menos favorable para la formación de brotes axilares en frutilla con 7.3.
En la Tabla 1 se muestra los resultados de la interacción de factores, donde se observa que Sweet Charlie generó una mayor cantidad de brotes en el medio MS + 1 mg L-1 de BAP + 0.5 mg L-1 de AIB; en cambio, la variedad Oso Grande en el medio MS + 0.5 mg L-1 de BAP + 0.5 mg L-1 de AIB incrementó el número de brotes.
Tabla 1. Efecto de la interacción de las variedades según la concentración de BAP en el número de brotes durante el segundo subcultivo.
Para el tercer subcultivo el ANVA detecto diferencias altamente significativas entre las variedades (F=42.62; GL2.84; P<0.05), medios de cultivo (F=40.46; GL2.84; P<0.05) y la interacción (F=12.06; GL2.84; P<0.05). Entre variedades, Oso Grande obtuvo mayor número de brotes con respecto a Sweet Charlie de 10.7 y 6.4 brotes respectivamente. Entre medios de cultivo, los medios de cultivo con MS + 0.5 mg L-1 de BAP + 0.5 mg L-1 de AIB y MS + 1 mg L-1 de BAP + 0.5 mg L-1 de AIB fueron estadísticamente similares y estos medios promovieron mayor número de brotes (10.3 y 11.1 respectivamente) en comparación con el medio con MS+1.5 mg L-1 de BAP + 0.5 mg L-1 de AIB se registró 4.5 brotes.
De la interacción de ambos factores en la Tabla 2 se observa que la variedad Oso Grande en los medios MS+0.5 mg L-1 de BAP+0.5 mg L-1 de AIB y MS+1 mg L-1 de BAP+0.5 mg L-1 de AIB promovieron mayor número de brotes que cuando fue suplementado con 1.5 mg L-1 de BAP+0.5 mg L-1 de AIB. En cambio, Sweet Charlie mostró una mejor respuesta en el medio que contenía MS+1 mg L-1 de BAP+0.5 mg L-1 de AIB logrando formar 10.9 brotes/explante pero, lo contrario sucedió cuando la concentración de BAP aumenta o disminuye.
Tabla 2. Efecto de la interacción de las variedades según la concentración de BAP en el número de brotes durante el segundo subcultivo.
]]> Durante los tres subcultivos ambas variedades se comportaron de forma diferencial en los tres medios de cultivo. Donde Oso grande en el medio MS+0.5 mg L-1 BAP + 0.5 mg L-1 de AIB presentó una buena producción de brotes de 6,11.5 y 14.7. Mientras, Sweet Charlie obtuvo una mayor producción de brotes en el medio MS+1 mg L-1 BAP+0.5 mg L-1 de AIB de 6, 11 y 11 (Figura 5).


Figura 5. Brotes obtenidos en Oso Grande en el medio con 0.5 mg L-1 BAP (Izq.) y Sweet Charlie con 1 mg L-1 BAP (Der.).
En los tres subcultivos, Oso Grande fue la que generó mayor producción de brotes en relación a Sweet Charlie. El comportamiento de ambas variedades es probable que se relacione con la capacidad de regeneración de brotes y viene determinado por el genotipo, como indica Pierik (1990). Esta afirmación es respaldada por Villegas (1990), quien menciona que no todas las variedades de frutilla responden de forma similar durante la multiplicación in vitro, por lo que el número de brotes es variable. Sin embargo, el medio con MS+1.5 mg L-1 de BAP+0.5 mg L-1 de AIB indujo una menor formación de brotes en ambas variedades. Dicha afirmación concuerda con Pereira (1998) quien menciona que a medida que se incrementa la concentración de citocininas en el medio para frutilla, observó una disminución en el número de brotes de la variedad Fern. Similares patrones fueron reportados por Ashrafuzzaman et al (2013) quienes trabajaron en frutilla, en concentraciones de 0, 0.5, 1.0, 1.5 y 2mg L-1 respectivamente obtuvo 2, 7, 4, 2 y 0 brotes respectivamente.
Las variaciones registradas en cuanto al número de brotes en el presente estudio concuerdan con Ramírez y Barrera (1998) quienes trabajaron con las variedades Brighton, Douglas, Fern, Solana, Pájaro y Tioga; las mismas que fueron sometidas a medios con distintas concentraciones de BAP (0.3, 1 y 5 mg L-1) suplementados con 1 mg L-1 de AIB. En este caso, observaron que a medida que se va aumentando la concentración de BAP en el medio se indujo una mejor respuesta en el número de brotes en las cuatro primeras variedades; en cambio, las variedades Pájaro y Tioga disminuyeron la cantidad de brotes.
Ambas variedades estudiadas, a partir del segundo subcultivo incrementaron el número de brotes, lo cual fue esperado, ya que los explantes tienden a acumular citocininas en sus tejidos a medida que se subcultiva en un medio con este regulador de crecimiento. Al respecto, Pérez (2004) indica que la mayor proliferación de brotes axilares recién se logra observar a partir del segundo subcultivo. Orellana (1998), menciona que a medida que aumenta el número de subcultivos hay una tendencia al incremento del número de brotes por explante.


Figura 6. Brotes procedentes de la variedad Oso Grande (Izq.) y Sweet Charlie (Der.).
Enraizamiento
]]> Los ANVAs detectaron diferencias altamente significativas para el número de raíces entre las variedades (F=5.37; GL2.84; P<0.05), medios de cultivo (F=8.45; GL2.84; P<0.05) y la interacción de ambos factores (F=8.31; GL2.84; P<0.05). Entre variedades, Oso Grande fue la que generó mayor número de raíces (6.1) en relación a la variedad Sweet Charlie (5.2). Entre medios de cultivo los estuvieron diluidos al 50 y 75% de las sales del MS generaron mayor número de raíces con valores de 6.3 y 6.4 respectivamente; en cambio, el medio con 25% de MS fue reducido el número de raíces.La Tabla 3 muestra que Oso Grande generó mayor número de raíces en los tres medios de cultivo. Por el contrario, Sweet Charlie logró un mayor número de raíces en los medios diluidos al 50 y 75% de MS en comparación con el medio que estaba diluido al 25% de MS en la que formó menor número de raíces.
Tabla 3. Efecto de la interacción de las variedades según la concentración de MS sobre el número de raíces.
El ANVA para la variable longitud de raíces muestra diferencias altamente significativas entre las variedades y la interacción de los dos factores de estudio (F=7.39; GL1.84; P<0.05) y (F=14.59; GL2.84; P<0.05) respectivamente. Sin embargo, no se detectaron diferencias estadísticas entre los medios de cultivo (F=1.54; GL2.84; P>0.05). Con relación al comportamiento de las variedades, Oso Grande generó mayor longitud de raíces en comparación con Sweet Charlie de 55.6 y 45 mm respectivamente. En la Tabla 4 se observa que Oso Grande al 25% MS generó una mayor longitud de las raíces, en comparación con los medios diluidos al 50 y 75% de MS. Entretanto, Sweet Charlie generó menor tamaño de las raíces en el medio al 25% de MS y cuando la concentración de las sales de MS fue al 50 y 75% obtuvo mayor longitud de la raíz.
Tabla 4. Efecto de la interacción de las variedades según la concentración de MS sobre la longitud de las raíces (mm).
La diferencia observada en la respuesta morfogenética in vitro entre las variedades Oso Grande y Sweet Charlie en el medio MS diluido al 25% viene determinada por el genotipo como afirman Grattaplagia y Machado (1990), citado por Calvete et al. (2002). Al respecto, se podría asumir que Oso Grande fácilmente llegó a habituar en este medio por lo que generó mayor longitud de la raíz, lo que no ocurrió con la variedad Sweet Charlie. En relación a este punto, Salisbury y Ross (1994) mencionan que la morfología radicular es controlada por mecanismos genéticos.
La variedad Oso Grande en los tres medios de cultivo (25, 50 y 75% de MS) llegaron a formar raíces el 100% de los explantes sembrados en cambio, los explantes de la variedad Sweet Charlie en el medio diluido al 25% de MS no todos llegaron a formar raíces, pero sí enraizaron en su totalidad en los medios diluidos M.S. al 50 y 75%. Similares resultados fueron observados por Scherwinski et al. (2004) quienes determinaron que las variedades Tangi y Hofla presentaron una favorable respuesta en cuanto al porcentaje de explantes enraizados en los medios diluidos al 50 y 75% de MS. Los resultados obtenidos concuerdan con ElKichaoui (2014) quien señala que en los medios diluidos al 50, 25 y 12.5% de manera proporcional reducen tanto el número y la longitud de raíces en frutilla.
Al mismo tiempo, se observó que los brotes de ambas variedades en el medio con 25% de MS en los márgenes de los foliolos mostraron una coloración rojiza (Figura 7), este hecho probablemente se deba a que, en esta dilución (25%) la concentración de las sales fue menor por lo que las vitroplantas mostraron esta sintomatología. Al respecto, el INTA (2004) menciona que la sintomatología que provoca la deficiencia de fósforo es con frecuencia la apariencia de coloraciones rojas o púrpuras en las hojas. De la misma manera se visualizó que las vitroplantas de ambas variedades presentaban una coloración verde claro en todo el follaje. La respuesta de la planta de frutilla a la carencia de nitrógeno es la reducción en la tasa de crecimiento y las hojas jóvenes de color verde pálido.
]]>

Figura 7. Hojas de las variedades Sweet Charlie (Izq.) y Oso Grande (Der.) con sintomatología de deficiencia de N y P.
Orellana (1998) menciona que el manejo de la concentración de sales es recomendado ampliamente para estimular el enraizamiento, lográndose la formación abundante de raíces al disminuir las sales a la mitad, un tercio o un cuarto de la concentración de los medios; sin embargo, el procedimiento más empleado es la reducción de las sales a la mitad, ya que una disminución mayor puede afectar el desarrollo general de la vitroplanta.
CONCLUSIONES
Una adecuada desinfección de las yemas provenientes de corona se presentó cuando fueron sumergidos en hipoclorito de sodio (NaClO) al 2% durante 25 minutos. Mientras que, en estolones fue con NaClO al 0.8% durante 13 minutos. Las yemas de estolones presentaron una mejor respuesta en condiciones in vitro debido a que regeneraron una hoja en 13 días en relación a las de corona que requirieron 28 días en formar una hoja.
En la fase de multiplicación durante el primer subcultivo en el medio MS suplementado con 0.5 mg L-1 de AIB + 0.5 mg L-1 de BAP ambas variedades (Oso Grande y Sweet Charlie) desarrollaron mayor número de brotes. En el segundo y tercer subcultivo la variedad Oso Grande logró formar mayor número de brotes en el medio con 0.5 mg L-1 de BAP, sin embargo, la variedad Sweet Charlie en el medio con 1 mg L-1 de BAP. De las dos variedades, Oso Grande fue la que desarrolló mayor cantidad de brotes en relación a Sweet Charlie en los tres subcultivos.
Se determinó para el enraizamiento las dos variedades los medios diluidos al 50 y 75% de MS promueven un buen crecimiento y desarrollo tanto de las raíces y del follaje. No obstante, con 25% de la concentración de las sales del medio MS los explantes de ambas variedades presentaron sintomatología de deficiencia de los elementos nutritivos (nitrógeno y fósforo).
BIBLIOGRAFÍA
]]>Ashrafuzzaman, M; Faisal, SM; Yadav, D; Khanam, D; Raihan F. 2013. Micropropagation of strawberry (Fragaria ananassa) through runner culture. Bangladesh J. Agril. Res. 38(3): 467-472. DOI: 10.3329/bjar.v38i3.16973 [ Links ]
Bhojwani, S; Razdan, K. 1983. Plant Tissue Culture. Theory and Practice. Elsevier. New York. 235 p. [ Links ]
Boxus, P. 1999. Micropropagation of strawberry via axillary shoot proliferation. In: Plant Cell Culture Protocols. Methods in Molecular Biology. Part III. Plant Propagation in vitro. Hall R. D. (ed.) Humana Press Inc., Totowa NJ, 111: 103-14. [ Links ]
Calvete, O; Norman, A; Suzin, S. 2002. Concentração de sacarose no enraizamento in vitro de morangueiro (en línea) Horticultura brasileira. v 20, tomo 2. Brasil. Consultado el 15 de oct. 2004. Disponible en http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0102 [ Links ]
Calzada, B. 1970. Métodos estadísticos para la investigación. Lima, Perú. Ed. Jurídica. 640 p. [ Links ]
ElKichaoui, A. 2014. In vitro, Propagation of Strawberry (Fragaria × annanasa Duch.) Through Organogenesis via Runner Tips Biology and Biotechnology Department, Islamic University-Gaza, Gaza strip, PNA. Pp. 619- 627. [ Links ]
INTA (Instituto Nacional de Tecnología Agropecuaria). 2004. Síntomas de deficiencia en el cultivo de frutilla. San Pedro, Argentina. [ Links ]
Gómez, R. 1999. Aplicaciones de la biotecnología en la mejora genética de plantas y la producción de semillas: Cultivo in vitro. Ed. rev. Santa Clara, Cuba. s.e. pp. 32-47. [ Links ]
Holmes, T; Infante, L; Schmidt, F; Vita, J. 2003. Fresa. (en línea). Consultado el 20 dic. 2003. Disponible en: http://www.geocities.com/Athes/Sparta/4704/contacto.htm [ Links ]
Jiménez, E. 1999. Aplicaciones de la biotecnología en la mejora genética de plantas y en la producción de semillas: Propagación Masiva de plantas in vitro. Ed. rev. Santa Clara, Cuba. s.e. pp. 1-46. [ Links ]
Montecinos, J. 1993. Manejo de huertos de frutilla (Fragaria ananassa Duch) en la décima región. Ed. rev. Argentina. s.e. 12 p. [ Links ]
Moradi, K, Otroshy, M; Azimi, MR. 2011. Micropropagation of strawberry by multiple shoots regeneration tissue cultures (en línea). Journal of Agricultural Technology 2011 Vol. 7(6): 1755-1763. Disponible en http://www.ijat-aatsea.com [ Links ]
Orellana, P. 1998. Propagación y mejora genética de plantas por biotecnología; Contaminación microbiana en el cultivo in vitro de plantas. (Pérez, J.). Impreso en Cuba. s.e. pp. 151-178. [ Links ]
Pereira, R. 1998. Determinación del protocolo adecuado para la micropropagación en fresa (Fragaria sp.). Tesis de Lic. Oruro, Bolivia. Universidad Técnica de Oruro. 100 p. [ Links ]
Pérez, J. 2004. Biotecnología Vegetal. (entrevista). Docente de la Carrera de Agronomía de la Escuela Militar de Ingeriría E.M.I. La Paz, Bolivia. [ Links ]
Pierik, R. 1990. Cultivo in vitro de las plantas superiores. Ed. rev. Editorial Mundi-Prensa. Madrid, España. 327 p. [ Links ]
Poma, E. 2004. Productor de frutilla de la carpa solar Cabaña la Esperanza. (entrevista). La Paz, Bolivia. [ Links ]
Ramírez, R. y Barrera, J. 1998. Inducción in vitro de brotes axilares de fresa (Fragaria ananassa Duch.) con distintos reguladores de crecimiento. Acta Universitaria. v. 2, tomo 1. Guanajuato, México. [ Links ]
Roca, WM; Mroginski LA. 1991, Cultivo de tejidos en la agricultura: fundamentos y aplicaciones. Ed. Centro Internacional de Agricultura Tropical, Colombia. 970 p. [ Links ]
Salisbury, F. y Ross, C. 1994. Fisiología vegetal. Ed. rev. México Editorial Iberoamericana. pp. 127-157. [ Links ]
Sánchez, C. y Salaverria JL. 2004. Control de la oxidación y la contaminación en el cultivo in vitro de fresa (Fragaria ananassa Duch.). Revista UDO Agrícola 4 (1): 21-26. [ Links ]
SAS Institute Inc. Statistics Analysis System.Cary, North Carolina, USA. 1998. [ Links ]
Scherwinski, J; Pereira, V; Ferreira, L; Luces, G. 2004. In vitro strawberry (Fragaria x aananassa Duchesne) rooting in different M.S. medium concentrations. [ Links ]
Ticona, V. 2000. Comportamiento de tres variedades de frutilla (Fragaria sp.) en diferentes métodos de cobertura aplicados al suelo bajo carpa solar. Tesis Lic. La Paz, Bolivia. Universidad Mayor de San Andrés. pp. 12-13. [ Links ]
Villegas, A. 1990. Micropropagación de fresa: Fundamento teórico-práctico del cultivo de tejidos vegetales. Estudio de la F.A.O. (Rosell y Villalobos). Roma, Italia pp.184-193. [ Links ]
]]>