
Evaluación de la actividad enzimática del Trichoderma inhamatum (BOL-12 QD) como posible biocontrolador
Evaluation of the enzymatic activity of Trichoderma inhamatum (BOL-12QD) as possible biocontroller
García-Espejo Cielo Noemí1, Mamani-Mamani Marisel Mercedes1, Chávez-Lizárraga Georgina Aurelia1*, Álvarez-Aliaga María Teresa2
1Laboratorio de Biotecnología Fúngica, Instituto de Investigaciones Fármaco Bioquímicas de la Facultad de Ciencias Farmacéuticas y Bioquímicas. Universidad Mayor de San Andrés. Av. Saavedra No 2224 Miraflores. La Paz-Bolivia.
cielitoc3@hotmail.com ]]>
*Dirección de contacto: Laboratorio de Biotecnología Fúngica, Instituto de Investigaciones Fármaco Bioquímicas de la Facultad de Ciencias Farmacéuticas y Bioquímicas. Universidad Mayor de San Andrés. Av. Saavedra No 2224 Miraflores. La Paz-Bolivia.
Tel. +591 (2) 73034060
+591 (2) 2229021
Georgina Aurelia Chávez-Lizárraga
E-mail address: georginacha@gmail.com
Historial del artículo.
Resumen
Se sabe que el Trichoderma spp. actúa como un biocontrolador natural de hongos patógenos, es por eso que este estudio se enmarca en las potencialidades de su actividad enzimática hidrolítica. En este trabajo, primero se determinó que la velocidad de crecimiento de Trichoderma inhamatum cepa BOL-12QD es de 9 horas. Después, proponemos un método simple, sensible basado en el uso de medio basal (MB) con quitina coloidal como única fuente de carbono suplementado con purpura de bromocresol para la determinación cualitativa de actividad quitinasa. Por otro lado se determinó la actividad celulolítica, proteolítica de Trichoderma inhamatum cepa BOL-12QD, se observó que la agitación el tipo, la concentración de sustrato son factores determinantes en la producción enzimática. Así, se evaluó la actividad celulolítica de Trichoderma inhamatum cepa BOL-12QD en agitación y estanco usando como sustrato carboximetilcelulosa (CMC), encontrándose que usando un 2% de sustrato se registra la mayor actividad a los 8 días de incubación en agitación con un valor de 99.23 UI/L. En relación a los resultados de estanco el valor óptimo es al cuarto día con un valor de 92.76 UI/L.
La actividad proteasa se determinó tomando en cuenta variables de agitación y estanco, usando diferentes tipos y concentraciones de sustrato al 2%, 4% y 6% (p/v) de extracto de carne, 1%, 3%, 5% (p/v) de gelatina, 1%, 2%, 4% (p/v) de caseína. La actividad proteasa más alta se obtuvo al cabo del séptimo día, encontrándose una actividad enzimática de 3075.45 UI/L en estanco a una concentración de 6% (p/v) en extracto de carne, usando gelatina al 3% (p/v) en estanco se encontró una actividad 568.36 UI/L al décimo día y en agitación se obtuvo un valor de 547.27 IU/L al doceavo día, mientras que usando caseína al 1% (p/v) en estanco se alcanza una actividad de 407.06 UI/L al quinto día, en agitación al 4% (p/v) de caseína al noveno día un valor de 269.88 UI/L.
La alta actividad de estas enzimas hace que Trichoderma inhamatum cepa BOL-12QD sea un biocontrolador por sus propiedades enzimáticas junto a una gama de mecanismos biológicos.
]]> Palabras clave: Trichoderma, actividad quitinolítica, actividad celulolítica, actividad proteolítica.Abstract
It is known that Trichoderma spp. acts as a natural biocontroller of pathogen fungi, is for this reason, that this research studies the potential of its hydrolytic enzyme activity. In this article, first we determined that the speed of growth of Trichoderma inhamatum cepa BOL-12QD is 9 hours. Later, we proposed a simple and sensitive method based in the use of basal media (BM) with coloidal chitin as the only carbon resource and supplemented with bromocresol purple for the qualitative determination of chitinase activity. On the other hand, it was determined the celullolytic and proteolytic activities of Trichoderma inhamatum cepa BOL-12QD and it was observed that agitation, type and concentration of sustrate are determinant factors in enzymatic production. Then, we evaluated the cellulolytic activity of Trichoderma inhamatum cepa BOL-12QD in agitation and stationary using carboxymethylcellulose (CMC) as sustrate, finding that using a 2% of sustrate the highest activity is registered at 8 days of incubation in agitation with a value of 99.23 IU/L. In relation to the results at stationary the optimal value is at the fourth day with a value of 92.76 IU/L.
The protease activity it was determined taking in consideration variables of agitation and stationary, using different types and concentration of sustrate at 2%, 4% y 6% (w/v) of meat extract, 1%, 3%, 5% (w/v) of jelly and 1%, 2%, 4% (w/v) of casein. The highest protease activity was obtained at the end of the seventh day with an enzymatic activity of 3075.45 IU/L at stationary using a concentration of 6% (w/v) of meat extract, and using jelly at 3% (w/v) at stationary it was found an activity of 568.36 IU/L on the tenth day and in agitation a value of 547.27 IU/L was reached on the twelveth day, while using casein at 1% (w/v) at stationary an activity of 407.06 IU/L is reached in the fifth day, and in agitation at 4% (w/v) of casein a value of 547.27 IU/L is obtained on the twelfth day, while using casein at 1% (w/v) in stationary an activity of 407.06 IU/L is reached on the fifth day, and in agitation at 4% (w/v) of casein in the ninth day a value of 269.88 IU/L is reached.
The high activity of these enzymes made of Trichoderma inhamatum cepa BOL-12QD an biocontroller because of their enzymatic properties along a number of biological mechanisms.
Key words: Trichoderma, chitinolytic activity, cellulolytic activity, proteolytic activity
Introducción
El control biológico involucra el uso de organismos beneficiosos, sus productos, como metabolitos secundarios reduce los efectos patogénicos de fitopatógenos en plantas y promueve una respuesta favorable por parte de esta Trichoderma spp.
]]> Ha sido ampliamente utilizada como un agente antagónico controlador, contra varias enfermedades producidas en plantas y frutos (Espinal 2009).Las especies del género Trichoderma spp. han sido ampliamente estudiadas por sus efectos como agente de control biológico de hongos fitopatógenos (Jayalakshmi et al. 2009). Se han identificado aislamientos con aplicaciones potenciales en el manejo de los hongos fitopatógenos en diversos cultivos de importancia económica empleándose exitosamente como bioplaguicídas en casas de cultivo y en aplicaciones en campo (Küçük & Kývanç 2008).
Los hongos del género Trichoderma spp. están presentes en casi todos los suelos agrícolas. El interés de su estudio proviene esencialmente de sus propiedades enzimáticas, estas facultades de antagonismo de Trichoderma spp. han sido descritas por diferentes autores y actualmente es uno de los microorganismos mayormente utilizados en el campo agrícola.
Trichoderma spp. actúa como biocontrolador afectando la pared celular de otros hongos, proceso que lo realiza mediante la hidrólisis enzimática, durante este proceso, secreta enzimas hidrolíticas como proteasas quitinasas, glucanasas, que hidrolizan la pared celular del hongo patógeno desnaturalizando de esta manera la pared del hongo patógeno (Kubicek et al. 2001) Trichoderma spp. secreta enzimas hidrolíticas cuando detecta presencia de otro hongo en su medio, produciéndose un fenómeno de respuesta enzimática (Kubicek et al. 2001).
Además de los efectos beneficiosos que ocurren en las interacciones con agentes patógenos, algunas especies de Trichoderma spp. también pueden colonizar la superficie de la raíz y causar cambios sustanciales en el metabolismo de la planta. Se estableció también que algunas interacciones sobre la planta, incrementa el crecimiento, aumento la disponibilidad nutriente, mejora la cosecha la producción y refuerza la resistencia a la enfermedad (Harman et al. 2004).
Estas enzimas, quitinasas, glucanasas degradan parcialmente la pared celular de diversos hongos (Zeilinger & Omann 2007), pueden ser inducidas artificialmente, cuando estos hongos son cultivados en medios líquidos suplementados con monómeros de quitina N-acetilglucosamina o con polímeros tales como laminarina, quitina o paredes celulares de hongos (Zeilinger & Omann 2007).
Evaluar la actividad quitinasa implica aplicar métodos colorimétricos (Monreal & Reese 1969) que son tediosos y no aplicables para identificar las cepas microbianas pobres en actividad quitinolítica, ensayos más simples y rápidos con quitina coloidal (fuente de carbono principal) suplementado en medio basal sólido observando un halo característico con un cambio de color debido a la digestión de quitina son las medidas de la actividad quitinasa más confiable, además económica (Rojas-Avelizapa et al. 2002). Sin embargo, este método también tiene una baja sensibilidad y sus resultados dependen de la concentración y el tamaño de las partículas de quitina coloidal, el grosor de los medios y la cantidad y tipo de inóculo (OBrien & Collwell 1987. Entre los organismos con mayor actividad celulolítica se encuentran los hongos, estos presentan características importantes como rápida colonización del sustrato y remoción de productos e hidrólisis, descomponen de forma primaria la materia orgánica, por lo tanto su recuperación se realiza en el suelo y en materiales de compostaje (Ponce & Pérez 2002).
La hidrólisis de la celulosa se realiza mediante un complejo enzimático llamado celulasas, constituido principalmente por tres enzimas: endoglucanasa, exoglucanasa y β-glucosidasas, que son producidas por algunos hongos y bacterias en condiciones normales, generando glucosa, principal producto que puede ser utilizado como fuente de carbono y energía por otros microorganismos fermentadores (Ponce & Pérez 2002).
La interacción de Trichoderma spp. contra el hongo patógeno se produce por un ataque lítico, en esta etapa ocurre la producción de enzimas líticas extracelulares, fundamentalmente quitinasas, glucanasas y proteasas, que degradan las paredes celulares del hospedante y posibilitan la penetración de las hifas del antagonista. Por los puntos de contacto donde se produce la lisis y aparecen los orificios, penetra la hifa del micoparásito en las del hongo hospedante. La actividad enzimática en Trichoderma spp. ha sido estudiada extensamente, así como las posibles funciones que desenvuelven en el micoparasitismo (Infante 2009).
Con base a estos argumentos, la presente investigación tiene como objetivo el determinar las variables que influyen en la producción de enzimas hidrolíticas importantes en el mecanismo de biocontrol en la cepa Trichoderma inhamatum BOL-12QD.
]]>Materiales y métodos
Aislamiento de Trichoderma inhamatum cepa BOL 12 QD. Se trabajó con la cepa liofilizada BOL-12QD del cepario del Laboratorio de Biotecnología Fúngica (LBF) que pertenece a Instituto de Investigaciones Fármaco Bioquímicas (IIFB).
Se activó aproximadamente 2µg de la cepa Trichoderma inhamatum BOL-12QD con un asa bacteriológica estéril, se inoculó en un frasco de 100 mL conteniendo 50 mL de caldo papa dextrosa (CPD) (250 g papa, 20 g glucosa, 1000 mL agua), se incubo a 30 °C en condiciones estanco y de agitación a 100 rpm (Shaker Innova 44) durante 7 días hasta crecimiento micelial (Castellanos et al. 2013). Para asegurar un correcto aislamiento se siguió el protocolo propuesto por Espinal 2009 con algunas modificaciones. Se tomaron 10 µL de caldo de ambos cultivos, se sembraron en placas Petri conteniendo agar papa dextrosa (PDA) (250 g papa, 20 g glucosa, 20 g agar, 1000 mL agua). En una segunda resiembra se tomaron 5 mm de agar con micelio de la placa Petri con un sacabocados estéril, se sembró en una nueva placa Petri con el mismo medio, la misma se dejó incubando a 30 °C durante 7 días hasta observar crecimiento.
Lavado monospórico. Esta técnica se realizó con la finalidad de conseguir un cultivo axénico (Castellanos et al. 2013). Se colocaron en una placa Petri 20 µL de agua estéril en seis puntos equidistantes de la caja Petri de tal manera que queden diametralmente opuesta una de la otra (Fig. 1).

Se inoculó en la primera gota 10 µL de la dilución de esporas con una concentración de 1x106 esporas/mL, a continuación se realizaron diluciones seriadas en cada gota de agua estéril, hasta llegar a una concentración de 3.1x103 esporas/mL, de la última dilución (última gota) se inoculó 20 µL en una placa Petri estéril se colocó agar 10 mL de PDA fresco de manera que quede una capa delgada, se esperó a que este se solidifique. Finalmente se observó al microscopio con objetivo 40x la espora más aislada, se tomó la muestra de la espora con un sacabocado estéril de 0.5 mm, se inoculó en otra placa Petri con medio PDA, se incubo a 30 °C por 14 días.
Cinética de crecimiento. Para medir la cinética (velocidad) de crecimiento, con un sacabocados estéril se hizo pozos de 0.5 cm en el agar PDA, se inoculó 1x106 esporas/mL de la cepa de Trichoderma inhamatum BOL-12QD en el pozo, se incubo la placa Petri a 30 °C hasta que el micelio detuviera su crecimiento por contacto directo con los bordes de la caja Petri. Se utilizó la placa Petri de 19 cm de diámetro (Apaza 2005).
El crecimiento del frente hifal se midió por el reverso de la placa Petri desde el borde del inóculo hasta la punta del micelio. El crecimiento se midió cada 24 h con una regla en milímetros (Apaza 2005).
]]> Control de pH. Para monitorear una baja en el pH de medio que indicaría la actividad enzimática de celulasa y proteasa, cada día se tomó una muestra de 1.5 mL (CDP) y se midió en pH-metro (Oakton) (Nutrición personalizada 2010).Determinación de proteínas totales. Para la determinación de proteínas totales se utilizó el método de Biuret (Quiroga-Flores 2011). En un tubo se adiciono 100 µL de la muestra filtrada previamente en un filtro de nitrocelulosa de 0.22 µm de poro. Se colocó 1 mL de reactivo de Biuret, se agito en un vórtex, se incubo 30 min a temperatura ambiente (~20 ºC), la prueba se realizó por triplicado, se realizó la lectura a 540 nm en el espectro de Elisa (BIOTEK.ELx800) el blanco utilizado fue el reactivo sin la adición de la muestra.
La curva de calibración del método se realizó con Albumina de Suero Bovino (BSA) preparando estándares de concentraciones de 1 a 10 g/mL.
Actividad Enzimática
Actividad Celulolítica. La evaluación de la influencia de la concentración de sustrato se realizó empleando medio mínimo basal (MMB) que contenía para 1000 mL de agua NA2HPO4 6.0g, KH2PO4 3.0 g, (NH4)2SO4 2.64 g, MgSO4 7H2O 0.5g, CaCl2 0.015g, MnSO4 3.0g, ZnSO4 3.0g. En este procedimiento se empleó botellas de vidrio de 100 mL, se alicuotó un volumen de 70 mL de MMB, que posteriormente fue autoclavado a 121 °C y 1.5 atm por 15 min, una vez frio el medio de cultivo se procedió a inocular un volumen de 100 µL de suspensión de esporas T. inhamatum cepa BOL-12QD a una concentración de 106 esporas/mL.
Se consideraron 3 repeticiones por prueba y la actividad se evaluó por 15 días. Para determinar la actividad celulasa, se utilizó como sustrato Carboximetilcelulosa (CMC) a concentraciones de 2% (p/v) en buffer citrato 0.05 M pH 5 en cada frasco de vidrio se inoculó 70 µL de sustrato (Chávez 2006).
La actividad se midió por la técnica de DNS según Miller (1959), consiste en un tubo blanco, tubo control, tubo test. El tubo blanco contiene sustrato de quitina coloidal 450 µL, agua 50 µL. El tubo control 450 µL de sustrato CMC, el tubo test contiene 50 µL de la muestra de cultivo previamente filtrada con filtros de celulosa de 0.22 µm, 450 µL de sustrato CMC. Se incubó los tubos a 50 °C por 60 min, los tubos se colocaron directamente en hielo, luego se añadió a cada tubo según el orden siguiente: al tubo blanco se añadió la solución de DNS 750 µL, al tubo control muestra del sobrenadante del cultivo 50 µL, solución de DNS 750 µL, al tubo test solución de DNS 750 µL, se incubaron los tubos a 90 °C por 5 min se dejó enfriando a temperatura ambiente. Se leyó al espectrofotómetro de ELISA (BIOTEK.ELx800) a 540 nm.
Actividad Proteolítica. Para la determinación de la actividad proteasa se utilizaron 70 µL de extracto de carne a concentraciones de 2%, 4% y 6% (p/v), de gelatina 1%, 3%, 5% (p/v), caseína 1%, 2%, 4% (p/v), las cuales fueron inoculadas en frascos de 100 mL conteniendo 70 mL de MMB.
Para determinar la actividad proteasa se utilizó el método de la Azocaseina (Manoj et al. 1988). A 1 mL de la muestra previamente filtrada en un filtro de 0.22 µm y 1 mL al 0.5% (p/v) de azocaseína en buffer tris-HCl (200 mM pH 7.4). Se incubó por 60 min a 30 °C. La reacción se detuvo adicionando 2 mL al 10% (p/v) de ácido tricloroacético. La muestra se centrifugó a 10000 rpm por 10 min. Se tomó el sobrenadante y se lee a 380 nm en un equipo de Elisa (BIOTEK.ELx800).
Actividad quitinolítica
]]> Preparación de quitina coloidal. Para determinar la actividad quitinasa se preparó quitina coloidal como sustrato, se pesó 1 g de quitina coloidal se añadió 10 mL de HCl concentrado, se dejó reposando 6 h. Se añadió 250 mL de etanol frio al 70 % en agitación continua de 10 a 20 min aproximadamente, se esperó a que la mezcla se estabilice, se ajustó el pH a 7.0. Se centrifugó a 8000 rpm 30 min 4 °C. El sedimento se lavó con agua destilada estéril mediante centrifugación a 3000 rpm durante 5 min a 4 °C hasta que el olor a alcohol se eliminó completamente. La quitina coloidal obtenida tenía una suavidad, consistencia pastosa y se almacenó a 4 °C hasta su uso posterior (Agrawal & Kotasthane 2012).Determinación cualitativa de actividad quitinasa. Para la determinación cualitativa de la actividad quitinasa-positivo se preparó un medio basal (MB) que comprende 0.3 g de MgSO4.7H2O, 3.0 g de (NH4) 2SO4, 2.0 g de KH2PO4, 1.0 g de ácido cítrico monohidratado, 15 g de agar, 200 µL de Tween 80, 4.5 g de quitina coloidal y 0.15 g de púrpura de bromocresol, el pH se ajustó a 4.7 y luego esterilizado en autoclave a 121 °C durante 15 min. El medio tibio se vertió en placas Petri una vez solidificado el medio se observó una coloración amarilla brillante, posterior a esto con un sacabocados estéril se hizo un pozo de 0.5 cm en el medio de cultivo que estaba en las placa Petri, se inoculó 1x106 esporas de la cepa T. inhamatum BOL 12-QD en el pozo, se incubo las placas Petri a 30 °C. La prueba se realizó por triplicado se dejó incubando hasta observar la formación de zona de color, que debe cambiar de amarrillo brillante a un violeta intenso (Agrawal & Kotasthane 2012).
Resultados
Aislamiento. Una vez aislada la cepa Trichoderma inhamatum BOL-12QD se identificaron las características macroscópicas como microscópicas del hongo mediante observación.
Las colonias de la cepa Trichoderma inhamatum BOL-12QD crecen y maduran a los 7 días de incubación en PDA a 30 °C.
Observación macroscópica. Para la identificación de este hongo se evaluaron las características morfológicas que presentaban en la caja Petri, de las cuales se observó lo siguiente: i) Lado anverso presenta características de un crecimiento algodonoso blanquecino que se compactan con el tiempo, el crecimiento se realizó en períodos de luz y oscuridad, se aprecia el crecimiento correspondiente a cada período. El crecimiento empieza con un color blanco algodonoso, continúa el crecimiento como un halo de tonalidad verde con una apariencia de anillos continua un color blanquecino y a continuación un segundo halo color verde hasta completar la caja Petri. ii) Lado reverso, presentaba un aspecto de frente hifal liso sin pigmentación respecto al medio (Fig. 2).
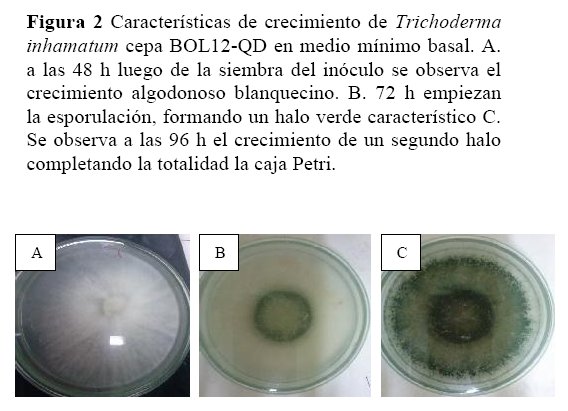
Observación microscópica. Para su identificación se realizó la tinción con colorante vegetal de color azul y se observó al microscopio con el objetivo 40x, la morfología al microscopio corresponde a hifas hialinas septadas, formando un ángulo de 90° sus conidios son hialinos, las fialides son hialinas están dispuestas en racimos y producen los conidios en el extremo. Sus conidios son unicelulares de forma redonda.
]]> Cinética de crecimiento. Para medir la cinética (velocidad) de crecimiento se trabajó con medio de cultivo PDA y se midió cada 24 h con una regla milimetrada se realizó la medición por Unidades Formadoras de Colonia (UFC) del reverso de la caja Petri desde el inóculo hasta la punta del micelio de 19 cm de diámetro, el frente hifal se midió en las cuatro orientaciones (norte, sur, este, oeste) el valor de coeficiente de correlación r obtenido en la gráfica es 0.944 por lo tanto el valor obtenido para la velocidad de crecimiento es de 9 h (Fig. 3).
Actividad Enzimática
Actividad Quitinasa. Para la detección de actividad quitinasa se utilizó el MMB suplementado directamente con quitina coloidal (4.5 g L-1) y púrpura de bromocresol (0.15 g L-1) el pH se ajustó a 4.7 con solución de HCl 3M. El medio resultante tenía un color amarillo brillante cuando se inoculó con la cepa el medio cambio de amarillo brillante a un color violeta intenso (Fig. 4).

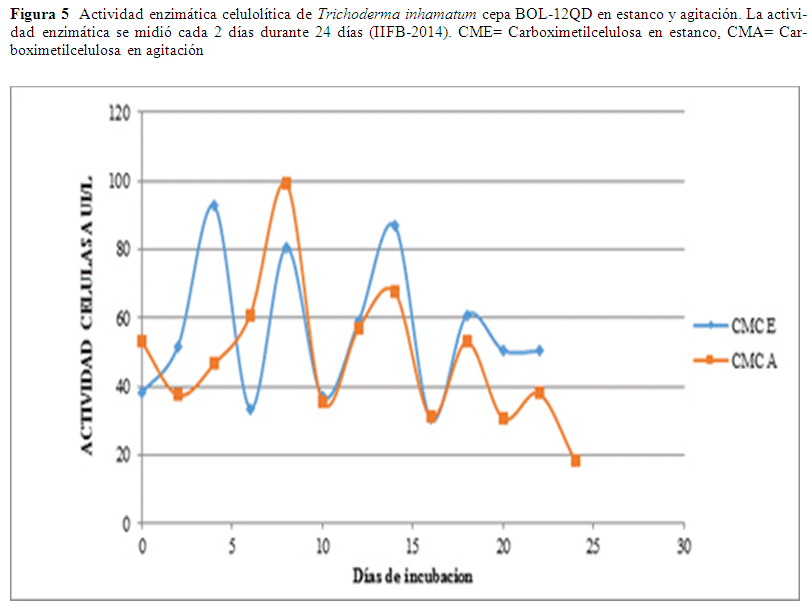
Actividad Celulolítica. La actividad celulolítica se expresa en términos de (UI/L). Las variables agitación y estanco fueron analizadas en este estudio con una concentración de sustrato de 2% (Fig. 5). Cada unidad de actividad enzimática fue definida como la cantidad de enzima requerida para liberar 1 μmol/min de azúcar reductor expresado como equivalentes de glucosa. La mayor actividad se observa a los 8 días de incubación en agitación con un valor de 99.23 UI/L este valor disminuye al décimo día a 35.53 UI/L, se observa que esta actividad enzimática va en aumento en el onceavo día de evaluación con valores de 57.08 UI/L y en el día 13 un valor de 67.62 UI/L en estos resultados se observa que se presenta un trayecto ascendente y progresivo hasta el último día de evaluación. En los resultados de estanco el valor óptimo es al cuarto día con un valor de 92.76 UI/L, desciende al sexto día a 33.62 UI/L, al octavo día 80.55 IU/L, estos valores presentan valores ascendentes (Fig. 5).
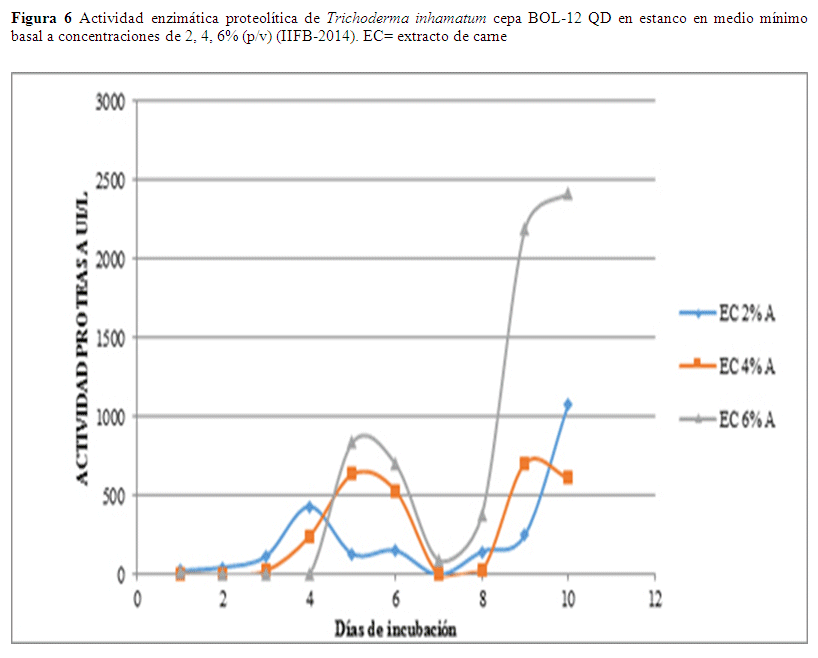
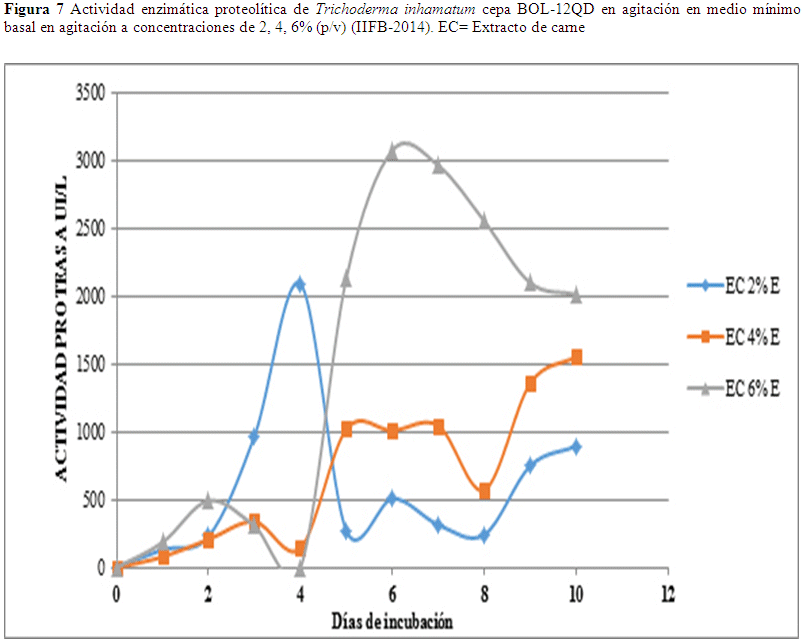
La mayor actividad proteasa en estanco fue de 3075.45 UI/L que se obtuvo el séptimo día usando una concentración de 6% (p/v) de extracto de carne, este valor desciende el octavo día a 2963.73 UI/L y el noveno día a 2553.53 UI/L (Fig.7), los valores presentan un trayecto descendente. En relación a los datos de concentración sustrato al 4% y 2% los valores no son relevantes (Fig. 6).
Se observan resultados de 568.36 UI/L al décimo día en estanco con el sustrato gelatina al 3% y un valor de 431.63 UI/L al 5%, estos valores presentan el mismo patrón ascendente y descendente y un valor de 212.35 UI/L al 1% al noveno día como se observa en Fig. 8.
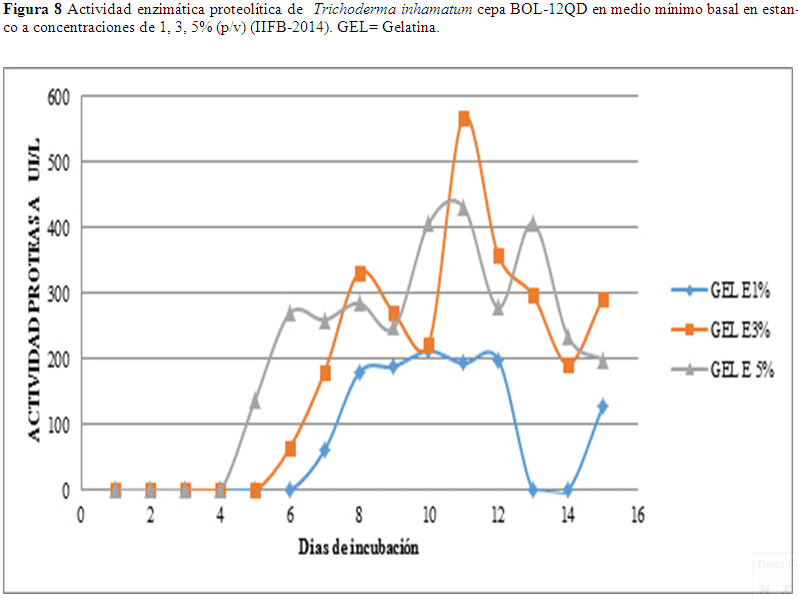
En la variable de agitación se observa un valor de 546.27 UI/L en el día doce con sustrato al 1%, este es un valor elevado con relación al onceavo día donde se observó una actividad de 410.37 UI/L al 3% y 441.77 UI/L al quinto día con sustrato al 5% (Fig. 9).
]]>
En relación a los datos de caseína el valor óptimo se alcanzó el quinto día con un valor de 407.04 UI/L en estanco usando una concentración de 1% de caseína como sustrato al 2% de sustrato los valores son invariables, se observa un valor de 161.91 UI/L al quinto día al 4% (Fig. 10).
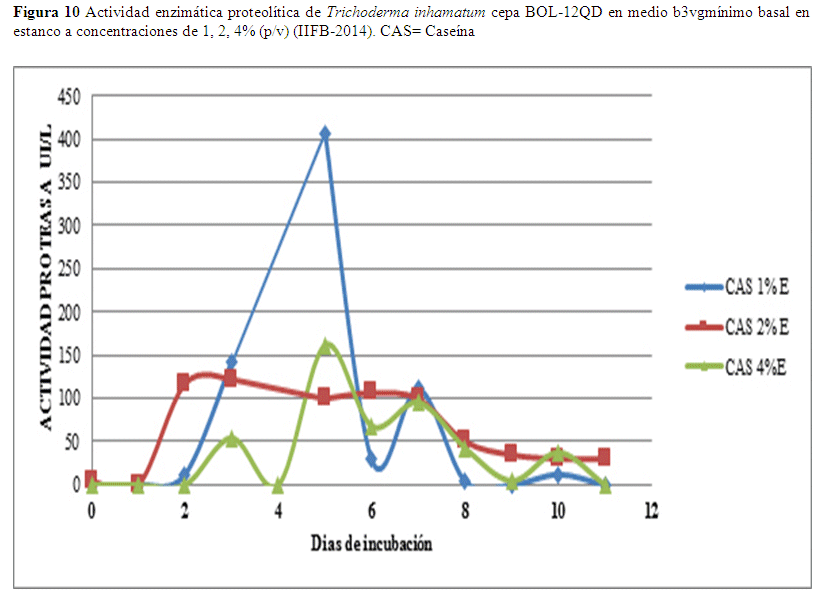
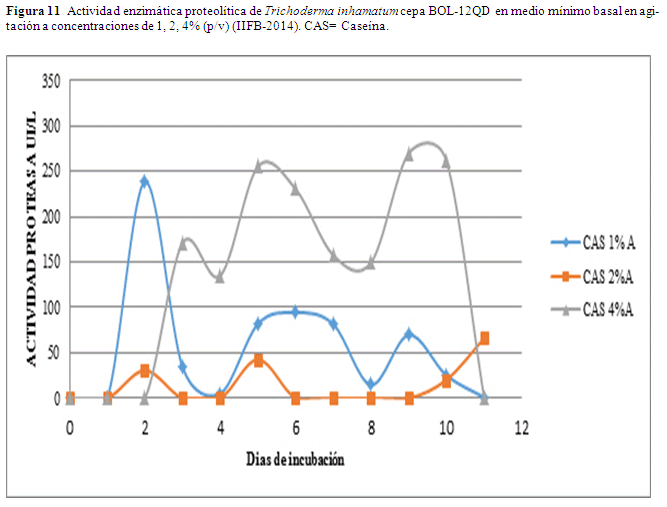
En agitación se observa un valor alto 269.88 UI/L al noveno día a una concentración de caseína al 4% este valor desciende a 261.13 UI/L. Usando 1% de caseína como sustrato el valor más alto se obtuvo el segundo día alcanzando 238.20 UI/L. Usando el 2% de caseína se observan los valores más bajos obteniéndose el máximo el quinto día alcanzando 42.68 UI/L (Fig. 11).
En la producción de enzimas celulolíticas las condiciones de estanco son más favorables si bien el valor más alto se obtiene en agitación este se alcanza al cabo de ocho días en cambio en condiciones de estanco se alcanza la máxima actividad enzimática el cuarto día habiendo una diferencia de aproximadamente el 7% entre ambas.
En el caso de enzimas proteasas se observó que el mejor sustrato es el extracto de carne al 6%, en este caso la agitación si hace que la actividad enzimática aparezca en forma más temprana.
]]>Discusión
En nuestro trabajo la cepa Trichoderma inhamatum BOL-12QD crece al séptimo día a 30 ºC en agar PDA se observó las zonas de crecimiento en presencia de luz y oscuridad dando apariencias de anillos concéntricos (Sánchez 2009) (Fig. 2), que son características de crecimiento característico del género Trichoderma que coincide con lo señalado por Sánchez (2009).
En relación a los resultados obtenidos para determinar la actividad enzimática de Trichoderma inhamatum Cepa BOL-12QD en la producción de las enzimas quitinasa, celulasa y proteasa. Se mostró que existe actividad quitinasa debido a que se evidencio un cambio de color en el medio sólido con quitina coloidal como sustrato y como indicador púrpura de bromocresol, este cambio de color se observa al momento del crecimiento de la cepa, hasta su esporulación, el medio mínimo basal suplementado con quitina coloidal como sustrato ha sido utilizado anteriormente para el aislamiento de microorganismos con actividad quitinolítica (Cody 1989). La evaluación de la actividad quitinasa con indicador de pH con púrpura de bromocresol es propuesta por, Agrawal (2012). Un cambio del pH evidencia actividad quitinasa la cual se corrobora con un cambio de color de amarillo a púrpura alrededor del inóculo sembrado, este cambio de color se debe a la degradación de quitina en N-acetil glucosamina (Fig. 4). Este método tiene ventajas importantes a diferencia de otros métodos donde las técnicas más sensibles requieren sustratos más caros. De acuerdo a los resultados obtenidos en este estudio es un método muy práctico y sencillo para determinar la actividad quitinasa, puede ser utilizado para un gran número de hongos de interés con actividad quitinolítica. Se podría modificar este método cambiando el sustrato lo cual permitiría hacer un screening más completo de microorganismos productores de enzimas de interés comercial.
En el análisis de la producción de la actividad celulolítica se midieron la liberación de azúcares reductores la cual se basa en la utilización de ácido 3.5-dinitrosalicílico que provocará la oxidación de los azúcares y al mismo tiempo su propia reducción, la curva estándar generada con glucosa se utilizó para determinar la reducción de concentración de azúcares.
La producción de celulasa en medio mínimo basal y CMC como sustrato, mostró actividad a partir de 40 UI/L y 60 UI/L al día de inicio de su evaluación, este factor posiblemente se debe a que el inóculo evaluado presentaba ya actividad en el medio de cultivo. En agitación se obtuvo un nivel máximo de actividad a los 8 días de incubación con un valor de 99.23 UI/L. En los resultados de estanco el valor óptimo es al cuarto día con un valor de 92.77 UI/L, en ambos casos se presentan valores ascendentes y descendentes hasta el último día de evaluación (Fig. 5). Este comportamiento se debe a que el hongo pasa por tres fases: fase logarítmica, estacionaria y de declinación en la fase logarítmica empieza el crecimiento acelerado, en la fase estacionaria cuando comienza a disminuir el crecimiento, debido a que el sustrato ha sido metabolizado o empieza la formación de sustancias tóxicas para el microorganismo y el crecimiento decae y por lo tanto la producción de sus metabolitos. La biomasa aumenta solo gradualmente o permanece constante durante esta fase estacionaria, debido a la lisis son liberados nuevos sustratos que pueden servir como fuente de energía y por lo tanto vuelve aumentar la asimilación del sustrato (Chávez 2006). Esta actividad es mayor a los resultados obtenidos de actividad celulolítica de Trichoderma inhamatum por Espinal 2009, donde utiliza como variable de estudio agitación-aeración y presenta el mejor resultado al cabo de 7 días de iniciada la experimentación, con una actividad enzimática de 78.70 UI/L. En relación a los resultados de este estudio se obtuvo un valor 14.08% más alto que el reportado por Espinal 2009. El hecho de utilizar un sustrato específico como CMC hace que exista mayor actividad incluso en estanco a 30 °C de temperatura.
En la actividad enzimática proteasa en estanco usando concentración de 6% (p/v) de extracto de carne se observaron resultados óptimos al cabo del séptimo día obteniéndose una actividad de 3075.45 UI/L, este valor desciende el octavo día a 2963.73 UI/L, y el noveno continua el descenso de la actividad llegando a 2553.53 UI/L (Fig. 7). Esos valores son más altos que los obtenidos usando el mismo sustrato en agitación (Fig. 6) y más altos que la actividad proteolítica en comparación a otras cepas fúngicas con actividad proteasa como se reporta en Cruz (2008) con actividades de 8D Chaetomium sp. 22.6 UI/L, 12D Stachybotrys sp. 37.9 UI/L, y 21D Eladia saccula (E. Dale) 37.1 UI/L.
En los resultados con el sustrato gelatina se observó un valor de 568.37 UI/L al cabo del décimo día 3% y 431.63 UI/L al 5%, un valor de 212.35 UI/L al 1% como se observa en Fig. 8. El valor más alto en la variable de agitación es 546.27 UI/L al día doce con 1% de sustrato, este es un valor elevado con relación al obtenido el onceavo día con 410.37 UI/L a una concentración de 3% y 441.77 UI/L al quinto día en concentración al 5% de sustrato (Fig. 9).
Se observa actividad enzimática en estanco con sustrato gelatina al cabo del cuarto día y en agitación empieza la actividad enzimática a los dos días. Aparentemente la agitación hace que los hongos estimulen su actividad enzimática que en condiciones de estanco ya que los hongos son aerobios y con agitación estimulamos su actividad.
Con el sustrato de caseína al 1% en estanco se obtiene un valor de 407.04 UI/L al cabo del quinto día (Fig. 10), al 2% de sustrato los valores son invariables, se observa un valor de 161.91 UI/L también al quinto día al 4%. En agitación se observa un valor de 238.20 UI/L al cabo del segundo día (Fig. 11), al 1%, al 2% se repite el mismo patrón que en estanco, se observa un valor de 269.88 UI/L al noveno día al 4%, valor que desciende a 261.13 UI/L (Fig.11).
]]> Con el sustrato de caseína se observa actividad a partir del segundo día en estanco y agitación, pero los valores no son tan buenos en relación con los sustratos de extracto de carne y gelatina. Es importante hacer notar que diferentes sustratos activan diferentes proteasas siendo así la proteasa que se produce al usar extracto de carne como sustrato es la más efectiva de acuerdo a nuestros resultados. Las proteasas pueden actuar degradando a las celulasas por lo cual recomendamos añadir algún inhibidor de proteasas que nos permita obtener una actividad celulolítica más alta.El método cualitativo en medio sólido para el ensayo de la actividad quitinasa es fácil, reproducible, sensible y es una opción económica para determinar actividad quitinolítica en caso un screening de cepas con posible actividad biocotroladora.
En el estudio se observa que existe mayor actividad proteolítica que celulolítica, esta elevada actividad proteolítica es importante en biocontrol. No obstante, para poder determinar cuál es la enzima más importante en biocontrol de hongos patógenos se recomienda purificar las enzimas para hacer estudios de confrontación dual con la enzima pura contra el fitopatógeno.
El éxito de estas enzimas como producto de antagonismo de la cepa Trichoderma inhamatum BOL-12QD frente a hongos patógenos está también relacionado por otros mecanismos por el cual este hongo tiene capacidad controladora por confrontación directa con patógenos y lograr en estos el micoparasitismo (Howell 2003) todos estos factores hace el género Trichoderma, sea un excelente controlador biológico.
Estudios futuros podrían enfocarse en la clonación de los genes que codifican estas enzimas en microorganismos en los que se pueda obtener una mayor cantidad de las mismas.
Conflictos de intereses
Los autores declaran que no existen conflictos de interés.
Agradecimientos
Se agradece a la cooperación de la Agencia Sueca de Cooperación para el Desarrollo Internacional (ASDI), con el proyecto de Biocontrol de la Antracnosis por el aporte financiero.
]]> Rawana Alkhalili por la proporción muy amable de quitina.
Literatura citada
Agrawal T, Kotasthane A. Chitinolytic assay of indigenous Trichoderma isolates collected from different geographical locations of Chhattisgarh in Central India. Springerplus. 2012; 73(1): 2-3. [ Links ]
Apaza L. Parámetros Físicos, Químicos y Biológicos Involucrados en el Control Biologico de Fitopatógenos por especies en Trichoderma. [tesis licenciatura]. La Paz: Universidad Mayor de San Andrés; 2005. p. 102.
Castellanos G, Jara C, Mosquera G. Guía Practica 6: Manejo del Hongo en el Laboratorio. Centro Internacional de la Agricultura Tropical (CIAT) 2013. p. 16.
Chávez M. Producción de Trichoderma sp. y Evaluación de su efecto en cultivo de Crisantemo. [tesis licenciatura]. Bogotá: Pontificia Universidad Javeriana; 2006. p. 127.
Cody RM. Distribution of chitinase and chitobiase in bacillus. Curr Microbiol. 1989; 19: 201-205. [ Links ]
Cruz C.A. Purificación y caracterización parcial de proteasas alcalinas a partir de hongos filamentosos implicados en la degradación del patrimonio documental en el Archivo Distrital de Bogotá. [tesis licenciatura]. Bogotá: Universidad Militar Nueva Granada; 2008.
Espinal C. Evaluación de la actividad biocontroladora de Trichoderma Inhamatum (Cepa Bol-12 Qd), frente a Botrytis Fabae, causante de la mancha chocolate en cultivos de Haba (Vicia Faba). [tesis licenciatura]. La Paz: Universidad Mayor de San Andrés; 2009. p. 130.
]]>Harman GE, Howell CR, Viterbo A, Chet I, Lorito M. Trichoderma species-opportunistic, avirulent plant symbionts. Nat Rev Microbiol. 2004; 2: 43-56. [ Links ]
Howell CR. Mechanisms employed by Trichoderma species in the biological control of plant diseases: The history and evolution of current concepts. Plant Dis. 2003; 87: 4-10. [ Links ]
Infante D, Martínez B, González N, Reyes Y. Mecanismos de acción de Trichoderma frente a hongos fitopatógenos. Rev Protección Veg. 2009; 24 (1): 14-21. [ Links ]
Jayalakshmi SK, Raju S, Usha-Rani S, Benagi VI, Sreeramulu K. Trichoderma harzianum L as a potential source for lytic enzymes and elicitor of defense responses in chickpea (Cicer arietinum L.) against wilt disease caused by Fusarium oxysporum f. sp. ciceri. Aust J Crop Sci. 2009; 3(1): 44-52. [ Links ]
Kubicek CP, Mach RL, Peterbauer CK, Lorito M. Trichoderma: from genes to biocontrol. J Plant Pathol. 2001; 83: 11-23. [ Links ]
Küçük Ç, Kývanç M. Mycoparasitism in the biological control of Gibberella zeae and Aspergillus ustus by Trichoderma harzianum strains. J Agric Technol. 2008; 4(2): 49-55. [ Links ]
Manoj MK, Indira D, Donald FG. Gerson Protease production by Bacillus subtilis in oxygen-controlled, glucose fed-batch fermentation. Appl Microbiol Biotechnol. 1988; 28: 404-408. [ Links ]
Miller GL. Use of dinitrosalysilic acid reagent for determination of reducing sugar. Anal Chem. 1959; 31: 426-428. [ Links ]
Monreal J, Reese ET. The chitinase of Serratia marcescens. Can J Microbiol. 1969; 15: 669-689. [ Links ]
Nutrición personalizada: Conocimiento avanzado transformando vidas [Internet]. Mexico; 2010 [Actualizado 20 Mar, 2014; citado 26 Ago, 2015] Disponible en URL: https://nutricionpersonalizada.wordpress.com/2010/01/18/microorganismos_crezcan/
]]>OBrien M, Collwell RR. A rapid test for chitinase activity that uses 4-methylumbelliferyl-N-acetyl-D-glucosaminide. Appl Environ Microbiol. 1987; 53: 1718-1720. [ Links ]
Ponce T, Pérez O. Celulasas y xilanasas en la industria. En Avance y Perspectiva. 2002. [En línea] vol. 21 sep-oct [09/07/2015] Disponible en: URL: http://www.cinvestav.mx/Portals/0/Publicaciones%20y%20.
Quiroga-Flores R. Aislamiento y cultivo de microorganismos capaces de degradar hexadecano y fenantreno de pozos abandonados con petróleo mediante procesos aerobios y anaerobios, Sanandita-Tarija-Bolivia. [tesis licenciatura]. La Paz: Universidad Mayor de San Andrés; 2011. p. 127.
Rojas-Avelizapa LI, Gomez-Ramirez M, Cruz-Camarillo R. In: Muzzarelli RAA., Muzzarelli C (eds). Fermentation of shrimp waste by Bacillus thuringiensis to produce proteo-chitinolytic enzymes and insecticidal crystals. Chitosan in Pharmacy and Chemistry, Atec, Italy. 2002. p. 479-487.
Sánchez-Pérez M. Aislamiento y caracterización molecular y agronómica de Trichoderma spp. nativos del norte de Tamaulipas. [tesis licenciatura]. Instituto Politécnico Nacional: Centro de Biotecnología Genómica; 2009. p 187.
Zeilinger S, Omann M. Trichoderma biocontrol:signal transduction pathways involved in host sensing and mycoparasitism. Gene Regul Syst Bio. 2007; 1: 227-234. [ Links ]
______________
]]>