
ARTÍCULO ORIGINAL
Propagación masiva de Polylepis tomentella Weddell ssp. nana
mediante técnicas de cultivo in vitro
Massive propagation of Polylepis tomentella Weddell ssp. nana
through in vitro culture techniques
Cecilia Vega-Krstulovic', Juan Carlos Bermejo-Franco, Gabriela Villegas-Alvarado,
Jorge Quezada-Portugal, Milenka Aguilar-Llanos & Esther Conde-Velasco
Unidad de Biotecnología Vegetal del Instituto de Biología Molecular y Biotecnología,
Facultad de Ciencias Puras y Naturales, Universidad Mayor de San Andrés, ]]>
Calle 27 s/n Campus Universitario Cotacota,
Email: kcecivegak@yahoo.es *Autora de correspondencia
Resumen
Polylepis tomen tella ssp. nana es una especie endémica de Bolivia, reportada únicamente en la provincia Arani (Cochabamba); está considerada En Peligro (EN), por lo cual es necesario el desarrollo de iniciativas que promuevan su conservación, siendo una alternativa el uso de técnicas de cultivo de tejidos vegetales. Se utilizaron yemas apicales que fueron desinfectadas en etanol e hipoclorito de sodio, evaluando el efecto del tiempo de inmersión, adición de carbón activado y aplicación de una solución antioxidante para su establecimiento in vitro. Los explantes obtenidos fueron sembrados en medio basal Chu et al. (1975). En la fase de multiplicación, los brotes fueron subdivididos e introducidos en el medio de Tremblay & Lalonde (1984), variando la concentración de los fitorreguladores para incrementar el número de brotes por explante. En la fase de enraizamiento se comparó el efecto de diferentes medios de cultivo sobre el número y la longitud de las raíces generadas in vitro. El tratamiento óptimo para la desinfección de yemas apicales consistió en la inmersión en solución de hipoclorito de sodio al 2% por 10 minutos; por otra parte, la aplicación de una solución de ácido cítrico/ácido ascórbico resultó ser efectiva para el control de la oxidación. La adición de carbón activado al medio de cultivo tuvo un efecto inhibidor en el crecimiento, incluso generando la necrosis de los tejidos. Para la multiplicación in vitro, el mejor medio fue, Tremblay & Lalonde (1984) suplementado con 0.23 mg/1 de bencil aminopurina y 0.1 mg/1 de acido indol butírico. En la fase de enraizamiento, el tratamiento óptimo tanto para la formación como para el desarrollo radicular de vitroplantas fue el medio de cultivo McCown & LLoyd (1980), al 50%, suplementado con 50 g/1 de sacarosa y 0.1 mg/I de acido indol acético.
Palabras clave: Polylepis, Propagación in vitro, Conservación, En Peligro.
Abstract
Polylepis tomentella ssp. nana is an endemic species from
Key words: Polylepis, in vitro propagation, conservation, endangered.
Introducción
Los bosques de Polylepis contienen una parte importante de la biodiversidad de Sudamérica (Yensen & Tarifa 2001). De acuerdo con estudios ornitológicos (Frimer & Nielsen 1989; Fjeldsa 1992, 1993 citados por Yensen & Tarifa 2001), en la región altoandina de Bolivia, más de 110 especies de aves utilizan los bosques de Polylepis y cerca de 40 especies dependen exclusivamente de estos bosques. Estos hábitats albergan especies endémicas y diferentes formas de vida vegetal, que incluyen plantas epífitas, lianas y numerosas especies herbáceas; además, incrementan la diversidad de mamíferos e insectos (Yensen & Tarifa 2001).
]]> Estos bosques son el tipo de hábitat más amenazado en Bolivia, estimaciones indican que menos del 10% de la extensión original sobrevive actualmente (Kessler 1995). Entre las amenazas que enfrentan se puede citar el sobre aprovechamiento de este recurso para la obtención de leña, los incendios dirigidos al rejuvenecimiento de los pastos (chaqueos), el pastoreo, la ampliación de nuevas zonas de cultivos, la producción de carbón vegetal y el empleo de prácticas forestales inadecuadas, las cuales valoran árboles exóticos sobre los nativos (Kessler & Driesch 1994).Además de estos factores es importante mencionar que la reproducción a partir de semillas se da en una escala muy limitada debido a su bajo poder germinativo. Según investigaciones realizadas por Prettell (1985) en Perú, Polylepis incana presentó valores de germinación 2-4%; de acuerdo a experiencias realizadas en Argentina, Guzmán (2006) reportó un 3.1% de plántulas germinadas para Polylepis tomentella. El bajo poder germinativo podría estar relacionado a los fenómenos propios de la especie como la dicogamia y la dispersión anemófila (Cruz 1999). Por otro lado, las plántulas son consumidas por pequeños roedores de la zona así como por el ganado (Hensen 1994). A todo lo señalado, se suma el hecho de que no existen políticas, planes o proyectos destinados a la conservación e incremento de las áreas forestales con especies de Polylepis.
Polylepis tomen tella ssp. nana (Rosaceae, Sanguisorbae) es un arbusto que alcanza una altura de
En cuanto a su distribución, la especie P. tomentella se encuentra en el centro y sur de Bolivia y partes adyacentes del norte de Argentina (Kessler & Fjeldsá 2004). Según Navarro & Maldonado (2004) señalan que algunas de sus subespecies se las puede encontrar en el piso puneño de la provincia biogeográfica boliviano-tucumana entre los 3.000-
Según Meneses & Beck (2005) y en cuanto al estado de conservación, P. tomentella ssp. nana es considerada una especie En Peligro (EN). De acuerdo a las categorías de
A través del uso de técnicas de cultivo de tejidos vegetales, como la propagación in vitro, es posible desarrollar alternativas de conservación ex situ, especialmente en especies que presentan problemas reproductivos, como es el caso de la keñua. Este tipo de técnicas tiene la ventaja de producir en forma masiva y en poco tiempo, gran cantidad de material vegetal, el cual puede ser utilizado para llevar a cabo programas de reforestación y restauración de poblaciones disminuidas o mantenimiento de poblaciones viables. Respecto al cultivo in vitro del género Polylepis, solo se tiene conocimiento de tres experiencias realizadas en Bolivia, las mismas que corresponden a investigaciones que avanzaron hasta su multiplicación y enraizanniento (Mamani 1999, Vega 2002, Quezada & Rocabado 2005).
El presente proyecto planteó realizar la producción masiva de vitroplantas de Polylepis tomentella ssp. nana mediante la aplicación del cultivo de tejidos vegetales y aprovechando las ventajas inherentes a la propagación in vitro. Con este fin, se formularon los siguientes objetivos: 1) Establecer explantes (yemas apicales) de Polylepis tomentella ssp. nana en condiciones in vitro, 2) Desarrollar la multiplicación in vitro de brotes caulinares y 3) Determinar el tratamiento óptimo para el enraizamiento in vitro.
Área de estudio
La colecta del material vegetal se realizó en el sector correspondiente al macizo Kuturi, ubicado en el camino que comunica las poblaciones de Arani y Vacas en la provincia Arani del departamento de Cochabamba (20 K 0211720 - 8056490 UTM, Fig. 1). La localización, reconocimiento y marcaje de la zona de colecta se realizó inicialmente gracias a la colaboración de personal perteneciente al Herbario Martín Cárdenas de Cochabamba (Fig.1).
El sitio se caracterizó por presentar un relieve abrupto, con suelos pedregoso-arcillosos, aledaños a zonas de cultivos agrícolas. De acuerdo a Fernández (1996), estos suelos presentan una saturación de bases muy alta, por lo que la reacción del suelo varía de moderadamente a fuertemente alcalinos. La vegetación predominante estuvo representada por el keñual (bosques de Polylepis tomentella ssp. nana). Los grupos más comunes de arbustos y subarbustos estuvieron representados por ejemplares de Baccharis, Berberis, Satu reja y Dodonaea, mientras que las especies herbáceas corresponden a la familia Poaceae.
]]>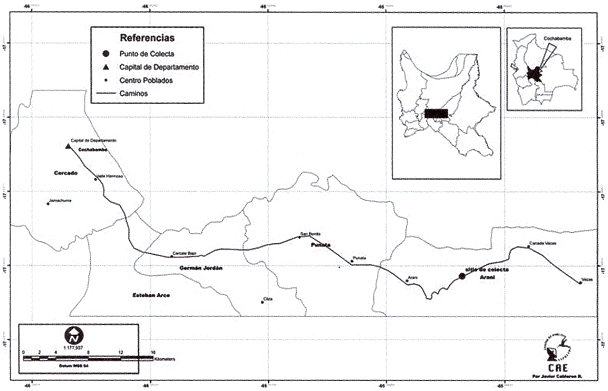
Fig. 1: Mapa de ubicación de la zona de colecta.
Métodos
Fase de campo. Selección, colecta y transporte del material vegetal
Para obtener el material vegetal, se procedió a la elección in situ de varios individuos de R tomen tella ssp. nana, los cuales presentaban las mejores características fenotípicas (follaje perenne y denso, numeroso renuevo de yemas apicales) y que, además, no se encontraran en estado de floración. La obtención de las muestras se realizó mediante colecta manual, a través del corte de ramas de 10-
Se realizaron tres viajes de recolección de material vegetal, los mismos que fueron efectuados en los meses de febrero, abril y mayo de 2004.
Identificación de la especie
Con el fin de verificar la identidad taxonómica del material vegetal colectado, se recurrió al Herbario Nacional de Bolivia (LPB), donde las muestras fueron identificadas por especialistas de dicha institución.
Fase de laboratorio
El trabajo de propagación in vitro se desarrolló en instalaciones de la unidad de Biotecnología Vegetal del Instituto de Biología Molecular y Biotecnología, perteneciente a
Se utilizaron yemas apicales de árboles de Polylepis tomentella spp. nana (Fig. 2). La introducción de dichos explantes se realizó de acuerdo a los viajes de recolección; de esta manera se plantearon diferentes ensayos para cada grupo de muestras (Grupo 1A = Primer viaje de recolección; Grupo 2A = Segundo viaje de recolección; Grupo 3A = Tercer viaje de recolección).
Fase I. Establecimiento
Durante esta etapa, se evaluó de forma progresiva el efecto del tiempo de desinfección, la adición de carbón activado al medio de cultivo y el efecto de la aplicación de compuestos antioxidantes en el establecimiento de yemas a picales de Polylepis tomentella ssp. nana bajo condiciones in vitro. Es importante mencionar que cada ensayo se realizó de forma separada con cada grupo de introducción.
La introducción del material vegetal (yemas apicales) en los medios de cultivo se realizó dentro de una cabina de flujo laminar, la cual fue previamente esterilizada mediante la aplicación de radiación ultravioleta por 20 minutos. Tanto el material como instrumental requeridos fueron también esterilizados en autoclave a 1 kg/cm2 por 20 minutos.
Efecto del tiempo de desinfección (Grupo 1A)
Los explantes fueron desinfectados en una solución de etanol al 70% (v/v) durante 1 minuto y posteriormente en hipoclorito de sodio (N aC10) al 2% a dos tiempos diferentes de inmersión: TI-A (10 minutos) y T2-A (15 minutos); se realizaron tres enjuagues consecutivos en agua destilada estéril, cada uno de cinco minutos. En una placa Petri

Fig. 2: Polylepis tomentella ssp. nana (Plantas fuente del material vegetal).
esterilizada y con la ayuda de una pinza y bisturí, se seccionaron los explantes axénicos eliminando los foliolos hasta obtener yemas apicales de 4-
Aplicando el tratamiento de desinfección determinado por el ensayo anterior, las yemas de este grupo fueron sembradas, por una parte, en tubos de ensayo conteniendo medio basal de Chu eta!. (1975) + KM (1975) + 1.0 mg/L BAP + 1.0 mg/LAG , + 0.5 mg/L AIB (T1-B) y por otra parte, en un segundo tratamiento consistente en el mismo medio de cultivo pero con la adición de carbón activado 2 g/ L (T2-B). Posteriormente los tubos fueron sellados, rotulados y trasladados a la sala de crecimiento, donde se aplicaron similares condiciones ambientales a las descritas para el ensayo inicial.
Efecto de la adición de soluciónantioxidante (Grupo 3A)
En esta ocasión se realizó una variante en el procedimiento consistente en un segundo remojo del material vegetal en una solución esterilizada de antioxidantes: ácido cítrico/ ácido ascórbico 300 mg/1 (T2-C), después de la desinfección con etanol e hipoclorito de sodio. El tratamiento T1-C consistió en la no aplicación de esta modificación. Posteriormente las yemas apicales fueron sembradas en tubos conteniendo medio basal de Chu et al. (1975) + KM + 1.0 mg/1 BAP + 1.0 mg/I AG3 + 0.5 mg/1 AIB, para luego ser transportadas a la sala de crecimiento.
En todos los casos, la toma de datos de cada uno de los tratamientos se efectuó a los 7, 14, 21 y 28 días después de ser introducidos los explantes en el medio de cultivo. Las variables medidas durante esta etapa fueron: porcentaje de contaminación, oxidación, porcentaje de necrosis, crecimiento relativo y porcentaje de sobrevivencia.
Fase II. Multiplicación
Luego del establecimiento de los explan tes in vitro y del inicio del crecimiento, se realizó la selección del material establecido que presentó mejor respuesta vegetativa. En la cámara de flujo laminar se procedió a seccionar la parte basal de los explantes, para luego transferirlos al medio basal de multiplicación Tremblay & Lalonde (1984) o TL, suplementado con 0.23 mg/1 de BAP y 0.1 mg/1 de AIB, en que permanecieron durante 30 días. Posteriormente, los brotes de los distintos grupos fueron subdivididos y traspasados a medios de cultivo, donde se varió la concentración de los fitorreguladores adicionados. Se realizaron cuatro subcultivos por grupo (cada 20 días) y las evaluaciones se efectuaron en el tercer y cuarto subctiltivo. Las variables evaluadas durante esta fase fueron: número de brotes, número de hojas, altura de brote (mm) y síntomas de marchitez. Los tratamientos probados se muestran en la tabla 1.
Tabla 1: Tratamientos ensayados en la etapa de multiplicación.
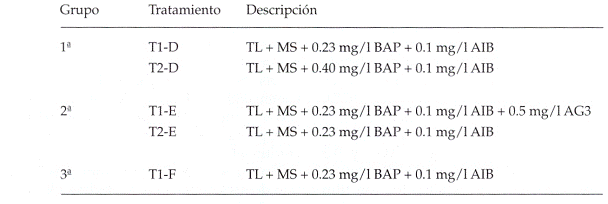
Fase III. Enraizamiento
]]> En esta fase se realizaron diferentes ensayos recomendados por expertos en el cultivo in vitro de especies forestales (Sharry S., J. Manzanera & M. A. Bueno, 2004, com. pers.), con el fin de determinar el medio óptimo para el enraizamiento de brotes de Polylepis tomentella ssp. nana. Los tratamientos planteados para esta fase se presentan en la tabla 2.Una vez determinado el medio óptimo para el enraizamiento de los brotes se prosiguió a incrementar el número de plántulas e nraizadas. Las variables evaluadas durante esta fase fueron: número de raíces, longitud de raíces (mm) y altura de la plántula (mm).
Análisis estadístico
Los datos obtenidos se analizaron a través de diseños estadísticos bloques al azar y completamente al azar con sus respectivos análisis de varianza (ANOVA). Cuando se encontraron diferencias significativas entre los tratamientos, se aplicó una prueba a posteori de Duncan (a = 0.05) para realizar comparaciones múltiples. La información se analizó empleando el programa estadístico MSTAT-C v. 1.41.
Resultados
Establecimiento - Efecto del tiempo de desinfección (Grupo 1A)
De acuerdo al análisis estadístico, no se presentaron diferencias significativas en el porcentaje de contaminación entre ambos tratamientos de desinfección propuestos. Dicho parámetro de forma general reportó valores menores al 35%, tal como puede verificarse en la figura 3. Entre los microorganismos contaminantes se pudo diferenciar diversos tipos de agentes fúngicos y bacterianos, siendo estos últimos los que se presentaron en mayor proporción en ambos ensayos. Para la variable necrosis, el análisis de varianza estableció que T2-A presentó mayor proporción de individuos necróticos (89%) en relación a Ti-A (78.5%), mostrando diferencias altamente significativas (P<0.01). El análisis descriptivo de la variable crecimiento relativo permitió observar que TI -A presentó explantes con un mayor crecimiento relativo en relación con T2-A, es decir, que las muestras del primer tratamiento presentaron un mayor crecimiento de la parte aérea respecto a los ejemplares sometidos a T2-A (Fig. 4). De forma general, se pudo evidenciar que en el tratamiento TI -A (NaC10 2% por 10 minutos) se presentaron explantes con un menor grado de oxidación y con
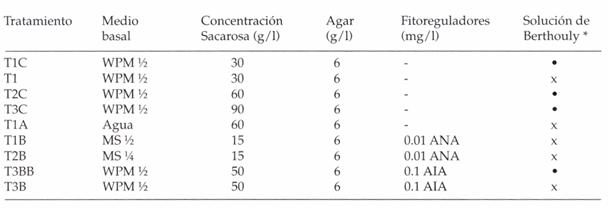
Tabla 2: Tratamientos ensayados en la fase de enraizamiento. Fuentes: WPM = Lloyd & Mc Cown (1980), ANA= Ácido naftalén acético MS = Murashige & Skoog (1962), AIA = Ácido indol acético, * = Solución de Berthouly et al. (1987); x = sin adición de solución Berthouly y con adición de solución Berthouly.

NaCIO, 10 min; T2-A = 2% NaC1O, 15 min.

Fig. 4: Crecimiento relativo de explantes sometidos a dos tratamientos (tiempos) de desinfección.
Tratamientos: T1-A = 10min; T2-A = 15min.
un crecimiento vegetativo superior en relación a la prueba contrastante (Fig.5).
Efecto de la adición de carbón activado (Grupo 2A)
La adición de carbón activado tuvo un efecto diferencial en la oxidación del medio de cultivo. Los resultados del análisis estadístico (Fig. 6), demostraron que el tratamiento T1- B (sin carbón activado) presentó mayores niveles de oxidación en relación a T2-B (con carbón activado), diferencias que resultaron altamente significativas (P<0.01). La presencia de carbón activado (tratamiento T2-B) produjo un mayor porcentaje de individuos necróticos (83.3%) en relación a T1-B (63.2%), tal como se observa en las Figs. 7 y 8, así como explantes con un crecimiento relativo menor (1.786) en comparación con el tratamiento T1-B (2.284), donde las diferencias que resultaron fueron altamente significativas (Fig. 9).

Fig. 5: Explantes de P. tomentella ssp. nana en tratamiento TI-A.
]]>
Fig. 6: Niveles de oxidación registrados en medios con y sin la adición de carbón activado.
Tratamientos: TI-B = s/ carbón activado; T2-B = c/ carbón activado.

Fig. 7: Explantes de P. tomentella ssp. nana en dos tratamientos antioxidantes. Tratamientos:
a-c= con carbón activado, b-d = sin carbón activado.
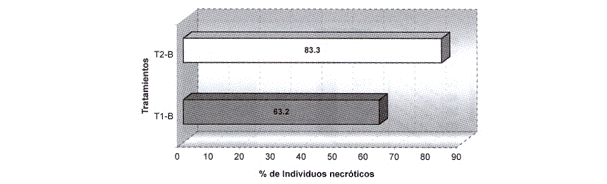
Fig. 8: Porcentaje de individuos necróticos registrados en medios con y sin la adición de carbón
activado. Tratamientos: T1-B = s/ carbón activado; T2-B = c/ carbón activado.

Efecto de la adición de solución antioxidante (Grupo 3A)
Los resultados obtenidos mostraron que el tratamiento T1-C presentó un mayor porcentaje de explantes necróticos (71.2%) en relación con la prueba T2-C (56.8%), que fue el tratamiento al que se le adicionó un enjuague en solución antioxidante (ácidos cítrico y ascórbico). Esto puede indicar que los explantes del primer ensayo presentaron una mayor oxidación, afectando a la viabilidad de los mismos y en consecuencia se produjeron los niveles de necrosis registrados (Fig. 10).
Adicionalmente, en el tratamiento T2-C se reportó un mayor porcentaje de sobrevivencia del material vegetal, registrando un promedio de 43.2%. Como se observa en
Multiplicación
De acuerdo con

Fig. 10: Necrosis de explantes registrados en medios con y sin la adición de solución antioxidante.
Tratamientos: T1-C = sin ácido cítrico-ascórbico; T2-C = con ácido cítrico-ascórbico.
]]>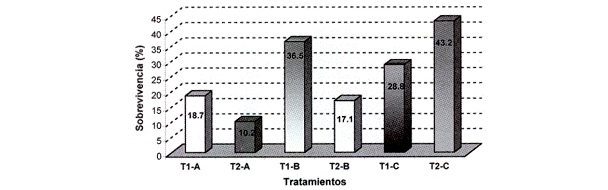
Fig. 11: Sobrevivencia de explantes sometidos a diferentes ensayos durante el establecimiento in vitro de Polylepis tomentella ssp. nana.
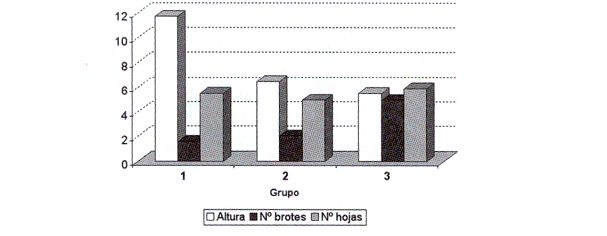
Fig. 12: Multiplicación de los grupos 1,2 y
Subcultivo grupo lA
El tratamiento consistente en TL + 0.23 mg/1 BAP + 0.1 mg/IAIB presentó explantes con un mayor número de hojas (11.036) en relación con el tratamiento T2-D (TL + 0.4 mg/1 BAP + 0,1 mg/lAIB) (Fig. 13). Aunque la tasa de brote por explante fue mayor en presencia de 0.23 mg /1de BAP, en este tratamiento se pudo verificar una mayor proporción de individuos con síntomas de marchitamiento a nivel foliar (aprox. 33%), en relación al tratamiento con 0.4 mg/1 BAP, en que se reportó un 4.5% de ejemplares con dichas características (Fig. 14).
En función a la información proporcionada por las diferentes variables analizadas, se pudo determinar que el tratamiento T1-D (TL + 0.23 mg /1 BAP + 0.1 mg/1 AIB) resultó ser la combinación óptima para la multiplicación de explantes establecidos de Polylepis fomente/la ssp. nana (Fig. 15) en condiciones de cultivo in vitro, por cuanto permitió obtener individuos vigorosos, con una importante tasa de brotación y mayor número de hojas por explante.
Subcultivo grupo 2A
Corno se observa en
Enraizamiento
]]> Los resultados de la fase de enraizamiento permitieron establecer que los tratamientos T2C, T2B y T3B presentaron un mayor número de raíces diferenciadas, en comparación al resto de los ensayos evaluados (Fig. 18); dichos tratamientos no demostraron diferencias significativas en los valores registrados para esta variable. Sin embargo, en lo que respecta a la longitud de raíces (Fig. 19) y la altura de la plántula (Fig. 20), el tratamiento T3B (1/2 WPM+ 50g/1 sacarosa + 0.1 AIA) tuvo efectos significativos en la respuesta de los explantes,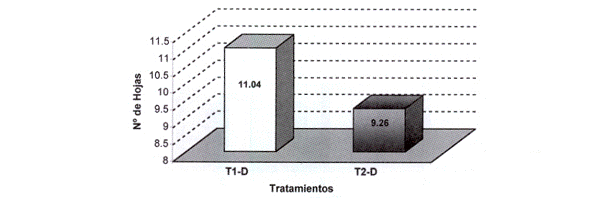
Fig. 13: Número de hojas en explantes sometidos a dos tratamientos con variaciones en la concentración de BAP (Tratamientos: T1-D = 0.23 mg/1 BAP; T2-D = 0.40 mg/1 BAP).
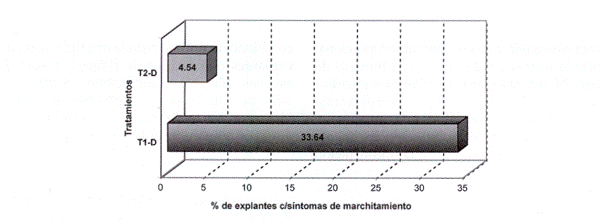
Fig. 14: Porcentaje de individuos con síntomas de marchitamiento. Tratamientos: T1-D = 0.23 mg/1 BAP; T2-D = 0.40 mg/1 BAP.

Fig. 15: Subcultivo grupo 1A a) 0.23 mg/1 de BAP (T1-D), b) 0.40 mg/1 de BAP (T2-D).
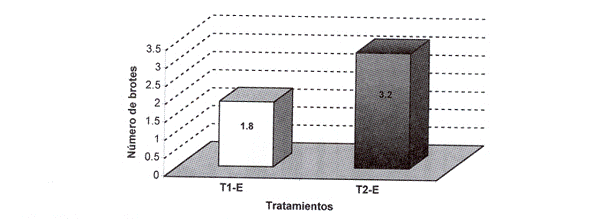
Fig. 16: Número de brotes sometidos a tratamientos con y sin la adición de AG3. Tratamientos: = 0.5 mg/1 AG3; T2-E = s/ AG3.

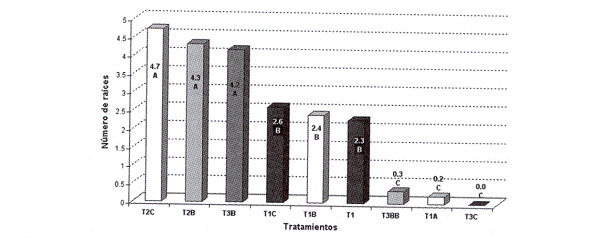
Fig. 18: Número de raíces formadas en función a diferentes tratamientos en Polylepis tomentella ssp. nana. Las barras con letras iguales no son significativamente diferentes (a= 0.05).
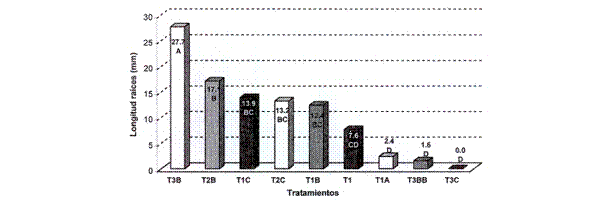
Fig. 19: Longitud de raíces en función a diferentes tratamientos de enraizamiento en Polylepis tomentella ssp. nana. Las barras con letras iguales no son significativamente diferentes (a= 0.05).
presentando estructuras radicales con una mayor longitud promedio (
Una vez obtenidas las vitroplantas se realizaron pruebas preliminares de aclimatación en condiciones de invernadero registrándose un 90% de sobrevivencia. Actualmente se están transplantando paulatinamente los plantines de Polylepis tomentella ssp. nana al Jardín Botánico
Discusión
Establecimiento
Los resultados en el efecto del tiempo de desinfección para el grupo 1A mostraron que los agentes bacterianos se presentaron en mayor proporción en ambos ensayos. Al respecto, Jiménez (1999) menciona que los métodos de desinfección utilizados no siempre eliminan a las poblaciones de bacterias asociadas a los tejidos de las plantas in vivo; muchas son capaces de permanecer latentes en el interior de las células, en los espacios intercelulares o en los haces conductores quedando protegidas, de esta manera, de los agentes químicos. Esto podría explicar los resultados obtenidos en cuanto a la presencia de una mayor proporción de contaminantes bacterianos. Por otra parte, la proporción superior de individuos necróticos observados en el tratamiento T2-A (NaCIO al 2% por 15 minutos) puede ser explicado por la mayor exposición que sufrieron los explantes al agente desinfectante en el tratamiento T2-A (2% NaCIO por 15 minutos), lo que permitió una mayor penetración del agente químico de tal manera que no solo produjo la eliminación de los microorganismos contaminantes, sino también pudo haber afectado a los tejidos internos y por tanto a la viabilidad del material vegetal.
]]> En base a la información recopilada por el análisis de las diferentes variables establecidas para esta fase, se pudo establecer que el tratamiento TI -A se presentó como óptimo para la desinfección inicial de yemas apicales de Polylepistomentella ssp. nana (Fig. 5), debido a que a través de este procedimiento los explantes fueron menos afectados (menor grado de oxidación y menores proporciones de necrosis),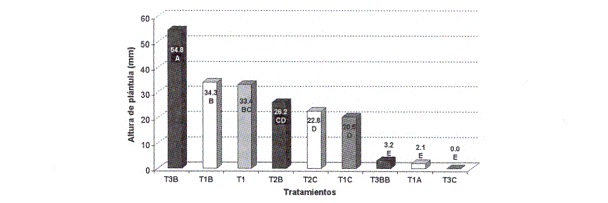
Fig. 20: Altura de plántula en función a diferentes tratamientos de enraizamiento en Polillepis fomente/la ssp. nana. Las barras con letras iguales no son significativamente diferentes (a= 0.05).

Fig. 21: Vitroplantas enraizadas de P. tomentella ssp. nana en tratamiento T3B. a) Planta entera y b) detalle de las raíces.
lo cual puede deberse a la menor exposición al agente desinfectante (2% NaC10 por 10 minutos) permitiendo, por tanto, un mejor desarrollo del material vegetal, traducido en términos de mayor tamaño de los individuos establecidos y un menor tiempo de generación de las primeras estructuras foliares, aspectos que son indicativos de una respuesta favorable del material vegetal a las condiciones de cultivo in vitro.
En cuanto al efecto de la adición de carbón activado (Grupo 2A) se ha observado que en el establecimiento in vitro de determinadas especies, especialmente leñosas, uno de los problemas que se enfrenta es la oxidación del medio de cultivo, debido a la liberación de compuestos fenólicos cuya acumulación puede resultar tóxica y, por tanto, afectar la viabilidad del material vegetal (Pierik 1990). Para contrarrestar el efecto de la oxidación fenólica, se adicionan sustancias antioxidantes al medio de cultivo, entre las cuales una de las más empleadas es el carbón activado (Darías 1993).
La respuesta diferencial de los resultados obtenidos responde a que el carbón activado tiene la propiedad, entre otras, de adsorber pigmentos fenólicos y diversos tóxicos incoloros (Margara 1988). De esta manera, se puede explicar el efecto positivo de la adición de esta sustancia al medio de cultivo, para contrarrestar la oxidación de los explantes de P. tomentella ssp. nana (Figs. 6 y 7). Sin embargo, su incorporación pudo afectar también la respuesta del material vegetal ya que, al mismo tiempo, tiene un efecto inhibidor del crecimiento de los explantes al ser un componente capaz de adsorber los reguladores de crecimiento contenidos en el sustrato, tal como menciona Margara (1988), aspecto que puede explicar las diferencias observadas entre tratamientos, especialmente en lo que respecta al crecimiento del material vegetal (Fig. 9), generando incluso la necrosis de los explantes.
La adición de solución antioxidante en el procedimiento de desinfección permitió obtener una mayor sobrevivencia de explantes, así como una menor proporción de individuos necróticos (Fig.10). Si bien estos resultados tienden a establecer una ventaja efectiva en la aplicación de dicha solución, el comportamiento observado también pudo ser producto de la combinación de procesos y condiciones de cultivos óptimos (tiempo de desinfección, eliminación de compuestos inhibidores de crecimiento y aplicación de solución antioxidante) determinados durante la estandarización del procedimiento de desinfección. Sin embargo, es posible que dicho comportamiento también esté relacionado con la época de colecta del material vegetal, ya que tanto los grupos 2A (tratamientos Tl-B, T2-B) y 3A (tratamientos Ti - C, T2-C) corresponden a muestras colectadas en época seca (abril y mayo), en relación al material correspondiente al grupo lA (tratamientos T1 - A, T2A), el cual fue obtenido en época húmeda (Fig. 11); sin embargo, este aspecto debe estar sujeto a mayores estudios.
Multiplicación
]]> De acuerdo a los datos obtenidos en el subcultivo del grupo 1A, se ha observado que la tasa de brote por explante fue mayor en presencia de 0.23 mg/1 de BAP (tratamiento T1-D). Sin embargo, en dicho tratamiento también se pudo verificar la aparición de una mayor proporción de individuos que presentaban síntomas de marchitez a nivel foliar (Fig.14). Esta diferencia puede ser explicada en función a la mayor cantidad de hojas generadas por los expla n tes, lo cual produjo por una parte un rápido consumo del medio nutritivo y por otra la reducción del espacio interno en los frascos de cultivo; condiciones tendieron a afectar la viabilidad de las estructuras foliares (Fig. 15).Los resultados del subcultivo del grupo 2A registraron menor formación de brotes en los explantes que fueron cultivados en medios con acido giberélico (Ti-E). Este fitorregulador tiene la capacidad de promover la elongación e inhibir la formación de brotes, de acuerdo a lo mencionado por Darías (1993), lo cual habría determinado una mayor elongación de los brotes y así su menor formación (Fig.17). Dichas observaciones concuerdan con la investigación realizada por Gonzáles (1998), donde se obtuvieron respuestas muy favorables en la regeneración de brotes de Aliso (Alnus acuminata) mediante el empleo de una combinación similar al tratamiento T2-E (s/ácido giberélico).
Enraizamiento
Los resultados observados en esta fase demostraron que el tratamiento T3B (1 /2 WPM+ 50g/1 sacarosa + 0.1 AIA) presentó la mejor respuesta del material vegetal, por cuanto se registraron explantes con mayor longitud promedio de raíces y plántulas que alcanzaron alturas superiores en relación a las observadas en otros tratamientos. Estas diferencias pueden ser atribuidas principalmente al efecto de interacción entre concentraciones del AIA y la sacarosa presentes en el medio de cultivo. El AIA es una auxina muy utilizada en esta etapa, debido a su característica de promotor de la formación de brotes radiculares; por otra parte, al aumentar la concentración de sacarosa, se logra producir un estrés fisiológico causado por el desequilibrio en el balance osmótico del sustrato, siendo dicho estrés el que genera la señal para la formación de nuevos brotes radicales (Moriconi eta!. 1991). El estudio realizado por Quezada & Rocabado (2005) indica que este tratamiento resultó ser el adecuado para inducir el enraizamiento in vitro de Polylepis racemosa ssp. lanata, coincidiendo con los resultados obtenidos en el presente trabajo.
Conclusiones
Para la desinfección de yemas apicales de Polylepis tomentella ssp. nana se determinó que el tratamiento óptimo consistió en la inmersión en solución de hipoclorito de sodio al 2% durante 10 minutos. El mejor tratamiento para el control de la oxidación resultó ser el enjuague de explantes ya desinfectados en una solución estéril de 300 mg/lde ácido cítrico y 300 mg/lde ácido ascórbico. A través de esta investigación, se determinó que la adición de carbón activado al medio de cultivo mostró un efecto inhibidor del crecimiento, generando incluso la necrosis de los tejidos.
Para la multiplicación in vitro de brotes caulinares de Polylepis tomentella ssp. nana se concluyó que el tratamiento óptimo para esta fase consistió en el uso del medio TL (Tremblay & Lalonde 1984), suplementado con 0.23 mg/1 de bencil aminopurina (BAP) y 0.1 mg /lde ácido indolbutírico (AIB), que resultó ser el balance hormonal adecuado (citoqu Mina /auxina) para la multiplicación de explantes establecidos de Polulepis tornentella ssp. nana en condiciones de cultivo in vitro, por cuanto permitió obtener individuos vigorosos, con una importante tasa de brotr y mayor número de hojas por explante.
Finalmente el tratamiento óptimo tanto para la formación y desarrollo radicular de las vitroplantas de Polylepis tomentella ssp. nana es el medio de cultivo Mc Cown & Lloyd (1980) al 50% de su concentración, con 50 g/ldesacarosa y 0.1 mg/1 de ácido indol acético (AIA).
Agradecimientos
Este trabajo se realizó gracias al financiamiento de Conservación Internacional y
Cruz, A.S. 1999. Efecto de sustratos orgánicos en la reproducción vegetativa de la queñua (P. incana, H.B.K.) Rosoideae. Tesis de ingeniería agronómica, Facultad de Agronomía, Universidad Mayor de San Andrés,
Darías, R. 1993. Recopilación de temas sobre técnicas de cultivo in vitro. Oruro, Bolivia. Universidad Camilo Cienfuegos de Matanzas, Santa Clara. 169 p.
Fernandez, E. 1996. Estudio fitosociológico de los bosques de kewiña (Polylepis spp.) en
Gonzales, C.O. & J.A. Vilca. 1998. Micropropagación vegetativa "in vitro" de aliso (Alnus acuminata). Red Andina de Semillas Forestales Chile, Colombia, Ecuador, Perú y Bolivia. (RASEFOR). Asociación Civil para
Hensen, I. 1994. Estudios ecológicos y fonológicos sobre Polylepis besseri Hieron, en la cordillera oriental boliviana. Ecología en Bolivia 23: 21-29.
Jiménez, E.1999.Aplicacionesde la biotecnología en la mejora genética de plantas y en la producción de semillas. Módulo 4. Propagación masiva de plantas in vitro. Instituto de Biotecnología de las Plantas, Santa Clara. 82 p.
Kessler, M. 1995. The genus Polylepis (Rosaceae) in
Kessler, M. & P. Driesch. 1994. Causas e historia de la destrucción de bosques altoandinos en Bolivia. Ecología en Bolivia 21: 1-18.
Kessler, M. & J. Fjeldsá. 2004. Conservación de la biodiversidad de los bosques de Polylepis de las tierras altas de Bolivia: Una contribución al manejo sustentable en los Andes. Centro para
Margara, J. 1988. Multiplicación vegetativa y cultivo in vitro Los meristemos y la organogénesis. Ediciones Mundi-Prensa, Madrid. 232 p.
Meneses, R.I. & S. Beck. 2005 Especies amenazadas de la flora de Bolivia. Conservación Internacional (C.I.) y
Artículo recibido en: Julio de 2006. Manejado por: Mónica Moraes. Aceptado en: Abril de 2007.
Moriconi, D. N., J. L. Burba & J. Izquierdo. 1991. Manual de intercambio y propagación de germoplasma de ajo a través de microbulbillos. FAO/RLAC, Santiago de Chile. 45 p.
Navarro, G. & M. Maldonado. 2004. Geografía ecológica de Bolivia: Vegetación y ambientes acuáticos. Editorial: Centro de Ecología Simón I. Patiño-Departamento de Difusión, Cochabamba. 719 p.
Pierik, R.L.M. 1990. Cultivo in vitro de las plantas superiores. Departament of Horticulture. Agricultural University Wageningen, versión española, Madrid. 325 p.
Prettell, J. 1985. Apuntes sobre algunas especies forestales nativas de la sierra peruana. Proyecto FAO/Holanda/INFOR, Lima. 113 p.
Rocabado, P. & J. Quezada. 2005. Inducción del enraizamiento in vitro de brotes caulinares de Polylepis racemosa a través del manejo de la concentración de ácido indolacetico (AIA) y sacarosa. BIOFARBO (13): 83-86.
Tarifa, T. & E. Yensen. 2001. Mamíferos de los bosques de Polylepis de Bolivia. Revista Boliviana de Ecología y Conservación Ambiental 9: 29-43. Fundación Simón y Patiño. Centro de Biodiversidad y Genética. Universidad Mayor de San Simón. Cochabamba.
]]> UICN. 2001. Categorías de la UICN, www. humboldt.org.co/conservacion/cat-uicn.Vega, C. 2002. Capacidad de regeneración de cuatro especies de keñua (Polylepis spp.) por medio de propagación in vitro. Tesis ingeniería agronómica, Carrera de Ingeniería Agronómica, Universidad Loyola,