
VACUNAS Y NUEVAS TENDENCIAS PARA EL VIRUS DEL PAPILOMA HUMANO
Vaccines and new trends for human papillomavirus
*Carola F. Carvajal Garcés, *Martha Morales Clavijo
* Medico Familiar Caja Nacional de Salud
]]> Recibido: 1-09-10; Aceptado: 15-10-10
RESUMEN
El cáncer cervical (CC) es la segunda neoplasia más común en mujeres a nivel mundial. Los VPH de tipo oncogénicos son la causa más frecuente, y hacia el año 2002 el cáncer cervico uterino fue el responsable de 274,000 muertes. Alrededor del 70% de los casos de CC son causados por dos de los VPH más oncogénicos: 16 y 18. Diez por ciento de los casos son causados por los oncotipos 45 y 31, los siguientes en frecuencia. La vacunación diseñada para evitar infecciones por VPH oncogénicos, aun cuando tiene el potencial de disminuir la morbimortalidad asociada con el CC y sus lesiones premalignas, no sustituye a las pruebas de tamizaje para diagnóstico temprano. Existen en el mercado dos preparaciones: Gardasil®, de Laboratorios Farmacéuticos Merck y Cervarix® de Laboratorios Glaxo Smith Kline. Nuevas herramientas se han diseñado para mejorar el marco de seguridad y eficacia de la vacunación, las cuales van desde mejorar la selección antigénica, la utilización de coadyuvantes para incrementar la inmunogenicidad e incluso la investigación sobre nuevas vías de administración. Estudios clínicos sobre la vacuna del VPH, que han tomado en cuenta estas características, reportan excelentes resultados en cuanto a seguridad, inmunogenicidad y eficacia para la prevención de infección por VPH. Hoy día, varios grupos están llevando a cabo investigaciones para desarrollar vacunas terapéuticas, lo que cambiaría el curso de esta patología; sin embargo, aún nos queda un largo camino que recorrer en este ámbito.
Palabras clave: VPH, vacunas.
ABSTRACT
Cervical cáncer (CC) is the second most common cáncer in women, caused by oncogenic types of human papiloma virus. In 2002 was responsible for 274,000 deaths worldwide. Approximately 70% of the cases of CC are caused by the two most common oncogenic HPV types: 16 and 18. 10% are caused by the next most common types: 45 and 31. Although preventive strategies such as vaccination do not substitute screening methods for CC, the development of these vaccines, designed to prevent infections caused by oncogenic types of HPV, have the potential to decrease morbidity and mortality associated with CC and precancerous lesions. Today are available in the market 2 types of vaccines: Gardasil® from Merck Pharmaceutical Laboratories and Cervarix from Glaxo Smith Kline Laboratories. Recently, new tools have being developed to improve the safety and efficacy or the HPV vaccines. These advances include improving the antige-nical selection, inclusión of coadjuvant agents to enhance the immunogenicity of the vaccine and investigation of new routes of administration. Clinical triáis of the HPV vaccine, that have used these technology, reported excellent safety, immunogenicity and efficacy for prevention of HPV infections. Today, many research groups, have being investigating and developing therapeutic vaccines, than may change the course of this disease; nevertheless, we have a long road to walk in this área.
Key words: HPV, vaccines.
]]>
INTRODUCCIÓN
El virus del papiloma humano (VPH) es la infección de transmisión sexual (ITS) más común.
Más del 50% de las mujeres y los hombres sexualmente activos son infectados por VPH en algún momento de sus vidas (1). Actualmente se considera a este virus un agente causal necesario para el cáncer cervical (CC). Aproximadamente el 100% de los CCU escamosos ó glandulares se asocian a la infecciones por esto que VPH es un agente que se ha establecido como causa necesaria pero no suficiente para el desarrollo de la enfermedad. No hay posibilidad de desarrollo de CCU en ausencia de VPH. El CC representa el 11% de todos los cánceres diagnosticados en mujeres en todo el mundo, convirtiéndose en la segunda neoplasia más frecuente a nivel mundial (1). Anualmente se estima que se presentan aproximadamente 500,000 casos nuevos en el mundo, de los cuales 80% ocurre en países en vías de desarrollo, lo que la convierte en la neoplasia más común en estos países, donde su incidencia llega a ser hasta de 40 por 100,000 mujeres(2).
Las verrugas genitales, el espectro benigno de la infección por VPH, representan un 33% de todos los diagnósticos en centros especializados en ITS. Más del 75% de los adolescentes y adultos de entre 15 y 49 años de edad se infectan por al menos un tipo de VPH a lo largo de su vida. La mayoría de las infecciones son subclínicas, detectables sólo por medio de una citología o mediante determinaciones de ADN vírico(2).
En algunos países donde se han instaurado como estrategia de salud la citología cervicovaginal, se ha aumentado la cobertura de esta prueba para disminuir la incidencia de lesiones premalignas y se tengan menos mujeres con CC. Sin embargo, a pesar de la estrategia de detección temprana, el CC sigue representando un grave problema de salud. La citología cervicovaginal tiene sus limitaciones y sus retos.
Desde el punto de vista diagnóstico tiene limitada sensibilidad y valor predictivo positivo. La experiencia del recurso humano juega un papel trascendental, ya que errores en la interpretación de la prueba podrían conllevar a un desenlace negativo en la mayoría de las pacientes(2).
¿Por qué una vacuna para el virus del papiloma humano?
¿Cuáles son las justificaciones racionales para que nosotros tomemos en cuenta incluir una vacuna contra el VPH?
1. Básicamente, más del 50% de los adultos sexualmente activos se infectan con VPH.
]]> 2. Porque se requiere hacer pruebas toda la vida y el cumplimiento de esto muchas veces es difícil, conllevando finalmente a costos elevados y sensibilidad limitada.3. Desafortunadamente la citología cervicovaginal detecta lesiones tempranas pero no las previene. De ahí que las vacunas son el futuro de la salud pública, en el ámbito local y mundial. Son las mejores estrategias en salud destinadas a invertir la pirámide en salud, haciendo una medicina preventiva más que curativa (3).
La vacuna contra el virus del papiloma humano, tiene actualmente dos presentaciones, Gardasil vacuna tetravalente (contra el carcinoma y contra las verrugas genitales) y bivalente Cervarix contra el carcinoma. En ambos casos se vacuna contra dos de los quince virus de alto poder oncogénico. Son los tipos 16 y 18, que se asocian al 70% de los carcinomas. Es una vacuna "profiláctica", no terapéutica(3).
EL VIRUS DEL PAPILOMA HUMANO (VPH)
El VPH es un patógeno exclusivamente intraepitelial con un genoma circular de 8 kb que se divide en seis genes tempranos (E7, E6, El, E2, E4 y E5) que codifican proteínas no estructurales y dos genes tardíos (Ll y L2) que codifican proteínas estructurales. Una característica clave de la infección por el VPH es su capacidad de provocar una infección multifocal una vez que infecta el epitelio de la región anogenital (4).
Existen más de 200 tipos de VPH estos difieren en cuanto a los tipos de epitelio que infectan. Algunos infectan sitios cutáneos, mientras otros superficies mucosas. En la actualidad, aproximadamente 20 millones de estadounidenses entre los 15 y 49 años (15% de la población) están infectados por el VPH (5). Cerca de la mitad de aquellos que están infectados con el VPH son adolescentes sexualmente activos y adultos jóvenes entre los 15 y 24 años. Entre un 5 y un 30% de las personas infectadas por el VPH están infectadas por varios tipos de VPH(4). Se estima que el 80% de la población mundial sufrirá un episodio de VPH a lo largo de su vida. Se relaciona con el 90% de cáncer de canal cervical y 40% de cáncer de vulva y pene y 12% con cáncer de vulva y de pene(4).

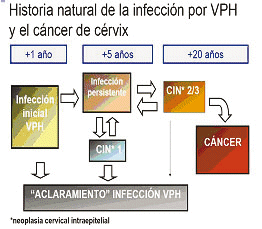
HISTORIA NATURAL DE LA INFECCIÓN POR VPH
]]> Las infecciones genitales por VPH, en la mayoría de los casos son asintomáticas y transitorias. Cerca del 70% de las mujeres con infecciones por el VPH se tornan negativas por el ADN del VPH en un año y el 91% en dos años. Las infecciones por el VPH 16 tienden a persistir más tiempo que las infecciones por otros tipos de VPH, pero en su mayoría son indetectables en 2 años(4).Únicamente alrededor de un 10% de las mujeres infectadas por el VPH padecerán de infecciones persistentes por VPH. Aquellas mujeres con una infección persistente por VPH de alto riesgo tienen mayor probabilidad de desarrollar lesiones premalignas y CC. Aún no está bien definido el riesgo de padecer lesiones de neoplasia intraepitelial cervical de grados 2 ó 3, para las mujeres con un riesgo persistente de contraer una infección por VPH de alto riesgo.
Según la Organización Panamericana de la Salud el tipo 16 es el factor viral oncogenico de alto riesgo mas prevalente para CCU y también se ha identificado que los tipos 18, 45, 58, 33 y 31 son dominantes en América Latina(3).
Cuatro de cada diez mujeres son VPH (+) al año de su debut sexual; seis de cada diez a los dos años. Se estima que el 80% de la población mundial sufrirá un episodio VPH a lo largo de su vida(3).
La distribución mundial de tipos de VPH en biopsias de CACU y en biopsias de neoplasias intraepiteliales de alto grado (CIN 3) ha sido recientemente publicada. En CACU la distribución para los cinco tipos más prevalentes es:
VPH 16-55.2%,
VPH 18-12.8%,
VPH 45-4.6%, ]]> VPH 31-3.8%,
VPH 33-3.7%
Bolivia tiene una de las tasas más altas de incidencia de este cáncer con 58/100,000, lo que significa un total de 661 muertes por año atribuidas al CACU(3).
MEDIDAS PREVENTIVAS
La prevención de la infección genital por el VPH es importante para reducir la prevalencia de las verrugas genitales, las citologías cervicovaginales anormales y el CC. En la actualidad una de las medidas preventivas para la infección por VPH es el desarrollo de vacunas contra la misma, debido a que se han demostrado anticuerpos contra proteínas del VPH en personas que presentaron regresión de la infección, por lo que es lógico suponer que una vacuna que simule la respuesta inmune para producir estos anticuerpos, sea eficaz para prevenir la infección por VPH (5).
Una meta clave en el desarrollo de vacunas contra el VPH, es diseñar una vacuna que manipule la respuesta inmune para crear una memoria inmunológica a largo plazo.
Algunas de las estrategias para lograr este objetivo incluyen la utilización de antígenos adecuados para estimular la respuesta inmune; desarrollo de nuevos coadyuvantes que promuevan la respuesta inmune primaria y en consecuencia la respuesta a largo plazo, y la investigación de inmunidad cruzada.
Hoy en día existen en el mercado dos preparaciones: Gardasil de Laboratorios Farmacéuticos Merck, y Cervarix de Laboratorios Glaxo Smith Kline. Son similares debido a que están conformadas por VLP (Virus Like Particles) del fragmento Ll de la cápside del VPH. La ausencia de ADN en las VLP hace que ambas sean seguras para utilizarse en las vacunas:(7)
Gardasil
]]> Es una vacuna tetravalente para los tipos de bajo riesgo 6 y 11 y de alto riesgo 16 y 18 (40 microgramos VLP de los tipos 11 y 16, y 20 microgramos de los tipos 6 y 18), que son responsables del 70% de los CC y del 90% de las verrugas genitales. Con el adyuvante hidroxifosfato sulfato de aluminio amorfo (225 μg).Fue desarrollada por los laboratorios Merck Research y Sanofi Pasteur MSD, aprobada por la FDA el 8 de junio de 2006. El esquema completo recomendado es la aplicación de tres dosis por vía intramuscular a los 0, 2 y 6 meses. Dosis 0.5 ce cada una(16). Las publicaciones existentes señalan a poco más de 5 años de seguimiento una eficacia de 96% (95% IC, 84-100) frente a la infección persistente de VPH, con una protección de 100% frente a NIC. Recientemente se ha comunicado, con un seguimiento de 18 meses, una protección del 100% (95% IC, 56-100) frente a NIV 2-3 (neoplasia intraepitelial vaginal). Asimismo, se han presentado algunos datos de inmunidad cruzada para los tipos 45, 31, 52 y 58 del VPH filogenéticamente cercanos, que sin estar cubiertos por la vacuna podrían significar un incremento de su poder profiláctico (8). Quedan en curso estudios contundentes que demuestren sin lugar a dudas el grado de eficacia de esta inmunidad cruzada hacia estos tipos de VPH. Los resultados de los estudios de inmunogenicidad de la vacuna tetravalente muestran que la respuesta inmunitaria de niños y niñas de 9 a 15 años es superior que en mujeres adultas jóvenes (16 a 23 años); con estudios que permiten suponer que la protección de esta vacuna podrá ser de larga duración(9).El 9 de junio de 2006, el Comité Asesor sobre Prácticas de Inmunización (ACIP, por sus siglas en inglés) recomendó el uso de la vacuna tetravalente en las mujeres entre 9 y 26 años de edad.
- El Gardasil previene cáncer cervical, vulvar y vaginal causado por VPH tipos 16 y 18.
- Prevención de verrugas genitales (condiloma acuminado) causadas por VPH tipos 6 y 11.
- Prevención de las siguientes lesiones precancerosas o displásicas causadas por VPH 6,11, 16 y 18:
- Neoplasia Intraepitelial Cervical (NIC) grado 273 Adenocarcionoma Cervical in situ (AIS).
- Neoplasia Intraepitelial Cervical (NIC) grado 1
- Neoplasia Intraepitelial Vulvar (NIV) grado 2 y 3.
- Neoplasia Intraepitelial Vaginal (NIVa ) grado 2 y3
- NIV grado 1 y NIVa grado 1.
]]> - También otorga protección para NIC grados 1,2 y 3 o AIS relacionados los VPH tipos 31, 32,52 y58 (16).Es la primera vacuna aprobada para el uso en mujeres entre 9-26 años, para la prevención de cáncer cervical, vulvar, vaginal, verrugas genitales y lesiones precancerosas. El esquema de vacunación recomendado tras el desarrollo clínico implica tres dosis intramusculares a los 0, 2 y 6 meses. El programa de desarrollo clínico de Gardasil incluyó más de 27.000 voluntarios adolescentes entre 9 y 15 años de edad y 20.541 mujeres de 16 a 26 años en 33 países. La eficacia de Gardasil fue evaluada en 4 ensayos clínicos. Los resultados de estos ensayos describen a los cinco años de seguimiento, una eficacia mantenida del 96% frente a la infección persistente de VPH, una protección del 100% frente a CIN 1 y una eficacia del 100% frente a CIN 2-3 con confirmación histológica(7).
1.-Niñas de 9 a 14 años. Máxima prioridad por su máximo potencial preventivo:
a. Elevada inmunogenicidad en este rango de edad.
b. No exposición previa al VPH y por tanto máximo potencial preventivo de la vacuna.
2- Mujeres hasta 25/26 años. Alta prioridad por evidencia de alto potencial preventivo.
a. Elevada inmunogenicidad en este rango de edad y eficacia demostrada.
b. Aquellas sin relaciones sexuales no habrán contactado con el VPH.
]]> c. Algunas con relaciones sexuales pueden no haber estado aún expuestas al VPH.
El esquema recomendado de vacunación es a los 0, 2 y 6 meses.
Se ha demostrado su posible administración simultánea con la vacuna contra el virus de la hepatitis B.
-No lleva time rosal (ni mercurio, por tanto).
-No se ha demostrado problema alguno en casos de sobredosis.
-Es compatible con los anticonceptivos orales.
-No se ha demostrado daño en caso de embarazo, ni de lactancia, pero no se recomienda su administración en estos casos (infrecuentes, además, en las edades recomendadas).
-No sabemos la correlación entre las cifras de anticuerpos en sangre y la eficacia de la vacuna. Desconocemos, pues, el resultado del binomio seroconversión-protección. No está demostrada su eficacia en niños (varones)(10).
Cervarix
]]> Consiste en VLP de proteínas Ll de VPH-16 y VPH-18 (20 microgramos de cada VLP). En el proceso de producción de antígenos se utiliza la tecnología de ADN recombinante BVES (baculovirus y cultivos de células). Contiene el adyuvante AS04 que es un lípido A monofosforilado (MPL 500 μg) e hidróxido de aluminio (50 μg).Esta vacuna fue desarrollada por el laboratorio Glaxo Smith Kline, dirigida específicamente a tipos de VPH de alto riesgo (16 y 18), se atribuye a su adyuvante AS04 una mejora en la respuesta inmunológica (12). El esquema completo recomendado incluye tres dosis a los 0, 1 y 6 meses, por vía intramuscular.Los resultados publicados hasta la fecha describen a los 4 y 5 años de seguimiento, una eficacia de 100% (95% IC, 30-100) frente a la infección persistente de VPH y una protección de 100% (95% IC, 42-100) frente a NIC. Ha mostrado también un cierto grado de protección cruzada frente a infección para los tipos VPH 31 (54.5% de eficacia) y VPH 45 (94.2% de eficacia). Fue aprobada por la Comisión Europea en septiembre 2007.(11)
Idealmente, la vacuna debe administrarse antes del inicio de la actividad sexual, entre los 11 y 12 años; incluso a los 9 años. Sin embargo, las mujeres sexualmente activas también pueden beneficiarse con la vacuna. Las mujeres infectadas por uno o más tipos de VPH recibirían protección únicamente para el tipo o los tipos en la vacuna que no tienen.
SEGURIDAD, EFICACIA Y DURACIÓN DE LA PROTECCIÓNDE LAS VACUNAS
En estudios realizados con más de 20,000 mujeres (entre 9 y 26 años de edad), se ha observado que las vacunas son seguras y no causan efectos secundarios serios. Los eventos adversos fueron, en su mayoría, un dolor leve en el sitio de la inyección.
El seguimiento de las cohortes (4-5 años) ha mostrado que la inmunidad adquirida posterior a la vacunación produce niveles de anticuerpos muy superiores a los que se producen ante la infección natural y modelos matemáticos elaborados a partir de otras vacunas sitúan una probabilidad de duración de por lo menos 15 años con niveles adecuados de inmunidad (títulos altos de anticuerpos); sin embargo, con los datos disponibles, no es posible saber si será necesario aplicar dosis de refuerzo(13).
Los ensayos clínicos realizados en mujeres sin VPH, entre 16 y 26 años de edad, demostraron una eficacia del 100% en la prevención de lesiones premalignas de cuello uterino causados por los tipos meta del VPH y una eficacia cercana al 100% en la prevención de lesiones premalignas vulvares y vaginales, así como de verrugas genitales causadas por los tipos meta del VPH en mujeres entre los 16 y los 26 años que no habían estado expuestas a los tipos específicos del VPH de la vacuna.
Estas vacunas son estrictamente profilácticas. Los datos actuales no indican que la vacunación tenga un efecto terapéutico en la infección por el VPH o enfermedades asociadas al VPH, incluidas las anormalidades en la citología cervicovaginal o las verrugas genitales.
Aunque es posible que la vacunación de los hombres con la vacuna tetravalente pueda ofrecer beneficios de salud directos a los hombres y beneficios de salud indirectos a las mujeres, actualmente no existen datos sobre su eficacia para respaldar el uso de la vacuna contra el VPH en los hombres. Se están realizando estudios de su eficacia en los hombres.
]]> No está claro el periodo de duración de la protección de la vacuna. Los estudios actuales (con un seguimiento de 5 años) indican que la vacuna es eficaz al menos por cinco años, pero se espera que pueda ser de por vida. En 10 años se notará el efecto de la vacuna sobre el cáncer cervical.Sin embargo, la inmunización con las vacunas disponibles para VPH de ninguna manera elimina la necesidad de pruebas de detección, por lo menos un 30% de los casos de CC que se presentan en la actualidad no podrán ser prevenidos por la vacuna, ya que no todos los tipos oncogénicos han sido incluidos. De ahí que las estrategias de tamizaje en las mujeres de mayor riesgo (mayores de 35 años), no sólo deben mantenerse sino fortalecerse con nuevas tecnologías que disminuyan los diagnósticos falsos negativos(14).
Resultados de los ensayos de vacunas profilácticas contra VPH
Existen diversos hallazgos claves respecto a la efectividad de las vacunas profilácticas contra VPH, 14, 15,16 entre ellos se encuentran:
1. Eficacia del 100% en la prevención de lesiones relacionadas con VPH 16-18, en mujeres antes del inicio de su vida sexual o que estén libres de la infección.
2. En mujeres con infección prevalente al VPH 16/18, la aplicación de vacunas no ha evidenciado un efecto.
3. Buena persistencia de anticuerpos durante 7 años.
4. Aceptable perfil de seguridad.
A este respecto, los resultados de los ensayos clínicos que se han desarrollado en más de 40 áreas geográficas en todo el mundo, han referido que las vacunas contra VPH son altamente eficaces contra infección persistente por VPH a los 6 y 12 meses21 y contra cualquier tipo de neoplasia intraepitelial cervical; en vacunas tetravalentes, también han sido eficientes contra lesiones genitales externas Actualmente, sin embargo, existen diversas controversias que serán dilucidadas en el futuro. Una de ellas se refiere a la vacuna bivalente contra VPH 16 y 18. Sus patrocinadores han referido un mayor nivel de eficacia cuando se utiliza adyuvante AS04. Asimismo, también se ha sugerido un mayor nivel de inmunogenicidad, cuyo impacto, en comparación con la vacuna tetravalente, no es conocido y posiblemente no se conocerá en el mediano plazo.
]]> En relación con la vacuna tetravalente contra los VPH 6, 11, 16 y 18, se ha documentado la utilidad para prevenir otro tipo de lesiones, entre ellas cánceres ano genitales, que incluyen el vulvar, vaginal y cáncer ano genital en hombres que tienen sexo con hombres. Asimismo, se ha documentado la prevención de otras enfermedades, como la papilomatosis respiratoria recurrente, las verrugas genitales, y una pequeña fracción prevenible de cáncer oro-faríngeo.Una limitación del uso de vacunas contra VPH es que éstas no tienen impacto cuando se administran en sujetos que cursan con infecciones de los tipos de VPH contenidos en la vacuna. Recientemente, sin embargo, se ha reportado que mujeres con seropositividad a VPH 16 y 18, en ausencia de infección clínica por VPH (ADN de VPH negativo), pueden beneficiarse con el uso de la vacuna.
Inmunogenicidad de las vacunas contra VPH
Con respecto a la inmunogenicidad de las vacunas, no se ha identificado una correlación de protección inmunológica en los vacunados, es decir, no se conoce el nivel mínimo requerido de anticuerpos para proteger contra la infección.
Lo que se ha establecido es la correlación entre presencia de anticuerpos y efecto profiláctico. Sin embargo, la inmunogenicidad se ha relacionado con la edad, y los niveles de anti-VPH en el mes séptimo con un esquema de tres dosis son estadísticamente más altos en las adolescentes menores de 12 años, en comparación con las adolescentes y mujeres de más edad.
En los estudios de inmunogenicidad llevados a cabo en los ensayos clínicos de vacunas contra VPH, es consistente la observación de un mayor pico de anticuerpos al séptimo mes del inicio de la vacunación. Posteriormente, se produjo un descenso paulatino de las GMT (títulos medios geométricos de IgG) y al llegar al mes 24 se estabilizaron, manteniéndose constantes hasta el mes 60(14).
La existencia de una respuesta inmunitaria de memoria se puso en evidencia en los sujetos previamente seropositivos frente a un VPH 16/18, cuando se les administró la vacuna y se observó un aumento considerable del título de anticuerpos frente a dicho VPH. Por otra parte, y más importante aún, es el hecho de que a un subconjunto de individuos (aproximadamente 80 sujetos), se les administró una dosis extra (cuarta dosis) de vacuna a los 60 meses de la primera vacunación y se detectó una rápida y vigorosa respuesta inmunitaria de memoria frente a los cuatro tipos de VPH incluidos en la vacuna, que excedió los niveles de GMT observados al séptimo mes de iniciada la vacunación(15).
Para la vacuna bivalente, la eficacia en mujeres se estableció en dos ensayos clínicos realizados en niñas y adolescentes de 10 a 17 años de edad. En todos los casos hubo seroconversión para ambos tipos de VPH, 16 y 18, después de la tercera dosis (en el mes 7), con unos GMT al menos 2 veces más elevados en comparación con mujeres vacunadas de 15 a 25 años(15).
Se conoce que la respuesta inducida de anticuerpos por la vacuna es mucho más alta que la que ocurre con la infección natural y que la respuesta inmune de las niñas de 9 a 11 años después de dos dosis de vacuna es similar o mayor a la obtenida después de tres dosis en mujeres de 16 a 26 años de edad, para las cuales se ha probado la eficacia de la vacuna.
De hecho, la respuesta inmune que genera la vacuna puede ser hasta 100 veces mayor a la inducida por la inmunidad natural. Con estos antecedentes, y desde la perspectiva de los servicios de salud, un esquema inicial con dos dosis y una tercera extendida tiene ventajas en su administración, ya que la organización de las estrategias para completar un esquema inicial de dos dosis, con una tercera a los 60 meses, es más sencilla.
]]> Antecedentes de vacunación con periodicidad de las dosis de 0, 6 y 60 mesesEl National Advisory Committee on Inmunization (NACÍ) en Canadá ha identificado la inmunogenicidad de dos dosis de vacuna y actualmente desarrolla una intervención en tres provincias de Canadá: British Columbia, Quebec y Nova Scotia que plantea el esquema con vacunación a los 0, 6 y 60 meses.39 Esta iniciativa es una de las 10 más relevantes que se implementan sobre la vacuna contra VPH en Canadá. Los argumentos para este tipo de intervención son los siguientes:
La inducción de anticuerpos por la vacuna es más alta que la producida por la exposición natural al virus.
La respuesta inmune de las niñas de 9 a 11 años de edad es similar a la obtenida después de tres dosis en mujeres entre los 16 y los 26 años de edad.
De acuerdo con estudios puente, nada indica que la vacuna será menos efectiva si se administra bajo un esquema extendido. Las intervenciones que se realizan regionalmente en Canadá son para determinar la inmuno genicidad y eficacia de este esquema.
La administración de la tercera dosis será en el momento en el que se requiere la máxima protección, es decir, alrededor del inicio de las relaciones sexuales.
Una dosis administrada a los cinco años de la primera vacunación tuvo una respuesta de anticuerpos más alta que la obtenida durante la vacunación primaria. Esta respuesta también ha sido observada con la vacuna contra la hepatitis B(17).
Conclusiones y recomendaciones del Strategic Advisory Group of Experts (SAGE)
Las siguientes son las conclusiones y recomendaciones del Strategic Advisory Group of Experts (SAGE) sobre inmunizaciones, de la Organización Mundial de la Salud, en la reunión de noviembre de 2008:
]]> La introducción de la vacuna profiláctica contra el virus del papiloma humano (VPH) puede ser de gran beneficio en el ámbito mundial.
Debido a la magnitud del cáncer cervical y otras enfermedades relacionadas a la infección con VPH, se recomienda que la vacunación contra el VPH se incluya en los programas nacionales de inmunización, considerando que la prevención del cáncer cervical constituye un problema de salud pública prioritario.
La introducción de las vacunas debe ser factible, sostenible y su financiamiento debe estar asegurado, por lo que ha de considerarse el costo-efectividad de las estrategias.
La vacunación es más eficaz en las mujeres que no han estado expuestas al VPH, por lo que el grupo blanco primario pueden ser las niñas y adolescentes entre los 9 y los 13 años de edad. Las decisiones finales deben basarse en los datos de edad de inicio de las relaciones sexuales y la factibilidad de facilitar la vacuna en escuelas, servicios de salud y la comunidad.
Es recomendable la vacunación de adolescentes de mayor edad como segundo grupo prioritario para la vacunación, en el caso de que sea económicamente factible, sostenible y costo-efectivo, y que además no sea causa de menor inversión de recursos para vacunar al primer grupo prioritario y que la proporción de adolescentes de mayor edad no expuestas al VPH sea significativa.
Actualmente no se recomienda vacunar a los varones.
Los estudios piloto en varios países sugieren que las estrategias basadas en la administración de la vacuna en las escuelas es factible.
Deben utilizarse estrategias que sean compatibles con la infraestructura de abasto, la capacidad de la red fría, y que además sean costo-efectivas y sostenibles para alcanzar la más alta cobertura posible.
Si la introducción se realiza por fases, deben privilegiarse las adolescentes con menor probabilidad de tener acceso al tamizaje de cáncer cervical en la vida adulta.
]]> La vacunación debe introducirse como parte de estrategias coordinadas de prevención del cáncer cervical y otras enfermedades relacionadas a la infección con VPH, como la educación para reducir las conductas que incrementan el riesgo de infectarse, la detección del cáncer cervical, así como el diagnóstico y tratamiento de las lesiones precursoras y del cáncer. Sin embargo, la vacunación no debe retrasarse en países donde una o más de esas intervenciones no puedan ser implementados al tiempo de la introducción de la vacuna. Las recomendaciones para el tamizaje del cáncer cervical deben seguir siendo las mismas en las mujeres vacunadas.
Las vacunas contra VPH se encuentran disponibles comercialmente, pero ningún país en Latinoamérica las ha introducido en el esquema de vacunación universal, a pesar de que existe una fuerte presión de la industria farmacéutica en países con ingresos medios para incorporarla como una política de salud(18).
La región de Latinoamérica tiene una incidencia y mortalidad por cáncer cervical entre 3 y 10 veces mayor que países industrializados y el PIB es un criterio recomendado por la OMS para implementar políticas de inmunización contra VPH; consecuentemente el PIB y el presupuesto en salud son considerablemente más bajos en Latinoamérica y no hay una justificación para implementar programas de vacunación poblacional contra VPH, ante el elevado costo. Un análisis de costo-efectividad de vacuna contra VPH en México determinó que las estrategias de prevención secundaria son más costo-efectivas para mujeres adultas, con la utilización del Papanicolaou y captura de híbridos. Para que la vacunación contra VPH sea costo-efectiva, deberá tener un costo no mayor de 18 USD por dosis.
Consideración ética en salud pública
La adopción de un esquema extendido de vacunación contra el VPH se justifica porque es seguro, se alcanzan niveles de inmunogenicidad adecuados, la logística de aplicación es más práctica y se incrementa la cobertura de detección en un tercio. Es una obligación del Estado combatir las desigualdades de salud y brindar protección en el ámbito de la prevención primaria y secundaria, con la mejor tecnología disponible en una elevada relación costo-beneficio. El esquema extendido atiende esta responsabilidad, ya que al aumentar la cobertura de protección en las niñas, se maximiza el beneficio ante recursos limitados, a diferencia de la otra propuesta en la que se salvan vidas pero sólo se beneficia a unas cuantas personas.
NUEVAS TENDENCIAS
Hoy día se están desarrollando vacunas terapéuticas, las cuales están diseñadas en contra de antígenos presentes en las células tumorales. En el caso del CC inducido por VPH, los blancos antigénicos más frecuentes son las proteínas E6 y E7, cuya expresión es necesaria para el mantenimiento del fenotipo tumoral.
Estas vacunas apuntan a controlar el cáncer asociado a VPH activando la propia respuesta inmune celular del paciente para reconocer y eliminar estas células que expresan proteínas extrañas.
]]> Las propuestas más novedosas en este ámbito incluyen modelos terapéuticos basados en inmunogenicidad a base de péptidos, vectores de ADN, víricos y bacterianos, inmunomoduladores, terapia fotodinámica, terapia basada en receptores de linfocitos T, etc. Los estudios preclínicos en modelos animales apuntan a la efectividad de una sola dosis de vacuna para lograr la erradicación de células tumorales. Sin embargo, es poco probable que esto pase en pacientes en quienes las células tumorales se han mimetizado con el sistema inmune para evadir su detección y erradicación. Debido a lo anterior, aún queda mucho campo para la investigación de nuevas medidas terapéuticas para las lesiones inducidas por VPH (18).
CONCLUSIÓN
Aunque la vacuna de VPH ofrece un nuevo enfoque prometedor para la prevención de infecciones por este virus y las condiciones asociadas a éste, las vacunas no sustituirán a las otras estrategias de prevención, como las pruebas de detección.
Hoy en día las vacunas contra VPH son una realidad y han marcado un hito histórico a nivel mundial en cuanto a la prevención de los posibles efectos que la infección por VPH podría causar. Es un hecho que estas vacunas ofrecen una gran oportunidad en la prevención del CC. El carcinoma escamoso del cuello uterino sería uno de los únicos cánceres que se podrían prevenir con una vacuna, incluyendo sus lesiones premalignas(18).
En Bolivia y en otros países latinoamericanos en desarrollo el principal reto que existe para la implementación de la vacuna es el económico, se requiere que los países desarrollados proporcionen la evidencia necesaria que justifique la implementación de esta vacuna en los programas de salud ya existentes y así buscar nuevas estrategias para obtener vacunas baratas y fáciles de distribuir.
Es imprescindible la implicación de los pediatras, así como de ginecólogos y especialistas en medicina familiar para una adecuada campaña de vacunación contra el VPH. Así mismo, deben llevarse a cabo campañas publicitarias sobre la prevención de VPH y los riesgos asociados a su transmisión. Aún quedan muchas cuestiones qué resolver en torno a estas vacunas, como la duración a largo plazo de la protección y la necesidad de una o varias dosis de refuerzo, la eficacia de la vacuna administrada en el sexo masculino, corroborar el perfil de elevada seguridad que se ha mostrado hasta la fecha, determinar la estrategia de vacunación en aquellos adultos jóvenes que previamente hayan tenido un posible o probable contacto con el virus, entre otras. Igualmente importante, es el desarrollo de vacunas terapéuticas, que aún representan un reto para los investigadores, ya que en el mundo existen millones de personas infectadas por VPH.
BIBLIOGRAFÍA
1. Einstein MH, Goldberg GL. Human papillomavirus and cervical neoplasia. Cáncer Invest 2002; 20(7 8): 1080-1085. [ Links ]
2. Franco EL, Franco ED, Ferenczy A. Cervical cáncer: epidemiology prevention and the role of human papillomavirus infection CMAJ 2001; 164(7).
3. http://www.ops.org.bo/servicios. [ Links ]
4. Silvestre Fernández, Julio; Asturizaga, David; Peredo Beltrán, Gonzalo.Virus papiloma humano y cáncer de cervix: avances en la patogenia, diagnóstico y prevención. Cáncer Invest 2002; 20(7 8): 1080-1085. [ Links ]
5. World Health Organization. Human papillomavirus infection and cervical cáncer. 2004. [ Links ]
6. En: http://www.who.int/vaccine_research/diseases/hpv/es/. [ Links ]
7. Centros para el Control y la Prevención de Enfermedades (CDC).Genital HPV Infection-CDC Fact Sheet. 2004. [ Links ]
8. En: http://www.cdc.gov/std/HPV/STDFact-HPV.htm. [ Links ]
9. Vizcaíno A, Moreno V, Bosch F, Muñoz N, Barros X, Parkin D. International trends in the incidence of cervical cáncer. Int J Cáncer 1998; 75: 536-545. [ Links ]
10. Dirección General de Información y Evaluación del Desempeño. Secretaría de Salud. Salud: México 2001: Cáncer cervicouterino. SSA 2002. [ Links ]
11. Muñoz N, Bosch F, Sanjosé S, Valadui P, Tormo J, Ascunce N y cols. El virus del papiloma humano en la etiología del cáncer cervicouterino. Bol of Sanit Panam 1993; 115(84): 301-308.
]]>12. Greer C, Wheeler C, Ladner M, Beutner K, Coyne MY, Liang H, et al.Human papillomavirus (HPV) type distribution and serological response to HPV type 6 virus-like particles in patients with genital warts. J Clin Mi-crobiol 1995; 33:2058-63. [ Links ]
13. Koutsky LA, Ault KA, Wheeler CM, Brown DR, Barr E, Álvarez FB et al. A controlled trial of a human papillomavirus type 16 vaccine. N Engl J Med 2002; 347: 1645-1651. [ Links ]
14.Clifford GM, Smith JS, Plummer M et al. Human papillomavirus types in invasive cervical cáncer worldwide: a meta-analysis. Br J Cáncer 2003; 88(1): 63-73. [ Links ]
15. Muñoz N, Bosch FX, Castellsague X, Díaz M, de Sanjose S, Hammouda D et al. Against which human papillomavirus types shall we vaccinate and screen? The international perspective. Int J Cáncer 2004; 111: 278-285.
16. Gardasil: Quadrivalent Human Papillomavirus (Types 6, 11, 16, 18) Recombinant Vaccine Product Information. Whitehouse Station, NJ. Merck&Co., Inc. http://www.merck.eom/product/usa/picirculars/g/gardasil/gardasil_pi.pdf. [ Links ]
17. Agencia Europea de Medicamentos (EMEA). Informe Público Europeo de Evaluación (EPAR) Cervarix. 2007.En: www.emea.europa.eu/humandocs/PDFs/EPAR/cervarix/H-721-es1.pdf. Consultado el 3 de febrero de 2008. [ Links ]
18. Stanley M, Lowy D, Frazer I. Prophylactic HPV vaccines: underlying mechanisms. Vaccine 2006; 24:S106-13.12. Jansen K, Shaw A. Human papillomavirus vaccines and prevention of cervical cáncer. Annu Rev Med 2004; 55:319-31. [ Links ] [ Links ]
Este artículo fue revisado bajo las Normas Internacionales de Index Médicas
]]> ]]>