
CÁNCER DE MAMA Y EMBARAZO: PRESENTACION DE DOS CASOS
* Carlos Gutiérrez Flores,* Erwin Hochstatter Arduz,* Oscar Niño de Guzmán Peña,** Rodrigo Heredia Alba
* Ginecólogo Obstetra C.N.S.-Docente Titular Ginecología U.M.S.S.
** Residente de 3er Año Cirugía General
]]>
RESUMEN
El cáncer de mama durante el embarazo es una circunstancia clínica infrecuente. Esta asociación plantea interrogantes en lo referente al manejo de la madre en su condición fisiológica especial y la seguridad del feto. Presentamos dos casos:
La primera paciente de 46 años en la cual durante el primer trimestre de embarazo se identifica un carcinoma mamario derecho. No tenía antecedentes de cáncer mamario familiar ni hereditario. La punción biopsia por aguja fina reveló adenocarcinoma de alto grado nuclear. Fue estadificado como T3 NI M0 Estadio IIIa. A las 13 semanas de embarazo se realizó una histerectomía en bloque más salpingo ooferectomia bilateral. Se inicio 4 ciclos de quimioterapia neoadyuvante A la conclusión tratamiento se realizo mastectomia
La segunda paciente de 37 años de edad que en su primera consulta prenatal a las 34 semanas, se diagnostica CA de mama derecha inflamatorio. Se estadifico T4 N2 M0 Estadio IIIb. Resultado de la PAAF concluyó positivo para células neoplásicas, compatible con adenocarcinoma. Se decide interrumpir el embarazo mediante cesárea mas ovariectomia bilateral a las 36 semanas. Posteriormente se realiza 4 ciclos de quimioterapia neoadyuvante, para finalmente realizar mastectomia simple.
Palabras claves: Cáncer mama; Embarazo; Quimioterapia.
ABSTRACT
Cancer of breast during the pregnancy is an infrequent clinic circumstance. This asociation raises questions with respect to the handling of the mother in special her condition fisiolgic and the security of the fetus. We presented displayed two cases:
The first patient of 46 ears in which during the first trimester a mamary carcinoma is identified straight. It Ins't antecedents of cancer mamary hereditary relative nor. Puncin biopsy by positive fine needle revel for adenocarcinom of high nuclear degree. That he was estadific like T3 NI M0 IIIa Stage. To the 13 weeks of realiz pregnancy one histerectomi in bilateral block whit salpingo ooferectomia. Beginning 4 cyles of neoadjuvant chemotherapy. To conclusin make mastectomia simple.
The second patient of 37 ears of age that in his first prenatal consultation to the 34 weeks, diagnostic inflammatory CA of right breast. That estadific T4 N2 M0 IIIb Stage. Result of positive for cels neoplasic, the PAAF concluy with adenocarcinom. It is decided To interrupt the pregnaney by means of bilateral surgeri but oferectomia to the 36 weeks, later is made 4 cycles of neoadjuvant chemotherapy, finally to make mastectomia simple.
]]> Key words: Cancer breast; Pregnancy; Chemotherapy.
INTRODUCCIÓN
El cáncer de mama y embarazo es definido como aquel carcinoma de la glándula mamaria que se diagnostica durante la gestación o durante el primer año del posparto. Se trata de una situación infrecuente, que es diagnosticada en aproximadamente 1 de cada 3.000 partos. Su incidencia varía entre el 0.76% a 3.8% de todos los casos nuevos de cáncer de mama. Corresponde a la neoplasia maligna más común asociada con la gestación y aunque el número es relativamente bajo, se espera que a futuro aumente debido a que cada vez es mayor el número de mujeres que postergan su primer parto hasta la cuarta o quinta década de su vida, período en el cual se incrementa la incidencia de cáncer de mama.
La búsqueda de un cáncer de mama durante el embarazo es compleja transcurriendo, en algunas oportunidades, varios meses antes de su confirmación diagnóstica. Este retraso diagnóstico se atribuye a varias razones en las que destacan los cambios fisiológicos que ocurren en las mamas durante embarazo por la influencia hormonal y la presunción de enfermedad benigna por parte del médico y/o de la paciente. Por otra parte, la mamografía no se realiza rutinariamente porque estas mujeres generalmente se encuentran bajo la edad en que este examen se recomienda como screening, aparte de que su rendimiento es limitado por la gran densidad de la glándula y el procedimiento podría ser riesgoso para el feto.
Una vez que se ha confirmado el diagnóstico, el manejo debe ser multidisciplinario. Se deben evaluar las modalidades terapéuticas actualmente disponibles, los beneficios y riesgos tanto de la cirugía radical y conservadora, de la quimioterapia y de la radioterapia. La radioterapia está contraindicada durante el embarazo por riesgo de irradiación al feto.
Una vez que se ha establecido el estadio del cáncer, la edad de gestación y discutido el plan terapéutico escogido, su aplicación no debe aplazarse por la coexistencia con el embarazo.
El carcinoma inflamatorio de mama (CIM) es una forma rara, pero particularmente agresiva de cáncer de mama. Es el tumor más maligno de todos los carcinomas mamarios. Su especial comportamiento biológico con rápida evolución local y una diseminación sistémica precoz, alto índice de recidiva loco regional y poca respuesta a los tratamientos han ubicado al CIM como la variedad de peor pronóstico. Su identificación del CIM se basa en la presentación clínica típica o en la demostración de la invasión tumoral en los linfáticos dérmicos.
El objetivo de esta comunicación es dar a conocer dos casos Clinicos de pacientes portadoras de embarazo asociado a cáncer de mama que fue manejado en nuestro hospital.
]]> Los cambios fisiológicos que ocurren en la mama durante el embarazo y la lactancia pueden motivar que la detección e interpretación de eventuales anormalidades mamarias presente dificultades desde el punto de vista clínico e imagenológico. La mayoría de las anomalías mamarias que se presentan en este período son de etiología benigna, sin embargo la aparición de cualquier alteración requiere una pronta evaluación conducente a confirmar o descartar la presencia de un cáncer de mama asociado al embarazo.El examen físico exhaustivo de mama previo al embarazo y la realización de una mamografía dependiendo de la edad de la paciente y de los factores de riesgo de cáncer mamario, son medidas esenciales para diagnosticar alguna anormalidad de esta glándula. Si el examen no se lleva a cabo durante la consulta inicial, una buena ocasión para detectar anomalías mamarias es el primer trimestre del embarazo, puesto que aún ocurren pocos cambios que puedan dificultar la valoración de las mamas. Posteriormente la mastalgia natural e hiperemia propias de las mamas grávidas y puerperales pueden entorpecer la palpación de un tumor y por consiguiente alejar la oportunidad de un diagnóstico temprano de cáncer de mama comprometiéndose de esta forma el pronóstico de la paciente. Se ha descrito que el retraso entre los primeros síntomas hasta que la detección de un tumor de mama en la embarazada plantea el desafío de determinar su naturaleza biológica tomando en cuenta el binomio madre hijo. Una aproximación diagnóstica inicial puede lograrse mediante la ¡maginología. El uso de la mamografía en la embarazada ha suscitado debates en cuanto al riesgo de irradiación a que se expone el feto y al rendimiento que tiene examen. Si bien es cierto que en el pasado no se indicaba por el temor de irradiación fetal, estudios recientes no avalan esta creencia, puesto que con las 2 proyecciones estándar del examen se somete al feto a sólo 0.4 mcCy (0.004 Gy) estableciéndose que dosis menores de 5 cGy no provocaría aumento del riesgo de malformaciones congénitas, aborto o restricción del crecimiento fetal por radiación ionizante. Respecto al rendimiento de la mamografía en la embarazada, las tasas de falsos negativos varían entre el 22% y el 75%, a raíz del aumento en el tamaño, vascularización y de la densidad glandular. En beneficio de la seguridad, se aconseja que la mamografía deba usarse en forma selectiva y con protección adecuada, cuando resulta necesario establecer la presencia de cáncer de mama bilateral y planificar la extensión de la cirugía.
La ecografía mamaria podría tener más ventajas que la mamografía como examen inicial, por tratarse de una técnica rápida, exacta e inocua para el feto, siendo capaz de diferenciar los quistes de los tumores sólidos en un 97% de los casos. Es también una buena guía para realizar citologías por punción aspirativa con aguja fina o biopsias percutáneas con aguja gruesa de tumores sospechosos.
La citología por punción aspirativa con aguja fina, aunque está recomendada, a menudo, es de muy difícil interpretación durante el embarazo. Este procedimiento sólo es útil cuando el resultado es positivo para células neoplásicas; los resultados negativos no descartan el diagnóstico de cáncer y requieren mayor investigación.
Si una vez realizada la evaluación del tumor mediante imaginología y eventualmente con citología por punción aspirativa, persiste la duda sobre la benignidad o malignidad debe procederse a su estudio histológico para establecer un diagnóstico definitivo, utilizando el método menos invasivo y de mayor rendimiento. Con tal objetivo se pueden realizar biopsias percutáneas o quirúrgicas idealmente bajo anestesia local. La biopsia percutánea tiene buen rendimiento y permite el diagnóstico de invasión. El riesgo de una fístula láctea secundaria al procedimiento probablemente ha sido sobrestimado.
El tipo histológico del Cáncer mamario durante el embarazo no difiere substancialmente al de una mujer no embarazada, siendo el carcinoma ductal invasor el más frecuente seguido por el carcinoma lobular invasor. Diferentes comunicaciones han mostrado que la mayoría de los cánceres son de alto grado y que es común la invasión linfática y vascular. En el estudio del Anderson Cáncer Center, el 79% de los pacientes presentaron linfonodos axilares positivos. Las metástasis nodales a la axila ipsilateral pueden ser una consecuencia de un diagnóstico tardío o de la conducta agresiva del tumor, no obstante hay que tener en cuenta que las mujeres jóvenes comparativamente con las mujeres de mayor edad, tienden a tener más metástasis nodales en el momento del primer diagnóstico. Usualmente los tumores presentan receptores de estrógeno y/o progesterona negativos.
Para estatificar el Cáncer mamario durante el embarazo se utiliza el sistema TNM. Como las mujeres con Cáncer mamario durante el embarazo a menudo presentan, al momento del diagnóstico, un tumor primario de gran tamaño y con frecuencia existe compromiso axilar lo que conlleva un estadio avanzado, puede ser necesario descartar metástasis sistémicas.
Para la estadificación se requiere tomar medidas especiales para no exponer al feto a la radiación. La radiografía de tórax no tiene contraindicación puesto se expone al feto a menos de 0,01 cGy pero aun así se recomienda protección abdominal. La ecografía abdominal para evaluar metástasis hepáticas es segura y no tiene inconvenientes en el embarazo.
La cintigrafía ósea no esta recomendada porqué utiliza isótopos radiactivos (Tc 99) al igual que tomografía computada por el riesgo de exposición fetal a la radiación y si se precisa de ella debe ser diferidas hasta el puerperio.
El carcinoma inflamatorio de mama presenta características clínicas propias definidas por la presencia de: Eritema, edema, predominando en la parte declive al principio, calor local, piel de naranja, rigidez glandular, a veces sensible a la palpación. La característica clínica esencial es una progresión muy rápida de los signos mencionados hasta un agravamiento considerable y una induración generalizada de la mama, con extensión del enrojecimiento y edema de la piel. El enrojecimiento de la piel es el rasgo más distintivo del CIM el que debe tomar más de la tercera parte de la piel mamaria y en general afecta la mayoría de la misma. Frecuentemente no se asocia la presencia de una masa palpable, para algunos, esta se encuentra en un 50% de los casos. La induración puede ocupar un cuadrante o la mitad de la mama y formar así un tumor dominante, aunque nunca bien delimitado.
]]> El CIM se considera en forma separada del estadio III por su distintiva presentación y evolución natural y el especial desafío que presenta a un tratamiento efectivo.El sello histopatológico del CIM es la presencia de émbolos tumorales en los linfáticos dérmicos e intramamamarios en forma extensa. En la dermis la invasión tumoral puede estar presente en grado variable o ausente.
No existe una verdadera inflamación, la obstrucción linfática es producida por un aumento de la presión capilar que explica el edema siempre presente. Se considera que el bloqueo de los linfáticos con congestión capilar resultante sería el fenómeno responsable del edema y eritema clínico.
La presencia de invasión linfática dérmica es raramente posible de identificar por medio de la biopsia con aguja, por eso se recurre a la biopsia incisional que debe incluir la extracción de: un fragmento de piel, tejidos subcutáneos, y un sector mamario. La misma se puede realizar en forma incruenta, con anestesia local. Los defensores de la misma afirman que debe ser realizada rutinariamente para corroborar el diagnóstico y previamente a toda acción terapéutica. Incluso se plantea la posibilidad de biopsias en zonas de piel adyacente al tumor, en apariencia sana para valorar la progresión lesional más allá de los límites mamarios.
La extensión lesional a distancia se evalúa con: radiografía de tórax, huesos, o perfil y enzimas hepáticas, ecografía, centellografia. La biopsia por aspiración de médula ósea y tomografía de cráneo se realizan si están clínicamente indicadas.
La valoración biológica debe incluir: valoración hematológica completa, marcadores tumorales (CA 15-3). dosificación de receptores hormonales.
El análisis de los niveles de receptores hormonales de estrógeno y progesterona se realiza en forma rutinaria para la mayoría de los autores, y se realiza por punción aspiración con aguja fina, o de las muestras biopsicas quirúrgicas, y se debe realizar antes de cualquier manipulación terapéutica.
CASO CLÍNICO
CASO N° 1
]]> Mujer de 46 años, portadora de coxoartrosis de cadera derecha, que desde hace 1 año se palpa una masa de crecimiento progresivo localizado en mama derecha. Acudió a nuestro centro por dolor a nivel de cadera derecha siendo tratada y manejada en el servicio de traumatología quienes posteriormente derivan al servicio de Ginecoobstetricia para manejo. Entre sus antecedentes ginecoobstétricos destacó menarquia a los 14 años, G5 P4 A0 C0, amenorrea de 3.5 meses. No refirió antecedentes de cáncer de mama familiar ni hereditaria. En el examen físico mamario se encontró mama izquierda de morfología normal, mama derecha (Fig. 1) aumentada de tamaño en región supraareolar y areolar interna se observa piel de naranja, umbilicacion del pezón ambas en forma discreta, se palpa masa que compromete ambos cuadrantes superiores e inferior externo de consistencia pétrea fija no dolorososa de 10 por 6 cm, se palpa ganglio en región axilar de 0.8 cm. móvil no doloroso. No se encontraron adenopatías cervicales sospechosas de malignidad.
Una ecografía mamaria mostró lesión nodular difusa en mama derecha de 10 x 6 cm. con zonas hipoecogénicas, de contornos irregulares. BIRADS IV resto del examen sin alteraciones (Figura 2). La ecografía pélvica que informa embarazo de 13 sem +- 1 sem. Se realizó punción biopsia con aguja fina del tumor concluyó positivo para células neoplásicas. compatible con adenocarcinoma de alto grado nuclear.
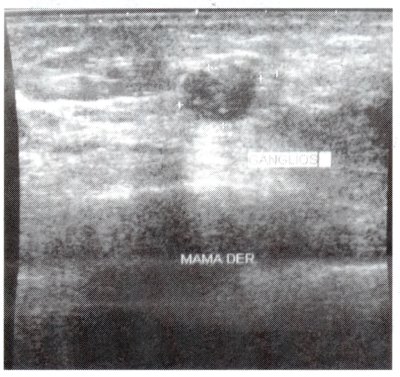
Fig. 2 Ecografía mamaria que muestra infiltración nodular difusa predominio cuadrantes superiores
Con los diagnósticos de carcinoma de mama derecha T3 N1 M0 Estadio III a y embarazo de 14 semanas. Se decidió interrumpir el embarazo mediante histerectomía en bloque mas salpingo ooferectomia bilateral. Posterior a su recuperación pasa a servicio de oncología para tratamiento por la especialidad, finalmente previa valoración por el servicio de oncología se realiza mastectomia.
CASO Nº 2
]]> Paciente de 37 años de edad que en su primera consulta prenatal a las 34 semanas, se diagnostica CA de mama derecha inflamatorio. Las características clínicas : Mama derecha (Fig. 3) con importante aumento de tamaño por el edema marcado, eritema y piel de naranja; masa palpable dura, fija, irregular de aproximadamente 7x7 cm. Adenopatía axilar ipsilateral de 4x4 cm. La paciente tiene dos hijos vivos nacidos por cesárea.
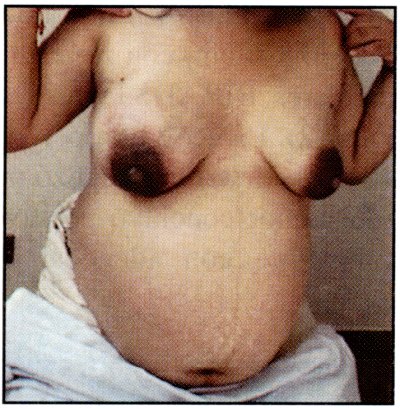
| Fig. 3 Mama derecha con importante aumento de tamaño por el edema marcado, eritema y piel de naranja; masa palpable dura, fija, irregular de aproximadamente 7 x 7 cm. |
La ecografía mamaria reporta masa sólida vascularizada con zonas de degeneración quistica. Se realiza en la misma fecha ecografía pélvica que informa embarazo de 34-35 sem. FUV de características normales para la edad gestacional.
Resultado de la PAAF concluyó positivo para células neo-plásicas, compatible con adenocarcinoma. Se decide interrumpir el embarazo mediante cesárea mas oferectomia bilateral, obteniéndose un recién nacido de sexo masculino, de 3980 g de peso. No hubo lactancia, posterior a su recuperación pasa al servicio de oncología donde se somete a 4 ciclos de quimioterapia neoadyuvante, previa valoración por el servicio de oncología pasa al servicio de Cirugía general donde se realiza mastectomia simple en el postoperatorio evolucionó satisfactoriamente. Finalmente se realiza quimioterapia y radioterapia post operatoria.
Actualmente ( 27 meses ) la paciente se encuentra asintomática con cáncer de mama controlado sin evidencias de recidiva local, regional ni sistémica y su hijo se encuentra eutrófico y con un desarrollo psicomotor adecuado para su edad.
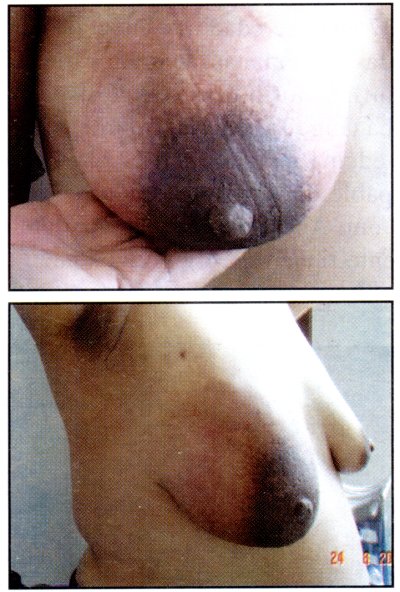
| ]]> Fig. 4 Mama derecha con importante aumento de tamaño por el edema marcado, eritema y piel de naranja, masa palpable dura, fija irregular de aproximadamente 7 x 7 cm. |
COMENTARIO
Establecido el diagnóstico de cancer de mama cada paciente necesita una decisión terapéutica individual, asumida por un equipo muldisciplinario y con la anuencia de la embarazada, tomando como referencia principal el estadio de la enfermedad y la edad gestacional del feto.
La cirugía puede realizarse en forma segura durante el embarazo. La conducta convencional es esperar que se hayan completado 12 semanas de gestación con el objeto de minimizar el riesgo de aborto espontáneo. La cirugía de elección para el es la mastectomia con disección axilar. La cirugía conservadora que implica mastectomia parcial más disección axilar no es recomendada en la primera mitad del embarazo puesto que la radioterapia requerida para completar el tratamiento local está contraindicada durante el embarazo, por el riesgo que implica para el feto la exposición a la radiación, sin embargo puede plantearse como una opción en el tercer trimestre del embarazo advirtiendo que los resultados cosméticos podrían ser pobres debido a los cambios anatómicos que ocurren en la mama durante el embarazo.
La radioterapia no se recomienda durante el embarazo debido a los riesgos de teratogenecidad e inducción de desórdenes malignos en el feto. Una dosis terapéutica habitual de 50 Gy se asocia con una dosis fetal de 3.9-15 cGy en el primer el trimestre del embarazo llegando hasta 200 cGy hacia el fin de éste, cuando el útero asciende hasta la vecindad del diafragma. El umbral de la dosis fetal de radiación sobre la cual puede verse abortos, teratogénesis o crecimiento anormal es de 10 a 15 cGy a las 20 semanas de edad gestacional y entre 25-50 cGy después de este período. Después del parto la radioterapia no tiene contraindicación.
Cuando una mujer sobrelleva un Cáncer mamario durante el embarazo, los agentes quimioterápicos son capaces de cruzar la placenta. Si son administrados antes de las 15 semanas de gestación, período en que se produce la organogénesis inicial del feto, pueden interferir la diferenciación celular. El primer trimestre del embarazo es el período más crítico en el cual pueden ocurrir daños severos en el feto que pueden provocar aborto espontáneo o daños subletales que inducen malformaciones, teratogénesis, mutaciones, carcinogénesis, toxicidad de órganos o retraso mental.
En efecto en este periodo, las malformaciones fetales asociadas a quimioterapia son 2.7-17% en contraste con la proporción usual de malformaciones en la población general que oscila entre 1-3%. Durante el segundo y tercer trimestres del embarazo la quimioterapia puede ser administrada con mínimas complicaciones para el feto y la madre.
Cuando es necesario usar quimioterapia se recomienda iniciar los ciclos a partir las 18 semanas de gestación. Se sugiere el uso de Ciclofosfamida, Doxorrubicina y Fluorouracilo. No se recomienda Metotrexato por tratarse de un antagonista del ácido fólico, elemento indispensable en el desarrollo del sistema nervioso fetal. El último ciclo debe ser administrado alrededor de la 34 semana de gestación y evitar que se produzca el parto entre día 1 y 14 del ciclo de la quimioterapia.
La mayoría de las drogas usadas en el tratamiento pueden ser detectadas en la leche de las puérperas, por lo cual la lactancia materna sólo se considera segura una vez transcurridas 2 a 4 semanas de completado el último ciclo de quimioterapia.
]]> La manipulación hormonal, si está indicada, se inicia posterior al parto y después de la realización de la quimioterapia. Aunque existen reportes de uso de tamoxifeno durante el embarazo se considera que la droga puede producir malformaciones fetales, por lo cual generalmente se contraindica durante la gestación.El pronóstico de las mujeres con Cáncer mamario durante el embarazo es similar pronóstico que las mujeres no embarazadas con la misma enfermedad. Petrek reporta que comparando estadio por estadio, no hay ninguna diferencia en la sobrevida entre las mujeres embarazadas y aquellas que desarrollan el cáncer sin estar embarazadas y que en el cáncer en estadio temprano ambos grupos tienen porcentajes de sobrevida de aproximadamente 80%. Sin embargo, como el Cáncer mamario durante el embarazo se diagnóstica con mayor frecuencia en estadios avanzados globalmente su pronóstico impresiona como muy adverso. No existe evidencia suficiente para afirmar que la interrupción del embarazo cambie el pronóstico.
En caso de carcinoma inflamatorio de mama
Tras la cirugía estaría indicado continuar con quimioterapia a base de los mismos fármacos y dosis hasta un máximo de 6 tandas, con el objeto de realizar un tratamiento sistémico complementario que reduzca la incidencia de metástasis a distancia.
En cuanto al tratamiento local, la indicación se establece casi siempre puesto que la respuesta local no se mantiene y el nuevo rebrote va a ser muy difícil de tratar localmente. Se prefiere la cirugía cuando se demuestra que queda masa tumoral y la radioterapia cuando no se evidencia resto tumoral, puesto que en muchas ocasiones de carcinoma inflamatorio puro sin tumor tras la mastectomía no se han encontrado células neoplasicas.
El intervalo ideal entre el tratamiento del cáncer de mama y el siguiente embarazo es desconocido.
BIBLIOGRAFÍA
1. SMITH LH, DANIELSEN B, ALLEN ME, CRESS R. Cancer associated with obstetric delivery: results of linkage with the California cancer registry. Am J Obstet Gynecol 2003: 189: 1128-35. [ Links ]
2. ANTONELLI NM, DOTTERS DJ. KATZ VL, KULLER JA. Cancer in pregnancy - a review of the literature: parts 1 and 2. Obstet Gynecol Surv 1996; 51: 125-42. [ Links ]
3. PAVLIDIS N, PENTHEROUDAKIS G. The pregnant mother with breast cancer: Diagnostic and therapeutic management. Cancer Treat Rew 2005 en prensa. [ Links ]
4. PAVLIDIS NA. Coexistence of pregnancy and malignancy. Oncologist 2002: 7: 279-87. [ Links ]
5. WOO JC. YU T, HURD TC. Breast cancer in pregnancy: a literature review. Arch Surg 2003; 138: 91-8 [ Links ]
6. SOROSKY JI. SCOTT-CONNER CEH. Breast disease complicating pregnancy. Obst Gynecol Clin North Amer 1998; 25: 353-63. [ Links ]
7. HOGGE JP, DE PAREDES ES, MAGNANTCM. LAGE J. Imaging and management of breast masses during pregnancy and lactation. Breast J 1999; 5: 272-83 [ Links ]
8. PUCKRIDGE PJ. SAUNDERS CM, IVES AD. SEMMENS JB. Breast cancer and pregnancy: a diagnostic and manamanagement dilemma. ANZ J Surg 2003; 73: 500-3. [ Links ]
9. ISAACS JH. Cancer of the breast in pregnancy. Surg Clin North Am 1995:75: 47-51. [ Links ]
10. LIBERMAN L. GIESS CS. DERSHAW DD, DEUTCH BM, PETREK JA. Imaging of pregnancy-associated breast cancer. Radiology 1994: 191: 245-8. [ Links ]
11. KELEHER AJ, THERIAULT RL, GWYN KM, HUNT KK, STELLING CB, SINGLETARY SE. AMES FC. BUCHHOLZ TA, SAHIN AA, KUERER HM. Multidisciplinary management of breast cancer concurrent with pregnancy. J Am Coll Surg 2002: 194: 54-64. [ Links ]
12. PSYRRI A, BURTNESS B. Pregnancy-associated breast cancer. Cancer J 2005; 11: 83-95. [ Links ]
13. KIRBY BLAND . EDWARD M. Copeland. III. Segunda Edición 2000 [ Links ]
14. KIRBY BLAND , EDWARD M. Copeland, III. Tercera Edición 2005. [ Links ]
]]>