ESTANDARIZACIÓN DE LA PRUEBA DE ELISA PARA EL INMUNODIAGNÓSTICO DE HIDATIDOSIS HUMANA EMPLEANDO ANTÍGENOS DE PRODUCCIÓN LOCAL
* Amilcar A. Flores L., * Patricia Rodriguez H.
* Lab. de Inmunología - SEDILAB (Fac. Medicina - UMSS)
Se describe una prueba cualitativa. Enzyme Linked Immunosorbent Assay (ELISA) para el inmunodiagnóstico de hidatidosis. El ELISA fue estandarizado usando líquido hidatídico proveniente de quistes desarrollados naturalmente en hígado de oveja. El ELISA -HID fue usado como test de screening para detectar anticuerpos específicos anti IgC en muestras de sueros de 17 pacientes confirmados por cirugía; fueron empleadas como sueros controles positivos, 26 muestras de sueros de personas sanas y 9 sueros de pacientes con otras infecciones por cestodos u otras infecciones. Los resultados del test de ELISA- HID mostraron que el test tiene una sensibilidad y especificidad del 100 % y 96 % respectivamente. Nosotros observamos una relativa frecuencia de reacciones cruzadas con otras enfermedades parasitarias (cisticercosis). Estas reacciones cruzadas con otros cestodos pueden ser resueltos testando estos con pruebas más específicas complementarias como el Inmunobloting. No se encontró reacciones cruzadas con muestras de sueros de pacientes con Hymenolepis nana, T. cruzi y T. gondii. La excelente sensibilidad y especificidad del ELISA- HID hace que el test sea una importante herramienta de diagnóstico para detectar anticuerpos específicos contra la equinococosis, cuyos resultados positivos pueden ser valorados por test confirmatorios como el Inmunobloting.
Palabras claves: E. Granulosus, Hidatidosis, Quiste Hidatídico, Reacción Cruzada, ELISA, Antígeno (Ag).
ABSTRACT
A quatitative enzime-linked immunosorbent assay (ELISA) for the immunodiagnosis of hidatidosis is described. The ELISA was standardized using Echinococcus granulosus cyst fluid antigen -ELISA obtained from Sheep Liver. (ELISA-HID) were used to screen for cyst hidatic-specific IgC antibidies in serum samples from 17 patients with surgycally confirmed hydatic disease, 26 serum samples of patients healthy and 9 samples of serum from patients whit other cestode infections or with an another illess were used as controls. The sensitivity and specificity the ELISA -HID was 100% and 96% respectively. We observed relatively frequent cross-reactions with other parasitic diseases (cysticecosis). Cestode- related cross-reactivity can be resolved by the complementary use of Taenia solium cysticercosis-specitic immunoblotting. No cross reacction were noted in patients infected with Hymenolepis nana, T. cruzy and T. gondii. The excellent sensitivity and specificity of the ELISA-HID make the assay a potentially usefull tool in screening for antibodies agains Equinococosis.
Key words: Echinococcus granulosus, hidatidosis, cyst hidatidic, cross reaction, ELISA, antigen (Ag)
INTRODUCCION
La Equinococosis o enfermedad hidatídica, posiblemente sea una de las enfermedades parasitarias más difíciles de entender debido a las peculiares formas larvales quísticas que se desarrollan,13 la hidatidosis humana es una enfermedad producida por el estadio larval de Echinococcus granulosus, la cual se produce cuando el hombre se convierte en huesped intermediario accidental de dicho céstodo, al consumir alimentos contaminados con huevos presentes en las materias fecales de los huéspedes definitivos.5,11, 14,20
]]> La localización más frecuente de estos quistes se halla en hígado, pulmones y en ocasiones puede ubicarse en cualquier otro organo1.La Hidatidosis es una zoonosis que afecta principalmente a las zonas agrícolas y ganaderas en America Latina.
Los países que registran los más altos índices de infección son Argentina, Chile, Uruguay, Brasil, Peru, y en menor escala, Colombia, Bolivia y Paraguay.18,19
En Bolivia no se cuenta con datos sobre la distribución de esta parasitosis, solo algunos reportes de rutina a nivel de mataderos, que son considerados incompletos, puesto que no incluyen casos de infestaciones humana, 15 aunque en nuestra casuística se encontró casos de hidatidosis humana.
El diagnóstico temprano y subsecuente tratamiento puede reducir la mortalidad, ya que la sintomatología varia de acuerdo a la tasa de desarrollo del parasito1,14.
En la gran mayoría de los casos el diagnóstico está establecido sobre las características clínicas de las lesiones, sintomatología y criterio epidemiológico.
El diagnóstico frecuentemente es confirmado por técnicas de imagen y métodos serológicos.16
Sin embargo la sintomatología clínica no aparece hasta que la estructura del parásito obtiene un cierto tamaño que normalmente requiere varios años después de la primera infección9
Ciertos casos controversiales en el diagnóstico de quistes hidatídicos se basa en el examen microscópico del líquido hidatídico, demostrando la presencia de protoescólices, ganchos o fragmentos de la membrana laminar.8,9,19
El diagnóstico serológico esta basado en la detección de anticuerpos,3 dicho diagnóstico se realiza por númerosas técnicas como la Hemaglutinación Indirecta (HAI), Enzime linked immuno sorbent assay (ELISA), Inmuno-fluorescencia (IFI), Inmunoelectroforesis e Inmunoprecipitación. 5,12,18,19
]]> Estas pruebas serológicas son una alternativa diagnóstica, ya que permiten un diagnóstico precoz de esta parasitósis. Sin embargo pese a la alta sensibilidad, de estas técnicas serológicas, tienen la desventaja de ser bastante inespecíficas por el número elevado de reacciones cruzadas que se presentan con otras infecciones parasitarias,22 tal el caso de que una reacción serólogica para hidatidosis, tiene reacciones cruzadas con cisticercosis y/o con T. saginata, lo que hace que ninguna de estas técnicas individualmente sea satisfactoria, por lo que se recomienda usar combinaciones de dos o más test.4El proposito del presente trabajo fue el estandarizar el test de ELISA empleando como antígeno, líquido hidatídico obtenido de quistes desarrollados naturalmente en vísceras de ganado ovino, ya que es imprescindible la necesidad de realizar pruebas inmunológicas confiables que puedan dar resultados inmediatos, que sean accesibles y tengan una buena aceptación por realizarse en periodos cortos de tiempo.
MATERIALES Y METODOS
Preparación del Antígeno
Un único lote de antígeno para el ELISA (Enzime Linked Immuno Sorbent Assay) fue preparado a partir líquido hidatídico obtenido de ganado ovino, infectado naturalmente. Solo fueron seleccionados los quistes Hidatídicos fértiles para el presente estudio, obtenidos del matadero del municipio de Quillacollo en el departamento de Cochabamba. La preparación del antígeno para hidatidosis se realizó siguiendo el protocolo descrito por Caron, A. (2001). El líquido hidatídico fue aspirado y transferido a tubos falcon de 50 ml y posterior centrifugado a 20.000 g. a 4 °C por 1 hora, el sobrenadante se dializó frente a agua destilada a una relación de 1:100 por 24 horas a 4 °C (con intervalos de cambio de agua destilada cada 8 horas) con agitación usando membranas de diálisis. Después de la diálisis, el líquido fue filtrado con filtros de porosidad de 0.45 y 0.22 µm (Millex filters, Millipore Corporation, Betford, MA, USA). El filtrado de líquido hidatídico fue dividido en alícuotas y almacenado en freezer de -80°C antes y después de su liofilización. La concentración de proteínas del antígeno se determinó mediante el método de Bradford modificado descrito por Spector T. (1 978), el cual empleó la albúmina Bovina Sérica (BSA) como proteína Standard. La cuantificación de proteínas antigénicas se realizó en el paquete estadístico Slide Write ver. 5.0 el cual tomo como curva estandar los valores de absorbancia del BSA expresados en Densidades opticas (DOs) y leída en un espectrofotómetro a 630 nm.
Sueros controles
Muestras de sueros fueron colectados de la seroteca del Laboratorio de Inmunología perteneciente a los laboratorios de SEDILAB y del Laboratorio de Parasitología de la Universidad Libre de Bruselas -Belgica: 1 7 muestras de sueros de pacientes positivos para Hidatidosis confirmados por la presencia del quiste en tejidos y serología, fueron empleados como sueros controles positivos. 26 sueros de pacientes sanos, 6 muestras de sueros de pacientes con cisticercosis confirmados por serología y clínica y 3 sueros de pacientes con otras patologías (Chagas, Toxoplasmosis y Hymenolepis nana) fueron empleados como sueros controles.
ELISA
La concentración óptima de los reactivos incluidos, la concentración del antígeno y la dilución óptima de sueros controles, fueron determinados por curvas de titulación (curvas dosis respuesta). Policubetas Inmunolon de Poliestireno (Maxi Sorb) fueron cubiertas con parafill en cada etapa del desarrollo la técnica de ELISA. Entre cada etapa de la reacción , las placas fueron lavadas 5 veces con intervalos de 1 minuto con PBS conteniendo 0,05% de Tween 20(PBS-T). Microplacas fueron incubadas toda la noche a 4°C con 50 µl de antígeno (diluidos en buffer Carbonato pH. 9.6 a una concentración de 8 µg/ml de proteínas solubles). Luego de la Saturación con 100 µl PBS - BSA al 1 % por dos horas a 37 °C, muestras de sueros diluidos 1:400 en PBS Tween 0.05%, BSA 03% (50µl) fueron incubados por 2 horas, sueros controles positivos, negativos y blanco de la reacción , fueron incluidos en cada ensayo de la placa. El conjugado (Ac anti - IgG, M, A (H + L ) humana marcada a la peroxidasa Bio-Rad Laboratorios fue diluido 1/1000 en PBS-Tween 0.05%, BSA 0.3 % e incubado por 1 hora a 37 °C.
El ensayo fue revelado adicionando 100 µl de enzima substrato consistiendo de ABTS (2.2 - Azino-di-(3 äthyl-benzthiazolinsulfonat (6)) (solución A) y peroxido de hidrogeno (solución B) vol. 1:1 por 15 minutos a temperatura ambiente y oscuridad. Las placas inmediatamente fueron leídas a 405 nm en un espectrofotómetro. El Cut - Off fue establecido usando la media de tres muestras no reactivas más tres desvíos estandar (Ads). La interpretación de los resultados se realizó en función al valor del Cut - Off donde muestras de sueros con valores inferiores al Cut - Off se consideraron como negativas y por el contrario muestras de sueros con valores superiores se consideraron Positivas. La evaluación de la sensibilidad y especificidad de la técnica de ELISA para ambas parasitosis se realizó empleando la tabla de cuatro casillas descrita por Gonzales, G. (1986).
RESULTADOS
Dosificación de Proteínas Antígenicas
El cálculo de la dosificación de proteínas antigénicas a partir de líquido hidatídico total, se realizó con el paquete estadístico Slide Write ver. 5.0, el cual tomó como curva estandar los valores de absorbancia del BSA expresados en Densidades opticas (DO), la cual linealizó aplicando la curva de regresión sigmoidal con un coeficiente de correlación de 0.937. Se determinó que la concentración de proteínas antigénicas solubles de líquido hidatídico proveniente de ganado ovino (oveja) fue de 16,213 mg/ml. La confirmación de los quistes hidatídicos se realizó por medio de la observación directa al microscopio del sedimento del líquido hidatídico donde se pudo observar los elementos característicos de esta especie de parásito (ganchos y protoescolices).
Estandarización de la técnica de ELISA -HID
La concentración del antígeno soluble y la dilución óptima de los sueros controles se realizó mediante curvas dosis respuesta.
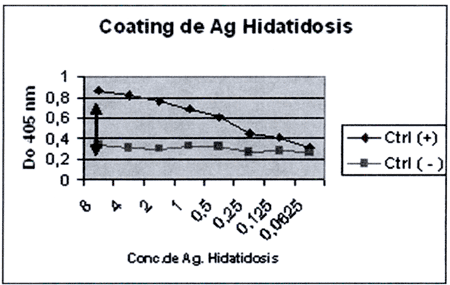
La gráfica 1 muestra el comportamiento de las diferentes concentraciones del antígeno (8µg/ml-0,0625 µg/ml) frente a una dilución de1/200 de los sueros controles positivos y negativos, donde podemos observar que la mejor concentración de antígeno fue de 8µg/ml.
Gráfica 1

Gráfica 2
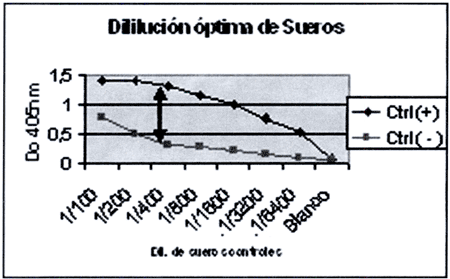
Evaluación de la técnica de ELISA - HID
La evaluación de la Técnica de ELISA estandarizada en nuestros laboratorios se realizó empleando 17 sueros controles positivos y 26 sueros controles negativos.
La gráfica 3 muestra el comportamiento de los sueros controles.
Gráfica 3
]]>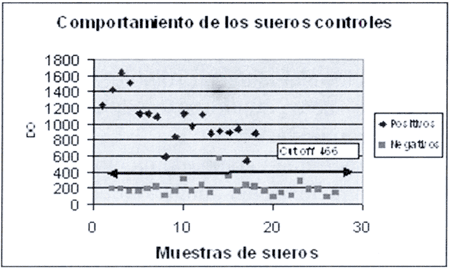
El calculo del Cut Off se determinó con la media de 3 controles negativos más 3 desviaciones estandar.
Determinación de la Sensibilidad y Especificidad del ELISA -HID
Se empleo la Tabla de Cuatro casillas para determinar la sensibilidad y especificidad del ELISA-HID, paralelamente a estas determinaciones se determinó: La precisión, valor predictivo positivo y valor predictivo negativo de la técnica.
Tabla 1
Tabla de cuatro casillas
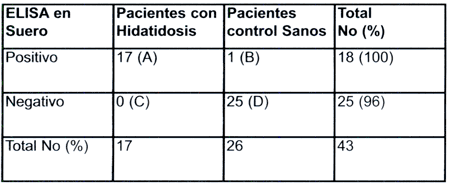
| La evaluación de la técnica de ELISA empleando extractos totales de líquido hidatídico mostró una sensibilidad del 100% (A /A +C); especificidad del 96 % (D/B +D); precisión del 97 % (A +D)/ (A + B+ C + D); valor predictivo positivo del 94 % (A / A + B) y un valor predictivo negativo del 100% (D/C + D). |
Estudio de las reacciones cruzadas
La tabla 2 muestra la evaluación del test de ELISA -HID frente a un panel de 9 sueros (6 de pacientes con Cisticercosis, 1 de paciente con Chagas, 1 paciente con Toxoplasmosis y 1 paciente con Hymenolepis nana), empleando como antígeno líquido hidatídico. Dos de 6 muestras de sueros de pacientes con cisticercosis, dieron riesgo de reacciones cruzadas. No se encontro resultados falsos positivos con ninguna otra muestra de sueros testados por el test de ELISA - HID.
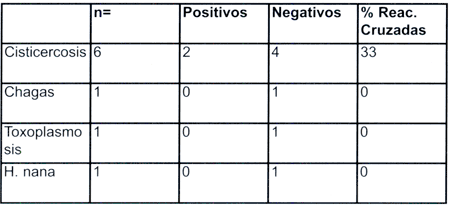
Tabla 2: Reacciones cruzadas
DISCUSION
La Hidatidosis humana está catalogada entre una de las más peligrosas enfermedades producidas por cestodos por lo cual su investigación es importante. Se realizó un gran esfuerzo para la identificación del parásito, como la purificación del antígeno para la aplicación en el ELISA. Sin embargo pese a estos factores es difícil obtener suficiente cantidad de este antígeno para su uso extensivo, este mismo hecho lo menciona Liance M. (2000). El inmunodiagnóstico es una importante herramienta en el diagnóstico de la infección de quistes hidatídicos,ya que juega un papel importante en la confirmación del diagnóstico clínico y en estudios epidemiológicos.3 En adición a las técnicas de imagen, un confiable serodiagnóstico, mejora el diagnóstico clínico del paciente en cuestión. Las técnicas serológicas convencionales estan basadas primeramente sobre test de screennig tal como un ELISA y una subsecuente confirmación por test como el Arco - 5 o el Immunobloting para el 8 Kd antfgen.3,14,17 El presente estudio se realizó para determinar el valor diagnóstico de la técnica de ELISA-HID estandarizada en nuestro laboratorio, empleando antígenos propios, para este objetivo sueros controles negativos y sueros controles positivos confirmados por test serológicos (ARCO-5 y ELISA) y la presencia del quiste en los tejidos, fueron testados por el ELISA-HID. Nuestras estrategia de evaluación incluía determinar la sensibilidad, especificidad, Valor predictivo positivo y negativo, así como la precisión del ELISA-HID. Nosotros mostramos que la sensibilidad y especificidad de la técnica de ELISA fue del 100% y 96% respectivamente, lo que demuestra su buena sensibilidad y especificidad. Otros autores obtuvieron similares resultados como Poretti et. al. (1999) quien obtuvo una sensibilidad del 91 % y especificidad del 82 % del ELISA o Verastegui, M. et. al. (1992) que hallo una sensibilidad y especificidad del 80 %, empleando líquido hidatídico como antígeno. Estas variaciones de sensibilidad y especificidad estan relacionadas con la calidad, naturaleza, (preparación y purificación del extracto antigenico), inmovilización del antígeno, como también de la metodología seleccionada para la actividad enzimatica, conjugado, substrata, dilución empleada en los sueros o el criterio empleado para el calculo del Cut - Off.9,17 El empleo de extractos totales como antígeno incrementa la sensibilidad de las pruebas de ELISA, sin embargo la gran desventaja es que provee un elevado porcentaje de reacciones cruzadas especialmente con cisticercosis y otras infecciones helmínticas.14 Es evidente que el empleo de antígenos purificados mejora la especificidad del ensayo pero conduce a una baja sensibilidad 14, pese a esto, varios autores mencionan que trabajar con antígenos purificados provee un confiable serodiagnóstico diferencial entre hidatidosis, cisticercosis y teniasis.2 Sin embargo la sensibilidad y especificidad no solo dependen de la estandarización de las técnicas, también depende de la respuesta inmune del hospedero, localización , número y estado evolutivo del parásito .4 Con respecto a este hecho Verastegui (1992) menciona que los pacientes con quistes hidatídicos hepaticos son los que mejor respuesta inmunologica presentan en comparación con pacientes con quistes pulmonares o en otras localizaciones. Las reacciones cruzadas halladas con cisticercosis empleando el ELISA-HID fue de 33%, este porcentaje hallado era de esperarse ya que varios estudios muestran que una mayoría de los test serológicos exhiben algo de reacciones cruzadas con sueros de pacientes con otras helmintiasis particularmente con cisticercosis causada por Taenia solium o hidatidosis causada por E. multilocularis, más aun si se emplea extractos totales de líquido hidatídico como antígeno 12, 14, 16, 17 Con respecto a este hecho Poretti D. encontro un 58% de reacciones cruzadas con sueros de pacientes con cisticercosis empleando su EgHF-ELISA Sin embargo estas dos infecciones son clínicamente muy diferentes, en aquellos pacientes que presentan desordenes neurológicos, tumores o lesiones en el cerebro quienes presentan una serología positiva para hidatidosis, el problema puede estar descartado testando el suero del paciente con un test para cisticercosis.14 En este estudio no se pudo determinar el porcentaje de reacciones cruzadas con otras helmintiasis ya que no se encontro resultados falsos positivos con ninguna de las muestras de sueros testados, sin embargo segun los reportes citados en este trabajo, existe reacciones cruzadas con H. nana, strongyloidiasis, toxocariasis, onchocercosis, y angiotrongyloidiasis o infecciones causados por nematodos. 16 Con respecto a este hecho, podemos indicar que nuestro número de muestras testadas para estas infecciones es muy bajo lo que no nos permite realizar una comparación más real con otros reportes. Con referencia a este hecho Coltorti et. al. (1990) mencionan que macromoleculas de diversos pesos moleculares portadoras de háptenos fosforilcolina (FC) han sido detectadas tanto en extractos como en productos de excreción de origen parasitario. Este hápteno esta ampliamente distribuido en la naturaleza y se lo considera como una de las causas de las reacciones cruzadas que se observa en el inmunodiagnóstico de enfermedades parasitarias.
Shepheerd y Mcmanus identiticaron el hápteno FC asociado a macromoleculas del líquido hidatídico y sugirieron su presencia en el Arco 5. El líquido hidatídico empleado contiene componentes séricos de la especie de la cual se obtuvieron los quistes y se ha sugerido que estos componentes podrían ser causa de las reacciones cruzadas.
]]> CONCLUSION
Este estudio revelo el considerable potencial del ELISA -HID para el diagnóstico de la Hidatidosis, sin embargo no podemos comparar su sensibilidad y especificidad con los del Inmunoblot, pero el ELISA es más barato y fácil de desarrollar cuando varios sueros necesitan ser testados, por lo cual el ELISA- HID estandarizado en laboratorio puede ser empleado como test serológico de screening, donde todos los casos positivos por el ELISA deberían entonces necesitar ser confirmados por el DD5 y EITB test. Con referencia a las reacciones cruzadas que presenta con muestras con cisticercosis, se puede superar testando un suero con un ELISA-HID positivo con un segundo test confirmatorio, para esto nosotros recomendamos usar el Inmunobloting o la técnica del ARCO-5, ya que al combinar el ELISA con los test confirmatorios respectivos se asegura el hecho de discriminar entre hidatidosis y cisticercosis y descartar las reacciones falso positivas que ocurren con otras helmintiasis.
BIBLIOGRAFIA
1. Acha P.N., Szyfres B. Zoonosis y Enfermedades Transmisibles al Hombre y los Animales. Publicación Científica No 503. Washington DC. 2da. Edición 1986 PP 734-751. [ Links ]
2. Akira I. Basic and Applied Immunology in Cestodes Infection: From Hymenolepis to Taenia and Echinococcus. International Journal for Parasitology. 1997; 27(10). pp. 1203-1211
3. Akira I., Liang MA., Schantz P.M., Liu YH., et al. Diferential Serodiagnostic tor Cystic and Alveolar Echinococcosis Using Fraction of Echinococcus granulosus Cyst Fluid (Antigen B) and E. Multilocularis Protoscolex (EM 18). The American Society of Tropical Medicine and Hygiene. 1999: 60(2). pp. 188-192.
4. Amelung G. Hidatidosis y Enfermedad Hidatidica. Monograias.com
5. Botero D., Restrepo M. Parasitosis Humana. 3ra. Edición . Ed.Corporación para Investigaciones Biologicas. Medellin Colombia 1998. pp. 342 - 367. [ Links ]
6. Caron, A. Servicio de Production d Antigenes Parasitaires. Institut Pasteur. Lille- Francia, 2001. [ Links ]
7. Coltorti E. A., E. Fernandez.. E.R. Marget., J. D. Scozzina., E.A.Cuarnera. Detección de portadores Asintomaticos de Quistes Hidatídicos: Aumento de la especificidad del ensayo Inmunoenzimatico. Rev. Inst. Med. Trop. Sau Paulo. Julho-Agosto 1990; 32 (4) pp. 275-284.
8. Clavel A., Varea M., Doiz O., Lopez L., Quilez J., Castillo F.J., Rubio C, Gomez L. Visualization of Elements: Comparason of several Technicques. Journal of Clinical Microbiology. 1999; pp. 1561-1563. .
9. Gonzales, G., Lorenzo C, Nieto A., Improved Immunodiagnostic of Cystic Hidatid Disease by Using a Sinthetic Pectide with Higher Diagnostic Value than that of its Parent Protein, Echinococcus granulosus Antigen B. Journal of Clinical Microbiology. Nov. 2000, P.1561-1563.
10. Gonzales C. Epidemiologia. Ed. Addison-Wesley Iberoamericana S A. Wilmington, Deloware. E.U.A. 1486. pp. 175-181. [ Links ]
11. Joklin, Willelt, Amos, Wilfert, Zinsser. Microbiologia. 20a edition. Ed. Panamericana. Buenos Aires Argentina. 1996. pp 1604-1605 [ Links ]
12. Kharebov A., Nahmias J., EL-ON J., Cellular and Humoral Immune Response of Hidatidosis Patients to Echinococcus Granulosus Purified Antigens. Am. J. Trop. Med. Hyg. 1997; 57(5). pp. 619-625.
13. Koneman. Allen. Dowell. Janda. Sommers. Winn. Diagnostico Microbiológico. 3ra. edición . Editorial Panamericana. Mexico DF. 1997. pp 753-759. [ Links ]
14. Lianc M., Janin V., Bresson - Hadni S., et. al. Immunodiagnosis of Equinococcus Infection: Confirmatory Testing and Species Differentiation by a New Commercial Western Blot. Journal Of Clinical Microbiology. Oct. 2000, p. 3718-3721.
15. Ministerio de prevision Social y salud Pública 1994. [ Links ]
16.Planchart, S., Botto C, Alarcon De Noya B., Bonifacino R., Vivas L., Spencer L., Vivas S. Evaluation of the double difusion, Enzime Immunoassay and Immunoblotting Techniques, for the Diagnosis of Human Hydatid disease in Tropical Areas. Rev. Inst. Trop. Sau Paulo. Maio-Junho 1994; 36(3). pp. 295-210.
]]> 17. Poretti D., D., Felleisen E., Grimm F., et. al. Diferential Immuni-diagnosis Between Cystic Hydatid Disease and Other Cross - Reactive Pathologies. Am. J.Trop. Med. Hyg. 1999;60(2), pp 193- 198.18. Sapunar G. Hidatidosis. Atias A. Parasitologia médica 3ra edición . Ed. Mediterraneo. Santiago de Chile. 1991. pp 338-353. [ Links ]
19. Sapunar G. Hidatidosis. Atias A. Parasitologia Clinica. 1ra edición. Ed. Mediterraneo. Santiago de Chile. 1996. pp 341-354. [ Links ]
20. Schants P.M. Equinococosis Hidatidosis (Enfermedad hidatidica). Goldsmith R., Heyneman R. Parasitologia y Medicina Tropical Ed. Manual Moderno. Mexico DF. 1995. pp 647-657 [ Links ]
21. Spector T. Reginement of the coomassie blue method of protein quantitation. A simple and linear spectrophotometric assay for less than or equal to 0,5 to 50 microgram of protien. Anal Biochem. 1978. May;86(1): pp. 142-146.
22. Verastegui. M., Moro P., Guevara A., Rodriguez T., Miranda E.,H. Gilman R. Enzime- Linked Immunoelectrotransfer Blot Test for Diagnosis of Human Hydatid Disease. Journal of Clinical Microbiology. 1997. pp.1557-1561.
]]>