Determination of the temperature, pH and concetration parameters
for α-Amilasa Mg a new enzyne
Determinación de los parametros temperatura, pH y concentración
para la nueva enzima α-Amilasa Mg
Jorge F. Yañiquez Vedia1,*, Susana Huanca Lopez1, Leslie K. Tejeda1, Enzo Aliaga Rossel2 ]]>
J. Mauricio Peñarrieta Loria1, Patricia A. Mollinedo Portugal1
1Food Chemistry Laboratory, Chemical Research Institute IIQ, Chemical Sciences Department, School of Pure and Natural Sciences FCPN, Universidad Mayor
de San Andres UMSA, P.O. Box 303, Calle Andrés Bello s/n, Ciudad Universitaria Cota Cota,
phone +59122792238, La Paz, Bolivia, jmpenarrieta10@umsa.bo, www.umsa.bo
* Corresponding author: jfyaniquez@gmail.com
2SWEBOL AB Biotech SRL. Avenida del Escultor 22 Cota Cota, Teléfono +59172078977, La Paz, Bolivia. Scheelevägen 22 22363
Lund, Sweden, www.swebol.com, enzo@swebol.com
Received: 04/19/2019 Accepted: 04/25/2019 Published: 04/30/2019
Physicochemical parameters as pH, concentration and temperature for alpha amylases reactions in different applications determine the efficiency of the enzymatic reaction. Present study shows the relationship between the physicochemical parameters and it is demonstrated that pH is a determining parameter for the maximum efficiency of the enzyme. The optimal values of these parameters are also determined for the enzymatic reaction at pH 5 and T = 50 ° C for a concentration of 5.6 U / mL of the enzyme, α-amylase Mg, modified according to the patent 002-2017.
Keywords. Co-factor, Magnesium, Characterization, α- Amilase.
Resumen
Los parámetros fisicoquímicos de pH, concentración y temperatura de las reacciones de las α-amilasas en sus diferentes aplicaciones, determinan la eficiencia de la reacción enzimática. El presente estudio muestra la relación entre los parámetros fisicoquímicos demostrándose que el pH es el parámetro determinante para la eficiencia máxima de la enzima. También se determinan los valores óptimos de estos parámetros para la reacción enzimática a pH 5 y T=50°C para una concentración de 5,6 U/mL de la enzima, α-amilasa-Mg, modificada de acuerdo a la patente 002-2017.
Palabras clave. Cofactor, Magnesio, caracterización, α - Amilasa.
INTRODUCCIÓN
Las α-amilasas son enzimas muy importantes por sus diferentes aplicaciones en la industria, tal como panadería, textiles, reducción de algodón entre otros. Uno de los usos más importantes de las α-amilasas es la producción de jarabe de glucosa a partir de almidón, el principal problema en este proceso, es modificar el pH=4,5 del sustrato (almidón crudo) a un valor de aproximadamente de pH=6, requerido para el uso de las α-amilasas[1]. Debido a este problema, existen muchos estudios enfocados a modificar de diferentes maneras la estructura de la enzima, para hacer más eficiente y viable la reacción. Así mismo, todos los reportes muestran la importancia y especificidad de las condiciones de pH y temperatura para una actividad máxima de estas enzimas. [2-3]
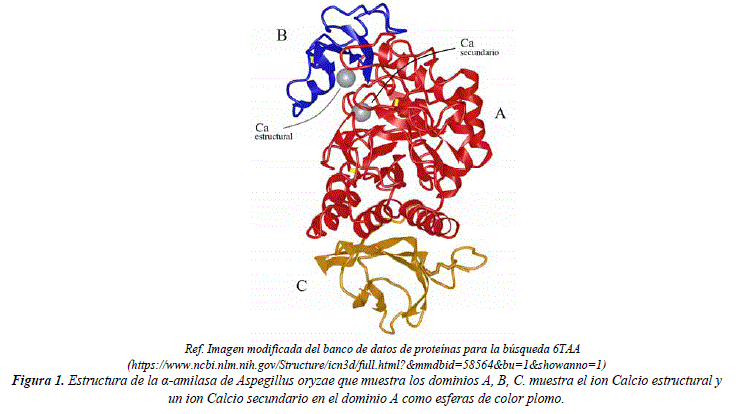
]]> La complejidad de las condiciones de reacción ha llevado a un estudio profundo de la estructura de las α-amilasas, mostrando evidentemente que su actividad es afectada por las variaciones más simples en la estructura, como el cambio de algún aminoácido en la secuencia general o de igual forma el cambio de los cofactores que son tan importantes como los cambios en la parte proteica. [4-6]La α-amilasa de Aspergillus oryzae ha sido descrita estructuralmente en diversos trabajos, esta presenta una estructura tridimensional de 3 dominios (A, B y C) y un ion Calcio estructural ubicado entre los dominios A y B, del cual sus ligandos están compartidos en ambos dominios y permite mantener la estructura estable del sitio activo.[7] Por otra parte, también existen sitios secundarios de enlace en los cuales existen iones Calcio que ayudan mantener la integridad estructural del sitio activo ante la desnaturalización por interacciones con el dominio B. [8]

El cambio de iones intercambiables en la estructura o cofactores, puede tener una gran importancia en la estabilidad enzimática como muestra el estudio de Prakash y Jaiswal [9] con diferentes iones como Calcio, Sodio y Cloro en los sitios activos de la α-amilasa. Los cambios en los sitios activos de estas enzimas, muestran también que algunas de estas modificaciones pueden ocasionar además la inactivación total de estas enzimas. [5-11].
Una de las caracterísiticas principales de las α-amilasas, esta dada por el Calcio estructural que tiene un gran impacto en la termoestabilidad de la enzima debido la formación de una estructura compacta [9], y su extracción causa la pérdida irreversible de actividad por desnaturalización debido a la inestabilidad estructural generada. [12]
Pocos trabajos científicos analizan el efecto de los cofactores en el rendimiento de estas reacciones aunque se enfatiza la importancia de los cofactores para determinar su especificidad y estabilidad molecular en condiciones óptimas. Yañiquez [13], en este estudio la sustitución de los iones Calcio por Magnesio en la α-amilasa de Aspergillus oryzae se determinó que la extracción indirecta de los iones Calcio periféricos o secundarios por con iones Magnesio afecta el rendimiento y la estructura de la enzima.
Una vez consolidada la estructura es importante establecer las nuevas condiciones para una máxima eficiencia de la reacción, los parametros fisicoquímicos establecidos son el pH, temperatura y concentración de la enzima son los que gobiernan el proceso. [14-16]
La enzima a evaluar en el presente estudio es una α-amilasa proveniente del Aspergillus oryzae, a la cual se le sustituyó el cofactor Calcio por Magnesio usando el método descrito en la patente de invención SP 002-2017 y se enfoca principalmente en determinar los parámetros de pH, temperatura y concentración de actividad máxima de la nueva enzima.
EXPERIMENTAL
]]> Reactivosα-amilasa-Mg obtenida bajo el procedimiento protegido legalmente bajo la patente de invención SP-002-2017. Almidón soluble de papa Grado Síntesis de Scharlab (G Perez, España); ácido Clorhídrico para Análisis de Biopack (Buenos Aires, Argentina); Iodo sublimado para ACS de Merck (Darmstadt, Germany); Ioduro de Potasio de Winkler LTDA. (Santiago, Chile).
Preparación del sustrato
Para la evaluación de la actividad enzimática de los parámetros de Temperatura y Concentración se prepara el almidón soluble al 2% con agua de grado Millipor, a 65°C con agitación constante.
Para la evaluación de actividad enzimática y pH el almidón soluble se gelifica a 65°C antes de la reacción para variar el rango de pH entre 2 a 10, empleando HCl (1M) e NaOH (1M).
Método para determinar la actividad enzimática
Se determinó el grado de hidrólisis de forma indirecta a través del complejo almidón-Iodo residual por espectrofotometría usando el método descrito por Xiao y Tsang [17]. Una mezcla de 200µL de almidón al 2% y 200µL de enzima a diferentes concentraciones, pH y temperatura respectivamente, es incubada a una temperatura constante por 30 minutos con agitación constante a 1000RPM en un Thermomixer confort marca Eppendorf.
Una vez concluido el proceso enzimático se desactiva la enzima con 100µL de HCl 1M, y se agregan 500µL de Lugol de concentración 0,04%, luego de 15 minutos, se siembran 150µL del complejo almidón-iodo en una placa Nunc 96well y se lee la absorbancia a 620nm en un lector de placas marca µQuant BioTeK.
Determinación de la actividad enzimática a concentración constante
De acuerdo al método descrito para determinar la actividad enzimática, se determina la correlación entre los parámetros variables de temperatura entre 20 y 70°C y el pH de 2 a 10, a concentración de enzima constante de 5,6U/mL.
]]> Determinación de la actividad enzimática a temperatura constanteEvaluando la actividad enzimática por el método espectrofotométrico del complejo Iodo-Almidón se mantiene constante la temperatura de reacción a 50°C. Los parámetros variables para el experimento son la concentración en el intervalo de 0 a 5,6U/mL y el pH de 2 a 10.
Determinación de la actividad enzimática a pH constante
Basados en la metodología descrita para la determinación de la actividad enzimática por espectrofotometría. Se evalúa el comportamiento de la enzima a pH=5 como constante. Los parámetros variables para el experimento son el intervalo de la concentración enzimática de 0 a 5,6U/mL y la temperatura entre 20 y 70°C.
RESULTADOS Y DISCUSIONES
Los valores de actividad enzimática fueron cuantificados como absorbancia del complejo Iodo-almidón. Se determinaron por medio del método amiloclástico. [17] Este método muestra la degradación del almidón por el proceso de hidrólisis enzimática con la nueva enzima α-amilasa Mg. [11] Como se muestra en las Figuras 2-6 una mayor actividad enzimática está dada por un valor menor de absorbancia, que a su vez tiene una relación directamente proporcional a la concentración remanente de almidón sin hidrolizar.
Considerando como base las condiciones fisicoquímicas de máxima actividad reportadas por varios autores para la enzima original (α-amilasa de Aspergillus oryzae) los parámetros analizados son: concentración de enzima α-amilasa Mg, pH y temperatura para la reacción de hidrólisis enzimática de almidón soluble estándar. [14-16]
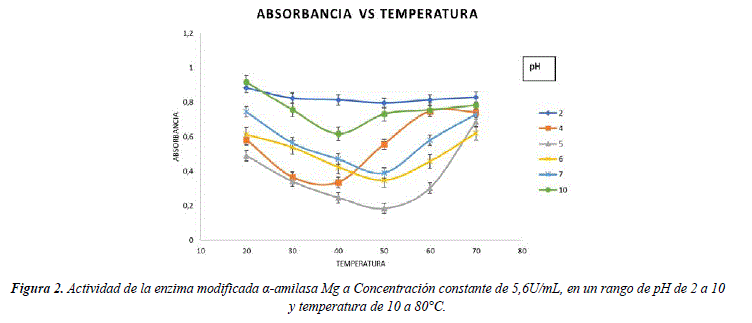
Los resultados de correlación entre los parámetros de temperatura y pH a una concentración constante se muestran en la Figura 2. La función matemática muestra principalmente que la mejor actividad enzimática está a temperaturas altas y pH ácidos, resultados que coinciden con los reportados por otros autores para este tipo de enzimas. [14]
Las condiciones de actividad máxima para la α-amilasa de Aspergillus oryzae están el intervalo de pH 4,5 a 5,5 y la máxima actividad en el intervalo 40 a 50°C. [15]
]]> Como resultado del análisis de las diferentes curvas para la enzima modificada, se observa en la Figura 2 que el pH de máxima actividad es 5 en el intervalo de temperatura de 20 a 60°C; donde el valle máximo de actividad se encuentra en 50°C y los valores encontrados para 40, 50 y 60°C a pH 5 son mayores al siguiente valle de actividad a pH=4.La actividad enzimática de la α-amilasa de Aspergillus oryzae a pH 5 no presenta una reducción mayor al 5% de actividad en el intervalo de temperatura de 40 - 50°C en comparación con el intervalo 50 - 60°C donde existe una pérdida del 30% de actividad, según los resultados descritos por Patel et al [15] y Kundu y Das [18].
Esta similitud en el comportamiento entre la α-amilasa Mg y la α-amilasa de Aspergillus oryzae se puede explicar por la presencia del ion Calcio estructural que mantiene la integridad del sitio activo de la enzima generando termoestabilidad en la enzima modificada como explica Prakash y Jaiswal[9]. Por tanto, en la α-amilasa Mg se mantiene la propiedad de termoestabilidad aunque se cambiaron los iones secundarios de Calcio por Magnesio.
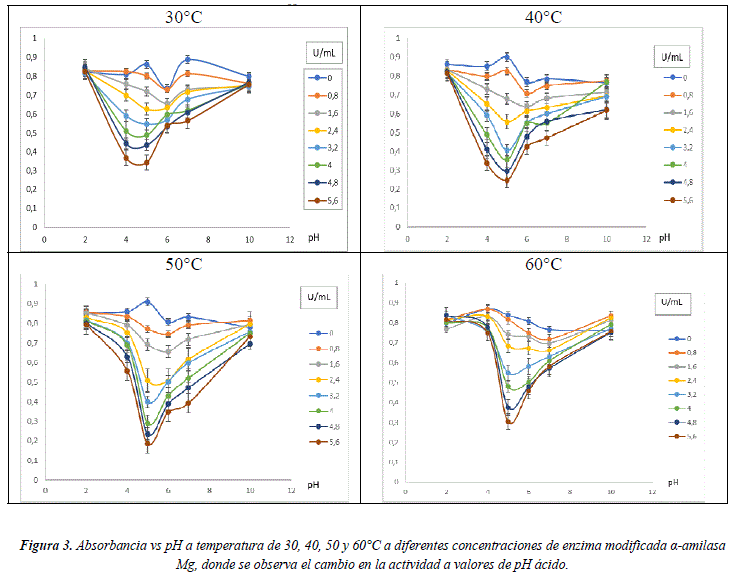
La relación entre la concentración de enzima α-amilasa Mg y los valores de pH a una temperatura constante fueron analizados en el rango de actividad entre 30 y 60°C, los valores de actividad enzimática máxima para cada temperatura fueron determinados en un rango de 0,8 a 5,6U/mL de concentración de enzima y pH entre 2 y 1. Los resultados se muestran en la Figura 3.
En el análisis de los datos se puede observar que la actividad enzimática tiene un mayor intervalo de absorbancia de 0,3 a 0,9 a valores de pH ácidos entre 2 y 6 a diferencia de los resultados en el intervalo de actividad entre 0,5 y 0,8 en el que se reducen a valores de pH basico entre 7 y 10 de este analisis se puede inferir que la relación entre estos dos parametros es inversamente proporcional dentro de los límites de detección del método empleado. Determinándose así que a pH ácido de 5 la temperatura óptima de reacción es de 50°C para una concentración de 5,6U/mL.
De acuerdo a los datos reportados por Patel et al[15] y Kundu - Das[18] para la α-amilasa de Aspergillus oryzae, el pH la actividad de la enzima es 5 a 50°C, que presenta una reducción del 4% de actividad cuando se reduce el pH a 4 y una reducción del 40% actividad a pH 3 para valores de pH ácidos, por el contrario en valores más básicos como pH 6 se observa una reducción del 20% de actividad, a pH 7 una reducción de 55% y a pH 10 no se presenta actividad enzimática.
Estos datos teóricos son diferentes a los obtenidos para la α-amilasa Mg estudiados en la Figura 3, porque a pH 4 esta enzima modificada presenta una reducción de actividad del 60% para 5,6U/mL. Y por el contrario en valores de pH básicos se tiene resultados parecidos, a pH 6 una reducción del 20%, en pH 10 la actividad es mínima, excepto el pH 7 que tiene una reducción de 30% de actividad enzimática.
La razón de este cambio en el comportamiento enzimático respecto al pH, puede ser explicada por la sustitución de los iones secundarios de Calcio por Magnesio que modifican el tamaño estructural de la enzima, menor tamaño iónico, así como por la diferente electroafinidad del Magnesio, además de los cambios en las interacciones Calcio estructural y Calcio secundario en los sitios activos como muestra Prakash y Jaiswal [9] en su estudio.
Comparando la información teórica con los resultados de la enzima α-amilasa Mg de la Figura 3, existe una similitud en los resultados obtenidos a temperatura 30°C, en este caso el efecto de separación dominios por la temperatura a la que reacciona la enzima puede ser la causa principal. [9]
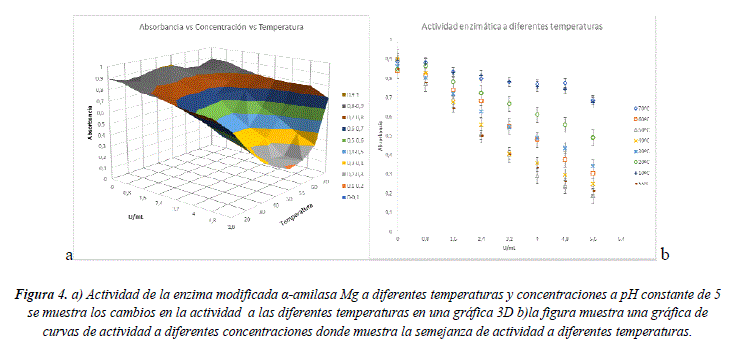
]]> Finalmente, la Figura 4 muestra la relación entre la temperatura y la concentración de la enzima α-amilasa Mg a pH = 5 constante siendo este el valor de pH óptimo determinado para la reacción de acuerdo a los resultados presentados en las Figura 2 y 3.Observando los datos de la Figura 4b, los resultados muestran que a temperatura de 70 y 10°C la hidrólisis enzimática es inactiva, a 10°C la enzima es muy estable y no reacciona sobre el sustrato a pesar de tener las condiciones de los otros parámetros, de igual forma a 70°C es todo lo contrario la enzima esta inactiva debido a que su estructura ha sido alterada y puede concluir que esta desnaturalizada por lo tanto no se produce la reacción y la absorbancia tiene un valor de 0,8 muy próximo al valor del blanco de la reacción de 0,9 de absorbancia.
Los valores de actividad enzimática en la Figura 4 muestran que en los intervalos de temperatura de 30 a 60°C y 40 a 55°C, tienen comportamientos funcionales similares y muestran que las interacciones a bajas temperaturas así como a temperaturas altas, dan resultados similares lo que muestra la estabilidad de la estructura de la enzima con el cofactor Mg. Sin embargo, la actividad enzimática de glucolisis en un intervalo entre 45 y 55 °C es la óptima determinándose que 50°C es el valor adecuado para que la reacción se lleve a cabo eficientemente con una absorbancia de 0,1 como se muestra en la Figura 4a.
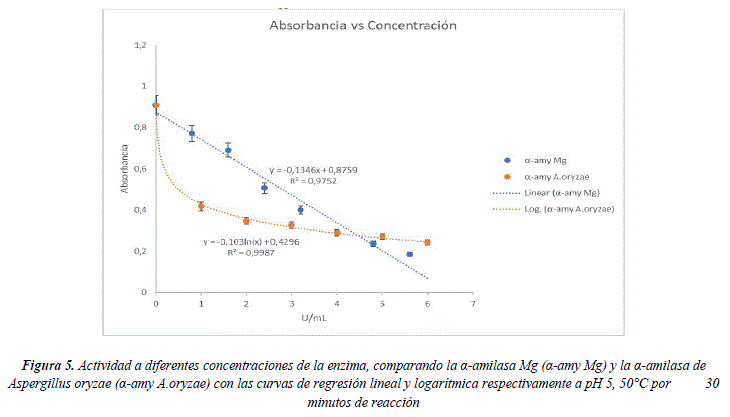
La actividad a diferentes concentraciones de la α-amilasa Mg y la enzima original en las condiciones de actividad máxima a 30 minutos de reacción se muestran en la Figura 5. De acuerdo a estos resultados, se determina que la enzima modificada tiene una correlación lineal entre actividad y concentración por el contrario la enzima original tiene una correlación logarítmica. Analizando, observamos que a altas concentraciones la α-amilasa-Mg tiene una mayor velocidad de reacción comparada a la enzima original, y se considera que la enzima es más rápida a concentraciones mayores a 4U/mL de ambas enzimas. La razón de este cambio es que la α-amilasa de Aspegillus oryzae tiene un paso limitante en su mecanismo de reacción que hace que el incremento en la concentración de la enzima no aumente la actividad enzimática: esta velocidad está definida por la estructura, tamaño y mecanismo de reacción del sitio activo en la enzima. [1]
La modificación en la estructura y tamaño de la enzima como consecuencia de la sustitución del Calcio secundario por Magnesio, afecta efectivamente al mecanismo de reacción y no presenta paso limitante respecto de la concentración enzimática. Por esta razón la enzima α-amilasa Mg muestra un tiempo menor de reacción y mayor eficiencia a concentración 5,6 U/mL que la enzima original.
Adicionalmente se analizaron los intervalos de actividad máxima reportados como absorbancia con los parámetros óptimos y tomando en cuenta los intervalos de actividad enzimática en la Figura 4. Este análisis determina que el rango pH es el parámetro preponderante para la reacción, por otro lado la temperatura puede variar en un rango no muy amplio entre 30 - 40°C, los datos también muestran que a pH cercano a 4 la reacción se puede desarrollarse pero con un rendimiento menor como se puede ver en la Figura 6.
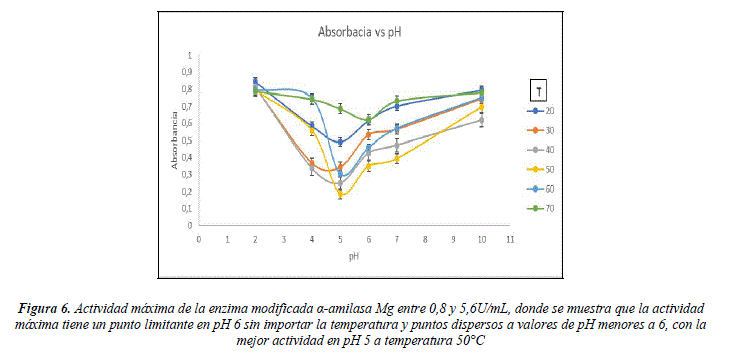
La Figura 6 también muestra que los valores de temperatura tienen un efecto positivo en la reacción cuando valores de pH estan fijos entre 4 y 5. También se puede ver que a pH 6 y 7 sin importar el valor de temperatura, ni la concentración se tiene una actividad enzimática reducida.
CONCLUSIONES
Analizando los resultados podemos concluir que la relación entre los parámetros de temperatura, pH y concentración para la nueva enzima α-amilasa-Mg depende de la estructura molecular y la forma de los sitios activos, como se reporta en estudios anteriores [1,9,10,11] mostrando que la nueva estructura es suficientemente estable y conserva los sitios activos para la hidrólisis de almidones.
A pesar de haberse modificado la estructura con el cambio de cofactor los parámetros fisicoquímicos de actividad máxima muestran un comportamiento normal y la relación entre ellos sigue lo reportado en bibliografía.
Se establece los nuevos rangos de parámetros fisicoquímicos para la reacción de hidrolisis de la α-amilasa Mg, de acuerdo a los resultados se muestra que a valores de pH ácidos y temperatura moderadas, la reacción es eficiente lo que hace más viable el uso de esta enzima en procesos industriales como la obtención de jarabe de glucosa.
Por otra parte, la sustitución de los cofactores secundarios Calcio por Magnesio, mantuvieron la termoestabilidad de la enzima pero modificaron el efecto del pH en su actividad máxima a valores de pH ácido, esto por el efecto de la electroafinidad y el tamaño de los iones Magnesio además de la no sustitución del ión Calcio estructural.
Igualmente se puede ver en las Figuras 2-6 que la temperatura de inicio de la reacción es menor comparada con las α-amilasas normales lo que hace más viable el uso de esta enzima α-amilasa Mg en sustratos termolábiles en medios muy ácidos.
El cambio de cofactor afecta al mecanismo de hidrolisis, mayor velocidad de reacción a concentraciones mayores a 4U/mL comparadas con la enzima original y una correlación lineal entre la actividad, concentración de enzima y sustrato.
]]> Por tanto, en procesos de hidrólisis de almidones la enzima α-amilasa Mg modificada de Aspergillius oryzae alcanza su mejor actividad a un pH de 5, temperatura de 50°C y una concentración de 5,6U/ mL sobre un sustrato de almidón preparado al 2% de concentración.
RECONOCIMIENTOS
Los autores agradecen a la Agencia Sueca de cooperación para el Desarrollo Internacional (SIDA) por el respaldo financiero. Al Dr. José Antonio Bravo por la donación de material de laboratorio.
REFERENCIAS
1. Van Der Maarel, M.J., Van der Veen, B., Uitdehaag, J.C., Leemhuis, H., & Dijkhuizen, L. 2002, Properties and applications of starch-converting enzymes of the α-amylase family, Journal of biotechnology, 94(2), 137-155.
2. Souza, P.M.D. 2010, Application of microbial α-amylase in industry-A review, Brazilian Journal of Microbiology, 41(4), 850-861.
3. Mojsov, K. 2012, Microbial alpha-amylases and their industrial applications: a review, International Journal of Management, IT and Engineering (IJMIE), 2(10), 583-609. [ Links ]
4. Gupta, R., Gigras, P., Mohapatra, H., Goswami, V.K., & Chauhan, B. 2003, Microbial α-amylases: a biotechnological perspective, Process biochemistry, 38(11), 1599-1616.
]]>5. Haki, G.D., & Rakshit, S.K. 2003, Developments in industrially important thermostable enzymes: a review, Bioresource technology, 89(1), 17-34. [ Links ]
6. Sundarram, A., Murthy, T.P.K. 2014, α-amylase production and applications: a review, Journal of Applied & Environmental Microbiology, 2(4), 166-175.
7. Brzozowski, A.M., Davies, G.J. 1997, Structure of the Aspergillus oryzae α-amylase complexed with the inhibitor acarbose at 2.0 Å resolution, Biochemistry, 36(36), 10837-10845.
8. Boel, E., Brady, L., Brzozowski, A.M., Derewenda, Z., Dodson, G.G., Jensen, V.J., Woldike, H.F. 1990, Calcium binding in alpha.-amylases: an x-ray diffraction study at 2.1-.ANG. resolution of two enzymes from Aspergillus, Biochemistry, 29(26), 62446249. [ Links ]
9. Prakash, O., Jaiswal, N. 2010, α-Amylase: an ideal representative of thermostable enzymes, Applied biochemistry and biotechnology, 160(8), 2401-2414.
10. Bolton, D.J., Kelly, C.T., Fogarty, W.M. 1997, Purification and characterization of the α-amylase of Bacillus flavothermus, Enzyme and Microbial Technology, 20(5), 340-343.
11. Zakowski, J.J., Bruns, D.E. 1985, Biochemistry of human alpha amylase isoenzymes, CRC Critical Reviews in Clinical Laboratory Sciences, 21(4), 283-322. [ Links ]
12. Oikawa, A., Maeda, A. 1957, The role of calcium in Taka-amylase A, The Journal of Biochemistry, 44(11), 745-752. [ Links ]
13. Yañiquez, J., 2016, Efecto del Mg como cofactor mayoritario en la enzima modificada α- amilasa Mg de Aspergillus oryzae, Tesis de grado Universidad Mayor de San Andrés, Bolivia.
14. Sahnoun, M., Bejar, S., Sayari, A., Triki, M.A., Kriaa, M., Kammoun, R. 2012, Production, purification and characterization of two α-amylase isoforms from a newly isolated Aspergillus oryzae strain S2, Process Biochemistry, 47(1), 18-25.
]]>15. Patel, A.K., Nampoothiri, K.M., Ramachandran, S., Szakacs, G., Pandey, A. 2005, Partial purification and characterization of-amylase produced by Aspergillus oryzae using spent-brewing grains, Indian Journal of Biotechnology, 4(1), 336-341. [ Links ]
16. Ramachandran, S., Patel, A.K., Nampoothiri, K.M., Chandran, S., Szakacs, G., Soccol, C.R., Pandey, A. 2004, Alpha amylase from a fungal culture grown on oil cakes and its properties, Brazilian archives of biology and technology, 47(2), 309-317. [ Links ]
17. Xiao, Z., Storms, R., Tsang, A. 2006, A quantitative starchiodine method for measuring alpha-amylase and glucoamylase activities, Analytical biochemistry, 351(1), 146-148. [ Links ]
18. Kundu, A.K., Das, S. 1970, Production of amylase in liquid culture by a strain of Aspergillus oryzae, Appl. Environ. Microbiol., 19(4), 598-603. [ Links ]
]]>