ARTÍCULOS ORIGINALES
Luteolin in peanuts’ shells (Arachis Hypogaea) in cultivars of Bolivia
Luteolina en cáscaras de maní (Arachis Hypogaea) en cultivares de Bolivia
Angela San Martín1, Gilberto Chui1, Aleida S. Romero2, Roberto Acebey2, Eloy Blanco3, Yonny Flores1, Giovanna R. Almanza1,*
*Corresponding author: giovyalmanza@gmail.com, galmanza3@umsa.bo
ABSTRACT
Peanut shells are a residue generated in big quantities in Bolivia. This residue contents luteolin, which is a flavonoid with demonstrated pharmacological properties as antioxidant, anti-inflammatory and antimutagenic. In this study, we analyzed the luteolin content in 41 samples of peanuts shells obtained from different cultivars mainly in the department of Chuquisaca, Bolivia. The luteolin content was quantified by an HPLC-DAD method using quercetin as internal standard. Results showed that content varies between 0.006 to 0.850 mg Lu/g of shells. Samples with the highest concentration of luteolin were: Larguillo Icla (roasted) (0,850 mg Lu/g of shells) sample obtained in the market of Sucre city, Phiti cintura colorado from Oroncota in Potosi with 0.673 mg Lu/g of shells and Pico y Loro obtained from Monteagudo in Chuquisaca with 0.589 mg Lu/g of shells. On the other hand, the EtOH extracts, which also showed interesting pharmacological properties, were also analyzed in their luteolin contents, determining concentrations of 79,728 and 74,188 mg Lu/g of extract in the cultivars Phiti cintura colorado from Oroncota in Potosí and Phiti cintura ladrillo from Padilla in Chuquisaca, respectively. Finally, it was determined that roasting temperature (80 ° C) does not affect luteolin.
Keywords: Luteolin, Arachis hypogaea, Peanuts shells, HPLC quantification, Chuquisaca, Bolivia.
Las cáscaras de maní son un residuo generado en grandes cantidades en Bolivia. Este residuo contiene luteolina, que es un flavonoide con demostradas propiedades farmacológicas como antioxidante, antiinflamatorio y antimutagénico. En este estudio, se analizó el contenido de luteolina en 41 muestras de cáscaras de maní obtenidos en diferentes cultivares principalmente del departamento de Chuquisaca, Bolivia. El contenido de luteolina se cuantificó por un método de HPLC-DAD utilizando como patrón interno quercetina. Los resultados mostraron que el contenido varía entre 0,006 y 0,850 mg Lu/g de cáscaras. Las muestras con mayor concentración de luteolina fueron: Larguillo Icla (tostado) (0,850 mg Lu/g de cáscaras) obtenida en el mercado de la ciudad de Sucre, Phiti cintura colorado de Oroncota en Potosí con 0,673 mg Lu/g de cáscaras y Pico y Loro obtenido de Monteagudo en Chuquisaca con 0,589 mg Lu/g de cáscaras. Por otra parte, los extractos de EtOH que también presentan propiedades farmacológicas interesantes, fueron también analizados en su contenido de luteolina, determinando concentraciones de hasta 79,728 y 74,188 mg Lu/g de extracto en los cultivares de Phiti cintura colorado de Oroncota en Potosí y Phiti cintura ladrillo de Padilla en Chuquisaca, respectivamente. Finalmente se determinó que la temperatura de tostado (80°C) no afecta a la luteolina.
INTRODUCCION
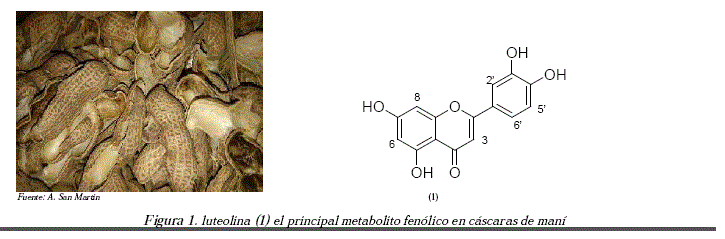
]]> La luteolina (3', 4', 5,7-tetrahidroxiflavona) (Lu) es un flavonoide producido por muchos alimentos y plantas medicinales. Tiene muchos usos como suplemento para la salud debido a sus propiedades farmacológicas [1]. Estas propiedades permiten considerar a la luteolina como un agente antiinflamatorio, neuroprotector y antialérgico [2-3], así como un agente con interesantes actividades antioxidantes [4-5] y anticáncer [6-11].Las cáscaras de maní son una de las fuentes comerciales más importantes de luteolina, estas cáscaras son de bajo costo ya que son un residuo de maní procesado [12].
El maní, Arachis hypogaea (Fabaceae), es un cultivo alimenticio producido en zonas tropicales y subtropicales [13]. Esta leguminosa es una planta domesticada que depende exclusivamente de la mano del hombre para sobrevivir, es endémica de América del Sur y algunos estudios indican que el origen de Arachis hypogaea subsp hypogaea es el sureste de Bolivia [14-15].
Bolivia es el cuarto exportador de maní en América Latina, con 25.951 toneladas producidas el 2016. Los cultivos se concentran principalmente en los valles de Chuquisaca, Tarija y Santa Cruz, aunque también está presentes en La Paz, Cochabamba, Beni y Potosí [16]. Para su venta en los mercados, el maní es tostado y descascarado (35% en peso) [17] generando grandes cantidades de residuos no utilizados o subutilizados, que son la materia prima de este estudio, por su contenido de luteolina.
En el presente trabajo se realizó la cuantificación de luteolina en 41 muestras de cáscaras de maní de cultivares obtenidos mayoritariamente en los valles mesotérmicos y zonas subtropicales de Chuquisaca (Muyupampa, Monteagudo y Padilla), así como en extractos etanólicos de las cáscaras. En adición, se realizó la cuantificación de luteolina, en muestras procesadas (tostadas) y no procesadas (sin tostar) de cáscaras obtenidas en los mercados de Sucre para determinar si el proceso de tostado afecta a la luteolina. Todo esto fue realizado con el objetivo de contribuir al potencial uso de estos residuos en suplementos para la salud, con base en el compuesto puro o el extracto etanólico rico en luteolina.
RESULTADOS Y DISCUSION
La materia prima fue principalmente proporcionada por el Banco de Germoplasma BIORENA de la USFX de Sucre y por el Instituto de Monteagudo (ISTAM). Las muestras se colectaron entre los años 2013 y 2016. Sólo cuatro muestras se han adquirido en los mercados de la ciudad de Sucre el 2016.
]]> Los extractos de cáscaras de maní se obtuvieron con etanol como disolvente y el contenido de luteolina en los extractos se cuantificó usando un método HPLC-DAD con patrón interno desarrollado en nuestro laboratorio con base en un método previamente establecido para flavonoides en Baccharis [18]. La curva de calibración se realizó utilizando estándar de luteolina (98% puro) como analito y estándar de quercetina (95% puro) como patrón interno.Se eligió un método con patrón interno, porque de acuerdo a varios autores es mejor que el método con patrón externo, ya que compensa internamente el efecto de variaciones menores sobre el tamaño del pico, como las comunes fluctuaciones debidas al peso o tamaño de la muestra. [19]
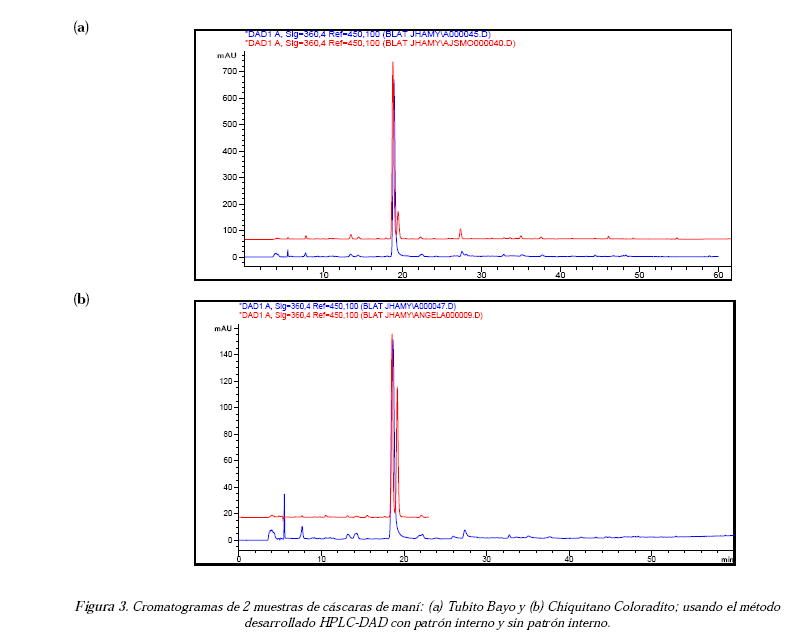
La quercetina fue seleccionada como patrón interno porque su tiempo de retención es cercano al de la luteolina pero ambas señales se distinguen (Figura 2), dando una curva de calibración (y = 5,1991x) con alta linealidad (R2 = 0.999) al graficar la relación de alturas de la señal de la luteolina respecto a la señal de la quercetina Vs la relación de las concentraciones de la luteolina respecto a la quercetina. Además, la quercetina es estable, no es reactiva en las condiciones de experimentación, tiene una estructura similar y por lo tanto de comportamiento equivalente a la del analito, y no está presente en las muestras de cáscara de maní, como se puede observar en la Figura 3 donde se muestran cromatogramas HPLC-DAD de dos cultivares de maní. Por lo tanto, cumple con todos los requisitos para ser un patrón interno [19].
Para la cuantificación de luteolina por el método desarrollado, los extractos secos se disolvieron con metanol (HPLC) y se analizaron por triplicado a 360 nm donde la luteolina aparece a un tiempo de retención de 18,7 min y la quercetina a 19,4 min (Figura 2 y Figura 3).
La Tabla 1 muestra los resultados del contenido de luteolina en extractos etanólicos y cáscaras de diversos cultivares de maní no procesados otorgados por los institutos BIORENA e ISTAM. La mayor parte de los cultivares (30 cultivares) pertenecen a la subespecie Arachis hypogaea subsp hypogaea mientras que sólo siete muestras (maní arbolito, fusilero, guano de oveja, coloradito paradito, tubito bayo, tubito colorado y blanco paradito) pertenecen a la subespecie Arachis hypogaea subsp fastigiata. Las muestras fueron recolectadas principalmente de las provincias Tomina y Hernando Siles de Chuquisaca que son grandes centros de producción de maní en Bolivia.
La Tabla 1 y la Figura 4 muestran que las cáscaras y extractos con mayor contenido de luteolina pertenecen a los cultivares phiti cintura colorado de Oronqota, Potosí (0,673 ± 0,082 mg Lu/g de cáscara; 79,728 ± 3,037 mg Lu/g de extracto), pico y loro de Monteagudo, Chuquisaca (0,589 ± 0,097 mg Lu/g de cáscara; 49,427 ± 0,994 mg Lu/g de extracto) y phiti cintura ladrillo de Padilla, Chuquisaca (0,419 ± 0,109 mg Lu/g de cáscara; 74,188 ± 3,748 mg Lu/g de extracto), por lo que se sugiere que de estos cultivares se hagan estudios más profundos para el desarrollo de potenciales suplementos para la salud en base a sus cáscaras. Por otra parte, es importante observar que la desviación estándar, en la cuantificación de luteolina en extractos y cáscaras, en algunos casos es elevada, errores atribuibles principalmente a errores manuales en el pesado de muestras.
]]>
Por otra parte, se realizó un estudio preliminar de muestras procesadas (tostadas) y no procesadas (sin tostar) ofrecidas en los mercados de la ciudad de Sucre (Tabla 2 y Figura 5), el que nos mostró que las cáscaras tostadas del cultivar conocido como Larguillo de Icla tienen un alto contenido de luteolina (0,850 ± 0,052 mg Lu/g de cáscara) mayor al determinado en las muestras sin procesar, siendo este similar a otros reportados en bibliografía que están en el rango de 0,547 a 4,485 mg/g de cascara de maní [12,17,20,21].
De acuerdo a los resultados de las cáscaras sin tostar (no procesadas) y tostadas (procesadas), el proceso de tostado no afecta a la luteolina, incrementándose su concentración en la cáscara probablemente por la pérdida de agua y otros en el proceso de tostado. Por tanto, el proceso inclusive resultaría beneficioso y esto es positivo considerando que la mayor parte de las cáscaras que se encuentran como residuos ya están tostadas. Para comprobar esto se realizó un estudio de termoestabilidad de la luteolina hasta una temperatura de 80ºC, temperatura a la cual, de acuerdo a informantes de Padilla, se realiza el proceso de tostado. El estudio de termoestabilidad fue realizado con luteolina aislada de la muestra de cáscara de maní tostado Larguillo Icla del mercado de Sucre (Figura 5) sometiendo a la muestra disuelta en EtOH a una temperatura de 80ºC y realizando el control de la luteolina por espectroscopía UV cada cierto tiempo hasta llegar a las 72 h. La Figura 6 muestra que la luteolina es estable a esta temperatura, mostrando resultados concordantes con otros estudios previamente realizados con este compuesto [22,23].
Finalmente, es importante mencionar, que estudios previos mostraron que no sólo la luteolina pura tiene propiedades farmacológicas, sino también los extractos metanólicos de cáscaras de maní, los cuales además de luteolina tienen otros compuestos de carácter fenólico como la 5,7-dihidroxicromona, el eriodictol y la 3,4,7-trihidroxiflavanona [24]. La extracción que se realizó fue con EtOH, otro alcohol de propiedades similares a las del MeOH pero menos tóxico, por lo que es probable que los extractos etanólicos también presenten propiedades antioxidantes y antiinflamatorias [20,21] debido a la presencia de compuestos fenólicos, así como propiedades antimutagénicas reportadas previamente para los extractos metanólicos [25]. Además, para fines de uso como suplemento para la salud, es importante mencionar que tanto la luteolina como los extractos metanólicos se absorben desde el intestino detectándose en el suero humano [26], por lo que pueden ser utilizados en suplementos de administración oral [3].
EXPERIMENTAL
]]> Material vegetalLas muestras de cultivares no procesados fueron proporcionadas por dos institutos de Chuquisaca, el Instituto de Agroecología y Seguridad Alimentaria de la Universidad San Francisco Xavier de Chuquisaca (BIORENA, USFX), y el Instituto Superior Tecnológico Agroindustrial de Monteagudo (ISTAM) a través de acuerdos de colaboración con el Instituto de Investigaciones Químicas de la Universidad Mayor de San Andrés (IIQ, UMSA).
Muestras de 19 cultivares fueron proporcionadas por el BIORENA (1, 6-13, 23, 25-27, 30-34 y 37), quienes realizaron las colectas a partir del año 2013, principalmente en áreas productoras de maní dentro el Departamento de Chuquisaca mostradas en la Tabla 1. Una vez colectadas las mismas fueron almacenadas a -5 °C en el Banco de Germoplasma del BIORENA dependiente de la USFX. El material genético conservado fue cultivado en el Municipio de El Villar durante los años 2014 a 2015, habiéndose obtenido rendimientos en estas accesiones de hasta 7,47 Tn/ha, mientras que el promedio nacional se encuentra muy por debajo de esos rendimientos. Las muestras fueron identificadas por el personal del mismo instituto, quienes además dieron los datos de los lugares de colecta. Una muestra de cada cultivar y la información correspondiente a su localización y producción se encuentran en el BIORENA, USFX.
Por otra parte, los restantes 18 cultivares, de la Tabla 1, se obtuvieron en colaboración del ingeniero Eloy Blanco del ISTAM, la colecta de los cultivares de maníes se realizó en comunidades de los municipios de Villa Vaca Guzmán (Muyupampa), Monteagudo y Padilla. Además, el Ing. Blanco proporcionó algunas variedades que poseía en el Instituto. Los cultivares colectados, fueron secados por el lapso de un mes a temperatura ambiente, en un ambiente debidamente ventilado del IIQ UMSA, protegiéndolos de los rayos del sol. La identificación de los cultivares fue realizada por el Ing. Blanco quien además posee en el ISTAM muestras de todos los cultivares proporcionados.
Finalmente, las muestras 38 al 41 fueron obtenidas en los mercados de Sucre, para poder realizar una comparación entre las muestras procesadas (tostadas) y no procesadas (sin tostar), así como de las muestras ofrecidas en los mercados de Sucre con las monitoreadas por personal del BIORENA e ISTAM. El nombre común de los cultivares y de la localidad de colecta fueron otorgados por las vendedoras del mercado. Muestras de estos cultivares se encuentran en el IIQ, UMSA.
Extracción
Una vez obtenidas las muestras secas, fueron trituradas con ayuda de una moledora eléctrica, evitando ser totalmente pulverizadas, posteriormente se tomó de 200 a 500 mg de cada muestra, adicionándoles etanol de 96º en la relación 1:15 (peso: volumen), sometiendo las muestras a un proceso de maceración con agitación constante, por el lapso de 4 horas a temperatura ambiente. Los extractos así obtenidos fueron filtrados a gravedad con papel filtro Whatman #4 y concentrados por rotaevaporación hasta sequedad. Finalmente, para eliminar por completo el solvente atrapado, fueron secados por 15 minutos más, en una bomba de alto vacío, obteniendo así los extractos secos y el rendimiento de cada extracto respecto al material seco. Esta operación se repitió por triplicado para cada muestra analizada.
Análisis por HPLC
Para la identificación y cuantificación de luteolina, se utilizó un equipo HPLC Agilent 1100 series acoplado a un detector de arreglo de diodos DAD (G1315B) Agilent. La columna utilizada fue una Agilent Technologies EclipsePlus C-18 (4.6×250mm×5μm) con una pre-columna de 0.5 μm. El compartimiento de la columna fue calentada a 40 ºC. Los solventes utilizados fueron acetronitrilo grado HPLC (Sigma-Aldrich), ácido fosfórico al 85% (Merck) y agua Ultrapurificada a 18.3 MΩ de resistencia, la cual fue filtrada con papel filtro de 0.45 µm en un sistema de filtración, Sartorius Stedim Biotech, antes de su uso.
Curva de calibración
]]> Para la curva de calibración se prepararon soluciones con 90 ppm del patrón interno, quercetina y diferentes concentraciones del analito a cuantificar, luteolina, 30, 60, 90, 120 y 150 ppm aforando cada solución a 1 ml. Con estas muestras se procedió al análisis por HPLC detectando el analito al tiempo de retención de 18,7 min y la quercetina a 19,4 min (Figura 2) y con la relación de alturas de la señal de la luteolina respecto a la señal de la quercetina Vs la relación de las concentraciones de la luteolina, respecto a la quercetina, se realizó la curva que sigue la ecuación Y= 5,1991X (R2=0,999).
Cuantificación de la luteolina
Para la cuantificación de luteolina, se procedió a disolver el total del extracto seco obtenido con 1 ml de metanol grado HPLC, filtrándolo previamente en membrana PTFE especiales de 0.45μm, para el análisis de HPLC. El extracto final fue trasvasado a los viales HPLC que ya contenían el patrón interno, quercetina.
El volumen de inyección de las muestras fue de 25 μL a un caudal de 0,6 ml / min. La fase móvil fue un sistema de disolvente binario que consiste en (A) 0.1% de ácido fosfórico y (B) acetonitrilo. El gradiente utilizado fue 25% B a 0 min, 28% B después de 5 min, 30% B después de 10 min, 32,8% B después de 17 min, 36% B después de 20 min y 100% B después de 22 min hasta los 25 minutos. La absorbancia UV del eluato, se registró utilizando un detector de arreglo de diodos múltiple a 210 nm, 280 nm y 360 nm. Las señales de la luteolina y quercetina fueron determinadas en el cromatograma a 360 nm a los tiempos de retención antes señalados y la cantidad de luteolina fue cuantificada utilizando la curva de calibración descrita. Todas las muestras fueron analizadas por triplicado reportándose el promedio ± la desviación estándar.
Aislamiento e identificación de la luteolina
Para el aislamiento de luteolina se pesó 1 g de extracto etanolico obtenido del cultivar larguillo tostado de Icla, el cual se lo disolvió en MeOH y se pasó por un cadrige (DPA-6S) para separar algunas impurezas, después de este proceso se obtuvo 329,5 mg del extracto tratado, que se sembró en una columna Sephadex LH-20 obteniéndose en las últimas fracciones 29,2 mg de luteolina pura por comparación con el estándar del compuesto.
Para confirmar su identificación se realizaron espectros de RMN de 1H y 13C obteniéndose los siguientes resultados, que confirmaron la estructura propuesta.
RMN 1H (300 MHz, DMSO) δ 7.41 (1H, dd, J= 8.1, 1.9 Hz, H-6), 7.38 (1H, d, J= 1.9 Hz, H-2), 6.87 (1H, d, J= 8.1 Hz, H-5), 6.65 (1H, s, H-3), 6.42 (1H, d, J= 1.8 Hz, H-8), 6.17 (1H, d, J= 1.8 Hz, H-6).
]]> RMN 13C (75 MHz, DMSO) δ 182.1 (C-4), 164.6 (C-7), 164.3 (C-2), 161.9 (C-9), 157.7 (C-5), 150.1 (C-4), 146.2(C-3), 121.9 (C-6), 119.4 (C-1), 116.4 (C-5), 113.8 (C-2), 104.1 (C-3), 103.3 (C-10), 99.2 (C-6), 94.3 (C-8).Termoestabilidad de la luteolina
Para la evaluación de la termoestabilidad, se preparó una solución de 5 ppm del compuesto aislado luteolina en EtOH al 96 °G, de esta solución se tomó una alícuota de 3 ml que fue sometida a calentamiento con una termocupla a 80°C por tiempos controlados de 1, 3, 7, 24, 48 y 72 h, después de cada lapso de tiempo se realizó un espectro de barrido UV entre 250 y 450 nm, midiéndose la absorbancia en el ![]() de 352 nm, con estos datos luego se realizó la gráfica de Absorbancia Vs Tiempo (Figura 6) que muestra la termoestabilidad de la luteolina.
de 352 nm, con estos datos luego se realizó la gráfica de Absorbancia Vs Tiempo (Figura 6) que muestra la termoestabilidad de la luteolina.
RECONOCIMIENTOS
Los investigadores agradecen al proyecto Productos fitoterapéuticos y cosmecéuticos a partir de residuos agroindustriales financiado por fondos ASDI concursables. Así como al proyecto Bases científicas para el desarrollo de productos naturales con valor agregado a partir de residuos de café y maní financiado por recursos IDH-UMSA.
Así mismo agradecen a los institutos BIORENA de la USFX, ISTAM e IIQ de la UMSA, por el apoyo en infraestructura, carga horaria de investigadores y equipos para la realización del presente trabajo.
NOTAS
1Laboratorio de Bioorgánica, Instituto de Investigaciones Químicas IIQ, Ciencias Químicas, Facultad de Ciencias Puras y Naturales FCPN, Universidad Mayor de San Andrés UMSA, P.O. Box 303, Calle Andrés Bello s/n, Ciudad Universitaria Cota Cota, phone +59122772269, La Paz, Bolivia, galmanza3@umsa.bo, www.umsa.bo
]]> 2Instituto de Biodiversidad y Recursos Naturales Aplicados al Desarrollo BIORENA Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca USFX, Sucre, Chuquisaca, Bolivia3Instituto Superior Tecnológico Agroindustrial de Monteagudo ISTAM, Monteagudo, Chuquisaca, Bolivia
REFERENCIAS
1. López-Lázaro M. 2009, Distribution and biological activities of the flavonoid luteolin; Mini Rev Med Chem. 9(1), 31-59. [ Links ]
2. Nabavi, S.F., Braidy, N., Gortzi, O., Sobarzo-Sanchez, E., Daglia, M., Skalicka-Woźniak, K., Nabavi, S.M., 2015, Luteolin as an anti-inflammatory and neuroprotective agent: A brief review, Brain Res Bull. 119(Pt A), .1-11. [ Links ]
3. Ueda, H.; Yamazaki, C.; Yamazaki, M., 2002. Luteolin as an anti-inflammatory and anti-allergic constituent of Perilla frutescens. Biol. Pharm. Bull. 25(9), 1197-202. [ Links ]
4. Pérez-García, F., Adzet, T., Cañigueral, S., 2000, Activity of artichoke leaf extract on reactive oxygen species in human leukocytes; Free Radical Research 33(5), 661-665. [ Links ]
5. Seelinger, G., Merfort, I., Schempp, C.M., 2008. Anti-oxidant, anti-inflammatory and anti-allergic activities of luteolin, Planta Med. 74(14), 1667-1677 [ Links ]
6. Horinaka, M., Yoshida, T., Shiraishi, T., Nakata, S., Wakada, M., Nakanishi, R., Nishino, H., Matsui, H., Sakai, T., 2005, Luteolin induces apoptosis via death receptor 5 upregulation in human malignant tumor cells; Oncogene 24(48), 7180-7189. [ Links ]
7. Lee, H.J., Wang, C.J., Kuo, H.C., Chou, F.P., Jean, L.F., Tseng, T.H., 2005, Induction apoptosis of luteolin in human hepatoma HepG2 cells involving mitochondria translocation of Bax/Bak and activation of JNK, Toxicology and Applied Pharmacology; 203(2), 124-131. [ Links ]
8. Chowdhury, A.R., Sharma, S., Mandal, S., Goswami, A., Mukhopadhyay, S., Majumder, H.K., 2002, Luteolin, an emerging anti-cancer flavonoid, poisons eukaryotic DNA topoisomerase I, Biochemical Journal 366 (2), 653-661 [ Links ]
9. Ko, W.G., Kang, T.H., Lee, S.J., Kim, Y.C., Lee, B.H., 2002, Effects of luteolin on the inhibition of proliferation and induction of apoptosis in human myeloid leukaemia cells; Phytotherapy research 16(3), 295298. [ Links ]
10. Lin, Y., Shi, R., Wang, X., Shen, H.M., 2008, Luteolin, a Flavonoid with Potential for Cancer Prevention and Therapy, Current Cancer Drug Targets, 8(7), 634-646. [ Links ]
11. Yasukawa, K., Takido, M., Takeuchi, M., Nakagawa, S., 1989, Effect of chemical constituents from plants on 12-O-tetradecanoylphorbol-13- acetate induced inflammation in mice. Chem Pharm Bull, 37(4), 1071-1073. [ Links ]
12. Qiu, J., Chen, L., Zhu, Q., Wang, D., Wang, W., Sun, X., Liu, X., Du, F., 2012, Screening natural antioxidants in peanut shell using DPPHHPLCDADTOF/MS methods, Food Chemistry, 135 (4), 23662371 [ Links ]
13. Bertioli, D.J., Seijo, G., Freitas, F.O., Valls, J.F.M., Leal-Bertioli S.C.M., Moretzsohn, M.C., 2011, An overview of peanut and its wild relatives; Plant Genetic Resources, 9(1), 134-149.. [ Links ]
14. Krapovickas, A., Gregory, W.C., 1994, Taxonomia del genero Arachis (Leguminosae), Bonplandia 8(1-4): 1-186. [ Links ]
15. Krapovickas A, Consideraciones prehistóricas sobre el origen del maní cultivado , 2004, Facultad de Ciencias Agrarias Universidad Nacional del Nordeste - Corrientes Sesión Pública del 5 de Noviembre de 2004 [ Links ]
16. http://www.ine.gob.bo/index.php/estadisticas-por-actividad-economica/industria-manufacturera-y-comercio-4, 30/7/2017.
]]>17. Radhakrishnan, R., Pae, S-B., Lee, B-K., In-Youl, B., 2013, Evaluation of luteolin from shells of Korean peanut cultivars for industrial utilization, African Journal of Biotechnology, 12(28), 4477-4480. [ Links ]
18. Almanza, G.R., Salcedo, L. 2012. De la planta al medicamento. Parte I Investigaciones de Baccharis latifolia (Chilca). Ed. I. Editorial Académica Española, Saärbrucken, Alemania, 174-190. [ Links ]
19. Snyder, L.R., Kirkland J.J., Dolan, J.W., 2010, Introduction to Modern Liquid Chromatography, Third edition, Hoboken, New Jersey-USA, Wiley & Sons., pp. 520-527. [ Links ]
20. Yen, G.C., Duh, P.D., 1995. Antioxidant activity of methanolic extracts of peanut hulls from various cultivars. Journal of the American Oil Chemists Society, 72 (9), 1065-1067. [ Links ]
21. Mar, M.W., Azizah, A-H., Badlishah, S.B., Farooq, A., Nazamid, S., 2011, Phenolic compounds and antioxidant activity of peanut's skin, hull, raw kernel and roasted kernel flour, Pakistan Journal of Botany, 43(3), 1635-1642. [ Links ]
22. Fischer, F., Zufferey, E., Bourgeois, J-M., Héritier, J., Micaux, F., 2011. UV-ABC screens of luteolin derivatives compared to edelweiss extract, Journal of Photochemistry and Photobiology B: Biology, 103(1), 8-15. [ Links ]
23. Murakami, M., Yamaguchi, T., Takamura, H., Matoba, T., 2004, Effects of thermal treatment on radical-scavenging activity of single and mixed polyphenolic compounds, Journal of Food Science, 69 (1), 710. [ Links ]
24. Wee, J. H., Moon, J. H., Eun, J. B., Chung, J. H., Kim, Y. G., & Park, K. H. 2007, Isolation and identification of antioxidants from peanut shells and the relationship between structure and antioxidant activity, Food Science and Biotechnology, 16, 116122. [ Links ]
25. Yen, G.C., Duh, P.D., 1996. Antimutagenic effect of methanolic extracts from peanut shells. Bioscience, Biotechnology, Biochemistry, 60(10), 16981700. [ Links ]
26. Shimoi, K., Okada, H., Furugori, M., Goda, T., Takase, S., Suzuki, M., Hara, Y., Yamamoto, H., Kinae, N., 1998, Intestinal absorption of luteolin and luteolin 7-O-beta-glucoside in rats and humans. FEBS Lett. 438(3), 220 224 [ Links ]
]]>