Oxidative stability in almonds of bertholletia excelsa; accelerated deterioration of the dry fruits under thermal conditions
Estabilidad oxidativa en almendras de Bertholletia excelsa; deterioro acelerado del fruto seco en condiciones termales.
Juan Carlos Callisaya A., Juan Antonio Alvarado K.
Department of Chemistry, Instituto de Investigaciones Químicas IIQ, Centro de Estudios e Investigaciones en Química de Alimentos CEIQA, Universidad Mayor de San Andrés UMSA, P.O. Box 303, Calle Andrés Bello s/n, Ciudad Universitaria, Cota Cota, Phone 59122792238, La Paz, Bolivia, jkallisaya34@gmail.com, jaalvkir@gmail.com
*Corresponding author: jkallisaya34@gmail.com
Abstract
Bertholletia excelsa (Lecythidaceae), amazonian almonds from Bolivia or Brazil nuts is an economically important plant in the Bolivian Amazonian region . It has a significant content of bioactive compounds with antioxidant properties such as vitamin C, E, (3-carotenes and a complex mixture of phenolic compounds. It is very susceptible to oxidative deterioration, which is the biggest problem in this type of food, with the altering of the texture, appearance, flavor and aroma. However, the high content of phenolic compounds inhibits lipid oxidation of these nuts, depending on the variation of the characteristic physical and chemical parameters.. The aim of this work is to determine the oxidative stability of lipids in of Bertholletia excelsa.
According to the experimental design (Diagram 1) we proceed to take 3 to 4 nuts for each one of the four heat treatments, each forty days. Determining the peroxidation is carried out with the TBARS technique. It occurs the formation of a coloured complex MDA-TBARS when the sample is treated with trichloroacetic acid (TCA). The extract obtained from the samples under acidic conditions is distilled, the solution of TB A is added to portions of the distillate under thermal conditions, the solution takes a pinkish coloration that can be spectrophotometrically quantified at a wavelength of 538 nm. The oxidative process of the dry fruit comports thermal conditions at four temperatures showing a zero-order kinetics. The concentration of MDA increases with the induced peroxidation accelerated process The useful life activation energy was 19,89 kcal/mol, a value according to the literature. Also, the lifetime estimated in the oxidative stability study concludes that at a storage temperature below -80°C, almonds have a duration of 7 years and at temperatures of 20, 25 and 45 ° C, the lifetime diminishes to 2.5; 2.4; and 2.1 years, respectively. The variation of the storage temperature at -80, 20, 25 and 40 ° C evidence a dependence between the rate constant of reaction "k" and temperature, wherein the variation in the degradation rate of lipids is increased at higher temperature.
Keywords: Antioxidant activity, Phenolic compounds, Bertholletia excelsa, Lecythidaceae
Resumen
La almendra amazónica o nuez de Brasil (Bertholletia excelsa) es una planta importante de la amazonia boliviana. Tiene un contenido importante de compuestos bioactivos con capacidad antioxidante como la vitamina C, E, (3- caroteno y una mezcla compleja de compuestos fenólicos. Es muy susceptible al deterioro oxidativo, que es el mayor problema en este tipo de alimentos, alterando la textura, apariencia, sabor y aroma. Sin embargo, el alto contenido de compuestos fenólicos inhibe la oxidación lipídica de los alimentos dependiendo de las condiciones físicas y propiedades químicas de las sustancias contenidas en las almendras. El objetivo de este estudio es determinar la estabilidad oxidativa de los lípidos en la almendra amazónica boliviana (Bertholletia excelsa).
De acuerdo al diseño experimental (diagrama 1) se procede a la toma de 3 a 4 nueces de almendra de cada tratamiento térmico, cada cuarenta días. La determinación de la peroxidación se realiza con la técnica TBARS. La formación del complejo MDA-TBARS colorido se produce cuando la muestra es tratada con ácido tricloroacético
(TCA). El extracto de las muestras obtenido bajo condiciones ácidas es destilado y la solución de TBA se agrega a porciones del destilado qué es incubado en caliente, la solución toma una coloración rosácea que se cuantifica mediante espectrofo tome tría a una longitud de onda de 538 nm.
]]> El proceso oxidativo de la almendra amazónica a las 4 temperaturas de estudio se ajusta a una cinética de orden cero, donde la concentración de MDA se incrementa en el proceso de aceleración inducida de la peroxidación. La energía de activación hallada según la ley de velocidad obtenida en el estudio de vida útil fue de 19,89 kcal/mol, valor que se encuentra dentro de los parámetros bibliográficos. Asimismo, el tiempo de vida estimada en el estudio de la estabilidad oxidativa, concluye que a una menor temperatura de almacenamiento -80 °C las almendras tienen una duración de 7 años y que a las temperaturas de 20, 25 y 45 °C el tiempo de vida va disminuyendo a 2,5; 2,4; y 2,1 años respectivamente. La variación de la temperatura de almacenamiento entre los rangos de -80, 20, 25 y 40 °C evidencia una dependencia entre la constante de velocidad de reacción "k" y la temperatura, donde la variación en la velocidad de degradación de los lípidos se incrementa a mayor temperatura.
INTRODUCCION
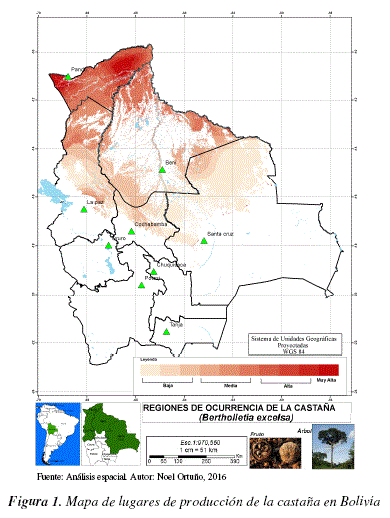
La empresa Tahuamanu S.A. está ubicada al norte de Bolivia, en la ciudad de Cobija capital del departamento de Pando y se especializa en el beneficio de la almendra amazónica, también conocida internacionalmente como "nuez de Brasil", Bertholletia excelsa sin cáscara, un fruto seco nutritivo y abundante de los bosques nativos cálidos y húmedos del norte amazónico (Norte de Bolivia, figura 1).
Bertholletia excelsa puede ser un componente importante de la dieta alimentaria humana. El consumo de la almendra amazónica provee macro y micronutrientes bioactivos, entre los cuales está el selenio.
El paradigma de 1955 que descalificaba el consumo de grasas saturadas, repercutió en cierta reducción del consumo de la almendra amazónica como fruto seco, debido a la preocupación por la ingesta de alimentos grasos, pues la almendra amazónica boliviana está constituida aproximadamente en un 60 a 70 % por ácidos grasos.
Sin embargo, el descubrimiento de los efectos beneficiosos de los compuestos fenólicos sobre el estrés oxidativo y de los ácidos grasos poliinsaturados (omega-3) sobre la salud cardiovascular, así como la quiebra del mencionado paradigma de 1955 al demostrarse que el organismo requiere cocientes especiales de consumo de ácidos grasos saturados, mono-insaturados, y poli-insaturados ha llevado a que nuevamente los frutos secos en general y las nueces en particular sean considerados dentro de la dieta como un alimento cuyo consumo es aconsejable.
En efecto, la composición de los ácidos grasos consumidos puede influir en varios procesos fisiológicos y bioquímicos, incluyendo: regulación de la presión arterial, metabolismo de la glucosa, metabolismo lipídico y deformabilidad de eritrocitos. [1]
]]> En el mundo, la almendra amazónica es producida por un árbol que pertenece a la familia de las Lecythidaceae de forma natural y silvestre en los bosques tropicales amazónicos de América del Sur de Venezuela, Colombia, Bolivia, Perú, Guayana y Brasil, [2]Debido a su ubicación geográfica, Bolivia es un productor natural de la almendra amazónica presentando condiciones de producción óptimas para su almacenamiento. Su alto costo para la industria se traduce en una oportunidad para la producción nacional en la medida que el país pueda producir los volúmenes suficientes y con la calidad óptima para competir y posicionarse de los mercados internacionales.
Actualmente, dada las nuevas tendencias de habito alimentario de las personas, cobra gran interés por los productos naturales, que han situado a los frutos secos en general y a la almendra amazónica en particular, en un lugar privilegiado como alimento para consumo como "snack nuts", rico en vitaminas liposolubles, bajo en contenido de carbohidratos, con 0% de colesterol, alto contenido de ácidos grasos del tipo omega-3 y omega-6 y con un bajo o nulo contenido de los del tipo trans.
La calidad de un alimento es importante, en un sentido más amplio la calidad probada de un alimento debe ser igual o superior a las expectativas de calidad del consumidor.
Un alimento es un sistema con parámetros fisicoquímicos en depresión constante en el tiempo en condiciones normales, vale decir, la calidad del mismo disminuye permanentemente. Existe un tiempo determinado, después de haber sido producido, en el que él producto mantiene un nivel requerido de sus propiedades sensoriales y de calidad, bajo ciertas condiciones de almacenamiento. Este constituye el período de vida útil o vida de anaquel del alimento. [3,4]
La oxidación es uno de los procesos más importantes en los alimentos, afectando muchas interacciones entre los componentes alimentarios lo cual conduce a productos deseables e indeseables. Los lípidos alimentarios son muy susceptibles a los procesos de oxidación, y por ello las reacciones de oxidación son la mayor causa de deterioro durante el procesamiento, almacenamiento y distribución del alimento.
Una de las maneras más efectivas de retardar la oxidación lipídica en los alimentos es incorporando antioxidantes; cuya acción se produce por una diversidad de mecanismos, incluyendo el control de oxidación de los sustratos (lípido y oxígeno), control de pro-oxidantes e inactivación de radicales libres. Recientemente ha crecido el interés por los antioxidantes naturales, qué se presume, son más confiables ya que son producidos en las plantas alimentarias. Lo atractivo en la aplicación de antioxidantes naturales como aditivos alimentarios se debe a su potencial benéfico a la salud. Esto es de especial importancia cuando los extractos ricos en componentes fenólicos de productos de una planta son aplicados como estabilizadores en los alimentos. [5]
Los antioxidantes endógenos de las plantas son capaces de inhibir la peroxidación lipídica en los alimentos y brindan protección contra el daño oxidativo a las membranas biológicas. Los productos de la peroxidación lipídica in vivo y la oxidación lipídica dietaría han demostrado ser la primera causa de muchas enfermedades, ejemplo; aterosclerosis, cáncer para nombrar los más importantes, y procesos de envejecimiento. Investigadores de la ciencia médica están validando con métodos modernos las terapias preventivas.
El análisis de los productos de la oxidación lipídica en los alimentos es difícil debido a su naturaleza compleja; la inestabilidad y grandes cantidades de sustancias interferentes en los alimentos, la sofisticación y a veces la falta de un método analítico específico y adecuado.
El análisis de antioxidantes naturales en alimentos que contienen mezclas complejas de compuestos de variado mecanismo de acción, se dificulta por lo complejo de la evaluación del estado oxidativo de los lípidos en el alimento. Los métodos para determinar la magnitud de la oxidación pueden alinearse en base a su utilidad prediciendo la estabilidad, vida de anaquel y aceptabilidad del consumidor.
]]> Los métodos cromatográficos están basados en el análisis de compuestos específicos volátiles incluyendo, el índice químico de oxidación, el grado de absorción del oxígeno que es útil en la evaluación del grado de oxidación, sin embargo la búsqueda de nuevos métodos, basados en la químiometria y electrónica son fuentes de métodos que llevan a la comprensión de la peroxidación lipídica y su influencia en la calidad del alimento. [5]La velocidad de oxidación de los lípidos depende de las condiciones de almacenamiento tales como la exposición a la luz, contenido de humedad, temperatura, y disponibilidad de oxígeno. El envejecimiento acelerado es un método dónde se selecciona los parámetros ambientales que son modificados para aumentar la velocidad de las reacciones químicas involucradas en el deterioro de un alimento. [6]
Varios parámetros físico-químicos pueden alterarse para aumentar la velocidad de reacción y por consiguiente el desarrollo de la rancidez, como la temperatura, catálisis de metal, aumento de la presión parcial del oxigeno para aumentar la velocidad de reacción de la interface, etc. [7] Sin embargo puesto que la velocidad de reacción aumenta exponencialmente con la temperatura absoluta [8] este parámetro es usualmente elegido para acelerar el proceso de oxidación.
Establecer las condiciones para acelerar un ensayo de vida de anaquel (ASLT: accelerated shelf-life test, siglas en ingles) no es una tarea fácil, puesto que es necesario escoger las condiciones que pueden ser usadas para incrementar la velocidad de oxidación y las determinaciones analíticas para seguir el proceso de la reacción, preferentemente midiendo los productos de la oxidación primaria o secundaria.
Finalmente, el paso más difícil es correlacionar el valor del periodo de inducción obtenido bajo las condiciones aceleradas de vida de anaquel del producto alimentario dentro del periodo de almacenamiento máximo [8] con este fin, es necesario llevar a cabo estudios cinéticos y aplicados a la ecuación de Arrhenius o calcular el aumento de la velocidad de oxidación producida por un aumento de temperatura. [9] Debido a las dificultades y limitaciones involucradas en esta metodología, la evaluación de la vida de anaquel de las grasas comestibles y aceites en condiciones de almacenamiento normales por ASLT son aun todavía un fin para la comunidad científica. [10, 11]
Este artículo describe el estudio cinético de la reacción de autoxidación de los lípidos de la castaña amazónica boliviana (Bertholletia excelsa) por aceleración inducida en almacenamiento a -80, 20, 25 y 45 °C donde se mide cada 40 días la formación de malondialdehido mediante el método TB ARS por un tiempo de 200 días.
EXPERIMENTAL
Materiales y métodos
Productos químicos
]]> Reactivo BHT (Butil hidroxitolueno), EDTA (Etilendiaminotetraacetato) TEP (1,1,3,3-tetraetoxipropano), TBA (Ácido tiobarbitúrico) Ácido acerico glacial, Ácido clorhídricoColecta de muestras
Las almendras amazónicas fueron ofrecidas por la empresa Tahuamanu S. A. las cuales se encontraban envasads al vacío en bolsas plásticas.
Después de recibidas, las muestras fueron congeladas a -80 °C hasta su análisis. Para el estudio de la almendra amazónica boliviana se diseñó un proceso de simulación cinética a diferentes temperaturas: - 80, 20, 25 y 45 °C. Este proceso es conocido como aceleración inducida, donde cada 40 días se procede a tomar 5 a 6 gramos de muestra a las temperaturas de estudio (Diagrama 1) hasta completar un tiempo final de 200 días.
El proceso de aceleración inducida se inició colocando aproximadamente 200 g de castaña (B. excelsa) en frascos de vidrio (4 muestras de estudio), los cuales fueron cerrados y se colocaron en estufas a las diferentes temperaturas de estudio. Al inicio del estudio se procedió a realizar el análisis de los diferentes ensayos para posteriormente proceder a cuantificarlos y obtener los datos iníciales a tiempo cero.
Obtención del extracto lipídico
La obtención del extracto lipídico, para realizar el monitoreo de la peroxidación lipídica se realizó a partir de muestras de almendra incubadas a las diferentes temperaturas de estudio (-80, 20, 25 y 45 °C), tomando 2 a 4 nueces de almendra enteras y luego molidas en un homogenizador; 5 g de muestra molida es homogenizada con 17,5 mL de agua destilada para luego sonicar y posteriormente proceder a destilar por 30 minutos. A un tubo de ensayo con tapa rosca se pipetea 5 mL de la solución obtenida (destilado) y de inmediato se agrega 5 mL de reactivo TBA tapando los tubos rápidamente.
Medición de la peroxidación lipídica
La mayor parte del malondialdehido (MDA) que se detecta durante el ensayo TBARS, se forma durante la oxidación lipídica; sin embargo, también puede proceder de la descomposición de peróxidos lipídicos por las condiciones de calor y acidez del ensayo, por lo que se añaden antioxidantes o compuestos quelantes como el butilhidroxitolueno (BHT) o EDTA para evitar la autoxidación de otros ácidos grasos insaturados (AGI) de la muestra (Gutteridge y Halliwell, 1990). Los protocolos propuestos para la determinación del complejo MDA-TBARS son muy variados, y se basan en el tratamiento de la muestra con ácido tricloroacético (TCA). El extracto alimenticio bajo condiciones ácidas es destilado y la solución de TBA se agrega a porciones del destilado qué es incubado en caliente, la solución toma una coloración rosácea que se cuantifica mediante espectrofotometría a una longitud de onda de 538 nm.
]]> Análisis estadísticoLos resultados para el estudio de la estabilidad oxidativa mediante el método TBARS se muestran como valores promedios y valores de ΔX de 9 replicas medidas por tres días. Los coeficientes de correlación lineal son calculados acorde al método de Pearson. Todos los cálculos han sido realizados con software Excel.
RESULTADOS Y DISCUSIÓN
Estudio de la estabilidad oxidativa
El índice TBARS es usado para evaluar la oxidación lipídica durante el almacenamiento. La presencia de las especies reactivas al ácido tiobarbitúrico "TBARS" se correlaciona con el grado de autoxidación secundaria en que los peróxidos son oxidados a aldehídos y cetonas. La oxidación lipídica es afectada por el tiempo (factor intrínseco) y temperatura (factor ambiental).
Los valores de TBARS obtenidos en muestras sometidas a aceleración inducida (Tabla 1, Figura 2) a diferentes temperaturas; - 80, 20, 25 y 45 °C muestran marcada relación notándose el incremento de la peroxidación en función del tiempo y la temperatura influyendo notablemente en la estabilidad oxidativa de la almendra amazónica, la cual es creciente, a temperaturas mayores la oxidación es más notoria que a una menor temperatura. Esto nos muestra de manera directa el daño celular producido por la peroxidación lipídica en las almendras, donde constantemente se incrementa la formación de malondialdehido en el tiempo de almacenamiento determinado a través de la variación del índice TBARS que es afectado significativamente por el tratamiento.
La concentración inicial de TBARS es 0,159 mg de malondialdehido (MDA)/(g de muestra), de acuerdo a Papadima y col. (1999) en productos cárnicos los valores de TBA son superiores a 1 mg considerados rancios y según Wenjiao y col. (2013) [12] esta rancidez se da cuando los valores de TBA son superiores a 2 mg. Tomando en cuenta estas observaciones, debemos acotar que las muestras de almendra amazónica tienen un porcentaje alto de lípidos respecto a los productos cárnicos, por lo cual los valores obtenidos son relativamente altos. También es útil mencionar que la recolección de las almendras se realiza semanas antes de que está llegue a la planta procesadora por lo tanto no es inmediata ya que durante este tiempo las nueces de almendra sufren deterioro por la humedad y temperatura del ambiente que son factores considerablemente cruciales que afectan la rancidez oxidativa del producto.
El incremento de la concentración al final de la peroxidación lipídica es de: 2,287; 1,538; 1,271 y 1,113 mg de malondialdehido (MDA)/g a 45, 25, 20 y -80 °C respectivamente.
Estos resultados demuestran que los productos de la oxidación lipídica se acumulan durante el proceso de aceleración inducida. Adicionalmente el índice inicial TBARS puede ser afectado por la composición de los lípidos, así como por el proceso industrial que se le aplica a la almendra amazónica.
]]>
Modelo cinético predictivo TBARS
Para el análisis del modelo cinético de la oxidación cinética, se sigue el modelo matemático propuesto por Labuza y Riboh [13], calculándose las curvas de regresión lineal para cada uno de los parámetros (Figura 11) con la finalidad de establecer el valor de k para predecir la cinética de la reacción.
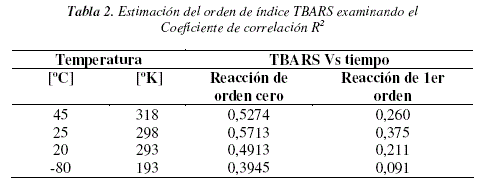
Los valores graficados son: TBARS Vs tiempo para todas las temperaturas estudiadas (Tabla 1, Figura 2) de donde se obtiene los valores de coeficiente de correlación R2 (Tabla 2), prediciendo así el orden de reacción.
En la Tabla 3 se muestran los valores de coeficientes de correlación a las diferentes temperaturas; 318, 298, 293 y 193 °K durante 200 días. Los valores de coeficiente de correlación fueron obtenidos aplicando las ecuaciones 2 y 3 para una reacción de orden cero como para una reacción de primer orden respectivamente, lo que nos permitió predecir el orden cinético de reacción. Los resultados nos muestran que para una cinética de orden cero el coeficiente de correlación tiende a 1, en tanto que los valores para una cinética de primer orden los valores son menores, por lo tanto la predicción del modelo cinético corresponde a una reacción cinética de orden cero.
Asimismo, la Figura 3 nos muestra la velocidad dependiente de la temperatura ya que a mayor temperatura la velocidad de reacción es también mayor.
]]>
Para predecir la energía de activación "Ea" de la reacción de oxidación en la castaña amazónica se hizo el calculó mediante la gráfica (Tabla 3), utilizando como modelo la ecuación de Arrhenius (Boekel 2008) [14]:
La ecuación modificada de Arrhenius está dada por:
Los diferentes valores de k se deben a las distintas temperaturas de trabajo, siendo mayores a temperaturas más altas de almacenamiento. Esto coincide con lo descrito en bibliografía, que indica que la rapidez de las reacciones químicas aumenta conforme se eleva la temperatura. [15]
Por lo tanto, se puede concluir que se obtiene una velocidad de deterioro más lenta a una menor temperatura, lo que permitirá un tiempo mayor de vida de anaquel para el producto.
Mediante la ecuación de Arrhenius (ecuación 5) es posible graficar los valores de las constantes de velocidad, obtenidas para las diferentes temperaturas, y obtener la energía de activación de la reacción de oxidación. Este ajuste se observa en la Figura 4.
Aplicando en: ln k = ln A -Ea/RT, ecuación de una recta de pendiente -Ea/R y ordenada en el origen ln A.
]]>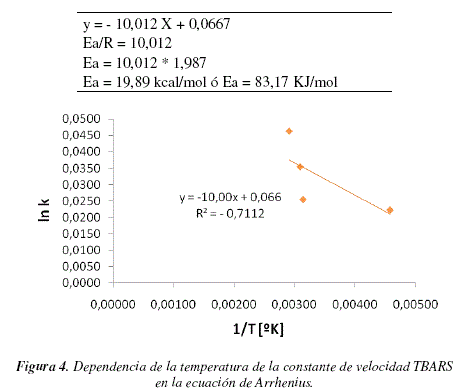
Datos bibliográficos reportados por Saguy y Karel [12] concluyen que, para que las reacciones de oxidación de lípidos procedan, se requiere una energía de activación entre 10 a 25 kcal/mol, mientras que para las reacciones de oscurecimiento no enzimático se requiere una energía de activación comprendida en el rango de 25 a 50 kcal/mol.
El valor obtenido de energía de activación (19,89 kcal/mol) se encuentra dentro el rango de una oxidación de lípidos, sin embargo se debe tomar en cuenta la posibilidad de que otras reacciones estén sucediendo en el proceso tanto de deterioro, como antioxidante (Figura 4) al mismo tiempo, debido a la complejidad del producto analizado.
La predicción del tiempo de vida de la almendra amazónica se realiza partir a través del modelo de Arrhenius.
La gráfica 5 muestra el gráfico Ln t Vs 1/T del logaritmo natural del tiempo de vida de anaquel contra el inverso de la temperatura para la almendra amazónica.
Este gráfico corresponde a la linealización del modelo de Arrhenius, el cual esta representado por la siguiente expresión:
La pendiente y el intercepto de esta recta permiten calcular los valores de los parámetros Ea y to:
]]> Ea/R = 722,4Ea = 722,4 * 1,986 cal/mol = 1434,69 cal/mol
to = e6,964 = 1057,86
Con estos valores se puede predecir el tiempo de vida de anaquel para la almendra amazónica a cualquier temperatura de almacenamiento. La temperatura normal de almacenamiento podría fijarse alrededor de 20 °C. Para esta temperatura el valor esperado de tiempo de vida de anaquel para la almendra amazónica en cuestión puede calcularse reemplazando los valores de energía de activación y del factor preexponencial en la ecuación 6:
t20.c = 1057,86 * e 1434,69/1,986*[(1/298,15)-(1/318,15)]
t20.c = 908,4 días = 2,49 años
Obteniendose los siguientes resultados Tabla 4:
CONCLUSIONES
]]> El proceso oxidativo de la almendra amazónica a las cuatro temperaturas de estudio se ajusta a una cinética de orden cero, donde la concentración de MDA se incrementa en el proceso de aceleración inducida. La energía de activación hallada según la ley de velocidad obtenida en el estudio de vida útil fue de 19,89 kcal/mol, valor que se encuentra dentro de los parámetros bibliográficos.De acuerdo a los resultados del tiempo de vida estimada en el estudio de la estabilidad oxidativa de la almendra amazónica, se concluye que a una menor temperatura de almacenamiento -80 °C las almendras tienen una duración de 7 años y que a las temperaturas de 20, 25 y 45 °C el tiempo de vida va disminuyendo: 2,5; 2,4; y 2,1 años respectivamente.
Al variar la temperatura de almacenamiento de la almendra amazónica entre los rangos de -80, 20, 25 y 40 °C se puso en evidencia una dependencia entre la constante de velocidad de reacción "k" y la temperatura, donde la variación en la velocidad de degradación de los lípidos se incrementa a mayor temperatura.
RECONOCIMIENTOS
Agradecemos a la Agencia de Desarrollo Internacional Sueca (SIDA) en el Proyecto "Antioxidantes en Alimentos de Bolivia" dentro del convenio de cooperación UMSA-ASDI, Universidad de Lund, Suecia, por el soporte financiero.
A la Empresa Tahuamanu S.A. representada por Oscar Farfán y Enrique Nelkenbaum por facilitar las almendras amazónicas. Un agradecimiento especial al Prof. Björn Bergenståhl, Universidad de Lund y al Prof. José Mauricio Peñarrieta, Universidad Mayor de San Andrés, por el apoyo técnico brindado. En la ejecución experimental agradecemos la cooperación de Milton Choque, Dora Cruz, Carolina Paredes, y Betty Quisbert.
REFERENCIAS
1. Amaral, J.S., Casal, S, Pereira J.A., Seabra, R.M., Oliveira, B.P. 2003, Determination of Sterol and Fatty Acid Compositions, Oxidative Stability, and Nutritional Value of Six Walnut (Juglans regia L.) Cultivars Grown in Portugal, Journal of Agricultural and Food Chemistry. 51, 7698-7702. [ Links ]
2. Augstburger, F., Berger, J. Agricultura Orgánica en el Trópico y Subtrópico. 1ra ed. Alemania; Asociación Naturland; 2000, pp. 1-3. [ Links ]
3. Casp, A., April, J.. Procesos de conservación de alimentos. 1999, Madrid: Ediciones Mundi-Prensa. [ Links ]
4. Kuntz, L.. Accelerated shelf life testing. 1991, Nueva York, Weeks Publishing Co. [ Links ]
5. Wasowicz, E., Gramza, A., Hêz, M., Jelen, H.H., Korczak, J., Melecka, M., Mildner-Szkudlarz, S., Rudzinska, M., Samotyja, U., Zawirska-Wojtasiak, R.. 2004, Polish Journal of Food and Nutrition Sciences, 13 (54), SI 1, pp. 87-100. [ Links ]
6. Su Chuen Ng. Effects of accelerated aging on lipid oxidation in Quinoa "Chenopodium quinoa" ,2003, MSc degree dissertation, University of Winsconsin, Stout. [ Links ]
7. Frankel, E.N.: In: Search of better methods to evaluate natural antioxidants and oxidative stability in food lipids. Trends Food Sci. Technol. 4,1993, pp. 220-225. [ Links ]
8. Ragnarsson, J.O., Labuza, T.P. 1977, Accelerated shelf-life testing for oxidative rancidity in foods- a review. Food Chem. 2 291-308. [ Links ]
9. Frankel, E.N. Lipid Oxidation. The Oily Press, Dundee (UK) 1998. [ Links ]
10. Kaya, A., Tekin, A.R., Öner, M.D. 1993, Oxidative stability of sunflower and olive oils: Comparison between a modified active oxygen method and long term storage. Lebensm.-Wiss. u. Technol. 26, 464-468. [ Links ]
11. Kowalski, B., Gruczynska, E., Maciaszek, K. 2000, Kinetics of rapeseed oil oxidation by pressure differential scanning calorimetry measurements. Eur. J. Lipid Sci. Technol. 102, 337-341. [ Links ]
12. Wenjiao F., Yongkui Z., Yunchuan C., Junxiu S., Yumen Y. 2014, TBARS predictive models of pork sausages stored at different temperatures. Meat Science, 96, 1-4. [ Links ]
13. Labuza, T.P.; Riboh, D. 1982, Theory and application of Arrhenius kinetics to the prediction of nutrient losses in foods. Food Technol., 36 (10), 66-74. [ Links ]
14. Boekel M. 2008, Kinetic modeling of food quality: a critical review. Comprehensive Reviews in food Science and Food Safety, 7,144-158. [ Links ]
15. González, F., Extracción de aceite de quínoa (Chenopodium quinoa Willd), proveniente de la Palmilla y Paredones y su posterior caracterización físico- química. 2005, Memoria para optar al título de Ingeniero en Alimentos. Santiago, Universidad de Chile. [ Links ]
]]>