CUANTIFICACION DE ALMIDON TOTAL Y DE ALMIDON RESISTENTE EN HARINA DE PLATANO VERDE (MUSA CAVENDISHII) Y BANANA VERDE (MUSA PARADISÍACA)
Vania Soraya Soto Azurduy
Universidad Mayor de San Simón, Facultad de Bioquímica y Farmacia, Cochabamba Bolivia
Keywords: Cuantificación, método enzimático, almidón total, almidón resistente
ABSTRACT
The present work is oriented to the quantification of resistant starch in banana and green banana flour using the enzymatic in vitro method, in this method a series of specific amiolitic enzymes participate to digest starch obtaining precise, fast potent and cost-effective results, in the evaluation of the resistant starch. The method used for the determination of total starch in banana and green banana flours was Holms, the main steps include: enzymatic degradation with α-amilasa Termamyl 120 L, which results in a partial hydrolysis, 30 minutes incubation with amyloglucosidase from Aspergillus niger obtaining a total hydrolysis. Finally determination of glucose was done with a glucose oxidase and peroxidase reagent. Quantification of resistant starch in banana and green banana flour was done using the Goñi I. method, initially an proteic hydrolysis with pespsine under acid pH conditions was carried out to simulate stomach physiologic conditions, the remotion of proteins increases α-amylasa accessibility. Digestible starch hydrolisis was followed with swine pancreatic α-amylase during 16 hours at neutral pH. After centrifugation hydrolysis products were eliminated, in the residue the indigestible starch remained. Finally was dispersed in a basic medium and totally hydrolyzed with Aspergillus niger amyloglucosidase, measuring the free glucose with a glucose oxidase and peroxidase reagent. The experimental results showed that the green banana (Musa paradisiaca) presented higher amount of total starch (73,42 %) and resistant starch (24,82 %) . A comparison with the green banana flour (Musa cavendishii) which show total starch (68,13 %) and resistant starch (21,06 %) was done. The test were done with six repetitions in each sample and each experimental method, a control sample of starch was used. Concluding that banana (Musa cavendishii) and green banana (Musa paradisiaca) are a good source of resistant starch which is very important and beneficial to the health and its use must be encouraged of these fruits natives from the region.
Corresponding author:
RESUMEN
]]> El presente trabajo está orientado a cuantificar el almidón resistente en harina de plátano y banana verde utilizando el método in vitro enzimático, en el cual participan una serie de enzimas amilolíticas específicas para la digestibilidad del almidón teniendo los beneficios de obtener resultados más precisos y confiables. El método para la determinación de almidón total en las harinas de plátano y banana verde fue el de Holm J.; entre los pasos principales incluyen la degradación enzimática del almidón con la presencia de una α-amilasa Termamyl 120 L dando una hidrólisis parcial y también una incubación con amiloglucosidasa de Aspergillus niger por 30 minutos consiguiendo así una hidrólisis total. Subsecuentemente determinación de glucosa con el reactivo de glucosa oxidasa/peroxidasa.4 Para la cuantificación de almidón resistente en harina de plátano y banana verde se utiliza el Método de Goñi I. ; que contempla primeramente una hidrólisis proteica con pepsina a pH ácido para simular las condiciones fisiológicas estomacales, la remoción de proteínas aumenta la accesibilidad de la α-amilasa. Seguida de la hidrólisis del almidón digestible con α-amilasa Pancreática Porcina durante 16 horas. Tras una centrifugación se eliminan los productos de hidrólisis, en el residuo permanece la fracción de almidón indigestible, se dispersa en medio alcalino e hidroliza en su totalidad con amiloglucosidasa de Aspergillus niger determinándose la glucosa liberada con un reactivo de glucosa oxidasa/peroxidasa.5 Los resultados de la parte experimental muestran que la harina de banana verde (Musa paradisíaca) presenta mayor cantidad de almidón total (73,42%) y de almidón resistente (24,82%) en comparación con la harina de plátano verde (Musa cavendishii) que presenta resultados de almidón total (68,13%) y de almidón resistente (21,06%) siendo mas bajos.Las pruebas se realizaron con seis repeticiones en cada muestra y en cada método experimental, además, se trabajó con muestra control. Llegándose a la conclusión de que el plátano (Musa cavendishii) como la banana verde (Musa paradisíaca) representan una buena fuente de almidón resistente que pueden ser aprovechados en la preparación de diversos productos propios de la región.
INTRODUCCION
El plátano es una fruta que se consume bastante en países del Caribe, Centroamérica, y Sudamérica. En Bolivia, sobre todo, se cultiva en la zona oriental, en chapare de Cochabamba, en Alto Beni, en los Yungas y Caranavi de La Paz, con una producción anual bastante alta. El plátano maduro es un alimento muy nutritivo, cuenta con gran cantidad de hidratos de carbono dotando de energía a nuestro organismo por su rápida digestión, su riqueza de potasio ayuda a la eliminación de líquidos y por lo tanto, ayuda a mejorar la hipertensión arterial, además de contener magnesio, ácido fólico, la vitamina C combinada con su riqueza en fósforo resulta ideal para el fortalecimiento de la mente, también contiene sustancias de acción astringente por la cantidad de taninos, sin despreciar su elevado aporte de fibra.1 El plátano y la banana verde contienen una elevada cantidad de almidón resistente, las investigaciones reportan que es muy beneficioso por sus efectos fisiológicos en el organismo como disminución del tiempo de tránsito intestinal, reducción de glucosa en sangre y consecuentemente, la cantidad del nivel de colesterol. El almidón resistente en el proceso de digestibilidad en un individuo sano no se absorbe en el intestino y sirve de alimento para las bacterias duodenales beneficiosas, esta digestión es muy similar a la proporción soluble de la fibra dietética. 2,3 El almidón resistente puede ser considerado como un ingrediente funcional que aumenta la calidad de los alimentos. Se lo llama así porque resiste a la digestión por parte de las enzimas amilolíticas y llega integro al intestino donde es fermentado por las bacterias duodenales, esta resistencia a la hidrólisis puede ser explicada por varios factores como grado y tipo de cristalinidad del grano de almidón, contenido de amilosa, morfología del gránulo, la presencia de complejos almidón-lipídico y almidón-proteína.2 Debido a los beneficios que trae el conocimiento sobre este almidón resistente, es importante hacer hincapié en el presente trabajo de cuantificar la cantidad de almidón resistente en dos variedades de plátano verde de la región mediante la utilización de métodos enzimáticos in vitro para obtener resultados con con precisión y rapidez.De esta manera es importante potencializar sus efectos benéficos con el fin de mejorar el estado de salud de la población en general y aportar alternativas para la prevención y control de enfermedades.
RESULTADOS
Valores de composición nutricional en dos variedades de harinas de plátano verde
Las dos variedades de harinas de plátano verde obtenidas fueron sometidas a análisis de composición nutricional básico.

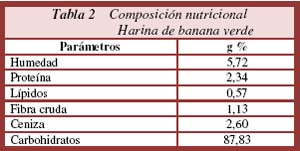
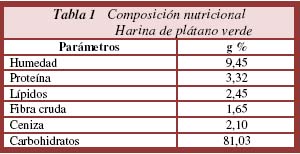
]]> En la Tabla Nº 1 y Tabla Nº 2 se presenta la composición nutricional de ambos tipos de harina, siendo la harina de banana con mayor cantidad de carbohidratos totales (87,83 %) en comparación con la harina de plátano (81,03%)
Porcentaje de medias de Almidón Total (AT), Almidón Disponible (AD) y Almidón Resistente (AR) en harina de plátano y banana verde
En la Tabla Nº 3 se obtuvieron los siguientes resultados de Almidón Total (AT), Almidón Disponible (AD) y Almidón Resistente (AR) en dos variedades de harinas de plátano y banana verde realizándose seis repeticiones. El contenido de Almidón Disponible se obtuvo de una diferencia entre los resultados de Almidón Total y de Almidón Resistente.
Los resultados obtenidos de harina de plátano verde fueron representados a través de diagramas de columnas, donde se muestra el porcentaje de Almidón Total, Almidón Disponible y Almidón Resistente (Figura Nº 1) de acuerdo a la Tabla Nº 3. Los resultados obtenidos de harina de banana verde fueron representados a través de diagramas de columnas, donde se muestra el porcentaje de Almidón Total, Almidón Disponible y Almidón Resistente (Figura Nº 2) de acuerdo a la Tabla Nº 3
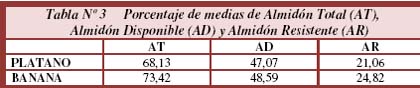
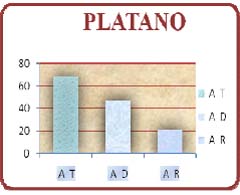
Figura Nº 1 Porcentaje de Almidón Total (AT), Almidón Disponible (AD) y Almidón Resistente (AR) en harina de plátano verde
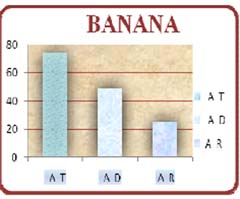
Figura Nº 2 Porcentaje Almidón Total (AT), Almidón Disponible (AD) y Almidón Resistente (AR) en harina de banana verde
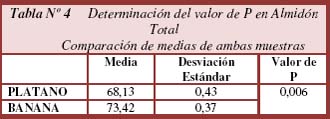
]]> Determinación del valor de P en Almidón Total, Almidón Disponible y Almidón Resistente por comparación de medias obtenido de harinas de plátano y banana verde.En la Tabla Nº 4 se realizó el test - student de comparación de medias entre harina de plátano y banana verde con los datos obtenidos de Almidón Total, determinándose el valor de P (£ 0,05). La desviación estándar es el grado de dispersión del valor de la media, de acuerdo a los datos obtenidos los valores de Desviación Estándar son muy bajos lo cual refleja la precisión de los análisis. Para esta aplicación el valor de P estadísticamente es significativo, es decir ambas medias tienen diferencia significativa entre si. Por lo tanto podemos decir que el Almidón Total contenido en la banana verde a comparación con el plátano verde difiere significativamente. En la Tabla Nº 5 se realizó el test - student de comparación de medias entre harina de plátano y banana verde con los datos obtenidos de Almidón Disponible determinándose el valor de P (£ 0,05).
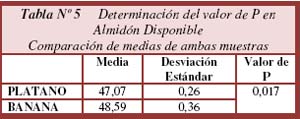
La desviación estándar es el grado de dispersión del valor de la media, de acuerdo a los datos obtenidos los valores de Desviación Estándar son muy bajos lo cual refleja la precisión de los análisis. Para esta aplicación el valor de P estadísticamente es significativo, es decir ambas medias tienen diferencia significativa entre si. Por lo tanto podemos decir que el Almidón Disponible contenido en la banana verde a comparación con el plátano verde difiere significativamente.
En la Tabla Nº 6 se realizó el test - student de comparación de medias entre harina de plátano y banana verde con los datos obtenidos de Almidón Resistente determinándose el valor de P (£ 0,05).

La desviación estándar es el grado de dispersión del valor de la media, de acuerdo a los datos obtenidos los valores de Desviación Estándar son muy bajos lo cual refleja la precisión de los análisis. Para esta aplicación el valor de P estadísticamente es significativo, es decir ambas medias tienen diferencia significativa entre si. Por lo tanto, podemos decir que el Almidón Resistente contenido en la banana verde en comparación con el plátano verde difiere significativamente.
]]> DISCUSIONLos resultados obtenidos en la composición nutricional de ambas variedades de plátano verde refleja elevada cantidad de carbohidratos totales (81-87%), una interesante cantidad de proteínas (2-3%) debido a que es una fruta y un buen aporte en minerales (2% de ceniza). Realizando un análisis de resultados obtenidos de Almidón Total (73%), se asemejan a los resultados obtenidos por Pacheco-Delahaye, 2001 en Venezuela con la misma variedad de Musa paradisiaca (81%), teniendo este ultimo trabajo algunas variaciones en el método utilizado para la determinación de Almidón Total como por ejemplo enzimas de diferente industria, menor tiempo de hidrolizado.2 Los resultados obtenidos de Almidón Resistente (21-24%), difieren un poco con los resultados obtenidos por Pacheco-Delahaye, 2001 con la misma variedad de harina (14%), teniendo diversificaciones en el método utilizado como diferente concentración de algunos reactivos, enzimas de diferente industria.2 Al realizar la comparación de medias en Almidón Total con el test - student y determinando el valor de P £ 0,05; se define que sus diferencias entre ambas variedades de plátanos, son altamente significativas, es decir ambas medías tienen diferencia significativa entre si por el valor de P £ 0,006. Respecto a la comparación de medias en Almidón Disponible con el test - student y determinando el valor de P £ 0,05; se define que sus diferencias entre ambas variedades de plátanos son altamente significativas, es decir ambas medías tienen diferencia significativa entre si por el valor de P £ 0,017. En relación a la comparación de medias en Almidón Resistente con el test - student y determinando el valor de P £ 0,05; se define que sus diferencias entre ambas variedades de plátanos son altamente significativas, es decir ambas medías tienen diferencia significativa entre si por el valor de P £ 0,007
SECCION EXPERIMENTAL
Tipo de estudio
El presente trabajo de investigación corresponde al tipo de estudio Analítico cuantitativo.
Las características y condiciones del problema de la investigación, están enmarcados en un estudio de carácter cuantitativo porque se determinó la cantidad de almidón total y de almidón resistente en harinas de plátano y banana verde procedentes de Cochabamba, tomando en cuenta que el almidón resistente no se digiere en el intestino y actúa como prebiótico para las bacterias duodenales beneficiando de esta manera a la salud gastrointestinal.
Desde el punto de vista metodológico el estudio cuantitativo, permite realizar un análisis a través de la medición, de la cantidad y el porcentaje de los datos obtenidos y posteriormente realizar una interpretación y comparación de los resultados.
Análisis estadístico
Se realizó análisis de varianza para determinar las diferencias significativas entre las medias de los procedimientos, los cuales fueron obtenidos de seis repeticiones, con un nivel de significancia de P £ 0.05
Se trabajó con el software de PC, utilizando el programa estadístico SPSS 15, para calcular las siguientes medidas estadísticas:
]]> · Media x· Desviación Estándar DE
Los resultados obtenidos fueron representados a través de diagramas de columna.
Cuantificación del contenido de almidón total mediante Método de J. Holm y colaboradores en las dos variedades de harina de plátano verde
Este método permite determinar la cantidad de almidón total de una muestra, con una disponibilidad completa del almidón a la degradación enzimática, en este procedimiento la etapa de gelatinización y licuefacción se realizó al mismo tiempo.
Se utilizó enzima Termamyl 120 L (α-amilasa termoestable. Industria Novo Nordisk, Dinamarca.) ; enzima amiloglucosidasa de Aspergillus niger NºA7420 Polvo liofilizado, 30-60 unidades / mg de proteína. Industria Sigma Aldrich; Reactivo enzima Glucosa Oxidasa / Peroxidasa Glox - Novum. Industria Kabi Diagnóstica; almidón soluble P.A. Nº 101252. Industria Merck Chemicals como control para la prueba.
Se utilizó el siguiente protocolo para la obtención y cuantificación del almidón total: 4
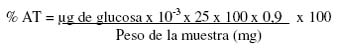
Este método determina la presencia de almidón resistente en los alimentos y aparenta en lo más posible las condiciones fisiológicas estomacales. Los propósitos principales de este procedimiento analítico son: eliminación de la proteína, eliminación del almidón digerible, solubilización e hidrólisis enzimática del almidón resistente; y la cuantificación del almidón resistente como glucosa liberada x 0,9. Se utilizó enzima pepsina de Mucosa Gástrica de Cerdo Nº107185 industria Merck Chemicals. 0.70 FIP-U/mg ajustado con sacarosa; enzima α-amilasa Pancreática Porcina NºA3176 Tipo VI-B, ≥ 10 unidades / mg. Industria Sigma Aldrich; enzima amiloglucosidasa de Aspergillus niger NºA7420 Polvo liofilizado, 30-60 unidades / mg de proteína. Industria Sigma Aldrich; reactivo enzima Glucosa Oxidasa / Peroxidasa Glox - Novum. Industria Kabi Diagnóstica. Se utilizó el siguiente protocolo para la obtención y cuantificación del almidón resistente: 5
![]()
REFERENCIAS
1 BOTANICAL ONLINE SL .Características de los plátanos los plátanos unas hierbas muy valiosas. Revista de Botánica [revista en internet] 2010. [acceso 25 de abril de 2010]. Disponible en: http://www.botanical-online.com/index.html [ Links ]
2 Pacheco D. E. Evaluación nutricional de sopas deshidratadas a base de harina de plátano verde. Digestibilidad in vitro del almidón. Acta Científica Venezolana. 2001; 52:283-291. [ Links ]
3 CRECES. Los alimentos y la salud, a la luz de los conocimientos actuales. Publicado en Revista Creces del Instituto de Nutrición de Venezuela [revista en internet]. 1998. [acceso 10 de marzo de 2009]. Disponible en: http://www.creces. cl/new/index.asp?tc=3&nc=2&imat=%20%20>%20%2068>68&art=68 [ Links ]
4 Holm J, Bjorck I, Drews A, Asp N-G. Un método rápido para el análisis de almidón. 1986; 38:224-226 [ Links ]
5 Goñi I, García-Díaz L, Mañas E, Saura-Calixto F. Análisis de almidón resistente: un método para alimentos y productos alimenticios. Revista de Química Alimenticia. 1996; 56: 445-449. [ Links ] ]]>