UNA VISION A LOS PROCESOS DE HIDRÓLISIS DE ELEMENTOS BIMETALICOS DE TRANSICION A PARTIR DEL MODELO DE CARGA PARCIAL
Agno Nilthon, Crespo Pedro, Cabrera Saúl
Laboratorio de Sólidos y Química Teórica
Instituto de Investigaciones Químicas (I.I.Q.), FCPN-UMSA
Campus Universitario, Cota-Cota.Calle Nro.27
Teléfono 591 2 795878 , Fax 591 2 772269 ]]>
RESUMEN
Se discute la aplicación del modelo de carga parcial propuesta por Livage (6) en las reacciones de hidrólisis para elementos bi - metálicos de transición demostrándose su coherencia para Mn, Fe, Co y Ni, y no así para Cu y Zn.
ABSTRACT
The application of the partial charge model, proposed by Livage is discussed. Application regards hydrolysis reactions for transition bi-metalic elements. Coherence for Mn, Fe, Co and Ni, was demonstrated, but no regularity was observed for Cu and Zn.
INTRODUCCIÓN
]]> Una de las rutas de síntesis de materiales mas ampliamente desarrolladas es la sol – gel, dicho proceso permite producir materiales con actividades ópticas, térmicas, eléctricas , mecánicas y químicas interesantes (1). En efecto, es importante mencionar que la productos industriales basada en procesos sol gel cubre una gran parte del mercado de materiales (2), otro gran campo de aplicabilidad de estos materiales sintetizados por esta ruta es los materiales catalíticos (3), para lo cual uno de los requisitos mas importantes es la obtención de materiales mixtos de dos o mas elementos (4), donde la presencia de los mismos permiten favorecer su actividad catalítica. La química de los procesos sol - gel esta basada en reacciones de hidroxilación y condensación de precursores moleculares, existiendo actualmente dos rutas claves, una a partir de precursores inorgánicos (sales metálicas), y la otra a partir de precursores organometalicos (5). El estudio de los procesos de hidrólisis y condensación en sistemas acuosos para iones metálicos de transición, a partir de sales inorgánicas ha sido uno de los temas de más interés para los químicos (5), en este sentido es importante comprender y proponer las especies primogéneas que son claves para los procesos de hidrólisis y condensación, de hecho Livage et al (6), desarrollan el modelo de carga parcial que permite proponer las especies precursoras en los procesos de hidrólisis, en función al pH de la solución. Este modelo, si bien permite sugerir dichas especies, ha sido todavía poco aplicado a resultados experimentales (7-10), en el presente trabajo se discute la posible aplicación del modelo en los procesos de hidrólisis de metales de transición divalentes, como son el Mn, Fe, Co y Ni.
PARTE EXPERIMENTAL
Se ha realizado la hidrólisis de sulfatos de los diferentes metales de transición divalentes (M = Mn, Fe, Vo, Ni, Zn, Cu), a partir de una solución, 0.25 M, con solución de NaOH 0.5 M., realizando un control del pH cuidadoso, hasta una relación molar OH/M = 2.5, en todos los casos la temperatura fue de 17°C. Para cada volumen de base adicionada se realizo una agitación continua de 3 minutos hasta no existir variación en el pH.
RESULTADOS Y DISCUSIÓN
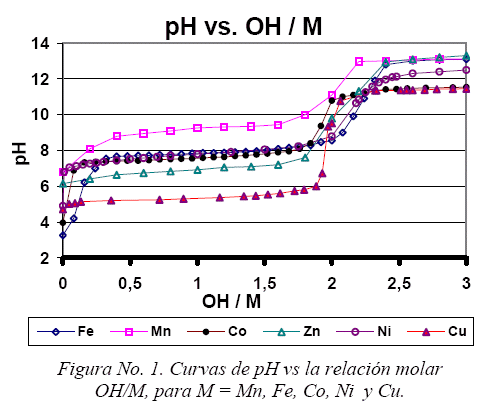
El comportamiento de las curvas de pH vs la proporción OH/M muestra un comportamiento típico de una reacción ácido - base, como se muestra en la figura No. 1, donde se observa claramente el punto equivalente en el punto de inflexión. Adicionalmente se puede identificar tres zonas importantes, la primera, la de pH inicial (OH/M = 0), en donde se encuentran las especies de partida parcialmente hidrolizadas dependiendo de las características del elemento, una segunda, que corresponde para 0 < OH/M < 2, donde se observa el incremento del pH hasta un valor casi constante, este comportamiento es producido por la neutraliza inicialmente los protones generados por la hidrólisis inicial del aquo complejo, el posterior comportamiento constante demuestra la hidrólisis y posterior hidrólisis y condensación de los complejos, en donde ocurre la precipitación, la tercera zona corresponde a un incremento violento del pH y una posterior estabilización del pH, la cual es consistente con el hecho de que bajo estas condiciones de relación molar OH/M mayores a 2, se tiene la presencia de exceso de oxidrilos.

Procesos de hidrólisis según el modelo de carga parcial:
]]> Las sales inorgánicas de metales de transición del primer periodo, presentan una alta solubilidad en agua, esta característica es función en gran medida del carácter fuertemente iónico entre el metal y el radical, de hecho esto permite que la entalpía de disolución sea favorable al proceso. En este sentido los iones metálicos existentes en un medio acuoso son solvatados por moléculas de agua, generándose aquo – iones (M(OH2)n)z+, en estas condiciones, de acuerdo a la teoría de iones blandos y duros (ref), se puede proponer que existe una transferencia de densidad de carga eléctrica desde el par solitario del oxigeno sobre los orbitales d vacíos del ion metálico (enlace σ M-OH2), esta transferencia será específicamente desde el orbital molecular enlazante 3a1 de la molécula de agua. Esto conduce a un debilitamiento de los enlaces σ O-H dentro de la molécula de agua, de hecho dependiendo del carácter duro del ion metálico (la dureza incrementa al incrementar la carga del ion y al disminuir su radio) se puede llegar a la ruptura de este enlace, generándose la desprotonación en diferentes grados, e incluso generándose la formación de especies oxo metalicas M= O. La reacción que define estos procesos es:![]()
donde h = es la proporción de hidrólisis
Según Livage et al. (6), la electronegatividad media Xp del precursor hidrolizado [ M(OH)h(OH2)n-h] (z-h)+ , depende del cation metálico Mz+ y de la proporción de la hidrólisis h ). En este sentido también, se debe considerar en función al principio de igualación de las electronegatividades de las especies en solución de R. T. Sanderson, el cual plantea que: “cuando dos o más átomos inicialmente con diferentes electronegatividades se combinan, estos tienden a ajustarse a una electronegatividad media en el compuesto”, por tanto considerando que en los procesos de hidrólisis y condensación un factor clave es la presencia en el medio de H+, es decir el pH, esto permite proponer que la interacción del H+ con el agua variara la electronegatividad media del sistema en función del pH, con la formación de especies H3O+, y (H2O―H―OH2)+, la ecuación que rige este comportamiento esta dado por la expresión (ref):
![]()
A partir del modelo de carga parcial, se puede asumir que el intercambio protónico entre el precursor [ M(OH)h(OH2)n-h] (z-h)+ y el agua, conduce a que las electronegatividades medias del precursor Xh y de la solución acuosa Xw se igualen: Xh = Xw, siendo posible, como lo propone Livage(6), calcular la proporción de hidrólisis h en función del pH, por medio de las siguientes ecuaciones:
![]()
donde la carga parcial δi es dada por:
![]()
donde la escala de electronegatividades utilizada es la de Allred – Rochow (126 – 128).
]]> En la tabla No. 1, se da los resultados de la carga parcial encontrados para diferentes elementos metálicos de transición bivalentes, donde se observa que en función a las características de los elementos (radio iónico, densidad de carga, electronegatividad), estos presentan en general una disminución del valor de la carga parcial con forme incrementa el pH, y la comparación entre los elementos del mismo periodo, muestra que hay un disminución hasta el Ni, el cual se constituye en un punto de inflexión donde posteriormente se incrementa. Esto permite dividir el comportamiento en dos grupos, el primero desde el Mn hasta el Ni, y el segundo el del Cu y Zn.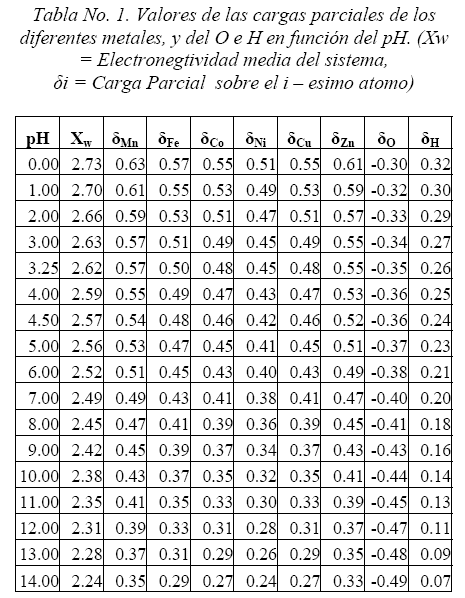
A partir de los resultados dados en la tabla anterior y en base al modelo de carga parcial de Livage et al (6) (ecc. 2), se ha calculado la proporción de hidrólisis, como se muestra en la siguiente tabla (Tabla No. 2):
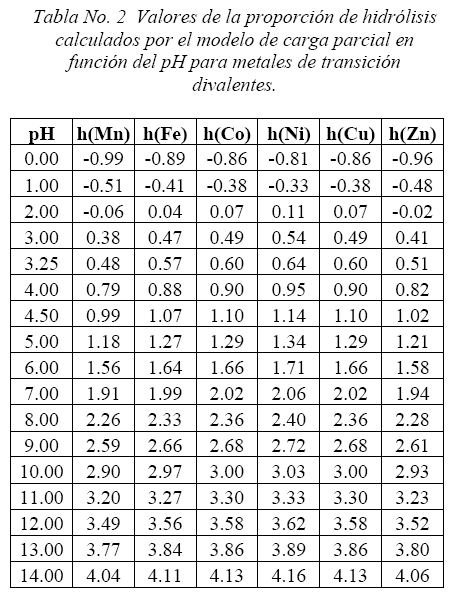
La figura No. 2, de pH vs. Relacion molar de OH/M, permite identificar el pH inicial (relacion molar inicial OH/M = 0.00), y a partir de ellos la proporción de hidrólisis a estos pH (tabla No. 2), como las especies presentes al iniciar el proceso de hidrolisis:
El análisis inicial de la proporción de hidrólisis da la impresión de que no existe una adecuada correlación entre el pH y la proporción de hidrólisis, no obstante el comportamiento de los valores de densidad de carga del metal obtenidos en estas condiciones son consistentes con los valores de electronegatividad del metal, como con la relación carga / radio del metal (que representa en cierto sentido la dureza de cada elemento), de hecho se observa que la densidad de carga del metal disminuye hasta el níquel, donde posteriormente incrementa, este comportamiento es consistente con el hecho de que cuanto mayor la electronegatividad del elemento, mayor será la densidad de carga que el elemento atraerá en sus enlaces con el oxigeno del oxidrilo o de las moléculas de agua de su primera esfera de coordinación, adicionalmente se puede observar que el Mn+2 puede ser considerado como el más duro y dado que el H2O como el OH son considerados también como duros, el carácter de enlace en este aquo complejo serán mas fuertes, es decir de mayor carácter iónico y fáciles de formar, tendiéndose a producir una mayor proporción de hidrólisis, no así en los demás elementos considerados como elementos intermedios entre duros y blandos, consecuentemente la interacción con el OH o el H2O es de fuerza intermedia, existiendo una buena correlación entre el comportamiento de la dureza y la proporción de hidrólisis.
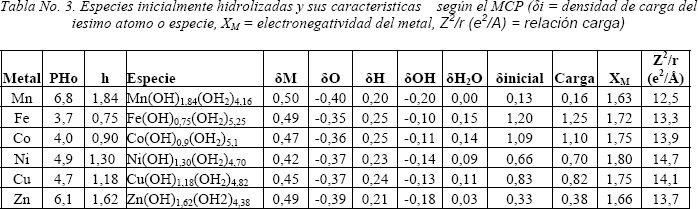
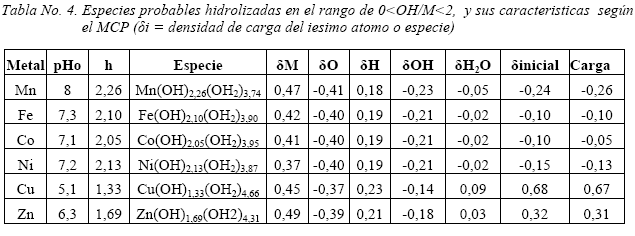
En la tabla No. 4, se observa las especies mas probables propuestas por el modelo de Livage para la zona 2 del proceso de hidrólisis y condensación de los metales de transición bivalentes, específicamente en la zona donde el pH no presenta grandes cambios, este comportamiento consistente con el proceso de condensación. Se puede identificar primero al Mn, el cual presenta una proporción de hidrólisis h = 2,26 mucho mayor a dos, esto sugiere que dentro de los elementos estudiados en este periodo realmente su alta electronegatividad y baja dureza de este elemento favorece en gran medida su hidrólisis, en un siguiente grupo se puede identificar al Fe, Co y Ni, los cuales presentan evidentemente un comportamiento casi similar, donde la especie lista para el proceso de condensación puede ser identificada como la con h aproximadamente 2,1, esto implica especies con la presencia de 2 oxidrilos por ion metálico, lo que implica que estas especies tienen carga cero, y están preparadas para producir la condensación. Finalmente, el caso del Cu y Zn, estos dos elementos muestran que las especies presentes no están completamente hidrolizadas, esto es por que los orbitales d están casi llenos, y esto produce un incremento en el radio iónico, el cual en los otros elementos del mismo periodo va disminuyendo, esto favorece la blandura del ion y por ende desfavorece la fuerza de enlace con el OH.
]]>
CONCLUSION
Se puede concluir que el modelo de carga parcial de Livage, permite proponer ciertas especies para la hidrólisis y condensación, las cuales son consistentes con el pH experimental, a excepción del Cu y Zn, para las cuales se plantea especies parcialmente hidrolizadas, esta anomalía es originada por el cambio del radio en la serie de los elementos metálicos bivalentes, y por lo tanto en sus propiedades blando – duro, que son consistentes con su acidez de dichos elementos.
BIBLIOGRAFÍA
[1]. C. Frie, G. Vincent, W. Finzel, J. Am. Chem. Soc., 1971, 93, 6805. [ Links ]
[2]. Sumio Sakka, Journal of sol – gel Science and Technology, Vol. 1, No. 1, 1993, 5
[3]. Chandler C., Roger C., Hampden-Smith M., Chem. Rev. , 1993, 93, 1205. [ Links ]
[4]. Mehrotra R., Rai A., Polyhedron, 1991, 10, 1967. [ Links ]
[5]. Naiini A., Ying J., Angew. Chem. Int. Ed. England, 1995, 34, 393. [ Links ]
[6]. J. Livage, M. Henry, C. Sánchez, Progr. Solid State Chem. 18 (1988) 259) [ Links ]
[7]. Bickmore C., Laine R., J. Am. Chem. Soc., 1996, 79, 2865. [ Links ]
[8].. C. Frye, G. Vogel, J. Hall, J. Am. Chem. Soc., 1961, 83, 996 [ Links ]
[9]. Verkade J. G., Acc. Chem. Res., 1993, 26, 483. [ Links ]
[10]. Pinkas J., Verkade J., Inorg. Chem., 1993, 32, 2711. [ Links ]
]]>