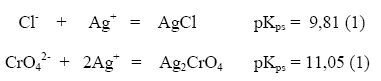
REVISION EXPERIMENTAL DEL INTERVALO DE pH PARA LA DETERMINACIÓN DE CLORUROS POR EL METODO DE MOHR
Galia Chávez Cury
Instituto de Investigaciones Químicas - Carrera de Ciencias Químicas - FCPN - UMSA
A revision of experimental pH titration range has been carried out in order to determine chloride ions in solutions containing 0,0100 M chloride and silver ions using the Mohr Method.
]]> Volumes at equivalent point obtained by potentiometry were compared with final volumes corrected against a blank at given pH values.Analysis of results, gave 1,67 % to 1,76 % as error in the measurements at the pH range between 6,0 y 9,0. However better results can be achieved with 1,50 % of error at the range from 7,0 to 8,0
Key words: Mohr Method, Potentiometry.
RESUMEN
Se realizó una revisión experimental del intervalo de pH de titulación, para determinar iones cloruros en soluciones que contienen 0,0100 M de iones cloruros e iones plata utilizando el Método de Mohr.
Se compararon volúmenes del punto equivalente obtenidos por potenciometría con los volúmenes del punto final corregidos con respecto al blanco a valores de pH dados.
Los análisis de resultados, dieron 1,67 % a 1,76 % como error en las medidas en el intervalo de pH entre 6,0 y 9,0. Sin embargo mejores resultados pueden ser logrados con un error de 1,50 % en el intervalo de 7,0 a 8,0
INTRODUCCION
]]> El Método de Mohr, es una de las técnicas volumétricas más antiguas, e involucra la titulación de cloruros y/o bromuros con una solución valorada de nitrato de plata, empleando como indicador cromato de potasio (1). El Método en general es utilizado para la determinación de cloruros no sólo en cantidades relativamente grandes sino también en cantidades pequeñas, como las contenidas en el agua, en cuyo análisis se utiliza profusamente (2)El Método consiste en una titulación por precipitación a temperatura ambiente de disoluciones generalmente de cloruros, con disolución valorada de nitrato de plata 0,1000 M, formando un precipitado blanco poco soluble de cloruro de plata y empleando como indicador una disolución de cromato de potasio al 5 % m/v. En el punto final los iones cromato reaccionan con los iones plata formando un precipitado de color rojo anaranjado, escasamente soluble. La titulación se lleva a cabo dentro de un intervalo de pH determinado, este intervalo varía levemente dependiendo de los diferentes autores de libros. La determinación de cloruros por el Método de Mohr, es un caso típico de una precipitación fraccionada. Las reacciones que se llevan a cabo son las siguientes:
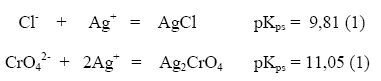
En este Método, la acidez de la solución resulta de primordial importancia. En soluciones ácidas, la concentración de iones cromato disminuye, pues reaccionan con los iones hidronios, produciéndose las siguientes reacciones (1):
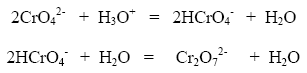
La solubilidad del bicromato de plata y del dicromato de plata es apreciablemente mayor que la del cromato de plata, de tal manera que para titular una solución ácida de cloruros, es necesario añadir mayor cantidad de iones plata y podría darse el caso de impedir por completo la precipitación del cromato de plata en medio ácido.
En soluciones demasiado básica se origina la siguiente reacción:
![]()
Con la cual precipita una considerable cantidad de plata como óxido, en vez de precipitar en las reacciones ordinarias de titulación de Mohr.
Algunos autores sugieren regular el pH a medio ligeramente ácido, con soluciones muy diluidas de ácido nítrico y para aumentar el pH, con soluciones diluidas de tetraborato de sodio.
]]> Este Método puede resultar rápido, además de preciso en las determinaciones de cloruros, sobre todo si se titulan bajo luz amarilla que permite una mejor visualización del punto final de la titulación.Los diferentes autores de libros hacen recomendaciones al respecto del intervalo de pH en la que se tienen que efectuar las titulaciones por el Método de Mohr, dichos intervalos se encuentran reportados en la Tabla Nº 1.

DISCUSION Y RESULTADOS, EXPERIMENTAL
Se prepararon soluciones estándar 0,0100 M de: cloruro a partir del cloruro de potasio p. a. e iones plata a partir de nitrato de plata p. a. También se preparó la solución de cromato de potasio al 5 % m/v.
Se realizaron las Titulaciones Potenciométricas a diferentes pH: 5, 6, 7, 8, 9 y 10, para los cual se midieron 50,00 ml de solución estándar de cloruro de potasio y se reguló el pH de trabajo con solución diluida de ácido nítrico (para bajar el pH) o solución diluida de tetraborato de sodio (para subir el pH).
En las titulaciones potenciométricas de cloruros se utilizó un pH-Metro Sargent-Welch Modelo LS, con escala de pH y de milivoltios. Se empleó como electrodo idicador, un electrodo de plata y como electrodo de referencia, un electrodo de plata-cloruro de plata. Para regular el pH, se empleo un electrodo de vidrio combinado (vidrio-calomel).
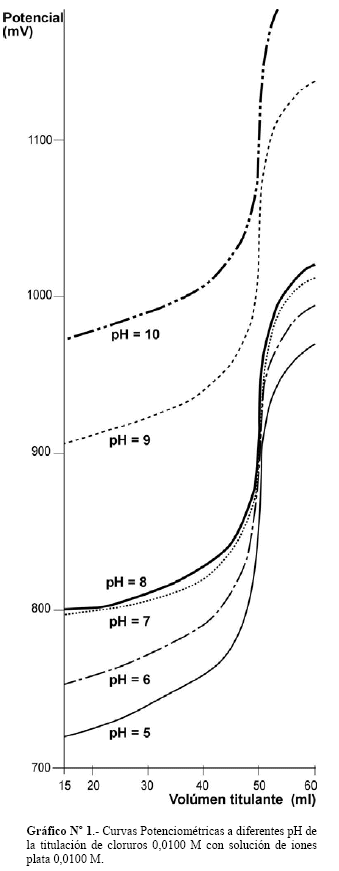
Se graficaron los datos de Potencial en mV en función de Volumen titulante en ml (Gráfico Nº 1).
]]>
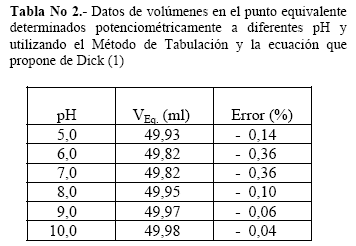
Se obtuviéron los volúmenes en el punto equivalente aplicando el Método de Tabulación y la ecuación para hallar el Volumen Equivalente, que propone Dick (1). Los volúmenes equivalentes (VEq.) calculados a diferentes pH se encuentran en la Tabla Nº 2.
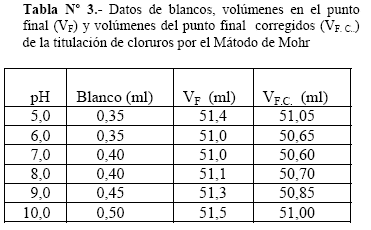
En la titulación volumétrica, se midieron también 50,00 ml de solución de cloruros 0,0100 M empleando 1,0 ml de indicador cromato de potasio al 5 % m/v (2). Estas titulaciones se efectuaron a los mismos pH en las que se realizaron las titulaciones potenciométricas. Se utilizó en el blanco para producir un efecto de enmascaramiento similar al del cloruro de plata, tierra silícea libre de cloruros, en lugar de carbonato de calcio. Los datos están reportados en la Tabla Nº 3
CONCLUSIONES
La Gráfica Nº 1 muestra las curvas de Titulación Potenciométrica de solución de cloruros 0,0100 M con iones plata 0,0100 M, en estas gráficas, se puede observar curvas bien definidas con saltos relativamente medianos alrededor del punto equivalente.
La Tabla Nº 2 muestra los volúmenes equivalentes experimentales de la titulación potenciométrica de cloruros a diferentes pH. También se observan los errores relativos, que fueron calculados comparando estos volúmenes con el volumen equivalente teórico para cada titulación que era de 50,00 ml. Los errores son menores al 0,40 %. Es importante indicar que los volúmenes equivalentes experimentales fueron determinados por duplicado y algunos por triplicado.
La Tabla Nº 3, muestra los datos experimentalmente de la titulación por el Método de Mohr, en ellos se puede notar que a pH 5 y pH 10, los volúmenes de reactivo titulante son mayores y los volúmenes de los blancos aumentan a medida que aumenta el pH. En esta Tabla también se muestran, los volúmenes del punto final corregidos (VF. C.) con respecto a los volumenes del blanco obtenido por el método de Mohr
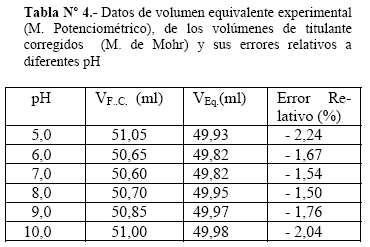
En la Tabla Nº 4, están los volúmenes equivalentes determinados potenciométricamente y los volúmenes finales corregidos, obtenidos por el método de Mohr. En estos datos, se puede notar que precisamente los volúmenes a pH 5,0 y pH 10,0 muestran errores mayores al 2,00 %. También se observa, que el intervalo de pH para realizar la titulación de cloruros por le Método de Mohr sería entre pH 6,0 y pH 9,0 con un error entre 1,67 % y 1,76 %. Sin embargo mejores resultados puede lograrse con un error del 1,5 % en el intervalo de pH entre 7,0 y 8,0.
REFERENCIAS
(1) Dick, J. G.: Química Analítica, 1ª ed., Editorial El Manual Moderno, S. A., México, 1979. [ Links ]
(2) Ayres, G. H.: Análisis Químico cuantitativo 7ª ed., Corporación Editora y Periodística, S. A., México, 1979. [ Links ]
(3)Vogel, A. I.: Química analítica Cuantitativa, Volumen 1, Editorial Kapelusz, Argentina, 1960. [ Links ]
(4) Skoog, D. A., West, D. M., Holler, F. J. y Crouch, S. R.: Fundamentos de Química Analítica, 8ª ed., Internacional Thompson Editores Spain, Madrid, España, 2005 [ Links ]
(5) Christian, G. D.: Química Analítica, 2ª ed., Editorial Limusa, México, 1981 [ Links ]
(6) Jackson, M. L.: Análisis Químico de Suelos, 3ª ed., Ediciones Omega, S. A., España, 1976. [ Links ]
]]>