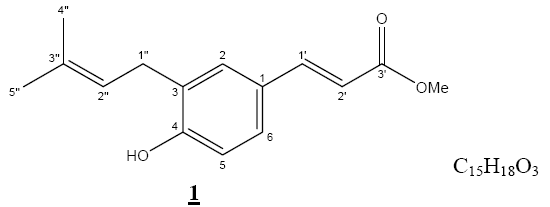
(E)-3-PRENIL-4-HIDROXICINAMATO DE METILO DE BACCHARIS SANTELICIS
J. R. Villagómez, Patricia Mollinedo, Giovanna R. Almanza*
Laboratorio de Productos Naturales, Instituto de Investigaciones Químicas, Carrera de Ciencias Químicas, Universidad Mayor de San Andrés, Campus Universitario de Cota Cota c. 27, La Paz, Bolivia
* Autor corresponsal: giovyalmanza@yahoo.com.ar
The research of the Bolivian plant Baccharis santelices gave the isolation of the esther methyl (E)-3-prenyl-4-hydroxycinamate, a derivative of p-coumaric acid with high antioxidant capacity (TEAC 3,4) comparable to the reference compound quercetine, which structure was identified by 1D and 2D NMR techniques. In addition, we identified oleanolic acid and stigmasterol, two common compounds in plants of the Bolivian Andean region.
Key words: BACCHARIS SANTELICIS, Asteraceae Compositae, coumaric acid derivatives, methyl (E)-3-prenyl-4-hydroxycinamate, antioxidant capacity, scavenger of free radicals
RESUMEN
La investigación de la especie Boliviana BACCHARIS SANTELICIS dio como resultado la obtención del ester (E)-3-prenil-4-hidroxicinamato de metilo (Plicatina B), un derivado del ácido p-cumarico con elevada capacidad antioxidante (TEAC 3,4) comparable al compuesto de referencia quercetina, cuya estructura fue elucidada por técnicas de RMN 1D y 2D. Adicionalmente, se identificó ácido oleanólico y estigmasterol, dos compuestos de presencia común en plantas de la región andina de Bolivia.
INTRODUCCION
La especie BACCHARIS SANTELICIS perteneciente a la familia Asteraceae o Compositae, es originaria de las altas montañas y punas del sur de Perú, oeste de Bolivia, norte de Chile y noreste de Argentina.[1]
Especies bolivianas del género Baccharis han sido estudiadas químicamente por su uso tradicional y alta disponibilidad física, determinándose en algunas de ellas, como B. drancunculifolia y B. obtusifolia, la presencia de derivados de ácido cinámico[2], [3]. En B. santelicis se identifico germacrano D, bicilogermacrano, espathulenol, algunos ent-clerodanos, cromenos y dos derivados del acido cinamico [4] .
]]> Los derivados del acido p-cumárico (ácido p-hidroxicinámico) pueden existir en dos formas isoméricas (cis Z o trans E), siendo la conformación trans la más común en la naturaleza por ser más estable [5]. Dentro de este tipo de derivados podemos encontrar al ester (E)-3-prenil-4-hidroxicinamato de metilo (Plicatina B) 1, aislado previamente en especies del género Baccharis y Psoralea [6,7].Estudios realizados de Plicatina B muestran que presenta actividad anti-microbiana, siendo el principio activo de la planta Psoralea Juncea [8], y actividad antimutagénica relacionada con la de los agentes antimutagénicos cinamil ester de Stirax asiatica [6]. Su actividad antimutagénica no es muy alta, pero su sencilla estructura promovió la obtención de análogos para estudios de estructura-actividad. Es así que tres análogos fueron sintetizados a partir del p-hidroxicinamato de metilo, el cual tras ser C-prenilado, fue derivado por saponificación, metoxilación del grupo fenol y reducción del ester a un alcohol. También se reporta la hidrogenación del doble enlace conjugado al ester realizada antes de la C-prenilacion. Todos los análogos obtenidos fueron sometidos a ensayos antimutagénicos concluyendo que todas las modificaciones realizadas disminuyen la actividad, exceptuando el producto con el doble enlace Δ1’,2’ hidrogenado que presentó mayor actividad que la Plicatina B y menor citotoxicidad [9, 10].
La actividad antimutagénica esta relacionada a las actividades antioxidante y anticancérigena, ya que las mutaciones pueden ser causadas por reacciones de oxidación de especies radicalarias de oxígeno, que a la larga pueden producir modificaciones genéticas y cáncer [11]. Por lo que en este trabajo se reporta la evaluación de la actividad antioxidante de los extractos de B. santelices así como del compuesto puro 1 mediante dos ensayos que evalúan su capacidad como atrapadores de radicales libres ABTS y DPPH. Además, se reporta por primera vez el aislamiento y elucidación estructural de Plicatina B (1) en una especie boliviana del género Baccharis. Finalmente, se muestra la presencia en esta especie vegetal de ácido oleanólico y el estigmasterol, dos compuestos de amplia distribución en el reino vegetal, particularmente en especies de la región andina de Bolivia. [12, 13]
RESULTADOS Y DISCUSIONES
El compuesto 1 fue aislado del extracto de acetato de etilo de las partes aéreas de B. santelices. Su estructura fue determinada mediante el análisis de datos de los espectros 1H-RMN, 13C-RMN, COSY H-H, HMQC y HMBC, de los cuales se indican los resultados en las tablas 1 y 2.

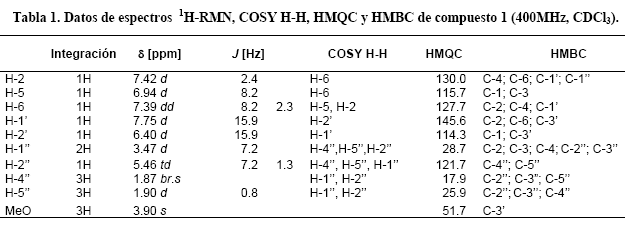
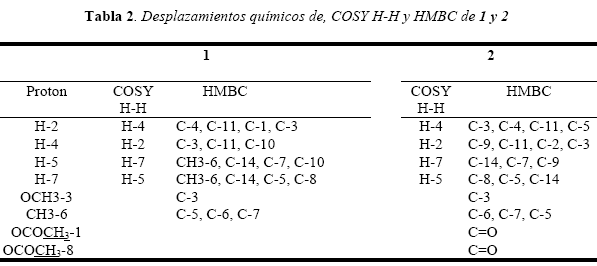
El espectro de RMN 1H muestra la presencia de 3 sistemas spin-spin: el primero corresponde a un grupo prenilo, el segundo a un grupo olefìnico α a carbonilo y el tercero a un sistema aromático ABX. Comenzando el análisis en campos altos se observa primero el sistema isoprenilado, con dos metilos desapantallados por la proximidad de un doble enlace, H-4” y H-5”, que muestran un acoplamiento alílico (J = 1.3 Hz) con el protón olefínico H-2”, el cual a su vez acopla vecinalmente con los protones metilénicos H-1” (J = 7.2 Hz), como se observa en la Figura 1. Adicionalmente se observan en el espectro COSY H-H correlaciones entre los metilos H-4’’ y H-5’’ con los protones metilénicos H-1’’ de carácter homoalílico.
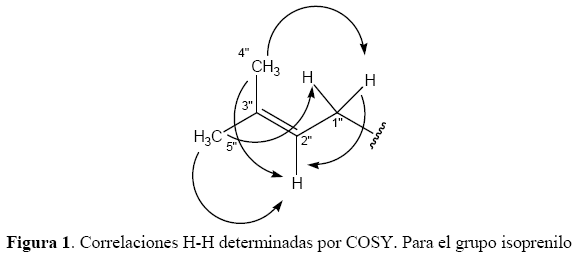
Al igual que los protones, los carbonos C-4’’, C-5’’, C-1’’ y C-2’’, asignados por HMQC, poseen un desplazamiento químico consistente con un grupo isoprenilo, así como el carbono C-3’’, cuya asignación fue resuelta en el espectro HMBC.
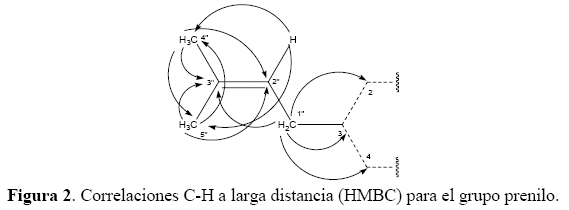
Las correlaciones heteronucleares a larga distancia HMBC para este grupo se muestran en la figura 2 donde es importante resaltar la correlación del H-1’’ con los carbonos C-2, C-3 y C-4 que nos permiten posicionarlo en el carbono C-3 del anillo aromático.
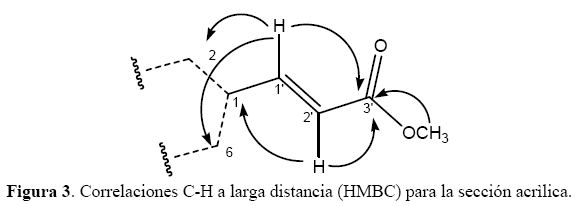
Los protones H-1’(δ 7.75 d) y H-2’(δ 6.40 d), del sistema olefínico, muestran mayor desplazamiento químico de lo normal por la proximidad de dos grupos desapantallantes, un anillo aromático y un ester. Su constante de acoplamiento de 15.9 Hz muestra una isomería trans, la más común en productos naturales. Su localización en la estructura se resolvió con el experimento HMBC que muestra la correlación del H-1’ y de un metoxilo a 3.9 ppm con un carbonilo a 168.5 ppm, indicando la presencia de un grupo ester α,β insaturado. Finalmente, las correlaciones del H-1’ con los carbonos C-1; C-2 y C-6 indican su posición en el carbono C-1 del anillo aromático (Figura 3).
]]>
Finalmente el sistema aromático presenta tres protones, el H-5 que muestra un acoplamiento orto con H-6 (J= 8.2 Hz), el protón H-6 que muestra acoplamientos orto y meta con H-5 y H-2, respectivamente (J= 8.2 & 2.2 Hz), y el protón H-2 que muestra un acoplamiento meta con H-6 (J= 2.2 Hz). En la figura 4, se muestran las correlaciones obtenidas por COSY H-H.

Los carbonos C-2, C-5 y C-6 se asignaron por correlaciones observadas en el espectro HMQC, mientras que los carbonos cuaternarios C-1, C-3 y C-4, se asignaron por las correlaciones HMBC (Tabla 1, Figura 5).
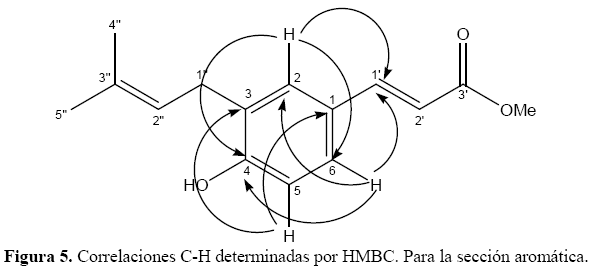
Finalmente, la sustitución faltante sobre C-4 puede ser resuelta por su desplazamiento químico (δ 157.2) que sugiere la presencia de un grupo hidroxilo. Todas las asignaciones realizadas se confirmaron por comparación con datos bibliográficos (Tabla 2) que confirman plenamente la estructura propuesta.
Considerando que el compuesto 1 tenía antecedentes de actividad antimutagénica [4,8] y que esta actividad esta normalmente relacionada a la actividad antioxidante [9], se evaluó tanto los extractos obtenidos como el compuesto 1 puro mediante dos técnicas, DPPH y ABTS, que determinan su capacidad como “scavengers” atrapadores de radicales libres. También se determinó el valor TEAC (capacidad antioxidante equivalente al Trolox) del compuesto 1, una de las formas más reconocidas de evaluar la capacidad antioxidante.
]]> Los resultados se encuentran en la tabla 3, observándose que tanto el extracto etanólico como el de AcOEt muestran un porcentaje de inhibición de radicales ABTS importante. El compuesto 1, obtenido del extracto de AcOEt, muestra aún mayor capacidad antioxidante, pareciendo ser uno de los principios responsables de la actividad del extracto de AcOEt, ya que tiene una interesante capacidad antioxidante como inhibidor de radicales libres (TEAC 3,4) comparable a la del compuesto utilizado como referencia quercetina (TEAC 4,8), que correlaciona con su actividad antimutagénica
EXPERIMENTAL
General
Material vegetal
La especie vegetal Baccharis santelicilis fue colectada, en abril de 2004 en el campus universitario de Cota Cota de La Paz, Bolivia. La identificación botánica fue realizada por la Lic. Lía de Michel experta del Herbario Nacional de Bolivia donde se puede encontrar un espécimen de la misma.
Extracción
973 g de partes aéreas de B. santelicis secas y molidas fueron sometidas a una maceración con Éter de Petróleo 20-40 por 48 h dando 15,6 g de un extracto Etéreo. El residuo vegetal fue sometido a una nueva extracción por maceración con AcOEt por 24 h obteniéndose 42,4 g de extracto. Finalmente, el residuo vegetal fue macerado con EtOH por 48 h obteniéndose 31,2 g de extracto etanólico.
]]> AislamientoEl compuesto 1 fue aislado del extracto de acetato de etilo de la planta, mediante una cromatografía VLC en Silicagel utilizando un gradiente de Eter de petróleo y AcOEt del 10 al 40%. El metabolito fue re-cristalizado en una mezcla al 10% de Eter de Petróleo en AcOEt obteniéndose 1,2 g del compuesto puro. Adicionalmente, la cromatografía VLC dio como resultado fracciones donde precipitaron el ácido oleanólico y el estigmasterol, compuestos caracterizados por comparación con muestras auténticas del Laboratorio mediante las técnicas TLC y Punto de fusión. El compuesto 1 fue identificado mediante un análisis de sus espectros de RMN 1D y 2D (Tablas 1 y 2).
Actividad antioxidante Método ABTS – Ensayo TEAC
El método ABTS es un método de screening para la evaluación de la capacidad antioxidante de distintas sustancias tanto hidrofílicas como lipofílicas.
El radical monocationico (ABTS•+) 2,2-azinobis-(ácido 3-etilbenzotialzolina-6-sulfónico) es producido por reacción entre ABTS 7mM en H2O y persulfato de potasio 2.45 mM. Dicha reacción da un compuesto coloreado que al cabo de 12-16 h es estable. Este compuesto, luego es diluido con metanol hasta llegar a una absorbancia de 0.7 medida a 734 nm. Las muestras a probar son preparadas a una concentración de 2.7 mg/mL. Para el ensayo se usa 1 mL de la solución de ABTS•+ con 10μL de cada muestra a probar, la reacción se estabiliza a los 4 min luego de los cuales se mide su absorbancia a 734 nm. Todas las determinaciones son corridas por triplicado. Se usa como Blanco metanol, como control positivo Quercetina 1000uM y ABTS•+ puro como control negativo. El % de inhibición es calculado mediante la siguiente formula:
% Inhibición = 100 - [ (Abs muestra – AbsQ(1000) * 100 / (Abs ABTS•+ – AbsQ(1000)]
La actividad antioxidante de los diferentes compuestos es medida en función del grado de decoloración que causan en la solución del radical monocatiónico ABTS•+. El ensayo de decoloración esta basado en la capacidad, de la sustancia a probar, de atrapar el electrón desapareado del radical monocatiónico ABTS•+ o de liberar un protón.
Para la determinación del valor de TEAC del compuesto puro, se prepara una solución del metabolito a una concentración 1mM y se realiza el ensayo ABTS, el porcentaje de inhibición a 734 nm es ploteado en función del metabolito estándar ácido 6-hidroxi-2,5,7,8-tetrametilcroman-2-carboxílico (Trolox, Aldrich Chemical Co., Gillingham, Dorset, U.K.). El valor TEAC es definido como la concentración del estándar Trolox con la misma capacidad antioxidante que una concentración 1mM del metabolito antioxidante bajo investigación y es expresada en comparación con el valor TEAC del metabolito de referencia quercetina.
La Quercetina, es un flavonoide muy conocido que se ha comprobado como neuroprotector, no se conoce el mecanismo de acción, pero es muy usado en muchas pruebas como patrón de comparación por su elevada actividad [14,15].
Actividad antioxidante. Método DPPH
]]> Este método, también es utilizado para el screening de muestras y también determina la capacidad antioxidante en función de la capacidad atrapadora de radicales libres. En este caso, del radical libre estable DPPH (1,1-difenil-2-dipicrilhidrazilo).Las muestras a evaluar son preparadas a la misma concentración que para el ensayo ABTS (2.7 mg/mL). Alícuotas de 30μL de la solución metanólica de cada muestra son añadidas a 3 mL de una solución metanólica al 0.004% de radicales libres DPPH. La reacción se estabiliza a los 30 min luego de los cuales se mide la absorbancia a 517 nm y se calcula el porcentaje de inhibición tomando como blanco metanol y como control positivo quercetina.
AGRADECIMIENTOS
A la Agencia Sueca de Cooperación Internacional ASDI/Sarec por el soporte financiero y al personal del Herbario Nacional de Bolivia por la identificación del material vegetal.
REFERENCIAS
[1] Cabrera A., “FLORA DE LA PROVINCIA DE JUJUY”, Parte X, Instituto Nacional de Tecnología Agropecuaria, Argentina, 212, (1978).
[2] Zdero C., Bohlmann F., Solomon J.C., King R. M. y Robinson H., Phytochemistry , 28, 531, (1989) [ Links ]
[3] Jakupovic J., Schuster A., Ganzer U., Bohlmann F. y Boldt P.E., Phytochemistry, 29, 2217, (1990) [ Links ]
[4] Zdero C., Bohlmann F. y Niemeyer N. H. Phytochemistry, 30, 1597-1601, (1991) [ Links ]
[5]Oliveira C., Schenkel E., Gosmann G., Palazzo de Mello J., Mentz L. Petrovick P., “FARMACOGNOSIA”, 1° edición, Ed. De UFSC. Brasil, 435-437, (1999)
[6] Mitscher L. A., Telikepalli H., McGhee E. y Shankel D. M., Mutation Research, 350, 143-152, (1996) [ Links ]
[7] Hamed A. I., Springuel I., El-emary N. A., Mitome H., y Yamada Y., Phytochemistry , 45, 1257-1261, (1997) [ Links ]
[8] Schmitt A., Telikepalli H., y Mitscher L. A. , Phytochemistry , 30, 3569-3570, (1991) [ Links ]
[9] Bates R. W., Gabel C. J., Ji J. y Rama-Devi T., Tetrahedron, 51, 8199-8212, (1995) [ Links ]
[10] Menon S. R., Patel V. K., Mitscher L. A., Shih P., Pillai S. P., y Shankel D.M., Journal of Natural Products, 62, 102-106, (1999) [ Links ]
[11] Laval J., Jurado J., Saparbaev M., Sidorkina O., Mutation Research, 402, 93–102, (1998)
[12] Flores Y., Sterner O., y Almanza G.R., Revista Boliviana de Quimica, 21, 31-35, (2004) [ Links ]
[13] Labbe C., Rovirosa J., Faini F.,. Mahu M., San-Martin A., y Castillo M. Joumal of Natural Produrts. 49, 517-518, (1986) [ Links ]
[14] Speisky H.,Cassels B., Lissit E. y Videla L., Biochemistry Pharmacology , 11, 1575-1581 (1991) [ Links ]
[15] Re R., Pellegrini N., Proteggente A., Pannala A. Yang M., Rice Evans C., Biochem. Soc. Trans., 1231, (1998) [ Links ]
]]>