PROPUESTA DE METODOLOGIA DE ANALISIS DE Fe Y Ti EN LA FRACCION PESADA DE MUESTRAS SEDIMENTOS ARENOSOS
Cori Wilson b, López Rafael c. Blanco Mario a, Cabrera Saúl c
a Instituto de Investigaciones Geológicas y del Medio Ambiente (IGEMA), UMSA, La Paz, Bolivia. email: mwblanco@latinmail.com
b Carrera de Química, Facultad Técnica, UMSA, La Paz, Bolivia.
c Instituto de Investigaciones Químicas (IIQ), UMSA, La Paz, Bolivia. email: saulcabreram@hotmail.com
]]>
RESUMEN
Después de verificar la existencia de hierro y titanio por el método de FRX en muestras de sedimentos arenosos, se realizo una concentración gravimétrica y la separación de la fracción magnética compuesta principalmente por Ilmenita y Magnetita. En el concentrado magnético se analizó hierro y titanio a través del método Dicromatometrico y Complexometrico estandarizado, donde el parámetro de pH para el análisis de Ti por retroceso sobre EDTA, con Talio es un factor clave para eliminar interferencias de hierro. Los resultados demuestran que no existe una interferencia apreciable entre Fe - Ti y el EDTA por tanto se puede cuantificar por separado cada metal con un nivel de confianza en el análisis de hierro de 95,0%, con error promedio de 0.4% en las determinaciones, y para el titanio, igualmente de 95,0%, con un error promedio de 0.2% en las determinaciones.
Key words : Estandarización, valoración, titulación
ABSTRACT
After verifying the iron and titanium existence by the FRX method in samples of sandy silts, one carries out the concentration gravimetric and later separation of the magnetic fraction compound mainly for Ilmenite and Magnetite. In the magnetic concentrate it was analyzed iron and titanium through a Dicromatometric and standardized Complexometric method, where the pH parameter for the analysis of Ti for setback EDTA with Talio, it is a key factor to eliminate iron interferences. The results demonstrate that an appreciable interference does not exist among Fe - Ti and the EDTA, therefore it can quantify for separated each metal with a level trust in the analysis of iron of 95,0%, with error average of 0.4% in the determinations, and for the titanium, equally of 95,0%, with an error average of 0.2% in the determinations.
INTRODUCCIÓN
Los métodos de análisis de elementos metálicos en muestras de sedimentos y rocas son múltiples, en muchos casos depende del equipamiento disponible, de la concentración y tipos de elementos en la muestra a analizar, etc. Modernamente se emplean métodos analíticos basados en técnicas de emisión atómica (fotometría de llama, ICP “Inductively coupled plasma”), absorción atómica (espectrometría de absorción atómica), o por florescencia de rayos X (FRX) (1 - 4), pero, pese a la generación de estos nuevos métodos, aun se usan los tradicionales, como colorimetría , gravimetría o complexometría los cuales en función de la complejidad de la matriz pueden ser mas adecuados. De hecho, las ventajas de cada método de análisis depende en muchos casos de su limite de detección o la diversidad de elementos que pueden ser analizados en forma simultanea, así por espectrometría de absorción o emisión atómica se puede analizar hasta 40 elementos con un limite de detección que varía entre 0,1 y 1ppm, no obstante para el caso de Fe y Ti suele transformarse en un proceso dificultoso por la interferencia mutua que presentan dichos elementos. Por otro lado si bien un equipo de FRX, permite la evaluación cualitativa de los elementos de manera rápida, la estandarización del método y la necesidad de contar con patrones, hace a la técnica complicada. Actualmente métodos más sofisticados, como el ICP ofrecen un alto limite de detección, esté es especialmente apropiado para la determinación de concentraciones pequeñas de elementos difíciles de atomizar como las tierras raras (REE), los alcalinotérreos, B, Si, U y Ta (4 – 5). Finalmente, hay que notar que si bien los métodos actuales tienden a optimizar el limite de detección, la rapidez y la variedad de elementos que se puedan analizar, no hay que olvidar que los métodos tradicionales de análisis pueden, sobre manera, servir para muestras de sedimentos y rocas que presenten contenidos altos de ciertos elementos, principalmente por su sencillez, sus bajos costos y la necesidad de poco equipamiento (6 - 7). En este sentido, el presente trabajo de investigación pretende demostrar la aplicabilidad de métodos tradicionales de complexometría, para el análisis de Ti por retroceso, y el de oxidación - reducción, específicamente dicrometría, para el análisis de Fe (II) y Ti(III), en muestras de “arenas pesadas” de sedimentos arenosos con altos contenidos de Ti y Fe.
]]>METODO DE ANALISIS
METODO VOLUMÉTRICO - COMPLEXOMETRICO EN EL ANÁLISIS DE TITANIO
El ión etilendiamino tetracetato, (CH2N)2(CH2COO-)4 (EDTA), representado por ![]() , forma complejos muy estables, en la razón uno a uno, con iones de los metales de la tabla periódica. Esta razón uno a uno en los complejos metal – EDTA proviene del hecho de que el ión
, forma complejos muy estables, en la razón uno a uno, con iones de los metales de la tabla periódica. Esta razón uno a uno en los complejos metal – EDTA proviene del hecho de que el ión ![]() posee en total seis grupos funcionales – cuatro grupos carboxílicos y dos grupos aminos que pueden ocupar cuatro, cinco o seis posiciones de coordinación en torno de un ión metálico central. La mayoría de las valoraciones metal-EDTA se efectúan en soluciones neutras o alcalinas, la razón de ello es que los complejos metal-EDTA, aunque en general son muy estables, pueden experimentar una reacción de disociación en presencia de un ácido:
posee en total seis grupos funcionales – cuatro grupos carboxílicos y dos grupos aminos que pueden ocupar cuatro, cinco o seis posiciones de coordinación en torno de un ión metálico central. La mayoría de las valoraciones metal-EDTA se efectúan en soluciones neutras o alcalinas, la razón de ello es que los complejos metal-EDTA, aunque en general son muy estables, pueden experimentar una reacción de disociación en presencia de un ácido:
![]()
En función del pH de la solución, la formación de iones hidrogeno como producto de reacción causa una disminución del pH y la reacción de la valoración deseada podría cesar o incluso invertirse, a menos que se amortigüe la solución contra el cambio de pH (pH 5 – 5.5). Por consiguiente, en la práctica se emplea (en exceso) un sistema amortiguador inocuo (CH3COOH/CH3COONH3). El proceso de análisis de Ti se ha desarrollado por retroceso, esto por que el complejo TITANIO-EDTA no se puede visualizar con ningún indicador colorimétrico, pero el exceso de EDTA puede ser titulado con una solución de (Tl+3)-Talio III sin interferir o romper el complejo TITANIO-EDTA (9) El indicador estándar para el análisis de Tl es el naranja de Xilenol al 1% cuyo viraje de color es amarillo-rojo-morado. Los valores de las constantes de equilibrio (Log Kw) en la formación de complejo para la titulación de Fe (II) 14.3, Fe (III) 25.1, Tl (III) 18.6, y Ti (III) 21.3, TiO (II) 17.3 con EDTA sugieren reacciones espontáneas.
PROCEDIMIENTO
1. Disolución de la muestra
]]> 2. Acondicionamiento del pH para la titulación (Solución Tampón)3. Adición de solución de EDTA en exceso.
4. Titulación con solución de Tl +3.
La formula general para determinar el % de titanio en la muestra, resulta dada por:
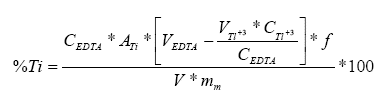
Donde:
: es el factor de dilución,
]]>
: Concentración molar de la solución de talio III
: Volumen gastado de la solución de talio III en ml
: Concentración molar de la solución de EDTA
: Masa molar del titanio
: Volumen añadido de solución de EDTA en ml.
: es la cantidad de milimoles de EDTA que reacciona con 1 milimol de titanio.
El método complexométrico para titanio puede presentar como interferencias a complejos de Fe - EDTA, por lo que se ha desarrollado la estandarización del método con soluciones puras de Ti, y de mezclas de Ti – Fe, estabilizándose el pH entre 5.0 a 5.5, este rango de pH permite la cuantificación de Ti sin la interferencia del Fe.
METODO OXIDACION – REDUCCION (DICROMATOMETRIA) EN EL ANALISIS DE Fe – Ti
La dicromatometría es uno de los métodos de análisis de oxidación – reducción más utilizado, esto por que las soluciones de dicromato de potasio son muy estables, pudiendo hervirse sin que ocurra descomposición apreciable debiendo ser protegidas de la evaporación. La única reducción importante en que interviene esta especie esta dada en la siguiente semi ecuación:
![]()
PROCEDIMIENTO
1. Disolución de la muestra de hierro.
2. Reducción cuantitativa de hierro III a hierro II, con un reductor adecuado seguida de eliminación del exceso del agente reductor.
3. Adición H2SO4 (acidifica el medio) y H3PO4 (el H3PO4 formara complejo solo con el Fe+3, facilitando la observación del cambio de color del indicador redox que es una sal de bario del ácido difenilaminsulfonico con un viraje entre blanco – verde – azul – violeta).
4. Valoración de la solución de hierro II.
Se puede deducir la formula general para determinar el % de hierro en la muestra, expresada como:
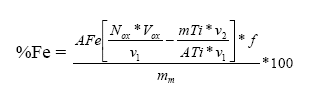
N ox: normalidad del K2 CrO
V ox: Volumen del K2 CrOque se gastara en ml ![]()
![]()
mTi: masa del titanio (determinado por complexometria) en mg
ATi: masa molar titanio en mg/mmol
mm es la masa de la muestra en mg
AFe : masa molar del hierro en mg/mmol
![]() : Factor de dilución
: Factor de dilución
Para la estandarización del método se han realizado los siguientes análisis:
]]>a) Titulación por retroceso de una muestra de titanio.
b) Titulación de muestras estándares de EDTA titanio - hierro con Tl (III).
c) Titulación de muestras de la sal de Mohr ((NH4)2Fe(SO4)2*6H2O) al 99% por dicromatometría.
d) Titulación de Ti(III) por dicromatometría.
e) Titulación de una mezcla de Ti y Fe por dicromatometría.
RESULTADOS
I. ESTANDARIZACION DE LOS METODOS
a) Titulación por retroceso de una muestra de titanio IV con Tl+3.
]]> Se han analizado muestras conocidas de titanio (Ti+4) 0,01M (20ml) – EDTA 0,01M (estandarizada a partir de la sal disodica de EDTA) (40ml de solución de EDTA en exceso), comprobando cuantitativamente la cantidad de estos con el volumen gastado de la solución de talio (Tl +3) 0,01M (estandarizada a partir del trifluoro acetato de talio (III)).Se han desarrollado los análisis cuatro veces para disminuir la incertidumbre, encontrándose un volumen medio de Tl+3 de 19.5±0.2 consistente con el valor teórico de 19.6, esto lleva a un error del orden del 2% en las medidas de concentración del Ti+4.
b) Titulación titanio IV en la presencia de hierro III con Tl+3.
Se ha evaluado muestras conocidas de titanio (Ti+4) 0,01M (20ml), hierro (Fe+3) 0,01M (Volumen variable de 10, 8, 6 y 4 ml) y EDTA 0,01M (40ml) comprobando cuantitativamente la cantidad de estos con el volumen gastado de la solución de talio. Se han desarrollado los análisis cuatro veces para disminuir la incertidumbre, encontrándose un volumen medio de Tl+3 de 19.5±0.2 consistente con el valor teórico de 19.6, esto lleva a un error del orden del 2% en las medidas de concentración del Ti+4, demostrando que la presencia de Fe+3 en diferentes proporciones no interfiere en el análisis.
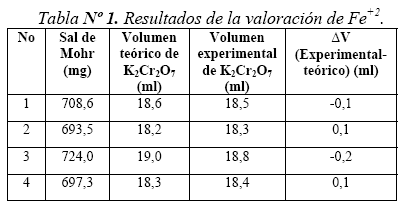
c) Titulación de muestras de hierro II (sal de Mohr () al 99% por dicromatometría.(NH4)2Fe(SO4)2*6H2O
Se ha valorado por cuadruplicado Fe+2 a partir de masas mm definidas de sal de Mohr (Tabla No. 1) disueltas en ácido clorhídrico, en presencia de H2SO4, H3PO4, con solución de dicromato de potasio estandarizada de una concentración de 0,0962 N. La desviación estándar de σn-1 ±0.2, esto lleva a un error del orden del 1% en las medidas de concentración del Fe+2.
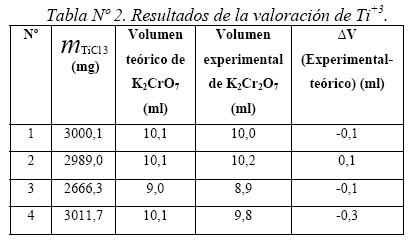
El procedimiento es similar al caso anterior, se ha utilizado masas de TiClen solución (Tabla Nº 2), La desviación estándar de σn-1 ±0.2, esto lleva a un error del orden del 1% en las medidas de concentración del Ti+3.
e) Titulación de una mezcla de Ti y Fe por dicromatometría
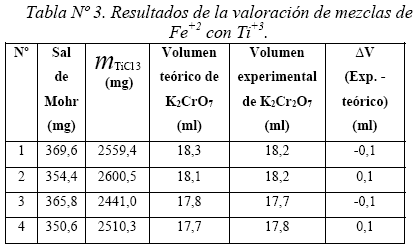
Se ha desarrollado la evaluación conjunta de Fe+2 y Ti+3, mezclando por cuadruplicadas masas de la sal de Mohr y de TiCl (Tabla Nº3), disolviendo la mezcla completamente con ácido clorhídrico, se ha regulado el medio con H2SO4 y H3PO4, desarrollándose la valoración con dicromato de potasio (0,0962N). La desviación estándar de σn-1 ±0.1, permite proponer un error del orden del 1% en las medidas de concentración del Ti+3.
II. ANALISIS DE “ARENAS PESADAS” DE SEDIMENTOS ARENOSOS
]]> Los materiales que se utilizan en este estudio corresponden a sedimentos asignados a la Formación Umala de edad pliocena, de origen lacustre, que en los lugares de muestreo presenta fuerte influencia fluvial, son ubicados sobre el camino carretero Patacamaya – Tambo Quemado y tienen las siguientes características:Muestra No.1. Obtenido sobre el Km 8 del camino Patacamaya hacia la estancia Copani.
Muestra No 2. Obtenido sobre el Km 80 del camino Patacamaya – Tambo Quemado.
Muestra No.3. Obtenido sobre el Km 90 del camino Patacamaya – Tambo Quemado.
En todos los casos, las muestras cuarteadas adecuadamente, con una masa inicial de 1500 gr. han sido tamizadas a malla 100 ASTM en seco, concentradas en mesa de oscilación y finalmente el concentrado separarlo en función a sus propiedades magnéticas (Tabla Nº 4).
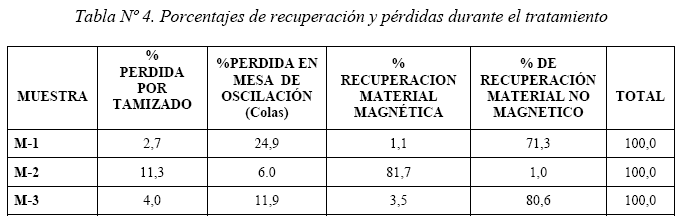
El estudio de fluorescencia y difracción de rayos X (FRX y DRX) de los concentrados magnéticos y no magnéticos en cada muestra permite diferenciar dos tipos de materiales:
Parte Magnética.
En todos los casos, los elementos determinados como mayoritarios son Ti y Fe, minoritarios P, Mg, Mn, Sr, y trazas Ni, Cu, Zn, Ga, Pb, Rb, Y, Nb y Ba. Los minerales mayoritarios identificados por DRX son ilmenita FeTiO3 y magnetita Fe3O4 (≈ 96%).
]]> Parte no Magnética.Los elementos mayoritarios son Ca, y Zr, los minoritarios Cr, Si, Al, Ti, Fe, y trazas Mg, P, Cu, Zn, As, Pb, Rb, Sr, Nb, Sn y Ba. Los minerales no metalicos identificados por DRX cuarzo y feldespatos (≈ 66%).
ANALISIS DE Fe Y Ti
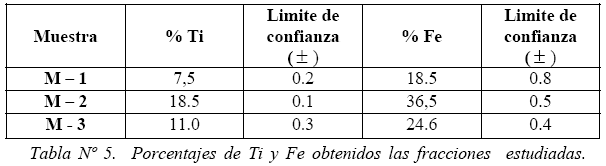
Los análisis por triplicado ha sido desarrollados para la muestra M – 1 en la fracción no magnética, en la M – 2 y M – 3 en la fracción magnética. Los métodos de análisis han sido los anteriormente estandarizados, teniendo los cuidados adecuados para llevar el Fe (III) y Ti (IV) a sus estados reducidos de Fe (II) y Ti (III) con amalgama de Zn. En la tabla Nº 5 se observa los % de Ti y Fe obtenidos en las diferentes muestras analizadas, encontrándose evidencias de los mayores contenidos de Fe y Ti para la muestra M – 2, seguida de la muestra M – 3, y bajas concentraciones de estos elementos en la muestra M – 1.
CONCLUSIONES
Se establece un método cuantitativo para analizar hierro y titanio en muestras de sedimentos arenosos que tienen alto contenido de ilmenita y magnetita, tanto en concentrados como en muestras brutas.
Una de las ventajas del método propuesto es que no requiere de la separación previa de titanio y hierro que significaría aumentar las etapas del proceso, utilizando más tiempo, reactivos y material.
]]> Se toma en cuenta el comportamiento que tienen ambos elementos (hierro y titanio), lo que ocasiona interferencia y reacción mutua, se propone el análisis por dicromatometria, que permite se titulen tanto al hierro como al titanio simultáneamente.El método, considera la estabilidad en el equilibrio de cada elemento cuando forma complejo con el EDTA a diferentes pHs (así a pH de 5,25 el complejo Titanio-EDTA y Talio-EDTA son estables solo que no se puede visualizar al primero pero si al segundo siendo este nuestro parámetro final para determinar solo el porcentaje de Titanio), y la reacción que tiene el hierro (III) con el pH utilizado, el cual definió el comportamiento de este frente al método volumétrico complexometrico utilizado.
Se demuestra que no existe una interferencia apreciable entre estos elementos y el EDTA por tanto se puede cuantificar por separado cada metal con un nivel confianza en el análisis de hierro de 95%, con error promedio de 0.45% en las determinaciones, y para el titanio, igualmente de 95%, con un error promedio de 0.16% en las determinaciones.
Debido a que la concentración de hierro y titanio en las muestras es considerada como mayoritaria (3.4.1), el método volumétrico es más simple y sencillo frente a los posibles métodos instrumentales o gravimétricos.
La FRX es un instrumentó muy útil para valorar la presencia de elementos en la muestra a nivel de mayoritarios, minoritarios y trazas.
BIBLIOGRAFIA
1) Balaram, V., S. L. Ramesh, y K. V. Anjaiah. 1995. Comparative Study of the Sample Decomposition Procedures in the Determination of Trace and Rare Earth Elements in Anorthosites and Related Rocks by ICP-MS. Fresenius' Journal of Analytical Chemistry 353 (2):176-182. (abstract only)
2) Boumans, P. W. J. M. (Ed). 1987a. Inductively Coupled Plasma Emission Spectroscopy. Part I: Methodology, Instrumentation, and Performance. Chemical Analysis: A Series of Monographs on Analytical Chemistry and Its Applications. Volume 90. John Wiley and Sons.
3) Burton, J. H. y A. W. Simon. 1993. Acid Extraction as a Simple and Inexpensive Method for Compositional Characterization of Archaeological Ceramics. American Antiquity 58 (1):45-59.
]]> 4) Hatcher, H., M. S. Tite, y J. N. Walsh. 1995. A Comparison of Inductively-Coupled Plasma Emission Spectrometry and Atomic Absorption Spectrometry Analysis on Standard Reference Silicate Materials and Ceramics. Archaeometry 37 (1):83-94.5) Kuleff, I. y R. Djingova. 1996. Provenance Study of Pottery: Choice of Elements to be Determined. Revue d'Archéométrie 20:57-67.
6) John G. Dick, “Química analítica “, ed. El manual Moderno, páginas. 234, 456, 678 – 89., 1980.
7) Arthur I. Vogel, “Química analítica Cuantitativa”, Ed. Kapeluz, México, 1976., pag. 894 – 899.
]]>