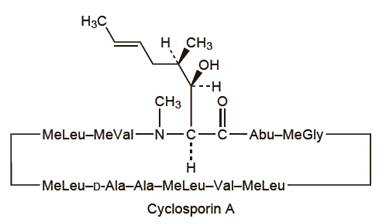
Validación del método para la cuantificación de ciclosporina a en sangre total por HPLC/DAD
Validation of the method for the quantification of cyclosporine a in whole blood by HPLC / DAD
Myriam Lina Trigo Orsini 1 Cinthia Maribel Parra Poma*
Instituto de Servicios de Laboratorio de Diagnostico e Investigación en Salud. Laboratorio de Biodisponibilidad y Bioequivalencia, Universidad Mayor de San Andrés, Av. Saavedra 2224. La Paz, Bolivia.1
Auxiliar de Investigación, Facultad de Ciencias Farmacéuticas y Bioquímicas, Universidad Mayor de San Andrés, Av. Saavedra 2224. La Paz, Bolivia.* mylitrigo@gmail.com ]]>
Resumen
El presente estudio describe la validación del método para la cuantificación de Ciclosporina A en sangre total por Cromatografía Líquida de Alta Resolución (HPLC) en Fase Reversa con Detector de Arreglo de Diodos.
La ciclosporina A es un fármaco inmunosupresor con un estrecho margen terapéutico además de su amplia variabilidad en los procesos farmacocinéticos, justifican su monitorización de dosis a pacientes con trasplantes de órganos para evitar los efectos secundarios y el posible rechazo del órgano trasplantado.
La separación de la Ciclosporina A de una matriz compleja como la sangre fue llevada a cabo de manera exitosa utilizando como fase estacionaria una columna C8 5um (250 mm x 4,6mm) o equivalente a L7 según la USP 37, la fase móvil fue una mezcla de acetonitrilo y agua en gradiente, flujo 1.4 ml/min, temperatura de la columna 75ºC y detección con Arreglo de Diodos a 210nm.
El método fue validado con los siguientes parámetros: especificidad, linealidad, precisión, exactitud, límite de detección y límite de cuantificación. También se realizó la prueba de aptitud del sistema. El método fue específico para la Ciclosporina A, la respuesta fue lineal en el rango de 100 a 1000 ng/mL de concentración del analito. El valor del coeficiente de variación o desviación estándar relativa (C.V. o DSR) para la precisión fue óptimo. La recuperación media fue de 103,06%. Y el límite de detección y cuantificación resultaron óptimos para la cuantificación de Ciclosporina en sangre total en el rango definido.
Finalmente el método cromatográfico nos permitió separar y cuantificar a la Ciclosporina A presente en las muestras de sangre de pacientes con transplante renal.
Palabras Clave: Ciclosporina A, Biodisponibilidad, Farmacocinética, Transplante Renal, Cromatografía Líquida de Alta Resolución.
This study describe the validation method for the quantification of Cyclosporin A in Whole Blood by Liquid Chromatography High Efficiency (HPLC) in reverse phase.
Cyclosporine A is immunosuppressant United Nations UN the narrow scam therapeutic margin: In addition to its extensive ¿variability in pharmacokinetic processes justify their monitoring dose Patients with organ transplants paragraph Avoid Side Effects and poaible organ rejection transplanted.
Separation of Cyclosporine A of a matrix complex as the blood was carried out successfully using as the stationary phase C8 column, the mobile phase is a mixture of acetonitrile and water gradient, flow 1.4 ml / min, Temperature column was 75 ° C detection 210 nm in one.
The method was validated with the following parameters: specificity, linearity, precision, accuracy, limit of detection and limit of quantification. Aptitude Test System was also performed. Was Method Specific for Cyclosporin A, the response was linear in the range 100 a 1000 ng/mL concentration of the analyte. The coefficient of variation or relative standard deviation (RSD or CV) for the precision was optimal. Recovery media WAS 103,06%. And the limit of detection and quantification were optimal for the quantification of total Cyclosporine in blood in the range defined.
Finally Chromatographic Method allowed us to separate and quantify Cyclosporin A in samples of patients with renal transplantation.
Keywords: Cyclosporine A, bioavailability, pharmacokinetics, renal transplantation, high-performance liquid chromatography.
INTRODUCCIÓN
]]> Ciclosporina ALa ciclosporina es un fármaco inmunosupresor ampliamente usado en el trasplante de órganos entre dos personas con el objeto de reducir la actividad del sistema inmunitario del paciente y el riesgo de rechazo del órgano. Ha sido estudiada en el trasplante de piel, corazón, riñón, pulmón, páncreas, médula ósea e intestino. La ciclosporina es un péptido no ribosomal cíclico de 11 aminoácidos (undecapéptido) producido por el hongo Tolypocladium inflatum Gams, aislado inicialmente de una muestra de suelo noruego.
Es insoluble en agua pero se disuelve fácilmente en solventes orgánicos, tiene un peso molecular de 1202,63 g/mol.

(Martindale, 2009)
Mecanismo de acción
La ciclosporina posee su capacidad inmunosupresora altamente selectiva en su unión a la proteína citosólica ciclofilina (una inmunofilina) de linfocitos inmunocompetentes, especialmente linfocitos T. Este complejo de ciclosporina y ciclofilina inhibe la calcineurina, la cual bajo circunstancias normales es responsable de activar la transcripción de interleucina-2 (Il-2). También inhibe la transcripción de la producción de linfocinas y la liberación de interleucinas y por lo tanto conduce a una reducción en la función de las células T-efectoras (linfocitos T efectores), sin afectar la actividad citostática.
Tiene también un efecto sobre las mitocondrias. La ciclosporina A inhibe la apertura del poro de transición de permeabilidad mitocondrial, de esta forma, inhibe la liberación del citocromo c, un potente factor de estimulación de apoptosis. Sin embargo, este no es el principal modo de acción para su uso clínico, pero si es una importante herramienta para la investigación acerca del fenómeno de la apoptosis, o muerte celular programada.
Farmacocinética
La biodisponibilidad oral de la Ciclosporina A varía entre 4 y 30% (Kahan B.D, 2012). Su absorción en la porción superior del intestino delgado es errática, incompleta y muy variable entre los distintos pacientes.
]]> El fármaco se distribuye ampliamente en todos los tejidos, mostrando un volumen de distribución de 3,5 a 13 l/kg de peso. Su lipofilia hace que se concentre en el tejido adiposo y ciertos órganos con un alto contenido lipídico, como hígado, páncreas El 50% del fármaco detectado en sangre está unido a la fracción celular, repartiéndose en un 80-90% a los eritrocitos y en un 4-20 % a los linfocitos. El 50-30% restante se encuentra en el plasma, unido a lipoproteínas circulante (aproximadamente en un 85-90%).La Ciclosporina A se metaboliza extensamente en el hígado, en el sistema enzimático microsomal del citocromo P-450. La excreción de Ciclosporina A y sus metabolitos es fundamentalmente biliar, siendo la excreción renal muy pequeña (>3%). Su semivida de eliminación, en condiciones normales, varía de diez-veintisiete horas. El aclaramiento plasmático oscila entre 5 y 20 ml/kg/min, encontrándose aumentado en pacientes pediátricos y disminuido en los casos de insuficiencia hepática.
Biodisponibilidad de la ciclosporina por vía oral
La ciclosporina es un medicamento que presenta una biodisponibilidad altamente variable al administrarla por vía oral. Esto se debe a que es prácticamente insoluble en agua. Por lo tanto, es necesario que se constituya una emulsión que permita la formación de micelas que puedan viajar por el medio acuoso constituido por los fluidos gastrointestinales para llegar a la pared intestinal y pasar a la sangre. De esta forma, la ciclosporina sólo puede absorberse en presencia de sales biliares que permitan la emulsificación (al igual que para muchos nutrientes de carácter lipídico) o bien gracias a formulaciones farmacéuticas que permitan la formación de micelas en ausencia de bilis. Por otro lado, la ciclosporina sólo puede ser absorbida en duodeno.
Por esta razón, la biodisponibilidad en adultos es mayor que la que se observa en pacientes pediátricos, ya que existen variaciones en la longitud duodenal entre estas dos poblaciones de pacientes.
Materiales y métodos
Muestras:
Se analizaron alrededor de 100 muestras de sangre total de personas que no tuvieron ningún trasplante de órganos para el proceso de validación del método, estas muestras fueron fortificadas a diferentes concentraciones de 100, 200 500 700, 1000 ng/mL con un Estándar de Ciclosporina A, también en este proceso se incluyeron 30 pacientes con trasplante renal pertenecientes al Programa Nacional de Salud Renal Dependiente del Ministerio de Salud y Deportes. Todas las muestras fueron tomadas por la mañana y para los pacientes con trasplante renal se tomaron las muestras en C0 y C2, es decir 5 minutos antes de que se administre la ciclosporina y 2 horas después de su administración ya que es el periodo donde el fármaco tiene la mayor concentración sérica. Las muestras se recolectaron en tubos Vaccutainer con EDTA 3K de 3 mL y se analizaron el mismo día de su recolección debido a que no existen estudios acerca de la estabilidad del fármaco y su degradación.
Reactivos y estándares de referencia: Todos los reactivos utilizados son calidad HPLC:
]]> Extracción de la muestra:Para el análisis se caracterizan 3 fases:
Fase de precipitación:
En un tubo de ensayo se mezclan 1mL de muestra (sangre total) + 2mL de una mezcla de acetonitrilo:agua pH3 (75:25), se agita en un vortex durante 2 segundos y luego se lleva a centrifugar durante 15 minutos a 3000 revoluciones por minuto (rpm).
Fase de Lavado:
Para esta fase se utilizó un Manifold conectado a una bomba de vacío, ya que se realizó la extracción en fase sólida con la ayuda de cartuchos de extracción Strata TM X 33um Polimeric Reversed Phase 60mg/3mL, se emplea un cartucho para cada muestra y el flujo de trabajo en general es de una gota cada 3 segundos.
Previamente se deben acondicionar los cartuchos activándolos con 1ml de Metanol grado HPLC, se eluye éste por presión negativa y a continuación se hace pasar por el cartucho en el siguiente orden:
El sobrenadante de la muestra que fue centrifugado.
3,2 mL de la mezcla de acetonitrilo:agua pH3 (20:80)
]]> 0,5 mL de Hexano
Los eluyentes de esta fase de lavado deben desecharse.
Fase de Extracción:
Luego se acondiciona el manifold para el proceso de recuperación colocando en el cartucho 1mL de diclorometano + 1mL de diclorometano + 0,3 mL de diclorometano, ya que este contiene a la Ciclosporina y sus metabolitos.
Lo recolectado se evapora a sequedad bajo corriente de Nitrógeno y el residuo seco se reconstituye con 250 µL de una mezcla de acetonitrilo:agua pH3 (50:50) y 500 µL de hexano, se agita durante un minuto, se deja reposar y se inyectan 50 µL de la fase acuosa en el HPLC.
Método cromatográfico:
El cromatógrafo Líquido de Alta Resolución utilizado fue un Jasco, equipado con inyector automático de 120 viales, un compartimento termostatizado de columna y con detector de Arreglo de Diodos.
La columna es C8 5um (250mm de longitud y 4,6 mm de diámetro interno), la fase móvil constituida por una mezcla de acetonitrilo:agua pH3 que varía de 45 a 55% los primeros 0.2 min, acetonitrilo:agua pH3 que varía de 52 a 48% los siguientes 20 min y acetonitrilo:agua pH3 que varía de 52 a 48% los siguientes 20.10 min. Posteriormente una fase de lavado de acetonitrilo:agua pH3 que varía de 63 a 37% desde el minuto 33. Además entre inyecciones existen 3 lavados de aguja constituida por acetonitrilo:agua 50 a 50% . El flujo de la fase móvil fue de 1,4 mL/min y la temperatura del compartimento termostatizado de 75ºC, el Detector se fijó a una longitud de onda de 210nm. Para el Lavado de los pistones se usó una mezcla de metanol:agua 50 a 50%.
VALIDACION:
LINEALIDAD Y RANGO
Se prepararon 5 niveles de concentración, cada nivel con tres réplicas, para linealidad del método (analito + matriz). A las siguientes concentraciones (100, 200, 500, 700, 1000 ng/mL)
Se determinó analizando repetidamente una misma muestra de forma consecutiva 6 veces, a la concentración media de la curva de calibración (500ng/mL).
Se evaluó la repetibilidad del método preparando muestras fortificadas a tres niveles de concentración (100, 500,1000 ng/mL).
La precisión intermedia mide la variabilidad del método en este caso se optó por días diferentes y analistas diferentes, realizando el análisis a la concentración media de la curva en matriz fortificada de 500 ng/mL y se calculó el coeficiente de variación total (CV).
Para evaluar la exactitud se prepararon 3 estándares por triplicado a concentraciones de 100, 500,1000 ng/mL y tres muestras fortificadas (matriz + analito) por triplicado a las mismas concentraciones de los estándares.
LÍMITES DE DETECCIÓN Y CUANTIFICACIÓN
Para evaluar el límite de detección y cuantificación se prepararon tres concentraciones menores al punto más bajo de la curva de calibración, (50, 70 y 90 ng/mL) por triplicado y se determinó la curva de calibración para estas concentraciones.
RESULTADOS:
]]> Determinación cualitativaSiguiendo la técnica cromatográfica descrita anteriormente, se procedió a la identificación de los compuestos mediante la comparación de los tiempos de retención (tR) de los estándares con los que se obtenían en las muestras de sangre. Así se observó que los tiempos de retención corresponden a: tR CsA: Treinta minutos.
VALIDACIÓN:
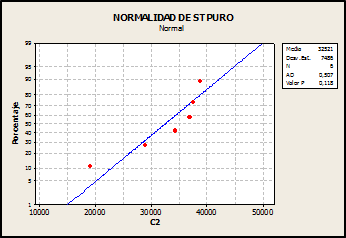
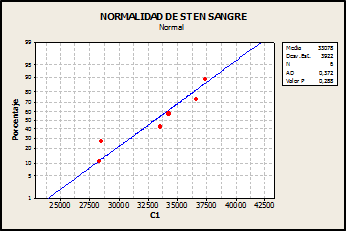
Validación del método analítico: ESPECIFICIDAD
Homogeneidad de varianzas

Prueba de t de Student-Fisher de comparación de dos medias con grupos independientes, para varianzas homogéneas

 ]]>
]]>
Validación del método analítico: LINEALIDAD Y RANGO
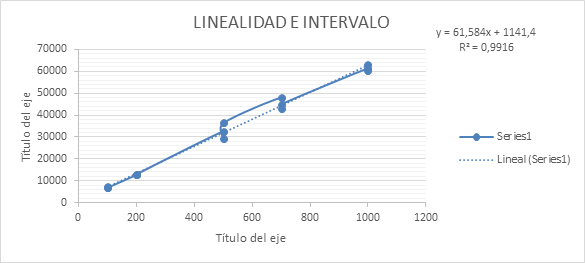
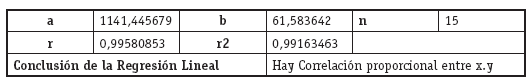
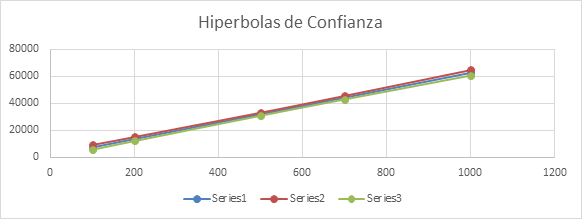
Coeficiente de correlación y Coeficiente de determinación
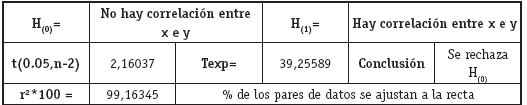


Precisión intermedia del método:
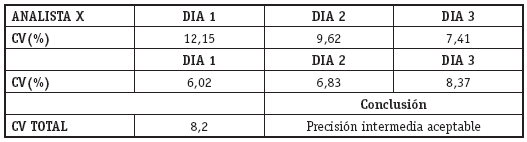
Validación del método analítico: EXACTITUD
Homogeneidad de varianzas

Recuperación media

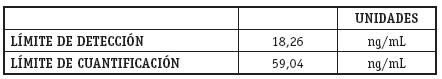
Validación del método analítico: LÍMITES DE DETECCIÓN Y CUANTIFICACIÓN
]]>
De acuerdo a los resultados obtenidos se puede discutir que:
· El método estandarizado y validado para la cuantificación de ciclosporina en sangre por Cromatografía Líquida de Alta Resolución con detector de Arreglo de Diodos es una alternativa eficiente debido a su especificidad para el análisis.
· Se validó el método analítico para la cuantificación de ciclosporina en sangre por cromatografía líquida de alta resolución en el Laboratorio de Biodisponibilidad y Bioequivalencia del Instituto de Servicios de Análisis de Laboratorio e Investigación en Salud (SELADIS) de la Facultad de Ciencias Farmacéuticas y Bioquímicas de la UMSA, con lo que se comprobó que éste cumple con todos los requerimientos exigidos en el protocolo. Por lo tanto, se puede asegurar que la metodología se encuentra en condiciones de ser utilizada para el análisis rutinario de determinación de ciclosporina en sangre lo que garantiza resultados confiables y reproducibles.
· El método luego de la validación resultó específico ya que es capaz de medir de manera inequívoca el analito, lineal, preciso y exacto.
· Los límites de detección y cuantificación son muy bajos, lo cual nos garantiza la cuantificación de ciclosporina en sangre en su concentración basal (C0) y en su concentración máxima (C2).
(AEFI), A. E. (2001). Validación de Métodos Analíticos. ciudad, editorial [ Links ]
AGILENT. (2006). www.agilent.com. Recuperado el 25 de Febrero de 2016, de http://www.mac-mod.com [ Links ]
AGILENT. (2009-2010). www.agilent.com. Recuperado el 03 de Febrero de 2016, de http://www.agilent.com [ Links ]
FDA, F. a. (2000). Guidance for Industry, Analytical Procedures and Methods Validation, Chemistry, Manufacturing, and Controls Docunmetation. [ Links ]
QUATTROCCHI, O. A., ANDRIZZI, S. I., & LABA, R. F. (1992). Introducción a la HPLC, Aplicación y Práctica. Buenos Aires: Artes gráficas Farro. [ Links ]
BOREL, J.F. (2002). History of the discovery of cyclosporin and of its early pharmacological development. [ Links ]
MEDEIROS M, CASTAÑEDA G. MUÑOZ R. (2001). Uso de ciclosporina en pacientes pediátricos. Bol Med Hosp lnf Mexico, pag.; 58:60-77. [ Links ]
MORALES, R. (s.f.). Centro de tecnología aplicada en BPMv. validación de técnicas analíticas. Cuantificación de acetaminofén por espectrofotometría UV. Análisis estadístico para linealidad, exactitud y precisión. Determinación de límites de detección y cuantificación. Purificación y Análisis de Fluidos Ltda., Bogotá. [ Links ]
]]>QUATTROCCHI, O. A., ANDRIZZI, S. I., & LABA, R. F. (1992). Introducción a la HPLC, Aplicación y Práctica. Buenos Aires: Artes gráficas Farro. [ Links ]
SKOOG, D. A. (2001). Principios de Análisis Instrumental. [ Links ]
The United States Pharmacopeial Conventio. Vol I. (2014). [ Links ]
VALLS, O., & DEL CASTILLO, B. (1998). Técnicas Instrumentales en Farmacia y Ciencias de la Salud. Barcelona: Ediciones Piros. [ Links ]
www.hielscher.com. (s.f.). Recuperado el 26 de Enero de 2016, de http://www.hielscher.com/formula-molecular-etanol.
]]> ]]>