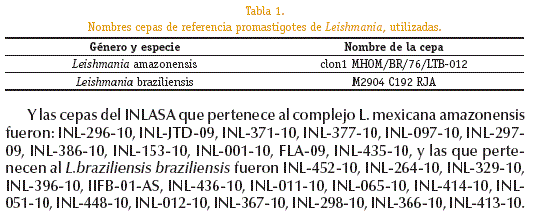
Susceptibilidad in vitro de promastigotes de Leishmania
frente a Anfotericina B, Miltefosina y los Alcaloides Totales
de Galipea longiflora mediante el Método Colorimétrico
XTT-PMS
SALAMANCA CAPUSIRI, EFRAIN1
ROMERO, DANITZA1 SANTALLA, JOSÉ A.2, ]]>
OPORTO, PATRICIA2
FLORES, NINOSKA1
GIMÉNEZ TURBA, ALBERTO1
1 Unidad Parasitología, Instituto de Investigaciones Fármaco Bioquímicas, Facultad de Ciencias Farmacéuticas y Bioquímicas,
Universidad Mayor de San Andrés.
2 Instituto Nacional de Laboratorios de Salud - INLASA - Laboratorio de Parasitología.
Av. Saavedra # 2224, Miraflores, La Paz-Bolivia.
CORRESPONDENCIA: ALBERTO GIMÉNEZ TURBA AGIMENEZ@MEGALINK.COME
FECHA DE RECEPCIÓN: 20 DE MARZO DE 2015 FECHA DE ACEPTACIÓN: 10 DE JUNIO DE 2015
]]>
En el presente trabajo se determino la susceptibilidad in vitro de 27 cultivos de promastigotes de Leishmania adaptados in vitro a partir de aislados de lesiones cutáneas de pacientes que asistieron a los laboratorios del IN LASA. Los antiparasitarios evaluados fueron Anfotericina-B, Miltefosina y los Alcaloides Totales de Galipea longiflora. Los resultados muestran un amplio rango de susceptibilidad de los diferentes aislados de L.m.amazonensis y L.b.braziliensis con CI50 para Anfotericina-B entre 0.06-0.42ug/mL y 0.03-0.41 ug/mL, y para Miltefosina CI50 entre 1.67-12.93ug/ mL y 1.25-21.17ug/mL y finalmente para los Alcaloides de Galipea longiflora CI50 entre 14.4-39.55ug/mL y 6-22.05ug/mL, respectivamente. De esta manera el método colorimétrico XTT-PMS muestra cepas circulantes de Leishmania con un amplio rango de susceptibilidad in vitro. Así L.b.braziliensis frente a Anfotericina-B presento mayor dispersión mostrándonos CI50 de hasta 14 veces superior en relación al más sensible, frente a Miltefosina un dispersión de CI50 de hasta 17 veces más respecto al más sensible y solo de 3 veces más al tratarlos con los alcaloides de Galipea longiflora, dispersión de datos que podría reflejar reportes anteriores al tratar esta enfermedad en Bo-livia. El método colorimétrico es una herramienta importante para determinar la susceptibilidad a los antiparasitarios utilizados en Bolivia.
Palabras Clave
Susceptibilidad, antiparasitarios, XTT-PMS, Anfotericina B, Miltefosina, Galipea longiflora, L.m.amazonensis, L.b.braziliensis, cepas circulantes, Leishmania, Leishmaniasis, Bolivia.
Abstract
This paper presents research results in determining the in-vitro susceptibility of 27 Leishmania promastigote cultures adapted to in-vitro conditions from skin lesion sam-ples of patients lending assistance to IN LASA laboratories. Antiparasitic activity was measured in the following: Amphotericin B, Miltephosine, and the total alkaloids pres-ent in Galipea longiflora. Results using IC50 show that the various isolated strains of L.m.amazonensis and L.b.braziliensis show a wide spectrum of susceptibility to Amphotericin B, from 0.06-0.42ug/mL to 0.03-0.41 ug/mL; to Miltephosine, from 1.67-12.93ug/mL to 1.25-21.17ug/mL; and to the total alkaloids of Galipea longiflora, from 14.4-39.55ug/mL to 6-22.05ug/mL respec-tively. Application of the XTT-PMS colorim-etry method reveals strains of Leishmania in circulation with a wide spectrum of in-vitro susceptibility. L.b.braziliensis showed a wide IC50 dispersal with Amphotericin B, up to 14 times greater than the most sen-sitive strain; Miltephosine showed an IC50 dispersal up to 17 times greater than the most sensitive strain; whereas the alkaloids of Galipea longiflora showed an IC50 dispersal of only 3 times greater than the most sensitive strain. This dispersal data is con-gruent with previous research regarding the treatment of Leishmaniosis in Bolivia. Colo-rimetry techniques are an important tool in determining susceptibility to antiparasitics used in Bolivia.
Key Words
Susceptibility, antiparasitic, XTT-PMS, Amphotericin B, Miltephosine, Galipea longiflora, L.m.amazonensis, L.b.braziliensis, strains in circulation, Leishmania, Leishmaniosis, Bolivia.
]]> INTRODUCCIÓN
Las Leishmaniasis son un grupo de enfermedades transmitidas por vectores que causan diferentes enfermedades por distintas especies de Leishmania y están presentes en todos los continentes habitados. Se estima que alrededor de 12 millones de personas están actualmente infectadas, más de 350 millones viven en zonas de riesgo y 2 millones de nuevos casos se producen cada año (Wert et al., 2011).
En Bolivia, aproximadamente 800.000 individuos se encuentra en alto riesgo de enfermar con leishmaniasis (Mollinedo, 2007), donde se administra como tratamiento los antimoniales pentavalentes (SbV), Anfotericina-B, pen-tamidina y recientemente se introdujo la miltefosina (Soto et al., 2008 ; Soto et al., 2006), la actividad de estos compuestos varia de acuerdo a la especie de Leishmania involucrada. El mal uso de los medicamentos y la mala administración ya sea por bajas dosis y tratamientos discontinuos son unas de las razones que llevan a fallas terapéuticas y aparición de formas de resistencia (Gil et al., 2007) como es el caso del glucantime, que se encuentra bien documentado en países como la India (Osorio et al., 2005 ; Nascimento-Zauli et al., 2010), y en Bolivia con un 10% de falla en el tratamiento, (Bermudez etal., 2006) a su vez también se observa una disminución de la sensibilidad al tratamiento de la Anfotericina B el cual fue reportado en cepas de pacientes tomados tras varias recaídas al tratamiento (Croft et al., 2006), lo mismo sucede en pacientes con L.visceral coinfectados con VHI (Koert et al., 2011) y se tendría una cura de solo del 50% de pacientes con L.mucosa en un ensayo realizado en Palos Blancos-Bolivia (Soto et al., 2007).
Por otro lado existen reportes del uso de Miltefosina al tratar paciente con L.cutánea en Bolivia con un 70% de cura (Soto et al., 2008) y al tratar pacientes con L.mucosa leve el 83% de cura y solo el 53% en L. mucosa grave (Soto et al., 2007). Por lo mencionado y ante la carencia de estudios al respecto se hace patente el determinar la susceptibilidad in vitro de las cepas circulantes en Bolivia a través de un método semicuantitativo frente a los antiparasitarios convencionales utilizados para esta enfermedad, teniendo de esta forma un esquema de susceptibilidad in vitro antes de iniciar un determinado tratamiento, evitando así el uso de un medicamento que muestre poca susceptibilidad in vitro y su posible posterior fallo terapéutico y así poder escoger terapias alternativas.
MATERIAL Y METODOS
Cepas utilizadas para los ensayos
Se utilizaron 27 cepas de Leishmania, aisladas en el Instituto Nacional de Laboratorios de Salud - INLASA a través de aspirado de lesión con jeringa como parte del procedimiento de diagnostico clínico, la muestra obtenida se inoculo en medio difásico NNN suplementado con 10% de Suero Bovino Fetal (SBF), el cual fue incubado a 26°C y así obtener los promastigotes de Leishmania, finalmente se inoculo los promastigotes obtenidos a medio Scheneider suplementado con 10% de SBF para obtener poblaciones parasitarias adecuadas para los ensayos de susceptibilidad in vitro. Las cepas de referencia utilizadas fueron (Tabla 1)
Preparación de los antiparasitarios.
]]> Los medicamentos evaluados fueron Anfotericina-B (ANFOTERICIN-CRISTÁLIA), Miltefosina (IMPAVIDO), y los Alcaloides Totales de Galipea lon-giflora (CAT).La Anfotericina B se diluyo en Medio Scheneider donde a partir de una solución madre (1mg/mL) se realizaron diluciones seriadas en concentraciones de 0.62 hasta 0.01ug/mL, preparado previo a su uso.
También se preparo una solución madre de Miltefosina 10mg/mL al igual que CAT utilizando DMSO (GC-Sigma-Aldrich) como solvente, a partir de esta solución se realizaron diluciones seriadas desde 100 hasta 1,5ug/mL, las concentraciones de DMSO fueron < al 1%.
Preparación placa de 96 pozos.
Se tomó 20uL de un cultivo in vitro de promastigotes de Leishmania (solución madre) y se depositó en 180uL de glutaraldehido (5%) para fijar los parásitos y poderlos contar en cámara de Neubauer. Se ajustó la población a 3x106 parásitos/mL con medio Schneider (pH=6.2) al 10% de SBF, para luego distribuirlos en placas de 96 pozos (Nunc) en un volumen de 10OuL (Giménez et al., 2005). A continuación se procedió a añadir las distintas concentraciones de los antiparasitarios en volumen similar al de los parásitos, se diseñó un blanco para cada concentración de las drogas así por ejemplo 100uL medio Schneider más 100uL de la concentración de drogas en estudio. Se realizó además un control de parásitos más DMSO al 1% (concentración no tóxica para los parásitos), para evaluar la viabilidad, además se coloco en cada placa y como controles las cepas de referencia frente a las distintas drogas en estudio. Las placas se incubaron durante 72 horas a 26°C.
Obtención de la CI50 por el método colorimétrico XTT-PMS
Luego de 72 horas de incubación a 26°C se procedió a la determinación del CI50 mediante el método colorimétrico XTT-PMS previamente descrito por Cornelly.et.al (Salamanca et al., 2008) donde el análisis de datos fue realizado en Microsoft Excel programa 2003 transformando las absorbancia a porcentaje de viabilidad de los parásitos, donde el 100% representa la absorbancia del control de parasitos sin extracto La conversión del porcentaje de viabilidad a su correspondiente valor de CI50 que se realizó por función de tendencia lineal que ajusta la recta calculada por el método de los mínimos cuadrados a los valores de las matrices Y= porcentaje de inhibición y X = concentración de la droga, devolviendo los valores de Y=50% de inhibición a su respectivo valor de X.(Cornelly et al., 2003)
RESULTADOS
Todas las muestras fueron obtenidas de pacientes que cursaban con leish-maniasis cutánea, quienes procedían de diferentes zonas del departamento de La Paz excepto INL-JTD-09y INL-FLA-09 que procedían del departamento Beni.
]]> Luego de un periodo de adaptación de los promastigotes aislados de las lesiones al Medio Schenider, se trabajo con todos los aislados puesto que todos se adaptaron muy bien al nuevo medio, teniendo así poblaciones ideales de trabajo (3x106Parasitos/mL) para realizar los ensayos de susceptibilidad in vitro.Ensayos de susceptibilidad
En todos los experimentos las cepas de referencia se evaluaron en paralelo con los aislados, así se procedió al ensayo de susceptibilidad in vitro de lascepas identificadas molecularmente como Leishmania.mexicana.amazonen-sis y L. braziliensis.braziliensis (Cárdenas et al., 2011) frente a Anfotericina B, Miltefosina y Alcaloides totales de Galipea longiflora como muestra la Tabla 2
Se pudo observar una variable susceptibilidad in vitro de las dos especies de Leishmania estudiadas mostrándonos inicialmente una diferencia entre los CI50 de L.amazonensis y L.braziliensis (cepas de referencia) frente a Anfote-ricina-B y Miltefosina, con CI50 de casi el doble en el caso de L.amazonensis, siendo así este un parámetro de diferencia entre estas dos especies.
La respuesta in vitro a Anfotericina-B de las diferentes cepas nativas de L.amazonensis nos permitió dividirlas según su CI50 en tres diferentes categorías, aquellas que respondieron muy bien como la cepa INL-386 con CI50 de 0,06±0,02ug/ mL, aquellas que tuvieron una respuesta poco alentadora como la cepa INL-297 con CI50 de 0,42±0,007|jg/mL (5 cepas) y quienes se encuentran alrededor de la CI50 de la cepa de referencia (CI500,21 ±0,06 ug/mL) como la cepa INL-297 con CI50 de 0,20±0,06 ug/mL (5 cepas)(Tabla 2) De la misma manera L.amazonensis frente a Mil-tefosina mostro una susceptibilidad variable, teniendo una gran cantidad de cepas con CI50 muy sensibles como la cepa INL-001 con CI50 de 1,67±0,72 ug/mL, o aquella con respuestas por encima del control (CI5010,45±1,4 ug/mL) (10 cepas) como la cepa INL386 con CI50 de 12,93±4,94ug/mL(Tabla 2), y finalmente se observo resultados más homogéneos al tratar con los alcaloides de Galipea longiflora ya que los CI50 de una mayoría (9 cepas) estaba cerca de la cepa control (CI50 de 19,54±5,5ug/mL) como la cepa INL-386, con CI50 de 16,95±3,18ug/mL y solo 2 cepas se encuentra por encima de la cepa control como la cepa INL-297 con CI50 38,15±5,16μg/mL. Mostrándonos así también cepas que tiene CI50 altos para un tratamiento pero siendo estas mismas sensibles para otro tratamiento como la cepa INL-371. (Tabla2)
Así también el método colorimétrico XTT-PMS nos permitió clasificar en diferentes categorías la respuesta in vitro (CI50) de L.b.braziliensis frente a los diferentes antiparasitarios. (Figura1)
Como se observa en la figura1 se tiene una variable susceptibilidad de las diferentes cepas nativas frente a Anfotericina-B, así tenemos aquellas (5 cepas) que tienen respuesta poco favorable como la cepa INL-011 con CI50 de 0,41 ±0,14ug/ mL, pero también se observo cepas (4 cepas) muy sensibles a este tratamiento, como INL-264 con CI50 de 0,03±0,007ug/mL, y muchas cepas (7 cepas) que se encuentran alrededor del control (CI50 de 0,09±0,01 ug/mL) como la cepa INL-065 con CI50 de 0,10±0,03ug/mL. De la misma manera se observo cepas de L.braziliensis frente a Miltefosina con CI50 elevados (7 cepas) como la cepa INL-366 con CI50 de 21,17±1,70ug/mL, sin embargo también observamos cepas nativas (5 cepas) con CI50 bastante sensibles como la cepa INL-396 con CI50 de 1,25±0,07ug/mLy muchas otras que se encontraban alrededor (4 cepas) de la CI50 del control (CI50 de 5,26±1,04ug/mL) como la cepa INL-452 con CI50 de 5,7±1,11μg/mL. Frente a los alcaloides Totales de Galipea longiflora tenemos 2 cepas por encima del control, como la cepa INL-012 con CI50 de 22,05±4,31ug/mL, y por el contrario cepas que son bastante sensibles (14 cepas) al tratamiento como la cepa INL-452 conCI50de6±0,14μg/mL.
]]> DISCUSIONES
La importancia práctica de este trabajo es que a través del método colo-rimétrico XTT-PMS podemos determinar la susceptibilidad in vitro de cepas nativas de Leishmania con una gran variedad de respuestas a un determinado tratamiento, así por ejemplo las cepas nativas frente a Anfotericina B nos mostraron una gran dispersión de CI50 para L.braziliensis teniendo valores de hasta 0,41ug/mL que equivaldría 14 veces más en relación a la cepa más sensible (CI50=0,03 ug/mL), esta dispersión de CI50 fue un poco menos en caso de L.amazonensis de hasta 7 veces más respecto a la cepa más sensible. Datos in vitro que nos muestran que muchas cepas pueden responder muy favorablemente a la Anfotericina-B pero otros no, observando así in vitro cepas de Leishmania de nuestro medio que evidentemente son inhibidas por esta droga, pero a dosis más altas, lo cual podría tener su implicancia a la hora de tratar a una persona enferma con esta droga ya que la resistencia a Anfotericina B puede surgir como resultado del mayor uso clínico de este antiparasitario en la terapia.(Al-Mohammed et al., 2005) así se observo que solo el 50% de pacientes con Leishmania mucocutanea (L.braziliensis) tratados con Anfotericina B en Palos Blancos -Bolivia fueron curados.(Soto et al., 2007)
Existen reportes del uso de Miltefosina frente a L panamensis al tratar Leis-hmaniasis Cutanea en Colombia con un 91% de cura, pero no recomiendan este tratamiento para L.braziliensis de Guatemala (Yardleey et al., 2005 ; Soto et al., 2004), en Bolivia existen reportes de 36 personas curadas de 44 tratados con Miltefosina en pacientes que cursaban con L.cutanea (L.braziliensis), observándose aumento de la lesión y presencia de parásitos en los que el tratamiento fallo y al tratar pacientes con L.mucosa leve el 83% de cura y solo el 53% en L mucosa grave (Soto et al., 2008). La susceptibilidad in vitro nos mostro una dispersión de CI50 para L.braziliensis con CI50 de hasta 21,17±1,7ug/mL que equivaldría a 17 veces más con respecto al más sensible (CI501,25±0,07ug/mL) y para L.amazonensis de hasta 8 veces más con respecto a la cepa más sensible. Claramente el método colorimétrico XTT-PMS nos permite ver que tenemos cepas circulantes de Leishmania muy sensibles a la Miltefosina quienes probablemente responderían muy bien al tratamiento in vivo como se vio en el estudio en Bolivia, sin embargo nos encontramos también con cepas que presentan CI50 que están muy por encima del más sensible, cepas que pueden reflejar la falla en los ensayos clínicos hechos en Bolivia. Y finalmente es muy interesante observar que la dispersión de CI50 de los Alcaloides de Galipea longiflora frente a L.braziliensis y L.amazonensis es más homogéneo que los dos anteriores, quizá por tratarse de un producto natural y un conjunto de moléculas, que en su momento serían motivo de discusión cuando se tenga los datos de los ensayos clínicos llevados a cabo en la localidad de Palos blancos. Además pudimos observar cepas nativas que no son muy susceptibles a un tratamiento pero responsen muy bien a otro. No existe un tratamiento completamente efectivo (100% de cura) frente a la Leishmaniasis, sin embargo si existen cepas de pacientes, con bastante sensibilidad in vitro a un determinado tratamiento, el poder determinar esta susceptibilidad in vitro podría ser de gran utilidad. Constituyéndose de esta manera el método colorimétrico en una herramienta importante para tener un esquema de susceptibilidad in vitro a las drogas de uso convencional frente a diferentes especies de Leishmania circulantes en nuestro país.
REFERENCIAS
Al-Mohammed, C., Bates, M., Paul, A. (2005). Production and Characterization of Sta-ble Amphotericin-Resistant Amastigotes and Promastigotes of Leishmania Mexicana. American Society for Microbiology, 49:3274-3280. [ Links ]
Bermudez, H., Rojas, E., Garcia, L., Desjeux, P., Dujardin, J., Boelaert, M., Chappuis, F.(2006). Generic sodium stibogluconate is as safe and effective as branded meglumine anti-moniate, for the treatment oftegumentary leishmaniasis in Isiboro Secure Park, Bolivia. Annals of Tropical Medicine and Parasitolo-gy, 100,591-600. [ Links ]
Cardenas, Oscar., Romero, Danitza., Salamanca, Efrain., Santalla, José., Oporto, Patricia., Ar-teaga, Daniela., Alvares, Ma.Teresa., Terrazas, Enrique., Flores, Ninoska., Giménez, Alberto. (2011) Análisis de marcadores moleculares para la tipificación de Leishmania spp circulantes en el departamento de La Paz-Boli-via. Biofarbo,..... [ Links ]
Cornelly, W., Espinosa, O., Montenegro, H., Cubila, L., Capson, T., Ortega-Barria, E., Romero, L.(2003). Hydrosoluble formazan XTT: Its application to natural products drug disco-very for Leishmania. J Microbiol Meth, 55, 813-816. [ Links ]
Croft, S., Shyam, S., Fairlamb, A.(2006). Clin. Microbiol, 19(1), 111-126
]]>Giménez, A., Gupta, M., Deharo, E. (2005). Manual de Técnicas de laboratorio para la evaluación de sustancias tripanocidas y leish-manicidas, 89-90. [ Links ]
Gil, E., Cunha, L., Goncalves, A., Souza, A., Valde-rrama, N.(2007). Importancia de los Compuestos Inorgánicos en el Tratamiento de la Leishmaniasis. Latin American Journal of Pharmacy,26 (3), 454-461. [ Links ]
Koert, R., Rachel, H., Solomon, Ch., Endas-haw, Aderie., Turid, P., Collin, S., Davidson, R.(2011). Limited Effectiveness of High-Do-se Liposomal Amphotericin B (AmBisome) for Treatment of Visceral Leishmaniasis in an Ethiopian Population With High HIV Preva-lence. Clinical Infectious Diseases, 53,152-58. [ Links ]
Mollinedo, S. (2007). Leishmaniasis. Guía Operativa para el Control en Bolivia. 1 ed. La Paz: Programa Nacional de Control de las Leishmaniasis....... [ Links ]
Nascimento-Zauli, Danilo.,Yokoyama-Yasuyama, J., Pereira, L., Pelli de Oliveira, M., Ribeiro-Dias, F., Dorta, M., Uliana, S.(2010). In vitro sensitivity of Leishmania (Viannia) brazilien-sisand Leishmania (Leishmania) amazonensis Brazilian isolates to meglumine antimoniate and amphotericin B.Tropical Medicine And International Health, 15,68-76. [ Links ]
Osorio, E., Robledo, S., Arango, G., Muskus, C. (2005). Leishmania: papel de la glicoproteí-na P en la medición de la resistencia a medicamentos y estrategias de reversión. Bio-médica, 25, 242-260. [ Links ]
Salamanca, E., Ruiz, G., Ticona, J.C., Giménez, Alberto. (2008). Método colorimétrico - XTT: como evaluación de alto rendimiento de sustancias con actividad leishmanicida. Biofarbo, 15, 21-27. [ Links ]
Soto, J., Rea, J., Valderrama, M., Toledo, J., Soto, P., Valda, L., Berman, J.(2008). Efficacy of Milte-fosine for bolivian cutaneous leishmaniasis. Am J Trop Med Hyg, 78, 210-211. [ Links ]
Soto, J., Soto, P. (2006). Miltefosina oral para el tratamiento de la leishmaniasis. Biomédi-ca, 26, 207-217. [ Links ]
Soto, J., Arana, A., Toledo, J., Rizzo, N., Vega, J., Diaz, A., Gutierrez, P., Arboleda, M., Junge, K., Engel, J., Sindermann, H. (2004). Miltefosi-ne for New World Cutaneous Leishmaniasis. Clinical Infectious Diseases, 38,1266-1272. [ Links ]
Soto, J., Toledo, J., Valda, L., Balderrama, M., Rea, I., Parra, R., Ardiles, J., Soto, P., Gomez, A., Mo-lleda, F., Fuentelsaz, C., Anders, G., Sinder-man, H., Engel, J., Berman, J. (2007).Treatment of Bolivian Mucosal Leishmaniasis with Mil-tefosine. Clinical Infectious Diseases, 44, 350-356. [ Links ]
Soto, J., Rea, J., Balderrama, M., Toledo, J., Soto, P., Valda, L., Berman, J. (2008). Efficacy of Milte-fosine for Bolivian Cutaneous Leishmaniasis. Am. J. Trop. Med. Hyg,78, 210-211. [ Links ]
Wert, L., Alakurtti, S., Corral, M., Fortun-Sànchez, S.,Yli-Kauhaluoma,M.(2011).Toxicityofbe-tulin derivatives and in vitro effect on promastigotes and amastigotes of Leishmania infantum and L. donovani. The Journal of Antibiotics,1-7. [ Links ]
Yardley, V., Croft, L., Doncker, S., Dujardin, Jean-Claude., Siddhartha, K., Suman, C., LLanos-Cuentas, A., Chappuis, F. (2005). The Sensitivity of clinical isolates of Leishmania from Perú and Nepal to Miltefosine. The American Society of Tropical Medicine and Hy-giene, 73,272-275. [ Links ]
]]>