7,5mg/día, tras 6 meses de tratamiento es de 19,39% y de 18,88% a los 12 meses. La incidencia de procesos infecciosos asociada al uso de metotrexate (dosis >12,5mg/semana), es de 12,76% a 6 meses de tratamiento y de 13,27% a 12 meses. Conclusiones En pacientes adultos de ambos sexos, sin factores de riesgo asociados, la corticoterapia prolongada (Prednisona en dosis mayor a 7.5mg/día durante más de 6 meses de tratamiento) produce el desarrollo de procesos infecciosos con mayor frecuencia y gravedad que la terapia con metotrexate incluso a dosis intermedia-alta (MTX >12.5mg / semana).]]>
7.5mg/day, after 6 months of treatment is 19.39% and 18.88% at 12 months. The incidence of infectious processes associated with the use of metotrexate (dose >12.5mg/week), is 12.76% at 6 months of treatment and 13.27% at 12 months. Conclusions In adult patients of both sexes, without associated risk factors, prolonged corticotherapy (Prednisone in doses greater than 7.5mg/day for more than 6 months of treatment) produces the development of infectious processes with greater frequency and severity than therapy with metotrexate even at intermediate-high dose (MTX >12.5mg / week).]]>
INCIDENCIA DE INFECCIONES EN PACIENTES CON ARTRITIS REUMATOIDE EN TRATAMIENTO CORTICOIDEO E INMUNOSUPRESOR
INCIDENCE OF INFECTIONS IN PATIENTS WITH RHEUMATOID ARTHRITIS IN CORTICOSTEROID AND IMMUNOSUPPRESSIVE TREATMENT
Dr. Raúl Arteaga Coariti1, Dra. Patricia Chacón Yucra2, Dr. Guillermo Urquizo Ayala3
1,2 Especialistas en Medicina Interna, Hospital de Clínicas
3 Jefe de la Unidad de Medicina Interna Hospital de Clínicas, La Paz, Bolivia
RESUMEN
Introducción
La artritis reumatoide (AR) es una enfermedad inflamatoria autoinmune, que requiere tratamiento farmacológico por tiempo muy prolongado. Se prescribe para su tratamiento fármacos con capacidad antiinflamatoria y potencial efecto inmunosupresor. Con estos fármacos los pacientes presentan menor intensidad inflamatoria, pero a la vez existe el riesgo de procesos infecciosos, siendo éstos, una importante causa de morbilidad y mortalidad.
Objetivo
Analizar la incidencia de infección durante el tratamiento corticoideo vs inmunosupresor en la terapia crónica en pacientes con artritis reumatoide.
Material y métodos
]]> Estudio de tipo analítico, observacional, retrospectivo, con selección por intención, no controlado, de cohorte, con estudio de riesgo, incidencia y asociación cruzada, realizado en el Servicio de Reumatología del Hospital de Clínicas de La Paz, Bolivia; en pacientes con diagnóstico de AR entre las gestiones 2010 - 2020, tanto en consultorio externo y sala de internación.Se seleccionaron pacientes con adultos, ambos sexos, con edad mayor a 18 años, con diagnóstico de artritis reumatoide según clasificación ACR 2010, clinimetría CDAI en grado de actividad, con indicación de tratamiento asociado (corticoide + metotrexato o incluso adición de cloroquina / hidroxicloroquina) de acuerdo a guías ACR/EULAR, que realice control regular (bimensual).
Resultados
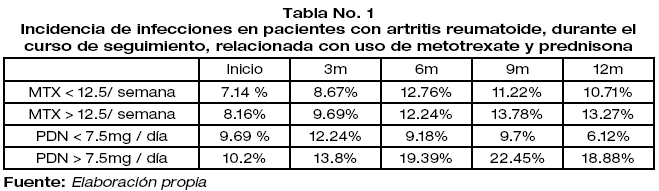
La incidencia de procesos infecciosos asociada al uso de prednisona con dosis >7,5mg/día, tras 6 meses de tratamiento es de 19,39% y de 18,88% a los 12 meses. La incidencia de procesos infecciosos asociada al uso de metotrexate (dosis >12,5mg/semana), es de 12,76% a 6 meses de tratamiento y de 13,27% a 12 meses.
Conclusiones
En pacientes adultos de ambos sexos, sin factores de riesgo asociados, la corticoterapia prolongada (Prednisona en dosis mayor a 7.5mg/día durante más de 6 meses de tratamiento) produce el desarrollo de procesos infecciosos con mayor frecuencia y gravedad que la terapia con metotrexate incluso a dosis intermedia-alta (MTX >12.5mg / semana).
Palabras clave
Inmunosupresión, corticoterapia prolongada, artritis reumatoide
ABSTRACT
Introduction
]]> Rheumatoid arthritis is an autoimmune inflammatory disease, which requires pharmacological treatment for a very long time. It is prescribed for its treatment drugs with anti-inflammatory capacity and potential immunosuppressive effect. With these drugs patients present lower inflammatory intensity, but at the same time there is a risk of infectious processes, these being an important cause of morbidity and mortality.Objective
To analyze the risk of infection with corticosteroid vs. immunosuppressive treatment in chronic therapy in patients with rheumtaoid arthritis.
Material and methods
Analytical, observational, retrospective study, with selection by intention, uncontrolled, cohort, with study of risk, incidence and cross association, carried out in the Rheumatology Service of the Hospital de Clínicas, La Paz, Bolivia, in patients who were diagnosed with RA between the 2010 - 2020 management, both in the outpatient clinic and the hospitalization room. Patients were selected with adults, both sexes, aged over 18 years, with a diagnosis of rheumatoid arthritis according to ACR 2010 classification, CDAI clinimetry in degree of activity, with indication of associated treatment (corticoid + methoroxate or even addition of chloroquine / hydroxychloroquine) according to ACR/EULAR guidelines, which perform regular control (bi monthly).
Results:
The incidence of infectious processes associated with the use of prednisone with doses >7.5mg/day, after 6 months of treatment is 19.39% and 18.88% at 12 months. The incidence of infectious processes associated with the use of metotrexate (dose >12.5mg/week), is 12.76% at 6 months of treatment and 13.27% at 12 months.
Conclusions
In adult patients of both sexes, without associated risk factors, prolonged corticotherapy (Prednisone in doses greater than 7.5mg/day for more than 6 months of treatment) produces the development of infectious processes with greater frequency and severity than therapy with metotrexate even at intermediate-high dose (MTX >12.5mg / week).
Keywords
]]> Immunosuppression, prolonged corticotherapy, rheumatoid arthritis
I. INTRODUCCION
La artritis reumatoide es una enfermedad inflamatoria autoinmune, de etiología desconocida, que requiere tratamiento farmacológico por tiempo prolongado e incluso de por vida. Dentro de su tratamiento, se encuentra contemplado el uso de fármacos con capacidad antiinflamatoria y potencial efecto inmunosupresor. Por este motivo los pacientes al mismo tiempo que desarrollan menor intensidad inflamatoria también presentan riesgo de enfrentarse a infecciones, siendo ésta, una importante causa de morbilidad y mortalidad. Esto ha generado un debate a nivel mundial sobre el tiempo de duración del uso de estos fármacos, así como las dosis, y su efecto en combinación. Se cree que la terapia con corticoides, se asocia con un mayor riesgo de infección, y, por otra parte, hay quienes afirman que el potencial efecto inmunosupresor de los denominados fármacos modificadores de la enfermedad reumatológica es el principal causante de la predisposición a infecciones. Sorprendentemente, a pesar de varias décadas de experiencia clínica, no existen consensos sobre los riesgos asociados a esta terapéutica.
La labor del medico clínico, es abordar los factores de riesgo de complicaciones (infecciosas en este caso ), de manera precoz, pero además tener conceptos claros en la interpretación de la clínica y los estudios laboratoriales ya que estos evalúan el grado de actividad inflamatoria, y, por tanto, marcan el curso de tratamiento a seguir. La falta de clasificación e interpretación de los métodos clinimétricos de seguimiento en la artritis reumatoide lleva a una mala interpretación de la actividad de esta enfermedad, por tanto, incrementa la probabilidad de realizar tratamientos con potencialidad inmunosupresora mas profunda, es decir, mayor dosis, tiempos mas prolongados, mayor combinación de fármacos. Por tanto, la presente investigación es útil para plantear esquemas de tratamiento, de mayor seguridad, pero de igual eficacia, para el paciente, así como el personal medico.
II. PLANTEAMIENTO DEL PROBLEMA
La infección es una causa importante de morbilidad y mortalidad en pacientes con artritis reumatoide (AR).
La mayor incidencia se ha atribuido a la enfermedad misma, a factores asociados como el tabaquismo y la terapia inmunosupresora, o finalmente una combinación de estos. Se cree que la terapia con glucocorticoides (GC), ampliamente utilizada en el tratamiento de la AR, se asocia con un mayor riesgo de infección, así como con otros efectos adversos bien establecidos. Se sabe que los GC alteran la función de los fagocitos y suprimen la inmunidad celular, lo que aumenta el riesgo de infección. Sin embargo, la medida en que la terapia con GC contribuye al aumento del riesgo observado en la AR no está clara.
]]> Se han realizado revisiones sistemáticas para abordar la eficacia de la terapia GC, así como múltiples resultados de seguridad de estudios controlados aleatorizados (ECA) en poblaciones con AR. Y si bien existen documentos en los que se busca establecer esta asociación, son contradictorios unos de otros, algunos señalando el evidente riesgo a procesos infecciosos, así como aquellos que no establecen un riesgo relativo que justifique eliminar a los GC del esquema terapéutico actual. Por otra parte, también se utilizan en el esquema de tratamiento fármacos modificadores de la enfermedad reumatología (DMARD), que se consideran ocasionan inmunocompromiso en el paciente con AR. Sin embargo, el en análisis comparativo del riesgo frente a GC se encontraron estimaciones más altas (riesgo de infecciones) en OR para la exposición a glucocorticoides que frente DMARD; incluso algunos autores consideran que DMARD en realidad disminuye el riesgo de infección. Además, en la búsqueda bibliográfica realizada no se encontró estudios realizados en nuestro medio. Por lo tanto, buscamos establecer el riesgo de infecciones asociado al uso de tratamiento corticoideo y DMARD, o sus combinaciones en pacientes con diagnostico de artritis reumatoide, del servicio de reumatología Hospital De Clínicas, con edades entre 18-60 años.
III. METODOLOGIA
1. DISEÑO DE INVESTIGACION
Estudio de tipo analítico, observacional, retrospectivo, con selección por intención, no controlado, de cohorte, con estudio de riesgo, incidencia y asociación cruzada, realizado en la unidad de reumatología, del Hospital de Clínicas Universitario, con datos de pacientes que realizaron seguimiento por diagnostico de AR entre las gestiones 2010 - 2020, tanto en consultorio externo y sala de internación del servicio de reumatología.
Se seleccionaron pacientes con adultos, ambos sexos, con edad mayor a 18 años, con diagnostico de artritis reumatoide según clasificación ACR 2010, clinimetría CDAI en grado de actividad, con indicación de tratamiento asociado (corticoide + metotrexate o incluso adición de cloroquina / hidroxicloroquina) de acuerdo a guías ACR/EULAR, que realice control regular (bi mensual) en el servicio de reumatología del Hospital de Clínicas Universitario.
Se consideró grupo expuesto aquellos que presentaban: a)
a) CRITERIOS DE INCLUSIÓN:
Pacientes adultos, con edad superior a 18 años, cumplidos al 1o marzo de 2020, ambos sexos, que cumplan criterios de clasificación de acuerdo a criterios ACR 2010 y cuenten con clinimetría DAS28 en grado de actividad (DAS28 > 2,6) al ingreso al estudio. Tratamiento en base a esquema asociado (corticoide / DMARD sintético no biológico), y que realice control mensual en servicio de reumatología - Hospital de clínicas.
b) CRITERIOS DE EXCLUSIÓN:
]]> Pacientes con comorbilidad demostrada que incremente riesgo de procesos infecciosos (Ej. Diabetes mellitus, alteración anatómica de vías urinarias, respiratorias, proceso oncológico, inmunodeficiencia secundaria).Pacientes que abandonen seguimiento en consultorio externo del servicio de reumatología. Pacientes con cumplimiento irregular al esquema de tratamiento indicado. Pacientes que durante el curso del estudio rechazaran seguir en el grupo de estudio.
a. OBJETIVOS: Determinar el riesgo de desarrollo de infecciones asociadas al tratamiento corticoideo e inmunosupresor:
i. Describir la incidencia de procesos infecciosos, en pacientes con diagnostico de artritis reumatoide, que reciban corticoterapia a dosis alta (Prednisona ≥ 7,5mg/día)
ii. Describir la incidencia de procesos infecciosos severos y no severos, en pacientes con diagnostico de artritis reumatoide, que reciban metotrexate con dosis superior a 12,5mg / semana.
iii. Describir el riesgo relativo asociado a sufrir procesos infecciosos, en pacientes que reciban corticoterapia a dosis alta, prolongada (Dosis > Prednisona 7,5mg ≥ 6 meses)
iv. Describir el riesgo relativo asociado a sufrir procesos infecciosos, en pacientes que reciban corticoterapia a dosis alta prolongada
v. Comparar el riesgo relativo entre el uso de corticoterapia prolongada a dosis elevadas y el uso de metotrexate > 12.5mg/ semana.
]]> IV. RESULTADOS
Tras la aplicación de los criterios de exclusión / exclusión de selección se determinó universo poblacional de 2660 pacientes, aplicando: a) Poder: 80%. B) Radio expuestos / no expuestos: 1:1. C) % prevalencia en el grupo no expuesto: 5,3 %, prevalencia % de resultado en el grupo expuesto: 13.3%, se obtuvo una muestra de 414 pacientes. De los cuales se procedió con distribución en dos grupos de igual numero. Grupo de pacientes no expuestos: 207, grupo de pacientes expuestos: 207.
La incidencia de procesos infecciosos asociada al uso de prednisona con dosis >7,5mg / día, tras 6 meses de tratamiento es de 19,39% y de 18,88% a los 12 meses. La incidencia de procesos infecciosos asociada al uso de metotrexate (dosis >12,5mg/semana), es de 12,76% a 6 meses de tratamiento y de 13,27% a 12 meses. Resultados desglosados de manera trimestral y comparativa para estos grupos se encuentran reflejados en la tabla No.1

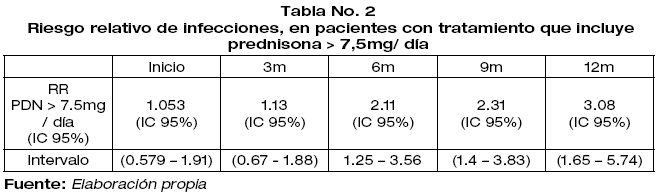
De acuerdo al análisis estadístico realizado el uso de corticoterapia con prednisona con dosis ≥7.5mg / día, se asocia con un RR 2.11 (IC 95% [1.25 - 3.56]) a 6 meses y RR 3.08 (IC 95% [1.65 - 5,74] a 12 meses de tratamiento (Tabla No. 2)
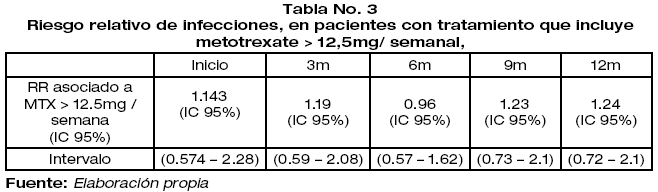
De acuerdo al análisis estadístico realizado el uso de metotrexate con dosis superior a 12.5mg / semana, se asocia con un RR 0.96 (IC 95% [0.57 – 1.62]) a 6 meses y RR 1.24 (IC 95% [0.72 – 2.1] a 12 meses de tratamiento (Tabla No. 3)
]]>
V. CONCLUSIONES
a. El uso de prednisona con dosis >7.5mg / día posterior al 6to mes de tratamiento incrementa la incidencia de procesos infecciosos.
b. El uso de metotrexate con dosis >12.5mg / semana, mantenido mas allá del 6to mes de tratamiento, no se relaciona con un incremento importante en la incidencia de procesos infecciosos.
c. El tratamiento con prednisona >7.5mg / día se asocia con un incremento escalonado y sostenido en el riesgo de procesos infecciosos hasta triplicar el mismo a los 12 meses de tratamiento (RR 3.08 IC 95% (1.65-5.74)
d. El tratamiento con metotrexate >12.5mg / semana no se asocia a un incremento del riesgo de procesos infecciosos (RR: 1.24 IC 95% (0.72 - 2.1) incluso mantenido a 12 meses de tratamiento.
e. Se concluye que, en pacientes adultos de ambos sexos, sin factores de riesgo asociados, la corticoterapia prolongada (PDN > 7.5mg/día sostenido mas allá del 6to mes de tratamiento) es un factor más importante en relación al desarrollo de procesos infecciosos que la terapia con metotrexate incluso a dosis intermedia-alta (MTX >12.5mg / semana).
VI. DISCUSION
]]> La artritis reumatoide (AR) es una enfermedad inflamatoria crónica que puede afectar articulaciones pequeñas y grandes, con posibilidad para producir su destrucción, así como su deterioro funcional, con potencial afección de la calidad de vida de los pacientes, incluso asociándose a supervivencia reducida, debido a la terapia o comorbilidades relacionadas con la enfermedad (1, 2). La carga individual es el resultado de déficits musculoesqueléticos, con la consiguiente disminución de la función física, la calidad de vida y el riesgo comórbido acumulativo (3). Por lo tanto, los esfuerzos para establecer el diagnóstico temprano, iniciar el tratamiento con prontitud y diseñar estrategias de tratamiento para controlar la inflamación y reducir o prevenir el consiguiente daño son primordiales. Esencialmente, la AR es una enfermedad por formación de auto anticuerpos (4). Con una terapia efectiva, las concentraciones de RF y ACPA disminuyen, pero los pacientes rara vez se vuelven negativos para ACPA, mientras que la RF puede disminuir e incluso los pacientes puedan ser seroconvertidos a negatividad para RF (5, 6), por tanto, en el seguimiento, no es realmente útil realizar mediciones seriadas de estos autoanticuerpos, La evaluación de la actividad de la enfermedad debe realizarse por uso de medios clinimétricos, los cuales hacen objetivo el seguimiento de los pacientes, entre estos CDAI, SDAI, DAS28 son los mas usados en nuestro medio, a la vez, utilizar medios laboratoriales (proteína C reactiva, VES) también son útiles en el seguimiento. Los fármacos antirreumáticos modificadores de la enfermedad (FARME o DMARD) disminuyen la inflamación y, por definición, reducen la progresión del daño estructural. Los antiinflamatorios no esteroideos (AINE), reducen el dolor, la rigidez e incluso pueden mejorar la función física, pero no interfieren con el daño articular, por tanto, no se consideran modificadores de la enfermedad. Al contrario, los glucocorticoides ofrecen efectos sintomáticos rápidos y modificadores de la enfermedad, pero están asociados con efectos secundarios graves a largo plazo, entre los que destacan los procesos infecciosos (7, 8).De acuerdo con las recomendaciones EULAR (9), el tratamiento debe iniciarse con un DMARD sintético convencional, idealmente metotrexate, más glucocorticoides en dosis bajas. Iniciar con tratamiento biológico no es lo más adecuado. Primero, los ensayos clínicos que compararon metotrexato más glucocorticoides con combinaciones de metotrexato más un agente biológico, no han mostrado diferencias significativas en los resultados (10), por tanto, no es sustancialmente mejor iniciar tratamiento con bDMARD que con metotrexate. En el caso de no encontrar respuesta terapéutica adecuada la dosis debe optimizarse, aumentando la dosis de metotrexate hasta 25mg / semanal (aproximadamente 0.3 mg / kg).
Las dosis bajas de glucocorticoides (equivalencia a prednisone <7,5 mg diarios) combinadas con metotrexato confieren protección estructural aditiva cuando se comparan con metotrexato solo (10). Con respecto a la elección de un DMARD sintético convencional, el metotrexato se considera el fármaco de anclaje que también optimiza la eficacia de los DMARD biológicos (bDMARD) (18, 20). Sin embargo, todavía no se ha demostrado de manera concluyente que el metotrexato sea superior a otros DMARD sintéticos convencionales (csDMARD) clínica o estructuralmente; más bien, las comparaciones con sulfasalazina o leflunomida revelaron resultados similares, pero las dosis de metotrexato en estos estudios fueron bajas en comparación con las que se usan actualmente (23).
Las recomendaciones nos mencionan que glucocorticoides orales deben reducirse y buscar suspenderse dentro de los 6 meses, cuando los csDMARD deberían haber inducido una mejora significativa (9). Varias revisiones que abordaron dosis más altas de glucocorticoides en el brazo de triple terapia llegan a conclusiones diferentes (11,12). De hecho, si se aplica la misma dosis de glucocorticoides en grupos de estudio, los ensayos controlados aleatorios más recientes no muestran una ventaja clínica, funcional o estructural significativa de combinaciones de DMARD sintéticas convencionales en comparación con la monoterapia con metotrexato, sino más toxicidad e interrupciones (13, 14). Todos los bDMARD exhiben una mayor eficacia cuando se combinan con metotrexato y presumiblemente cualquier otro csDMARD, especialmente leflunomida (15). Ningún bDMARD utilizado como monoterapia ha demostrado una superioridad clínica o funcional estadísticamente significativa en comparación con el metotrexato (16, 17, 18). Además, el metotrexato en combinación con glucocorticoides mostró eficacia clínica, funcional y estructural similar al metotrexato más agente biológico (19).
Como ya se mencionó, la AR se asocia con una morbilidad significativa y una supervivencia reducida. Se ha sugerido un mayor riesgo de infecciones asociado a AR, así como al tratamiento asociado (20), con especial preocupación con respecto a las infecciones de tejidos blandos, genitourinarias y pulmonares. El grado en que este riesgo puede ser elevado por fármacos inmunosupresores (DMARD y corticoides), no está completamente claro. Sin embargo, algunos estudios nos dan luces: Dixon y col. (21) encontraron, en pacientes con AR tratados con DMARD, una tasa de infecciones graves igual a 414 eventos por 10 000 pacientes/año. Por el contrario, Kroesen et al. (22) examinaron los datos de un registro de pacientes con AR a un período de 2 años. En su estudio reporta tasa de infecciones sorprendentemente baja (80 casos por 10000 pacientes/año), lo que puede explicarse en parte porque estos pacientes con RA eran relativamente jóvenes (edad mediana de 53 años). Una nueva revisión sistémica / metaanálisis realizada por Dixon, encontró 5,8% de infecciones respecto a 5,4% de pacientes que no incluyeron GC en su tratamiento. El riesgo relativo estimado de infección asociado con la terapia con GC fue de 0,97 (RR: 0,97 [0,69 - 1,36]) (23). Así también desarrollo un análisis de estudios observacionales, en la que la terapia con GC sistémicos se asoció con un mayor riesgo de infecciones (RR, 1.67 [1.49, 1.87]). Por medio del mismo, los autores concluyeron en que no está claro en qué medida el riesgo de infección está influenciado por la terapia GC acumulativa. Sin embargo, la dosis de la terapia GC varió sustancialmente entre los ECA y los estudios observacionales, quizás siendo el motivo por el se muestran resultados tan dispares. Con sus estudios concluyo: "...que el riesgo de infección asociado con la terapia de GC sistémica en pacientes con RA es incierto. Sin embargo, un hallazgo consistente es que no podemos descartar la posibilidad de un mayor riesgo clínicamente importante" (1). Al contrario, Doran et al, concluyeron que el uso de glucocorticoides sistémicos se asociaba a RR: 2.56, (IC del 95%: 2.29-2.85); azatioprina RR: 1,52(IC 95%: 1,18 a 1,97) y metotrexate RR: 1.16 (IC 95%: 1.02-1.33) siendo este el DMARD que menos asociación tuvo con procesos infecciosos (21). De acuerdo a nuestros hallazgos ratificamos estas observaciones, siendo que se demuestra que el tratamiento con dosis elevadas de prednisona, por tiempos prolongados se constituyen en un factor de riesgo mayor respecto al uso de metotrexate. De la misma manera, estos hallazgos fueron descritos en revisiones previas realizadas en nuestro medio (25).
La presente investigación presenta varios puntos débiles, se hubiera enriquecido si se hubiera podido contar con valores de clinimetría, en todos los pacientes incluidos en el estudio, siendo que existe una relación casi lineal entre la actividad de la enfermedad y el deterioro de la función física o la progresión del daño (3). Así, podríamos obtener datos en relación a la actividad de la enfermedad y la el uso de MTX o PDN, las dosis y por tanto el RR asociado a los niveles de actividad de los pacientes. Esto se planteará para futuras investigaciones.
VII. RECOMENDACIONES.
a. De ser posible la corticoterapia debe llevar un curso descendente, hasta alcanzar dosis <7.5mg / día posterior al 6to mes. Esta practica disminuirá la de incidencia de procesos infecciosos. Por tanto, se sugiere establecerlo como una medida de practica adecuada en el curso de seguimiento a pacientes con AR. Los GC son y seguramente seguirán siendo un fármaco importante en el esquema de tratamiento de la AR. Sin embargo, incluso la literatura revisada señala que entre 30% - 60% de los pacientes con AR permanecen con GC a largo plazo, situación que consideramos, debe ser individualizada en el curso de tratamiento.
b. Las infecciones son una complicación común, costosa y mórbida para los pacientes con AR, la actividad de la enfermedad, la multimorbilidad y los medicamentos potencialmente inmunosupresores contribuyen al riesgo de infección. Conociendo esto, es muy frecuente encontrar pacientes que reciben corticoterapia a dosis altas por tiempos muy prolongados, en lugar de iniciar tratamiento con DMARD debido a que se asume que estos tienen mayor efecto inmunosupresor en los pacientes. Por medio de los resultados planteados en el presente estudio podríamos refutar en cierto grado esta concepción. Al contrario, queda demostrado que el uso de MTX es mas seguro que el uso de PDN a dosis atas y por tiempos prolongados. Sin embargo, es finalmente el clínico quien debe valorar el curso de tratamiento mas adecuado para el paciente.
]]> c. La columna vertebral de la terapia de mantenimiento actual para la AR sigue siendo csDMARD, que en nuestro medio principalmente incluye metotrexato. Los datos obtenidos por medio de este estudio proporcionan información importante sobre el riesgo de infección con metotrexato, demostrando su seguridad, ya se asocian a incremento estadísticamente no significativo en el análisis de RR para infecciones. Al no presentar mayor incidencia en procesos infecciosos administrar metotrexate con dosis >12.5mg / semana se podría considerar como practica segura e incluso considerarse con una practica beneficiosa en el tratamiento de AR. En conjunto, este trabajo y los datos de observación de cohortes internacionales revisadas sugieren, que podríamos considerar usar e incluso llegar a mantener esta dosis con un margen de seguridad amplio.
REFERENCIAS
1. Dixon WG, Suissa S, Hudson M. The association between systemic glucocorticoid therapy and the risk of infection in patients with rheumatoid arthritis: systematic review and meta-analyses. Arthritis Res Ther. BioMed Central; 2011 Aug 31;13(4):R139–14.
2. Lampropoulos CE, Orfanos P, Bournia V-K, Karatsourakis T, Mavragani C, Pikazis D, et al. Adverse events and infections in patients with rheumatoid arthritis treated with conventional drugs or biologic agents: a real world study. Clin Exp Rheumatol. 2015 Mar;33(2):216–24.
3. Smolen JS, Aletaha D, McInnes IB. Rheumatoid arthritis. Lancet. 2016 Oct 22;388(10055):2023–38.
4. Zhao X, Okeke NL, Sharpe O, Batliwalla FM, Lee AT, Ho PP, et al. Circulating immune complexes contain citrullinated fibrinogen in rheumatoid arthritis. Arthritis Res Ther. BioMed Central; 2008;10(4):R94–13.
5. Barra L, Pope J, Bessette L, Haraoui B, Bykerk V. Lack of seroconversion of rheumatoid factor and anti-cyclic citrullinated peptide in patients with early inflammatory arthritis: a systematic literature review. Rheumatology (Oxford). 2011 Feb;50(2):311–6.
6. Böhler C, Radner H, Smolen JS, Aletaha D. Serological changes in the course of traditional and biological disease modifying therapy of rheumatoid arthritis. Annals of the Rheumatic Diseases. BMJ Publishing Group Ltd; 2013 Feb;72(2):241–4.
7. Urquizo G, Arteaga R, Chacon P. Utilidad de los reactantes de fase aguda en el diagnóstico clínico. Rev Med La Paz [Internet]. 2019;25(2):91–8.
]]> 8. Kirwan JR. The effect of glucocorticoids on joint destruction in rheumatoid arthritis. The Arthritis and Rheumatism Council Low-Dose Glucocorticoid Study Group. New England Journal of Medicine. 1995 Jul 20;333(3):142–6.9. Doran MF, Crowson CS, Pond GR, O’Fallon WM, Gabriel SE. Frequency of infection in patients with rheumatoid arthritis compared with controls: a population-based study. Arthritis & Rheumatism. John Wiley & Sons, Ltd; 2002 Sep;46(9):2287–93.
10. Smolen JS, Landewé R, Breedveld FC, Buch M, Burmester G, Dougados M, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological diseasemodifying antirheumatic drugs: 2013 update. 2014. pp. 492–509.
11. Nam JL, Villeneuve E, Hensor EMA, Conaghan PG, Keen HI, Buch MH, et al. Remission induction comparing infliximab and high-dose intravenous steroid, followed by treat-to-target: a double-blind, randomised, controlled trial in new-onset, treatment-naive, rheumatoid arthritis (the IDEA study). Annals of the Rheumatic Diseases. 2014 Jan;73(1):75–85.
12. Smolen JS, Aletaha D, Keystone E. Superior efficacy of combination therapy for rheumatoid arthritis: fact or fiction? Arthritis & Rheumatism. John Wiley & Sons, Ltd; 2005 Oct;52(10):2975–83.
13. Gaujoux-Viala C, Nam J, Ramiro S, Landewé R, Buch MH, Smolen JS, et al. Efficacy of conventional synthetic disease-modifying antirheumatic drugs, glucocorticoids and tofacitinib: a systematic literature review informing the 2013 update of the EULAR recommendations for management of rheumatoid arthritis. Annals of the Rheumatic Diseases. 2014 Mar;73(3):510–5.
14. Verschueren P, De Cock D, Corluy L, Joos R, Langenaken C, Taelman V, et al. Methotrexate in combination with other DMARDs is not superior to methotrexate alone for remission induction with moderate-to-high-dose glucocorticoid bridging in early rheumatoid arthritis after 16 weeks of treatment: the CareRA trial. Annals of the Rheumatic Diseases. BMJ Publishing Group Ltd; 2015 Jan;74(1):27–34.
15. de Jong PH, Hazes JM, Han HK, Huisman M, van Zeben D, van der Lubbe PA, et al. Randomised comparison of initial triple DMARD therapy with methotrexate monotherapy in combination with low-dose glucocorticoid bridging therapy; 1-year data of the tREACH trial. Annals of the Rheumatic Diseases. 2014 Jul;73(7):1331–9.
16. De Stefano R, Frati E, Nargi F, Baldi C, Menza L, Hammoud M, et al. Comparison of combination therapies in the treatment of rheumatoid arthritis: leflunomide-anti-TNF-alpha versus methotrexateanti-TNF-alpha. Clin Rheumatol. Springer-Verlag; 2010 May;29(5):517–24.
17. Burmester GR, Rigby WF, van Vollenhoven RF, Kay J, Rubbert-Roth A, Blanco R, et al. Tocilizumab combination therapy or monotherapy or methotrexate monotherapy in methotrexate-naive patients with early rheumatoid arthritis: 2-year clinical and radiographic results from the randomised, placebo-controlled FUNCTION trial. Annals of the Rheumatic Diseases. 2017 Jul;76(7):1279–84.
]]> 18. Breedveld FC, Weisman MH, Kavanaugh AF, Cohen SB, Pavelka K, van Vollenhoven R, et al. The PREMIER study: A multicenter, randomized, double-blind clinical trial of combination therapy with adalimumab plus methotrexate versus methotrexate alone or adalimumab alone in patients with early, aggressive rheumatoid arthritis who had not had previous methotrexate treatment. Arthritis & Rheumatism. John Wiley & Sons, Ltd; 2006 Jan;54(1):26–37.19. Klareskog L, van der Heijde D, de Jager JP, Gough A, Kalden J, Malaise M, et al. Therapeutic effect of the combination of etanercept and methotrexate compared with each treatment alone in patients with rheumatoid arthritis: double-blind randomised controlled trial. Lancet. 2004 Feb 28;363(9410):675–81.
20. Scher JU, Littman DR, Abramson SB. Microbiome in Inflammatory Arthritis and Human Rheumatic Diseases. Arthritis Rheumatol. John Wiley & Sons, Ltd; 2016 Jan;68(1):35–45.
21. Doran MF, Crowson CS, Pond GR, O’Fallon WM, Gabriel SE. Frequency of infection in patients with rheumatoid arthritis compared with controls: a population-based study. Arthritis & Rheumatism. John Wiley & Sons, Ltd; 2002 Sep;46(9):2287–93.
22. Dixon WG, Watson K, Lunt M, Hyrich KL, Silman AJ, Symmons DPM, et al. Rates of serious infection, including site-specific and bacterial intracellular infection, in rheumatoid arthritis patients receiving anti-tumor necrosis factor therapy: results from the British Society for Rheumatology Biologics Register. Arthritis & Rheumatism. John Wiley & Sons, Ltd; 2006 Aug;54(8):2368–76.
23. Kroesen S, Widmer AF, Tyndall A, Hasler P. Serious bacterial infections in patients with rheumatoid arthritis under anti-TNF-alpha therapy. rheumatology. 2003 May;42(5):617–21.
24. Bernatsky S, Hudson M, Suissa S. Anti-rheumatic drug use and risk of serious infections in rheumatoid arthritis. rheumatology. 2007 Jul;46(7):1157–60.
25. Arteaga R, Chacon P, Urquizo G. Riesgo de infecciones en pacientes con tratamiento corticoideo prolongado. Rev Med La Paz. 2020;26(2):57–66.
]]>