
APLICACIÓN DE LA GUÍA DE TOKIO EN COLECISTITIS AGUDA LITIÁSICA
TOKYO GUIDE APPLICATION IN LITHIASIC ACUTE CHOLECYSTITIS
Dra. Coral Marina Ramos Loza*, Dr. Jhosep Nilss Mendoza Lopez Videla **, Dr. Javier Alejandro Ponce Morales***
* Médico Residente Tercer año Cirugía General Hospital General La Paz
** Médico Emergencias Hospital Arcoíris ]]>
Los autores niegan conflictos de intereses.
Autor responsable de correspondencia: Dra. Coral Marina Ramos Loza. Celular:75853438 email: marin.coral1676@gmail.com
RECIBIDO: 11/04/2018
APROBADO: 02/05/2018
RESUMEN
Las Guías de Tokio (TG-13) se utilizan para diagnosticar, evaluar la gravedad y guiar el manejo de la Colecistitis Aguda (CA). El objetivo de nuestro estudio fue aplicar las Guías de Tokio en el diagnóstico de CA de los servicios de emergencias y cirugía en el Hospital de Clínicas, durante abril a noviembre de 2017. La población estuvo constituida por 222 pacientes que ingresaron con síntomas de CA a los servicios de cirugía y emergencias; la edad promedio fue 40 ± 10 años y el 86% fueron mujeres (Grado I: 89.6%, Grado II: 9.4%, Grado III: 0%). Haciendo una correlación según TG-13 y los hallazgos quirúrgicos implicó que 14% tenían una colecistitis aguda edematosa, 5% colecistitis aguda necrotizante clasificados según la guía de Tokio como colecistitis aguda leve y 3% con diagnóstico de colecistitis aguda reagudizada con colecistitis aguda moderada. Se observó que la TG13 presentó una sensibilidad del 83% para el diagnóstico de CA, concluyendo que las TG-13 son aplicables en nuestro medio, permiten diagnosticar, clasificar adecuadamente y contar con una pauta de manejo para un tratamiento oportuno.
Palabras clave: Colecistitis Aguda, Guías de Tokio, Colecistectomía, Grado de Severidad.
Tokyo Guidelines (TG-13) are used to diagnose, assess severity and guide the management of Acute Cholecystitis (AC). The aim of our study was to apply Tokyo Guidelines in the diagnosis of AC in emergency and surgery services at Hospital de Clínicas, between April to November 2017. It was studied 222 patients who were admitted with AC symptoms to surgery and emergency services. 40 ± 10 was the average age, 86% were women, 89.6% corresponded to Grade I, 9.4% Grade II and grade III was not present. Performing a correlation according to TG-13 and surgical findings it was observed that 14% had an acute edematous cholecystitis, 5% acute necrotizing cholecystitis classified as mild acute cholecystitis according to Tokyo Guidelines, and 3% with diagnosis of exacerbated acute cholecystitis and with moderated acute cholecystitis. TG-13 showed a sensibility of 83% for AC diagnosis. It is concluded that TG-13 are applicable in our setting, they allow to diagnose, to classify adequately, and to have a management guideline for AC opportune treatment.
Key words: Acute Cholecystitis, Tokio Guidelines, Cholecystectomy, Severity grade.
INTRODUCCIÓN
La Colecistitis Aguda es la complicación más común de la colelitiasis, representa del 6 al 11% de los cuadros de abdomen agudo en adultos, con una probabilidad de ser operado de urgencia del 6-8%. La CA se incrementó en más de 20% en las últimas 3 décadas y se calcula aproximadamente que se realizan 700.000 colecistectomias cada año en U.S.A. con un costo de 6.5 billones de dólares, convirtiéndola en un problema sanitario a nivel mundial, tanto en términos de morbilidad, impacto social, impacto económico e impacto en la calidad de vida1,2.
Para establecer consensos actualizados en el manejo de colecistitis y colangitis el año 2007, en Japón, se establecieron las Guías de Tokio con la participación de más de 20 países; ésta iniciativa nace con Miura F. y Col (2007)3 posteriormente se realizaron cambios en base a estudios retrospectivos (Takada T. y col 2013)4. Yokoe M y Col, en 2013,5 promueven una revisión de los nuevos criterios de diagnóstico y manejo de la colecistitis aguda según las TG-13, indicando que la sospecha diagnóstica se puede tener con la combinación de un criterio local con otro sistémico, la aplicación de la misma tiene una sensibilidad de 91.2% y una especificidad de 96.9% según la literatura.2,4,5(Cuadro 1)
La manifestación clínica más importante para el diagnóstico de colecistitis aguda es el dolor abdominal presente en hipocondrio derecho y epigastrio (72-93%), seguido en frecuencia por náusea y vómito. No existe estudios de laboratorio específico, sin embargo el diagnóstico se sustenta en la elevación de la cifra de leucocitos mayores a 10,000/ul o de la PCR mayor a 3 mg/dl, y alteraciones leves en perfil hepático. Las bilirrubinas totales pueden elevarse hasta 4mg/dl en ausencia de complicaciones. Para el diagnóstico de colecistitis aguda la combinación del signo de Murphy ultrasonográfico con PCR elevada tiene una sensibilidad de 95%, especificidad de 76% y valor predictivo positivo de 96%.6 El ultrasonido es el primer estudio a solicitar, tiene una sensibilidad de 50-88% y una especificidad de 80-88%
]]> De acuerdo a TG-13 podemos clasificar a la colecistitis aguda según sus criterios de severidad en: Leve, Moderada y Severa (Cuadro 2). La clasificación de severidad es importante puesto que de ella dependerá el paso a seguir en cuanto al tratamiento, para lo cual se debe de tomar en cuenta el microorganismo, la sensibilidad local, antecedente de uso de antibiótico 6 meses previo, función renal y hepática, historia de alergias y de otros eventos adversos.Tomando en cuenta las últimas actualizaciones TG-13 (2018)7,8,9 y considerando que en el Hospital de Clínicas existe una investigación acerca de la validez de la guía de Tokio para el manejo de la CA10 se pretende continuar con el estudio, aplicando TG-13 en las unidades de emergencias y cirugía general, una prueba que permite el diagnóstico de colecistitis, y a su vez comparar y correlacionar con los resultados intraoperatorio y anatomopatológico en pacientes que ingresaron al Servicio Cirugía del Hospital Clínicas.
MATERIALES Y MÉTODO
Estudio prospectivo de corte trasversal de una serie de casos observados entre los meses de Abril a Noviembre del 2017 en pacientes del Hospital de Clínicas Universitario de La Paz. Previo a la realización del estudio se solicitó autorización escrita de la Dirección Médica para la obtención de los registros. Se firmo un compromiso de confidencialidad, comprometiéndose a no revelar los datos personales de los participantes del estudio. La población estuvo constituida por 222 pacientes que ingresaron con la aplicación de TG-13 presentando signos de CA porlos servicio de Cirugía y Emergencias. Se realizó una observación directa del paciente e indirecta por medio de formulario de recolección de datos y las historias clínicas para la recolección de la información; los datos fueron tabulados con el programa IMB SPSS Statistic versión 22.
Confirmado el diagnóstico, el siguiente paso fue el manejo de los pacientes de acuerdo la severidad siguiendo las TG-13 (Figura 1), se pudo apreciar que la aplicación de forma indirecta dependerá de la experiencia de cada servicio y de la disponibilidad de medios para su resolución, así como los antecedentes que estos presenten, tal como se menciona en la literatura.11-14
RESULTADOS
De los 222 pacientes que ingresaron al estudio únicamente se operaron a 205, la edad promedio de presentación fue de 40 ± 10años, el género femenino fue el más representativo, el tiempo de evolución del cuadro clínico tuvo un promedio de 1 a 5 días (42.8%), con un 75% menor o igual a una semana. El signo predominante según TG-13 fue el dolor en Hipocondrio derecho presente en el 96% de los pacientes.
]]>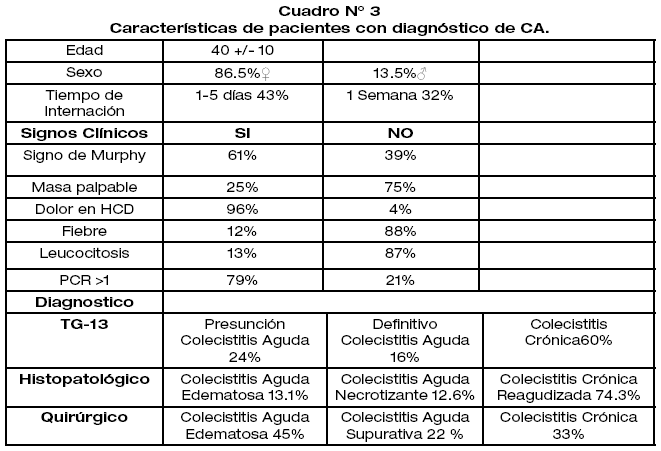
De los pacientes estudiados el 24% fueron diagnosticados como presunción de CA según la guía de Tokio, solo el 16% con diagnóstico definitivo de colecistitis aguda y 60 % como colecistitis crónica lo cual guarda concordancia con el examen histopatológico reportado como colecistitis crónica reagudizada en un 74.3%, seguido de colecistitis aguda edematosa en un 13.1% (Figura 2). De los pacientes intervenidos quirúrgicamente el hallazgo intraoperatorio más frecuente (45%) fue la colecistitis aguda edematosa, y un 33% con hallazgos de colecistitis crónica.
La correlación entre los días de evolución y el diagnostico histopatológico, la colecistitis aguda edematosa curso con un tiempo de evolución de 1 a 5 días, y aquellos pacientes con tiempo de evolución mayor a 1 mes cursaron con colecistitis aguda necrotizante, resaltando también que la colecistitis crónica reagudizada puede tener desde un tiempo de evolución menor a 1 día hasta mayor a 1 mes, lo cual se observapor la consulta médica tardía por parte de los pacientes (Figura 2).
En nuestro estudio la colecistitis aguda fue leve en un 89.6%, seguida en menor porcentaje por el grado II moderada 10.4%; no encontrándose en este periodo CA grave según la TG-13. La correlación entre los días de evolución y el diagnostico histopatológico implica que de 205 pacientes que fueron intervenidos quirúrgicamente 45% cursaron con CA Edematosa, con un tiempo de evolución de 1 a 5 días, solo un 5% presentaron aumento de tamaño vesicular y sus paredes tuvieron un grosor < 5 mm. En 7.3% pacientes hubo líquido peri vesicular y lito enclavado en bacinete. Por otra parte, en 13% se presentó piocolecistitis y se evidencio aumento de tamaño vesicular, de estos un 48% tuvieron engrosamiento de pared.
Haciendo una correlación según el diagnóstico de los hallazgos quirúrgicos (Figura 3) corresponden a la leve: 45% de los pacientes con colecistitis aguda edematosa, 22% Colecistitis aguda supurativa (9% de Hidrops y 13% piocolecistitis) y 33% con colecistitis crónica;de los catalogados con CA moderada (n:6)16% presentaron colecistitis aguda edematosa y 84% con piocolecistitis. La correlación de ambas variables implica que, 29 pacientes tenían una colecistitis aguda edematosa, 11 colecistitis aguda necrotizante clasificados según TG-13 como colecistitis aguda leve y 6 con diagnóstico de colecistitis aguda reagudizada con colecistitis aguda moderada.
DISCUSIÓN
Los resultados de nuestro estudio sugieren que los criterios de TG13 presentaron buena sensibilidad para diagnosticar la CA; los hallazgos más sensibles para colecistitis fueron el dolor en HCD 96% y PCR>1 79%. Figueiredo et al comenta que la CA es cada vez más frecuente en la población joven, nosotros contamos con una media de edad de 41±10 años más frecuente en mujeres 86.5%. La mayoría de los pacientes con Grado I, Grado II se sometieron a una colecistectomía temprana. La menor sensibilidad se apreció en la falta de fiebre y leucocitosis desde el inicio del cuadro lo cual disminuyo la sensibilidad. La Sociedad Mundial de Cirugía de Emergenciaen sus recomendaciones estableció que ningún signo clínico o hallazgo de prueba de laboratorio puede establecer o excluir el diagnóstico de colecistitis aguda.15
]]> A diferencia de Ambe y col6 que incluyeron solo colecistitis con 3 días de evolución máxima, se incluyeron todas las colecistitis agudas independientemente del tiempo de evolución, sin embargo el tiempo de evolución más frecuente en la población de estudio fue de 1 a 5 días en una representación de 42.8%. La correlación entre los días de evolución y el diagnostico histopatológico implica que de los 205 pacientes que fueron intervenidos quirúrgicamente cuyo diagnóstico fue colecistitis aguda edematosa cursaron con un tiempo de evolución de 1 a 5 días, y aquellos pacientes con tiempo de evolución mayor a 1 mes cursaron con un estadio más avanzado como ser la colecistitis aguda necrotizante, resaltando también que la colecistitis crónica reagudizada puede tener desde un tiempo de evolución menor a 1 día o cuadro de evolución mayor de 1 mes, como es de esperarse, esto debido a que no siempre es factible intervenir a todos los pacientes dentro sus primeras horas.En correlación con los hallazgos quirúrgicos solo 5% de los pacientes tuvieron leucocitosis mayor a 10.000/ul y estuvo en relación con el diagnostico quirúrgico de piocolecistitis. Las restantes formas macroscópicas halladas en el acto quirúrgico no excedieron los 10.000/ul de leucocitos; estos datos concuerdan con el trabajo de Nikfarjam et al16, que indica que mientras más complicada es la colecistitis el recuento leucocitario se eleva significativamente, considerándolo un factor de riesgo para predecir la presencia de colecistitis gangrenosa. En cuanto a los hallazgos ecográficos se apreció la poca sensibilidad del examen para predecir la CA siendo necesaria la correlación clínica coincidiendo con los hallazgos de Motta y col afirmando que los descubrimientos ecográficos para predecir CA son limitados.17
Al analizar los resultados se evidencio que el hallazgo intraoperatorio más frecuente fue la colecistitis aguda edematosa 42% y colecistitis crónica reagudizada 33%. Sin embargo difiere en relación al diagnóstico histopatológico pues el más frecuente reportado fue de colecistitis crónica reagudizada en un 74.3%, seguido de colecistitis aguda edematosa en un 13.1%. La mayoría de los pacientes no acuden cuando presentan los primeros sintomas, lo cual genera una inflamación crónica y datos de fibrosis sin embargo no deja de ser un cuadro de inflamación crónica reagudizada, datos similares se encontraron en otros estudios11-13 donde los diagnósticos anatomopatológico eran distintos a los preoperatorios, el diagnostico mayoritario fue colecistitis crónica. La correlación, según TG-13, 30% de los pacientes que ingresaron con el diagnostico de presunción de colecistitis aguda fueron catalogados histológicamente como colecistitis aguda edematosa, 54% como colecistitis crónica reagudizada, y de aquellos los que ingresaron con diagnóstico definitivo de colecistitis aguda, 37% de ellos reportaron como colecistitis aguda edematosa y 63% como colecistitis crónica reagudizada y 114 catalogados como colecistitis crónica, que según el reporte histopatológico corresponden a pacientes con colecistitis crónica reagudizada. La relación entre el diagnostico quirúrgico con el diagnostico histopatológico 13 coinciden con el diagnostico de colecistitis aguda edematosa, 11 tenían el diagnostico de colecistitis aguda edematosa las mismas que fueron reportadas en la patología como colecistitis aguda necrotizante y 69 como colecistitis crónica reagudizada. 16 de los pacientes con piocolecisto reportaron como hallazgo histopatológico colecistitis aguda edematosa. El resto de los pacientes fueron catalogados como colecistitis crónica reagudizada.
Según las TG-13 actualizadas, el 2018 los pacientes que presentan una colecistitis aguda grado I serían candidatos a una colecistectomía laparoscópica, aquellos que presentan una colecistitis grado II podrían ser manejados por vía laparoscópica (en centros con experiencia) o por vía percutánea, y los pacientes con un grado III se beneficiarían con una colecistostomía percutánea.9,18
En nuestro estudio la colecistitis aguda fue leve en un 89.6%, seguida en menor porcentaje por el Grado II moderada, y no se observó el Grado III (según TG-13G). Haciendo una correlación según el diagnóstico de los hallazgos quirúrgicos, corresponden a la leve 47% con colecistitis aguda edematosa, 6% con colecistitis aguda supurativa, 12% con piocolecisto y 36% con colecistitis crónica. De los pacientes con Grado II, 16% reportaron colecistitis aguda edematosa y 84% piocolecisto. La correlación de ambas variables implica que 29 pacientes tenían una colecistitis aguda edematosa, 11 colecistitis aguda necrotizante clasificados según la guía de Tokio como colecistitis aguda leve y 6 con diagnóstico de colecistitis aguda reagudizada con colecistitis aguda moderada.
Durante el periodo de estudio no se reportaron casos de CA Grado III una entidad que puede darse hasta en el 30% de las colecistitis según diferentes series. 19,20.
Ante lo expuesto nuestro estudio revela que la Guía de Tokio es una herramienta útil para el diagnóstico de colecistitis aguda y aplicable en nuestra población por su alta sensibilidad y especificidad por tanto es fiable para determinar si un paciente cursa con un cuadro de colecistitis aguda leve moderada o severa y es una pauta válida para el manejo oportuno.
Por lo tanto las Guías de Tokio aplicadas de forma precoz son de utilidad para el diagnóstico y planificación del tratamiento adecuado, ya que todo paciente con colecistitis aguda debe ser hospitalizado y posterior a su clasificación y categorización ser programado para cirugía inmediata o diferida, ya que la colecistectomía es el tratamiento definitivo para estos pacientes.
En conclusión, la Guía de Tokio para colecistitis aguda litiásica es aplicable en nuestro medio, ya que nos permite diagnosticar, clasificarla adecuadamente según criterio de gravedad y contar con una pauta de manejo para un tratamiento oportuno, llegando a posibilitar la comparación y correlación con los resultados intra-operatorio y anatomopatológico en pacientes internados en las unidades de cirugía.
]]> REFERENCIAS
1. Figueiredo JC, Haiman C, Porcel J, Buxbaum J, Stram D, Tambe N, Cozen W, Wilkens L, Le Marchand L, Setiawan VW. Sex and ethnic/racial-specific risk factors for gallbladder disease. BMC Gastroenterol. 2017 Dec 8; 17(1):153. [ Links ]
2. Stinton LM, Shaffer EA. Epidemiology of Gallbladder Disease: Cholelithiasis and Cancer. Gut and Liver. 2012;6(2):172-187. [ Links ]
3. Miura F, Takada T, Kawarada Y, Nimura Y, Wada K, Hirota M, et al.Flowcharts for the diagnosis and treatment of acute cholangitis and cholecystitis: Tokyo Guidelines. J HepatobiliaryPancreat Surg. 2007; 14(1):27-34. [ Links ]
4. Takada T, Strasberg SM, Solomkin JS, Pitt H a., Gomi H, Yoshida M, et al. TG13: Up dated Tokyo Guidelines for the management of acute cholangitis and cholecystitis. J HepatobiliaryPancreat Sci. 2013; 20(1):1-7 [ Links ]
5. Yokoe M, Takada T, Strasberg SM, Solomkin JS, Mayumi T, Gomi H, et al. New diagnostic criteria and severity assessment of acute cholecystitis in revised Tokyo guidelines. J HepatobiliaryPancreat Sci. 2013;19(5):578–85.
6. Ambe PC, Christ H, Wassenberg D. Does the Tokyo guidelines predict the extent of gallbladder inflammation in patients with acute cholecystitis? A single center retrospective analysis. BMC Gastroenterology. 2015; 15:142. [ Links ]
7. Takada T, Strasberg SM, Solomkin JS, Pitt HA, Gomi H, Yoshida M, et al; Tokyo Guidelines Revision Committee. TG13: Updated Tokyo Guidelines for the management of acute cholangitis and cholecystitis. J HepatobiliaryPancreat Sci. 2013 Jan; 20(1): 1-7. [ Links ]
8. Mayumi T, Okamoto K, Takada T, Strasberg SM, Solomkin JS, Schlossberg D, et al Tokyo Guidelines 2018: management bundles for acute cholangitis and cholecystitis. J HepatobiliaryPancreatSci. 2018 Jan; 25(1):96-100. [ Links ]
9. Yokoe M, Hata J, Takada T, Strasberg SM, Asbun HJ, Wakabayashi G, et al.Tokyo Guidelines 2018: Diagnostic criteria and severity grading of acute cholecystitis (with videos). J HepatobiliaryPancreat Sci. 2018 Jan;25(1):41-54. [ Links ]
10. Ramos C. Validación de la Guía De Tokio en el manejo de la colecistitis aguda litiásica en la Unidad De Cirugía General del Hospital de Clínicas Julio A Diciembre 2016;1:1-5
11. Okamoto K, Suzuki K, Takada T, Strasberg SM, Asbun HJ, Endo I, et al. Tokyo Guidelines 2018: flowchart for the management of acute cholecystitis. J HepatobiliaryPancreat Sci. 2018Jan; 25(1): 55-72. [ Links ]
12. Joseph B, Jehan F, Dacey M, Kulvatunyou N, Khan M, Zeeshan M, Gries L, O'Keeffe T, Riall TS. Evaluating the Relevance of the 2013 Tokyo Guidelines for the Diagnosis and Management of Cholecystitis. J Am Coll Surg. 2018 Mar 23. pii: S1072-7515(18)30225-4.
13. Cheng WC, Chiu YC, Chuang CH, Chen CY. Assessing clinical outcomes of patientswith acute calculous cholecystitis in addition to the Tokyo grading: a retrospective study. Kaohsiung J Med Sci. 2014 Sep;30(9):459-65. [ Links ]
14. Hayasaki A, Takahashi K, Fujii T, Kumamoto K, Fujii K, Matsumoto E, Miyahara S, Kusuta T, Azumi Y, Isaji S. Factor Analysis Influencing Postoperative Hospital Stay and Medical Costs for Patients with Definite, Suspected, or Unmatched Diagnosis of Acute Cholecystitis according to the Tokyo Guidelines 2013.Gastroenterol Res Pract. 2016;2016:7675953. [ Links ]
15. Zenobii MF, Accogli E, Domanico A, Arienti V. Update on bedside ultrasound (US) diagnosis of acute cholecystitis (AC). Intern Emerg Med. 2016. Mar;11(2):261-4. [ Links ]
16. Nikfarjam M, Niumsawatt V, Sethu A, Fink MA, Muralidharan V, Starkey G, Jones RM, Christophi C. Outcomes of contemporary management of gangrenous and non‐gangrenous acute cholecystitis. HPB. 2011; 13: 551-558. [ Links ]
17. Ansaloni L, Pisano M, Coccolini F, et al. 2016 WSES guidelines on acute calculouscholecystitis. World J EmergSurg 2016; 11:25. [ Links ]
18. Janikow C, Corti E, Menso N, Moretti G, Alé M, Sánchez M, Lada PE. Useful of Tokyo guidelines in the diagnosis of acute cholecystitis. Anatomopathologiecorrelationship. Rev FacCien Med UnivNac Cordoba. 2017; 74 (2): 88-92. [ Links ]
19. Yokoe M, Takada T, Hwang TL, Endo I, Akazawa K, Miura F, et al. Descriptive review of acute cholecystitis: Japan-Taiwancollaborative epidemiological study. J HepatobiliaryPancreat Sci. 2017Jun; 24(6): 319-328.
]]>20. Yokoe M, Takada T, Hwang TL, Endo I, Akazawa K, Miura F et al. Validation of TG13 severity grading in acutecholecystitis: Japan-Taiwan collaborative study for acute cholecystitis. J Hepatobiliary Pancreat Sci. 2017 Jun;24(6):338-345. [ Links ]
]]>