
Micro-encapsulación de aceite de chía
Microencapsulation of Chia oil
María Belén Goitia Funes, David Amurrio Derpic
Universidad Católica Boliviana Dept. de Ciencias Exactas e Ingeniería, c. Márquez s/n, Campus Tupuraya, Cochabamba, Bolivia.
amurrio@ucbcba.edu.bo
Resumen: Aceite de chía fue micro-encapsulado en matrices de gelatina y de alginato tanto por el método de extrusión como por el método de emulsión con eficiencias comprendidas entre buena (62,12%) y excelente (99,55%). Las cápsulas formadas fueron caracterizadas según tamaño (400-1.800 μm), composición (37-64% aceite), condiciones de liberación (similares al estómago, similares al intestino delgado) y cinética de liberación. Se encontró que las micro-cápsulas de alginato se liberan bajo condiciones similares a la del estómago con una cinética de potencia correspondiente a f=k.tn mientras que las micro-cápsulas de gelatina se liberan en condiciones similares a las del intestino delgado con una cinética sigmoidal correspondiente a df/dt=k1f(k2-f).
Palabras clave: Aceite de chía, ácidos grasos omega insaturados, micro-encapsulación.
Abstract: Chia oil was microencapsulated with gelatin and with alginate applying extrusion and emulsión techniques. Encapsulation efficiencies ranged between good (62.12%) and excellent (99.55%). The microcapsules were characterized according to size (400-1,800 μm), composition (37-64% oil), and liberation conditions (similar to the stomach, similar to the small intestine). We found that the alginate based microcapsules released their oil under conditions similar to the stomach following power law kinetics: f=k.tn, whereas the gelatin based microcapsules released their content under conditions similar to the small intestine following sigmoidal kinetics: df/dt=k1f(k2-f).
Keywords: Chia oil, omega unsaturated fatty acids, microencapsulation
]]> 1. Introducción
La chía (Salvia hispánica), es una planta originaria de la región comprendida entre México y Guatemala que fue cultivada desde la antigüedad por los pueblos mesoamericanos. Relatos históricos de la conquista atestiguan que las semillas de la chía eran muy apreciadas como medicina, por su aceite y como alimento, siendo incluso objeto de tributo por parte de los estados subordinados a la capital, Tenochtitlán.
Con la caída del imperio azteca su uso prácticamente desapareció por 500 años hasta que en la década de 1990 fue redescubierta comercialmente en base a su alto contenido en aceites omega insaturados. Típicamente, la semilla contiene entre 18,5 y 22,3% de proteína, fibra (20,1-36,1%) y entre 21,5 y 32,7% de aceites de los cuales 60-67% corresponden al ácido α-linolénico [1-6]. Además de su altísimo contenido en aceites no saturados, tiene una proporción muy conveniente de 3 a 1 entre ácidos grasos omega-3 y omega-6.

Los beneficios de incorporar ácidos grasos omegas insaturados en la dieta son hoy en día conocidos, pero su incorporación en la alimentación está dificultada por la sensibilidad de dichas sustancias [8]. Al ser ácidos poliinsaturados, estos reaccionan fácilmente con agentes como la luz y el oxígeno, produciendo compuestos con sabores y olores desagradables además de perder los beneficios nutritivos que originalmente poseían. Su ingesta por vía oral, los expone además a la acción de los ácidos del estómago, donde pueden ocurrir reacciones de isomerización y condensación en virtud a los bajos valores de pH presentes. La solución estudiada en el presente trabajo consiste en encapsular el aceite en micro esferas de un material apropiado que pueda proteger los ácidos grasos omega insaturados, enmascarar su sabor y que al mismo tiempo pueda liberar el aceite en un momento oportuno para que el cuerpo pueda asimilarlo.
El presente trabajo evalúa diferentes métodos de micro-encapsulación [9] del aceite de chía, caracteriza los productos obtenidos y luego estudia las condiciones de liberación del aceite encapsulado.
2. Parte experimental
Aceite de chía fue adquirido en el mercado local. Su espectro infrarrojo muestra una elevada proporción entre la absorbancia a 2.855 cm-1 (vibración C(sp2)-H) y la absorbancia a 3.013 cm-1 (vibración C(sp3)-H), equivalente a un número de iodo de 221 según correlaciones establecidas [10].
Alginato de sodio, Gelatina neutra, emulsificadores (Emustab®1 y XP 3000®2) de grado alimenticio fueron adquiridos del comercio especializado. Los espectros infrarrojos fueron tomados con un espectrómetro Shimadzu IRPrestige-21.
]]> 2.1 Proceso de micro-encapsulación2.1.1 Extrusión con alginato de sodio
Alginato de sodio (0,38 g) fue disuelto en 25 ml de agua destilada previamente calentada hasta 40°C. Se dejó enfriar la solución hasta 25°C antes de añadir una mezcla previamente preparada de 22,28 g de aceite de chía con 1,78 g de Emustab® (emulsificante) y 2,3 g de glicerina (plastificante/humectante), de esta manera, mediante agitación se logró formar una emulsión estable de alginato de sodio con aceite de chía. La mezcla resultante fue extruida gota a gota a una solución agitada de cloruro de calcio (3 g) en 100 ml de agua por medio de una jeringa equipada de una aguja de 0,33 mm de diámetro interno. Las gotas añadidas gelifican al entrar en contacto con la solución de cloruro de calcio bajo forma de pequeñas esferas. Las cápsulas así formadas fueron mantenidas en el baño de cloruro de calcio por 15 minutos sin agitación para lograr su completa gelificación, luego fueron filtradas sobre papel y lavadas con agua destilada. Se obtuvieron cápsulas con 45,66 % de humedad.
2.1.2 Emulsión con alginato de sodio
Una emulsión de aceite de chía (22,28 g) con 1,78 g de Emustab® en 25 ml de agua destilada, alginato de sodio (0,38 g) y glicerina (2,3 g) fue preparada tal como se describió en el anterior punto. De la mezcla resultante, 48,64 g fue dispersada en 60 ml de vaselina líquida bajo agitación vigorosa (aprox. 1.600 rpm), formándose pequeñas gotas de la solución dispersa en el aceite mineral. La dispersión acuosa fue gelificada y endurecida en un baño de cloruro de calcio (7,5 g de CaCL2 en 150 ml de agua). Las partículas fueron filtradas y lavadas como se describió en el anterior punto. Se obtuvieron cápsulas con 47,88% de agua (figura 2).

2.1.3 Extrusión con gelatina
Gelatina neutra (6,25 g) fue disuelta en 25 ml de agua destilada a 40°C. Se añadió en caliente una mezcla previamente preparada de 32,07 gr de aceite de chía con 3,2 g de XP 3000 (emulsificante) y 10 g de glicerina (plastificante/humectante), de esta manera se logró obtener una emulsión estable. La mezcla resultante fue extruida gota a gota a un baño de vaselina fría por medio de una jeringa equipada de una aguja de 0,33 mm de diámetro interno. Al entrar en contacto con la vaselina fría se logró una gelificación instantánea de las gotas y, por ende, la encapsulación del aceite de chía. Las cápsulas fueron reticuladas en un baño de 50 ml de formaldehído al 38% a temperatura ambiente durante 10 minutos, luego fueron filtradas y lavadas con abundante agua destilada. Se obtuvieron cápsulas con 61,24% de agua.
2.1.4 Emulsión con gelatina
]]> Una emulsión de aceite de chía (32,07 g) con XP 3000® (3,2 g), gelatina neutra (6,25 g en 25 ml de agua) y glicerina (10 g) fue preparada tal como se describió en el anterior punto. Se dispersó 77,35 g de la emulsión resultante en 95 ml de vaselina líquida bajo agitación vigorosa (aprox. 1.600 rpm). La mezcla fue enfriada a 5°C para endurecer las cápsulas de gelatina, añadiéndose luego 30 ml de una mezcla a volúmenes iguales de isopropanol y formaldehído como agentes deshidratantes y reticulantes respectivamente. Las pequeñas cápsulas fueron filtradas y luego lavadas con abundante agua destilada. Se obtuvieron cápsulas con 57,08% de humedad.
3. Resultados
3.1 Distribución de tamaños
El diámetro de las micro-cápsulas fue determinado por medio de un microscopio óptico conectado a una cámara la cual permitía generar una escala sobre la imagen de las partículas. Un número representativo de las mismas fue tomado para determinar visualmente la distribución de tamaños.
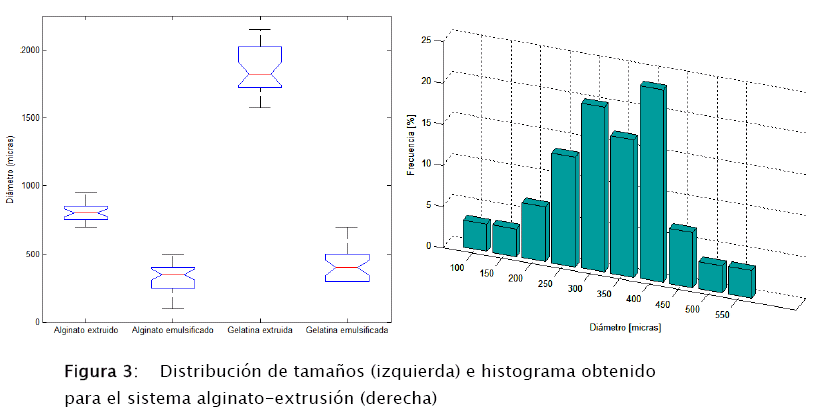
En líneas generales se puede constatar que el proceso de encapsulación por emulsión brinda las cápsulas de menor diámetro (Diámetro medio < 500 μm) mientras que el uso de la gelatina da lugar a mayor dispersión en el tamaño de las micro-cápsulas. En todos los casos se encontraron 2 máximos en la distribución de diámetros.
3.2 Eficiencia de encapsulación
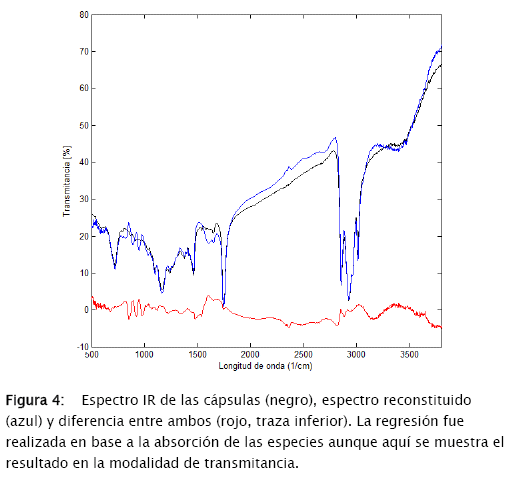
Una vez las micro-cápsulas formadas, el líquido residual resultante fue tratado con CCl4 para extraer la porción de aceite que no habría sido encapsulada. Se tomó el espectro IR de la solución y por medio de una curva patrón preparada previamente se determinó la concentración de aceite no encapsulado gracias a su absorbancia a 1.748 cm-1 (νco).

3.3 Composición
La composición de las micro-cápsulas fue obtenida por medio de un análisis multivariante del espectro IR de las micro-cápsulas molidas en una matriz de KBr y procesadas con Matlab®.
Se prepararon seis pastillas diferentes de KBr cada una con una masa conocida de los diferentes componentes (aceite de chía, gelatina neutra, alginato de sodio, Emustab, XP 3000 y glicerina). Se tomó también un espectro con una mezcla conocida de los diferentes ingredientes propios a cada método de encapsulación. Un análisis multivariante de los espectros de las micro-cápsulas formadas por los diferentes métodos permitió caracterizar la composición de las mismas (tabla 2).
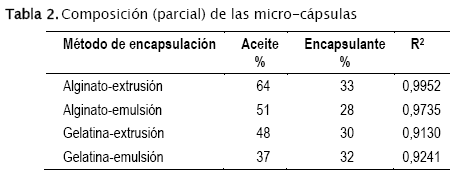
Se validaron los resultados obtenidos realizando el cálculo inverso: la reconstitución del espectro original a partir de los espectros individuales multiplicados por sus fracciones respectivas (figura 4).
3.4 Cinética y mecanismo de liberación [11]
]]> La cinética de liberación del aceite de chía fue estudiada bajo condiciones que simulaba las del estómago (37°C, pH=1,5 ± 0,5). En todos los casos estudiados se aplicó una leve agitación de 65 ± 10 rpm.Debido a que el aceite es inmiscible en el agua, existe la dificultad de la toma de muestras sobre un mismo recipiente debido a que la solución no es homogénea y también existe el inconveniente de que parte del aceite liberado en el tiempo quedara adsorbido sobre las paredes de vidrio del recipiente, es por ello que se decidió realizar 8 análisis diferentes cada uno con 30 mg de cápsulas. Cada 30 minutos las cápsulas fueron retiradas por filtración, el recipiente y el papel filtro fueron lavados con CCl4 y el mismo solvente fue reutilizado para extraer el aceite de la solución acuosa. La extracción se realizó en embudos de separación (1 ml de CCl4 por cada 10 ml de solución) agitando suavemente para evitar la formación de espuma. La fase orgánica fue analizada por espectroscopia IR en una celda de bromo ioduro de talio KRS-5.
En el caso de las micro-cápsulas formadas con alginato, se obtuvieron datos para caracterizar la cinética de liberación del aceite de chía mientras que las cápsulas de gelatina no liberaron su aceite en condiciones similares a las del estómago como tampoco lo hicieron a pH neutro. La cinética de liberación del aceite de las cápsulas de gelatina fue determinada en condiciones similares a las del intestino delgado (37°C, pH=6,8), añadiendo una mezcla de enzimas típicas .
3.4.1 Correlaciones causales
Además de la cinética de liberación, interesa conocer el mecanismo por el cual las microcápsulas liberan su carga. Se consideraron cuatro casos en los cuales un mecanismo explicaría la cinética observada (orden 0, orden 1, Higuchi y Hixson-Crowell).
En el caso que la disolución siga una cinética de orden 0, se espera que la fracción disuelta f siga una relación df/dt=k y por ende f=kt+fo donde fo correspondería a la cantidad inicialmente disuelta en la solución.
Los resultados obtenidos están reproducidos en la tabla 3:
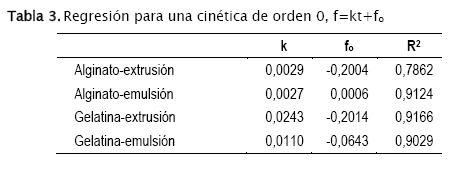
Los resultados obtenidos no tienen coeficientes de correlación muy elevados además de requerir fracciones iniciales negativas.
]]> En el caso que la disolución siga un orden 1, se espera que la fracción disuelta f siga una relación df/dt=kf y por ende f=foe(-kt) donde fo correspondería a la fracción inicialmente disuelta en la solución.Los resultados obtenidos están reproducidos en la tabla 4:
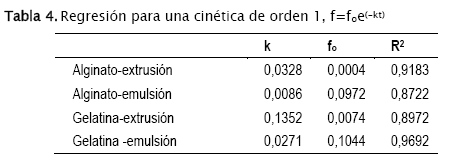
Encontramos nuevamente coeficientes de correlación relativamente bajos.
Cinética de Higuchi
El modelo propuesto por Higuchi fue utilizado para describir la liberación por difusión de una sustancia desde una matriz. La ecuación puede ser representada por: ![]() donde f es la cantidad de sustancia liberada en un tiempo t por unidad de área α. C es la cantidad de sustancia inicial, Cs es la solubilidad de la sustancia y D es el coeficiente de difusión. La ecuación puede resumirse como
donde f es la cantidad de sustancia liberada en un tiempo t por unidad de área α. C es la cantidad de sustancia inicial, Cs es la solubilidad de la sustancia y D es el coeficiente de difusión. La ecuación puede resumirse como ![]() . Los resultados obtenidos son los siguientes (Tabla 5):
. Los resultados obtenidos son los siguientes (Tabla 5):
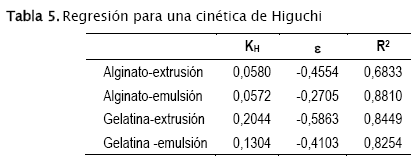
Los bajos coeficientes de correlación y la necesidad de tener una fracción negativa en solución sugieren que la difusión no es el mecanismo que controla la liberación del aceite.
]]> Cinética de Hixson-CrowellEl modelo propuesto por Hixson y Crowell considera los casos de liberación de sustancias causada por erosión de la matriz en las que estas se encuentran. El modelo considera que las proporciones geométricas de las matrices se mantienen constantes, resultando en que la cinética de liberación tendría que seguir una ley:![]() . Los resultados obtenidos se resumen en la tabla 6 para una regresión correspondiente a
. Los resultados obtenidos se resumen en la tabla 6 para una regresión correspondiente a ![]()
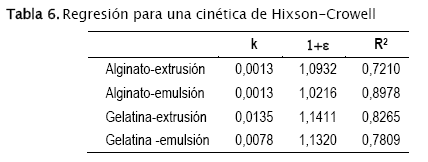
Nuevamente encontramos bajos coeficientes de correlación, lo que sugiere que la erosión de la matriz no corresponde a la cinética de liberación del aceite.
3.4.2 Correlaciones empíricas
Se consideraron también correlaciones empíricas y se evaluaron opciones de efecto de reventón de la cápsula y de tiempos de espera. Los modelos evaluados corresponden a una cinética de potencia n, a la cinética de Weibull y a una cinética sigmoidal.
La cinética de potencia sigue la ley: f = ktn, ecuación a la cual podemos incorporar un efecto de tiempo de inducción L y un efecto reventón b de manera que la ecuación se podría expresar como: f = k(t L)n + b. Se ajustaron numéricamente los valores de k, L, b y n para minimizar los errores cuadrados y se encontró que el escenario que incluía tanto al tiempo de iniciación como al efecto reventón daba resultados complejos de modo que solo se rescatan las situaciones donde ya sea hay un efecto de tiempo de iniciación, o se tiene solamente un efecto de reventón. Los resultados encontrados fueron los siguientes (Tabla 7):
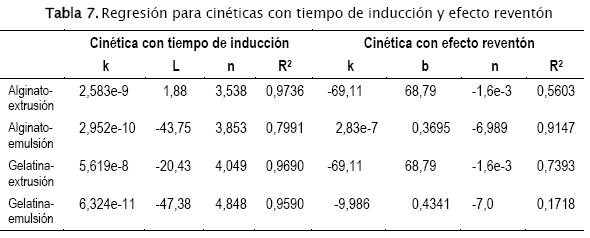
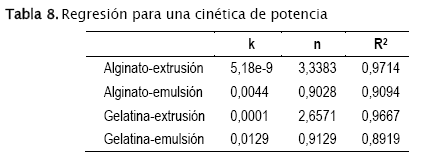
De todos los modelos examinados, la cinética de potencia es la que mejor explica los datos observados para las micro-cápsulas formadas con alginato.
La cinética de Weibull buscar ajustar los datos experimentales a la siguiente expresión: f=1-exp(-t+L)b/a) donde a corresponde a la escala del tiempo, L es el tiempo de inducción y b es un parámetro que fija la forma de la curva (parabólica si b<1, exponencial si b=1 y sigmoidal si b>1). Los valores de L, b y a fueron ajustados numéricamente minimizando los errores cuadrados. Los resultados encontrados con (L ≠ 0) y sin (L=0) desfase fueron los siguientes (Tabla 9):
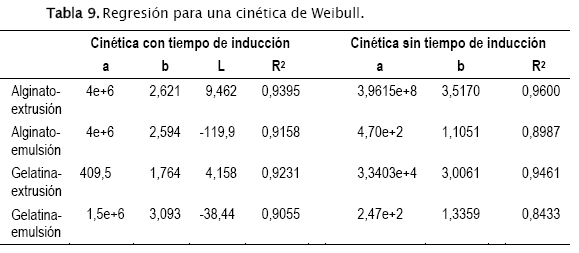
Puesto que los valores de b eran todos mayores a uno, se consideró también buscar una correlación con una cinética sigmoidal. Una expresión apropiada correspondería a ![]() y cuya solución lleva a
y cuya solución lleva a ![]() donde
donde ![]() y b es un tiempo de inducción. Los resultados obtenidos fueron los siguientes:
y b es un tiempo de inducción. Los resultados obtenidos fueron los siguientes:
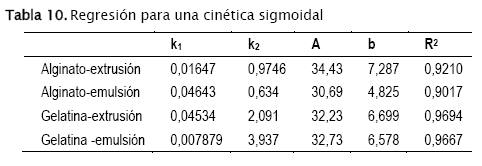
De todos los modelos examinados, la cinética sigmoidal es la que mejor explica los datos observados para las micro-cápsulas formadas con gelatina.
]]>4. Conclusión
Se logró encapsular aceite de chía en matrices de gelatina y alginato tanto por el método de extrusión como por el método de emulsión con eficiencias comprendidas entre buena y excelente. Las cápsulas formadas fueron caracterizadas según tamaño, composición, mecanismo de liberación y cinética de liberación. Se encontró que las micro-cápsulas de alginato se liberan bajos condiciones similares a la del estómago con una cinética de potencia correspondiente a f = 5.18x10-19t3.33 mientras que las micro-cápsulas de gelatina se liberan en condiciones similares a las del intestino delgado con una cinética sigmoidal correspondiente a ![]()
Notas
1Emustab es un emulsificante alimenticio de Duas Rodas Industrial (Brasil). Es una mezcla de monoglicéridos, monoestearato de sorbitán, monoestearato de polioxietilensorbitán y sorbato de potasio
2XP 3000 es un emulsificante alimenticio de Duas Rodas Industrial (Brasil). Es una mezcla de monoglicéridos, goma guar y fécula de mandioca
3Pantyrase® medio comprimido. El comprimido entero tiene: Pancreatina (175 mg), Amilasa (4200 U.F.I.P.), Lipasa (5367 U.F.I.P.), Proteasa (222 U.F.I.P.), Extracto de bilis de buey (25 mg), Dimethicona (25 mg), Hemicelulosa (unidad hemicelulosa 125) 50 mg.
Referencias Bibliográficas
]]> [1 ] Porras-Loaiza, P.; Jimenez-Munguia, M. T.; Sosa-Morales, M. E.; Palou, E.; Lopez-Malo, A. (2014).Physical properties, chemical characterization and fatty acid composition of Mexican chía (Salvia hispanica L.) seeds. International Journal of Food Science and Technology 2014, 49, 571577[2] Ixtaina, V. Y.; Martínez, M. L.; Spotorno, V.; Mateo, C. M.; Maestri, D. M.; Diehl, B. W. K.; Nolasco, S. M.; Tomás, M. C.(2011). Characterization of chia seed oils obtained by pressing and solvent extraction. Journal of Food Composition and Analysis 24, 166174 [ Links ]
[3] Capitani,M. L; Ixtaina, V. Y.; Nolasco, S.M.; Tomás, M.C. (2013). Microstructure, chemical composition and mucilage exudation of chia (Salvia hispanica L.) nutlets from Argentina. Journal of the Science of Food and Agriculture 93, 15, 3856-3862 [ Links ]
[4] Porras-Loaiza, P.; Jiménez-Munguía, M. T.; Sosa-Morales, M. E.; Palou, E.; López-Malo, A. (2014). Physical properties, chemical characterization and fatty acid composition of Mexican chia (Salvia hispánica L.) seeds. International Journal of Food Science and Technology 49, 571577 [ Links ]
[5] da Silva Marineli, R.; Aguiar Moraes, E.; Alves Lenquiste, S; Teixeira Godoy, A.; Nogueira Eberlin, M.; Maróstica jr. M. R. (2014). Chemical characterization and antioxidant potential of Chilean chia seeds and oil (Salvia hispanica L.) LWT - Food Science and Technology 59, 1304-1310 [ Links ]
[6] Ayerza, R.; Coates, W. (2004). Composition of chia (Salvia hipanicá) grown in six tropical and subtropical ecosystems of South America Trop. Sci., 44,131-135 [ Links ]
[7] Sahagún, Fr. Bernardino de, (1575-1577). La Historia Universal de las Cosas de Nueva España. Manuscrito (Codex Florentino). https://www.wdl.org/en/item/10096/view/3/658/ (acceso 03.2016). [ Links ]
[8] Ixtaina, V. Y.; Nolasco, S. M.; Tomás, M. C. (2012). Oxidative stability of Chia (Salvia hispánica L.) seed oil: effect of antioxidants and storage conditions. J. Am. Chem. Oil Soc. 89: 1077-1090. [ Links ]
[9] Kaushik, P.; Dowling, K.; Barrow, C. J.; Adhikari, B.(2014)
Microencapsulation of omega-3 fatty acids: A review of microencapsulation and characterization methods. Journal of functional foods Vol. 19, part B, 868-881
]]>[10] Arnold, R. G.; Hartung, T. E. (1971). Infrared spectroscopic determination of degree of unsaturation of fats and oils. Journal of food science. 36,1,166-168. [ Links ]
[11 ] Costa, P.; Sousa Lobo, J. M. (2001). Modeling and comparison of dissolution profiles. European Journal of Pharmaceutical Sciences, 13, 123-133. [ Links ]
]]>