PRESENCIA DE INTEGRONES Y SU RELACIÓN CON LA RESISTENCIA A ANTIMICROBIANOS EN CEPAS DE Pseudomonas aeruginosa
* María del Rosario Manzur Soria,** Zulema Bustamante,** Gerardo Gonzales
* Medico General
** Estudiante de Medicina UMSS
]]>
RESUMEN
Debido a que en nuestro medio existe una carencia de datos estadísticos con respecto a la incidencia de infecciones producidas por P. aeruginosa en la población y la resistencia que presenta frente a una variedad de antimicrobianos, el presente estudio tiene como propósito fundamental aportar información y datos sobre la distribución y frecuencia (previa estandarización de la técnica para la detección) de los integrones clase 1 y 2 y su relación con la multirresistencia a antimicrobianos. Para este fin, se obtuvieron muestras de P. aeruginosa de diferentes laboratorios y hospitales del Departamento, a las que se les realizó la prueba de susceptibilidad antimicrobiana, crecimiento de las bacterias a presión selectiva, extracción de ADN y por último detección de integrones clase 1 y 2 con partidores específicos.
De 41 muestras obtenidas de P. aeruginosa. se detectó usando PCR, la presencia de integrones clase 1 y clase 2, identificándose éstos en el 58.5 % de las cepas. El 29.27 % de los aislados, llevaba integrones clase 1, el 12,20 % integrones clase 2 y el 17.07 % llevaba ambas clases de integrones. La asociación entre integrones clase 1 y la resistencia múltiple a antimicrobianos fue estadísticamente significativa (chi-cuadrado 0.0033), demostrando la existencia de una fuerte correlación, caso contrario a lo que ocurrió con la asociación entre integrones clase 2 (chi-cuadrado 0.8528). La autenticidad de los productos obtenidos de la PCR, se confirmaron realizando ensayos de restricción con la enzima SphI y la enzima HaeIII.
Este es el primer reporte que muestra la prevalencia de integrones clase 1 y la relación con la multirresistencia en aislados de P. aeruginosa en Cochabamba, Bolivia.
Palabras claves: Integrones, Resistencia antimicrobiana, Plásmidos conjugativos.
ABSTRACT
Due to the fact that in our environment there is an absence of statistical data related to the incidence of infections produced by P. aeruginosa in our population and the resistance that it presents with respect to a variety of antimicrobial agents, this study aims basically at providing information and data about distribution and frequency (after having standardized the detection techniques) of the integrons classes 1 and 2, and their relationship with their multi resistance to antimicrobial agents. For this purpase, samples of P. aeruginosa were obtained from different laboratories and hospitals in the State of Cochabamba, which were tested for antimicrobial sensibility, as well as for growth of bacteria under selective pressure, DNA extraction and finally detection of integrons class 1 and 2 with specific primers.
Using PCR, integrons class 1 and 2 were detected in 41 samples of P. aeroginosa, identifying these ones in 58.5% of the strains: 29.7% of those isolated, carried integrons class 1, 12.2% had integrons class 2, and 17.07% had integrons of both classes. The association between class 1 integrons and multiple resistance to antimicrobial agents was statistically significant (chi square = 0.0033) thus showing a strong correlation, as opposed to what happened with the association among class 2 integrons (chi square = 0.8528) The authenticity of the products obtained from the PCR was confirmed through restriction tests made with SphI and HaeIII enzymes.
This is the first report that shows prevalence of class 1 integrons and the relation with multi resistance aisolated strains of P. aeruginosa in Cochabamba, Bolivia.
]]> Key words: Integrons, Antimicrobial resistance, Conjugative plasmids.
INTRODUCCION
El papel de Pseudomonas aeruginosa como agente patógeno responsable de infecciones comunitarias y, sobre lodo, nosocomiales está plenamente reconocido. Es muy frecuente que la elección del tratamiento antimicrobiano más adecuado para tratar las infecciones que produce esta bacteria, sea problemática, debido a que P. aeruginosa posee una elevada resistencia intrínseca a múltiples antibióticos, lo que conlleva una reducción de las posibilidades terapéuticas. Por otra parte, es un microorganismo que tiene una elevada capacidad para adquirir nuevos mecanismos de resistencia, por lo general, mediante mutaciones (Vila, 2002).
Muchos genes de resistencia a antibióticos están localizados en plásmidos y en transposones (Levesque, et al, 1995). La transmisión horizontal de genes de resistencia, es un mecanismo para la transmisión y diseminación de resistencia a múltiples drogas entre bacterias patógenas (Carattoli, 2001) y en los últimos años, se ha relacionado la multirresistencia a los antibióticos con la presencia de integrones y elementos genéticos que pueden contener uno o varios cassettes genéticos de resistencia, considerados como mecanismos eficientes por los cuales las bacterias pueden adquirir genes de resistencia (Ramírez et al, 2004). La transferencia de estos elementos entre diferentes bacterias puede ocurrir por conjugación, transformación o transducción (González, et al, 2004; Carattoli, 2001), procesos básicos en la transferencia de genes entre bacterias.
Los integrones, son elementos genéticos que contienen un sistema de recombinación sitio específica que tienen la habilidad de integrar y movilizar cassettes genéticos (Young, et al, 2002; Fluit y Schmitz, 1999), poseen dos segmentos conservados, separados por una región variable que puede incluir genes de resistencia a antibióticos o cassettes de función desconocida (Levesque, et al, 1995). Los cassettes genéticos, consisten en una secuencia codificante. El extremo 3' CS, tiene una longitud de 2kb, y la secuencia es menos conservada entre los distintos integrones que el extremo 5' CS que tiene una longitud de 1.36 kb. En este extremo, se localiza un elemento de 59 bases, denominado attC. (Carattoli, 2001; Martínez, 2005).
Los cassettes, generalmente, confieren resistencia a antibióticos; pueden ser movilizados independientemente por la integrasa del integrón. Los rearreglos de los cassettes en la región insertada, pueden alterarse por escisión de cassettes individuales o nuevos cassettes pueden precisamente insertarse (Collins, 1995), Varios estudios indican que el nivel de expresión de un gen de resistencia depende de la posición del cassette genético dentro de la región insertada, afectando el nivel de resistencia al antibiótico.
Los componentes esenciales de un integrón, incluyen el gen de la integrasa (IntI), el sitio de unión o atadura (attI) y uno o dos promotores responsables de la expresión de los cassettes genéticos insertados (fig. 1) (Clark, et al, 1999; Carattoli, 2001; Severino y Magalhaes, 2004). Para la actividad de los integrones, se requiere de la Integrasa. Esta enzima, cataliza la recombinación entre dos secuencias cortas de ADN que pueden ser de dos clases: attI o attC, que son los sitios primarios de reconocimiento de la integrasa (García, s/a).
]]>
Fig. 1: Representación de la estructura básica del integrón. (González, et al,2004)
Se han definido 4 clases de integrones, basados en la homología de la proteína de la integrasa (40 - 60 % idénticos).
Holmes y colaboradores (2003), mencionan, que el integrón de clase 1 tiene una influencia fuerte en la resistencia a múltiples antibióticos y se han asociado con el desarrollo de multirresistencia en Enterobacteriaceae en medio ambientes hospitalarios (Leverstein, et al, 2002), los integrones clase 1 se caracterizan por la presencia de 2 segmentos conservados: 5'CS y 3'CS (Fig. 1), El 5' CS (segmento conservado) contiene el gen intI, el sitio attI y el promotor; el 3' segmento conservado codifica los genes sulI y qacEA1 y un marco de lectura abierto (ORF), orf5 (Dalsgaard, et al, 2000). Los genes sulI y qacEA1 confieren resistencia a sulfonamidas y componentes de amonio cuaternario y bromuro de etidio respectivamente (Leverstein, et al., 2002; Fluit, l999; Patridge, et al, 2000; Severino y Magalhaes, 2004). Los cassettes genéticos de resistencia a antibióticos están integrados entre los segmentos conservados 5' y 3'. El integrón designado como In0 no contiene genes insertados, haciendo a las regiones 5' y 3' adyacentes una a la otra.(Carattoli, 2001)
Los integrones clase 2, se encuentran incluidos en la familia Tn7 de los transposones, contienen tres cassettes genéticos integrados dhfrl, sat, aadAl que confieren resistencia a trimetropin, estreptomicina, y espectinomicina (Roy, 1995). Los integrones de la clase 3, codifican la integrasa intI3, que muestra 61% de homología con la secuencia de aminoácidos de la integrasa int.l, sólo se han observado en plásmídos y los integrones de la clase 4, se han identificado principalmente en el cromosoma de Vibrio cholerae (Carattoli, 2001).
El objetivo del presente trabajo fue detectar la presencia de Integrones de clase 1 y 2 en el ADN de cepas aisladas de muestras clínicas de Pseudomonas aeruginosa, mediante reacción en cadena de la polimerasa (PCR) y relacionar la presencia de integrones con la clase de resistencia que presentan las cepas estudiadas.
MATERIALES Y MÉTODOS
Cepas Bacterianas
Se obtuvieron 41 muestras clínicas de P. aeruginosa procedentes de diferentes laboratorios y centros hospitalarios del departamento durante el periodo de Mayo a Octubre de 2002; 15 de las muestras fueron proporcionadas por el Instituto Gastroenterológico Boliviano Japonés (GASTRO), 8 por la Escuela Técnica de Salud, 5 por la Caja Petrolera de Salud (CPS), 3 por el Hospital Univalle, 2 muestras por el Laboratorio Asistencial de la Facultad de Bioquímica y Farmacia, 2 del laboratorio Fénix, 2 del Laboratorio Central, 2 del Laboratorio Jhon, 1 de Plusmed y 1 muestra de Laboratorio Labimed perteneciente a la Facultad de Medicina.
]]> Como controles positivos para la detección de integrones clase 1 y 2, se usaron las muestras UC-4 E. coli 162 (R483) Tn7 (+), intI2 (+); UC-7 E. coli C600 (R388), intI1 (+), proporcionadas por el Dr. Gerardo González, del Departamento de Microbiología de la Facultad de Ciencias Biológicas de la Universidad de Concepción, Chile.Las cepas de Pseudomonas aeruginosa AATCC 27853, proporcionadas por la Caja Petrolera de Salud y el Instituto Gastroenterológico Boliviano Japonés, se emplearon como patrones estándar del halo de inhibición del antibiograma. Todas las bacterias se conservaron a 4°C en medio Soft.
La identificación y determinación de la sensibilidad antimicrobiana (Ceftazidima, Imípenem, Gcntamicina, Amíkacina, Cefoperazona, Cclcpime, Ciprofloxacina, Aztreonam), se estudió por el método de difusión en disco-placa, siguiendo las recomendaciones del NCCLS.
Extracción del ADN
De un cultivo de una noche de crecimiento de las bacterias a presión selectiva en caldo tripticasa en presencia de una concentración de sulfametoxazol/trimetoprim de 160 ug/ml y Estreptomicina de 15 ug/m (para detección de integrones clase 1 y 2 respectivamente), se centrifugó 1 ml de la muestra a 10000 r.p.m. y se resuspendió nuevamente en 200 ul de TE buffer. Esta suspensión se hizo hervir durante 30 minutos, se agregó 100 ul de cloroformo, se centrifugó a 12000 r.p.m. por 5 minutos y la fase acuosa que contenía el ADN se empleó en las PCR.
Detección de Integrones clase 1 por amplificación del ADN mediante PCR
Para la amplificación de los fragmentos de los integrones de la clase 1, se utilizaron los iniciadores descritos por González y colaboradores, el 2004, y sintetizados por EUROGENTEC:
]]> Las concentraciones finales de la mezcla para la reacción de amplificación fueron: tapón de reacción lX, Taq ADN polimerasa (Taq Gol Star) en una concentración de 0.5 unidades, 0.2 mM de cada dinucleótidos trifosfatos (dNTPs), 10 pmoles de cebador y 1 ul de muestra. Como cepa control se utilizó UC-7 E. coli C600 (R388), que contiene intI, cuyo tamaño de fragmento amplificado es de 892 pb. La amplificación se realizó en 2 ciclos iniciales de: 96 °C 30 seg, 63 °C 1 minuto, 70 °C 3 minutos, seguido de 35 ciclos de 96 °C 30 seg, 63 ºC 30 seg, 70°C 3 minutos, y una extensión final de 70 °C por 5 minutos y parada de la reacción a 4°C. Los productos de amplificación se observaron con luz ultravioleta tras electroforesis en geles de agarosa al 1 %.Int A: ATCATCGTCGTAGAGACGTCGG
Int B: GTCAAGGTTCTGGACCAGTTGC
Detección de Integrones clase 2 por amplificación del ADN mediante PCR
Para la amplificación de integrones de clase 2, se utilizaron los iniciadores descritos por Gonzáles y colaboradores, en 2004, y sintetizados por EUROGENTEC:
Inti2F: GCAAATGAAGTGCAACGC
Inti2R: ACACGCTTGCTAACGATG
Las concentraciones finales de la mezcla para la reacción de amplificación fueron: tapón de reacción 1X, Taq ADN polimerasa (Eppendorf) en una concentración de 0.5 unidades, 0.2 mM de cada dinucleótidos trifosfátos (dNTPs). 2.5 mM de acetato de magnesio, 10 pmoles de cebador y 1 ul de muestra. Como cepa control se utilizó UC-4 E. coli 162 (R483). que contiene int2, cuyo tamaño de fragmento amplificado es de 467 pb. Las condiciones de amplificación fueron las mismas que se utilizaron en el integrón 1. Los productos de amplificación se observaron con luz ultravioleta tras electroforesis en geles de agarosa al 1.5%.
Electroforesis de los productos de la PCR en geles de agarosa
Los productos de amplificación, se separaron por electroforesis en geles de agarosa a una concentración de 1 % en tampón TAE 1X, para la separación de los productos de amplificación del gen intI 1. Para la separación de los productos de amplificación del gen inti2, la concentración de agarosa utilizada fue de 1.5%. La siembra se realizó con 10 ul del producto de PCR del gen intI 1, utilizando un marcador de peso molecular de lKb DNA Ladder de Promega y, como control interno la cepa de referencia UC-7 E. coli. Los productos de PCR del gen inti2, se sembraron después de mezclar 7 ul del ADN amplificado con 3 ul de tampón de carga (azul de bromofenol), como marcador de peso molecular se utilizó l00bp DNA Ladder de Promega (y, como control interno la cepa de referencia UC-4 E. coli).
Una vez que fueron cargados los pocillos en el gel de agarosa, se aplicó un voltaje de 100 V durante aproximadamente 50 minutos para la separación del gen intI 1 y 1 hora y 5 minutos en el caso del gen inti2. Posteriormente, el gel se colocó en una solución de bromuro de etidio a una concentración de 0.5 ug/ml , por un tiempo de 20 minutos. Las bandas de amplificación se visualizaron mediante un transiluminador de luz ultravioleta.
]]> Digestión de los productos de amplificación con enzimas de restricciónPara confirmar la existencia de los genes intlI e inti2, se realizó la digestión parcial de los productos de amplificación con las enzimas de restricción SphI que origina dos fragmentos de 393 y 499 pb en el gen intI 1 y la enzima HaeIII que origina dos fragmentos de 197 y 270 pb para el gen inti2.
La digestión se realizó en un volumen final de 10 ul, de acuerdo al protocolo proporcionado por el Dr. González (2005): 2.5 ul del producto de PCR, 1 ul de buffer de la enzima, 6 ul de agua destilada estéril y 0.5 ul de la enzima. La mezcla se incubó a 37 °C. en baño maría por toda la noche y los productos de restricción se analizaron en un gel de agarosa a 1.5% en tampón TAE., se sembró 8 ul del producto de la digestión y aplicó un voltaje de 100V por 45 minutos. Se utilizaron marcadores de peso molecular de 1 kb DNA Ladder de Invitrogen y de 100 bp DNA Ladder de Promega, la visualización de los fragmentos de restricción se realizó bajo luz ultravioleta en un transiluminador.
Análisis Estadístico
El análisis estadístico se desarrolló con el paquete estadístico SAS versión 9.0, realizando un análisis de distribución de frecuencias. Se aplicó la prueba de Chi cuadrado en el programa SPSS con un intervalo de confianza del 95% de seguridad para establecer la asociación de la resistencia a antibacterianos con la presencia, ausencia y el número de integrones existentes en cada muestra.
RESULTADOS
Prueba de Susceptibilidad a antimicrobianos
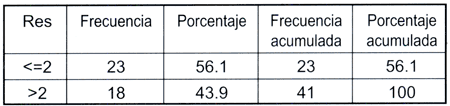
De los ocho antibióticos utilizados en la prueba de susceptibilidad, la mayoría de las cepas (48,8%) aisladas de P. aeruginosa presentaron marcada resistencia a gentamicina, 39 % a cefoperazona, 34,1% a amikacina, 34,1 % a ciprofloxacina, 31.7 % a cefepime, 31.7 % a aztreonam y 28.8 % a ceftazidima. En contraste, la resistencia a imipenem se presentó en 3 de los aislados, siendo éste el agente antimicrobiano que presentó mayor actividad frente a P. aeruginosa. De las 41 muestras solo 4 presentaron sensibilidad a todos los antimicrobianos utilizados. Como se puede apreciar en la tabla 1, las cepas de P. aeruginosa fueron clasificadas en dos grupos dependiendo del número de antimicrobianos por el que presentaban resistencia. El 56.1 % (23 de las 41) de las cepas, presentaban resistencia a 2 o menos antimicrobianos (<=2) y el 43.9 % (18 de 41) fueron resistentes a 3 o más antimicrobianos ( >2 cepas multirresistentes).
]]> Clasificación por multiresistencia bacteriana
Tabla 1: Clasificación de las muestras de acuerdo a la resistencia en el número de antimicrobianos
Resultado de la detección del Gen IntI 1
Los genes IntI1 del Integrón clase 1, fueron detectados en el 46.34 % (19) de los aislados analizados.
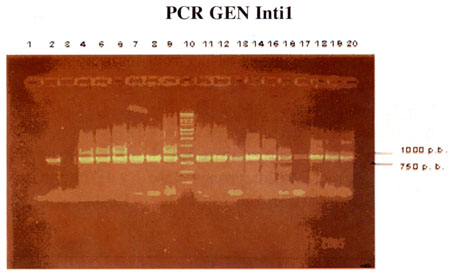
| Figura 2: Representación de la imagen de gel de los productos de amplificación PCR de las muestras de P. aeruginosa positivas para el gen intI1: carril 1: control neg., carril 2: muestra 6. carril 3: muestra 11, carril 4: muestra 16, carril 5: muestra 17, carril 6; muestra 18, carril 7: muestra 19, carril 8: muestra 20, carril 9: muestra 22. carril 10: marcador de peso molecular, carril 11: muestra 24, carril 12: muestra 25, carril 13: muestra 27, carril 14: muestra 28, carril 15: muestra 31, carril 16: muestra 32, carril 17: muestra 33, carril 18: muestra 34, carril 19: muestra 35, carril 20: control UC 7. |
Para confirmar la autenticidad de los productos obtenidos por PCR, se realizaron ensayos con la enzima de restricción SphI, para el gen intI1. obteniéndose como resultado las dos bandas esperadas de 393 y 499 p.b. (Fig. 3), confirmando de esta manera que los productos obtenidos por PCR. correspondían al gen intI1.
]]>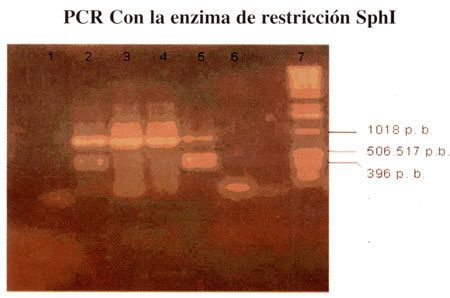
| Figura 3: Análisis del producto de PCR para intI1 mediante la enzima de restricción SphI. carril 1: control negat., carriles 2 y 5: muestra digerida, carril 3 y 4: muestra sin digerir, carril 6: control negativo, carril 7: marcador de peso molecular. |
De las 19 muestras que llevaban integrones clase I (tabla 2), el 31.58 % correspondía a muestras que presentaban resistencia a 2 o menos antimicrobianos y el 68.42 % presentaba resistencia a 3 o más antimicrobianos respecto al 77.27 % y 22.7 % respectivamente de las muestras que no dieron resultados positivos a la detección de integrones clase 1.
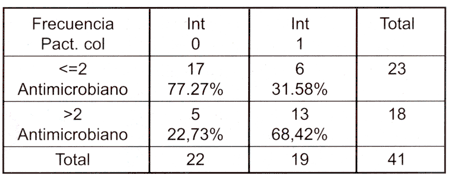
| Tabla 2: Asociación entre el número de resistencia a antimicrobianos y la presencia de integrones clase 1 en las muestras analizadas. |
En relación a la correlación entre la presencia de integrones clase 1 y la multirresistencia bacteriana, ésta fue estadísticamente significativa (X2-test= 0.0033).
]]> Resultados en la detección del gen Intl 2
Solo 12 muestras (29.27%) fueron identificadas como positivas para el gen intI2 (integrón clase 2), generando un producto del tamaño esperado (467 p.b.) como se observa en la figura 4.
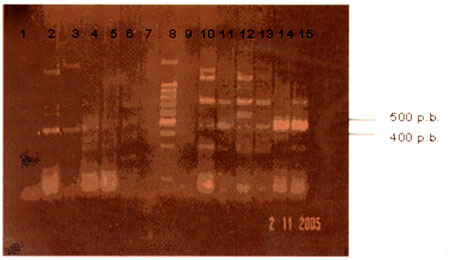
| Figura 4: Resultado de los productos de amplificación de la detección del gen intI2. Carril I: control neg., carril 2: muestra 5, carril 3: muestra 8, carril 4: muestra 14, carril 5: muestra 16, carril 6: muestra 19, carril 7: muestra 22, carril 8: marcador de peso molecular, carril 9: muestra 25, carril 10: muestra 27, carril 11: muestra 28, carril 12: muestra 29, carril 13: muestra 35, carril 14: muestra 39, carril 15: control UC4. |
Para confirmar la autenticidad de los productos obtenidos por PCR, se realizaron ensayos con la enzima de restricción HaeIII (Fig.5). Obteniéndose las bandas esperadas de 197 y 270 p.b.; confirmando de esta manera que los productos obtenidos por PCR. correspondían al gen intI2.
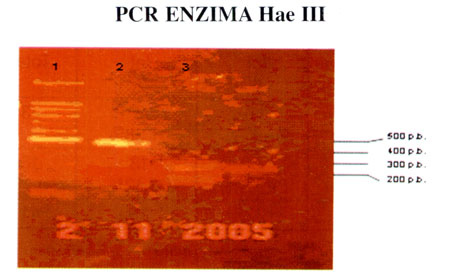
| Figura 5: Análisis del producto de PCR para intI2 mediante la enzima de restricción HaeIII. El detalle de la gráfica se encuentra en la tabla: carril 1: marcador de peso molecular, carril 2: muestra sin digestión, carril 3: muestra digerida. |
De los diferentes aislados que contienen integrones clase 2, el 58.33 fe (7) eran resistentes a 2 o menos antimicrobianos y 41.67% (5) presentaron resistencia a 3 o más (tabla 3).
]]>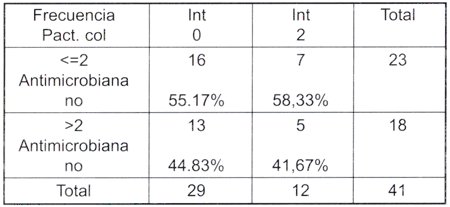
| Tabla 3: Asociación entre el número de resistencia a antimícrobianos y la presencia de integrones clase 2 en las muestras analizadas. |
Se puede apreciar claramente, que no existe diferencia entre la presencia de integrones clase2 y la multiresistencia bacteriana, la respuesta de las muestras frente a la resistencia bacteriana fue la misma que en aquellas muestras que carecen de integrones clase2, la correlación entre la presencia de integrones clase 2 y la multirresistencia bacteriana no fue estadísticamente significativa (p=0.8528).
Como puede observarse, la tabla 4 muestra claramente que en cepas de P. aeruginosa el integrón clase 1 fue el que se encontró en mayor cantidad respecto al integron clase 2. De 41 muestras. 12 (29.27 %) llevaban integrones clase 1; 5 llevaban integrones clase 2 (12.20 %); 7 (17.07 %) tenían los dos tipos de integrones y a 17 muestras (41.46 %) no se les encontró ninguna de las clases de integrones estudiados. En total. 19 integrones clase 1 y 12 integrones clase 2 se identificaron en 24 de los 41 aislados de P. aeruginosa.
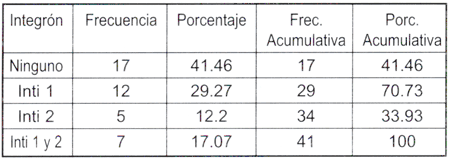
Tabla 4: Distribución de los tipos de integrones en muestras de P. aeruginosa
Al determinar la asociación de la presencia de integrones con la resistencia a múltiples antibióticos en cepas de P. aeruginosa, los aislados se clasificaron en dos grupos: resistentes a dos o menos antimicrobíanos y resistentes a 3 o más antimicrobianos. De las muestras que presentan resistencia a 3 o más antimicrobianos, el 34.1 % (14 de 41) poseían integrones. Solo el 9.76 % (4 muestras) que no poseían integrones tenían resistencia a 3 o más antimicrobianos. El 24.4 % (10) de las muestras que presentaban integrones tenían resistencia a 2 o menos antimicrobianos, y el 31.7 % (13) que no presentaban integrones tenían resistencia a 2 o menos antímicrobianos. Se puede observar claramente que los integrones clase I han sido detectados en mayor proporción (21.95 %) en muestras que presentan multirresistencia (tabla 5).
]]>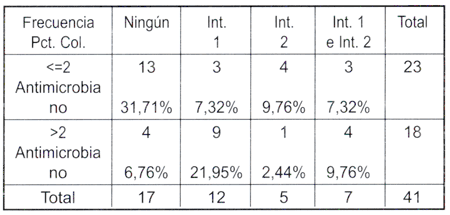
Tabla 5: Resultado del análisis estadístico entre la clase de integrones y el perfil de resistencia bacteriana.
En el presente estudio de las 18 muestras que presentaron multirresistencia. el 75 % (9) poseía integrones clase 1, el 57.14% (4) llevaba los dos tipos de integrones y el porcentaje de las muestras que no poseían integrones y las que poseían sólo el integrón clase 2 no tiene una variación significativa, 23.53 % y 20 % respectivamente (gráfico 1).
Distribución de las clases de integrones

Gráfico 1: Distribución de las clases de integrones de P. aeruginosa y su relación con la resistencia bacteriana.
En las muestras que presentan resistencia a 2 o menos antimícrobianos, se observa que no existe diferencia entre las que llevan integren clase 2 de las que carecen de integrones, pero sí existe diferencia entre las muestras que llevan integrones clase 1 y que presentan resistencia a 3 o más antimicrobianos como se observa en la tabla 5.
DISCUSIÓN
]]> La presencia de integrones clase 1 en cepas que presentan múltiple resistencia a antimicrobianos es bien conocida, hecho que se corrobora en el presente estudio y que se compara con datos proporcionados por Gonzáles y colaboradores (2004), que indican que los integrones clase 1 son predominantes en klebsiella pneumoniae (68.4%). Se puede observar claramente que los integrones clase 1 han sido detectados en mayor proporción en muestras que presentan multirresistencia . Estos datos se encuentran contrastados con los de Van Loom (2004), que encontró que, sólo 1 cepa de 69 aislados de P. aeruginosa llevaba integrón clase 1, indicando que los integrones clase 1 sólo tienen un pequeño rol en la resistencia a drogas en esta especie.Debido a que los patrones de resistencia antimícrobiana cambian constantemente, se puede advertir, que en la biología molecular encontraremos la explicación de los principios que producen la emergencia de bacterias resistentes a varios antibióticos.
La técnica de PCR empleada en el laboratorio de Biología Molecular, para la detección de integrones clase 1 y 2, es un método rápido, un valioso procedimiento y una herramienta simple, que puede emplearse de forma rutinaria para identificar posibles brotes potencialmente epidémicos: esto es importante para la introducción oportuna de medidas de control específicas, evitar su diseminación y transmisión.
CONCLUSIONES
El estudio de la sensibilidad de las muestras de P. aeruginosa a los diferentes antimicrobianos utilizados permitió evaluar la respuesta de los microorganismos a uno o varios antimicrobianos.
Los resultados obtenidos de la prueba de susceptibilidad a antimicrobianos, muestran que de 41 muestras, el 56.10% son resistentes a 2 o menos antimicrobianos y el 43.9 % son resistentes a 3 o más antimicrobianos. En cepas que presentaron resistencia a 2 o menos antimicrobianos se detectó con mayor frecuencia integrones clase 2 (80%), pero este resultado no presenta diferencia significativa (chi-cuadrado 0.8528) en relación a la respuesta a antimicrobianos que presentan las cepas que carecen de integrones (76.47 %). Se detectó con mayor frecuencia integrones clase 1 (75 %) en cepas que presentaron resistencia a 3 o más antimicrobianos, 54.14% de las bacterias multirresistentes presentaron los dos tipos de integrones, el 20 % (n=1) tenía el integrón clase 2 y el 23.53 % carecía de ambos tipos de integrones.
En el presente trabajo, la correlación entre la presencia del integrón clase 1 y la multirresistencia en cepas de P. aeruginosa fue estadísticamente significativa (chi-cuadrado 0.0033).
La autenticidad de los productos obtenidos de la PCR, se confirmaron realizando ensayos de restricción con la enzima SphI que originó dos fragmentos de 393 y 499 p.b. para el gen IntI1 y la enzima HaeIII que originó dos fragmentos de 197 y 270 p.b. para el gen inti2.
De acuerdo a los resultados del presente trabajo, se ha encontrado que las cepas analizadas que presentan integrón clase 1, presentan elevada resistencia a antimicrobianos de primera línea: sulfametoxazol-trimetropin, gentamicina. Es importante destacar también la resistencia hacia quinolonas y cefalosporinas, que puede ser debido al uso indiscriminado de estos antibióticos en la población cochabambina.
]]>BIBLIOGRAFÍA
1. CARATTOLI. A. (2001) importance of integrons in the difusión of resistance. Vet. Res. 32: 243-259.
2. CLARK, C.N., et al (1999) Detection of a Streplomycin/Spectinomycin Adenylytransferase Gene (aadA) in Enterococcus faecalis. Antimicrobial Agents and Chemotherapy, January.p. 157-160. Vol. 43. Nº. 1. [ Links ]
3. COLLINS. M. C; HALL. M. R. (1995) Expression of antibíotic resistance genes ín Ihe integraled cassettes of integrons. Antimicrobial Agents and Chemotherapy. Jan.1995. p. 155-162.
4. FLUIT, A. C; Schmitz, F. J. (1999) Class 1 integrons. gene cassettes, mobility and epidemiology. Eur. J. Clin. Microbiol. Infects. Dis. 18:761-770.
5. GONZÁLES, G. el al (2004) Integrones y cassettes genéticos de resistencia: estructura y rol frente a los antibacterianos. Rev. Méd. Chile. 619-626.
6. HOLMES, J. A.,et al (2003) Recombination activity of a distinctive Integron-Gene cassette system associated wilh Pseudomonas stutzeri populations in soil. Journal Bacteriology, February, p. 918-928. Vol.185, Nº 3.
7. LEVERSTEIN, M.A. et al. (2203) Multidrug resistance among Enterobacteriaceae is strongly associated with the presence of integrons and is independent of species or Isolate Origin. The Journal of Infectious Diseases 187:251-259.
8. LEVERSTEIN, M.A. et al (2002) Presence of integron-associated resistance in the Community is widespread and contributes to multidrug resistance in the Hospital. Journal of Clinical Microbiology, August. p. 3038-3040, Vol. 40, Nº 8.
]]> 9. LÉVESQUE. C. el al (1995) PCR Mapping of Integrons Reveals Several Novel Combinations of Resistance Genes. Antimicrobial Agents and Chemotherapy, Jan., p. 185-191.10. NATIONAL COMITÉ FOR MEDICAL LABORATORY STANDARD (NCCLS) (2003). Texto proporcionado por el INAMEN.
11. PATRIDGE.R.S.et al.(2000)Definition of the aattIl site of class 1 integrons. Microbiology 146:2855-2864.
12. RAMÍREZ, M. (2004) Perfil Plasmídico y resistencia antimicrobiana en cepas de Shigella aisladas en Cuba. Rev. Cubana Me.Trop.56(3):178-85.
13. ROY, P. (1995) Integrons: novel mobile genetic elements mediating antibiotic resistance in Enterobacteria and Pseudomonas APUA.Newsletter 13(3): 1.4-6.
14. SEVERINO. P.; MAGALHAES, V. D. (2004) integrons as tools for epidemiológical studies. Clinical Microbiology and Infection. Vol. 10 Issue2 Page 156.
15. LOON, VAN. Et al (2004) Evaluation of genetic determinante involved in B-lactam-and multirresistance in a surgical ICU. Int. Journal Antimicrob.Agents 24, 130-134.
16. VILA, J.; FRANCESC, M. (2002) Lectura interpretada del antíbiograma de bacilos gramnegativos no fermentadores. Enferm Infecc Microbiol Clin., 20(6):304-12.
17. YOUNG, J. et al (2002) Epidemiológica! typing and prevalence of integrons in multirresistant Acinetobacter strains. Apmis Vol. 110 Issue 3 Page 247.
]]>