INTRODUCCIÓN
La resistencia antimicrobiana (RAM) es la capacidad de los microorganismos a resistir a la acción farmacológica de los antibióticos, misma que representa una grave amenaza para la Salud Pública nacional e internacional. En este contexto, numerosos estudios han evidenciado una relación directa entre el uso indiscriminado de antibióticos y las RAM, reportando un elevado índice de mortalidad como consecuencia de la evolución y generación de nuevos mecanismos de resistencia farmacológica 1,3.
El Centro para Control y Prevención de Enfermedades (CDC) ubicado en los Estados Unidos informa que el costo humano y económico de la RAM es muy elevado. Se estima que cerca de 2 millones de infecciones se producen por microorganismos multirresistentes a los antibióticos y cerca de 23.000 muertes al año. Estudios sugieren que el impacto a la economía y gastos públicos con relación a la resistencia de los antimicrobianos en países de bajo y mediano desarrollo podrían ser mucho mayores. Un informe revelado por el Ministro de Reino Unido ha proyectado que sin la ayuda de la comunidad internacional a los países de bajo desarrollo, se producirán alrededor de 10 millones de muertes por infecciones RAM para el año 2050, superando la mortalidad por cáncer y otras patologías, además de afectar significativamente la economía mundial 4,5.
América Latina refleja que, los microorganismos multidrogorresistentes y extremo drogorresistentes son la principal causa de las infecciones y muertes relacionadas a la atención hospitalaria. Por otro lado, los datos procedentes de la red de vigilancia RAM (RELAVRA) revelan un creciente desarrollo de la resistencia de bacterias intrahospitalarios, como Klebsiella pneumoniae (KPC), cuyo porcentaje de resistencia a los fármacos carbapenémicos está aumentando en Latinoamérica y el mundo desde principios del 2014, llegando a cifras del 21 % de resistencia en algunos casos6,7.
En este sentido Brasil fue uno de los primeros países en reportar casos de resistencia antimicrobiana para K. pneumoniae productora de carbapenemasas (KPC), en el año 2003. Posteriormente en el año 2005, Colombia y Argentina reportaron otros casos de RAM para K. pneumoniae. Hasta el año 2019 todos los países latinoamericanos ha reportado casos de RAM, con diferentes mecanismos de resistencias8.
Ecuador en el año 2010 dio conocer uno de los primeros casos de resistencia antimicrobiana para Klebsiella pneumoniae productora de carbapenemasas tipo KPC-2, esta enzima inhibe la acción de los fármacos de tipo carbapenémicos. Hasta la fecha se han reportado innumerables investigaciones de RAM, para los cuales los microorganismos han desarrollado múltiples mecanismos de resistencia, y entre los más preocupantes destacan: BLEE, KPC y, más recientemente, NDM y mcr-19,8.
Alrededor de todo mundo existen diversos estudios sobre la RAM, sin embargo, en Ecuador donde las condiciones clínicas, ambientales y tecnológicas son diferentes. Las investigaciones se limitan a las elaborados por Iñiguez, et al. (2012), donde identificaron por primera vez una cepa aislada de K. pneumoniae productora de carbapenemasas tipo 2, las realizadas por la Pontificia Universidad Católica del Ecuador (PUCE) y el Instituto Nacional de Investigación en Salud Pública (INSPI) (Tamayo et al., 2016) en donde se revelan más casos de resistencia de microorganismo en los hospitales.
Por lo tanto, esta revisión tuvo como propósito generar información actualizada, sobre los principales mecanismos de resistencia en Ecuador. Además, la vigilancia de la RAM permite generar información relevante sobre los cambios de patrones de resistencia a los antimicrobianos. Con la consecuente generación de estrategias de prevención, control y orientación en la toma de decisiones en políticas públicas 10,11.
El objetivo de la presente investigación fue analizar la evolución de la resistencia antimicrobiana en Klebsiella pneumoniae a partir de la prevalencia de los principales mecanismos de resistencia que este patógeno presenta en Ecuador, durante el periodo 2000-2020.
Tabla 1. Esquema de la pregunta pico.
MÉTODO
Se realizó una revisión sistemática de la literatura científica de estudios observacionales, de resistencia antimicrobiana en Klebsiella pneumoniae. Con base a la metodología PRISMA (Preferred Reportin Items for Systematic Reviews and Meta-Analyses 12. Se realizó una búsqueda bibliográfica de artículos originales y meta análisis en las bases de datos Medline (Pubmed), SciELO, Web of Science y Lilacs mediante los descriptores en Ciencias de la Salud (DeCS) y MesH (Medical Subject Headings): Klebsiella pneumoniae/ Klebsiella pneumoniae; resistencia a Antibióticos; /resistance to Antibiotics; farmacorresistencia bacteriana /bacterial drugresistanc, identificados tras la formulación de la pregunta PICO, y con la ayuda de los operadores booleanos OR/O y AND/Y.
Se consideraron artículos en inglés y español, con combinaciones de términos. Abarcando artículos publicados desde enero de 2000 hasta diciembre de 2020, en idioma inglés o español. Fueron elegidos aquellos artículos primarios. La evaluación de la calidad de los artículos seleccionados, el análisis de la variabilidad, validez y fiabilidad de los artículos seleccionados fueron valorados por la metodología PRISMA en base a los de criterios de selección de búsqueda de bibliografía y selección de estudios, y a nivel de evidencia que estos presentaban.
Se incluyeron aquellos estudios que cumplían las siguientes características: estudios experimentales, estudios observacionales analíticos y descriptivos, estudios de casos y controles, y reporte de casos. Además, se incluyeron aquellos que se tenga libre acceso al documento completo en formato digital, en el periodo comprendido de los últimos veinte años y en idioma de publicación inglés, español.
El criterio de exclusión consistió, en el análisis del título de los artículos y la revisión del resumen, de los cuales se excluyeron aquellos artículos que presentaron: especies de bacterias diferentes a K. pneumoniae, estudios realizados en otras especies que no sean humanos, estudios experimentales realizados en pequeñas poblaciones de humanos, entrevistas, cartas, reseñas y estudios no relacionados con prevalencia y resistencia de Klebsiella pneumoniae.
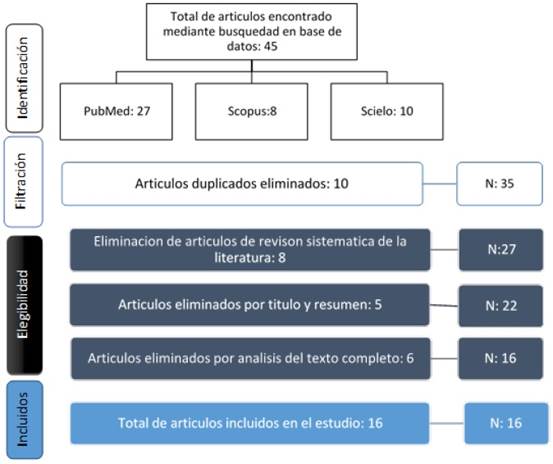
Para evaluar resistencia antimicrobiana en Klebsiella pneumoniae a partir de la prevalencia de los principales mecanismos de resistencia, se realizó una búsqueda de información empleando combinaciones de términos y operadores booleanos en la búsqueda general de la base de datos; PubMed donde se obtuvo 27 artículos, Scopus 8 artículos y Scielo 10 artículos, dando un total de 45 artículos.
Siguiendo la metodología prisma de los 45 artículos se revisaron los duplicados, seleccionando 35 artículos, se eliminaron artículos de revisión sistemática, obteniendo 27 para el análisis. Después de aplicar los criterios de inclusión y exclusión, se asignaron 22 artículos para revisión detallada del texto completo, seleccionando 16 artículos para la extracción y análisis de datos. Ver Figura 1.
RESULTADOS
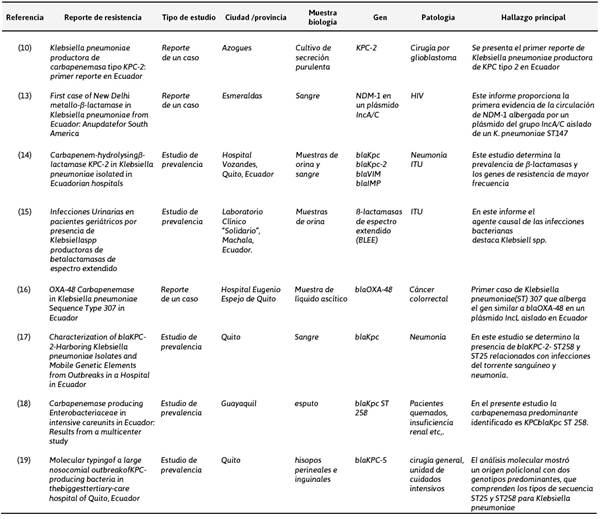
Cuatro de los estudios se realizaron la ciudad de Quito reportando los genes de resistencia blaKpc, blaKpc-2, blaVIM, blaIMP y blaOXA-48 el más reciente. Guayaquil por su parte reporta el gen de resistencia blaKpc ST 258, en la ciudad de Azogues reporta blaKpc-2, contrario a esto Esmeralda reporta el gen de resistenciaNDM-1 siendo la primera evidencia de tipo New Delhi metalobetalactamasa que albergada por un plásmido del grupo IncA/C aislado de un K. pneumoniae ST147. Ver Tabla 2.
Tabla 2 Resumen de casos reportado y estudios realizados en Ecuador en función a los mecanismos y genes de resistencia en Klebsiella pneumoniae.
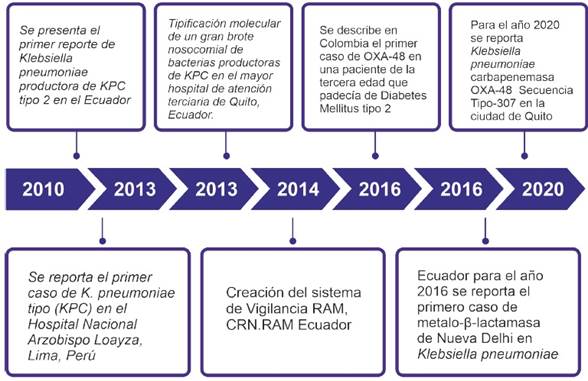
A continuación se detalla una línea de tiempo desde el 2010 como primer caso reportado en la ciudad de Quito de Klebsiella pneumoniae productora de KPC tipo 2, tres años más tarde, 2013, Perú reporta el primer caso de K. pneumoniae tipo (KPC) en el Hospital Nacional Arzobispo Loayza, para el mismo año en la ciudad de Quito se realiza una tipificación molecular de un gran brote nosocomial de bacterias productoras de KPC, con estos antecedes se decide la Creación del sistema de Vigilancia RAM de Ecuador. En el año 2016, Ecuador reporta el primer caso de metalo-β-lactamasa de Nueva Delhi en Klebsiella pneumoniae, y como último dato para el año 2020 reporta Klebsiella pneumoniae carbapenemasa OXA-48 Secuencia Tipo-307 en la ciudad de Quito. Ver Figura 2.
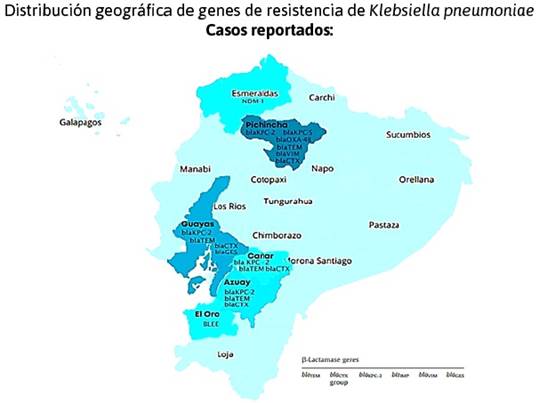
La Distribución geográfica de genes de resistencia de Klebsiella pneumoniae se establece principalmente en las provincias de Pichicha, Guayas y Azuay, sin embargo, en la provincia de Esmeralda se reporta Klebsiella pneumoniae de Nueva Delhi, considerado un gen de gran relevancia por la facilidad de crear mecanismos de resistencia antimicrobiana. Ver Figura 3.
DISCUSIÓN
La resistencia antimicrobiana de Klebsiella pneumoniae, es una de las grandes preocupaciones de la red de Salud Pública, tanto de los países desarrollados y en vías de desarrollo, por lo tanto, es necesario una correcta información sobre el uso de antibióticos ya que esto optimizará el uso racional de los mismos, controlando las bacterias multirresistentes, y ayudando prevenir nuevas resistencias 20,22.
En sí, las infecciones por Klebsiella pneumoniae no muestra un afinidad especifica por un órgano o tejido, ya que era considerado como una bacteria saprofítica en el hombre colonizando la piel, nasofaringe y tracto gastrointestinal, sin embargo, a partir de los años 70, la epidemiología y amplio espectro de este microorganismo, cambió drásticamente cuando Klebsiella pneumoniae se estableció mayoritariamente en los ambientes intrahospitalarios, convirtiéndose en una de las principales causas de infecciones nosocomiales, aumentado la tasa de mortalidad y disminuyendo las opciones terapéuticas para su tratamiento 23,21,22.
Klebsiella pneumoniae era muy poco común para el año 2000 en Ecuador, sin embargo, en el años 2010, un trabajo realizado por Iñiguez et al., reportaron por primera vez una cepa de Klebsiella pneumoniae productora de carbapenemasas (KPC) tipo 210, tratándose de un paciente de 24 años de edad de sexo masculino, sin antecedentes de viaje al exterior, que fue sometido a cirugía en la ciudad de Azogues, Hospital Homero Castanier. La identificación se realizó mediante PCR determinando la carbapenemasas tipo 2 y su mecanismo de resistencia. Tras este reporte se empezó a identificar más casos de resistencia en las principales ciudades del país.
Por su parte, para el año 2005, Colombia reporta su primer caso Klebsiella pneumoniae tipo (KPC)24. Velásquez, et al, en el año 2013, reportaron el primer caso de K. pneumoniae tipo (KPC) en el Hospital Nacional Arzobispo Loayza, Lima, Perú, en una paciente diagnosticado con lupus eritematoso sistémico acompañado de insuficiencia renal 24. Cabe destacar que los tres casos, se trata de pacientes con patologías crónicas permaneciendo internado en hospitales por más de tres días, convirtiendo a K. pneumoniae como una bacteria de predominio intrahospitalario de grandes desafíos en el tratamiento clínico 25. Según Vera et al. 2017, aunque se trata de una misma enzima (KPC) están pueden tener diferentes mecanismos de resistencia y de espectro, dependiendo directamente de la localización molecular 20, para Pitout 2015, el predominio molecular en nuestra región es Tn4401, plásmidos de tipo IncFII, CC25826.
A principios del año 2011 un nuevo mecanismo de resistencia para K. pneumoniae se empezó a reportar en Latino América , tratándose de la enzima New Delhi metallo-beta-lactamase (NDM-1), iniciando con Guatemala y posteriormente, Colombia 2013, desde allí se han ido reportando casos de este tipo de resistencia en cada país 27. Álvarez et al., 2016, reportaron el primero caso de esta enzimametalo-β-lactamasa de Nueva Delhi de Klebsiella pneumoniae en Ecuador tratándose de un paciente seropositivo VIH. La identificación del microorganismo se la realizó mediante secuenciación del ADN bacteriano, la caracterización del plásmido se desarrolló a través de la tipificación de replicones. Cabe destacar que este reporte representa las primeras evidencias de genes de resistencia NDM-1 en el país y consecuente en la provincia de Esmeraldas 13.
Para el año 2016, Resurrección, reportaron el primer caso de K. pneumoniae, de tipo NDM en el Hospital Nacional Dos de Mayo de Perú, identificando y caracterizando a través de tipificación molecular y genes de resistencia 28. Este estudio da mortalidad global alta de alrededor 55%, en contraste, el Instituto Ecuatoriano de Seguridad Social (IESS) reporta una mortalidad del 41 al 55%, similares a los datos presentados por Resurrección et al., los estudios comparados presentan datos equiparables, ya sea por la cercanía culturales y ambientales de los dos países 28,27,29.
Contrario a esto para el año 2020 Villacís, reporta Klebsiella pneumoniae carbapenemasa OXA-48 secuencia Tipo-307 en la ciudad de Quito; se trata de un paciente de origen ucraniano con antecedentes de cáncer colorrectal, la identificación se lo realizó mediante la secuencia del multilocus según las recomendación del Instituto Pasteur. Cabe mencionar que la principal característica de carbapenemasa OXA-48 es capacidad de movilidad, y en particular este clon se lo relaciona con la presencia de elementos móviles 30,27. El genoma ST307 perteneciente Klebsiella pneumoniae carbapenemasas OXA-48 constituyes algunos genes de virulencia, lo que sugiere Villa et al., que este clon contienes viarias ventajas y una de ellas es la rápida diseminación a nivel intrahospitalarios 27,29.
Vanegas, describe en Colombia el primer caso de OXA-48 en una paciente de la tercera edad que padecía de Diabetes Mellitus tipo 2. Para ambos casos los pacientes tenían un historial médico de haber sido intervenido quirúrgicamente, esto hace sospechar que la diseminación del microorganismo prevalece a nivel hospitalario y posiblemente las áreas de quirófano son las de mayor frecuencia 31.
CONCLUSIÓN
La resistencia microbiana representa un gran problema de nivel de los sistemas de salud ya sea por aumento de la alta tasa de mortalidad o falla en el terapia farmacológica, aumentando la estancia hospitalaria, y consecuentemente generando un significativo el gasto público de los hospitales, por lo tanto, el establecer medidas de control y prevención, así como la detección precoz en el diagnostico son una estrategia clave para disminuir la propagación de este tipo de cepas resistentes.
Además, se debe controlar la rápida propagación de los genes de resistencia, así como uso racional de los antibióticos en los profesionales de la salud y los hábitos de prescripción ya que en actualidad Klebsiella pneumoniae es considerado un problema emergente de Salud a nivel mundial con tendencia a seguir desarrollando mecanismos de resistencia a antimicrobianos.
En cuanto la evolución de la resistencia antimicrobiana en Klebsiella pneumoniae, se puede rescatar que este microorganismo ha avanzado mucho desde su primer reporte en 2010, hasta su último reporte en el año 2020, ya sea generando nuevos mecanismos de resistencia o reforzando los mismo. Además, es importante tomar en cuenta que la rápida propagación de la resistencia a antimicrobiana se le atribuye a la variabilidad de los genes de virulencia y la velocidad diseminación en los ambientes intrahospitalarios, convirtiendo a Klebsiella pneumoniae tipo KPC-2 la de mayor prevalencia comparada con otras especies.
Finalmente, los principales reportes de esta investigación se realizaron en las grandes ciudades, Quito, Guayaquil y Cuenca, ya sea por facilidad de los equipos de diagnóstico o la ubicación de los centros de investigación, lo que genera una mayor accesibilidad comparada a las otras ciudades