Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Investigación & Desarrollo
versión impresa ISSN 1814-6333versión On-line ISSN 2518-4431
Inv. y Des. vol.1 no.15 Cochabamba 2015
ARTÍCULOS - INGENIERÍAS
EXTRACCIÓN DE PECTINA DE RESIDUOS DE CÁSCARA DE NARANJA POR HIDRÓLISIS ÁCIDA ASISTIDA POR MICROONDAS (HMO)
PECTIN EXTRACTION FROM ORANGE PEELS WASTE BY MICROWAVE ASSISTED ACID HYDROLYSIS (MWAH)
Vanesa Y. Zegada Franco
Centro de Investigaciones de Procesos Industriales (CIPI)
Universidad Privada Boliviana
vanesa.zegadaf@gmail.com
(Recibido el 30 de octubre 2014, aceptado para publicación 20 de mayo 2015)
RESUMEN
Se presenta un estudio de comparación, a nivel laboratorio, de dos métodos de extracción de pectina a partir de residuos de cáscara de naranja: el método por hidrólisis ácida convencional y el método de extracción por hidrólisis ácida asistida por microondas (HMO). Los tiempos requeridos para la extracción por HMO fueron considerablemente menores. Se establecen los siguientes valores óptimos para la operación de hidrólisis mediante ambos métodos, dentro de los rangos estudiados: 2,17 para el pH y 18:1 para la proporción de solvente:materia prima(mL:g). El tiempo óptimo para la extracción HMO fue 7 min. Se ha obtenido una ecuación, que representa el desempeño de la extracción de pectina HMO con confiabilidad dentro del intervalo de valores estudiado, para estimar el porcentaje de rendimiento en función del pH, proporción solvente: materia prima y tiempo de extracción. Aplicando este método se pretende generar un ahorro de energía y tiempo en el proceso de producción de pectina.
Palabras Clave: Pectina, Microondas, Hidrólisis Ácida, Residuos de Naranja (Citrus cinensis).
ABSTRACT
A comparison study, at laboratory scale, of two pectin extraction methods using orange peels waste is presented: conventional acid hydrolysis and acid hydrolysis assisted by microwave (MWAH). Extraction times were considerably lower for MWAH. The following optimal values for both methods were determined within the studied ranges: 2.17 for pH and 18:1 for solvent:raw material ratio. The optimal time for HMO was 7 min. An equation that represents the performance of MWAH pectin extraction, reliable within the studied range, was obtained, to estimate the recovery percentage as a function of pH, solvent:raw material ratio and extraction time. By applying this method, a save of energy and time on pectin extraction process is expected.
Keywords: Pectin, Microwave, Acid Hydrolysis, Orange Peels (Citrus cinensis) Waste.
1. INTRODUCCIÓN
La pectina es un polisacárido empleado como aditivo natural en diversas industrias de alimentos, como gelificante, espesante, estabilizante y emulsificante de otros productos. Asimismo, en la industria farmacéutica y el área de biotecnología, la pectina se utiliza en la formulación de fármacos, cosméticos, con fines terapéuticos y otros [1, 2].
La pectina se encuentra presente en todos los tejidos vegetales, aunque, por su contenido, sólo algunas variedades son adecuadas para la extracción comercial. Actualmente, a nivel industrial, la pectina se extrae comúnmente de residuos de manzana o naranja, derivados de la producción de sidra y jugos(Voragen, F., et al.[3]). Otras interesantes fuentes alternativas para la extracción de pectina a partir de residuos industriales son los provenientes del procesamiento de papaya, mango, melocotón, girasol, café y cacao [3-7].
Para la extracción convencional de pectina, es necesario el calentamiento de elevadas cantidades de solvente a temperaturas superiores a 60 °C durante periodos típicamente mayores a 30 minutos y que pueden llegar hasta 6 horas(Voragen, F., et al.[3]), lo cual representa un elevado consumo de energía, contraponiéndose a la tendencia actual de utilizar métodos de producción cada vez más eficientes energéticamente en el ámbito industrial. Este uso de energía, puede reducirse sustancialmente aplicándose un calentamiento homogéneo por radiación, mediante el método de extracción de pectina por hidrólisis ácida asistida por microondas (HMO) [8 - 10], que se analiza en el presente estudio.
2. ESTRUCTURA QUÍMICA, PROPIEDADES Y PROCESOS DE OBTENCIÓN DE LA PECTINA
● Estructura Química de la Pectina
La pectina es un carbohidrato complejo, que contiene al menos 65 % de unidades de ácido galacturónico, C6H10O7 [3]. Las cadenas de pectina están formadas por anillos de este ácido, cuyo número varía, desde algunos centenares, hasta alrededor de 1 000, con masas moleculares de aproximadamente 50 000 a 150 000 daltons [1]. Cada anillo de la cadena posee un grupo carboxilo (-COOH), que puede estar esterificado con metanol, produciendo ésteres metílicos (-COOCH3), o quedar neutralizado por una base, como se esquematiza en la cadena con cuatro anillos de ácido de la Figura 1.
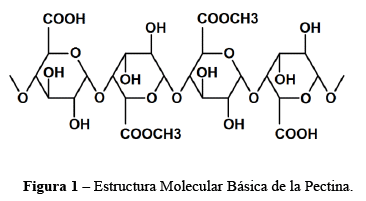
El ácido galacturónico de la pectina, viene acompañado, también, de azúcares neutros, como la D-galactosa, L-arabinosa y L-ramanosa[1], [6], [11]. La Figura 1, muestra el cuerpo principal de la pectina, pues su estructura real es bastante compleja y es un gran desafío acomodar toda la información que se tiene sobre esta molécula en un modelo estructural, a pesar de ello, se han desarrollado varios modelos hipotéticos de este compuesto[12].
Las pectinas se clasifican según su grado de esterificación, GE, expresado en porcentaje, ya que sus propiedades gelificantes están principalmente determinadas por el mismo. Según Sriamornsak[1], el GE varia 20 y 40% en las pectinas comerciales de bajo metoxilo y entre 60 y 75% en las de alto metoxilo.
El proceso de extracción convencional por hidrólisis ácida de la pectina de residuos de naranja, da como resultado, una pectina con aproximadamente 70 % de esterificación, aunque puede alcanzarse grados de esterificación mayores[6]. Para la producción de otros tipos de pectina, con menores grados de esterificación, debe hidrolizarse algunos ésteres metílicos adicionales, generalmente, mediante una extracción prolongada, tratamientos ácidos o alcalinos en alcohol o haciendo uso de enzimas desesterificantes (como la pectina esterasa) [3], [6]. Cuando la pectina se somete a una desesterificación alcalina, en presencia de amoniaco, se forman amidas (–COONH2) en las cadenas ácidas, obteniéndose la pectina amidada[3].
A mayor grado de esterificación, se obtiene una gelificación más rápida. En función a dicha velocidad de gelificación y dependiendo de si están o no amidadas, las pectinas de alto y bajo metoxilo se subdividen como se detalla en la Figura 2[3].
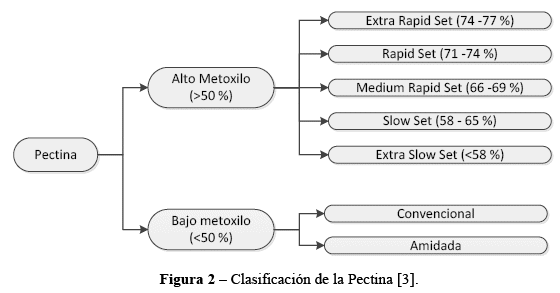
● Parámetros de Medición de la Calidad de la Pectina
La pureza de la pectina se mide mediante el porcentaje de ácido galacturónico, que representa la masa total de anillos de dicho ácido, sobre la masa total de pectina. Tiene un valor mínimo de 65 % según la FAO y la FDA [13], [14], aunque, según lo normado por la USP (United States Pharmacopeial Convention) este porcentaje debe encontrarse encima del 74 %,[14], [15].
Las características gelificantes están determinadas por el porcentaje de metoxilación de la pectina, calculado por la relación entre la masa total de grupos éster metílicos, sobre la masa total de pectina[13]. Para pectinas de alto metoxilo, este porcentaje debe encontrarse por encima del 6,7 % según lo normado por la USP[15].Porcentajes menores a este valor, corresponden a pectinas de bajo metoxilo[7].
El grado de esterificación se mide dividiendo las unidades de grupos metoxilo entre las unidades de ácido galacturónico, determinadas mediante titulaciones de muestras tratadas de pectina [13].
● Proceso de Obtención de la Pectina
Aunque existen diversas variantes del proceso de obtención de pectina, a continuación se describe el básico y típico, que se divide en tres fases: pre-tratamiento, extracción y homogeneización.
El pre-tratamiento consta del secado del material del cual se extraerá la pectina hasta aproximadamente un 10% de humedad, seguido de una trituración. La extracción consiste, básicamente, en la hidrólisis ácida (la etapa más importante) en condiciones específicas de pH, temperatura y tiempo, las cuales son las variables independientes que determinan la calidad del producto y el rendimiento del proceso. Las etapas subsecuentes son: la operación de clarificado, donde se separa la solución de pectina del bagazo, una precipitación alcohólica y posterior centrifugado o filtrado, donde se aísla la pectina de dicha solución. Finalmente, la pectina húmeda se seca con aire caliente hasta una humedad apropiada, para luego lograr la homogeneización del tamaño de partícula del producto mediante el pulverizado como se detalla en la Figura 3.
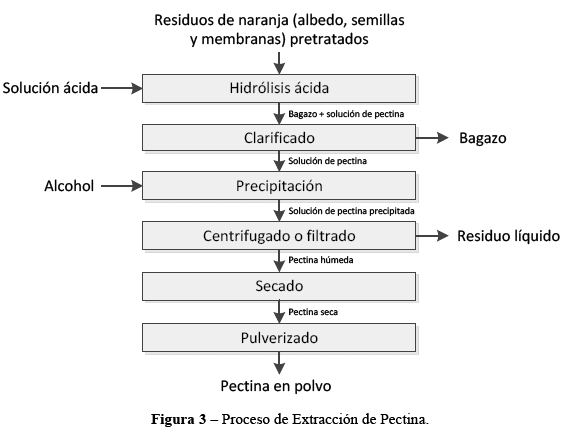
● Variables del Proceso de Extracción de Pectina
En general, combinaciones de pH bajo, temperatura alta y tiempo elevado, dan lugar a la degradación de la pectina, reduciendo el tamaño de las moléculas, afectando, de esta manera, su viscosidad. Bajo estos parámetros, se incrementa también la hidrólisis de los grupos carboxilos, reduciendo el porcentaje de esteres metílicos en las cadenas. En el caso opuesto (pH alto, temperatura baja y tiempo corto) se logra hidrolizar un porcentaje muy bajo de pectina, obteniéndose un bajo rendimiento.
El rango de pH generalmente utilizado para la extracción de pectina varía entre 1,5 y 3[3]. Dentro de este rango, Joye, D. y Luzio, G. [16], A. han probado que, sin adición de sales polivalentes, en extracciones con un pH entre 3 y 3,3 es posible extraer sólo la pectina no sensible al calcio, mientras que, con un pH cercano a 2 se logra, también, la extracción del resto de la pectina.
Fishman, M. L., et al.[10], utilizando valores de pH entre 1 y 3, han confirmado el incremento del rendimiento con el descenso del pH y, por otro lado, la obtención de una mayor masa molar y viscosidad intrínseca con el incremento del mismo. Por lo tanto, es recomendable acercarse a un valor medio dentro de este rango.
Del mismo modo, en estudios pasados se han utilizado medios alcalinos para la extracción de pectina. Mediante la extracción bajo estas condiciones, se ha logrado una ruptura de enlaces similar a la de la extracción en medio ácido, sin embargo, se causa inestabilidad en la cadena principal de la pectina, que tiende a descomponerse y, en consecuencia, no es posible realizar la precipitación alcohólica [9].
Mientras el tiempo de extracción por el método convencional varía entre 30 y 360 minutos[3], diversos estudios del método microondas han obtenido buenos resultados con tiempos menores a 15 minutos. Yeoh, S., et al. [9] obtuvieron un rendimiento casi constante para tiempos que variaron entre 5 y 15 minutos, afirmando, además, que al aplicar una extracción por HMO durante 15 minutos, se logró obtener la misma cantidad de pectina que con una extracción de 3 horas por el método Soxlet. Por su parte, Fishman, M. L., et al. [10] aplicaron un método de extracción por HMO bajo presión elevada, utilizando residuos de lima, con un tiempo de extracción que varió entre 2,5 y 15 minutos, obteniendo los mejores rendimientos para el rango de 2,5 a 6 minutos.
Paralelamente a las ventajas de la extracción asistida por microondas, relacionadas al ahorro de energía y tiempo, existen algunos peligros con respecto al efecto de las ondas electromagnéticas en la estructura molecular y las células del material sobre el cual se aplican. Zhongdong, L., et al. [17] realizaron un estudio de imagen, a nivel microscópico, comparando la pectina extraída por los métodos por hidrólisis convencional y por HMO. Los resultados demostraron que, a una potencia de 1000 W y aplicando 5 minutos de extracción, la radiación microondas tiene un efecto destructivo sobre la organización de la estructura de la piel de naranja; efecto más intenso que el ocasionado realizando una extracción durante 18 horas por el método convencional. Por otra parte, el efecto de hinchazón generado por las microondas causa, inclusive, daño en las células. Por esta razón, es necesario el estudio de menores potencias de operación.
Las temperaturas generalmente aplicadas para la extracción de pectina varían entre 40 y 100 °C. Gilabert [6] ha demostrado que, aplicando una temperatura elevada (80 °C), durante un periodo mayor a 40 minutos, se reduce el tamaño de las cadenas y el poder gelificante de la pectina. Al emplearse el calentamiento por microondas en la extracción, por el contrario, la muestra no se expone durante un periodo elevado a temperatura alta ni pH bajo, lo cual, podría mejorar la calidad de la pectina. Sin embargo, puede darse lugar a otro tipo de degradación causada por las ondas electromagnéticas propias de la radiación microondas.
Por otra parte, el mayor porcentaje de los costos del proceso de obtención de pectina, a nivel industrial, es generado por el solvente ácido y alcohol usados en las operaciones de hidrólisis y precipitación, respectivamente. Por esta razón, en este estudio se analizan, también, las proporciones óptimas de uso de estos dos compuestos en dichas operaciones.
3. MÉTODOS Y PROCEDIMIENTOS EXPERIMENTALES
● Recolección, Pre-tratamiento y Conservación de la Materia Prima
Se recolectó aproximadamente 8 kg de residuos de naranja, incluyendo el albedo (o parte interna blanca da la cáscara), semillas y membranas, de diferentes vendedores ambulantes de jugos, con el fin de tener una muestra con características del fruto y grados de madurez variados. Se secó las muestras hasta un 10 % de humedad, se las trituró y almacenó protegidas de la luz y la humedad del ambiente. El material resultante del procedimiento descrito se denomina como materia prima en la presente investigación. Mediante dos operaciones de extracción de pectina (al inicio y al final del estudio, dos meses después), bajo condiciones idénticas, se comprobó que la materia prima no se degradó durante el periodo de desarrollo del estudio.
● Caracterización de los Residuos de Naranja
La determinación de la humedad se realizó mediante un humidímetro de rayos infrarrojos. El contenido de pectina se determinó empleando el método propuesto por Nielsen [18]. Ambas determinaciones se realizaron por duplicado.
● Variables de la Operación de Hidrólisis
El proceso de hidrólisis se realizó con 60 g de materia prima por prueba, en un sistema abierto, sin agitación, irradiado con 540 W a una frecuencia de 2 450 MHz, empleando ácido cítrico como solvente, a una temperatura de 91 °C (temperatura de ebullición del solvente a la presión atmosférica local, 75,1±0,5 kPa).
Los factores experimentales independientes adoptados en el experimento y sus respectivos niveles de variación, se presentan en la TABLA 1. Dichos valores se establecieron después de realizar pruebas preliminares de extracción.Se aplicó un análisis ANOVA, mediante el software Statgraphics Centurion versión XV, con un diseño factorial de los tres factores a dos niveles, aleatorizado, sin bloques, incluyendo dos puntos centrales y con un nivel de significancia igual a 0,05. En total, se realizaron 10 pruebas, incluyendo los dos puntos centrales, lo cual permitió tener 3 grados de libertad para el error.

Se consideró como objetivo, la maximización de tres variables de respuesta: rendimiento, porcentaje de ácido galacturónico y porcentaje de metoxilos del producto final.
El cálculo del rendimiento de cada corrida se realizó sobre el peso de la materia prima (en base seca).Los porcentajes de ácido galacturónico y metoxilos en el producto final de cada corrida, se determinaron por titulación, de acuerdo con el método establecido por la FAO [13] para la caracterización de pectinas.
● Análisis del Porcentaje de Solvente para la Operación de Precipitación
El proceso de precipitación se ejecutó haciendo uso de etanol comercial (96 % de pureza), con 5 minutos de agitación y 20 minutos de reposo.
Se estudió el porcentaje mínimo de volumen de etanol respecto al volumen de solución de pectina (resultante del proceso de hidrólisis) a usarse, sin alterar el rendimiento del proceso. Los niveles de este porcentaje de etanol se muestran en la Tabla 2.

Seaplicó para el análisis, un diseño simple, con un solo factor categórico, aleatorizado, sin bloques, con un nivel de significancia de 0,05.significancia de 0,05. Se desarrollaron 4 corridas, obteniéndose 2 grados de libertad para el error. Los resultados se analizaron, también, haciendo uso del software Statgraphics Centurion versión XV.
Inicialmente se construyó un diseño de tres niveles (40, 50 y 60%), sin embargo, se comprobó que no era posible la precipitación de pectina para el menor valor (40%), por lo tanto se consideró el valor mínimo como 50%. La variable de respuesta fue el rendimiento, buscándose la maximización de la misma.
● Comparación de los Métodos de Extracción Convencional y Microondas
Con el fin de verificar si los efectos de los niveles de los factores del modelo planteado, son lineales sobre la variable de respuesta, se desarrolló el análisis del efecto de la curvatura de los valores de entrada, con los datos de las pruebas de extracción por el método asistido por microondas. De no ser así, sería necesario plantear un diseño con tres niveles para cada factor (en lugar de dos). Una vez realizada la verificación mediante el software Statgraphics Centurion versión XV, se determinaron la ecuación de regresión ajustada a los datos y la correspondiente superficie de respuesta, para el método de extracción microondas.
Se tomaron parámetros óptimos de pH y proporción de solvente del método de hidrólisis asistida por microondas, determinados por la ecuación, para realizar las pruebas de extracción por el método convencional. Se realizaron 4 pruebas de extracción por el método convencional, utilizando 40 gramos de materia prima por prueba, con un tiempo de extracción igual a 45 minutos, en un sistema cerrado, con agitación y con todos los demás parámetros de operación idénticos a los de la extracción por microondas.
Se comparó el rendimiento calculado, mediante la ecuación de regresión ajustada del método microondas, con el rendimiento obtenido mediante el método convencional, aplicándose, en ambos, los parámetros óptimos de operación. La calidad promedio del producto extraído mediante el método de hidrólisis ácida asistida por microondas, a un mismo pH que para el método convencional, se comparó con la calidad promedio del producto obtenido por este último método.
4. RESULTADOS Y DISCUSIÓN
● Caracterización de la Materia Prima
La humedad determinada para los residuos de naranja, que comprenden el albedo de la cáscara, las semillas y las membranas del fruto (como se muestra en la Figura 4a), fue de 83,35%.

La determinación del porcentaje de pectina se realizó sobre la materia prima pre-tratada (Figura 4b). Empleando 5 g de la misma, se obtuvo 2,09 y 2,50 gramos de pectina, que representan el 41,9 y 41,7 % con un promedio de 41,8 %. En base al último dato y al porcentaje de humedad determinado, el valor del porcentaje de pectina en base húmeda es 7,73%.
● Análisis de las Variables de Proceso para la Operación de Hidrólisis
Los resultados de rendimiento y calidad obtenidos en las pruebas de hidrólisis ácida asistida por microondas se detallan en la Tabla 3.

El rango de variación del rendimiento es amplio (desde 2,5 hasta 21,1 %), lo cual demuestra que por lo menos una de las variables estudiadas tiene un efecto significativo sobre el mismo.
El porcentaje de ácido galacturónico fluctúa entre 53,3 % y 64,8 %, encontrándose debajo del límite establecido para pectinas comerciales, de 65 %. Por lo tanto, es posible que la pectina obtenida contenga impurezas como galactanos, xilanos, hemicelulosas u otras sustancias que son susceptibles a la precipitación alcohólica.
Por otra parte, el porcentaje de metoxilos tiene un rango de variación entre 6,0 y 7,1 %, sin embargo, estos valores no pueden tomarse de referencia para determinar si la pectina es de alto o bajo metoxilo, ya que el porcentaje de ácido galacturónico es bajo y, como se mencionó, es posible la presencia de impurezas. Por esta razón, se determinó el grado de esterificación de la pectina, cuyos valores varían entre 62,7 y 73,3, categorizándose a las muestras, de esta manera, como pectina de alto metoxilo de los tipos mediumrapid set y rapid set.
Para conocer el efecto de los parámetros de operación en las variables de respuesta, las hipótesis nula y alternativa planteadas para el experimento fueron las siguientes:
- Ho: El factor experimental (j) no influye sobre la variable de respuesta (i)
- Hi: El factor experimental (j) influye sobre la variable de respuesta (i)
En base a los resultados obtenidos en el experimento, se determinó el rechazo o aceptación de la hipótesis nula de cada factor experimental sobre cada variable de respuesta, con un nivel de confianza del 95 %, Tabla 4.
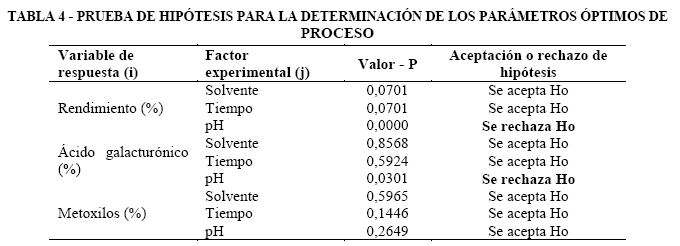
En función al análisis ANOVA, el tiempo y la proporción de solvente no generan un incremento significativo en el rendimiento, dentro de los rangos de variación establecidos, mientras el pH sí lo hace. Ninguno de los parámetros afecta al porcentaje de metoxilos. El porcentaje de ácido galacturónico se ve modificado únicamente por el pH.
Los diagramas de efectos estandarizados, presentes en la Figura 5, esquematizan la variación positiva o negativa de las variables de respuesta, en función a los factores experimentales. La longitud de cada barra equivale al efecto estandarizado (efecto estimado dividido por su valor estándar). La línea vertical indica la separación entre los efectos significativos y no significativos. Mediante el color gris claro (+) se representa una relación positiva entre la variable de entrada y la variable de salida (un mayor valor en la variable de entrada, genera un mayor valor en la variable de salida).Al contrario, el color gris oscuro (-) representa una relación negativa entre estas variables (un menor valor en la variable de entrada, genera un mayor valor en la variable de salida).
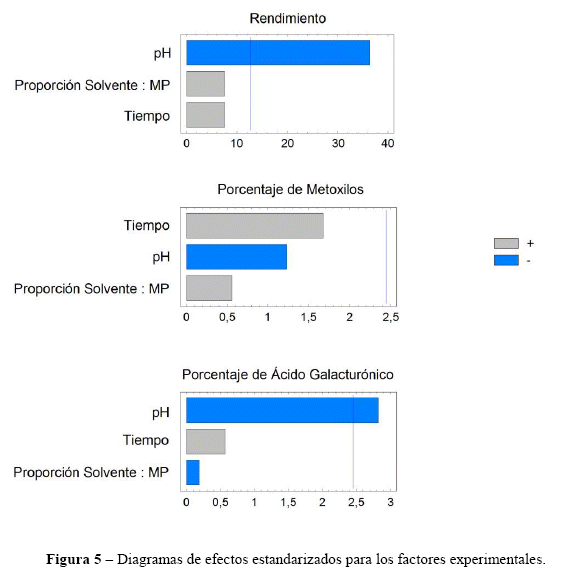
En base a estas consideraciones, se aprecia que tanto la influencia del pH en el rendimiento como en el porcentaje de ácido galacturónico es inversa, es decir:
- A menor pH, mayor rendimiento
- A menor pH, mayor porcentaje de ácido galacturónico
El efecto individual que tienen los factores experimentales sobre las variables de respuesta, se esquematiza en la Figura 6. Se observa una mayor pendiente en la variación del pH sobre el rendimiento y el pH sobre el porcentaje de ácido galacturónico.
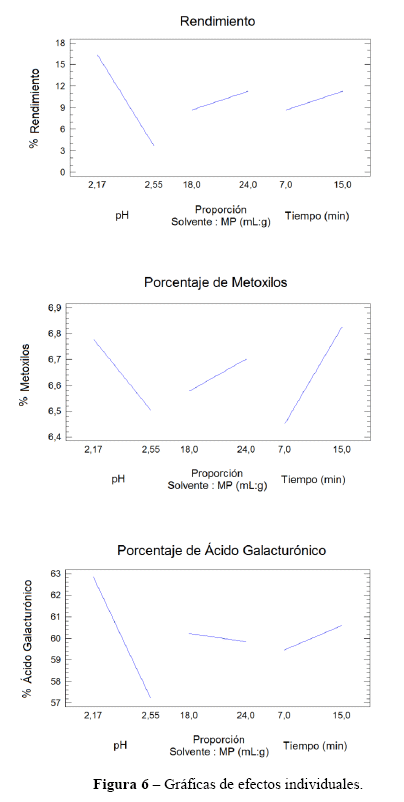
● Análisis del Porcentaje de Etanol para la Operación de Precipitación
Los resultados de las pruebas de precipitación se exponen en la Tabla 5.

Las hipótesis nula y alternativa planteadas para el experimento son las siguientes:
- Ho: Un porcentaje de 50 % en volumen de etanol respecto a la solución a precipitar no genera un menor rendimiento
- Hi: Un porcentaje de 50 % en volumen de etanol respecto a la solución a precipitar genera un menor rendimiento
Se obtuvo un valor de P igual a 0,6668 (mayor a 0,05); por lo tanto, se acepta la hipótesis nula, con un nivel de confianza del 95 %. Es posible aplicar un porcentaje de etanol igual al 50 % respecto a la solución a precipitar, sin afectar el rendimiento del proceso.
● Análisis del Método de Extracción asistido por Microondas
Para el análisis del efecto de la curvatura de los valores de entrada se asignó a la prueba un valor de significancia de 0,05 y se planteó las siguientes hipótesis:
- Ho: Los efectos de los niveles de los factores son lineales
- Hi: Los efectos de los niveles de los factores no son lineales
Se obtuvo un valor P de 0,1991 (mayor a 0,05), por lo tanto, se acepta la hipótesis nula, con un nivel de confianza del 95 %. Los efectos de los niveles de los factores sobre la variable de respuesta son lineales: el diseño es el adecuado para modelar el experimento.
Una vez verificado el modelo, en base a los resultados obtenidos en las pruebas experimentales, se estableció siguiente ecuación para el rendimiento en función al pH, la proporción de solvente PS en mL/g y el tiempo de extracción TE en min, para el método de extracción asistido por microondas.
![]()
Mediante la ecuación de regresión, se obtuvo el gráfico de respuesta modelo para el rendimiento, Figura 7, en función al pH y la proporción de solvente, para un tiempo medio de 11 minutos.
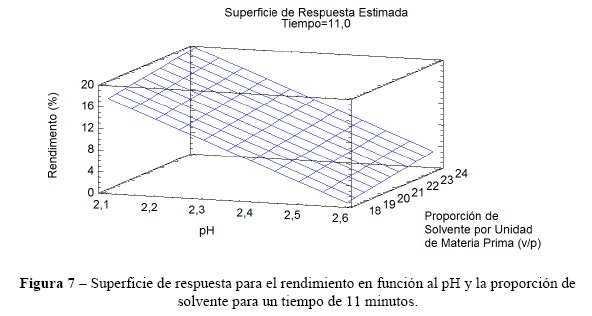
● Comparación del Rendimiento y la Calidad para los Métodos de Extracción HMO y Convencional
La comparación de los rendimientos de ambos métodos bajo los parámetros óptimos de operación se presenta en la Tabla 6. Se muestran, también, las características del producto final obtenido mediante ambos métodos y los estándares normados para estas características.
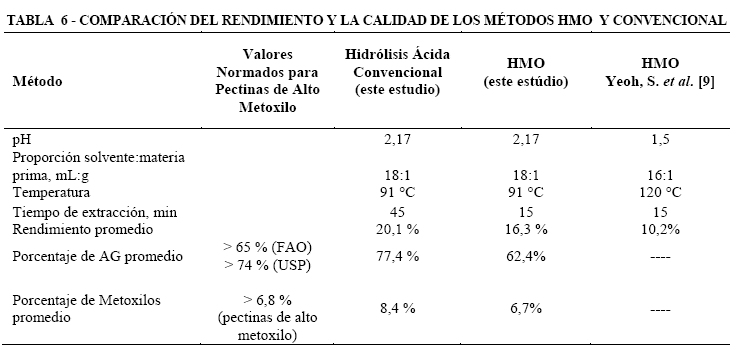
Comparando el estudio realizado por Yeoh, S. et al. [9] con el presente estudio, se observa un rendimiento 6,1% menor. A pesar de que en el trabajo de Yeoh, S. et al. [9] el pH aplicado es menor y la temperatura de extracción mayor, lo cual debería incrementar el rendimiento, la materia prima utilizada no pasa por un proceso de secado y triturado, como el realizado en esta investigación, lo cual, con certeza, perjudica al rendimiento de la extracción. Por otra parte, no se especifica la potencia utilizada en la extracción microondas, que en caso de haber sido menor, podría haber reducido el rendimiento. Un factor adicional que ocasiona esta variación es que en el estudio de Yeoh, S. et al., se cuantificó solamente la pectina, libre de otras impurezas (hemicelulosas, xilanos y otras) que precipitan junto con la pectina en el proceso, mientras que la metodología aplicada en el presente estudio no permitió la diferenciación entre la pectina pura y dichas impurezas. Por esta razón, también puede observarse un porcentaje de ácido galacturónico bajo que se incrementaría al separarlas.
Comparando el método microondas con el convencional, mediante este último método se obtiene un incremento en el rendimiento de aproximadamente 23 %, con un incremento del tiempo de extracción de 200 %. Esto demuestra el ahorro en energía y tiempo permitido al aplicar el método HMO.Sin embargo, las características de calidad de la pectina obtenida por el método microondas, son inferiores a las del método convencional, obteniéndose una mayor pureza aplicando este último método.
● Producto Final
Una muestra de la pectina en polvo obtenida en laboratorio mediante el método de extracción por microondas, empleando los parámetros óptimos de operación, con una humedad de 8,7 %, se expone en la Figura 8.

5. CONCLUSIONES
Se establece los siguientes valores óptimos para la operación de hidrólisis mediante ambos métodos, dentro de los rangos estudiados:
Dentro del rango de pH 2,17 a 2,56, se establece como valor óptimo 2,17, por obtenerse con este valor un mayor rendimiento y un mayor porcentaje de ácido galacturónico.
Para una proporción de solvente:materia prima (mL:g) dentro del rango de 18:1 a 24:1, no se detectó una variación significativa en el rendimiento ni en la calidad de pectina, por lo cual es posible usar la cantidad mínima (18:1) de solvente sin afectar estas variables.
Para la extracción microondas, periodos entre 7 y 15 minutos tampoco tuvieron efectos significativos sobre el rendimiento y la calidad del producto.
En cuanto a la operación de precipitación, se concluye que es viable la reducción del porcentaje de solvente a un 50 % de la solución a precipitar, sin afectar el rendimiento del producto. Valores menores corren el riesgo de no permitir la precipitación, como aconteció para un valor de 40% de solvente.
Como se demostró en el presente estudio y en el estudio realizado por Yeoh, S. et al. [9], el método de extracción por microondas hace posible el ahorro de energía, además de emplear un tiempo de proceso bastante más corto, comparado con el método convencional. Como complemento a ambos estudios, es conveniente realizar el análisis de la potencia de operación del equipo microondas, con el fin de evaluar su efecto sobre el rendimiento, además de comprobar si ésta influye en la ruptura de enlaces de las muestras. Además, se sugiere analizar tiempos de operación menores a los tiempos analizados en ambos estudios, contrastándolos con distintos valores de potencia.
Finalmente, a pesar de generarse un ahorro de energía significativo mediante el método asistido por microondas, se hace necesario el estudio del efecto de éstas, sobre la estructura molecular de la pectina a diferentes potencias, ya que, según el estudio desarrollado por Zhongdong, L. et al. [17], a una potencia elevada (1000 W), durante 5 minutos, se han presentado daños en la estructura de la cáscara de naranja y en sus células.
6. AGRADECIMIENTOS
Agradezco sinceramente al Ing. Luis Arteaga por haber sido mi mentor en el desarrollo de este estudio y al Dr. Ramiro Escalera por haberme guiado y cooperado en el desarrollo del presente artículo.
7. BIBLIOGRAFÍA
[1] P. Sriamornsak. "Chemistry of Pectin and Its Pharmaceutical Uses : A Review." Silpakorn University International Journal,vol. 3, pp. 206-208, 2003.
[2] P. Mamani et al."Pectina: Usos Farmacéuticos y Aplicaciones Terapéuticas." en: Anales de la Real Academia de Farmacia, Madrid, España, vol. 78, no. 1, 2012, pp. 82-97.
[3] F. Voragen et al. Advances in Pectin and Pectinase Research. Ed. Springer, 2003. ISBN 9789401703314.
[4] T. Iglesias y J. Lozano. "Extraction and characterization of sunflower pectin." Journal of Food Engineering, vol. 62, no. 3, pp. 215-223, 2004.
[5] F. Castillo et al."Reaprovechamiento Integral de Residuos Agroindustriales: Cáscara y Pulpa de Cacao para la Producción de Pectinas." Revista Latinoamericana el Ambiente y las Ciencias, vol. 1, pp. 45-66, 2010.
[6] J. Gilabert. "Degradación Enzimática y Características Físicas y Químicas de la Pectina de Bagazo de Melocotón." Tesis Doctoral. Universitat de Lleida, 1998.
[7] J. I. García. "Evaluación del Rendimiento de Extracción de Pectina en Aguas Mieles del Beneficiado de Café Procedentes del Desmusilaginado Mecánico." Tesis de Pregrado, Universidad de El Salvador, 2009.
[8] Y. Zouambia et al."A new approach for pectin extraction: Electromagnetic induction heating." Arabian Journal of Chemistry. [Online] Avaible: http://dx.doi.org/10.1016/j.arabjc. 2014 [Accessed 2014.11.011].
[9] S. Yeoh et al. "A Comparison of Different Techniques for Water-Based Extraction of Pectin from Orange Peels." Chem. Eng. Comm., vol. 195, , pp. 511-520, 2008.
[10] M. L. Fishman et al. Microwave-assisted Extraction of Lime Pectin. Carbohydrate Research, vol. 323, pp. 1170-1177.
[11] International Pectin Producers Association. "What is pectin?."[Online]. Avaible: http://www.ippa.info/what_is_pectin.htm. 2001. [Accedido en julio de 2013].
[12] Voragen, A., et al. Pectin, a versatile polysaccharide present in plant cell walls. Struct Chem,20, 2009, pp. 263–275
[13] Food and Agriculture Organization of the United Nations. Monographs 7: Pectins. [Online]. (URL, http://www.fao.org/ag/agn/jecfa-additives/specs/monograph7/additive-306-m7.pdf), 2009. (Accedido en marzo de 2013)
[14] Herbstreith & Fox. Regulations for Purity Requirements of Pectines. [Online]. (URL, http://www.herbstreith-fox.de/fileadmin/tmpl/pdf/qualitaet/HF_Rechtsvorschriften_Reinheitsanforderungen_en.pdf), 2009. (Accedido en marzo de 2013).
[15] U.S. Pharmacopeia Expert Comite. Monographs 2: Pectin [Online]. (URL, http://www.pharmacopeia.cn/v29240/usp29nf24s0_m61250.html). (Accedido en agosto de 2015). [ Links ]
[16] Joye, D., & Luzio, G.. Process for selective extraction of pectins from plant material by differential pH. Carbohydr. Res., 43 (4), 2000, pp. 337–342.
[17] Zhongdong, L., et al. Image Study of Pectin Extraction from Orange Skin Assisted by Microwave.Carbohydrate Polymers, 64, pp. 548-552.
[18] Nielsen, S. Food Analysis. Second Edition. Aspen Publishers, Inc., Gaithersburg, MD, 1998.














