Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Investigación e Innovación Agropecuaria y de Recursos Naturales
versión impresa ISSN 2409-1618
RIIARn vol.1 no.1 La Paz 2014
ARTÍCULOS
Influencia de la dosis de estiércol ovino y bioinsumo en la
Mineralización del Nitrógeno
Influency of the dosae to sheep manure and bioinsumo in
Nitrogen Mineralization
Roberto Miranda1., Milenka Lascano 2., Aylin Caballero3, Hugo Bosque4
1 Docente investigador de la Facultad de Agronomía
2 Becaria del proyecto AndesCrop.
3 Investigadora del Proyecto.
4 Docente de la Facultad de Agronomía y Coordinador
Nacional del Proyecto Andes Crop.
RESUMEN
Los abonos orgánicos como los estiércoles, se constituyen en una alternativa para realizar un manejo sostenible del suelo, en zonas como el altiplano de Bolivia en general y en la producción de quinua en particular, sin embargo, es necesario contar con información sobre la capacidad de este abono de proporcionar nitrógeno al suelo y por lo tanto a las plantas. El objetivo del presente trabajo, fue determinar la influencia de la dosis de estiércol ovino y de un bioinsumo (Terrabiosa), en la generación de nitrógeno mineral, en el tiempo. El diseño estadístico aplicado fue el de completamente al azar. Se tuvieron dos factores. El factor A, constituido por dosis de estiércol aplicado al suelo en cantidades de 0, 10 y 20 ton ha-1 y el factor B, conformado por la presencia y ausencia de un bioinsumo (Terrabisosa). Cada tratamiento con tres repeticiones, haciendo un total de 18 unidades experimentales. La evaluación del nitrógeno mineral fue realizada a los 1, 15, 22, 51, 64, 80, 99, y 125 días después de la incubación. Los resultados muestran que el bioinsumo en forma aislada no tiene efecto en la mineralización del nitrógeno como amonio, mientras que si influyó en la mineralización del nitrato y del nitrógeno mineral. El nitrógeno mineral producido luego de 125 días, fue el doble bajo la aplicación del bioinsumo asociado con el estiércol ovino.
Palabras Clave. Nitrógeno, Bioinsumo, Terrabiosa, Estiércol de ovino, Mineralización del nitrógeno.
ABSTRACT
Organic fertilizers such as manure constitute an alternative for sustainable land management in areas as the Bolivian Altiplano in general and for quinoa production in particular, however, it is necessary to have information on the ability of this fertilizer to provide nitrogen to the soil and therefore the plants. The aim of this study was to determine the influence of the dose of sheep manure and a bioinsumo (Terrabiosa) in the generation of mineral nitrogen in time. The statistical design applied was completely random. Two factors were taken. The factor A, consisting of doses of manure applied to the soil in amounts of 0, 10 and 20 t ha-1 and the B factor, consisting of the presence and absence of a bioinsumo (Terrabisosa). Each treatment with three repetitions, with a total of 18 experimental units. Mineral nitrogen assessment was performed at 1, 15, 22, 51, 64, 80, 99, and 125 days after incubation. The results show that the bioinsumo in isolation has no effect on the mineralization of the nitrogen as ammonia, whereas if influenced mineralization and mineral nitrate nitrogen. The mineral nitrogen produced after 125 days, was doubled underthe application of bioinsumo associated with sheep manure.
Keywords. Nitrogen, Bioinsumo, Terrabiosa, Sheep manure, Nitrogen mineralization.
INTRODUCCIÓN
El cultivo de la quinua, se desarrolla en el Altiplano Boliviano con la aplicación de abonos orgánicos como es el estiércol de ganado ovino o camélido. Esta práctica es muy común en estas zonas, sin embargo se desconoce la dosis adecuada a aplicar al suelo para satisfacer la demanda de nutrientes por el cultivo. Los abonos orgánicos, en general, se caracterizan por la liberación paulatina de nutrientes, sin embargo ello depende de factores como la humedad, temperatura, textura del suelo, además de la composición química del material orgánico (Leite, 2003). Es sabido que la materia orgánica, promueve la retención de iones, además de mejorar las condiciones físicas del suelo como la estructura y la aireación, reduciendo la compactación y aumentando la actividad microbiana (Primo et al. 2012).
La calidad del estiércol de oveja y llama, utilizado en la producción de quinua, varia conforme la zona, tipo de ganado, alimentación y edad entre otros, variando el contenido de nitrógeno total entre 1,4 a 0,94% (FAUTAPO, 2008). Según Osco (2007), evaluaciones de estiércol de ganado ovino, en el altiplano boliviano, indicaron un contenido de nitrógeno total de 0,55 a 1,95%; 0,01 a 0,31% de fósforo y entre 0,15 a 1,26% de potasio.
Sin embargo, cuando este estiércol está expuesto a las condiciones ambientales, como altas temperaturas, puede perder rápidamente sus cualidades nutritivas, por esa razón, los nutrientes presentes en estos tipos de abonos orgánicos, se tornan asimilables para las plantas solamente después de los procesos de mineralización Yagodin (1986).
En cuanto al nitrógeno, este es después del agua, el nutriente más limitante para la productividad de las plantas de zonas áridas y semiáridas. La poca materia orgánica del suelo no puede ser utilizada por las plantas directamente, y para ello debe descomponerse y mineralizarse, procesos que son llevados a cabo principalmente por microorganismos del suelo, los cuales a su vez, en ambientes áridos, no tienen siempre condiciones ideales par a su actividad en cuanto a temperatura y humedad, por lo que los procesos de mineralización de nitrógeno en zonas áridas se dan por periodos breves de tiempo generalmente posterior es pequeños pulsos de precipitación (Celaya - Castellanos, 2011).
Los suelos del altiplano boliviano, se caracterizan por tener bajos contenidos de nutrientes y materia orgánica. En cuanto al nitrógeno, en suelos del altiplano sur, este se encuentra entre valores de 0,03 a 0,08 % de nitrógeno total (Miranda, 2012; FAUTAPO, 2008), de este contenido, el nitrógeno mineral varía entre 1 a 10%, lo que representa 3 a 1,2 kg. Miranda (2012) en suelos del altiplano central encontró valores inferiores a 3 mg kg de suelo, lo que equivale aproximadamente a 4,5 kg de nitrógeno mineral por hectárea. Está claro que, el nitrógeno es un elemento que limita la fertilidad de los suelos de estos ecosistemas, ya que la productividad de cultivos, como la quinua, está relacionada con la extracción y acumulación de nitrógeno en sus tejidos y sobre todo en el grano (Miranda, et al. 2012; Orsag et al., 2011; Inda, 2010).
A fin de estimular la actividad de los microorganismos, Ortuño et al., (2010), proponen el uso de boinsumos. La Terrabiosa es un bioinsumo, activador y biodegradador de la materia orgánica que tiene la propiedad de mejorar el proceso de compostaje y eliminar olores indeseables. Este producto orgánico basado, en hierbas medicinales y aromáticas contiene más de 30 bacterias ácido lácticas, bacterias fotosintéticas y levaduras benéficas, con un bajo pH de 3,5. Es una mezcla de bacterias, ácidos lácticos, bacterias fotosintéticas y levaduras (PROINPA, 2012). La Terrabiosa es una mezcla de hierbas aromáticas orgánicas, que son fermentadas con una combinación especial de cultivos ácido láctico. Durante la fermentación se forma el ácido láctico, lo que da un bajo pH de 3.5. Este bajo pH previene el desarrollo de bacteria dañina en el producto terminado.
El concepto de nitrógeno potencialmente mineralizable (No) fue propuesto inicialmente por Stanford y Smith (1972) y se refiere a la cantidad del nitrógeno orgánico edáfico que puede ser convertido por la actividad de la biomasa microbiana aerobia heterótrofa a formas inorgánicas solubles (fundamentalmente NH+4 y NO-), lo cual es una alternativa eficaz para cuantificar el aporte de nitrógeno del suelo para los cultivos.
Según Pratt et al., (1973) la tasa de mineralización es la clave para la aplicación de cualquier material orgánico al suelo. Los factores que afectan la mineralización pueden ser ambientales (temperatura, humedad), las características del residuo orgánico (carbono metabólico y estructural) y de manejo del mismo. Entre los factores ambientales destacan el tipo de suelo, aeración, temperatura y potencial de agua del suelo, tipo y diversidad de microorganismos. Las condiciones óptimas para una mineralización adecuada incluye: suelo franco, 30 a 35 °C temperatura del suelo, -33 a -10 KPa de potencial de agua del suelo (80% del espacio poroso está con agua), 15 a 20% de aeración (oxígeno), pH de 6 a 8 y diversidad de microorganismos del suelo (Stanford y Epstein, 1973).
Con relación a la descomposición y/o biodegradación del estiércol, algunas de las estructuras de la biodegradación del estiércol son la celulosa, la hemicelulosa, almidón, lignina, entre otras, las cuales por la actividad de la acción enzimática de los microorganismos, son biodegradadas de grandes polímeros a simples monómeros, liberándose también iones. Ambos subproductos llegan a ser aprovechados por las plantas, así como por los mismos microorganismos (Flores et al., 2008). En cuanto al manejo, se debe tomar en cuenta la época y forma de aplicación del estiércol al suelo, sistema de labranza entre otros factores que determinan la mineralización del nitrógeno. La tasa de mineralización de nitrógeno, en condiciones controladas, para un suelo areno francoso fue de 0,62 a 0,64 mg/kg-día. (Miranda, 2012).
MATERIALES Y MÉTODOS
El trabajo fue realizado en el laboratorio de suelos de la facultad de agronomía de la Universidad Mayor de San Andrés. El suelo fue obtenido de una parcela con siete años de descanso con quinua de la comunidad de Villa Patarani, del Altiplano Central de Bolivia, la misma se ubica entre las coordenadas 16°42'12" latitud Sud y 67°52'11'' longitud Oeste. El suelo recolectado presentó 64% de arena, 17% de arcilla y 19% limo, siendo catalogados como de textura franco arenoso. La muestra de suelo fue recolectada en una bolsa oscura a 10 cm de profundidad en fecha 23 de noviembre del año 2011, con ayuda de una pala de corte, a diferentes puntos a fin de conseguir una muestra compuesta. Posteriormente fue trasladada al laboratorio de suelos de la Facultad de Agronomía en la ciudad de La Paz y almacenada. El estiércol de oveja, también fue recolectado de la misma comunidad de un corral en la misma fecha. Ambos insumos fueron tamizados en una malla de 4,5mm de diámetro y mezclados de acuerdo a los tratamientos correspondientes. Este estiércol presenta 2,09% de nitrógeno, 0,36% de fósforo y 0,66 de potasio. El contenido de materia orgánica fue de 32,96% y pH de 7,43.
El bioinsumo "terrabiosa" fue provisto por la institución PROINPA, este producto es una mezcla de hierbas aromáticas orgánicas, que son fermentadas con una combinación especial de cultivos ácido láctico. Durante la fermentación se forma el ácido láctico, lo que da un bajo pH de 3.5. Este bajo pH previene el desarrollo de bacteria dañina en el producto terminado.
El diseño experimental utilizado fue de completamente al azar con tres repeticiones y un arreglo bifactorial. El factor A fue Con Bioinsumo (CB) y Sin Bioinsumo (SB) y el factor B por la dosis de estiércol (0, 10, 20 ton ha-1), haciendo un total de 18 unidades experimentales. Los tratamientos fueron: SB+0 ton est; SB+10 ton est; SB+20 ton est; CB+0 ton est; CB+10 ton est; + CB+20 ton est., cada tratamiento con tres repeticiones haciendo un total de 18 unidades experimentales. Las unidades experimentales fueron constituidas por frascos de acrílico de 110 ml de capacidad. Para la evaluación del nitrógeno mineral fueron colocados tres frascos de acrílico al interior de un frasco de vidrio de capacidad de 1500 ml, la cual contenía una tapa de rosca plástica. Todas las unidades experimentales fueron mantenidas en incubadora, en ausencia de luminosidad y a una temperatura de que varió entre 13 a 15 grados centígrados. La humedad fue mantenida a valores cercanos a la capacidad de campo (18%) y la aireación fue controlada abriendo los frascos cada 2 a 3 días por 15 minutos, aproximadamente, para favorecer la oxigenación. La evaluación del nitrógeno mineral fue realizada a los 0, 5, 10, 14 20, 30, 50, 80, 110 y 140 días después de la incubación, en cada fecha de muestreo fueron analizados el nitrógeno mineral como amonio (y nitratos (según la metodología propuesta porTedesco (1995), en la que, una muestra de 12,5 gramos de suelos fue agitado con 50 ml de una solución de KCl 1M posteriormente agitada durante 30 minutos a 180 rpm en un agitador mecánico anual. Para la determinación de amonio, se utilizó 0,2 gramos de óxido de magnesio, el cual fue destilado durante dos minutos, recolectándose un volumen de 35 a 40 ml, recogido en un matraz con 5 ml de acido bórico como indicador. Para la determinación del nitrógeno en forma de nitratos, la muestra agitada con cloruro de potasio, fue tratada con 0,2 gramos de aleación de varda, destilado por dos minutos y recolectada en un matraz con 5 ml de acido bórico como indicador. El nitrógeno mineral fue determinado con la siguiente expresión:

Para estimar el nitrógeno potencialmente mineralizable, a partir de los valores de nitrógeno mineral acumulado, se utilizó un modelo potencial de ajuste a través de regresión no lineal propuesto por Broadment (1986), N=Atb, que es un modelo parabólico.
RESULTADOS Y DISCUSIÓN
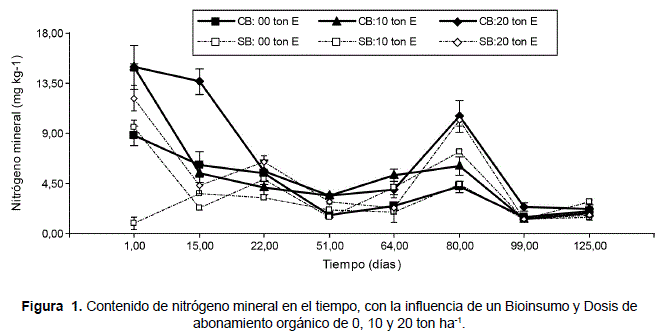
De acuerdo a la figura 1, el nitrógeno mineral, disminuye en el tiempo, con oscilaciones en algunas fechas, según Da Cas (2009), estas oscilaciones pueden estar influenciadas por las intensidades de los procesos de nitrificación e inmovilización en el suelo, debido a la presencia de los microorganismos. El tratamiento que no recibió ningún contenido de estiércol y bioinsumo presentó los valores más bajos, aunque el comportamiento fue similar en el tiempo. Otro factor que pudo haber influenciado en estas oscilaciones, son las alternancias de humedad en el suelo, que podrían haber afectado la actividad de los microorganismos, pese a que se controló la humedad, manteniéndola a valores cercanos a capacidad de campo, con la adición de agua, en función al peso de la muestra. Al cabo de los 125 días de la incubación, el nitrógeno mineral, llego a estabilizarse en valores de 1,8 a 2 mg kg-1 de suelo, para todos los tratamientos. En condiciones de campo, las oscilaciones serán mucho más evidentes, debido a las fluctuaciones de temperatura y humedad, lo que limitará el proceso de mineralización a los eventos donde se produzcan precipitaciones pluviales (Celaya y Castellanos, 2011).
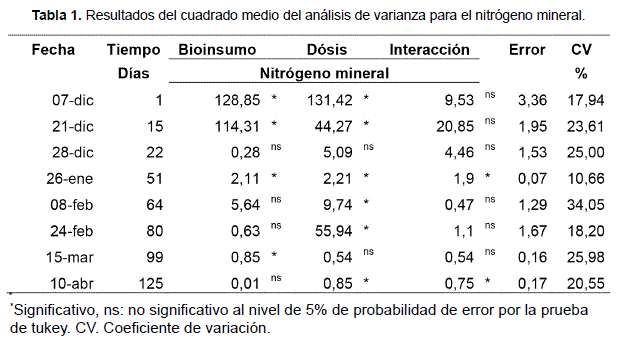
De acuerdo al cuadrado medio del análisis de varianza (Tabla 1), el nitrógeno mineral (amonio y nitratos) en ciertas fechas es significativo para el Bioinsumo y dosis, es decir que estos factores influyeron en el contenido de nitrógeno mineral, sin embargo no se pudo apreciar una interacción entre estos dos factores para el comportamiento del nitrógeno mineral. Para otras fechas, no hubo diferencias para el nitrógeno mineral debido a la presencia del bioinsumo o la dosis. Estos resultados, muestran que el nitrógeno mineral es un parámetro sensible a la dosis de estiércol aplicado al suelo, la misma pudiera estar asociada a las variaciones de temperatura, humedad y presencia de microorganismos. Asimismo, Galvis y Hernandes (2004), mencionan que la tasa de mineralización no es constante y cambia bajo las mismas condiciones de humedad y temperatura, de acuerdo a las características del suelo, ambiente y sistema de producción.
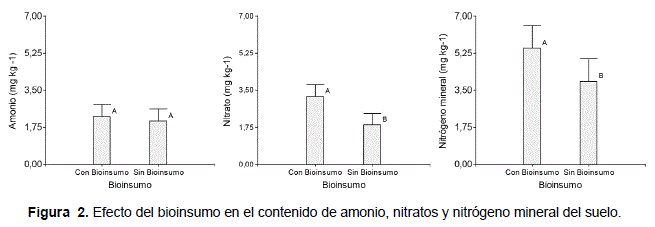
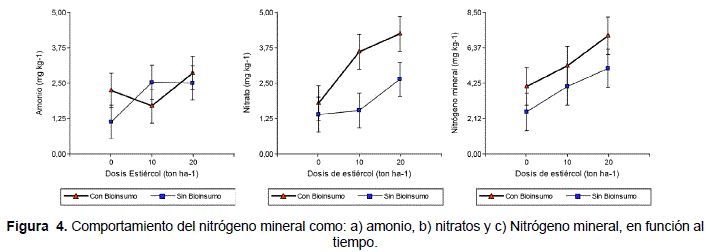
Según la figura 2, el efecto del bioinsumo no ocasiono diferencias significativas al 5% en la generación de amonio (Figura 2a). En cambio, el bioinsumo incidió a la mineralización del nitrato y también del nitrógeno mineral en su totalidad. Este hecho pudo deberse a la acidez del bioinsumo, la cual según las especificaciones técnicas de PROINPA, el pH de este insumo es de aproximadamente 3,5 y el amonio es mas disponible a pH básicos.
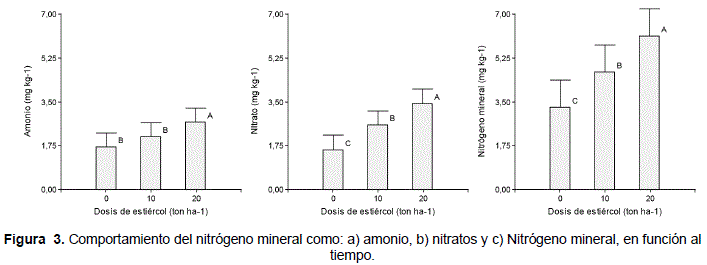
En relación a la dosis de aplicación, hubo mayor generación de amonio, nitratos y por lo tanto de nitrógeno mineral, a medida que la dosis de estiércol fue incrementado (Figura 3).
Según la Figura 4, hubo interacción entre la dosis de estiércol utilizado y el bioinsumo Terrabiosa. Cuando no hay estiércol en el suelo, el bioinsumo aplicado al suelo, genera más amonio y nitrato. A medida que se aplica estiércol al suelo, el bioinsumo parece tener más efecto en la mineralización del nitrógeno mineral.
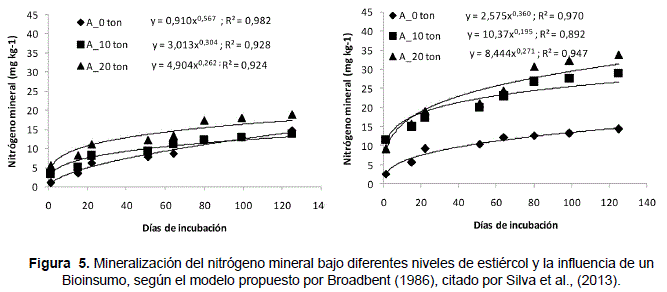
En relación a la tasa de mineralización, el modelo aplicado fue el propuesto por Broadbent (1986), el cual es una función potencial. De acuerdo a este modelo, la mineralización del nitrógeno fue influenciada por la adición de la Terrabiosa y las dosis de estiércol, llegando a producirse 28 y 33 mg de nitrógeno mineral por kg de suelo en presencia de la Terrabiosa y a 10 y 20 ton ha-1de estiércol respectivamente, frente a 13 y 19 mg kg-1 sin influencia del Bioinsumo y bajo los mismos niveles de estiércol (Figura 5). Pese a estos resultados, los valores de nitrógeno mineral son menores en relación a los reportados en otros trabajos (Flores, 2008; De Oliveira et al., 2002).
Estos datos de mineralización corresponden a condiciones de laboratorio, donde la humedad del suelo se mantuvo en un 80% de la capacidad de campo y la temperatura entre 13 y 15 grados centígrados. En condiciones de campo, la tasa de mineralización no es constante, ya que las condiciones ambientales como la temperatura y humedad del suelo, varían en función de la época seca o húmeda (Miranda, 2012; Caballero, 2011). La aplicación de niveles de estiércol entre 10 y 20 ton ha-1, produjeron una mayor mineralización en un inicio, para luego estabilizarse. Asimismo, entre los tratamientos con el uso de la Terrabiosa y sin Terrabiosa, se determinó que el bioinsumo, influye en la mayor tasa de mineralización del nitrógeno.
CONCLUSIONES.
La aplicación de Terrabiosa (Bioinsumo), influyó más en la generación de nitrato que de amonio en forma independiente. Por otro lado, el nitrógeno mineral producido luego de los 125 días de incubación aumentó con el incremento de la dosis de estiércol.
AGRADECIMENTOS
Al proyecto AndesCrop y la Facultad de Agronomía de la Universidad Mayor de San Andrés, por el apoyo económico y logístico.
BIBLIOGRAFÍA
Broadbent, F. E. 1986. Empirical modeling of soil nitrogen mineralization. Soil Science, v.141, 208-213. [ Links ]
Celaya, H., Castellanos, A. 2011. Mineralización de nitrógeno en el suelo de zonas áridas y semiáridas. Terra Latinoamericana. V. 29, n. 3, 343-356. [ Links ]
Da Cas, V. L. S. 2009. Mineralização do carbono e do nitrogênio no solo com o uso de lodo de esgoto e palha de aveia. Tesis de Maestría. Universidad Federal de Santa Maria. Estado Sur Del Brasil. 69 p. [ Links ]
De Oliveira, F. A., Gianello, C., Tedesco, J., Riboldi, J,. Meurer, E. J., Bissani, C. A. 2002. Empirical models to predict soil nitrogen mineralization. Ciencia Rural. v. 32, n. 3, 393-399. [ Links ]
FAUTAPO. 2008. Programa Quinua Altiplano Sur. Informe: Fertilidad, uso y manejo de suelos en la zona del Intersalar, Departamentos de: Oruro y Potosí. Oruro - Bolivia. 105 p. [ Links ]
Flores, J. P., Corral, B., Quezada, A., Sotomayor, V., Rivera, L. M. 2008. Mineralización de Nitrógeno en Suelos Tratados con Estiércol Bovino y Cultivado con Algodonero. Informe de Proyecto de Investigación. Universidad Autónoma de ciudad de Juárez. Instituto de ciencias biomédicas. Chihuahua - México. p55. [ Links ]
Galvis, A.,Hernández, M. 2004. Cálculo del nitrógeno potencialmente mineralizable. Interciencia. v. 29, n. 7, 383-377. [ Links ]
Inda, R. 2010. Evaluación del comportamiento del nitrógeno, en parcelas con cultivo de quinua bajo diferente manejo de suelos (Municipio salinas de Garci Mendoza), Oruro. Tesis de Licenciatura. La Paz, Bolivia. Universidad Mayor de San Andrés. 138 p. [ Links ]
Leite, L. F. C. et al. 2003. Estoques totais de carbono orgânico e seus compartimentos em Argissolo sob floresta e sob milho cultivado com adubação mineral e orgânica. Revista Brasileira de Ciência do Solo, n. 27, 821-832. [ Links ]
Miranda, R. 2012. Adubação orgânica em condições de Irrigação suplementar e seu efeito na Produtividade da quinua (Chenopodium quinoa Willd) no planalto da Bolívia. Tesis de Doctorado en la Ciencia del Suelo. Universidad Federal de Santa Maria. Santa Maria, Brasil. 98p. [ Links ]
Miranda, R., Carlesso, R., Huanca, M., Mamani., P., Borda, A. 2012. Rendimiento y acumulación de nitrógeno en la quinua (Chenopodium quinoa Willd) producida con estiércol y riego suplementario. Venesuelos. 20: 21-29. [ Links ]
Orsag, V., Castro, E., Leon, M. L., Pacosaca, O., Mamani, F. 2012. Evaluación de la fertilidad de los suelos en la zona intersalar. Producción sostenible de quinua. DANIDA, PIEB. La Paz Bolivia. 174p. [ Links ]
Ortuño, N., Claros, M., Angulo, V., Navia, O., Meneses, E. 2010. Biofertilizantes artesanales con microorganismos rizosfericos nativos para una producción orgánica de quinua en Bolivia. In: III CONGRESO MUNDIAL DEL LA QUINUA. Oruro Bolivia. 42p [ Links ]
Pratt, P.F., F.E. Broadbent y J.P. Martin. 1973. Using organic wastes as nitrogen fertilizers. Calif. Agric. v. 27, n. 1, p. 10-13. [ Links ]
Primo, M. T. et al. 2012. Contribuição da adubação orgânica na absorção de nutrientes ena produtividade de milho no semiárido paraibano. Agrária. Pernambuco. v. 7, n. 1, 81-88. [ Links ]
PROINPA, 2012. Desarrollo de bioinsumos: Un aporte a la soberanía alimentaria de Bolivia. Disponible en:
//www.proinpa.org/index.php?option=com_phocadownload