Introducción
En la práctica veterinaria de pequeñas especies, las razones principales de consulta son las dermatopatías bacterianas1,2. Siendo en su mayoría ocasionadas por Staphylococcus pseudintermedius, que forma parte de la microbiota cutánea de los perros1, junto a S. aureus3,4.
Los antibióticos locales y sistémicos de amplio espectro son frecuentemente utilizados para combatirlas5,6, pueden ser suministrados por diferentes vías, la tópica, la más empleada mediante diversas presentaciones como champús, cremas y geles7,8. No obstante, su utilización inadecuada ha generado resistencia bacteriana en animales de compañía9-12. Esto, resulta ser un problema para animales y humanos puesto que los estafilococos, que forman parte de la microbiota humana y animal, pueden actuar como reservorio de genes de resistencia13.
Al mismo tiempo, muchas de estas afecciones en la piel pueden ser consideradas secundarias y frecuentemente relacionadas con patologías intestinales14.
Por tal razón, en dermatología se ha postulado como alternativa, el uso de probióticos orales15-17, aceites esenciales18-20 e hipoclorito de sodio21. Sin embargo, los bacteriófagos, que son los depredadores naturales de las bacterias, se perfilan como una excelente opción, por sus propiedades líticas, incluso en bacterias resistentes a antimicrobianos. Asimismo, se destaca como ventaja potencial su capacidad de multiplicación en el sitio de infección22, su alta especificidad, por lo que no afecta la a las bacterias benéficas23. A pesar de estas ventajas, se conoce que dichos virus pueden transmitir genes de virulencia y resistencia antimicrobiana mediante la transducción24,25. De ahí, debe caracterizarse genéticamente a los fagos que se usarán como terapia.
Por su parte, los fagos autóctonos son una tendencia emergente, que se utilizan cuando los productos comerciales no tienen el efecto deseado26. Este tipo de bacteriófagos son aquellos aislados de ambientes en los que se encuentra la bacteria objetivo, con el propósito de asegurar que la bacteria objetivo forme parte del espectro del fago a emplear.
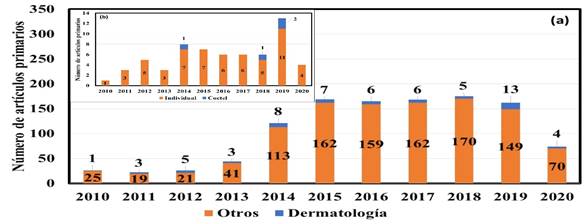
Figura 1a Publicaciones de artículos científicos primarios de bacteriófagos en dermatología veterinaria. b Publicaciones de artículos científicos de bacteriófagos en dermatología que utilizaron cócteles de fagos. Información obtenida de la base de datos de Scopus (Criterio de búsqueda: Título de artículo, resumen y palabras clave: “veterinary” and “bacteriophage” and “dermatology” en el periodo 2010-2021)
En el último decenio, se han divulgado gran cantidad de artículos científicos primarios sobre la utilización de bacteriófagos para el control bacteriano en medicina veterinaria, no obstante, existen pocos trabajos en dermatología (Figura 1a). Del mismo modo, se cuentan con escasos trabajos sobre cócteles de fagos (Figura 1b).
El presente trabajo se enfoca en el uso de cócteles de bacteriófagos líticos no transductores como sustitutos de antimicrobianos para combatir enfermedades de piel de origen bacteriano, las vías de aplicación en dermatología, su comparación con los antimicrobianos y el uso de fagos autóctonos.
Materiales y métodos
Se realizaron búsquedas en la base de datos Scopus de enero de 2010 a diciembre 2021 cuyo criterio de selección fue, que en el título de artículo, resumen y palabras clave contengan los términos: “veterinary”, “bacteriophage”, “dermatology” y “cocktail”. La información obtenida se clasificó según especie animal y la vía de aplicación estudiada. Para el desarrollo del presente artículo se excluyeron los trabajos que utilizaron los fagos para detección de bacterias patógenas, reducción de carga bacteriana en carcasa, desinfección de instalaciones, del mismo modo, se excluyeron las investigaciones básicas (caracterización genotípica y fenotípica).
Desarrollo
Bacteriófagos. También denominados fagos, son virus que infectan y lisan bacterias27. Los fagos fueron reportados28 y aislados por primera vez29 al inicio del siglo XX, dando inicio de la fagoterapia (FT) cuatro años después de su descubrimiento, no obstante, la aparición de los antibióticos desplazó a los fagos por ser más baratos y poseían mayor espectro30. Actualmente, la resistencia antimicrobiana y los nuevos descubrimientos en FT, se están volviendo a emplear para combatir enfermedades bacterianas, el primer reporte de FT en animales de compañía en el año 200631. Estos virus son abundantes en la naturaleza32, se caracterizan por ser muy específicos. Aunque su especificidad puede darse a nivel de cepa33-35, se han reportado fagos que infectan a más de un género bacteriano36.
Por su ciclo infectivo, pueden ser clasificados como virulentos o líticos (FaL) y templados (FaT). Los virulentos impiden la multiplicación bacteriana, sin embargo, los FaT le permiten, cuando las bacterias se encuentran en baja densidad37,38. Asimismo, los FaT están involucrados en la transmisión de genes de virulencia y resistencia antimicrobiana27,39,40.
La infección lítica comienza con el reconocimiento de fago receptores en la superficie bacteriana, tales como: antígenos41, pili42, glucano43, polisacáridos44, proteínas45 y otras estructuras, dando lugar a la adsorción viral, posteriormente, el fago implanta su material genético (ARN o ADN) en la bacteria, destruye el material genético de la bacteria hospedadora mediante acción enzimática, se ensambla y se replica. Finalmente, los nuevos fagos producen holinas y endolisinas, las holinas son proteínas transportadoras que permiten a las endolisinas (enzimas) atravesar la membrana hasta su sitio de acción, degradando el peptidoglucano30 y así formar poros, causando despolarización que produce lisis bacteriana, con ello la liberación de nuevos fagos46. No obstante, el ciclo lítico puede presentar fallas al destruir el material genético bacteriano y ensamblar fagos con fragmentos de este, fenómeno llamado transducción.
La transducción puede ser generalizada o especializada, la primera, por errores en el ensamblaje de los nuevos fagos, se producen virus con material genético bacteriano y viral exclusivamente24,25, la segunda, se mezcla el genoma bacteriano y viral, dando como resultado fagos con ambos genomas24, en ambos, si la bacteria posee genes de resistencia y virulencia, estos serán transmitidos en el siguiente ciclo25, por lo tanto, se deben utilizar FaL no transductores.
Fago resistencia. Los fagos y bacterias han co-evolucionado, las bacterias desarrollaron estrategias para eludir y superar a los fagos. Se han reportado casos de fago-resistencia bacteriana en medicina veterinaria33,47-49, estudiando sus diferentes mecanismos como: pérdida de fago-receptores, modificación de fago-receptores, sistema CRISPR-Cas, sistema abortivo y producción de matriz de polisacáridos50.
Algunas estrategias bacterianas se enfocan en evitar la adsorción del fago mediante la modificación de fago receptores, su pérdida, y la producción de polisacáridos. Pero, los fagos pueden cambiar sus fibras de cola para encontrar receptores recién alterados51 y producir despolimerasas52. Asimismo, las bacterias pueden atacar el material genético del fago usando el sistema CRISPR-Cas, sin embargo, algunos fagos evitan la degradación de su material genético utilizando una cubierta proteica53. Finalmente, cuando las estrategias anteriores no son suficientes para evitar la infección viral, las bacterias recurren al sistema abortivo54.
Por otro lado, en casos de resistencia a fagos individuales podemos utilizar cócteles de fagos49,55 y quorum quenching56-58. No obstante, también se ha reportado fago-resistencia a cócteles de fagos33,47,48, para estos casos se puede utilizar quorum quenching o cambiar la composición del cóctel de fagos.
Si bien es cierto que la resistencia a fagos es un problema para la FT, se reportó que las bacterias resistentes a fagos reducen su capacidad de crecimiento y la absorción de nutrientes33. Además, se reportó que bacterias resistentes a fagos exhibieron sensibilidad a antibióticos a los que eran resistentes y menor virulencia59,60.
Bacteriófagos versus antibióticos. A pesar que, los antibióticos tópicos suelen ser utilizados en lesiones focalizadas y superficiales61, estos pueden generar un desbalance en la microbiota cutánea por su amplio espectro62. En contraste, la especificidad de los bacteriófagos permite que otras bacterias fuera de su rango no se vean afectadas, lo que garantiza que la microbiota benéfica prolifere sin problemas23,63.
Por otro lado, los fármacos tópicos pueden diluirse o inactivarse mediante enzimas u otros mediadores inflamatorios64. A diferencia de los fagos que, por su continua multiplicación, penetran los tejidos en presencia de bacterias activas, lo que es particularmente útil en el tratamiento de infecciones en tejidos con menor aporte sanguíneo65.
Es preciso señalar, que la resistencia antimicrobiana (AMR) es el factor principal que ha impulsado la búsqueda de otras alternativas terapéuticas. Está claro que los antibióticos sistémicos suelen generar mayor resistencia que los tópicos66,67, que se recetan con mayor frecuencia en las dermatopatías caninas68,69.
No obstante, esto ha normalizado los tratamientos empíricos70,71, realizados sin las pruebas microbiológicas de sensibilidad pertinentes, que pueden derivar a su vez en el incremento de la AMR.
Esta resistencia a su vez se ha visto incrementada parcialmente por malas prácticas en la clínica veterinaria diaria, destacándose su uso de manera preventiva en casos como vacunaciones, esterilizaciones, entre otros72. Por el contrario, se ha informado el empleo de bacteriófagos de manera preventiva produce mejores resultados que un tratamiento, en ratones infectados con E. coli CVCC193, aquellos que fueron inoculados con fagos 24 h previas, mostraron una tasa de supervivencia del 80-100 %, en comparación con aquellos a los que se les administró 3 h después (40-50%)73.
En general, las infecciones crónicas son difíciles de tratar con éxito en AMR, lo que incrementaría la duración del tratamiento y pone en riesgo la vida del paciente74. En este caso, el uso de antimicrobianos enterales, para llegar a zonas de la piel, se deben utilizar concentraciones más elevadas de estos fármacos por la pobre irrigación que poseen estos tejidos, contribuyendo en la presentación de efectos secundarios en mascotas sometidas a estos medicamentos. Son variados los efectos adversos que presentan los animales en tratamiento, y pueden afectar su calidad de vida. Los problemas gastrointestinales, y en casos más raros, anemias hemolíticas, y daño renal agudo75.
Debido a que el uso de virus (fagos) en mascotas pueda ser éticamente controversial, podría verse comprometido el bienestar animal76,77, existen pocos estudios que han utilizado fagos como tratamiento único en infección bacteriana en animales de compañía, dado que no es una práctica muy conocida en el campo de Medicina Veterinaria de pequeñas especies. Sin embargo, un estudio señalo una percepción positiva de esta terapia alternativa, tanto de médicos veterinarios, como propietarios, siendo un indicativo en su futura masificación12.
A pesar de ello, se han realizado terapias a base a bacteriófagos en caninos con otitis externa crónica, que recibieron tratamiento antimicrobiano previo, con una resolución positiva tras el tratamiento31,78, de ahí, su uso para tratar afecciones persistentes, puede considerarse como una alternativa viable sin efectos secundarios graves.
Al mismo tiempo, en lo económico, los costos médicos se incrementan en pacientes con infecciones bacterianas resistentes, mientras que la FT se cree que es menor que la antibioterapia, si se cuenta con un centro especializado79.
En cuanto a la administración, los bacteriófagos, sobre los antibióticos, estos se multiplican de manera logarítmica, de ahí que necesitarían menor número de aplicaciones80, reduciendo, de esta forma el periodo de tratamiento.
Al igual que los antibióticos, la FT también puede verse afectada por la resistencia bacteriana81,82, sin embargo, la resistencia a los fagos puede anticiparse, usando parte de una estrategia terapéutica que aproveche esta compensación evolutiva83. Entre las estrategias, la disminución de la virulencia de cepas fago-resistentes60,84,85, y atenuación variada de acuerdo, si se realiza la terapia con fagos únicos, o cócteles, la segunda opción presento mejores resultados86.
Desde una perspectiva práctica, para que los fagos se utilicen ampliamente en el tratamiento de infecciones bacterianas, tendrían que ser eficaces en combinación con antibióticos87. Se ha señalado que los fagos pueden reducir la concentración mínima inhibitoria (CMI) de cepas bacterianas drogo-resistentes, aunque esto dependerá de la clase de antibiótico y la concentración de bacteriófagos-antibióticos que se utilicen en conjunto88. De modo que los fagos podrían influir positivamente en la sensibilización de bacterias resistentes a antimicrobianos89.
No obstante, algunos autores han justificado los FaL puedan ser capaces de transmitir horizontalmente genes de AMR a otras bacterias a través de la transducción generalizada90, lo que se consideraría contraproducente el empleo de FaL transductores de forma terapéutica. En oposición a estos hallazgos, se señaló que los genes de resistencia a los antimicrobianos rara vez se codifican en los fagos, ya que dicho proceso raramente ocurre en el ciclo lítico del fago91. En la actualidad, el papel de los fagos en la transducción de genes AMR sigue generando debate, y es necesario realizar más estudios al respecto.
En cuanto a la comparación de fagos y antibióticos in vivo, un estudio señaló que los fagos (1x109 UFP/animal) tuvieron efecto similar a vancomicina (15 mg/kg) y mejor efecto que clindamicina (20 mg/kg) en la reducción de lesiones cutáneas en ratones de laboratorio con S. aureus ATCC 25923 (6x109 UFC)92.
Otro estudio de naturaleza similar señaló, en grupos de ratones inoculados con P. aeruginosa y tratados con fago ZCPA1 (1x109 UFP/mL) en dosis únicas (reducción de 4 log10 del conteo bacteriano total) y múltiples (>4 log10), evidenciaron una resolución al 100 % de las heridas y una regeneración óptima de la piel, mientras que el grupo tratado con gentamicina tópica (2 log10) presentó expansión y agrandamiento del área afectada, que derivó en heridas purulentas que no cicatrizaron93. En definitiva, el uso de fagos, ya sea solos o con antibióticos, revelarán resultados superiores que la antibioticoterapia tradicional.
Cócteles de bacteriófagos en veterinaria. Como se mencionó anteriormente los fagos son muy específicos, lo que limita el espectro de los fagos individuales. Por tal motivo, se combinan fagos individuales para ampliar dicho espectro, a esta mezcla se conoce cóctel de fagos, puede ser simple o mixta26, es decir, puede infectar bacterias de un mismo género o de varios géneros bacterianos. Los cócteles de fagos fueron ampliamente estudiados en animales de producción para combatir bacterias patógenas en distintas especies animales, con excelentes resultados (Tabla 1), se ensayaron diferentes vías de administración, la oral e inmersión como alternativas en dermatología veterinaria. La primera puede utilizarse para mantener la salud intestinal e indirectamente proteger la piel, los títulos de fagos pueden reducir por cambios de pH del tracto gastrointestinal si no tienen protección94-96, mientras, la segunda, se puede utilizar para tratar directamente lesiones dérmicas.
Por otro lado, los cócteles en veterinaria se utilizaron en medio líquido (agua) o sólido (alimento), teniendo mejores resultados en medios líquidos (Tabla 1, 2 y 3).
Bacteriófagos en dermatología de animales de compañía. Existen pocos estudios sobre la utilización de fagos en dermatología, ya sea dentro en la medicina veterinaria, o humana, sin embargo, sugieren que podrían ser útiles para tratar el pioderma4,97-100. Esta podría estar causada por una gran variedad de microrganismos, tales como S. aureus, susceptible al fago ΦSA012, al ser aplicado de manera intravenosa o intraperitoneal en un ratón que padecía de mastitis causada por dicha bacteria97.
Además, otro reporte realizado in vivo en ratones, señaló la eficacia del bacteriófago ΦDMSA-2 frente a S. aureus resistente a meticilina (MRSA), fue aplicado por vía tópica sobre una herida generada por escisión quirúrgica infectada, se logró la erradicación de la infección y reepitelización completa de la lesión en un período de 12 a 16 días según la dosis diaria utilizada100, señalando el uso de fagos es eficaz para las infecciones causadas por S. aureus.
Por otro lado, el fago VB_SauS_SH-St 15644 provoco la lisis del 32 % de cepas MRSA in vitro, y logró disminuir el progreso de la infección in vivo al ser aplicado de manera subcutánea en ratones98. El bajo porcentaje de actividad lítica podría deberse a la especificidad del fago, de ahí, el uso de cócteles podría ser útil para evitar este problema. De igual manera, la aplicación del fago SaGU1 en forma tópica a ratones fue eficaz para impedir la agravación de la infección por S. aureus consiguiéndose disminuir la presencia de bacterias99.
Además, los fagos resultaron útiles en disminuir los mecanismos de defensa de las bacterias, tal como fue el fago phiIPLA-RODI, junto con la proteína lítica CHAPSH3b logró reducir la formación del biofilm de S. aureus, también se observó una reducción en bacterias viables luego de su aplicación101.
Tabla 1 Efecto del uso de cócteles de fagos en veterinaria
| Bacteria hospedadora | Fago | Familia de fago | Dosis fago | Procedencia del fago | Vía de administración | Animal | Resultado | Referencias |
|---|---|---|---|---|---|---|---|---|
| C. pertringens | CPAS-7, CPAS-12, CPAS-15, CPAS-16, CPTA-37, CPLV-42 | Siphoviridae | 2.5x109 UFP/Animal | Granjas avícolas | Buffer SM | Pollos | Reducción de mortalidad de 66.67 a 18.00 % | 104 |
| Agua | Reducción de mortalidad de 66.67 a 3.33 % | |||||||
| Alimento | Reducción de mortalidad de 66.67 a 5.33 % | |||||||
| Salmonella gallinarum | ST4, L13, SG3 | Siphoviridae | 1.0x108 UFP/ kg | Aguas residuales | Alimento | Pollos | Reducción de mortalidad de 40.00 a 25.00 %. | 105 |
| Salmonella typhimurium ATCC 14028 | SEP-1, SGP-1, STP-1, SS3eP-1, SalTP-2, SChP-1, SAP-1, SAP-2 | - | 5.0x109 UFP/ Animal | Aguas residuales y heces | Alimento | Lechones | Reducción de Salmonella en heces | 106 |
| E. coli APEC | TM1, TM2, TM3, TM4 | Siphoviridae | 1x1010 UFP/animal | Aguas residuales | I.V. | Codornices japonesas | Reducción de mortalidad de 46.60 a 13.30 % | 107 |
| Aeromonas hydrophila | 50AhydR13PP, 60AhydR15PP. | Myoviridae | 1x105 UFP/mL | - | Inmersión | Anguila europea | Reducción de mortalidad de 60.00 a 20.00 % | 108 |
| 25AhydR2PP | Podoviridae | |||||||
| Pseudomonas fluorescens | 22PfluR64PP, 67PfluR64PP, 71PfluR64PP, 98PfluR60PP. | Podoviridae |
I.P.: intraperitoneal, I.V.: intravenosa.
Sin embargo, in vitro comprobaron la eficiencia de fagos para eliminar MRSP, y controlar el biofilm presente, los fagos utilizados de las familias Myoviridae y Siphoviridae, de estos vB_SpsS-SN8, vB_SpsS-SN10, vB_SpsS-SN11, vB_SpsS-SN13, phiSA012, ph 0044 y ph 0045 manifestaron tener actividad lítica. Por otro lado, pSp-J y pSp-S previnieron la formación de biofilm a dosis bajas y lograron degradarlo a dosis altas34. No obstante, estas MRSP fueron de manera in vitro, y aun se requieren más estudios para determinar su eficacia in vivo.
Pseudomonas aeruginosa es otra bacteria frecuentemente relacionada con pioderma, en especial en otitis canina102. Se reportó un caso31 de un paciente de raza San Bernardo que la padecía a causa de P. aeruginosa, y al ser tratado con un fago, presentó una mejora sin efectos secundarios, 9 meses después de la aplicación del fago, ya no se observó la presencia de esta bacteria. Por otro lado, los fagos ΦS12-1 y ΦR18, de las familias Myoviridae y Podoviridae respectivamente, resultaron tener actividad lítica in vitro contra diversas cepas de P. aeruginosa aisladas de la piel de caninos103.
Dado que P. aeruginosa en la lista de prioridad de la OMS de bacterias multirresistentes109, estos estudios son de suma importancia al ser una alternativa para combatir la resistencia bacteriana.
Por último, también se ha utilizado FaL contra la Klebsiella pneumoniae in vivo, el fago ZCKP8, de la familia Siphoviridae, fue aplicado de manera tópica en heridas abiertas infectadas en ratones. Se logró cerrar dicha herida en un 99 % después de 17 días, en comparación al grupo control, la lesión se cerró en un 79.76 %, evidenciándose la reepitelización del tejido en aquellos tratados con fagos110.
Esto sugiere que existe un gran potencial para el uso de fagos dentro de la medicina clínica de animales de compañía. Además, su uso posee diversas ventajas, como la facilidad de obtenerlos, ya que presentan diversas procedencias (Tabla 2 y 3).
Por otro lado, existe también una variedad de vías de aplicación (Tabla 2), facilitando su empleo según la zona a tratar. Sabiendo que el 36 % de propietarios prefieren la vía tópica y el 1 % las vías parenterales111, la vía tópica puede emplearse mediante cremas o baños, facilitando la aplicación para los propietarios, no obstante, podría ser difícil controlar la dosis viral y muchas veces las mascotas podrían lamerse, interfiriendo con el tratamiento, que sería adecuado recomendar el uso de collar isabelino. Del mismo modo, las vías intradérmica y subdérmica serían adecuadas para los médicos veterinarios, además, permiten controlar la dosis aplicada de manera más exacta y protegen a los fagos de factores externos como lamidos, rayos UV, etc.
Cócteles en dermatología veterinaria de animales de compañía. Si bien es cierto, los fagos son altamente específicos, lo que reduce su rango de infección, sin embargo, se ha señalado que los cócteles de fagos son útiles en erradicar este P. aeruginosa, incluso existen reportes que presentan actividad lítica contra cepas bacterianas multidrogorresistente (MDR), extensivamente drogorresistente (XDR) y pandrogorresistente (PDR)112.
El uso de un cóctel de fagos para el tratamiento en canes diagnosticados con otitis por P. aeruginosa, se utilizó seis fagos (BC-BP-01 hasta el BC-BP-06), señalaron actividad lítica, sin efectos secundarios aparentes, logrando erradicar la enfermedad78.
Con respecto a otras bacterias que generan lesiones en la piel, como E. coli, P. aeruginosa y S. aureus, se aplicó un cóctel de forma tópica de tres diferentes fagos para cada una de éstas, logrando erradicar la infección en un aproximado de 9 a 13 días. En el caso de E. coli, 16.70 % de las lesiones se sanaron en 9 días, y el restante a los 13 días. Con respecto a P. aeruginosa, 55.50 % de las lesiones estaban libres de bacterias en 9 días, y 45.50 % a los 13 días, por último, en aquellas lesiones generadas por S. aureus, 60 % se sanaron en 9 días, las restantes, a los 13 días después de la aplicación del cóctel de fagos113.
Con respecto a MRSA, se ha reportado el uso de otro cóctel de fagos, con 3 diferentes fagos de la familia Myoviridae, aplicando de manera tópica, se logró disminuir la carga bacteriana, siendo igual o incluso más eficiente que la vancomicina114, cabe resaltar que no se reportaron casos de mortalidad o efectos secundarios en los ratones tratados con fagos.
El uso de un cóctel de fagos suele ser mucho más eficaz en comparación de un fago individual, en lesiones por K. pneumoniae en ratones, fueron tratados con 5 fagos individuales, y un cóctel de 5 fagos. Dicho cóctel fue más eficiente para eliminar la carga bacteriana y disminuyó el tiempo de cicatrización de la herida, a diferencia de los fagos individuales121.
El empleo de cócteles de fagos para tratar infecciones, señala la necesidad de bancos de fagos, que recolecten, caractericen y conserven, estos virus. No obstante, hasta la fecha son muy pocos los establecidos122. Una red mundial de tales bancos reduciría drásticamente la posibilidad de algún brote bacteriano amenazante y de difícil tratamiento, sin embargo, en la actualidad aún es un proceso largo y complicado el asignar fagos para determinadas necesidades123. A pesar de ello, en los centros veterinarios se podría optar por aislar bacteriófagos de las aguas residuales de baños medicados, o de muestras fisiológicas (piel y heces) de los pacientes atendidos, para así contar con un banco de fagos propio de la clínica con fines terapéuticos.
Tabla 2 Espectro de fagos utilizados para combatir bacterias patógenas en dermatología veterinaria in vitro
| Bacteria hospedadora | Fago | Familia de fago | Procedencia del fago | Resultado | Referencias |
|---|---|---|---|---|---|
| S. pseudintermedius (41 cepas) | pSp-J | Siphovirus | Suelo y agua de parques de mascotas | Placas de lisis | 34 |
| S. pseudintermedius (47 cepas) | pSp-S | ||||
| S. pseudintermedius E133 S. pseudintermedius E140 | vB_SpsS-SN8, vB_SpsS-SN10, vB_SpsS-SN11, vB_SpsS-SN13 | Siphoviridae | Heces de perro | Placas de lisis | 40 |
| S. schleiferi, S. intermedius y S. pseudintermedius | PhiSA012 | Myoviridae | Aguas residuales | Placas de lisis | 115 |
| S. pseudintermedius SP015, SP017, SP197, SP251, SP253. | ɸDP001 | Siphoviridae | Saliva de perro | Placas de lisis | 116 |
| S. pseudintermedius SP015, SP017, SP070, SP145, SP188, SP195, SP197, SP251, SP253, SP276. | ϕSA039 | Myoviridae | Aguas residuales | Placas de lisis | |
| S. pseudintermedius SP015, SP017, SP070, SP197, SP251, SP253, SP276. | ϕSA012 | Myoviridae | Aguas residuales | Placas de lisis | |
| P. aeruginosa | BrSP1 | Myoviridae | Aguas residuales | Placas de lisis | 117 |
| S. pseudintermedius 625, 2854, CCM 2885, CCM 7315, CCM 7829, CCM 7830, 33, 35, 259, 621. | QT1 | Siphoviridae | Colección Félix d'Hérelle | Placas de lisis | 118 |
| Staphylococcus spp. | W15, W17, W33, W31, W36 | Myoviridae | Agua de mar | Placas de lisis | 119 |
| P. aeruginosa | pPa_SNUABM_DT01 | Myoviridae | Muestras de agua | Placas de lisis | 120 |
Fagos autóctonos o autofagos. Desde el punto de vista práctico, se podrían emplear productos comerciales y colecciones de fagos de universidades y diversos centros de investigación, donde se evidencia el uso de productos comerciales de fagos118. Sin embargo, su alta especificidad podría limitar el efecto esperado, ya que es posible que las bacterias presentes en los pacientes no sean susceptibles a estos. Frente a este escenario, se pueden obtener o aislar fagos del paciente donde se encuentra el agente patógeno, denominando a este virus como fago autóctono o autofago26,126. Además, se considera también autofago al fago exógeno que se aplica en un individuo para luego ser reasislado127.
Los fagos autóctonos pueden utilizarse como cóctel para reducir la probabilidad de fago resistencia y ampliar su espectro. Como se ha descrito previamente, los fagos pueden obtenerse de la piel y heces (Tabla 2), a su vez se llega a considerar una de las principales fuentes de autofagos en dermatología de animales de compañía.
En canes se han reportado los fagos T4virus, Jerseyvirus, T5virus, Phix174microvirus, N4virus, T7virus, Bppunalikevirus, Bxz1virus, asimismo, bacteriófagos pertenecientes a las familias Myoviridae, Podoviridae, Siphoviridae y otros no identificados en el viroma fecal de perros sanos y aquellos con enteropatía128,129.
Tabla 3 Efecto de la utilización de fagos para combatir bacterias patógenas en dermatología in vivo
| Bacteria hospedadora | Fago | Dosis fago (UFP/ animal) | Procedencia del fago | Vía | Número de dosis | Especie animal | Resultado | Referencias |
|---|---|---|---|---|---|---|---|---|
| P. aeruginosa | BC-BP-01, BC-BP-02, BC-BP-03, BC-BP-04, BC-BP-05, BC-BP-06. | 6x105 | - | Tópica | 1 | Canis familiaris | Reducción de P. aeruginosa | 78 |
| S. aureus ATCC 25923 | F1, F4, F7, F8, F9, F10. | 1x109 | Hisopados nasales, faríngeos y aguas residuales | SC | 14 | Mus musculus | Reducción de signos clínicos y cura clínica. | 92 |
| K. pneumoniae B5055 | Kpn5 | 2x1010 | Aguas residuales | Tópica | 1 | Mus musculus | Reducción de K. pneumoniae | 124 |
| S. aureus SA325 | JD007 | 5x108 | Heces de pollo | ID | 1 | Mus musculus | Prevención y reducción de abscesos. | 125 |
UFP: unidades formadoras de placa. SC: Subcutánea. ID: intradérmica.
Del mismo modo, se reportó que la garrapata alberga una baja cantidad de fagos de las familias: Myoviridae, Podoviridae, Siphoviridae, Sphaerolipoviridae y Microviridae, los cuales podrían ser absorbidos al momento de alimentarse u originarse en la misma garrapata130.
Respecto, estudios in vitro, los autofagos vB_SpsS-SN8, vB_SpsS-SN10, vB_SpsS-SN11, vB_SpsS-SN13 se aislaron de la piel y mucosas de un paciente canino, autofagos con actividad lítica frente a S. pseudintermedius E133 y E14040 de igual modo, el autofago ɸDP001, hallado en la saliva de perro que lisó a S. pseudintermedius116.
En cuanto a estudio in vivo92 utilizaron un coctel de autofagos (F1, F4, F7, F8, F9 y F10), obtenidos de hisopados nasales, faríngeos y aguas residuales, con carácter lítico frente S. aureus en ratones aplicados vía subcutánea. Del mismo modo, han empleado fagos autóctonos en ganado bovino como el fago SAvB14 que se aisló de la secreción de la glándula mamaria de vacas con mastitis, con alta actividad lítica contra S. aureus var. Bovis131.
Los autofagos tienen la ventaja de poder aislarse directamente del entorno afectado y futuramente prepararse para su aplicación, siendo más específico y efectivo que un cóctel comercial126, recalcando que los autofagos serán más selectivos y más eficaces por el efecto que tienen en la zona de infección, permitiéndonos catalogar a los autofagos como una alternativa terapéutica.
Conclusión
Los bacteriófagos son un excelente sustituto de antibióticos, puesto que son más específicos y no lisan a bacterias benéficas, tienen actividad lítica contra bacterias resistentes a antimicrobianos. No obstante, existen bacterias resistentes a fagos, siendo desfavorable para la terapia de fagos, sin embargo, se reportó que muchas veces al adquirir esta resistencia, reducen su virulencia o se vuelven sensibles a antibióticos a los que eran resistentes. Además, si dichas bacterias mantienen su virulencia y resistencia antimicrobiana, se puede usar cocteles de fagos o quorum quenching.
Respecto a las vías de aplicación, la tópica y parenteral son las óptimas para tratar piodermas en animales de compañía.
En el presente estudio, destacamos que se deben utilizar los FaL en lugar de templados, para asegurar la lisis bacteriana incluso cuando las bacterias se encuentren en baja densidad. Del mismo modo, estos FaL no deben poseer genes de resistencia y virulencia, de esa manera, se evita que las bacterias objetivo no adquieran dichos genes mediante la transducción. Asimismo, la presentación adecuada es en forma de cóctel, dado que aumenta el espectro lítico y disminuye el riesgo de fago resistencia. En resumen, se pueden usar fagos autóctonos cuando los cocteles de fagos comerciales o de estudios previos no tienen el efecto deseado. Por lo tanto, se concluye que los cócteles de autofagos líticos no transductores son una alternativa contra la resistencia antimicrobiana en dermatología de animales de compañía. Finalmente, se recomienda comparar el uso de estos cócteles con otros sustitutos de antibióticos y evaluar su posible sinergismo para reducir bacterias patógenas en piel.











 text in
text in 
 uBio
uBio 


