Journal of the Selva Andina Biosphere
versão impressa ISSN 2308-3867versão On-line ISSN 2308-3859
J. Selva Andina Biosph. v.1 n.1 La Paz 2013
ARTÍCULO DE INVESTIGACIÓN
Respuesta de variedades mejoradas de papa (Solanum tuberosum L.) al estrés hídrico por sequía
Response of potato varieties improved (Solanum tuberosum L.) to water stress by drought
Gabriel Julio1*, Veramendi Silene1, Angulo Ada1, Magne Jury1
1Fundación PROINPA, Regional Valles Norte, Casilla 4285, Cochabamba, Bolivia.
*Dirección de contacto: Julio Gabriel
Fundación PROINPA, Casilla 4285, Cochabamba, Bolivia. Tel: (591) 4 4319595, Fax: (591) 4 4319500.
E-mail address: j.gabriel@proinpa.org
Historial del artículo
Recibido agosto, 2012.
Devuelto enero 2013
Aceptado agosto, 2013.
Disponible en línea noviembre 2013
Resumen
Con el objetivo de evaluar la respuesta antioxidante al estrés hídrico por sequía en siete variedades mejoradas de papa, se evaluó la actividad enzimática de la Catalasa (CAT), el Ascorbato peroxidasa (ASPX) y la guayacol peroxidasa (POX). Los resultados mostraron que las variedades Aurora, Victoria y Jaspe fueron resistentes al estrés hídrico por sequía y mostraron valores superiores en la actividad enzimática de la CAT, ASPX y POX, que sus propios controles. Esto confirmó que estas variedades fueron las más resistentes al estrés hídrico por sequía. En cambio, los clones 00-216-3, 00-207-6 a y las variedades Desirée y Salomé, mostraron los valores más bajos que sus controles. Indicando esto, que estas variedades fueron susceptibles al estrés hídrico por sequía. Sin embargo, la variedad Salomé con 20 días de estrés hídrico por sequía contrariamente a lo que se esperaba, mostró altos valores de actividad enzimática, respecto a sus controles. Esto sugirió que ésta variedad probablemente tuvo otros mecanismos de resistencia al estrés hídrico por sequía que le permitieron reaccionar a estreses más drásticos de sequía. Por último, la permeabilidad cuticular mostró que las variedades Aurora y Victoria tuvieron bajos contenidos de clorofila en referencia a sus controles que mostraron altos contenidos de clorofila.
Palabras clave: Enzimas antioxidantes, actividad enzimática, clorofila, resistencia, severidad.
Abstract
In order to evaluate the antioxidant response to water stress by drought in seven improved varieties, we assessed the enzymatic activity of catalase (CAT), ascorbate peroxidase (ASPX) and guayacol peroxidase (POX). The results showed that the Aurora, Victoria and Jaspe varieties were resistance to water stress by drought and showed higher values in the enzymatic activity of CAT, ASPX and POX, that their own controls. This confirmed that these varieties were more resistant to water stress by drought. In contrast, clones 00-216-3, 00-207-6 and Desirée and Salome varieties, showed resistance and lower values than their controls. However, the Salome variety with 20 days of drought water stress contrary to what was expected showed high levels of enzyme activity compared to controls. This suggested that this variety probably had other mechanisms of resistance to water stress by drought that allowed more dramatic reaction to drought stress. Finally, cuticular permeability showed that Aurora and Victoria varieties had low chlorophyll content in reference to its controls that showed high chlorophyll content.
Key words: Antioxidant enzymes, enzyme activity, chlorophyll, resistance, severity.
Introducción
El cultivo de papa es conocido por su sensibilidad a la sequía y su efecto en la productividad depende de la intensidad, duración y etapa fenológica en la que se presenta así como de la estrategia inherente del genotipo (Mamani 2000, Gabriel et al. 2011a).
La resistencia a la sequía de un cultivo hace referencia a su capacidad para crecer satisfactoriamente en zonas con déficit hídrico. Las modificaciones que tienen lugar en la estructura y función de las plantas para aumentar la probabilidad de sobrevivir y reproducirse en un ambiente determinado se llama adaptación (Charco 2002). Las respuestas adaptativas al estrés pueden clasificarse en: a) El control de la homeostasis, que incluye homeostasis iónica y la osmótica. b) El control del daño y la reparación o detoxificación. c) El control del crecimiento. Estos mecanismos actúan conjuntamente ya que la señal de homeostasis regula negativamente la respuesta de detoxificación, entonces ambas respuestas inducen la tolerancia al estrés, el cual regula negativamente la inhibición del crecimiento provocada por la aparición de las condiciones ambientales adversas. El segundo mecanismo repara la alteración del equilibrio entre las especies peroxidantes y los anti oxidantes, a favor de las primeras (Sies 1991). Esta alteración bioquímica se manifiesta como un incremento en la tasa de producción de ERO.
Las especies reactivas de oxígeno (ERO), también llamadas especies activas de oxígeno (EAO) son resultado de la reducción parcial del O2 atmosférico. Existen básicamente cuatro formas de ERO celular, oxígeno molecular singlete (1O2), radical superóxido (O2‑), peróxido de hidrógeno (H2O2) y el radical hidroxilo (HO·), cada uno con la característica vida media. Las ERO pueden ser extremadamente reactivas, especialmente el oxígeno molecular singlete y el radical hidroxilo y a diferencia del oxígeno atmosférico pueden oxidar múltiples componentes celulares como proteínas y lípidos, ADN y ARN. Las ERO se producen continuamente en el cloroplasto, mitocondria y peroxisomas.
En condiciones normales, la producción y remoción de las ERO está estrictamente controlada. Sin embargo, el equilibrio entre la producción y la depuración de éstas puede ser perturbado por diversos factores fisicoquímicos, como son el déficit hídrico, la salinidad, las temperaturas extremas, la excesiva o insuficiente radiación luminosa, la anaerobiosis por encharcamiento o inundación, los factores mecánicos como el viento o la compactación del suelo, viento fuerte y las lesiones (Cabrera 2006, Mano 2002). Cuando, tanto por un aumento de producción cuanto por una disminución en los mecanismos de defensa, se pierde el balance entre la aparición de especies nocivas y la capacidad de la célula de evitar su acumulación, ocurre una situación conocida como estrés oxidativo. En estas condiciones las especies activas del oxígeno reaccionan con las macromoléculas de las células modificando su estructura y su función y dando lugar a alteraciones que pueden conducir a la muerte celular.
En el caso de déficit hídrico, si este es prolongado en el tiempo, este ocasionara inevitablemente daño oxidativo debido a la sobreproducción de especies reactivas de oxígeno.
Por lo tanto el incremento en la capacidad de eliminación de estas ERO por parte de la planta es considerada como síntoma de tolerancia, mientras que la ausencia de respuesta o una disminución res pecto de los valores control se considera síntoma de sensibilidad (Hernández & Jiménez 2000, Toumi et al. 2010).
El mantenimiento de las ERO a un nivel compatible con el funcionamiento celular normal se lleva a cabo por diversas actividades con capacidad antioxidante y que se clasifican en enzimáticas y no enzimáticas (Foyer et al. 1994, Perl-Treves & Perl 2002).
Un antioxidante es cualquier substancia que a bajas concentraciones comparadas con las del sustrato oxidable, inhibe o disminuye significativamente la oxidación de este sustrato. Las ERO que se llegan a producir en las células son eliminadas por varios sistemas antioxidantes que se clasifican como sistema antioxidante enzimático y no enzimático (Perl-Treves & Perl 2002).
Entre los antioxidantes enzimáticos se tiene a la Catalasa (CAT) que elimina H202 en los peroxisomas, superóxido dismutasa (SOD) que elimina el anion-radical superóxido, Ascorbato peroxidasa (ASPX) que elimina H202 en diversos compartimentos, guayacol peroxidasa (POX) (Moller et al. 2007).
Otras enzimas de este grupo que desempeñan un papel importante en la detoxificación celular son: la monodehydroascorbate reductasa (MDHAR), dehidroascorbato reductasa (DHAR) y la glutatión peroxidasa (GPX) (Arora et al. 2002). Entre los Antioxidantes no enzimáticos, se tiene a los antioxidantes liposolubles como los carotenoides y alfa tocoferol y a los hidrosolubles como el ácido ascórbico y glutatión.
Desde el punto de vista agrícola, las posibles soluciones frente al estrés hídrico pasan por la modernización de los sistemas de regadío y por la utilización de cultivos con pocas necesidades hídricas. Por ello, numerosos proyectos de investigación a nivel mundial están orientados a la obtención de variedades que sean capaces de resistir mejor las condiciones adversas de falta de agua (Parry et al. 2005).
SOD es la enzima que encabeza en el ataque a las ERO debido a que remueve rápidamente uno de las primeras ERO en ser producidas: el superóxido. La SOD dismutasa, el superóxido en oxígeno y H2O2. Sin embargo, esta reacción solo convierte una ERO en otra y el H2O2 también debe ser destruido. Es aquí donde intervienen enzimas como la CAT y la ASPX. La CAT es una enzima que contiene hierro en su estructura y cataliza la dismutación del H2O2 en agua y oxígeno mole cular (Arora et al. 2002). Esta enzima se encuentra en todos los organismos eucariota aeróbicos y constituye un mecanismo esencial para la eliminación del H2O2 generado en los peroxisomas por oxidasas que participan en la ß-oxidación de ácidos grasos, la foto respiración y el catabolismo de las purinas. La CAT fue una de las primeras enzimas en ser aislada y obtenida con un alto grado de pureza. Todas las formas enzimáticas de la CAT son tetraméricas con pesos moleculares de aproximadamente 220 KDa. Múltiples formas de la CAT han sido descritas en numerosas plantas. Estas formas han sido clonadas principalmente de maíz (Terán & Singh 2002).
El ASPX es un sistema eficiente en las plantas y está formado por el sistema ácido ascórbico y la enzima ASPX. El ASPX es una enzima que con tiene un grupo hemo y requiere de la presencia de ascorbato en cantidades considerables para su estabilidad y funcionalidad. Reduce el H2O2 a agua utilizando el ascorbato como co-factor. La actividad ASPX ha sido reportada principalmente en cloroplasto y citosol (Arora et al. 2002). En los cloroplastos, la SOD y la enzima ASPX se presentan en forma soluble y unida a los tilacoides.
El Ascorbato es el antioxidante cuantitativamente predominante en las células vegetales, se encuentra en todos los compartimentos subcelulares, incluido el apoplasto, en concentraciones que oscilan entre 2-25 mM. El ascorbato es oxidado por el oxígeno, el anión superóxido, el oxígeno singlete y el peróxido de hidrógeno para dar lugar al radical monodeshidroascorbato, el cual se desproporciona en ascorbato o dehidroascorbato (Smirnoff 2000). Desempeña un papel fundamental en la fotoprotección y la regulación de la fotosíntesis, y preserva las actividades de enzimas que tienen iones metálicos de transición (Cu2+, Fe2+) como grupo prostético. El ascorbato es también un poderoso antioxidante secundario, ya que reduce la forma oxidada de la α-tocoferol. Adicionalmente, es el re ductor utilizado para la hidroxilación de residuos de prolina de la extensina, una proteína de la pared celular. También está implicado en la elongación de la raíz, el funcionamiento de los estomas, y desempeña una función crítica asociada a los mecanismos a través de los cuales las plantas perciben los cambios medio ambientales y responden a ellos (Noctor & Foyer 2005).
La POX utiliza como sustratos al guayacol y al peróxido de hidrogeno. Asimismo, desempeña una función catalítica importante al reducir los niveles de H2O2 en los tejidos vegetales, evitando con ello que este compuesto se difunda entre las membranas biológicas para reaccionar con iones libres como el Fe2+ y generar el potente radical hidroxilo, a través de la reacción de Fenton (Vogiatzi et al. 2009).
Por otra parte, se han encontrado evidencias de que las ERO también funcionan como señales moleculares que median respuestas a varios estímulos (Desikan et al. 2004).
Entre las especies reactivas del oxígeno, el H2O2 parece ser que desempaña el papel más importante en la señalización de los cambios estresantes, debido a su elevada estabilidad y largo tiempo de vida media (Hung et al. 2005). Si el H2O2 sirve como señal al estrés, las fluctuaciones de H2O2 en plantas podrían reflejar cambios espaciales y temporales en el ambiente (Hung et al. 2005). En apoyo a esta idea, un aumento brusco del estado oxidativo es una respuesta común a estreses avió ticos y bióticos (Desikan et al. 2003). Estos estreses incluyen patógenos, elicitores, daños mecánicos en el vegetal, calor, bajas temperaturas, luz UV y ozono. Por ejemplo, en invierno el descenso hasta 4ºC causó en las hojas de Triticum aestivum un aumento en los niveles de H2O2 de tres veces en comparación con el control durante un minuto de ensayo (Desikan et al. 2003).
Sobre la base de lo anteriormente mencionado, la presente investigación tuvo el objetivo de evaluar la respuesta antioxidante al estrés hídrico por sequía en variedades mejoradas de papa.
Materiales y métodos
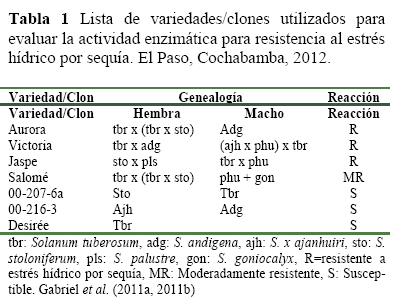
Material vegetal, para la evaluación de la actividad enzimática se utilizaron tres variedades resistentes al estrés hídrico por sequía (Gabriel et al. 2011a, 2011b) y cuatro variedades /clones susceptibles (Tabla 1).
Experimento en invernadero, se implementó en un invernadero de la Fundación PROINPA en el año 2012, ubicada a 13 km en la zona del Paso de la provincia Quillacollo en Cochabamba, a 17º 21 01.91de latitud sud y 66º 15 44.34de longitud Oeste, con una altura de 2613 msnm, una precipi tación media anual de 512 mm y una temperatura promedio de 17.4 ºC.
Los tratamientos fueron la combinación de dos factores: 1) Siete variedades de papa y 2) Tres niveles de estrés hídrico por sequias (Sin sequía, 10 y 20 días de sequía). Estos tratamientos se iniciaron a los 79 días después de la siembra (dds) (Mamani 2000). El experimento se implementó en un diseño de bloques completos al azar en arreglo de par celas divididas con tres repeticiones (Martínez-Garza 1998). Cada unidad experimental tuvo cuatro macetas con una planta/maceta. Las macetas fueron de plástico de 1 kg de capacidad y se uso sustrato estéril con chala de arroz, arena lama y tierra vegetal en una proporción 1:1:1. Los riegos fueron realizados con una probeta graduada, utilizándose 0.5 L de agua/maceta. La variable evaluada fue la marchites o severidad (S), utilizando la escala de Blum (1993) modificada por Angulo et al. (2009).
Experimento en laboratorio, se tomó una muestra de cada variedad y se hizo la lectura por triplicado para cada cuantificación enzimática. La colecta se realizó en hojas de plantas sometidas a estrés hídrico por sequía a los 10 días y a los 20 días (tratamiento) y en hojas de plantas no estresadas (control). Posteriormente se conservaron a -80 °C en un freezer Continental 260 hasta su análisis.
Preparación de los extractos enzimáticos, el material colectado fue triturado y congelado en nitrógeno líquido, el buffer de extracción enzimático se preparó según la metodología de Frary et al. (2010). Donde se utilizó 0.1% de polivinil polipirrolidona (PVPP), 100mM de tampón fosfato de potasio a pH 7.0, 1 mM de EDTA, 1 mM de ácido ascórbico. Los extractos se centrifugaron en una microcentrífuga Legend Micro 21 marca Thermo Scientific, a 10000 rpm por 20 min a 4 °C y los sobrenadantes se retiraron a otro tubo para las determinaciones de la CAT, ASPX y POX.
Determinación la actividad de la enzima CAT, se preparó una mezcla de reacción conteniendo 100 mM tampón fosfato de potasio (pH 6.5), 1.0 mM EDTA, 60.0 mM H2O2 (Aebi 1983). La actividad se determinó siguiendo la descomposición de peróxido de hidrógeno (H2O2) a 240 nm en un espectro fotómetro Marca Biorad.
La ASPX se cuantificó utilizando el método descrito por Nakano & Asada (1987), Asada (1992). La mezcla contenía 90 mM de tampón fosfato de potasio (pH 7.0), 0.1 mM EDTA, 0.65 mM ascorbato, y 1.0 mM H2O2. La actividad se determinó siguiendo la descomposición de H2O2 dependiente de as corbato a 290 nm. Las mediciones se realizaron en un espectrofotómetro marca Biorad.
Para determinar el POX se preparó una mezcla de reacción conteniendo 100 mM tampón fosfato de potasio (pH 6.5), 1.0 mM EDTA, guaiacol, y 50% H2O2, (Aebi 1983). La actividad se determinó siguiendo la descomposición de H2O2, utilizando guaiacol como agente donador de hidrógeno a 470 nm.
El cálculo de la actividad de las enzimas antioxi dantes se utilizó la siguiente fórmula (Frary et al. 2010): CAT, ASPX, POX activity (Unit) = (∆abs /min x reaction volumen)/0.001.
Permeabilidad cuticular, fue medida en base a ex tracción de clorofila, adaptado de acuerdo a metodología descrita por Zhang et al. (2005), Kosma et al. (2009). Las plantas fueron aclimatadas por un periodo de 3 horas en oscuridad, cubriéndolas con bolsas negras, antes de la medición. Luego se colectó una hoja, de la misma posición para todas las plantas en estudio y se sumergió en tubos de ensayo de 50 mL de capacidad con 15 mL de etanol 80% (v/v a temperatura ambiente). Los tubos falcón de 50 mL, fueron agitados a 30 rpm en un agitador orbital Labnetorbit 300 y en la oscuridad. Fueron tomadas alícuotas de 200 µL con micropipetas marca Biohit de cada tubo para medir la clorofila, a 647 y 664 nm, a intervalos de 1 h durante 6 h y posteriormente a las 24 h. Los datos fueron expresados como porcentaje del total de clorofila extraída a las 24 h en etanol 80% (v/v).
Análisis estadístico, los datos de la variable severidad o marchitez que satisfizo o se aproximó a los supuestos de distribución normal y homogeneidad de varianzas, se analizó de acuerdo al modelo estadístico planteado (Martínez-Garza 1998). Sobre la base del modelo definido se realizó un análisis de varianza para probar hipó tesis de los efectos fijos y comparaciones de medias mediante contrastes de un grado de libertad para determinar las variedades más resistentes. El análisis de varianza también sirvió para estimar los componentes de varianza para los efectos alea torios. Los análisis indicados se realizaron utilizando el Proc GLM del SAS (SAS 2004).
Para el análisis estadístico de comparación entre el tratamiento y el control de la actividad enzimática se hizo una prueba de T-test (SAS 2004).
Resultados
Análisis de la resistencia al estrés hídrico, el análisis de varianza de la severidad o marchitez, mostró que el efecto de sequía y variedad fueron significativos al Pr<0.01 de probabilidad (Tabla 2), indicando esto que ambas variables tuvieron un valor diferente con un nivel de sequía y al menos en una variedad. Así mismo, la interacción sequia * genotipo fue significativo, sugiriendo que el efecto de los niveles de sequía sobre la severidad fue diferente en al menos una variedad, por lo que sería posible encontrar variedades/clones con un alto grado de resistencia a sequía.
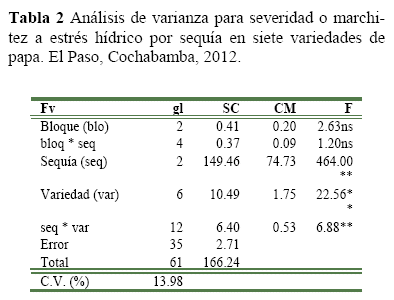
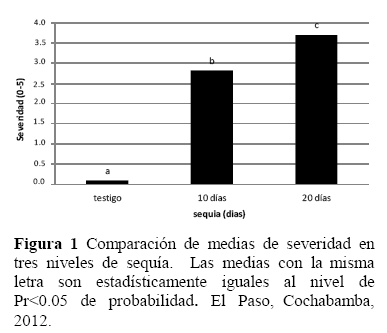
La comparación de medias de severidad (Figura 1), mostró diferencias significativas (Pr<0.01) entre los tres niveles de sequía, donde la sequía para 20 días registro mayor severidad, indicando esto que las variedades/clones presentaron una mayor severidad (marchitez) cuando las plantas sufrieron una deficiencia de agua de 20 días.
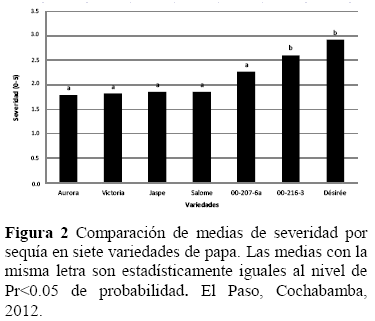
La comparación de medias de severidad entre variedades (Figura 2), mostró una amplia variación frente a la sequía, donde las variedades con menor severidad (marchitez) fueron Aurora, Victoria, Jaspe y Salomé, sugiriendo que estas variedades presentarían una alta resistencia al estrés hídrico por sequía, por lo que, además de ser una buena fuente de genes de resistencia, serian aptos para zonas agrícolas o épocas con mínima disponibilidad de agua.
Análisis de la actividad enzimática, El análisis de T-test realizado para cada variedad (T) y su testigo (C) no mostró diferencias significativas al Pr<0.05 de probabilidad para ninguna de las variedades estudiadas (Tabla 3). Con excepción de la variedad Desirée que mostró diferencias significativas para el contenido de POX.
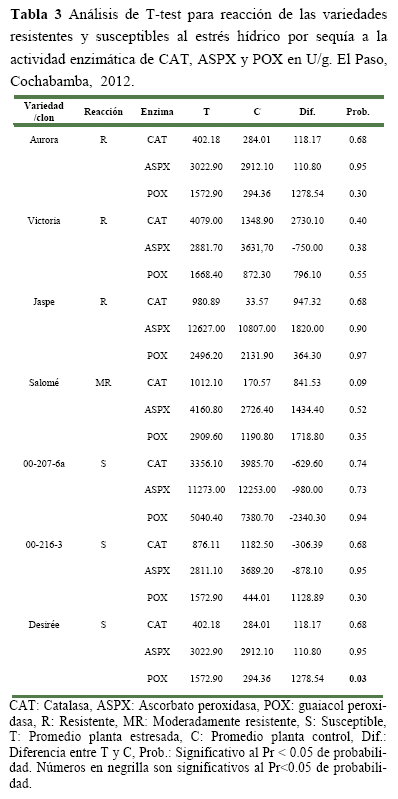
Sin embargo, se debe mencionar que aun cuando no se detectó diferencias significativas, el experimento es válido porque se lograron observar diferencias marcadas entre las enzimas evaluadas en plantas estresadas y su control respectivo. En este sentido, en los siguientes párrafos se hace un análisis de las mismas, considerando tanto el estrés hídrico por sequía a los 10 días como a los 20 días.
Evaluación del estrés hídrico por sequía a los 10 días, se observó que las variedades Aurora, Victoria y Jaspe (Tabla 4) bajo sequia de 10 días mostraron valores superiores en la actividad enzimática de la CAT (188.63 U/g, 758.10 U/g y 251.00 U/g respectivamente), ASPX (2130.38 U/g, 2487.24 U/g y 1300.18 U/g respectivamente) y POX (148.79 U/g, 586.00 U/g y 383.68 U/g respectivamente) que sus propios controles. Esto indica que la resistencia de estas variedades podría estar relacionada con la remoción de las ERO mediante estas tres enzimas. En cambio, la variedad Salomé solo mostró un ligero incremento en la producción de la enzima ASPX con respecto a su control.
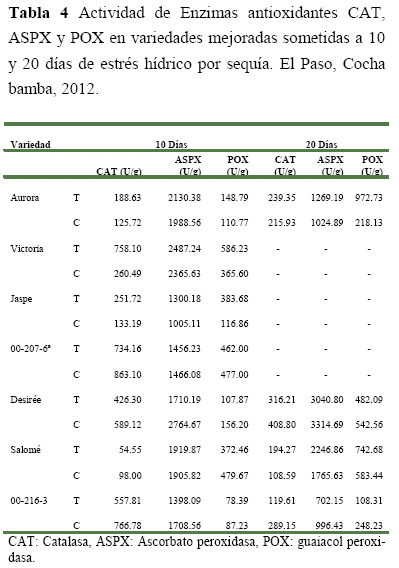
Esto indica que la resistencia de esta variedad po dría estar dada por la remoción de Ero mediante esta única enzima. En el caso del clon 00-207-6a la resistencia que presenta podría involucrar otros mecanismos diferentes a estas tres enzimas para la remoción de las ERO producidas. Por otra parte, la variedad Desirée y el clon 00-216-3 mostraron valores más bajos que sus controles. Indicando esto, que la susceptibilidad de estas variedades podría estar dada por un incremento en la producción de ERO y una disminución en la producción de enzimas removedores de ERO.
Evaluación del estrés hídrico por sequía a los 20 días, se observó (Tabla 4) que la variedad Aurora nuevamente mostró valores mayores de la actividad enzimática de la CAT (239.35 U/g), ASPX (1269.19 U/g) y POX (972.73 U/g) con respecto de sus controles, lo que indica que esta variedad presentó la misma actividad enzimática bajo un nivel mayor de estrés hídrico. Esta actividad enzimática antioxidante aparentemente le confiere resistencia a diferentes niveles de estrés hídrico a esta variedad.
La variedad Salomé nuevamente mostró valores mayores de la actividad enzimática para ASPX (2246.86) con respecto a su control. Por otra parte, también mostró un incremento en las actividades de la CAT (194.27 U/g) y POX (742.68 U/g) res pecto a sus controles. Esto indicó que la variedad Salomé necesita un estrés hídrico mayor para inducir una actividad en estas enzimas.
En cambio, el clon 00-216-3 y la variedad Desirée volvieron a mostrar valores más bajos de actividad enzimática de la CAT (119.61 y 316.21 U/g respectivamente), ASPX (702.15 y 3014.80 U/g respectivamente) y POX (108.31 y 482.09 U/g respectivamente) respecto a sus controles. Esto indica que estos genotipos la susceptibilidad de estos genotipos podría deberse a la incapacidad de remover ERO, lo cual ocasionaría severo estrés oxidativo.
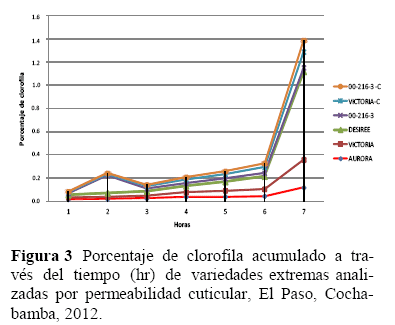
Permeabilidad cuticular, en referencia a la permeabilidad cuticular (Figura 3), se observó que las variedades Aurora y Victoria tuvieron menores contenidos de clorofila en referencia a sus controles y a las variedades susceptibles. Indicando esto que la resistencia de estas variedades al estrés hídrico estaría relacionada con una reducción en el contenido de clorofila durante el estrés hídrico.
Análisis de correlación, de Pearson entre CAT, ASPX y POX (Tabla 5), mostró sola mente una alta correlación positiva y alta mente significativa al Pr<0.01 de probabilidad para POX y ASPX.

Discusión
Se observó a través de la evaluación en invernadero y laboratorio, que la resistencia a niveles de estrés hídrico de 10 y 20 días de duración en las variedades de papa Aurora, Victoria y Jaspe aparentemente estaría relacionada con la actividad de las enzimas CAT, ASPX y POX. Estos antioxidantes enzimáticos estarían involucradas en la remoción de las ERO. Por su parte, la variedad Salomé registró un incremento en la producción de la enzima ASPX, en ambos niveles de estrés (10 días y 20 días). En cambio, el incremento de las enzimas CAT y POX solo se observó para el estrés de 20 días de duración.
El mecanismo antioxidante utilizado para explicar los resultados indicados, se basó en la eliminación del exceso de especies reactivas del oxígeno, formadas en las células de la planta, lo cual se atribuye a la acción eficiente de enzimas como la CAT, ASPX y POX en su conjunto. Existe la hipótesis de que la ASPX, enzima ubicada en cada compartimento celular donde se producen ERO podría funcionar como un regulador preciso de niveles intracelulares estables de ERO, posible mente con propósitos de señalización, mientras la enzima CAT, la cual se ubica exclusivamente en los peroxisomas, podría funcionar como removedor principal del exceso de producción de ERO bajo condiciones de estrés.
En el caso de la variedad Salomé el nivel de ERO obtenido después de 10 días de estrés hídrico podría ser insuficiente para inducir la actividad de la enzima CAT, la cual sería activada solamente después de un estrés de 20 días de duración. En cambio en las variedades Aurora, Victoria y Jaspe se observó una actividad temprana de la CAT, lo cual podría significar que el estrés hídrico por sequía de 10 días en estas variedades genera cantidades mayores de ERO o también podría significar que el sistema de remoción de ERO en estas variedades es mucho más complejo que en la variedad Salomé. Asimismo, estas variedades podrían presentar una resistencia constitutiva en lugar de inducida.
En un estudio realizado en plantas de papa transgénica modificadas para la sobre-expresión de las enzimas de ASPX y CuZnSOD se observó un in cremento en la remoción de las ERO dentro los cloroplastos. Este estudio mostró que la expresión conjunta de las enzimas ASPX y CuZnSOD (bajo el control de un promotor inducido por estrés oxidativo) y el transporte simultáneo a los cloro plastos prueban ser altamente eficientes en incrementar la tolerancia al daño oxidativo inducido mediante un estrés abiótico.
En este caso la enzima CuZnSOD jugó un papel similar al de la CAT en nuestro ensayo. Entonces, se confirmó que en la papa estas dos enzimas juegan un papel importante en la resistencia a estrés hídrico probablemente a través de la remoción de ERO. Ahora la actividad antioxidante no solo se interpreta como el proceso de atrapar ERO sino también como un mecanismo que evita la formación de estas especies reactivas de oxígeno, junto a procesos de reparación y eliminación de los productos de oxidación (Mano 2002), por ello podría ser que la actividad de las enzimas CAT, ASPX y POX sería más compleja que la simple remoción de ERO.
Las variedades Aurora, Victoria, Jaspe y Salomé pueden ser utilizadas en ambientes donde hay escases de lluvias y también como fuente valiosa de genes para transferir a otras variedades.
Las variedades que mostraron actividad enzimática disminuida en relación al control, no tuvieron la capacidad de inducir la activación de las enzimas CAT, ASPX y POX y probablemente por ello no tuvieron la capacidad de eliminar o reducir el efecto oxidante de las ERO formadas por el estrés al que fueron sometidas, como es caso de la variedad Desirée y el clon 00-216-3.
Sin embargo, es importante considerar que la actividad enzimática puede variar por distintas causas, como el estadio fisiológico de la planta u órgano en el momento de la colecta y procesamiento de las muestras y además por los factores ambientales como la temperatura, el pH y el estado hídrico de la planta, a ello se debe añadir el método emplea do para la extracción y cuantificación enzimática (Shylesh & Padikkala 1999).
Conflictos de interés
Esta investigación y no presenta conflictos de interés.
Agradecimientos
Se agradece el apoyo económico del proyecto Fontagro - CLIPAPA (FTG/RF-1025-RG).
Literatura citada
Aebi H. Catalase in vitro. Metho Enz. 1983; (105): 121-126. [ Links ]
Angulo A, Siles M, Ríos R, Gabriel J. Caracterización de 118 accesiones de arveja (Pisum sativum L.) del Banco de Germoplasma del Centro de Investigaciones Fitoecogenéticas de Piruma ni para resistencia a sequía. Revista de Agricultura, Bolivia. 2009; 42(60):25-31.
Arora A, Sairam RK, Srivastava GC. Oxidative stress and antioxidative system in plants. Current Science. 2002; 82:1227-1238. [ Links ]
Asada K. Ascorbate peroxidase-a hydrogen pero xide scavenging enzyme in plants. Physiol Plant. 1992; 85:235-241. [ Links ]
Blum A. Selection for sustained production in water deficit environments. Crop Sci. 1993; I: 343-347. [ Links ]
Cabrera YA. Efecto de Phythopthora capsici sobre el metabolismo del glutatión en suspensiones celulares de chile habanero (Capsicum chinen se Jacq.). Tesis Licenciatura. Universidad Autónoma de Yucatán. Mérida, México. 2006.
Charco J. Una introducción al estudio de la velocidad de regeneración natural del bosque mediterráneo y factores antropozoógenos que la condicionan. Páginas 115-152 in J. Charco García (ed.). La regeneración natural del bosque mediterráneo en la península Ibérica. ARBA & Ministerio de Medio Ambiente. Ciudad Real. 2002. [ Links ]
Desikan R, Cheung MK, Clarke A, Golding S, Sagi M, Fluhr R, et al. Hydrogen peroxide is a common signal for darkness and ABA-induced stomatal closure in Pisum sativum. Funct Plant Biol. 2004; 31:913-920. [ Links ]
Desikan R, Hancock JT, Neill SJ. Oxidative stress signaling. In H. Hirt and K. Shinozaki (eds.), Plant responses to abiotic stress: topic in curr ent genetics. Springer-Verlag, Berlin, Heidelberg, New York. 2003; 121-148. [ Links ]
Foyer CH. Oxidant and antioxidant dignalling in plants: a reevaluation of the concept of oxide tive stree in a physiological contex. Plant Cell Env. 2002; 28:1056-1071. [ Links ]
Frary A, Göl D, Keleş D, Ökmen B, Pınar H, Ö Şığva HÖ, et al. Salt tolerance in Solanum pennellii: antioxidant response and related QTL. BMC Plant Biol. 2010; 10:58-74. [ Links ]
Gabriel J, Porco P, Angulo A, Magne J, La Torre J, Mamani P. Resistencia genética a estrés hídrico en variedades de papa (Solanum tuberosum L.) bajo invernadero. Revista Latinoamericana de la Papa. 2011a, 16(2):173-208.
Gabriel J, Pereira R, Gandarillas A. Catálogo de nuevas variedades de papa en Bolivia. Fundación Proinpa, Cochabamba, Bolivia. 2011b; 55 pp. [ Links ]
Hernandez JA, Jimenez A. Tolerance of pea (Pisum sativum L) to long term salt stress is associated with induction of antioxidant deferences. Plant Cell Env. 2000; 23:853-862. [ Links ]
Hung SH, Yu CW, Lin CH. Hydrogen peroxide functions as a stress signal in plants. Bot Bull Acad Sin. 2005; 46:1-10. [ Links ]
Kosma DK, Bourdenx B, Bernard A, Parsons EP, Lü S, Joubès J, et al. The impact of water deficiency on leaf cuticle lipids of Arabidopsis. Plant Physiol. 2009; 151:1918-1929. [ Links ]
Mamani P. Effet de la secheresse sur six varietés de ponme de terre dans les andes boliviennes. Tesis M.Sc., Universite Catholique de Louvain. Bélgica. 2000; 43 pp. [ Links ]
Martinez-Garza A. Diseños experimentales: Métodos y elementos de teoría. Editorial Trillas, México D.F., México. 1988; 756 pp. [ Links ]
Mano J. Early events in enrionmental stresses in plants-induction mechanisms of oxidative stress. Page 217-246 in Oxidative stress in plants, UK. 2002. [ Links ]
Moller IM, Jensen P. Oxidative modifications to cellular components in plants. Ann Rev Plant Biol. 2007; 58:459-481. [ Links ]
Nakano Y, Asada K. Purification of ascorbate peroxidase in spinach chloroplasts; its inactivation in Ascorbate-depleted medium and reactivation by monodehydroascorbate radical. Plant Cell Physiol. 1987; 28(1):131-140. [ Links ]
Noctor G, Foyer CH. Ascorbate and glutathione: keeping active oxygen under control. Annu Rev Plant Physiol Mol Biol. 2005; 49:249-279. [ Links ]
Parry M, Rosenzweig C, Livermore M. Climate change, global food supply and risk of hunger. Phil Trans Royal Soc B. 2005; 360:2125-2138. [ Links ]
Perl-Treves R, Perl A. Oxidative Stress: An introduction in Inzé, D. and Van Montagu M. (eds). Oxidative stress in plants. London: Taylor & Francis. 2002; 1-32. [ Links ]
SAS Institute Inc. SAS/STAT Users Guide, Version 9.2, Fourth Edition, Vol. 2, SAS Institute Inc., Cary, N.C. 2004.
Sies H. Oxidative Stress: From Basic Research to Clinical Application. Amer J Med.1991; 91: 31-38. [ Links ]
Smirnoff N. Ascorbic acid: metabolism and functions of a multi-facetted molecule. Current Op Plant Biol. 2000; 3:229-235. [ Links ]
Shylesh BS, Padikkala J. Antioxidant and anti-inflammatory activity of Emilia sonchifolia. Fitoterapia. 1999; 70(3):275. [ Links ]
Terán H y Singh SP. Biotecnologia V14 CS3.indd 262 en Crop Sci. 2002; 42: 64-70.
Toumi I, Moschou PN, Paschalidis KA. Abcisic acid signals reorientation of polyamine metabolism to orchestrate stress responses via the polyamine exodus pathway in grapevine. J Plant Physiol. 2010; 167:519-525. [ Links ]
Vogiatzi G, Dimitris DT, Christodoulos CS. The role of oxidative stress in atherosclerosis hellenic. J Cardiol. 2009; 50:402. [ Links ]
Zhang JY, Broeckling CD, Blancaflor EB, Sledge MK, Sumner LW, Wang ZY. Overexpression of WXP1, a putative Medicago truncatula AP2 domain-containing transcription factor gene, increases cuticular wax accumulation and enhances drought tolerance in transgenic alfalfa (Medicago sativa). Plant J. 2005; 42: 689-707. [ Links ]











 uBio
uBio