Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Ciencia, Tecnología e Innovación
versión impresa ISSN 2225-8787
Rev. Cien. Tec. In. vol.17 no.20 Chuquisaca dic. 2019
Artículo
Efecto de oligosacáridos y enzimas sobre biopelículas generadas por Candida glabrata en prótesis dentales
Effect of oligosaccharides and enzymes on biofilms generated by Candida glabrata in dental prostheses
María De La Cruz 1 *, Estefanía Tiburcio 2, Jazmín Morales 2, Agatha Bastida 2, María Ulloa3
1 Facultad de Odontología y Facultad de Ciencias de Enfermería y Obstetricia. Universidad Mayor, Real y Pontificia de San Francisco Xavier de Chuquisaca.
2 Instituto de Química Orgánica General, CSIC, Madrid-España.
3Programa de Microbiología-Micología. Facultad de Medicina. Universidad de Chile.
Recibido septiembre 13, 2019; Aceptado octubre 21, 2019
Resumen
La C. glabrata frecuentemente coloniza la cavidad oral de los adultos mayores. Las biopelículas generadas por C. glabrata con perfil de sensibilidad disminuida o resistencia a fluconazol adheridas a prótesis dentales, son un factor de riesgo para la candidiasis subprotésica y mortalidad en adultos mayores hospitalizados. La resistencia de C. glabrata, especialmente por su capacidad de producir biopelículas, lleva a falla terapéutica odontológica y requiere investigar alternativas terapéuticas.
En consecuencia, nuestro estudio investigó el efecto de oligosacáridos como antifúngicos y enzimas hidrolíticas como biomoléculas reductoras de biopelículas generadas por C. glabrata. Se analizaron 37 cepas de C. glabrata (11 de ellas, formadoras de biopelículas) aisladas de 81 adultos mayores (con consentimiento informado) que residen en Hogares de acogida en Sucre, Bolivia. La susceptibilidad antifúngica de los oligosacáridos fue estudiada mediante difusión en agar y CIM mediante micro dilución en caldo RMPI según CLSI. La actividad sobre las biopelículas según el método de O'Toole y Kolter. Resultados: El quitosano Ch-D, presentó buena actividad antifúngica para C. glabrata.
El uso de lisozima a 50 ng/ml, muestra una excelente actividad como agente reductor de biopelículas de 24 horas, en aislados de prótesis dentales. Conclusiones: Nuestro estudio evidenció, que la longitud de la cadena, como la presencia de grupos aminos en los oligosacáridos, son claves para la actividad antifúngica frente a C. glabrata. En el caso de biopelículas formadas, la actividad de la lisozima podría ser útil. Ambas moléculas, podrían ser una buena alternativa para tratamiento de C. glabrata y evitar la aparición de candidiasis subprotésica.
Palabras Clave
Candida glabrata, biopelículas, carbohidratos, lisozima, quitosano
Abstract
C. glabrata frequently colonizes the oral cavity of older adults. Biofilms generated by C. glabrata with a diminished sensitivity profile or resistance to fluconazole attached to dental prostheses, are a risk factor for subprothetic candidiasis and mortality in hospitalized older adults. The resistance of C. glabrata,
especially for its ability to produce biofilms, leads to dental therapeutic failure and requires researching therapeutic alternatives. Therefore, the aim of this work was to study the effect of oligosaccharides as antifungals and hydrolytic enzymes as biomolecules reducing biofilms generated by C. glabrata.
37 strains of C. glabrata (11 of them, biofilm-forming) isolated from 81 older adults (with informed consent) residing in care homes in Sucre, Bolivia, were analyzed. The antifungal susceptibility of oligosaccharides was studied by diffusion in agar and MIC by means of microdilution in RMPI broth according to CLSI. The activity on biofilms according to the O'Toole and Kolter method.
Results: Ch-D chitosan showed good antifungal activity for C. glabrata. The use of lysozyme at 50 ug / ml shows an excellent activity as a 24-hour biofilm reducing agent in dental prosthesis isolates. Conclusions: Our study showed that chain length, such as the presence of amino groups in oligosaccharides, are key to antifungal activity against C. glabrata. In the case of biofilms formed, the activity of lizosima could be useful. Both molecules could be a good alternative for the treatment of C. glabrata and avoid the appearance of subprosthetic candidiasis.
Keywords
Candida glabrata, biofilms, oligosaccharides, lysozyme, chitosan.
Introducción
En adultos mayores colonizados por C. glabrata, se ha observado con frecuencia la presencia de candidiasis oral por esta levadura, la cual se adhiere a las superficies de las prótesis dentales formando biopelículas, presenta sensibilidad disminuida o resistencia a fluconazol y antimicóticos de uso oral y puede causar mortalidad en pacientes hospitalizados (Millsop & Fazel 2016). El desarrollo de la candidiasis está determinado por los factores de virulencia de la levadura y por las condiciones clínicas de los pacientes (Lyu et al. 2016). Por otro lado, son escasos los fármacos con buena actividad antifúngica y que penetren la matriz de las biopelículas, como es el caso de la caspofungina (Kovacs et al. 2016) o el voriconazol (Rodrígues et al. 2017). Tres grandes familias han sido descritas como antifúngicos (Wiederhold 2018); polienos (anfotericina B, nistatina y natamicina), equinocandinas (caspofungina, micafungina y anidulafungina) y azoles (miconazol, voriconazol, itraconazol, isovuconazol y fluconazol). Sin embargo, la resistencia de C. glabrata a estos antifúngicos ha reducido el arsenal terapéutico para tratamiento de candidiasis, tanto oral como sistémica. A esto se suma, que el fluconazol es un fungistático que no presenta punto de corte de sensibilidad en los métodos de difusión agar y Concentración Inhibitoria Mínima (CLSI y EUCAST) para reportar uso terapéutico. La falta de antifúngicos con actividad sobre biopelículas formadas por levaduras, en el tratamiento de pacientes con candidiasis oral es cada vez más frecuente, por lo que surge la necesidad de encontrar nuevos compuestos bioactivos alternativos para uso terapéutico (Pereira et al. 2013). En el caso de infecciones orales por C. glabrata, los ensayos in vitro frente a diferentes antifúngicos han demostrado su resistencia y actividad variable a miconazol, fluconazol, e itraconazol. Por otro lado, nistatina, anfotericina B, isavuconazol, itraconazol, posaconazol, y voriconazol son muy activos.
La C. glabrata es una especie que frecuentemente coloniza la cavidad oral de los adultos mayores, se adhiere a los tejidos gingivales y superficies acrílicas de la prótesis dental adaptándose a las condiciones de oxigeno reducido. Es una levadura que metaboliza azúcares tipo glucosa y es muy resistente al estrés oxidativo. Entre los factores que favorecen la infección por C. glabrata, se encuentra la formación de biopelículas en superficies tisulares hidrofóbicas debido a la presencia de proteínas tipo adhesinas (poseen dominios hidrófobos serina-treonina) que incrementan la aglutinación de las células fúngicas.
El crecimiento y maduración de las biopelículas conlleva la formación de una matriz extracelular rica en polisacáridos y proteínas, principalmente de tipo 1,3-P-glucanosiltransferasas responsables del incremento en la longitud de los oligosacáridos presentes en la pared celular, consolidando la estructura de la biopelícula (Fernández. 2017). La arquitectura de las biopelículas, así como su composición (carbohidratos en la matriz extracelular) depende del tipo de cepa de Candida spp., por ejemplo C. glabrata está formada por blastosporas íntimamente unidas formando agregados (rica en glucosas y proteínas) (Cinquin & Lopes 2019). Los principales mecanismos de resistencia de las biopelículas son: i) presencia de células con actividad metabólica débil, ii) extrusión activa a través de bombas de eflujo de la droga debido a un estrés ambiental, iii) variación en la concentración en la densidad celular dentro de la biopelícula y iv) baja difusión de la droga a través de la matriz extracelular.
La C. glabrata se ha convertido en un importante patógeno emergente en personas mayores, siendo el principal agente causal de la candidiasis oral. Reportes en México describen una prevalencia de 83% en portadores de prótesis dental en personas de 38 a 63 años (Ibáñez et al. 2017).Un estudio de historias clínicas de un Hospital Universitario Nacional de Taiwan, entre los años 2000-5 reportó que la segunda especie aislada fue C. glabrata representando un 41% en 471 casos (30%), una resistencia del 11% a fluconazol y una tasa de mortalidad del 58% en 30 días. (Ruan et al. 2008). Un estudio de candidemia realizado en Reino Unido entre el 2011 al 2017, de 119 pacientes, en el grupo de 75 adultos mayores, presentó una prevalencia de 27,7%. (Smyth et al. 2018). En un estudio realizado en un hospital de Buenos Aires, se identificaron 374 episodios de candidemia, con una incidencia de 2.21 /1000 asociada a C. glabrata (13.9%) siendo un 52,7% detectada en adultos mayores de 64 años y con una tasa de mortalidad del 47,9% (Tiraboschi et al. 2017).
La resistencia y la sensibilidad disminuida de C. glabrata al fluconazol, ha llevado a la falla terapéutica odontológica en la candi diasis oral.
Estudios moleculares explican este perfil de resistencia, como es el caso de una mutación silenciosa en el 2,4% de los aislamientos de C. glabrata en un factor de trascripción (CgPDR1) responsable de la resistencia a azoles en pacientes con candi diasis oral, debido a una sobre expresión de una proteína ABC trasportadora promoviendo la salida de la droga al exterior (Tantivitayakul et al. 2019).También se ha demostrado que la baja actividad de los azoles frente a los biopelículas se debe a que el antifúngico no es capaz de ingresar completamente a las células de las biopelículas de C. glabrata. También se ha reportado que algunas drogas, como la anfotericina B, actúa bien solo en fases iniciales de la formación de biopelículas, ya que los carbohidratos presentes en la matriz actúan como un agente quelante, así el uso de enzimas para el tratamiento de la disociación de las biopelículas podría ser una buena solución.
Hasta la fecha los principales compuestos descritos en la literatura como posibles agentes frente a la formación de biopelículas son; EDTA como agente quelante, L-Acetil-cisteína como agente reductor, uso de antimicóticos, DNasas y quitosanos para recubrir superficies inertes evitando la formación de la biopelícula (Costa et al. 2017).
Debido a lo anteriormente expuesto, nos planteamos investigar el uso de oligosacáridos de diferente longitud, con grupos funcionales con carga positiva (aminos) y negativos (sulfatos y ácidos) para determinar su efecto sobre Candida y por otro lado el uso de enzimas hidrolíticas como posibles biomoléculas reductoras de biopelículas generadas por la especie C. glabrata, tras su adherencia a prótesis dentales (Saggu et al. 2019).
Materiales y métodos
Población en estudio
En este estudio participaron 81 adultos mayores que cumplieron los criterios de inclusión: uso de prótesis, edad mayor de 60 años y residente en hogares de acogida y firmaron el consentimiento informado. Fueron excluidos del estudio: adultos mayores bajo tratamiento sistémico, tópico antimicrobiano o antimicótico, estados postrante, degenerativo o cáncer (cuya participación no esté autorizada por el médico). De los 81 adultos: 37 estaban colonizados por C. glabrata y 11 de ellas correspondieron a cepas de C. glabrata formadoras de biopelículas. Las variables dependientes son la actividad antifúngica y el efecto reductor de biopelículas de C. glabrata, de los compuestos oligosacarídicos y enzimas hidrolíticas y las variables independientes concentración y tiempo de formación de las biopelículas (con un crecimiento de una OD= (McFarland Turbidity Standard N°0.5) considerado 0h y con un crecimiento de 24h).
Compuestos y enzimas empleadas
Como oligosacáridos se usaron cuatro tipos de quitosanos, dos monosacáridos de tipo aminoglicósidos y cinco oligosacáridos de tipo condroitin de bajo peso molecular (10 KDa) (Benito-Arenas et al. 2018). Todos los compuestos fueron sintetizados en el laboratorio de Química Orgánica General (CSIC) en Madrid, España; excepto algunos quitosanos comerciales de Sigma-Aldrich (St. Louis, MO, USA) (Quitosano de alta viscosidad Ch-A (Ref. 419419, Mm 310000-375000 Da. >75% desacetilado), Quitosano de media viscosidad Ch-B (Ref. 44887, Mm 190000-310000 Da. 75-85% desacetilado), Quitosano de baja viscosidad Ch-C, (Ref. 44869 Mm 50000-190000 Da. 75-85% desacetilado). El derivado de quitosan Ch-D se preparó en el laboratorio de Química Orgánica General (CSIC Madrid, España) (con una desacetilación del 88,5% desacetilado) a partir del quitosano de media viscosidad mencionado anteriormente. Los quitosanos Ch-D1, Ch-D2 y Ch-D3 se obtuvieron variando las condiciones de la síntesis del compuesto de quitosano Ch-D. Las enzimas usadas fueron todas de Sigma (lisozima, N-acetil-P-manosamina,a glucosidasa tipo I, neurominidasa, y trehalasa).
Preparación del compuesto Ch-D
Los quitosanos se purificaron antes de ser usados, se les disolvió en medio ácido (1% (v/v) de ácido acético glacial al 99%), se mantuvo en agitación 3h a 40°C y se centrifugó para eliminar las partículas insolubles. El sobrenadante se dializó en agua en medio ácido (membranas de 6-8 KDa) y posteriormente se liofilizaron y neutralizaron con NaOH a un valor de pH final de 5.6. Se perdió un 28% en masa al purificar el quitosano de alta viscosidad, un 31% en el de media y un 43% en el de baja viscosidad. Esto nos indicó que las muestras presentan muchos adyuvantes y polímeros de muy bajo peso molecular. Las soluciones de quitosano usadas en los discos y medios de cultivo se disolvieron en HCL 0.25N y se ajustaron a pH 5.6 con NaOH 1N.
Para la síntesis del compuesto Ch-D se pesaron 14,4mg de quitosano de media viscosidad previamente purificado y liofilizado. Se disolvió en 1,5mL de ácido acético al 2% w/v. Después se añadió 2,5mL de sosa (NaOH), a una concentración 6,5 N, para que la disolución resultante (4mL totales) posea una concentración de 4,1N. Una vez añadida la sosa a la disolución de quitosano, se agitó durante unos minutos y después se sometió a microondas a 80 ° C durante 30 min (200W, 20bar, 15s preagitación, en modo dinámico). Tras su enfriamiento se procedió a diálisis (6-8KDa) en agua en medio ácido y posterior liofilización. Las condiciones para la síntesis de los compuestos Ch-D fueron; Ch-D1 (Ch-C, 5NNaOH, 20', 100C), Ch-D2 (Ch-B, 5N NaOH, 20',100C), Ch-D3 (Ch-B, 5N NaOH, 30',100C). Se identificaron por RMN-H1(Pereira et al 2015) y de IR.(Negrea et al 2015)
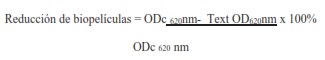
Para observar la desacetilación del quitosano se compararon los espectros de IR del quitosano desacetilado con el espectro de la quitina (quitosano totalmente acetilado), que posee un 100% de acetilación. Así se determinó que nuestro compuesto presentaba un 11,5% de acetilación.
Aislamiento, identificación y formación de biopelículas de C. glabrata
Se realizó el aislamiento de C. glabrata en 81 adultos mayores residentes de 3 hogares de acogida "Mercedes", "25 de Mayo" y "Santa Rita" de la ciudad de Sucre en Bolivia. Los aislamientos se hicieron por hisopado de la superficie de prótesis dentales de la arcada superior o inferior. Cada muestra se depositó en un vial para su traslado al laboratorio de Microbiología de la Facultad de Ciencias de Enfermería y Obstetricia (UMRPSFXCH) en Sucre, Bolivia. Para el aislamiento de C. glabrata se empleó el Agar Sabouraud (Difco) (glucosa 40 g, agar 20g, cloranfenicol 0,05g y 1L de agua, a un pH 6,5). Se realizó la siembra de las muestras obtenidas de las prótesis por agotamiento en el agar mencionado y se incubó a 37 °C por 72h en aerobiosis. Fueron identificadas mediante CROMagar Candida (CHORMagar Candida, Francia), microcultivo y API/ ID32 Candida (bioMèrieux).
Para determinar la capacidad de formación de biopelículas de las 37 cepas de C. glabrata obtenidas de las prótesis dentales, se empleó el ensayo adaptado del método de O'Toole y Kolter (O'Toole & Kolter 1998) descrito por Gómez y Cols (Gómez et al. 2013). Se empleó: FBS (Suero Bovino Fetal 50% Bovino IgG, <1 mg/mL Hemoglobina, <20 mg/dL), PBS (tampón fosfato 0,01M pH7.4 Sigma, USA), medio M 130 a pH 6.5, solución violeta de Genciana (Sigma Aldrich, USA),
decolorante (25% Acetona/75% Propanol) y placas de 24 pocillos de poliestireno (USA). Para la lectura se empleó el lector de microplacas (SpectraMax Plus 384 Microplate Reader) a una longitud de onda de 620 nm, se midió la OD de las biopelículas formadas a 37 °C a las 24 horas. La capacidad de formación de las biopelículas se expresó como unidad BBU (Unidad de Biomasa de Biofilm) y se clasificaron en las categorías de no formadoras de biopelículas (DO< DOc) y formadoras de biopelículas (DO<DO< 2DOc).
Actividad antifúngica de los compuestos bioactivos
Para determinar la actividad antifúngica de los compuestos oligosacáridos se utilizó el método de difusión en agar (Gary et al. 2018). Se usó agar Mueller-Hinton suplementado con 2% de glucosa y 0,5ug/ml azul de metileno. Se usaron discos estériles de papel filtro de 10 mm (Sigma Aldrich, USA) impregnados con los compuestos. Como controles se emplearon las cepas C. parapsilosis, (ATCC 22019), C. krusei (ATCC6258) y C. glabrata (CECT 1448) obtenidos de Sigma Aldrich. Se emplearon discos antimicóticos (6mm) de fluconazol (25 ug) y voriconazol (1ug) de OXOID, UK. Los discos fueron impregnados con los compuestos bioactivos de oligosacáridos (condroitin, quitosanos y derivados de aminoglicósidos) a 3 distintas concentraciones (500-50ug/ml).
A partir de una cepa incubada de 24 horas en agar Sabouraud suplementado con cloranfenicol, se preparó un inóculo estandarizado según la escala de 0,5 Mc Farland empleando el turbidìmetro (bioMèrieux, Francia), posteriormente se sembró en agar Mueller Hinton suplementado con glucosa y azul de metileno, se incubó a 37°C por 24 horas y posteriormente se midieron las zonas de inhibición. En la interpretación de los controles, se consideró los valores de Instituto de Estándares Clínicos y de Laboratorio (CLSI) M44-A2 Vol.29 N°.17, agosto 2009/ M60, marzo 2017.
Para el control de calidad se emplearon los discos de voriconazol (1ug) con C. parapsilosis (ATCC 22019) rango de halo de inhibición 28-37mm, C. krusei (ATCC 6258) rango de halo de inhibición 16-25mm y en la lectura de los discos de fluconazol (25ug) se consideró en la C. parasilopsis un rango de halo de inhibición de halo de 22-33 mm.
Determinación de la Concentración Inhibitoria Mínima (CIM)
El estudio de susceptibilidad de los compuestos bioactivos se realizó mediante el método de microdilución en caldo RPMI 1640 suplementado con MOPS a pH 7 según recomendaciones del (CLSI). Se empleó un inóculo ajustado al 0,5 Mc Farland (0,5-2,5 x105 UFC,/ml) espectrofotómetro a 530 nm. (uv/visble espectrofotómetro), se incluyeron: un pocillo con el crecimiento de levadura en estudio más el compuesto, y se incluyeron como controles : un pocillo con el crecimiento de levadura sin el compuesto, otro pocillo sólo con medio RPM1 y otro pocillo con levadura más caspofungina. y. Se incubó a 35 °C a las 48 h con agitación constante y se leyó la OD en el lector de microplacas (SpectraMax Plus 384 Microplate Reader) a 530 nm. Al cultivo de levadura a una OD de 0.5 se añadieron concentraciones variables de los antifúngicos de interés; para los compuestos Ch-D, y alginato 5-200ug/ml, para voriconazol 0.5-5 ug/m, para fluconazol 1-20ug/ml.
Actividad de compuestos activos sobre la formación de biopelículas de C. glabrata.
Se empleó el ensayo adaptado del método de O'Toole y Kolter, destinado a evaluar el efecto de los nuevos compuestos sobre la formación de biopelículas generadas por C. glabrata. Para la preparación del inóculo se empleó un cultivo de C. glabrata en agar Sabouraud de 24 horas de incubación, a partir del cual se suspendieron 3 a 5 colonias en caldo M130 y se incubó a 37 ° C durante 24 horas con una agitación constante (OD530nm 1.5), posteriormente se tomaron 75-100 ul de este cultivo y se le añadieron 10ml de medio M130, para alcanzar una OD de 0,145 a 530nm. Esta metodología se aplicó a cada una de las cepas de C. glabrata aisladas de las prótesis dentales y a su control C. glabrata (CECT 1448).
Los oligosacáridos y enzimas (0-1mg/ml) se usaron a diferentes concentraciones y se agregaron cuando los cultivos presentaban una OD de 0.5 (t=0) y una OD de 1.5 (t=24h).Se incubaron en ambos casos a 37°C por 24h.
Para medir el efecto de reducción de biopelículas de Candida glabrata de los compuestos bioactivos, se consideró la unidad de BBU expresada en porcentaje según la siguiente formula:
Reducción de biopelículas = ODc 620nm- Text OD620nm x 100% ODc 620 nm
ODc 620 nm
Análisis de los resultados
Se realizó la prueba de normalidad mediante el Test de Shapiro Wilk con un valor p<0,05 y un nivel de confianza del 95%. Luego se comparó los resultados obtenidos con la prueba de Tukey y mediante una ANO VA se contrastó los análisis de varianza de los tratamientos de los compuestos bioactivos según concentración y tiempo de formación de las biopelículas de cepas clínicas de C. glabrata.
Resultados
En el presente estudio, participaron 81 adultos mayores residentes de 3 hogares de acogida "Mercedes", "25 de mayo" y "Santa Rita" de la ciudad de Sucre en Bolivia. De los 81 adultos, el 77.8% estaban colonizadas por Candida spp. Por otro lado, el 45,7% presentó candidiasis sub-protésica, de las cuales se evidencia un franco predominio de C. glabrata (29,6%) (Figura 1-A).
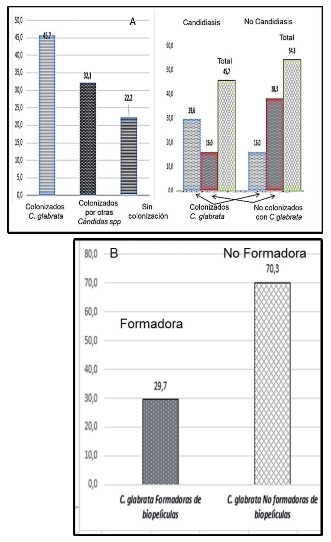
Figura 1A.- Colonización de Candida de 81 muestras de prótesis dentales de residentes de hogares de acogida de Sucre (Bolivia).Fuente: Registro Laboratorio Microbiología Carrera de Enfermería UMRPSFXCH Cultivo positivo y tipificación de la especie por API 32 y VITEK
De estas las 81 muestras se detectó que un 29,7% de las cepas de C. glabrata generaban biopelículas. Nuestros resultados evidencian un alto número de prótesis colonizadas por C. glabrata siendo responsable de la mayoría de los casos presentes de candidiasis en estos individuos (Figuras 1- A y 1-B).
Actividad antifúngica de los oligosacáridos.
Nuestros resultados contemplan el uso de tres tipos de oligosacáridos sobre C. glabrata: (a) cinco compuestos de estructura polisacarídica tipo condroitin sulfatados y no sulfatados (condroitin persulfatado (C-PS), condroitin sulfatado en las posiciones 4,6 (C-4,6S), condroitin sulfatado en la posición 6 (C-6S), condroitin sin sulfatar (C-0S), y condroitin sulfato en la posición 4, (C-4S) (Benito-Arenas et al. 2018), (b) dos compuestos derivados de aminoglicósidos (unidades mínimas neamina, y estreptidina) (Zárate et al. 2019) y (c) cuatro compuestos tipo quitosano (quitosano de alta viscosidad (Ch-A), de media (Ch-B), de media con mayor grado de deacetilación (Ch-D) y de baja viscosidad (Ch-C) (Figura 2).
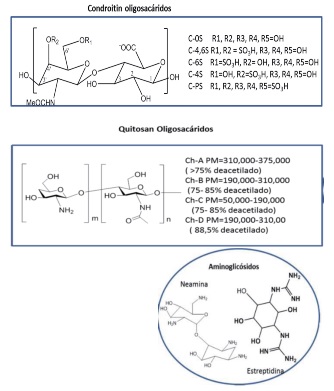
Figura 2.- Estructura de los compuestos oligosacáridos usados como antifúngico frente a las cepas de C. glabrata.
En la Figura 2 se observa la composición química de los carbohidratos usados.
Por un lado, los glucosaminoglucanos (condroitin) son oligosacáridos de distinta longitud constituido por unidades repetitivas del disacárido N-acetilgalactosamina-P-(l-4)-Acido glucurónico.
Dichos disacáridos, en la naturaleza están sulfatados principalmente en las posiciones 4' y 6' de la unidad N-acetilgalactosamina. En nuestro grupo de investigación, hemos llevado a cabo la sulfatación en todas las posiciones posibles, para ver su influencia sobre la actividad fúngica en C. glabrata (Benito-Arenas et al. 2018) (Figura 2).
Por otro lado, se han usado derivados de antibióticos aminoglicósidos, tipo estreptidina y neamina que presentan un alto grado de grupos aminos en sus estructuras (4 grupos amino por monosacárido). Por último se han usado quitosanos con diferente grado de viscosidad y número de grupos aminos presentes por disacárido.
Actividad antifúngica de los oligosacáridos mediante método de difusión en agar.
Los resultados de la actividad antifúngica de estos oligosacáridos por el método de difusión en agar sobre las cepas de Candida spp. (C. glabrata, C. krusei y C. parapsilosis) demostraron que los quitosanos con peso molecular intermedio y mayor número de grupos aminos en sus monosacáridos presentaron mejor actividad antifúngica frente a la cepa de C. glabrata.
Se estudiaron a su vez, varios compuestos de quitosano de peso molecular medio con diferente cantidad de grupos aminos (85-88,5%), siendo el compuesto Ch-D el que presentó los mejores resultados (Tabla 1).
Tabla 1.- Valores de actividad antifúngica de alginato y el compuesto Ch-D sobre cepas de C. glabrata, C. krusei y C. parapsilosis. Como control positivo se usó Fluconazol y Voriconazol.
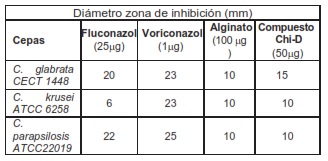
Nota. El disco estéril empleado para los ensayos fue de 10mm de diámetro para alginato y el compuesto Ch-D. Para el caso de los controles de Fluconazol y Voriconazol fue de 6mm de diámetro.
El Ch-D se diferencia de los otros quitosanos por poseer mayor número de grupos aminos primarios en su estructura (88,5%) presentando un halo de inhibición de 15mm sobre la C. glabrata CECT 1448 (Tabla 1, Figura 3) y 14 mm frente a cepa clínica (Tabla 2. Figura 3). Se empleó como control del ensayo el fluconazol (20 mm), y el voriconazol (26 mm) Se usó alginato como de polisacárido (control negativo) no observándose halo de inhibición. (halo10 mm). (Tabla 1, Figura 3). Otros compuestos de quitosano poseen menor actividad al Ch-D sobre la C. glabrata (CECT 1448). (Tabla 2.)
Tabla 2.- Comparación de la actividad antifúngica de los compuesto Ch-D y caspofungina sobre cepas de C. glabrata CECT (1448) y cepas clínicas. Como control positivo se empleó Caspofungina.
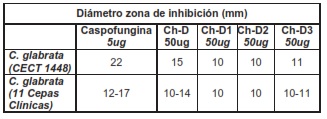
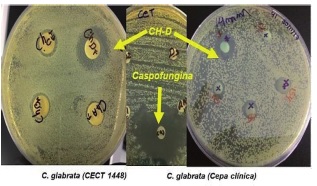
Figura 3.- Cepa de C. glabrata tipo (CECT 1448) y de un aislados de prótesis dental frente a discos impregnados compuestos de Ch-D y caspofungina.
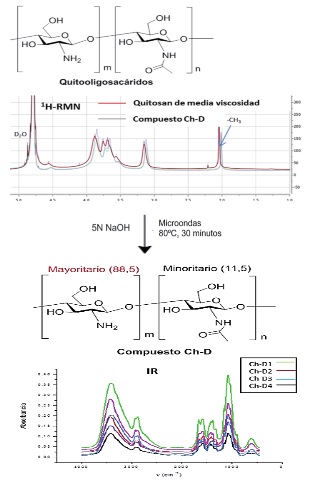
En el esquema 1 se representa la síntesis del compuesto Ch-D y su caracterización química (1H-RMN, IR). El quitosano está formado por unidades repetitivas de disacáridos tipo D-glucosamina-P-(l-4)-N-acetil-D-glucosamina. l grupo acetilo del monosacárido N-acetil-D-glucosamina es el indicativo de su deacetilación para incrementar el número de grupos aminos en el polisacárido. Las condiciones óptimas de deacetilación usadas para incrementar el número de grupos aminos fue una reacción en microondas a presión con una temperatura de 80°C, durante 30 minutos y una concentración de sosa cinco norma. Condiciones más drásticas (mayor concentración de sosa, más tiempo de reacción o más temperatura) dio lugar a la hidrólisis de dichas unidades disacarídicas (se detectó por la resolución en el espectro de 1H-RMN) con lo que la hidrólisis del polímero dio lugar a la pérdida de la actividad. Esta misma reacción se llevó a cabo con quitosano de alta y baja viscosidad dando lugar a una menor actividad antifúngica. En el espectro de 1H-RMN (espectro de protón) se observó una disminución a 2ppm correspondiente a los tres protones (-CH3) del grupo acetilo en comparación con el quitosano de partida, indicativo de la deacetilación llevada a cabo. En el espectro de IR, se representan los espectros de quitosanos de media viscosidad sometidos a diferentes condiciones de deacetilación, y se observa que la banda correspondiente a la interacción del carbonilo (-C=O) presenta menos intensidad, mientras que la banda correspondiente a los grupos de los aminos primarios (-NH2) se incrementa (Esquema 1). Estos resultados permiten deducir que la actividad fúngica viene determinada en un polisacárido derivado de quitosano por la presencia de grupos aminos y su longitud de la cadena.
Esquema 1.- Esquema de síntesis del derivado de quitosano de media viscosidad (polisacárido Ch-D), espectro de protón (1H-RMN) de los polisacáridos Ch-B y Ch-D. Espectro de Infra Rojo (IR) del polisacárido Ch-D variando las condiciones de reacción (ver Métodos)
Actividad antifúngica mediante determinación de Concentración Inhibitoria Mínima (CIM) del polisacárido Ch-D.
Se determinó la Concentración Inhibitoria Mínima (CIM) del derivado Ch-D, que fue el que presentó la mejor actividad antifúngica frente a las cepas de Candida. Como controles se usó voriconazol, fluconazol y como control negativo alginato (Tabla 3).
Tabla 3.- Valores de Concentración Inhibitoria Mínima (CIM) para fluconazol, voriconazol, alginato como controles y el polisacárido Ch-D derivado del quitosano de media viscosidad tratado en medio básico frente a cepas de C. glabrata ECET 1448, C. krusei ATCC 6258 y C. parasilopsis ATCC22019 .
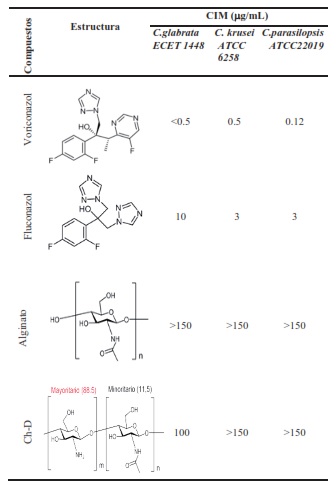
De los resultados obtenidos tras determinar la actividad antifúngica de diferentes oligosacáridos por el método de difusión agar y por la concentración inhibitoria mínima (CIM), se puede concluir que oligosacáridos no funcionalizados con grupos aminos no presentan actividad antifúngica y aun así dependen a su vez del tipo de organismo tratado. Por el contrario, compuestos oligosacáridos de peso molecular medio con alta concentración de grupos aminos, como el derivado de quitosano Ch-D, presenta una actividad antifúngica que puede ser considerada a futuro.
Actividad de compuestos activos sobre formación de biopelículas.
Ensayos con enzimas hidrolíticas.
Existe numerosa evidencia científica que muestra cómo Candida spp se adhiere. al soporte acrílico de las prótesis dentales formando biopelículas. Normalmente se ubica en la mucosa del paladar debajo de la superficie de la prótesis superior, ocasionando estomatitis. En este estudio se investigó el efecto que ejercen las enzimas hidrolíticas sobre estas biopelículas generadas por la especie C. glabrata en diferentes tiempos de su formación (al inicio y en estadio intermedio). Las enzimas usadas en nuestro ensayo fueron; N-Acetil-P-manosaminidasa, a-glucosidasa (hidroliza glucosas con enlace tipo alfa) Tipo-1, N-Acetil-P-galactosaminasa, Neuraminidasa (hidroliza ácido siálico de la membrana celular), lisozima (hidroliza N-acetilmurámico-P 1,4-N-acetil-D-glucosamina) y trehalasa (hidroliza glucosa-a 1,1-glucosa).
Dichas enzimas se probaron con 11 biopelículas generadas de aislados de C. glabrata de prótesis dentales. Se estudió la concentración de la enzima (12,5ug/ml a 50 ug/ml), así como su efecto a diferentes tiempos de formación, ya que como es sabido son parámetros clave (etapa temprana y madura).
De todas las enzimas estudiadas sólo la lisozima presentó buena actividad reductora de biopelículas generadas por C. glabrata (Figura 4). La lisozima específicamente hidroliza los enlaces P-l,4-glicosídicos de disacáridos tipo N-acetilmurámico/N-acetilglucosamina en la composición de los peptidoglicanos presentes en la pared celular.
El estudio in vitro del efecto de la concentración de la lisozima (12,5ug/ml, 25ug/ml y 50ug/ml) sobre las 11 muestras de prótesis dentales que generaban biopelículas y C. glabrata de la CECT como control a 37°C en Sabouraud medio, en el cual se llevó a cabo, tal como ha sido descrito para el caso de Candida albicans (Sebaa et al. 2017). La biomasa de la biopelícula se cuantificó sobre un soporte de poliestireno de 96 pocillos por tinción con violeta de genciana. Así, el efecto reductor de biopelículas por esta enzima se realizó a dos tiempos distintos, al inicio de la formación de biopelículas (OD620nm del cultivo de 0.5, t=0h) reduciendo en este caso la formación de las biopelículas para la cepa de C. glabrata a una concentración de 50ug/ml con un efecto (0,28 ± 0.07 - 0.78 ± 0.03 BBU) inferior al efecto de la caspofungina a una concentración de 2ug/ml (0.93 BBU ± 0.03) (control positivo) con un valor de p<0.0001 siendo estadísticamente significativas. Y otro ensayo consistió en la adición de la lisozima en una etapa intermedia de las biopelículas (a OD620nm 1.5 t=24h) a una concentración de 50 ug/ml redujo las biopelículas (0,28 ± 0.06 - 0,62 ± 0.03 BBU) en un 25 % con un efecto igual o mayor al control positivo de la caspofungina (0.56 ± 0.17 BBU) con un valor p<0,05 siendo estadísticamente significativo el efecto de la enzima a diferentes concentraciones sobre las biopelículas de cepas clínicas y la cepa de referencia. (Figura 4).
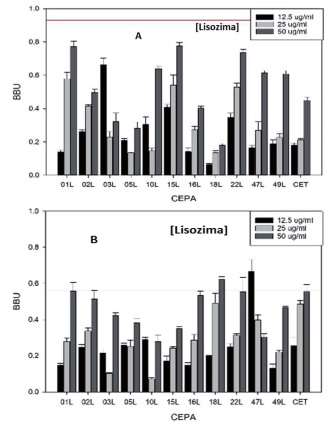
Figura 4.- Actividad reductora de biopelículas generadas por C. glabrata en 11 muestras de prótesis dentales usando lisozima a dos tiempos (A t=0 y B t=24h) y a diferentes concentraciones (50ug/ml, 25ug/ml y 12,5ug/m).Control de cepa C. glabrata (CECT 1448).
Estos resultados están en concordancia con los datos presentados por Sebaa y colaboradores, donde demuestran que las concentraciones <30ug/ml de lisozima son capaces de reducir la biopelícula generada por la adhesión tanto de la cepa control C. albicans (ATCC 10231) como las biopelículas generadas por las cepas clínicas. Nuestros resultados muestran que la adición de esta enzima en concentraciones superiores a 5ÜLig/ml sobre biopelículas ya formadas en superficies de resinas acrílicas, podría ser un buen tratamiento para la eliminación de las mismas.
Discusión
La C. glabrata se ha convertido en el patógeno emergente en personas mayores reconociéndole como el agente causal de la candidiasis oral, tal como se ha demostrado en la literatura. El problema que presenta el uso de fluconazol u otros antifúngicos en clínica se debe a que C. glabrata presenta resistencia y sensibilidad disminuida frente a este antifúngico.
De las 81 muestras obtenidas de adultos mayores residentes en hogares de acogida de la ciudad de Sucre (Bolivia) 37 de ellas eran portadoras de prótesis dentales colonizadas por cepas de C. glabrata y el 45,7% presentó candidiasis subprotésica. Por otro lado, el 29,7% de las cepas de C. glabrata fueron generadoras de biopelículas. Estos datos confirman la importancia de C. glabrata en un alto número de prótesis orales colonizadas por la especie C. glabrata, siendo la responsable de la mayoría de los casos presentes de candidiasis en estos individuos.
El perfil de susceptibilidad del polisacárido Ch-D, derivado de quitosano de media viscosidad, evidenció la mayor actividad antifúngica con la cepa de C. glabrata, mientras que el polisacárido de alginato, aun siendo un polímero similar al quitosano (no contiene grupos aminos), no presentó actividad antifúngica. La actividad del oligosacárido Ch-D podría explicarse a que dicho polímero pudiera estar actuando sobre la membrana celular mediante una interacción electrostática con los fosfolípidos de la membrana cargados negativamente (bacterias y hongos) (Verlee et al. 2017). En cambio los polisacáridos de condroitin, los cuales presentan grupos sulfatos y ácidos (cargas negativas) no presentan actividad fúngica (Palma - Guerrero et al 2010, Marquez et al. 2013). Por otro lado, gracias a las propiedades de biodegradabilidad y no toxicidad que presentan los polímeros de quitosano hacen al polisacárido Ch-D de media viscosidad un buen candidato para ser usado frente a la cepa de C. glabrata en clínica (Cheung et al. 2015). Estos resultados son coincidentes con lo descrito en la literatura donde estudios realizados sobre el potencial antifúngico de nano partículas de quitosano (o quitosan) en solución sobre Colletotrichum fragariae y Candida albicans evidencian que las concentraciones de 50 y 75 ug/ml impidieron el crecimiento del hongo filamentoso (Constantini et al., 2018) e inhibe la formación de la biopelícula en un 90% probablemente debido a que impiden la adhesión de la levadura al cambiar la hidrofobicidad del medio (Costa et al. 2017). Para el caso de los compuestos derivados de aminoglicósidos, neamina y estreptamina, aunque presentan un alto grado de grupos aminos son mono y disacáridos, es decir una longitud de cadena muy corta y quizás eso explicaría la ausencia de actividad frente a Candida. Por ello, al diseñar un antifúngico debería tenerse en cuenta longitudes de cadena largas y alto grado de grupos aminos.
La lisozima, ya descrita en la literatura como agente antimicrobiano, resultó ser una buena biomolécula como agente reductor de biopelículas generadas por C. glabrata en estado intermedios (tiempo de adición 24h) en prótesis dentales a una concentración de 50|j,g/ml, presentando valores de actividad mejores al que presenta la caspofungina utilizada como control. Los mecanismos de resistencia en biopelículas aún no están completamente comprendidos, por ello la disponibilidad de nuevas biomoléculas, en combinación con enzimas pudiera ser una buena alternativa de evitar la formación de biopelículas de C. glabrata en prótesis dentales o de su reducción una vez formadas.
El mecanismo por el cual la lisozima actúa en la pared de la levadura no está bien dilucidado (Raglan y Criss 2017) pero se podrían postular tres supuestos:(a) hidrólisis enzimática de los enlaces de los monosacáridos (N/O-glicosídicos) que forman los polisacáridos y las proteínas estructurales de la pared celular del hongo resultando en la lesión de la membrana citoplasmática y/o (b) posible deterioro de la membrana plasmática externa seguido por una activación de varias enzimas (quitin sintetasa, manasa sintetasa) que son las responsables de codificar los componentes de la pared de la levadura y/o (c) propiedades de aglutinamiento tal como han defendido algunos autores en la literatura (Sebaa et al. 2017, Ellepola et al. 2018).
Finalmente, nuestro estudio aporta evidencia de una buena actividad antifúngica del CH D sobre C. glabrata, y a la lisozima en la reducción de biopelícula de esta especie de Candida. Ambas moléculas, podrían ser a futuro, una buena alternativa para tratamiento de prótesis colonizadas con C. glabrata y evitar la aparición de candidiasis subprotésica.
Consideraciones éticas
El comité de Ética Nacional en Bolivia aprobó los protocolos de toma de muestra y directrices para la participación segura de los adultos mayores en hogares de acogida de la ciudad de Sucre, Bolivia. Se realizó el consentimiento informado a los adultos, personal de salud y tutores previo a la toma de muestra, precautelando la salud de los participantes y llevó a cabo los ensayos laboratoriales.
Agradecimientos
Este trabajo se ha podido llevar a cabo gracias al apoyo de fondos propios del autor y financiamientos externos: Laboratorio de Microbiología de la Carrera de Enfermería (UMRPSFXCH) destinado al aislamiento e
identificación de cepas C. glabrata Laboratorio Del Programa de Microbiología (Universidad de Chile) perfil de resistencia de las cepas y el Proyecto iCOOP (Refe. COOPB20237) para realizar los ensayos de los compuestos en el laboratorio de Química Orgánica General del Consejo Superior de Investigaciones Científicas de Madrid (España).
Abreviaturas
CLSI: Global laboratory standards for a healthier world. htpps://clsi.org/
EUCAST: The European Committee an Antimicrobial Susceptibility Testing. htpps://eucast.org/
CECT: Colección Española de Cultivos Tipo. htpps://cect.org/
ATCC: American Type Culture Collection. htpps://atcc.org/
CIM: Concentración Inhibitoria Mínima.
Bibliografía
Benito-Arenas R, Doncel-Pérez E, Fernández-Gutiérrez M, Garrido L, García-Junceda E, Revuelta J, Bastida A, Fernández-Mayoralas A. A holistic approach to unravelling chondroitin sulfation: Correlations between surface charge, structure and binding to growth factors. Carbohydr Polym. 2018, 15;202:211-218. doi: 10.1016/j.carbpol.2018.08.120. [ Links ]
Cinquin B, Lopes F. Structure and Fluorescence Intensity Measurements in Biofilms. Methods Mol Biol. 2019;2040:117-133. doi: 10.1007/978-1-4939-9686-5-7 [ Links ]
Constantini R, Ventura-Aguilar RI, Hernàndez-López M, Bautista- Baños S, Barrera-Necha LL. Antifungal potential of chitosan nanoparticles and cranberry extract against Colletotrichum fragariae in strawberry. Rev Iberoamericana de Tecnología Postcosecha 2018; 19(1). [ Links ]
Costa EM, Silva S, Veiga M, Vicente S, Tavaria FK, Pintado ME. Investigation of chitosan's antibacterial activity against vancomycin resistant microorganisms and their biofilms. Carbohydr Polym. 2017 Oct 15;174:369-376. doi: 10.1016/j.carbpol.2017.06.087. [ Links ]
Cheung, R., Ng, T., Wong, J., & Chan, W. Chitosan: An update on potentialbiomedical and pharmaceutical applications. Marine Drugs, 2015, 13,5156. [ Links ]
Ellepola ANB, Dassanayake RS, Khan Z. Impact of Brief Exposure to Drugs with Antifungal Properties on the Susceptibility of Oral Candida dubliniensis Isolates to Lysozyme and Lactoferrin. MedPrincPract2018; 27: 523-530. DOI: 10. 1159/000493391. [ Links ]
Fernández M.E. Tesis "Estudio de la formación de biopelículas de Candida spp. y evaluación de nuevas combinaciones farmacológicas". Universidad de Navarra, Facultad de Ciencias, España. 2017. Directores: Dr. José Luis del Pozo León y Dra. Emilia Cantón Lacasa [ Links ]
Gary W. Procop, CLSI, M44Ed3E, Method for Antifungal DiskDiffusion Susceptibility Testing ofYeasts, 3rdEdition, 2018. ISBNnumber: 978-1-68440-030-0) [ Links ]
Gómez J, Gómez -Lu M, BAS P, Ramos C, Cafini F, Maestre J, et al. ¿Es la cuantificación del biofilm un elemento diferenciador en la patogenia de bacilos gramnegativos? Revista Española de Quimioterapia. 2013; 26(2). [ Links ]
Ibáñez N.G, Bonilla CR, Ayala JL. Frecuencia de candidiasis oral asociada al uso de prótesis dentales en pacientes de la Clínica Odontológica de la Universidad Anáhuac Norte. Medigraphic. 2017 Mar; 74(2), 74-78. [ Links ]
Kovács R, Bozó A, Gesztelyi R, Domán M, Kardos G, Nagy F, Tóth Z, Majoros L. Effect of caspofungin and micafungin in combination with farnesol against Candida parapsilosis biofilms. Int J Antimicrob Agents. 2016 Apr; 47(4):304-10. doi: 10.1016/j.ijantimicag.2016.01.007. [ Links ]
Lyu X, Zhao C, Yan ZM, Hua H. Efficacy of nystatin for the treatment of oral candidiasis: a systematic review and meta-analysis. Drug Des Devel Ther. 2016;10: 1161-71. doi: 10.2147/DDDT. [ Links ]
Marquez GI., Akuaku, J., Cruz, I., Cheetham, J., Golshani, A., & Smith, M. L. Disruption of protein synthesis as antifungal mode of action bychitosan. International Journal of Food Microbiology, 2013, 164, 108-112. http://dx.doi.org/10.1016/j.ijfoodmicro.2013.03.025. [ Links ]
Millsop JW, Fazel N. Oral candidiasis. Clin Dermatol. 2016 Jul-Aug;34(4):487-94. doi: 10.1016/j.clindermatol.2016.02.022. [ Links ]
Negrea P, Caunii A, Sarac I, Butnariu M. Digest Journal of Nanomaterials and Biostructures 10, 4, October - December 2015, p. 1129 - 1138. https://ad-astra.ro/2016/05/05/the-study-of-infrared-spectrum-of-chitin-and-chitosan-extract-as-potential-sources-of-biomass/. [ Links ]
O'Toole GA, Kolter R. Initiation of biofilm formation in Pseudomona florescens WCS365 proceeds via múltiple, convergent signalling pathways: a genetic analysis. Molecular Microbiology. 1998 May; 28, 3. doi: 10.1046/j. 1365-2958.1998.00797. [ Links ]
Palma-Guerrero, J., López-Jimenez, J. A., Perez-Berna, A. J., Huang, I. C., Jansson, H.B., Salinas, J. Membrane fluidity determines sensitivity of filamentous fungi to chitosan. Molecular Microbiology, 2010, 75, 1021-1032. https://doi.org/10.111 1/j.1365-2958.2009.07039.x [ Links ]
Pereira CA, Toledo BC, Santos CT, Pereira ACB, Back-Brito GN, Kaminagakura E, Cardoso Jorge AO. Opportunistic microorganisms in individuals with lesions of denture stomatitis. Diagnostic Microbiology and Infectious Disease 76 (2013) 419-424. http://dx.doi.org/10.1016/j.diagmicrobio.2013.05.001 [ Links ]
Pereira A.G.B, Muniza E.C, Hsiehb Y-L. 1H NMR and1H-13C HSQC surface characterization of chitosan-chitinsheath-core nanowhiskers. Carbohydrate Polymers 123 (2015) 46-52.https://doi.org/10.1016/j.carbpol.2015.01.017. [ Links ]
Ragland SA, Criss AK. From bacterial killing to immune modulation: Recent insights into the functions of lysozyme. PLoS Pathog 2017, 13(9): e1006512.https://doi.org/10.1371/journal.ppat.1006512 [ Links ]
Rodrigues CF, Rodrigues ME, Silva S, Henriques M. Candida glabrata Biofilms: How Far Have We Come? JFunji. 2017 Mar; 3 (1 doi: 10.3390/jof3010011). [ Links ]
Rodrigues C, Gonçalves B, Rodrigues M, Silva S, Azeredo J, Henriques M. The Effectiveness of Voriconazole in Therapy of Candida glabrata's Biofilms Oral Infections and Its Influence on the Matrix Composition and Gene Expression. Mycopathologia. 2017 Aug; 182, 7-8. doi: 10.1007/s1 1046-017-0135-7. [ Links ]
Ruan S, Lee LJYH. Candida glabrata fungaemia in intensive care units. Clinical Microbiology and Infection. 2008 Feb; 14(2 DOI: 10.1111/j.1469-0691.2007.01892.x). [ Links ]
Saggu SK, Jha G, Mishra PC. Enzymatic Degradation of Biofilm by Metalloprotease From Microbacterium sp. SKS10. Front Bioeng Biotechnol. 2019 Aug 7;7:192. doi: 10.3389/fbioe.2019.00192. [ Links ]
Sebaa S, Hizette N, Boucherit-Otmani Z, Courtois P. Dose-dependent effect of lysozyme upon Candida albicans biofilm. Mol Med Rep. 2017 Mar;15(3):1135-1142. doi:10.3892/mmr.2017.6148. [ Links ]
Smyth J, Mullen C, Jack L, Collier A, Bal A. Diabetes, malignancy and age as predictors of Candida glabrata bloodstream infection: A re-evaluation of the risk factors. Journal Mycologi Medical. 2018, Sep, 28, 3. doi 10.1016/j.mycmed.2018.05.004). [ Links ]
Tiraboschi I, Pozzi N, Farías L, García S, Fernández N. Epidemiology, species, antifungal resistance and outcome of candidemia in a university hospital in Buenos Aires, Argentina for 16 years. Revista Chilena Infectologia. 2017 Oct;34(5 doi: 10.4067/S0716-10182017000500431) [ Links ]
Tantivitayakul P, Lapirattanskul J, Kaypetch R, Muadchiengka T. Missense mutation in CgPDR1 regulator associated with azole-resistant Candida glabrata recovered from Thai oral candidiasis patients. Journal Global Antimicrobial Resistence. 2019 Jan; 15(19 doi: 10.1016/j.jgar.2019.01.006.). [ Links ]
Verlee A, Mincke S, Stevens CV. Recent developments in antibacterial and antifungal chitosan and its derivatives. Carbohydr Polym. 2017 May 15; 164:268-283. doi:10.1016/j.carbpol.2017.02.001. [ Links ]
Wiederhold NP. The antifungal arsenal: alternative drugs and future targets. Int J Antimicrob Agents. 2018 Mar; 51 (3) : 333-339. doi: 10. 1016/j.ijantimicag. 2017. 09.002. [ Links ]
Zárate SG, Bastida A, Santana AG, Revuelta J. Synthesis of Ring II/III Fragment of Kanamycin: A New Minimum Structural Motif for Aminoglycoside Recognition. Antibiotics (Basel). 2019 Aug 2;8(3). pii: E109. doi: 10.3390/antibiotics8030109. [ Links ]














