Journal of the Selva Andina Research Society
versão On-line ISSN 2072-9294
J. Selva Andina Res. Soc. vol.8 no.2 La Paz 2017
Artículo Original
Inoculación de Trichoderma harzianum en Zea mays y su efecto a la adición del fertilizante nitrogenado al 50%
Inoculation of Trichoderma harzianum on Zea mays its effect on the addition of nitrogen fertilizer at 50%
Tavera-Zavala Dulce Daniela1, Hernández-Escareño Jesús Jaime2, Ulibarri Gérard3, Sánchez-Yáñez Juan Manuel1*
1Laboratorio de Microbiología Ambiental, Instituto de Investigaciones Químico Biológicas. Ed-B3 C.U. Universidad Michoacana de San Nicolás de Hidalgo, Morelia, Mich, México.
2Microbiología y Micología Veterinarias. Facultad de Medicina Veterinaria y Zootecnia. Universidad Autónoma de Nuevo León. Av. Francisco Villa S/N, Ex Hacienda “El Cánada”, Escobedo, N.L. México.
3Department of Chemistry and Biochemistry, Lauretinan University 935 Rasmey Lake Rd Suddbury, Ontario P3E2C6. Canada.
*Dirección de contacto: Laboratorio de Microbiología Ambiental, Instituto de Investigaciones Químico Biológicas. Ed-B3 C.U. Universidad Michoacana de San Nicolás de Hidalgo, Morelia, Mich, México.
Juan Manuel Sánchez–Yáñez
E-mail address: syanez@umich.mx
Historial del artículo.
Recibido Diciembre, 2016.
Devuelto mayo 2017
Aceptado junio, 2017.
Disponible en línea, agosto, 2017.
Resumen
El cultivo de Zea mays (maíz) normalmente requiere de fertilizante nitrogenado (FN), comúnmente aplicado como NH4NO3 (nitrato de amonio), el que en exceso provoca la pérdida de productividad del suelo. En Z. mays una alternativa de solución para la reducción y optimización de la dosis del FN es la inoculación con una dosis de esporas y micelio de Trichoderma harzianum que lo facilite. El objetivo de esta investigación fue analizar el efecto de 3 dosis de T. harzianum en Z. mays al 50% del FN. El experimento se realizó en un invernadero bajo un diseño experimental de bloques al azar, con 5 tratamientos, 5 repeticiones, mediante las variables-respuesta fenología: altura de planta (AP) y longitud radical (LR) y biomasa: peso fresco y seco aéreo/radical (PFA/PFR)/ (PSA/PSR) a plántula y floración, los datos experimentales se validaron por Tukey al 0.05%. Los resultados mostraron que ciertas dosis de inoculo de T. harzianum en Z. mays causaron un efecto positivo en la germinación con un 92% valor numérico estadísticamente diferente al 81% en Z. mays sin inocular al 100% de FN o control relativo (CR). A plántula Z. mays con T. harzianum a la dosis 40 g/100 g de semilla registró un PSA de 0.32 g, un PSR de 0.25 g valores numéricos estadísticamente diferentes a los 0.21 g de PSA, 0.19 g de PSR de Z. mays con el FN al 100% o CR. A floración hubo un efecto positivo de 40 g de T. harzianum/100 g de semilla con 1.98 g de PSA y 1.29 g de PSR: ambos valores numéricos fueron estadísticamente diferentes a los 1.65g de PSA y 1.00 g PSR de Z. mays con el FN al 100% o CR. Lo anterior sugiere que la dosis de inoculo T. harzianum tuvo el suficiente número de propagulos viables para transformar los exudados de semilla y raíz en sustancias promotoras del crecimiento vegetal (SUPOCEVE); para que no obstante la reducción del NH4NO3 al 50% se haya optimizado por el Z. mays sin afectar su sano crecimiento.
Palabras clave: Suelo, fertilizante nitrogenado, Z. mays, fenología, T. harzianum, fitohormonas.
Abstract
The crop Zea mays (maize) requires nitrogen fertilizer (NF) usually as NH4NO3 (ammonium nitrate), which applied in excess causes loss of productivity in soil. An alternative to reduce and optimize the dose of NF in crop Z. mays is to inoculate it with Trichoderma harzianum. The main objective was to analyze the effect of three doses of T. harzianum in Z. mays at 50% of NF. This experiment was performed in a greenhouse under an experimental design of random blocks, with 5 treatment and 5 replicates, the response variables used were: phenology: seedling height (SH) and root length (RL), and biomass: aerial and radical fresh/dry weight (AFW/ADW)/(RFW/RDW) at seedlings and flowering stage, the experimental data were analyzed by Tukey 0.05%. The results showed a positive effect of the specific density of all viable structures of T. harzianum in Z. mays since was observed 92% of seed germination, numerical value statistical difference to the 81% in Z. mays without inoculum and NF at 100% or relative control (RC). At seedling Z. mays with T. harzianum 40 g/100 g seeds registered an ADW of 0.32 g and a RDW of 0.25 g, these values were statistical different to the 0.21 g of ADW, and 0.19 g of RDW in Z. mays without inoculum and fed with NF at 100% or RC. The above mentioned suggests that T. harzianum transform seed and root exudates in plant growth promoting substances (PGPS), optimizing the use of NH4NO3 and allowing its reduction until 50% without causing a nutritional deficit on normal Z. mays growth.
Key words: Soil, nitrogen fertilizer, Z. mays, phenology, T. harzianum, phytohormones.
Introducción
En la producción mundial de la gramínea Zea mays (maíz), se necesita fertilizante nitrogenado (FN) como factor principal limitante de su crecimiento, el FN más común es el NH4NO3 (nitrato de amonio), ya que es esencial en la síntesis de ácidos nucleicos y proteínas en la división celular que dará origen a la formación de tejidos vegetales, siendo uno de los principales elementos del rendimiento, formación y llenado del grano en la mazorca de Z. mays, generalmente el FN se da manera no regulada en función a la demanda de N (nitrógeno), de la variedad, tipo de suelo, si el sistema es de riego o temporal. La dosis del FN normalmente excede la cantidad que el cultivo vegetal necesita para un sano crecimiento, por lo que el N que no se absorbe, en suelo ocasiona pérdida de productividad (Forest et al. 2013). Una solución alternativa que evita la hiperfertilización nitrogenada y optimiza la absorción del FN en Z. mays es la inoculación con microorganismos promotores de crecimiento vegetal (MPCV), los más conocidos son de los géneros y especies bacterianos del tipo: Azospirillium, Azotobacter, Bacillus, Burkholderia, (Bashan & Levanony 1990, Bashan et al. 1996). Así como micorrizas vesículo arbusculares principalmente el género Glomus hoy llamado Rhizopagus inoculado en Z. mays, ya sea de manera individual o en combinación con algunos otros géneros bacterianos señalados (Valdivia-Urdiales et al. 1999). Con resultados variables en la respuesta positiva de Z. mays al decremento del FN entre el 10 al 50%, sin embargo existe una inconsistencia en el efecto benéfico de estos microorganismos promotores del crecimiento vegetal, en Z. mays por diversas razones: incompatibilidad de éstos con la especie vegetal, agentes fitopatógenos que impiden su acción favorable (Bolan 1991, Van Cleemput & Hera 1996). Mientras que en los general Trichoderma harzianum, frecuentemente se ha utilizado como agente de control biológico contra hongos y bacterias fitopatógenas (Benítez et al. 2004, Rawat & Tewari 2011). Aunque con mínima información sobre el empleo de T. harzianum como facilitador de la regulación y optimización de FN en cultivos básicos del tipo de Z. mays (da Silva Lima et al. 2014), a pesar de la evidencia de que podría convertir exudados de semilla y raíces en sustancias promotoras del crecimiento vegetal (SUPOCEVE) como: auxina, giberelina o citocininas que inducen la formación de un mayor número de raíces laterales, que en consecuencia aumentan la capacidad de absorción del FN, al reducir esta dosis y no obstante se optimice (Ortiz-Castro et al. 2009, Candelero et al. 2015, Romero-García et al. 2016). Tal como lo señalan Cubillos-Hinojosa et al. 2009 quienes reportaron la acción benéfica de T. harzianum en la germinación y crecimiento temprano de Passiflora edulis (maracuyá) en invernadero, mediante la síntesis SUPOCEVE en las raíces de esta planta. Mientras que López et al. 2010 reportaron el efecto positivo de T. harzianum en Z. mays en su fenología y biomasa mediante la conversión de los exudados de semilla en SUPOCEVE. De la misma forma Akladious & Abbas 2012 investigaron la acción favorable de T. harzianum al generar ácido indol acético (AIA) en Z. mays que le indujo un mayor crecimiento de la longitud radical, así como aumento en el peso seco total, con un sistema radical mejor en la absorción del FN. Candelero et al. 2015 registraron que la inoculación de T. harzianum en semillas de Capsicum chinense (chile) incrementó su peso seco aéreo (PSA), y en la altura de plata (AP), se demostró que este hongo transformó los exudados de raíz; como el triptófano en auxina para mejorar la absorción del FN. A pesar de lo anterior, es escasa la información en la literatura sobre la regulación y optimización del FN en Z. mays con base en la dosis T. harzianum empleada al decrecer la cantidad del FN aplicado en esta gramínea. Por lo anterior el objetivo de este trabajo fue analizar el efecto de la inoculación de 3 dosis de Trichoderma harzianum en el crecimiento de Zea mays a dosis 50% del FN.
Materiales y métodos
Condiciones ambientales en el invernadero para observar el efecto de Trichoderma harzianum en Zea mays. Esta investigación se realizó en el invernadero del laboratorio de Microbiología Ambiental del Instituto de Investigaciones Químico Biológicas de la UMSNH, Morelia, Mich, México. La temperatura promedio fue de 23.2 °C, luminosidad de 450 μmol·m-2·s-1, humedad relativa de 67%. Para este ensayo se utilizó un suelo no estéril colectado de un sitio ubicado a los 19º 39 27 de latitud norte 100º 19 59 de longitud oeste, con una altitud de 1820 msnm de clima templado en un terreno agrícola denominado La cajita de la Tenencia Zapata del municipio de Morelia, Mich., México sobre el Km 5 de la carretera Morelia-Pátzcuaro, Mich, México. El suelo del experimento se colecto de un terreno agrícola ubicado a los 19º 39 27 de latitud norte 100º 19 59 de longitud oeste, con una altitud de 1820 msnm de clima templado. Las propiedades del suelo determinadas fueron: pH 6.02 moderadamente ácido, con un 3.58% o bajo contenido de materia orgánica, con 26.64 C mol (+) Kg-1 una alta capacidad de intercambio catiónico, con una textura clasificada según FAO como franco-arcillosa. Este suelo se solarizó a 70 °C/48 h para minimizar el problema de plagas y enfermedades. Mientras en el invernadero se aplicaron plaguicidas de baja toxicidad y cultivos vegetales trampa para evitar el ataque por plagas y enfermedades vegetales (Morales et al, 2009).
Inoculación de Zea mays con Trichoderma harzianum. En esta fase del ensayo previa a la inoculación de Z. mays (semilla certificada donada por el Ministerio de Agricultura de México (SAGARPA) con T. harzianum, que se obtuvo de la colección del laboratorio de Microbiología Ambiental del Instituto de Investigaciones Químico Biológicas de la UMSNH, y que fue aislada de madera en descomposición (Romero-Garcia et al 2016). Lo primero que se estableció fue la cantidad de propágulos viables del hongo, por la técnica de cuenta viable en placa en agar papa dextrosa agar, con el uso de solución salina y detergente como liquido de dilución, así como la concentración de propágulos de T. harzianum de cada dosis: 20, 30 y 40 g /100 g de semillas, (contenía 4 x 106 unidades formadoras de propagulos o UFP/g de inoculo) según se describe en Sánchez-Yáñez (2007). La semilla de Z. mays se desinfectaron con hipoclorito de sodio (Clorox®) 0.6%/2.5 min, se enjuagaron 6 veces con agua estéril, luego se desinfectaron con alcohol 70%/5 min, se enjuagaron 5 veces con agua estéril, entonces por cada 100 g de semillas de Z. mays se inocularon con 20, 30 y 40 g de T. harzianum (Romero-García et al. 2016) cultivadas en las jarras de Leonard por 62 días.
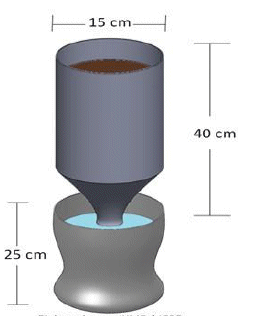
Siembra de Zea mays inoculado con Trichoderma harzianum. En esta etapa del ensayo 1.0 kg de suelo se colocó en el contenedor superior del sistema jarra de Leonard (Figura 1) mientras que el FN o el agua, se colocó, en el reservorio de la parte inferior, ambas partes se conectaron por una tira de algodón de 20 cm. El FN con NH4NO3 en concentración 1.0 y 0.5 g/L, en acuerdo con la concentración recomendada para Z. mays en la región (Vallejo et al. 2004), el pH del FN se ajustó 6.8-7.0 g/L.
Figura 1. Diseño de una jarra de Leonard (Garcia-González et al. 1995)
En la tabla 1 se describe el diseño experimental, que consistió en 5 tratamientos con 5 repeticiones, el ensayo se realizó en 62 días. En el que se sembraron semillas de Z. mays irrigadas solo con agua o control absoluto (CA), semillas alimentadas con el FN a dosis del 100% o control relativo (CR), para este tratamiento se aplicó el fertilizante conocido como ULTRASOLMR. Por lo que por cada 100 g semillas de Z. mays se inocularon con las 3 dosis de T. harzianum: 20 g, 30 g y 40 g: y alimentaron con el 50% del FN, para medir lo anterior se emplearon las siguientes variables respuesta: porciento (%) de germinación y días a emergencia, 30 días posteriores a la siembra, en Z. mays se midió la fenología, la biomasa aérea como radical, con una regla calibrada para la altura de planta (AP) y la longitud radical (LR), para la biomasa aérea y radical se determinó el peso fresco aéreo (PFA) y radical (PFR) con una balanza electrónica, para el peso seco aéreo (PSA) y (PSR) se secaron en horno a 70°/48 h y se pesaron, a floración 60 días después de medir el estadio de plántula. Los datos experimentales se analizaron por Tukey HSD P<0.05% con el programa estadístico Statgraphics Centurión (Romero-García et al. 2016).
Tabla 1. Diseño experimental para analizar el efecto de 3 dosis de Trichoderma harzianum en Zea mays con NH4NO3 al 50 %

(+) = agregado, (-) = no agregado; 1n=5
Resultados
En la tabla 2 se muestra el porcentaje (%) de germinación y los días a emergencia de la semilla de Z. mays, con 40 g de T. harzianum/100 g de semilla, ahí registró un valor de 92%, estadísticamente diferente comparado con el 91% de germinación en Z. mays sin inocular e irrigada solo con agua o CA, comparado con el 81% de la germinación observado en Z. mays a la dosis 100% del FN o CR, en relación a los días a emergencia, el menor tiempo se detectó en las semillas irrigadas solo con agua con 10.2 días, valor estadísticamente diferente a la semilla con T. harzianum 20 g/100 g de semillas en 10.9 días, mientras que con 30 g/100 g de semilla se registró a 11.15 días, en tanto que con 40 g de T. harzianum/100 g de semilla se registraron 11.0 días.
Tabla 2. Efecto de la inoculación de 3 dosis de Trichoderma harzianum sobre el porcentaje de germinación y los días a emergencia de la semilla de Zea mays al 50% de NH4NO3

*Letras distintas indican diferencia estadística al 0,05% según Tukey. **Señalan el error STD.
La tabla 3 muestra el efecto de T. harzianum en la fenología y biomasa de Z. mays a los 30 días posteriores a la siembra, con la dosis 40 g/100 g de semilla que indujo una AP de 37.59 cm, una LR de 25.59 cm, un PFA de 4.09 g, un PFR de 3.84 g, un PSA de 0.32 g, un PSR de 0.25 g estos valores numéricos con diferencia estadística comparados con Z. mays sin inocular e irrigado solo con agua con una AP de 34.44 cm, una LR de 20.63 cm, un PFA de 2.45 g, un PFR de 1.63 g, un PSA de 0.20 g, un PSR de 0.15 g, en tanto con la dosis 40 g T. harzianum/100 g de Z. mays se observó una diferencia estadística comparada con la AP de 34.34 cm y la LR de 19.94 cm, con un PFA de 2.59 g, un PFR de 1.98 g, un PSA de 0.21 g y un PSR de 0.19 g en Z. mays sin inocular y alimentado con el FN al 100%.
Tabla 3. Efecto de la inoculación de 3 dosis de Trichoderma harzianum en la fenología y biomasa de Zea mays a plántula al 50% de NH4NO3
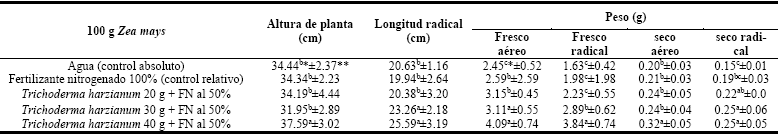
*Letras distintas indican diferencia estadística al 0,05% según Tukey. **Señalan el error STD.
La tabla 4 muestra el efecto de T. harzianum sobre la fenología y biomasa de Z. mays a los 60 días después de la siembra, donde con 40 g/100 g de Z. mays registro una AP de 67.13 cm, una LR de 27.38 cm, un PFA de 18.69 g, un PFR de 11.59 g, un PSA de 1.98 g y un PSR de 1.29 g, mientras que con 30 g de T. harzianum/100 g de semilla se registró una AP de 70.50 cm, una LR de 31.38 cm, un PFA de 18.39 g, un PFR de11.71 g, un PFA de 1.93 g, un PSR de 1.41 g, todos estos valores fueron estadísticamente diferentes a la AP de 56 cm, la LR de 18.50 cm, con un PFA 9.39 g, PSR de 4.38 g, PSA de 1.14 g y PSR de 0.58 g registrados en Z. mays sin inocular e irrigado solo con agua o CA y a la AP de 62.63 cm y LR de 21.38 cm, al PFA de 13.34 g, un PFR de 6.99 g, un PSA de 1.65 g, un PSR de 1.00 g en Z. mays alimentado con el 100% del FN o CR.
Tabla 4. Efecto de la inoculación de 3 dosis de Trichoderma harzianum en la fenología y biomasa de Zea mays a floración al 50% del NH4NO3 a los 62 días después de la siembra
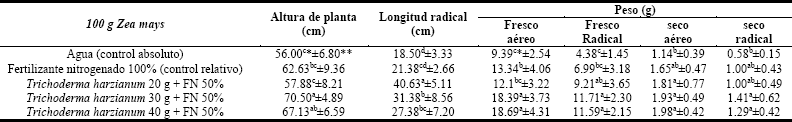
*Letras distintas indican diferencia estadística al 0.05% según Tukey. **Señalan el error STD.
Discusión
Los valores de porcentaje de germinación reportados en la Tabla 2 sugieren que la concentración 40 g T. harzianum/100 g Z. mays estimuló una germinación dependiente de la conversión de exudados de semilla ciertos aminoácidos aromáticos que ha sido identificados en los exudados del 98% de las variedades de Z. mays (Schiltz et al. 2015) en SUPOCEVE, las cuales están estrechamente asociadas con la germinación de semillas, al interrumpir su condición fisiológica de latencia (Harman et al. 2004, Sadsk et al. 2016). Esto se apoya también por el análisis que se ha hecho de las enzimas que se activan durante la germinación de semillas, ya que algunas de las que participan en el 99% de los hechos registrados en la germinación, degradan la capa que recubre el endospermo de la semilla, lo que facilita la emergencia del primordio del tallo y raíz (Kucera et al. 2005). Los valores de la fenología y biomasa observados en la Tabla 3 apoyan que el incremento en la AP, en la LR de Z. mays con 40 g T. harzianum /100 g de semilla en la etapa de plántula, muestran indirectamente la conversión exudados de las raíces de Z. mays para la generación de SUPOCEVE, lo que mejoro la absorción y optimización del FN reducido al 50%, que dio lugar a un crecimiento sano (Ortuño et al. 2013), de la misma manera, la ganancia en la biomasa fresca como seca de Z. mays lo que indirectamente indica que, T harzianum reconoce algunos de los principales compuestos orgánicos que la raíz de la gramínea libera, durante su crecimiento, y que el hongo convierte en ciertas tipos de hormonas que mejoran su capacidad de absorción radical del N, a pesar de reducir la dosis del FN. La conversión de los exudados de la raíz de Z mays en SUPOCEVE, dio como resultado un mayor número de raíces primarias laterales (Himanen et al. 2002, Gupta et al. 2014), que favorecieron una mayor área de exploración radical, para optimizar al máximo el FN reducido al 50 % (Forde & Lorenzo 2001, Harman et al. 2004, Gravel et al. 2007, Rawat & Tewari 2011, Akladious et al. 2012). Los resultados de la fenología y biomasa registrados en la Tabla 4 indican que la inoculación de Z. mays con las dosis 30 y 40 g de T. harzianum/100 g de semilla incrementaron tanto la AP como la LR en etapa de floración, esto sugiere que T. harzianum transformó algunos compuestos orgánicos derivados de la fotosíntesis de Z. mays en SUPOCEVE del tipo auxina, para favorecer una mayor elongación del tallo, con una acelerada y mayor formación de raíces laterales, con ello hubo una mejor exploración en el suelo, lo que hizo eficiente absorción de FN reducido al 50% (Forde & Lorenzo 2001, Gravel et al. 2007, Candelero-De la Cruz et al. 2015, Romero-García et al. 2016). Las dosis 30 y 40 g T. harzianum /100 g de Z. mays causaron una respuesta positiva en el sistema radical de Z. mays, de tal manera que indirectamente se registraron cambios en las densidad del sistema radical, en el peso fresco y seco, en la altura de la planta, en la dimensiones de la hojas, lo que la literatura explica como efectos derivados de la síntesis de SUPOCEVE por T. harzianum (Gupta et al. 2014), y aunque la densidad de la población del hongo solo de determino al inicial con 40 x 106 UFP/g de raíces de plántula de Z. mays y finalizar con 400 x 106 UFP/g de raíces al final el ensayo. Hecho que no se registró en el Z. mays usado como CA y/o CR; lo cual implica que el incremento en el área de exploración radical (Gupta et al. 2014), que derivó en un aumento en la optimización de la absorción del FN reducido al 50%, mostrado por el evidente sano crecimiento de Z. mays, en comparación con las misma variables respuesta de Z. mays (CR y/o CA). Mientras que también fue evidente que la densidad y la cantidad de inoculante a base de los propagulos de T. harzianum con la mayor dosis empleada de 40g/100 g de semilla de Z. mays, apoya el argumento de que la sensibilidad de estos propagulos a los factores físicos (luz solar, temperatura del suelo), químicos: pH, y biológicos: como la competencia nativa antagonista y depredadores de T. harzianum que disminuyen sus formas viables responsables del efecto positivo en la raíz de Z. mays. Lo anterior indica que una elevada concentración de propagulos de T. harzianum fue necesaria, para logar el resultado positivo mostrado en el sano crecimiento de Z. mays, en contraste con lo observado en Z. mays usado como CR sin inocular pero alimentado con el 100% del FN y en el usado como CA, y que fue avalado por la diferencia estadística , mientras que también se demostró que es posible reducir la dosis de FN sin causar problemas nutricionales en los primeros estadios de su crecimiento, fundamentales para un producción rentable, de un cultivo agrícola de importancia doméstica como Z.mays. En la agricultura convencional, en la protegida como en la orgánica el empleo de T harzianum se ha limitado a un agente de control biológico de hongos y bacterias fitopatógenas, esta investigación apoya su papel como HOPOCEVE en la producción de Z. mays bajo un esquema que busque optimizar el FN, reducido a un nivel que no ponga en riesgo el sano crecimiento de esta gramínea. Con base a los resultados la dosis 40 g de T. harzianum/ 100 g Z. mays fue suficiente para registrar un efecto positivo, que involucra la conversión de los exudados de semilla y raíz en SUPOVECE, demostrado indirecta mente por la fenología y biomasa del crecimiento sano del sistema radical Zea mays con lo que se evita la perdida de fertilidad del suelo y la posible contaminación ambiental al minimizar la cantidad de FN libre en el suelo.
Conflictos de intereses
Los autores de este artículo, declaramos que no existe ningún conflicto de interés en la planificación, ejecución y redacción de la investigación realizada, como con aquellas personas e instituciones que económicamente apoyaron.
Agradecimientos
Al proyecto 2.7 (2017) de la Coordinación de Investigación Científica de la Universidad Michoacana de San Nicolás de Hidalgo, Morelia, Mich, México y a BIONUTRA S.A. de C.V., Maravatio, Michoacán, México.
Literatura citada
Akladious SA, Abbas SM. Application of Trichoderma harziunum T22 as a biofertilizer supporting maize growth. Afr J Biotech 2012; 11:8672-83. [ Links ]
Bashan Y, Holguín G, Ferrera-Cerrato R. Interacción entre plantas y microorganismos benéficos. I. Azospirillum. Terra Latinoam 1996; 14: 159-94. [ Links ]
Bashan Y, Levanony H. Current status of Azospirillum inoculation technology: Azospirillum as a challenge for agriculture. Can J Microbiol 1990; 36(9):591-608. [ Links ]
Benítez T, Rincón AM, Limón MC, Codón AC. Biocontrol mechanisms of Trichoderma strains. Int Microbiol 2004; 7(4):249-60. [ Links ]
Bolan NS. A critical review on the role of mycorrhizal fungi in the uptake of phosphorus by plants. Plant Soil 1991; 134:189-207. [ Links ]
Candelero-De la Cruz J, Cristóbal-Alejo JRA, Reyes-Ramirez A, Tun-Suarez JM, Gamboa-Angulo MM, Ruiz-Sánchez SE. Trichoderma spp promotoras del crecimiento en plántulas de Capsicum chinense Jacq. y antagónicas contra Meloidogyne incognita. Phyton 2005; 84(1):113-9. [ Links ]
Candelero-De la Cruz J, Cristóbal-Alejo JRA, Reyes-Ramírez A, Tun-Suárez JM, Gamboa-Angulo MM, Ruíz-Sánchez E. Trichoderma spp. promotoras del crecimiento en plántulas de Capsicum chinense Jacq y antagónicas contra Meloidogyne incognita. Phyton 2015; 84:113-9. [ Links ]
Cubillos-Hinojosa J, Valero N, Mejía L. Trichoderma harzianum como promotor del crecimiento vegetal del maracuyá (Passiflora edulis var. flavicarpa Degener). Agron Colomb 2009; 27(1):81-6. [ Links ]
da Silva-Lima L, Lopes-Olivares F, Rodrigues de Oliveira R, García-Vega MR, Oliveira-Aguiar N, Pasqualoto-Canellas L. Root exudate profiling of maize seedlings inoculated with Herbaspirillum seropedicae and humic acids. Chem Biol Technol Agric 2014; 23: 1-18. [ Links ]
Forde B, Lorenzo H. The nutritional control of root development. Plant Soil 2001; 232: 51-68. [ Links ]
Forest I, Reichb PB, Tilman D, Hobbie SE, Polasky S, Binder S. Nutrient enrichment, biodiversity loss, and consequent declines in ecosystem productivity. Proc Natl Acad Sci USA 2013; 110(29):11911-6. [ Links ]
García-González MM, Sánchez-Yáñez JM, Peña-Cabriales JJ, Moreno Z. Respuesta de maíz (Zea mays L.) a la inoculación de bacterias fijadoras de nitrógeno. Terra Latinoam 1995; 13:71-80. [ Links ]
Gravel V, Antoun H, Tweddel RJ. Growth stimulation and fruit yield improvement of greenhouse tomato plants by inoculation with Pseudomonas putida or Trichoderma atroviride: Possible role of indole acetic acid (IAA). Soil Biol Biochem 2007; 39(8):1968-77. [ Links ]
Gupta VK, Schmoll M, Herrera-Estrella A, Upadhyay RS, Druzhinina I, Tuohy MG. Biotechnology and biology of Trichoderma. Ed. Elsevier. Poland; 2014. p. 415-25.
Harman GE, Howell CR, Viterbo A, Chet I, Lorito M. Trichoderma species-opportunistic, avirulent plant symbionts. Nat Rev Microbiol 2004; 2(1):43-56. [ Links ]
Himanen K, Boucheron E, Vanneste S, de Almeida EJ, Inzé D, Beeckman T. Auxin-mediated cell cycle activation during early lateral root initiation. Plant Cell 2002; 14(10):2339-51. [ Links ]
Kucera B, Cohn MA, Leubner-Metzger G. Plant hormone interactions during seed dormancy release and germination. Seed Sci Res 2005; 15: 281-307. [ Links ]
López Y, Pineda JB, Hernández A, Ulacio D. Efecto diferencia de seis aislamientos de Trichoderma sobre la severidad de Rhizoctonia solani, desarrollo radical y crecimiento en las plantas de maíz. Bioagro 2010; 22(1):37-42. [ Links ]
Morales RV, Garay RB, Romero, HA. Sánchez-Yáñez, JM. Insecticidas biológicos en el control de insectos plaga: agrícolas, forestales, de almacén y urbanas en México. [Consultado 20 abril 2017]. Disponible en: http.www.mono grafias.com. [ Links ]
Ortiz-Castro R, Contreras-Cornejo HA, Macías-Rodríguez L, López-Bucio J. The role of microbial signals in plant growth and development. Plant Signal Behav 2009; 4(8):701-12. [ Links ]
Ortuño N, Miranda C, Carlos M. Selección de cepas de Trichoderma spp generadoras de metabolitos secundarios de interés para su uso como promotor de crecimiento en plantas cultivadas. J Selva Andina Biosph 2013; 1:16-32. [ Links ]
Rawat R, Tewari L. Effect of abiotic stress on phosphate solubilization by biocontrol fungus Trichoderma sp. Curr Microbiol 2011; 62(5): 1521-6. [ Links ]
Romero-García VE, García-Ortiz VR, Hernández-Escareño JJ, Sánchez-Yáñez JM. Respuesta de Phaseolis vulgaris a microorganismos promotores de crecimiento vegetal. Scientia Agropecuaria 2016; 7:313-9. [ Links ]
Sadsk KS, Flah HI, Ekhlas AEK. Effect of Gibberellic acid and Trichoderma spp. efficiency on seeds germination, speed percentage, the activity of Peroxidase and Amylase enzyme of two eggplant (Solanum melongena) Hybrids. Int J Multidiscip Curr Res 2016; 4:1112-4. [ Links ]
SAGARPA. Sistema Nacional de Certificación de Semillas, www. gob.mx. [ Links ]
Sánchez-Yáñez J.M. Breve tratado de microbiología agrícola, teoría y práctica, Ed. Instituto de Investigaciones Químico-Biológicas. Universidad Michoacana de San Nicolás de Hidalgo. COSUSTENTA, SA de CV, CIDEM, SEDAGRO. Morelia, Mich., México; 2007. p. 111.
Schiltz S, Gaillard I, Pawlicki-Jullian N, Thiombiano B, Mesnard F, Gontier E. A review: what is the spermosphere and how can it be studied? J Appl Microbiol 2015; 119(6):1467-81. [ Links ]
Valdivia-Uridales B, Fernández-Brondo JM, Sán chez-Yáñez JM. Efecto de la co inoculación de Pseudomonas putida y Glomus spp sobre trigo. Rev Latinoam Microbiol 1999; 41:231-7. [ Links ]
Vallejo-Delgado LH, Ramirez-Diaz JL, Chuela-Bonaparte M, González-Iñiguez RM. Tecnología para producir maíz en el bajío michoacano. Campo Experimental, Uruapan. CIRPAC. 2004. Folleto para productores de maíz Num3. Uruapan Michoacán, México; 2004. p. 32.
Van Cleemput O, Hera C. Fertilizer nitrogen use and efficiency in different cropping systems. Terra Latinoam 1996.14:40-58. [ Links ]
______________











 uBio
uBio