Journal of the Selva Andina Research Society
versão On-line ISSN 2072-9294
J. Selva Andina Res. Soc. vol.8 no.1 La Paz 2017
Artículo Original
Población fúngica en suelos productores de quinua (Chenopodium quinoa Willd), bajo diferentes sistemas de manejo en la comunidad Kerecaya Municipio de Salinas de Garci Mendoza
Fungal population in soils producing quinoa (Chenopodium quinoa Willd), under different management systems in the community Kerecaya Municipality of Salinas de Garci Mendoza
Paco-Pérez Victor1*, Loza-Murguia Manuel2,3, Vino-Nina Lourdes1, Calani-Bueno Eusebio1, Serrano-Canaviri Teófilo1
1Universidad Católica Boliviana San Pablo - UCBSP. Unidad Académica Campesina Tiahuanacu UAC-T. Ingeniería Agronómica. Km 74. Carretera Internacional La Paz-Desaguadero. Tel +591-2-2895100. La Paz, Bolivia.
2Universidad Católica Boliviana San Pablo - UCBSP, Unidad Académica Campesina Carmen Pampa-UAC-CP, Ingeniería Agronómica. Coroico-Nor Yungas-La Paz, Bolivia. +591(2)8781991.
3Departamento de Enseñanza e Investigación en Bioquímica & Microbiología-DEI&BM. Unidad Académica Campesina Carmen Pampa-UAC-CP.
*Dirección de contacto: Unidad Académica Campesina Tiahuanacu UAC-T. Ingeniería Agronómica. Km 74. Carretera Internacional La Paz-Desaguadero. Tel +591-2-2895100. La Paz, Bolivia
Víctor Paco-Pérez E-mail address: vicpaco@hotmail.es
Historial del artículo.
Recibido febrero, 2015.
Devuelto noviembre 2015
Aceptado noviembre, 2016.
Disponible en línea, febrero, 2017.
Resumen
La comunidad de Kerecaya (3700-4000 msnm) del municipio de Salinas de Garci Mendoza del altiplano Sur de Bolivia, pese a sus riesgos climáticos, el productor valora un suelo pobre para su subsistencia. Las parcelas de quinua presentan materia orgánica inferior a 093%, humedad del suelo menor a 12.9%, temperatura del suelo por debajo de 8.5 oC y pH inferior a 8.0. Se estudió la población de hongos en tres tipos de suelos que fueron: sin labranza (puruma), tradicional y mecanizado. Las muestras húmedas del suelo se recolectaron a una profundidad de 6 a 25 cm al azar en zig-zag, estas fueron procesadas mediante el método de dilución seriado e inoculadas en placas con 0.5 mL y se evaluó las colonias por método UFC´s/g de suelo, el género de Penicillium spp., con mayor población de 65.1%, seguido por Aspergillus spp., con 24.1% y Trichoderma spp., con menor abundancia de 13.8% y la población promedio en UFC´s/g de suelo fue de 1035.4 en sin labranza (puruma), 959.7 en tradicional y 868.2 en el mecanizado y la mayor población se presentó en el mes de febrero de 1572.8 UFC´s/g de suelo. Con estos datos se requiere investigar otros parámetros que influyen en la comunidad microbiana en esta comunidad.
Palabras clave: UFC´s, Penicillium, Aspergillus, Trichoderma, Salinas de Garci Mendoza.
Abstract
The Kerecaya community (3700-4000 msnm) of the municipality of Salinas of Garci Mendoza of the south altiplano of Bolivia, in spite of your climatics risks. The plots of quinoa present lower organic matter to 0.93%, humidity of the smaller earth to 12.9%, temperature of the earth for under 8.5 oC and pH lower to 8.0. The population of funguses in three types it has studied of earths that went: without farm (without entropic intervention), traditional and mechanized. The humid samples of the earth were gathered to a depth of 6 to 25 cm at random in zig-zag, these to be prosecuted by means of the method of seriate dilution and inoculated in plates with 0.5 mL and it is evaluated the colonies for UFC´s/g of earth, the genre of Penicillium spp., with major population of 65.1%, followed for Aspergillus spp., with 24,1% and Trichoderma spp., with minor great quality of 13,8% and the population average in UFC´s/g of earth it went of 1035.4 in without farm (without entropic intervention), 959.7 in traditional and 868.2 in the mechanized and the major population was presented in the month of February 1572.8 UFC/g of earth.
With this data, it is necessary to investigate other parameters that influence the microbial community in this community.
Key words: UFC’s, Penicillium, Aspergillus, Trichoderma, Salinas de Garci Mendoza.
Introducción
Los hongos se presentan generalmente como finos filamentos, constituyen un grupo muy numeroso de organismos que presentan una amplia distribución en la naturaleza, contribuyendo a la descomposición de la materia orgánica y participando en los ciclos biológicos. Se han descrito aproximadamente 500 000 hongos, pero se estima que pueden existir entre 1 y 1.5 millones de especies, un pequeño número son patógenos de animales y plantas (Aristegui 2002).
Su distribución en el suelo está determinado por la disponibilidad de materia orgánica, son considerados como saprofitos, es decir, que crecen en tejidos muertos, realizan la descomposición de la materia orgánica, generalmente se encuentran en la capa superior del suelo. Su función básica es la descomposición y mineralización de los residuos orgánicos frescos o recién incorporados al suelo (Medel 2006).
Producen enzimas y metabolitos que contribuyen al ablandamiento y a la transformación de sustancias orgánicas, también metabolizan compuestos carbonados de muy difícil degradación como la celulosa, hemicelulosa y la lignina (Coyne 2000, Benzina et al. 2001).
La microbiota en los suelos cultivados se incrementa con los años de descanso. La fertilidad del suelo está controlada por las actividades biogeoquímicas de la microbiota que actúa como abastecedor potencial de nutrientes para las plantas (Silva de Carry & Angulo 2006).
Al igual que los otros organismos, son un componente vital en el funcionamiento de los ecosistemas, contribuyendo en el desarrollo de poblaciones vegetales y animales, siendo capaces de poseer vida latente por periodos largos soportando condiciones adversas (Herrera 2000).
Las simbiosis con micorrizas, es decir, las asociaciones entre hongos-raíces de plantas, varían según la clase del hongo y plantas involucradas. En esta asociación, la planta proporciona los compuestos carbonados, procedentes de la fotosíntesis, al hongo heterotrófico. Por otro lado, los hongos derivan agua y minerales esenciales del suelo que después de pasar por los tejidos fúngicos, son incorporados a los tejidos de la planta (González & Valenzuela 1993).
Los grupos importantes de hongos que se encuentran en el suelo son: Zigomycota, Ascomycota, Deuteromycota y Basidiomycota. La mayoría se aíslan del suelo, son generalmente los géneros: Penicillium, Geotrichum, Aspergillus y Trichoderma que pertenecen a deuteromicetos (Benzina et al. 2001).
Las raíces de las plantas están pobladas de hongos, algunos de estas movilizan nutrientes minerales hacia las raíces de las plantas, aumentan la capacidad de retener agua en sequía, fijan nitrógeno y fósforo, protegen a raíces de fitopatógenos por espacio liberando sustancias que los inhiben. Los géneros más importantes asociados a las raíces de las plantas son Aspergillus spp., Penicillium spp., Rhizopus spp., y Trichoderma spp., los dos primeros movilizan el fosforo y nitrógeno del suelo, mientras el ultimo sostiene la humedad en raíces en condiciones de sequía (Benzina et al. 2001, Michael 2006).
El rendimiento de quinua (Chenopodium quinoa Willd) en el año 1999 fue de 630 kg/ha/año en el altiplano Sur de Bolivia, en transcurso de 10 años el rendimiento descendió hasta 558 especialmente en la pampa (Joffre et al. 2011).
El descenso se debe al creciente desarrollo del mercado internacional sobre la demanda de la quinua (Chenopodium quinoa Willd), esta demanda ha llevado a una fuerte presión sobre los suelos productivos del altiplano sur boliviano, los productores se han visto obligados a comprar maquinarias agrícolas para barbechar, sembrar y trillar, reduciendo al mínimo la cobertura vegetal, destruyendo los agregados y la estructura porosa del suelo. Se ha empezado a cultivar en áreas que tradicionalmente estaban destinadas al pastoreo y se han reducido los tiempos de descanso. Esta presión está llevando a un empobrecimiento de los suelos y a una pérdida de fertilidad por extracción de nutrientes. Si bien la quinua puede crecer y producir en suelos áridos con muy poco contenido en nutrientes, en esas condiciones los rendimientos son bajos, disminuyendo así los ingresos de los productores.
En este trabajo se plantea la búsqueda de identificar géneros de hongos en suelos con manejo tradicional, mecanizado y sin labranza (puruma) y comparar la población de hongos por tipo de manejo en siete meses de evaluación.
Materiales y métodos
Ubicación geográfica. El presente trabajo de investigación se realizó en la comunidad de Kerecaya municipio de Salinas de Garci Mendoza de la provincia Ladislao Cabrera al Sur del departamento de Oruro, geográficamente está situada a 19º3815 latitud Sur y 67º4027 longitud Oeste, a una distancia 280 km de la ciudad de Oruro y a una altitud de 3759 msnm (Vallejos-Mamani et al. 2011).
Características agroecológicas. El municipio de Salinas de Garci Mendoza, está compuesto de suelos arenosos y salinos aproximadamente 40% de planicie con erosión eólica frecuente. Se pueden encontrar procesos volcánicos, dando origen a serranías, montañas, mesetas y colinas. En las geomorfías de procesos fluvio lacustres, que han producido terrenos más productivas como llanuras aluviales y las llanuras de piedemonte volcánicas (PIEB 2010).
Clima. La zona de estudio corresponde al tipo semiárido con fríos extremos secos en invierno. El ciclo hidrológico está caracterizado por época seca y fría en los meses de marzo a noviembre y la época lluviosa de diciembre a febrero. La temperatura media anual es de 8.9 ºC, la máxima 18.7 ºC y la mínima de -2.9 ºC; la precipitación media anual de 150 a 300 mm (FAUTAPO 2008).
Suelos. Las zonas productoras de quinua real en el altiplano sur del país presentan suelos con contenido de sales y varían de textura (arenosos, arena francoso y arenosos arcillosos) con pH modernamente alcalino en su mayoría. Asimismo, los problemas de erosión eólica son frecuentes, lo cual, da lugar a una de las regiones más áridas de Bolivia con una alta vulnerabilidad ecológica (Vallejos-Mamani et al. 2011).
Se ejecutaron en tres fases i) Fase de campo, ii) Fase de laboratorio, iii) fase de gabinete.
Encuesta a productores de quinua (Chenopodium quinoa Willd). La información fue construida mediante la aplicación de entrevistas al azar con la ayuda de un formulario de apoyo semiestructurado, con preguntas cerradas y abiertas a 32 productores de la comunidad de Kerecaya,
Se eligieron tres parcelas con mayor homogeneidad de manejo tradicional, mecanizado y también se identificaron tres áreas del suelo sin labranza (puruma) para la recolección de las muestras de suelo, luego se visitó a las parcelas seleccionadas personalmente para verificar la homogeneidad.
Medición de temperatura del suelo. Para determinar la temperatura del suelo, se utilizó un geotermómetro de suelo Arias-Cifuentes & Piñeros-Espinosa (2008). En cada parcela de quinua (Chenopodium quinoa Willd) con manejo tradicional, mecanizado y en suelo sin labranza (puruma), se tomaron seis puntos de medición de la temperatura del suelo en un esquema de zig-zag, se limpiaron los primeros 5 cm de la superficie del suelo y luego se ha introducido el geotermómetro a una profundidad de 20 cm aproximadamente durante un tiempo de 5 min, pasado este tiempo se registró el valor de la temperatura.
Recolección de muestras. Se recolecto las muestras del suelo húmedo en cada mes de evaluación una sola vez a las 11:30 am de agosto 2012 hasta febrero 2013 en parcelas de quinua (Chenopodium quinoa Willd) en descanso (campaña agrícola de gestión 2011-2012) con manejo tradicional, mecanizado y en suelos sin labranza (puruma), Bautista et al. (2011). Para la recolecta, se limpiaron los primeros 5 cm de la superficie y a partir de 6-25 cm de la capa arable se recolecto las muestras con pala en un esquema de zig-zag. En cada parcela se seleccionó tres puntos de muestreo, en cada punto de muestreo se tomó con cinco submuestras. Las submuestras se mezcló homogéneamente y se cuarteo en cuatro, una cantidad aproximadamente de 200 g se llevó al laboratorio de Centro de Investigación de la Quinua de Salinas de Garci Mendoza en frascos estériles herméticamente cerrados y correctamente identificados, las muestras fueron procesadas en laboratorio el mismo día.
En el mes de septiembre se recolectaron las muestras de los tres tipos de suelos con cantidades de aproximadamente de 500 g con los pasos mencionados anteriormente y se enviaron al laboratorio de Servicios Analíticos-Laboratorio Químico (Espectrolab) de la Universidad Técnica de Oruro (UTO) para determinar la materia orgánica.
Determinación de pH del suelo. Para determinar el pH de las muestras del suelo, se siguió las normas mencionadas por la FAO (2009). Se pesaron de cada muestra 10 g de suelo y se mezclaron con 25 mL de agua destilada en un vaso precipitado estéril de 250 mL, luego se ha introducido el electrodo del pH-metro, posteriormente se registró el valor de pH.
Determinación de humedad del suelo. Para determinar el porcentaje de humedad de las muestras del suelo, se realizó por diferencia entre peso húmedo y peso seco Santana (2011), se hizo pasar las muestras del suelo por un tamiz de 1.5 mm para descartar las piedras pequeñas y material vegetal de mayor diámetro, luego se pesaron 50 g (peso inicial) en balanza analítica y se depositaron en un sobre de papel sabana para luego introducir a la estufa a una temperatura de 105 oC durante 48 h, pasado este tiempo se volvieron a pesar (peso final).
II. Fase de Laboratorio.
Preparación y esterilización de medios de cultivo. Los medios de cultivo se han preparado y esterilizado de la siguiente manera: se diluyeron en 500 mL de agua destilada según la referencia indicada en su etiqueta y se ajustó el pH a 5.6 para Agar Papa-Dextrosa (PDA), Agar Sabouraud (AS) a 6.0 con solución buffer.
Dilución seriada del suelo. Las diluciones seriadas del suelo se realizaron dentro de la cámara de flujo laminar. Las muestras del suelo se hicieron pasar por un tamiz estéril de 1.5 mm para descartar piedras pequeñas y material vegetal de mayor tamaño para luego preparar una solución patrón del suelo, para lo cual, se añadió 10 g de suelo en 90 mL de agua destilada estéril y se agito por 10 min (solución patrón 1:10), de esta solución se tomó 1 mL con la pipeta y se mezcló con 9 mL de agua destilada estéril en un tubo de ensayo, se suspende a la solución 1:100, se repitió este paso hasta obtener la dilución deseada.
Inoculación de las diluciones a las placas. Las manipulaciones para inoculación de las diluciones a las placas, se realizaron dentro de la cámara de flujo laminar. Se tomó con la pipeta 0.5 mL de las diluciones 10-3, 10-4 y 10-5 y se extendió en las cajas Petri con (PDA) solidificado con tres repeticiones por dilución y por muestra de suelo para después incubar las placas a la estufa de cultivo a una temperatura de 28 oC durante 5 días, luego se evaluó y se tomó la decisión de trabajar con la dilución de 10-3 con tres repeticiones por muestra de suelo. Se descartó las diluciones 10-4 y 10-5 por lo que no formaron colonias.
Conteo de unidades formadoras de colonias (UFC´s). El conteo de UFC´s se realizó dentro de la cámara de flujo laminar, pasados 5 días de incubación, se contaron detalladamente las UFC´s de hongos formadas en las placas con PDA.
Aislamiento de las UFC´s por estriado. El aislamiento de las UFC´s, se realizó dentro de cámara de flujo laminar, que consiste en separar las UFC´s en PDA, se esterilizó la asa de siembra al rojo vivo en mechero bunsen, luego se dejó enfriar sobre una caja Petri estéril para luego tomar una pequeña muestra de las UFC´s e inocular en nuevas cajas Petri con AS por el método de estría de cuatro cuadrantes para después encubar las placas a la cámara de incubadora a una temperatura de 28 oC durante 5 días, posteriormente se volvió a aislar nuevamente las UFC´s por estriado con los pasos ya mencionados, este método se repitió hasta obtener colonias puras de las especies de hongos.
Tinción de las muestras. Se realizaron las tinciones con los colorantes de azul lactofenol y violeta genciana para que permita distinguir con facilidad las características morfológicas de los hongos en el microscopio, se cubrió con una pequeña gota de azul de lactofenol en algunos casos y en otras con violeta genciana al centro del portaobjeto con el gotero, con la ayuda de cinta adhesiva transparente se tocó a la UFC´s del hongo e inmediatamente se pegó sobre la gota de colorante del porta objeto para después observar al microscopio localizando con el objetivo de 10X, posteriormente pasando al de 40X y por ultimo con el objetivo de 100X para poder ver la morfología del hongo.
Cálculo del porcentaje de humedad del suelo. En la determinación de los porcentajes de humedad de las diferentes muestras del suelo, Santana 2011, Aguilera et al. 2001, que mencionan después del secado de las muestras en la estufa a una temperatura de 105 oC durante 48 h se calcula con la siguiente fórmula:
![]()
Cálculo del promedio de la temperatura del suelo. Se calcularon los promedios de las temperaturas con la siguiente expresión:
![]()
Cálculo de UFC´s/ g de suelo. Se determinaron con la ecuación propuesta por Santana (2011).
![]()
Donde:
UFC g-1 = Unidades formadores de colonias por gramo de suelo
ΣC = Suma de las colonias contadas en las placas
d = Factor de dilución utilizado para inoculación a las placas
s = Cantidad de suelo (g) utilizado en la dilución seriado
Análisis estadístico. Para la interpretación de las diferentes variables de respuesta del objetivo se realizó mediante un análisis descriptivo (cualitativo) y se sometió a un análisis de varianza (cuantitativo) Bautista et al., (2011).
Factores de estudio. El factor de estudio (variable independiente) fue los diferentes sistemas de manejo del suelo en producción de quinua (Chenopodium quinoa Willd) y los diferentes meses, corresponde a factores que fueron:
| Factor A: sistemas de manejo de quinua | Factor B: meses | |
| a1: Suelo sin labranza (puruma) a2: Suelo tradicional a3: Suelo mecanizado | b1: Agosto b2: Septiembre b3: Octubre b4: Noviembre | b5: Diciembre b6: Enero b7: Febrero |
Variables de respuesta. Determinación de pH, materia orgánica, humedad del suelo, temperatura del suelo a 20 cm de profundidad.
Descripción macroscópica (forma, color, tamaño y textura) de hongos aislados y desarrollados sobre AS.
Población de hongos en unidades formadores de colonias por gramo de suelo (UFC´s/g de suelo).
Modelo estadístico. Los resultados obtenidos, para su interpretación fueron sometidos a un análisis de varianza (ANVA) con el diseño completamente al azar (DCA) con dos factores utilizando el programa Statistical Analysis System (SAS) versión 9.2 con un nivel de confianza de 95% con el siguiente modelo lineal (Delgado 2013).
![]()
| Donde: |
| |
| Yijk | = | Población fúngica en diferentes manejos del suelo y meses en la ijk –ésima unidad experimental. |
| µ | = | Es la media general. |
| Ai | = | Efecto de la i – ésimo manejo del suelo. |
| Bj | = | Efecto del j – ésimo diferentes meses. |
| ABij | = | Es la interacción de la i – ésimo manejo del suelo y el j – ésimo meses. |
| Eijk | = | Error experimental asociado a la ijk – ésima unidad experimental. |
Resultados
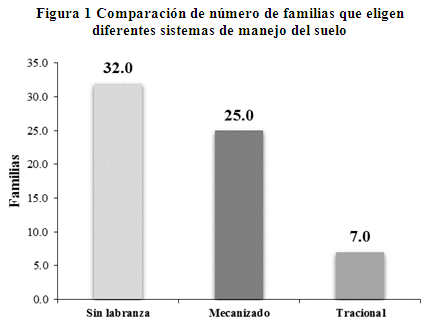
Figura 1 Comparación de número de familias que eligen diferentes sistemas de manejo del suelo
Discusión
Determinación cualitativa de parcelas de quinua (Chenopodium quinoa Willd). Para caracterizar las parcelas de quinua de la comunidad de Kerecaya del municipio de Salinas de Garci Mendoza, 32 productores de quinua, todos los productores cuentan con terrenos sin labranza (puruma) (figura 1), esto es debido a que los productores tienen grandes extensiones de terrenos, 25 realizan prácticas de manejo mecanizado, este sistema eligen especialmente por la facilidad de barbechado y sembrado de quinua en lugares de planicie, 7 familias realizan prácticas de manejo tradicional, este sistema se realiza manualmente en menores superficies con la ayuda de herramientas ancestrales como liukana o taquisa en lugares de laderas y serranías, no se tiene uso de maquinaria agrícola por el difícil acceso a las parcelas, por este motivo la gran mayoría de los productores no optan por este sistema de manejo del suelo.
FAUTAPO (2008), menciona que el sistema de producción mecanizado en cuatro municipios productores de quinua del altiplano Sur de Bolivia es 76.1%, esto es debido a la facilidad de producir en las planicies con maquinaria agrícola y 23.8% manejo tradicional, estos sistema es ancestralmente practicado en lugares de semiladera y ladera que son más adecuados para la producción de la quinua, debido a menor riesgo de heladas, sequias y al ataque de plagas. Estos valores muestran mayor una tendencia al manejo mecanizado, similares a los resultados obtenidos en el presente trabajo, para que la gran mayoría de los productores obtén al sistema mecanizado probablemente se debe a la facilidad de producir grandes extensiones en planicies, por tanto, en algunos municipios los tractores pueden ser utilizados con mayor frecuencia para las actividades de barbecho, siembra y trilla de quinua (Chenopodium quinoa Willd), por otro lado, en otros municipios la maquinaria agrícola probablemente es utilizado con menor frecuencia por la topografía que presentan sus suelos, otra de las causas para la mecanización puede ser por la demanda de la quinua en el mercado que es cada vez mayor.
Soraide-Lozano (2011), menciona que el manejo tradicional se siembra manualmente con la ayuda de taquisa o liukana en lugares de ladera y semiladera, en donde se cava un hoyo hasta encontrar la humedad del suelo, cuya profundidad depende principalmente de la preparación de suelo y de la lluvia oportuna, este sistema es costoso y no se puede sembrar extensiones grandes. Por otro lado, la siembra mecanizado consiste en la utilización del tractor con su implemento de siembra, los productores de quinua de la comunidad de Kerecaya afirman que en manejo tradicional solo se puede sembrar en pequeñas superficies, esto no justifica la demanda de la quinua, esta es la causa para que los productores se vean obligados a que opten por el sistema mecanizado que es fácil de cultivar en grandes dimensiones en lugares de planicie.
Otro estudio realizado por FAUTAPO (2009), afirma que en el municipio de Salinas de Garci Mendoza, el 13% realizan un manejo del suelo tradicional y 87% hacen una labranza mecanizado. Al respecto, los resultados en el presente trabajo son similares con mayor número de familias que se inclinan al manejo mecanizado.
pH en diferentes suelos de quinua (Chenopodium quinoa Willd). En la tabla 1, se observan los valores de pH, en el suelo sin labranza (puruma) 8.0, suelo tradicional 7.9 y 7.8 suelo mecanizado, valores determinados, que corresponden a moderadamente alcalino, característico de las regiones áridas y semiáridas, que presentan sales especialmente de calcio, magnesio y sodio en forma de carbonatos, por lo tanto, el pH del suelo con manejo mecanizado no varía con significancia respecto al suelo sin labranza (puruma) por la presencia de sales que se tiene en la zona.
Según FAUTAPO (2009), indica que los diferentes suelos del altiplano Sur del departamento de Oruro tienen pH ligeramente alcalinos, en llanuras del piedemonte de 3% de pendiente el pH es 8.0, mientras en lugares de serranías de 35% de pendiente el pH es de 7.0. Estos valores son similares a los resultados obtenidos en el presente trabajo, la mínima variación se debe quizás al contenido de sales que existen en el suelo de un lugar a otro.
Vallejos-Mamani et al. (2011), señala que la mayoría de los suelos de la provincia de Ladislao Cabrera presentan pH dentro del rango de moderadamente alcalino de 7.6 a 8.0. Los resultados obtenidos en el presente trabajo muestran estos valores pH, la causa para que los suelos presenten este tipo de pH es debido al ascenso de sales de las capas freáticas a las capas superficiales, principalmente en los meses de alta evapotranspiración (mayo a diciembre).
Materia orgánica en parcelas seleccionadas. En la tabla 2, se observan los valores de materia orgánica de los diferentes suelos en el mes de septiembre 2012, el suelo sin labranza (puruma) presenta 0.93% relativamente superior a los con manejo tradicional y mecanizado, el suelo tradicional con 0.87%, que es inferior al suelo sin labranza (puruma), pero superior al suelo con manejo mecanizado y finalmente el suelo con manejo mecanizado contiene 0.69% de materia orgánica que es inferior a los suelos sin labranza (puruma) y tradicional.
La materia orgánica de estos suelos muestra contenidos muy bajos, probablemente se deba a la presencia de poca vegetación, bajas precipitaciones y extremas temperaturas de la zona. Por lo tanto, la poca materia orgánica que contiene los suelos de planicie, es reducida con la introducción de maquinaria agrícola, ya que los abonos que se incorporan a las parcelas, una parte de las partículas finas son erosionados por el viento en el momento de labores como barbechado, rastrado y siembra.
Miranda et al. (2009), menciona que los suelos de la comunidad de Irpani contienen 0.78% de materia orgánica a una profundidad de 0 a 20 cm de capa arable, distante a 10 km aproximadamente de la comunidad de Kerecaya. Según los valores obtenidos de materia orgánica en el presente trabajo de investigación son similares y se clasifica como suelos de muy baja fertilidad. La causa para que estos suelos tengan muy bajo contenido de materia orgánica, probablemente se debe a las condiciones climáticas adversas de la zona, que influyen en la producción de biomasa y en la descomposición de la materia orgánica, a esto se suma también la práctica del mono cultivo de la quinua y el arrancado desde la raíz en el momento de la cosecha.
Humedad en suelos seleccionados. En la tabla 3, se presentan promedios de humedad desde agosto 2012 a febrero 2013, el contenido de humedad es similar, suelo sin labranza (puruma) 12.9%, relativamente superior a los suelos con manejo tradicional y mecanizado, suelo tradicional 12.8% inferior al suelo sin labranza (puruma), pero superior al suelo mecanizado y finalmente con un promedio 12.6% el suelo mecanizado, que es inferior a suelos sin labranza (puruma) y tradicional. Estos suelos contienen bajos porcentajes de humedad debido a su menor capacidad de retención de agua y por la presencia de materia orgánica muy bajo, por lo tanto, la incorporación de materia orgánica en estos suelos es primordial para la retención de la humedad.
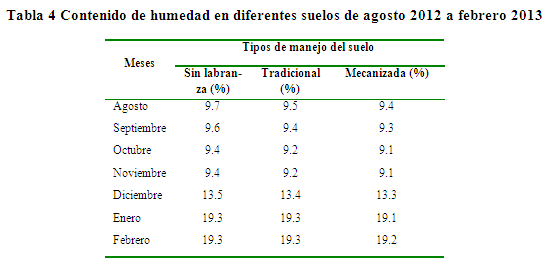
En la tabla 4, el contenido de humedad en diferentes suelos de agosto 2012 a febrero 2013, en los tres tipos de suelo se observa similar comportamiento de humedad, donde relativamente desciende la humedad en los meses de agosto, septiembre, octubre y noviembre, pero en época húmeda (diciembre, enero y febrero) aumenta la humedad del suelo. En los diferentes suelos, la retención de humedad es bajo incluso en los meses de mayor precipitación como enero y febrero, esto se debe a que el agua gravitacional de la lluvia se infiltrada rápidamente por la fuerza de gravedad a napas subterráneas por los poros que presentan estos suelos. La quinua (Chenopodium quinoa Willd) sembrada en los meses de agosto, septiembre, octubre y noviembre sobreviven y se desarrolla con la poca humedad existente, esto se debe a la humedad retenida con poca energía en estos suelos es agua disponible para el cultivo.
Ticona & Bernal (2013), en un estudio realizado en la comunidad de Santiago de Chuvica, del departamento de Potosí a 3686 msnm del altiplano Sur de Bolivia, afirma que la humedad de 0 a 20 cm de profundidad varía entre 5.9 a 6.4%. Los valores logrados de la humedad en el presente trabajo no muestran similar comportamiento en los diferentes suelos especialmente en época seca. Esta diferencia probablemente se debe a la recolecta de las muestras de 6 a 25 cm de profundidad del suelo en el presente trabajo de investigación, por otro lado, para la recolección de muestras se retiró los primeros 5 cm de la superficie del suelo.
PIEB (2010), menciona que la quinua se caracteriza por ser el único cultivo que se adapta a las condiciones ambientales extremas del lugar de Salinas de Garci Mendoza, donde las heladas son de 270 a 330 días al año y la vegetación es pequeña, espinosa y escasa. Los resultados de la humedad del suelo en los diferentes meses en el presente trabajo reflejan evidentemente que la quinua se adapta a condiciones adversas de la zona. Las primeras siembras se realizan en el mes de agosto, donde la humedad en los diferentes suelos es inferior a 9.7%.
Temperatura de la profundidad del suelo. En la tabla 5, los promedios de temperatura a 20 cm de profundidad, se observan similares temperaturas, el suelo sin labranza (puruma) 8.5 oC, relativamente mayor al con manejo tradicional y mecanizado, el tradicional con 8.4 oC, superior al mecanizado, pero inferior al sin labranza (puruma) y el mecanizado con 8.3 oC, que es menor a los sin labranza (puruma) y tradicional.
Las temperaturas a 20 cm de profundidad de estos suelos son bajos, esto se debe a que los suelos de la zona son arenosos y arena francosos, estos suelos tienen poca capacidad de retención de la temperatura por los poros que presenta. En estos suelos, la absorción energética de las radiaciones del sol es rápido y la emisión lo propio.
No se reportan estudios similares, pero FAO (2009), menciona que la temperatura del suelo es primordial para la actividad de los microorganismos en la descomposición y transformación de materia orgánica, con una temperatura de 0 a 5 oC en el suelo es una restricción térmica en el crecimiento de las raíces de la mayoría de especies y la germinación de la mayoría de semillas es imposible. Las temperaturas a 20 cm de profundidad de los diferentes suelos en el presente trabajo son superiores a 8.3 oC, esta es la razón para que la quinua sembrada germine y emerja con la poca humedad existente en el suelo en mes de agosto, donde las temperaturas en la superficie del suelo a un llegan a -11 oC.
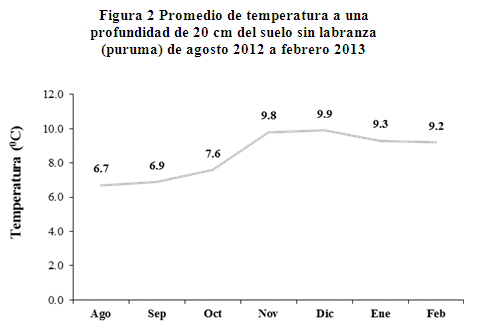
En la figura 2, se presenta los promedios de temperatura de los diferentes meses a una profundidad de 20 cm del suelo sin labranza (puruma), donde se aprecia que la temperatura más baja del suelo es 6.7 oC en el mes de agosto y 9.9 oC en diciembre. Las temperaturas en los meses de enero y febrero son de 9.3 y 9.2 oC respectivamente, inferiores a los meses de noviembre y diciembre, probablemente se debe a las escasas radiaciones del sol por la presencia de precipitaciones en estos meses.
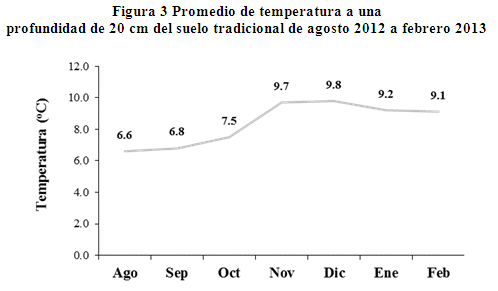
En la figura 3, se observa los promedios de temperatura de los diferentes meses a una profundidad de 20 cm del suelo tradicional, en el cual, en mes de agosto se presenta una temperatura de 6.6 oC y en el mes de diciembre la temperatura es 9.8 oC, las radiaciones del sol son intensos durante el día, cuando las radiaciones del sol son escasas por causa de las precipitaciones en los meses de enero y febrero, las temperaturas llegan a 9.2 y 9.1 oC respectivamente.
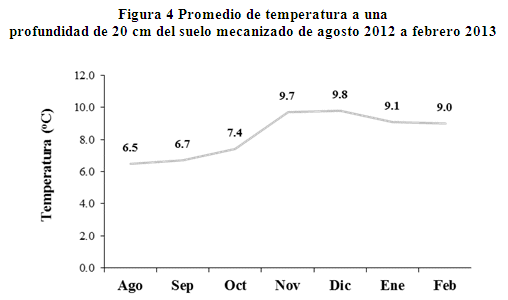
En la figura 4, los promedios de la temperatura de diferentes meses a una profundidad de 20 cm del suelo mecanizado, se observa la temperatura más baja de 6.5 oC en el meses de agosto, las temperaturas mínimas del ambiente llegan a -11 oC, la temperatura más elevada llega a 9.8 oC en diciembre cuando las temperaturas más bajas del ambiente llegan todavía a -2.1 oC y en los meses de enero y febrero donde las precipitaciones se presentan con mayor frecuencia que en otros meses y las radiaciones del sol son escasas por causa de las precipitaciones, las temperaturas del suelo en estas condiciones llegan a 9.1 y 9.0 oC respectivamente.
Coyne (2000), menciona que la sombra y el recubrimiento de las plantas al suelo interceptan la radiación solar, de igual forma el color del suelo también afecta a la temperatura debido al efecto de albedo. Los suelos oscuros presentan un albedo bajo y absorben mayor energía que los suelos claros, la temperatura del suelo depende de la profundidad, donde se puede encontrar en un suelo oscuro de 19 a 35 oC a 10 cm de profundidad, las actividades de microorganismos en estas condiciones son mayores. Los valores de temperaturas en los diferentes meses en el presente trabajo son inferiores a 9.9 oC, esto probablemente se debe a la evaluación a una profundidad de 20 cm, otro de las causas para que las temperaturas del suelo se presenten bajos puede ser por el color claro de los suelos.
SENAMHI, reporta las temperaturas del mes de julio 2012 a marzo 2013 de la localidad de San Martin a 3732 msnm a una distancia 26 km aproximadamente de Salinas de Garci Mendoza, donde afirma que la temperatura máxima llega a 21.8 oC y la mínima -2.6 oC. Estos valores son superiores debido a las lecturas tomadas del ambiente y una altura de 1.5 m de la superficie del suelo, mientras los datos obtenidos en el presente trabajo son tomados a 20 cm del interior de suelo. Aproximadamente existe una diferencia de 2.4 oC entre el suelo y el ambiente en los diferentes meses, esto refleja que el suelo siempre será inferior en cuanto a su temperatura con respecto al ambiente.
Hongos en suelo sin labranza (puruma)
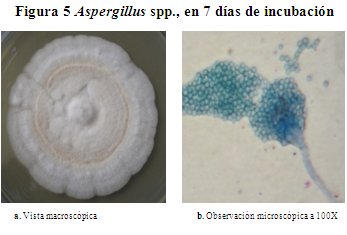
Descripción macroscópica del género Aspergillus spp. En la figura 5, se observa una colonia redonda de hongo Aspergillus spp., desarrollado sobre el AS a 28 oC, la superficie de color blanco al principio y se torna a crema con el pasar del tiempo, forman anillos concéntricos bien pronunciados y con elevación central ligeramente levantada, tiene textura algodonosa de borde irregular, no presenta pigmentación ni exudaciones y no posee coloración en el reverso. Alcanzan un diámetro de 4.9 cm en 7 días de incubación.
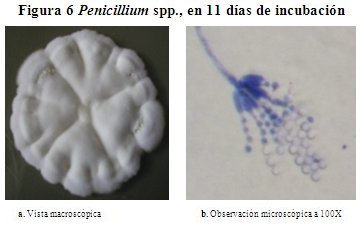
Descripción macroscópica del género Penicillium spp. En la figura 6, se aprecia el hongo Penicillium spp., de colonia redonda desarrollado sobre el AS a 28 oC, presenta color blanco en la superficie con surcadas radiales bien pronunciados, al principio color crema en el reverso con el pasar del tiempo se torna de amarillo, textura yesosa con borde irregular, no tiene pigmentación, pero con pequeñas gotas de exudación de color blanco cristalina. Alcanza en 11 días de incubación un diámetro de 2.1 cm.
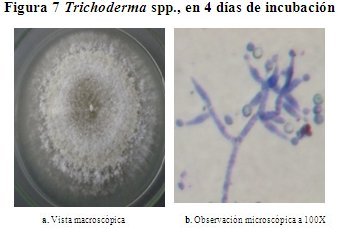
Descripción macroscópica del género Trichoderma spp. En la figura 7, se observa la colonia de hongo Trichoderma spp., desarrollado sobre el AS a 28 oC, la superficie de color blanco con anillos concéntricos de color amarillo ligeramente pronunciada, no presenta elevación central, pero en el reverso tiene un color crema, textura algodonosa sin pigmentación ni exudación, posee borde irregular. Alcanza un diámetro de 6.7 cm en 4 días de incubación.
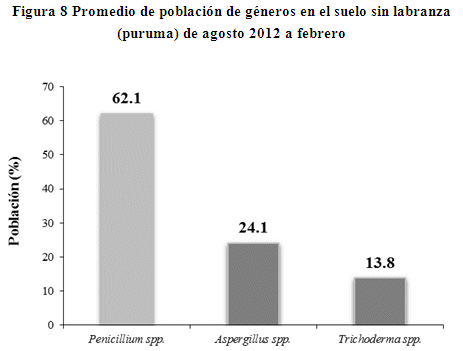
En la figura 8, se muestra los promedios de géneros encontrados en el suelo sin labranza (puruma), donde se observa que el género Penicillium spp., es mayor con una población de 62.1%, Aspergillus spp., con población intermedia de 24.1% y el género Trichoderma spp., con menor población de 13.8%. En los suelos de la comunidad de Kerecaya la mayor población de hongos pertenecen al género de Penicillium spp. En estos suelos la materia orgánica es 0.93%, con promedio de humedad 12.9%, temperatura inferior a 9.9oC a una profundidad de 20 cm del suelo y con un pH de 8.0.
Los géneros de hongos descritos en el presente trabajo de investigación no coinciden con lo mencionado por Condori (2012), afirma que los géneros de hongos del municipio de Salinas de Garci Mendoza, son cuatro (Aspergillius spp., Penicillium spp., Trichoderma spp. y Sporothix spp.) en un estudio realizado en la identificación de hongos en nueve comunidades, donde recolecto las muestras del suelo de septiembre a febrero, en suelos pajonales, tholares, lampayales y de las parcelas de la quinua en descanso. Los resultados puede ser que varíen por las diferentes zonas de muestreo del suelo y por la forma de recolecta de las muestras, ya que colecto las muestras al pie de la especie. El método de la recolecta del suelo en la presente investigación no fue al pie de ninguna vegetación, la muestra se recolecto solamente en parcelas de descanso del cultivo de quinua y en suelos sin labranza (puruma), otra de las causas para no encontrar los cuatro géneros puede que sea por la colecta de muestras solamente de una sola comunidad.
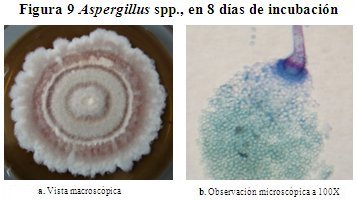
Descripción macroscópica del género Aspergillus spp. En la figura 9, se observa la colonia de hongo Aspergillus spp., desarrollado sobre el AS a 28 oC, la superficie presenta un color blanco al principio con el tiempo muestra una tonalidad de café, hacia el centro con anillos concéntricos y con elevación central ligeramente pronunciada, en el reverso al inicio de color café claro con el tiempo se torna a café oscuro, tiene una pigmentación café, posee textura algodonosa sin exudación, presenta borde irregular. Alcanza un diámetro de 3.4 cm en 8 días de incubación.
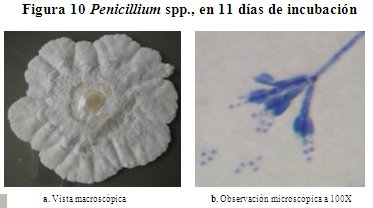
Descripción macroscópica del género Penicillium spp. En la figura 10, se aprecia la colonia de hongo Penicillium spp., desarrollado sobre el AS a 28 oC, color blanco en el superficie con surcados radiales bien pronunciados, carece de pigmentación, tiene textura yesosa sin exudaciones, no presenta coloración en el reverso, tiene borde irregular. Alcanza un diámetro de 6.2 cm en 11 días de incubación.
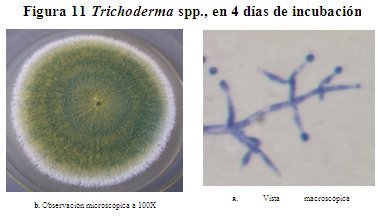
Descripción macroscópica del género Trichoderma spp. En la figura 11, se observa la colonia de hongo Trichoderma spp., desarrollado sobre el AS a 28 oC, la superficie de color verde amarillento al principio con el tiempo se torna a verde oliva con borde blanco, forma anillos concéntricos no bien pronunciados hacia el centro, textura granulosa sin pigmentación ni exudaciones, en el reverso sin coloración, no presenta elevación central, colonia redonda con borde irregular. En 4 días de incubación alcanza un diámetro de 4.8 cm.
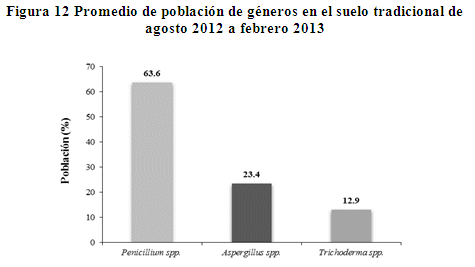
En figura 12, se muestra los promedios de la población de géneros descritos en el suelo tradicional, donde el género Penicillium spp., presenta mayor población con 63.6%, Aspergillus spp., con una población intermedia de 23.4% y el género de Trichoderma spp., presenta menor población de 12.9 %. En este suelo la mayoría de los hongos pertenecen al género Penicillium spp., donde la materia orgánica es 0.87%, la humedad promedio del suelo de 12.8%, temperatura promedio de 8.4oC y un pH de 7.9.
Según Ferrera-Cerrato & Alarcón (2007), menciona que no todos los organismos que habitan en el suelo tienen los mismos requerimientos para desarrollarse, aunque en forma general, los microorganismos son más numerosos en suelos con humedad cercana a capacidad de campo, con pH cercano a la neutralidad, alto contenido nutricional y una temperatura cercana a 30 oC. Quizás esta sea uno de los factores para no hallar más géneros de hongos en la comunidad de Kerecaya, por la textura arenosa del suelo que presenta la zona retiene la humedad menor a 12.8%, materia orgánica de 0.93% que es clasificado como muy baja, con promedio de temperatura inferior a 8.5oC a una profundidad de 20 cm del suelo y con pH que varía entre 7.8 a 8.0.
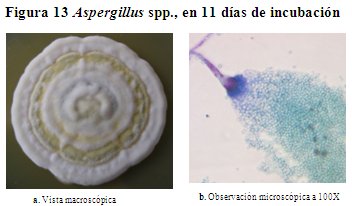
Descripción macroscópica del género Aspergillus spp. En la figura 13, se aprecia la colonia de hongo Aspergillus spp., desarrollado en AS a 28 oC, presenta la superficie de color blanco con anillos concéntricos hacia el centro bien pronunciadas de color amarillo, con elevación central ligeramente pronunciada, tiene textura yesosa sin exudaciones, en el reverso de color crema con surcados radiales, posee borde irregular. Alcanza un diámetro de 4.4 cm en 11 días de incubación.
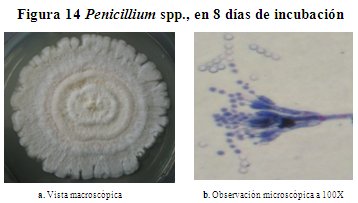
Descripción macroscópica del género Penicillium spp. En la figura 14, se presenta la colonia de hongo Penicillium spp., desarrollado en AS a 28 oC, la superficie de color blanco con anillos concéntricos hacia el centro de color crema bien pronunciados, no presenta elevación central, en el reverso sin coloración al principio pero con el pasar del tiempo se torna de amarillo con un color blanco en el borde, textura algodonosa sin exudación ni pigmentación, tiene borde irregular. Alcanza en 8 días de incubación un diámetro de 3.2 cm.
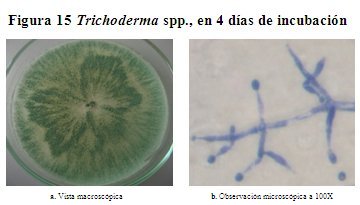
Descripción macroscópica del género Trichoderma spp. En la figura 15, se aprecia la colonia de hongo Trichoderma spp., desarrollado en AS a 28 oC, la superficie al principio de color verde amarillento pero con el tiempo se torna verde oliva, no forma anillos concéntricos y carece de elevación central, tiene textura granulosa sin pigmentación ni exudación, en el reverso no presenta coloración, es una colonia redonda con borde irregular. Tiene gran velocidad de crecimiento, el diámetro que alcanza es de 4.9 cm en 4 días de incubación.
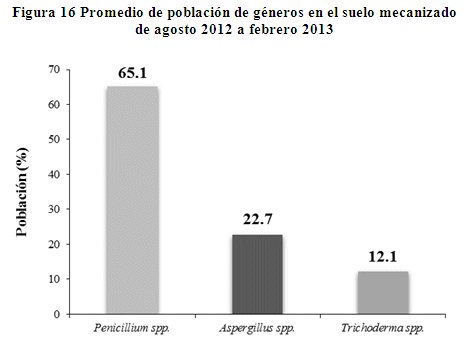
En figura 16, se observa el promedio de la población de géneros hallados en suelo mecanizado, el género Penicillium spp., con mayor población de 65.1%, seguido por Aspergillus spp., con una población intermedia de 22.7% y el género Trichoderma spp., con menor población de 12.1%. En este suelo mecanizado la materia orgánica de 0.69%, humedad promedio del suelo de 12.6%, temperatura promedio del suelo de 8.3 oC a 20 cm de profundidad y un pH de 7.8. En estas condiciones la población de Penicillium spp., aumento con respecto al suelo sin labranza (puruma) que presenta una población de 62.1%, mientras que los demás géneros disminuyeron de población.
Usnayo (2007), menciona que los géneros del altiplano son: Circinutrichum spp., Stephanoma spp., Cephalosporium spp., Bdellospora spp., Blatomyces spp., Trinacrium spp., Verticium spp., Dendrodochium spp., Choanephora spp., Botritys spp., Paecielomyces spp., y Mycotypha spp., en un estudio realizado de las orillas de Lago Titicaca del departamento de La Paz y de orillas de río Desaguadero del departamento de Oruro, donde recolecto las muestras de paja brava (Stipa spp.) de las raíces y del tallo, por otro lado, de los nudos de la quinua (Chenopodium quinoa Willd) y de suelos que rodeaba las mencionadas especies. Estos géneros encontrados es mayor a los resultados de la presente investigación, la variabilidad puede darse por las diferentes zonas, la forma de recolecta y la humedad del suelo, ya que en las orillas del Lago Titicaca como del rio Desaguadero existe mayor porcentaje de humedad y las precipitaciones en estos lugares son superiores con respecto al altiplano Sur de Bolivia.
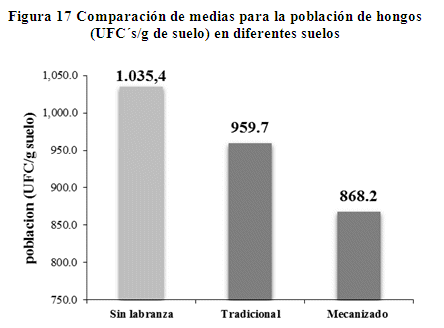
Determinación cuantitativa de población fúngica en UFC´s/g de suelo En la tabla 6 y figura 17, se observa la comparación de medias para de población de hongos (UFC´s/g de suelo) en diferentes suelos, donde la población promedio de hongos en diferentes sistemas de manejo del suelo, muestra claramente que el suelo sin labranza (puruma), es superior (P > 0.05) en población con 1035.5 UFC´s/ g de suelo, a los suelos tradicional y mecanizado.
En el suelo tradicional, la población fúngica presenta de 959.7 UFC´s/g de suelo, que es inferior (P < 0.05) al suelo sin labranza (puruma), pero superior al sistema mecanizado. El suelo mecanizado, presenta menor población de hongos con 868.2 UFC´s/g de suelo en comparación a los suelos sin labranza (puruma) y tradicional.
Toro-Moreira (2005), en un estudio realizado en suelos del cultivo de banano en Porvenir en el departamento de La Paz, afirma que existe una población de 33463 UFC´s/g de suelo en sistema orgánico y 59839 UFC´s/g de suelo en sistema tradicional. Las poblaciones son mayores a los resultados del presente trabajo, probablemente se debe a las condiciones que presenta la zona del trópico. Los tractores en la zona de estudio se han introducido aproximadamente en el año 80 y para controlar plagas en los cultivos, han utilizado insecticidas organofosforados (Tamaron y Folidol) hace 20 a 25 años atrás, estos factores puede que influya en el comportamiento de la población de hongos en la zona.
Frioni (1999), menciona que a una profundidad de 12 a 20 cm del suelo y con 3.1% materia orgánica, se puede encontrar una población de 77500 UFC´s/g de suelo, este biota puede ser mayor que las bacterias y su micelio puede extenderse de 10 a 100 m/g de suelo superficial y pueden alcanzar aproximadamente de 500 a 5.000 kg/ha. Estos valores son superiores a los resultados del presente trabajo, probablemente la diferencia se debe al contenido muy bajo en materia orgánica que presentaron los suelos de estudio.
Valencia (2009), afirma que a una profundidad de 20 cm en diferentes suelos fértiles se han cuantificado el número de los hongos por gramo de suelo de 80000 a más de un millón aproximadamente, esto probablemente puede ser equivalente de 1000 a 1500 kg/ha. Este mencionado es superior a los valores del presente trabajo, para que exista esta diferencia probablemente se debe a las condiciones adversas (poca humedad, bajas temperaturas casi todo el año, contenido de materia orgánica baja y con escasa vegetación) de la zona de estudio.
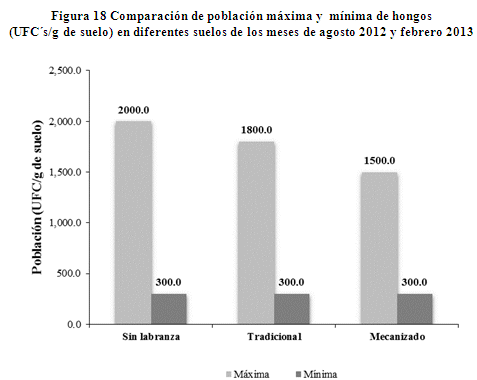
En la figura 18, se aprecia la población máxima y mínima de hongos (UFC´s/g de suelo) en diferentes suelos. En sin labranza (puruma) se observa que la población máxima en UFC´s/g de suelo alcanzo a 2000.0 en el mes de febrero, con temperatura de 9.2 oC del suelo a una profundidad de 20 cm y con 19.3% de humedad del suelo, la población mínima llega a 300.0 UFC´s/g de suelo en mes de agosto con 9.7% de humedad y 6.7 oC de temperatura del suelo. Este resultado indica que la población de hongos se incrementa en el suelo con la humedad adecuada (capacidad de campo).
De la misma manera se ilustra que la máxima población de hongos (UFC´s/g de suelo) en el suelo tradicional llega a 1800.0 en el mes de febrero, cuando la humedad del suelo llega a 19.3% y con 9.1 oC de temperatura del suelo, la población mínima llega a 300.0 UFC´s/g de suelo en el mes de agosto, donde la temperatura del suelo es de 6,6oC de a una profundidad de 20 cm y con 9.5% de humedad. Estos resultados indican que la humedad del suelo es primordial para el incremento de la población de hongos en el suelo.
Asimismo se aprecia en el suelo mecanizado la población máxima de 1500.0 UFC´s/g de suelo en el mes de febrero cuando la humedad del suelo es 19.2% con una temperatura de 9.0 oC a 20 cm de la profundidad del suelo, la población mínima es de 300.0 UFC´s/g de suelo en el mes de agosto, donde la temperatura del suelo llega a 9.4 oC y con una humedad de 8.4%. La población de hongos del mes de agosto muestra una disminución aproximadamente de 20% con respecto al mes de febrero.
Un estudio realizado en altiplano central por Sivila de Cary & Hervé (2006), en suelos con leguminosas nativas. Donde comparó parcelas de cinco años de descanso con alto porcentaje de leguminosas y la otra con 30% de gramíneas (carece de leguminosas), en el cual, encontró en parcelas con leguminosas nativas una población de 6400 UFC´s/g de suelo y con 5600 UFC´s/g de suelo en parcelas con gramíneas. Estos valores son superiores a los resultados del presente trabajo de investigación, la diferencia quizás se debe al contenido de las leguminosas que son micorrizables, por otro lado, puede que influya los años de descanso de las parcelas, la precipitación y la temperatura que son superiores con respecto al Sur del departamento de Oruro, donde las condiciones son muy adversas, las parcelas solo descansan un año y que la quinua no es micorrizable, por estos factores puede que tenga una amplia diferencia en la población de hongos, ya que se encontró las poblaciones máximas de 2000.0 UFC´s/g de suelo en suelo sin labranza (puruma), 1800.0 UFC/g suelo en suelo tradicional y 1500.0 UFC/g suelo en suelo mecanizado.
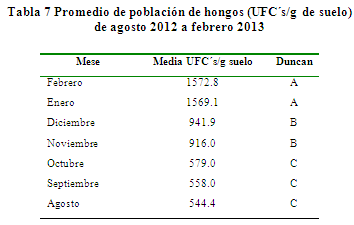
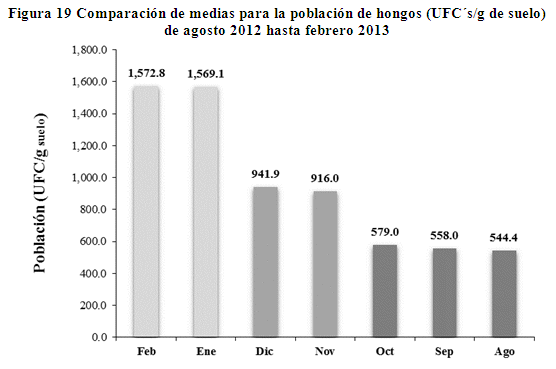
Población de hongos (UFC/g de suelo) en diferentes meses. En la tabla 7, se presenta los valores del promedio de la población de hongos en UFC´s/g de suelo de los diferentes meses, donde se observa tres grupos similares. Los meses de enero y febrero presentan similares poblaciones de hongos con 1572.8 y 1569.1 UFC´s/g de suelo respectivamente, pero superiores (P > 0.05) a los meses de agosto, septiembre, octubre, noviembre y diciembre. La población de hongos en los meses de diciembre y noviembre son similares con 941.9 y 916.0 UFC´s/g de suelo respectivamente, pero inferiores a los meses de enero y febrero y los meses de octubre, septiembre y agosto, presentan similares poblaciones de hongos con 579.0, 558.0 y 544.4 UFC´s/g suelo respectivamente, pero inferiores (P < 0.05) a los meses de enero, febrero, noviembre y diciembre.
En la figura 19, muestra mayor población de hongos en los meses con mayor humedad y en los meses de diciembre y noviembre la población es 59.1% aproximadamente en relación a los meses con mayor humedad. Aparentemente, en estos meses, la humedad aumentó por la mínima precipitación, entonces se traduce en el incremento de la población fúngica. En los meses de agosto, septiembre y octubre la población de hongos es la tercera parte de lo que se puede encontrar en los meses lluviosos, estos valores son proporcionales a los porcentajes de humedad de esos meses.
Sivila de Cary & Angulo (2006), menciona que existe diferencias en población de hongos en un estudio realizado en suelos con diferentes descansos agrícolas, donde recolecto muestras en época seca y húmeda, en el cual, encontró una población de 211100 UFC´s/g de suelo en parcelas de 1 a 4 años de descanso, 267800 UFC´s/g de suelo en suelos de 5 a 9 años. Este estudio se realizó en altiplano central, donde la precipitación media anual es de 400 mm, temperaturas medias mensuales entre 8 a 11 oC, pH del suelo es de neutro a moderadamente ácido y en un suelo franco arenoso, estas condiciones de la zona son diferentes al altiplano Sur del país, quizás por estos factores la población de hongos encontrados son inferiores incluso en los meses lluviosos (enero y febrero) con promedios de 1572.8 y 1569.1 UFC´s/g de suelo respectivamente.
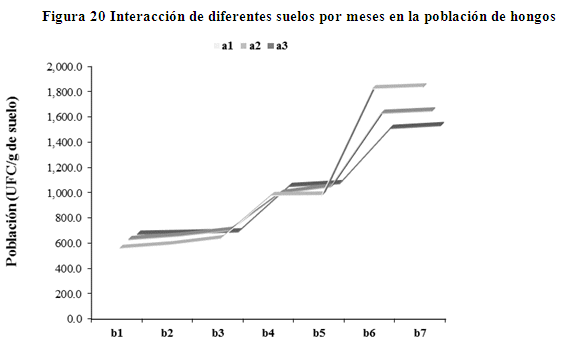
Análisis de varianza de efectos simples para la interacción de diferentes manejos del suelo y meses. En la figura 20, se presenta la interacción de diferentes suelos (A) por meses (B) en la población de hongos, donde se observan los meses de agosto (b1), septiembre (b2) y octubre (b3) no presentan diferencias en la población de hongos (UFC´s/g de suelo) en los tres sistemas de manejo (a1, a2 y a3) del suelo de quinua. De igual forma se aprecia que en los meses de noviembre (b4) y diciembre (b5) presenta diferencias en el comportamiento de la población de hongos (UFC´s/g de suelo), siendo el de mayor población el suelo sin labranza (a1) y de menor población el suelo mecanizado (a3).
Por otro lado los meses de enero (b6) y febrero (b7) presentan diferencias altamente significativas en la población de hongos (UFC´s/g de suelo), donde presenta mayor población el suelo sin labranza (puruma) (a1), seguido por el suelo tradicional (a2) con población intermedia y en el mecanizado (a3) con baja población de hongos.
Según Sivila de Cary & Angulo 2006, Alexander (1980), indican que las colonias son predominantes en los suelos ácidos, ya que con esta clase de pH las colonias favorecen a la captación de agua y nutrimentos para el suelo, además no presentan competencia con bacterias y actinomicetos. Los suelos del presente trabajo de investigación presentan pH moderadamente alcalinos, en estos suelos, la población de colonias de hongos totales son inferiores en los meses con menor porcentaje de humedad y aumenta la población en los meses lluviosos, esto se traduce, que la población de hongos es proporcional a la humedad y no tanto así al pH del suelo, ya que la humedad influye en el ciclo metabólico de los hongos.
Alexander (1980), menciona que la deficiencia de nitrógeno, materia orgánica y otros factores provocan que sea deficiente la presencia de hongos en el suelo. El contenido de nitrógeno en los suelos de estudio es 0.02% que es clasificado como muy bajo, quizás por este motivo se presentó menor población en los meses de agosto, septiembre y octubre, pero cuando la humedad del suelo sube se encontró diversidad de hongos (color y forma) en los tres tipos de suelos, pero con una población muy reducida.
PIEB (2010), afirma que los suelos del intersalar son arenosos con escasa vegetación, salinos y erosionados. Este puede ser una de las causas para que la población de hongos en el suelo presente escasa en comparación a los suelos del altiplano central del país, donde presentan poblaciones de 5600 a 6400 UFC´s/g de suelo. Otro de los factores puede ser por el contenido muy bajo de la materia orgánica y por baja retención de humedad en el suelo.
En la comunidad de Kerecaya los diferentes sistemas de manejo presentan frágiles suelos a la erosión (eólica y hídrica) con humedad y materia orgánica muy bajo y a este se suma la mecanización del cultivo de quinua (Chenopodium quinoa Willd) que influye directamente a la población de los microorganismos de hongos que son encargados de descomponer y mineralizar la materia orgánica para que las plantas puedan aprovechar para su normal desarrollo y por tanto en su productividad. En este sentido, amerita una reflexión integral sobre la sostenibilidad del suelo y a este cultivo para las repercusiones de su actual producción a largo plazo. Por otra parte, la repoblación camélida en la zona es de vital importancia por los aportes de abono que influyen directamente en la fertilidad de los suelos.
Conflictos de intereses
Los autores declaran que no tienen conflictos de interés con la presente investigación.
Agradecimientos
Se agradece al técnico de laboratorio de Servicios Analíticos-Laboratorio Químico (Espectrolab) de la Universidad Técnica de Oruro (UTO). A los productores de quinua de la comunidad de Kerecaya municipio de Salinas de Garci Mendoza de la provincia Ladislao Cabrera al Sur del departamento de Oruro.
Literatura citada
Aguilera MP, Vélez PE. Aproximación al estudio del efecto de la cobertura vegetal sobre los grupos bacterianos proteolíticos y celulolíticos en el departamento del Quindio. [Tesis de Licenciatura].Pontificia Universidad Javeriana. Facultad de Ciencias. Bogotá-Colombia. 2001. p. 98.
Alexander M. Introducción a la microbiología del suelo. AGT. México. 1980. p. 491. [ Links ]
Arias-Cifuentes EL, Piñeros-Espinosa PA. Aislamiento e identificación de hongos filamentosos de muestras de suelo de los Paramos de Guasca y Cruz Verde. [Tesis de Licenciatura] Pontificia Universidad Javeriana. Facultad Ciencias. Bogotá. Colombia. 2008. p. 204.
Aristegui B. El reino de los hongos. Rev. Iberoam Micol. 2002; 8: 1-4. [ Links ]
Bautista F, Palacio J, Delfín H, Paéz R, Carmona E, Delgado M. Técnicas de muestreo para manejadores de recursos naturales. 2da ed. CIGA. Universidad Nacional Autónoma de México. Segunda edición. 2011. p 770.
Benzina A, Verlag N, Villingen S. Agricultura orgánica fundamentos para la región andina. Editorial Neckar. Verlag-Alemania. 2001; 102-120, 831-837.
Condori L. Aislamiento e identificación de hongos provenientes de suelos del municipio de Salinas de Garci Mendoza, provincia Ladislao Cabrera-Oruro. [Tesis de Licenciatura]. Universidad Técnica de Oruro. Facultad de Ingeniería Agronómica. 2012. p. 51.
Coyne M. Microbiología del Suelo: Un Enfoque Exploratorio. Ed. Paraninfo. España. 2000. p. 416.
Delgado-Callisaya PA. Principios de investigación científica y uso óptimo del análisis estadístico. La Paz-Bolivia. S.e. 2013. p. 92-93.
FAO. Organización de las Naciones Unidas para la Agricultura y la Alimentación. Guía para la descripción de suelos. Traductor R. Vargas Rojas. (Proyecto FAOSWALIM, Nairobi, Kenya-Universidad Mayor de San Simón, Bolivia). Cuarta edición. Roma-Italia. 2009. p. 43.
FAUTAPO. Educación para el Desarrollo. Estudio de suelos del área productora de quinua real, Altiplano sur boliviano, Informa final. Sucre-Bolivia. 2008. 18 p.
Ferrera-Cerrato R, Alarcón A. Microbiología agrícola. Hongos, bacterias, micro y macrofauna, control biológico y planta-microorganismos. Primera edición. S.L. México. Editorial Trillas. 2007. p. 57.
Frioni L. Procesos microbianos. Editorial de la fundación Universidad Nacional de Rio Cuarto Argentina. 1999. p. 4-8. [ Links ]
González-Velázquez A, Valenzuela R. Los boletáceos y gonfidiáceos del Estado de México I. Rev Mex Mic. 1993; 9:35-46. [ Links ]
Herrera T. Hongos en peligro de extinción que habitan en México. Rev Mex Biodiv. 2000; 9:13-14. [ Links ]
Joffre R, Vassas A, Cortes G. Emergencia de la quinua en el comercio mundial: consecuencias para la sostenibilidad social y agrícola en el altiplano sur de Bolivia, conferencia pública, 28 de abril 2011. Alianza Francesa, La Paz-Bolivia. 2011.
Medel R. Ascomycetes citados de México IV: 1996-2006. Rev Mex Micol. 2007; 25: 69-76. [ Links ]
Michael G. Fungi in biogeochemical cycles. School of Life Sciences. University of Dundee. Cambridge UP. First published. New York-Estados Unidos. 2006. p. 22-23, 67-69.
Miranda R, Huanca M, Mamani P, Aliaga S, Yucra E, Garcia M. Rendimiento y acumulación de nitrógeno en la quinua (Chenopodium quinoa Willd) producido con estiércol y riego suplementario. Proyecto QUINAGUA. Facultad de Agronomía. UMSA. La Paz-Bolivia. s.p. 2009.
PIEB. Programa de Investigación Estratégica en Bolivia. Producción de quinua en Oruro y Potosí. La Paz-Bolivia. Ediciones Montserrat Fernández. 2010. p 8-11.
Santana L. Manual de prácticas microbiología industrial. Universidad Autónoma de ciudad Juárez. Instituto de Ciencias Biomédicas. Departamento de Ciencias Químico-Biológicas. Programa de Biología. México. 2011. p. 47. [ Links ]
Sivila de Cary R, Angulo W. Efecto del descanso agrícola sobre la microbiota del suelo (Patarani-Altiplano central boliviano). Ecología en Bolivia. 2006; 41(3): 103-115. [ Links ]
Soraide-Lozano D. La quinua real en el altiplano sur de Bolivia. Primera edición. S.L. Bolivia. S.e. 2011. p. 63. Disponible en http://www.in foquinua.bo/filepublicacion/DO%20Quinua% 20Real%20ASur%20Bolivia%20X1_min.pdf.
Ticona E, Bernal I. Evaluación comparativa del rendimiento de la quinua, bajo siembra directa y trasplante en el inicio de la época lluviosa. Capitulo II. In Vargas el at. (Editores). Congreso científico de la quinua (memorias) La Paz-Bolivia. 2013. p. 137-147.
Toro-Moreira T. Evaluación poblacional de microorganismos en suelos con manejo orgánico y tradicional del banano (Musa sp.) en Porvenir La Paz. [Tesis de Licenciatura]. Universidad Mayor de San Andrés. Facultad de Agronomía. 2005. p. 116.
Usnayo P. Optimización de medios de cultivo, para la producción de enzimas ligninolíticas, por cepas fúngicas aisladas del altiplano boliviano. [Tesis de Licenciatura]. Universidad Mayor de San Andrés. Facultad de Ciencias Farmacéuticas y Bioquímicas. 2007. p. 132.
Valencia C. Bioquímica de suelos. Universidad Nacional Autónoma de México. Facultada de Estudios Superiores Cuautitlán. S.e. 2009. p. 24.
Vallejos-Mamani PR, Navarro-Fuentes Z, Ayaviri-Nina D. Medio ambiente y producción de la quinua. Estrategia de adaptación a los impactos del cambio climático. La Paz-Bolivia. Editorial Claudia Adriázola. 2011. p 37-40.
______________











 uBio
uBio