Journal of the Selva Andina Research Society
versão On-line ISSN 2072-9294
J. Selva Andina Res. Soc. vol.7 no.2 La Paz 2016
NOTA DE INVESTIGACIÓN
Avaliação de protocolos para extração de DNA Genômico de sangue Bovino
Evaluation protocols for the extraction of genomic DNA from Bovine blood
Crispim Bruno do Amaral1, Nascimento André Vieira2, Romero Ândrea Renata da Silva2, Fernandes Juliana dos Santos2, Banari Alexandre Campos2, Seno Leonardo de Oliveira3, Grisolia Alexéia Barufatti1*
1Faculdade de Ciências Exatas e Tecnologia da Universidade Federal da Grande Dourados-FCBA/UFGD, Mato Grosso do Sul – Brasil.
2Faculdade de Ciências Biológicas e Ambientais da Universidade Federal da Grande Dourados-FCBA/UFGD, Mato Grosso do Sul – Brasil.
3Faculdade de Ciências Agrárias da Universidade Federal da Grande Dourados-FCA/UFGD, Mato Grosso do Sul -Brasil.
*Endereço de contato: Faculdade de Ciências Exatas e Tecnologia da Universidade Federal da Grande Dourados-FCBA/UFGD, Mato Grosso do Sul – Brasil.
Alexeia Barufatti Grisolia.
E-mail: alexeiagrisolia@ufgd.edu.br
Historial del artículo.
Recibido marzo, 2016.
Devuelto julio 2016
Aceptado julio, 2016.
Disponible en línea, agosto, 2016.
Resumen
Estudos básicos sobre técnicas de extração de DNA são de extrema importância para o sucesso de trabalhos científicos no campo da biologia molecular. A extração e a purificação de ácidos nucleicos constituem etapas fundamentais para o estabelecimento de posteriores análises genéticas. Objetivou-se neste trabalho avaliar a eficácia de diferentes protocolos de extração de DNA por meio da determinação de quantidade, qualidade e a possibilidade de amplificação por meio de PCR do material genético extraído. Utilizou-se amostras de sangue de dez animais, que foram submetidas à extração de DNA e, logo após à reação em cadeia pela polimerase (PCR). Os resultados das análises obtidas por nanofotometria indicaram que a quantidade e a qualidade do DNA genômico foram consideradas satisfatórias, em todos os protocolos, para a realização da PCR, mas houve diferença estatística significativa entre os parâmetros analisados, tanto na quantidade quanto na qualidade (p < 0.05) do DNA obtido. O protocolo de extração utilizando sangue total foi mais eficiente quanto ao tempo e a qualidade do DNA extraído, entretanto em todos os processos de extração houve ausência de degradação. Também foi demonstrado a possibilidade de amplificação da região do exon 2 do gene da leptina de bovinos no DNA extraído.
Palavras chave: Teste de extração, PCR, bovinos, biologia molecular.
Abstract
Basic studies on DNA extraction techniques are very important for the success of scientific papers in the field of molecular biology. The extraction and purification of nucleic acids are critical steps for establishing further genetic analysis. The objective of this study was to evaluate the efficacy of different protocols for DNA extraction by determining the quantity and quality of extracted genetic material and the possibility of amplification by PCR. We did DNA extraction and PCR of ten bovine blood samples. The test results obtained by spectrophotometry indicated that the quantity and quality of genomic DNA were considered satisfactory in all protocols for PCR. However, there was a statistically significant difference between the parameters measured, both in quantity and in quality (p <0.01). The extraction protocol using whole blood was more efficient in terms of time and quality; there was no degradation in all processes of extraction. It was also demonstrated that the possibility of amplification of the region of exon 2 of the leptin gene in extracted DNA exists.
Key words: Test extraction, PCR, bovine, molecular biology.
Introdução
Estudos básicos sobre técnicas de extração de DNA são de extrema importância para o sucesso de trabalhos científicos no campo da biologia molecular. A extração de material genético puro e de boa qualidade é pré-requisito para qualquer análise molecular. Diferentes métodos de extração de DNA têm sido utilizados e estão bem estabelecidos para diferentes espécies. Entretanto, em função da variabilidade da composição das amostras biológicas e das condições laboratoriais, são necessárias algumas modificações e adaptações nos protocolos (Marengoni et al. 2006).
Atualmente amostras de DNA genômico extraído de animais de interesse zootécnico, em especial bovinos, podem ser utilizadas para vários fins, como por exemplo, diagnóstico clínico de doenças, teste de paternidade para registro genealógico, melhoramento genético, planejamento de cruzamentos e estimativa de valor genético de animais de elite (Dias-Salman & Mussolini-Laureano 2006).
A reação em cadeia da polimerase (PCR) é uma técnica amplamente empregada em estudos moleculares, em virtude da relativa facilidade de amplificar in vitro regiões específicas do genoma de qualquer organismo. A PCR possibilita a amplificação de sequências de DNA presentes em misturas complexas e permite estudos de natureza variada, tais como desenvolvimento de métodos de diagnósticos altamente sensíveis e específicos, obtenção de grandes quantidades de DNA para sequenciamento e análises sobre a diversidade genética de populações (Oliveira et al. 2007).
Apesar da facilidade de amplificação de DNA possibilitada pela técnica de PCR, existe a necessidade da padronização dos protocolos de extração para obtenção do mesmo em boa qualidade. Para extração do material genético a partir de sangue total, os kits comerciais disponíveis, em geral, resultam em purificações de boa qualidade para utilização nas mais variadas técnicas moleculares, dentre as quais a PCR, mas possui como desvantagem o alto custo por amostra, que fica em torno de cinco vezes o valor de uma reação de PCR (Araujo et al. 2009).
Para cada tipo de amostra, vários protocolos podem ser testados, adaptados e otimizados, de maneira que amostras de DNA de boa qualidade possam ser obtidas. Pesquisar métodos alternativos de extração de DNA que possam ser rápidos, práticos, de menor custo, e eficazes no que tange à quantidade, qualidade e possibilidade de amplificação por PCR, do DNA extraído, podem possibilitar a organização de bancos de DNA, aplicação da pesquisa em outros estudos, como diagnósticos retrospectivos, identificação de indivíduos, estudos populacionais e envios de amostras à distância (Barea et al. 2004).
Diante da necessidade do aprimoramento de técnicas de extração do ácido desoxirribonucleico, de maneira que os custos e os benefícios sejam satisfatórios e reprodutíveis, possibilitando sua utilização em estudos posteriores, como a PCR. O objetivo do trabalho foi testar e avaliar protocolos de extração de DNA, determinando a sua quantidade, qualidade e a viabilidade de amplificação.
Material e métodos
Material. Foram utilizadas amostras de sangue de 10 animais Bos indicus, provenientes da Agropecuária Jorge Ferreira - Fazenda Tuju Puitan, município de Iguatemi – MS.
Métodos. Colheita de sangue: Foram coletados 4.5 mL de sangue da veia jugular e armazenados em tubos do tipo vacutainer com EDTA potássico. Esse material foi acondicionado em freezer -20 ºC até seu processamento.
Extração de DNA genômico. A extração de DNA foi realizada no Laboratório de Biotecnologia aplicada à Produção Animal, Faculdade de Ciências Agrárias da Universidade Federal da Grande Dourados (FCA/UFGD), cinco dias após a colheita do sangue.
As amostras foram submetidas à extração de DNA utilizando três protocolos diferentes: sangue total utilizando o Kit comercial Wizard® Promega e sangue total e leucócitos a partir de protocolos convencionais adaptados.
Protocolo de extração de DNA de sangue total (descrito por Sambrook et al. (1989) e adaptado por Crispim et al. (2012). Foram aliquotados 300 µL de sangue em microtubo de polipropileno de 2 mL e acrescentados 2.2 µL de proteinase K (20 mg/ml) e 500 µL de SDS (do inglês, Sodium Dodecyl Sulfate) a 20%, homogeneizados em vortex e incubados a 60 ºC em banho-maria por 1 h e 30 min. Após a incubação, foram adicionados 800 µL de clorofórmio nos microtubos e agitados vigorosamente em vortex até completa homogeneização; em seguida, foram acrescentados 350 µL de solução de precipitação protéica (3 M acetato de potássio, 6.6 M ácido acético glacial) e homogeneizados novamente em vortex. Os microtubos com a solução foram centrifugados a 19.722 g por 10 min para que a fase aquosa pudesse ser retirada e transferida para outro microtubo. Foi adicionado 1 mL de etanol 100% gelado e logo em seguida, homogeneizado por inversão até a formação de precipitado (entre 30 e 60s). Posteriormente, o material foi centrifugado a 17.005 g por 5 min e após centrifugação desprezou-se o sobrenadante e acrescentou-se 1 mL de etanol 70%; centrifugou-se novamente por dois minutos, e desprezou-se o sobrenadante. Após esta etapa o microtubo foi invertido para a secagem do sedimento (10 a 15 min), adicionou-se 100 µL de TE (10 mM Tris HCl, 1 mM EDTA) pH 8.7 com RNase (Promega) 10 µg/µL, e por último incubou-se a 37 ºC por 1 h sendo posteriormente, armazenados em freezer a -20 ºC até o momento do uso.
Protocolo de Extração de DNA de leucócitos (adaptado de Olerup & Zetterquist (1992) Processamento do Sangue Total e Obtenção de Leucócitos. O sangue (4.5 mL) que estava em tubos vacutainer com EDTA potássico, foi transferido para tubo de 15 mL e centrifugado por 15 min a 388 g e em seguida, descartou-se o sobrenadante com cuidado para não remover as células brancas que se encontravam na interface. Posteriormente, o volume dos tubos foi ajustado para 5 mL com solução A (250 µL Tris HCl pH 7.6 1 M; 250 µL MgCl2 0.5 M; 50 µL NaCl 5 M e completar com água ultrapura para 25 mL. Autoclavar por 20 min a 1 atm. Armazenar a 4 ºC por uma semana). Em seguida foram adicionados 10 mL do tampão da solução A, e homogeneizado no vortex, até a obtenção de uma coloração escura e homogênea. Logo após, foi centrifugado por 10 min a 693 g. Dispensou-se o sobrenadante com cuidado por inversão e deixou-se escorrer lentamente o líquido. O sedimento foi ressuspendido em 5 mL do tampão de hemólise e misturado bem por inversão, em seguida foi centrifugado a 693 g por 10 min e descartou-se o sobrenadante, essa lavagem foi realizada quatro vezes, e em seguida, as células brancas foram ressuspendidas em 500 µL do tampão de hemólise e colocadas em microtubos de 1.5 mL. A lavagem foi repetida quatro vezes até a obtenção das células brancas (sem coloração avermelhada), e posteriormente ressuspendidas em 500 µL do tampão de hemólise e colocadas em microtubos de 1.5 mL. Foram novamente centrifugadas por 1 minuto a 10.621 g e descartado o sobrenadante (deixou-se apenas um filme de solução, ~1 mm de espessura). Esse sedimento de leucócitos foi conservado em microtubos no freezer a -20 ºC.
Extração do DNA de leucócitos. Foram adicionados 500 µL de solução de Proteinase K (5 µL de Tris HCl pH 8.0 1 M; 10 µL de NaCl 5 M; 10 µL de EDTA pH 8.0 0.5 M; 12.5 µL de SDS a 20 % e completar o volume com 460, 5 µL de água ultrapura. Adicionar 2 µL de solução de proteinase K na concentração 20 mg/mL no momento do uso) ao sedimento de leucócitos separados da etapa anterior e misturados no vortex até o mesmo se desprender do fundo do tubo, em seguida foi incubado a 55 ºC no banho-maria até dissolver o precipitado (4 a 6 h). Após a incubação, acrescentou-se 210 µL de TE pH 7.6 e 240 µL de NaCl 5 M, agitou-se por inversão e incubou-se no gelo por 15 min. Posteriormente, as amostras foram centrifugadas por 15 min a 10.621 g e o sobrenadante foi transferido para dois tubos de 1.5 mL. Foi adicionado 1 mL de etanol absoluto gelado e os tubos foram invertidos várias vezes até a visualização da nuvem de DNA, em seguida foram centrifugados por 15 min a 10.621 g e o sobrenadante foi descartado. A seguir foi realizada uma lavagem com 500 µL de etanol a 70% gelado, centrifugado por 5 min a 10.621 g, descartado o etanol e deixado para secagem no fluxo laminar ligado por 25 min. O pellet foi ressuspendido em 250 µL de solução TE e 0.25 µL de solução de RNase (10 µg/µL) e incubado por 12 h a 4 ºC.
Protocolo de extração de DNA com Kit Comercial Wizard® PROMEGA. O protocolo para extração de DNA utilizando o kit comercial Wizard® PROMEGA (Promega Bio Sciences, LLC. San Luis Obispo, CA, USA.) foi realizado de acordo com as normas do fabricante (Promega 2014), a partir de 300 µL de sangue e, por fim, as amostras armazenadas em freezer -20 °C.
Análise da quantidade e qualidade do DNA. A quantidade e a pureza do DNA extraído a partir dos três protocolos foram obtidas por meio de espectrofotometria, utilizando o espectrofotômetro NanoPhotometerP-Cass (Implen Inc., EUA). Nesse método, a análise da pureza do DNA baseia-se na propriedade da molécula de absorver radiação ultravioleta no comprimento de onda de 260 nm/280 nm, e por meio da razão aferida nas amostras foi possível determinar a concentração de DNA.
Além disso as amostras de DNA foram submetidas à eletroforese em gel de agarose a 1.5%, com voltagem de 120 V, por 30 min. O gel foi preparado com tampão TBE (1x) e corado com brometo de etídio. O DNA foi visualizado no gel e fotografado em fotodocumentador (UVP) sob luz UV.
Reação em cadeia da polimerase (PCR). As amostras de DNA extraídas a partir de leucócitos e sangue total foram submetidas à PCR para o éxon 2 do gene da leptina bovino (Buchanan et al. 2002). Foram utilizadas a seguintes sequências de oligonucleotídeos iniciadores: Foward (5 ATGCGCTGTG GACCCCTGTATC 3) e Reverse (5 TGGTGTCATCCTGGACCTTCC 3). Foi preparada uma reação de 25 µL contendo: 12.5 µL de PCR Master Mix (Promega, USA), 10 pmoles de cada um dos oligonucleotídeos iniciadores e 50 a100 ng de DNA genômico. As reações em cadeia pela polimerase foram realizadas em termociclador (BIORAD) e consistiu em pré-aquecimento de 94 ºC por quatro minutos antes da inicialização dos 30 ciclos, cada qual conduzido a 94 ºC por 45 s, 56 °C por 55 s para o anelamento dos primers e extensão, a 72 oC por 45 s catalizada pela atividade da DNA polimerase, e então uma extensão final por quatro minutos a 72 ºC. Todas as reações foram conduzidas utilizando-se uma amostra controle negativo, onde o DNA foi substituído por igual volume de água ultrapura.
Os fragmentos amplificados foram separados por eletroforese em gel de agarose a 2.0%, a uma voltagem de 120 V, por 40 min. O gel foi preparado com tampão TBE (1x), corado com brometo de etídio. O marcador de peso molecular utilizado foi 100 pb DNA Ladder (PROMEGA). Os produtos da PCR e o controle negativo foram submetidos à eletroforese em gel de agarose acrescidos do tampão de corrida. A banda de DNA foi visualizada e fotografada em fotodocumentador (UVP) sob luz UV.
Análise estatística. Foram estimadas a média aritmética e o desvio padrão para os resultados de quantificação de DNA obtido. Os dados de concentrações e razão 260/280 resultantes da quantificação do DNA dos três protocolos foram submetidos aos testes de Shapiro-Wilk e Bartlet, para verificação da normalidade e homogeneidade das variâncias. Para atender as pressuposições da análise de variância foi necessária a transformação dos dados de concentração e razão 260/280 utilizando o método de Boxcox, que quando obtido resultado significativo (p < 0.05), o teste de comparação de médias Tukey foi aplicado. Todas as análises estatísticas foram prosseguidas em Software R v. 3.2.1 (R Development Core Team 2012).
Resultados
A concentração de DNA obtido com o protocolo de extração a partir de sangue total apresentou média de 54.77 µg/μL, com razão entre as leituras das absorbâncias 260/280 nm variando de 16 a 90.2 µg/μL. Para as amostras extraídas com o protocolo de DNA de leucócitos, o rendimento médio foi de 163.36 µg/μL, e a razão entre as leituras 260/280 variaram entre 77.2 e 252.0 µg/μL. Com o Kit comercial, obteve-se concentração média de 24.89 µg/μL e razão entre leituras 260/280 variando de 12.5 a 56.1 µg/μL (Tabela 1).
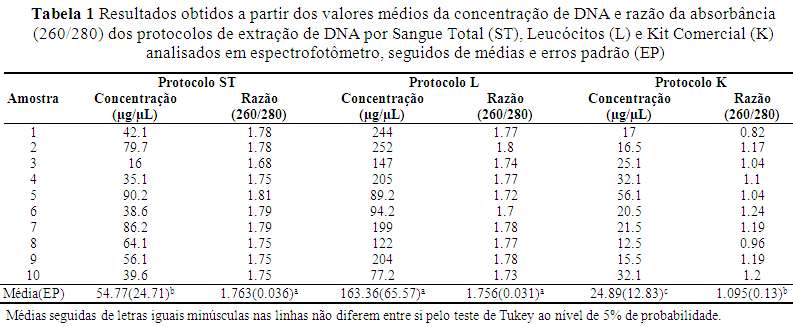
Observou-se diferença (P < 0.05) entre as concentrações de DNA bovino extraído com as três metodologias. No protocolo de extração de DNA a partir de leucócitos (L), foi obtido melhores resultados, seguido pelos protocolos de extração de DNA de sangue total (ST) e por fim o protocolo de extração realizado com Kit comercial (K).
Os níveis de pureza, representados pela razão entre as absorbâncias 260/280 nm, apresentaram diferença significativa. Os melhores resultados foram observados para os protocolos de extração de DNA de sangue total e leucócitos.
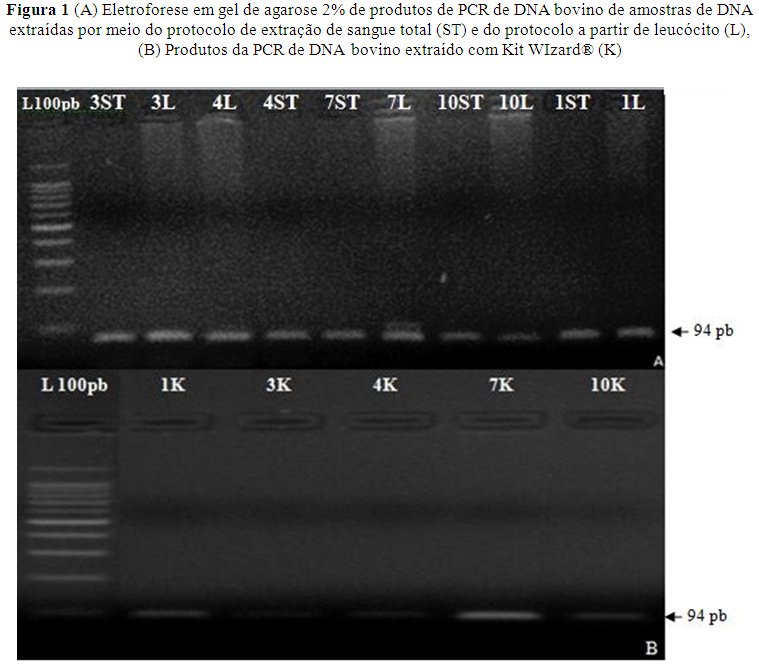
Foi possível observar a amplificação por PCR de uma região do éxon 2 do gene da leptina, constituída de 94 pb, a partir do DNA genômico bovino obtido pelos três métodos de extração testados conforme demonstrado na Figura 1.
Discussão
Os métodos de extração utilizados foram capazes de proporcionar DNA de qualidade, com concentrações e pureza satisfatórias para utilização em PCR. Dentre os benefícios previamente descritos, do emprego do sangue total para esse procedimento, encontram-se a facilidade de obtenção, quantidade satisfatória de DNA e baixa incidência de contaminação (Caldart et al. 2011).
Houve diferença entre os protocolos utilizados no presente estudo, tanto na quantidade quanto na qualidade do DNA. Valores de razão de absorbância inferiores a 1.8 resultam de contaminação com proteínas. No entanto, valores como 1.7, obtidos no presente estudo, podem ser considerados satisfatórios para utilização em PCR (Regitano 2001, Lee et al. 2010).
Após eletroforese em gel de agarose 2%, foi possível visualizar a presença de DNA genômico, fornecendo indícios da eficiência das técnicas utilizadas. As amostras de DNA extraídas pela metodologia de sangue total apresentaram características visivelmente melhores quanto à concentração e pureza quando comparada com as demais. O material genético obtido por meio da extração com o kit comercial resultou em menor rendimento de DNA e, por fim, as amostras extraídas a partir de leucócitos demonstraram concentração satisfatória, no entanto houve presença de rastros no gel, indicando a baixa qualidade do DNA (Silva et al. 2013).
Apesar de Posnett et al. (1991) relatarem que a extração de DNA utilizando clorofórmio pode acarretar em perda de DNA e, consequentemente, resultados falso-negativos. No presente trabalho, o DNA extraído com o protocolo de sangue total, utilizando clorofórmio, obteve melhores resultados em relação à qualidade das amostras, apresentando resultados semelhantes aos de Canola et al. (2007) que observaram maior eficiência utilizando um protocolo de extração de DNA de sangue com fenol-clorofórmio.
Considerando o tempo despendido para a realização de cada protocolo, o kit comercial demonstrou ser um método rápido (1h), seguido pelo protocolo de extração a partir de sangue total (2h e 30 min) e extração de DNA de leucócitos, que por ser executada em duas etapas, exigiu maior tempo (8h e 30 min).
A avaliação eletroforética do DNA mostrou que a extração utilizando clorofórmio e proteinase K apresentou melhores resultados quanto ao tempo de execução do protocolo e a qualidade do DNA obtido, o que torna essa uma alternativa viável, corroborando com os resultados de Moore & Dowhan (1995), Magajevski & Gírio (2008).
Este estudo permitiu comparar algumas técnicas de extração de DNA rotineira em laboratórios, apontando as vantagens e desvantagens de cada uma delas quanto à quantidade e qualidade do material extraído. Apesar da quantidade e rapidez apresentada pelo kit comercial, o mesmo obteve baixa razão, provavelmente por contaminações proteicas ou reagentes, o que pode interferir em análises futuras. Quanto à metodologia utilizando leucócitos, os principais entraves foram o tempo de manipulação e presença de rastros no gel de agarose (Caldart et al. 2011).
Com base nos resultados obtidos, pôde-se concluir que, todos os métodos avaliados neste estudo têm grande utilidade para extração de DNA genômico de boa qualidade. No entanto, o protocolo de extração utilizando sangue total demonstrou ser mais eficiente quanto ao tempo, qualidade do DNA extraído, além de apresentar concentração satisfatória e baixo custo despendido, sendo acessível às diversas infra-estruturas laboratoriais.
Conflito de Interesse
Declaro que este trabalho não gera conflito de interesse de ordem: pessoal, comercial, acadêmico, político e financeiro.
Agradecimientos
UFGD, FUNDECT e CAPES pelo apoio financeiro. Agropecuária Jorge Ferreira pela colaboração no fornecimento do material biológico.
Literatura citada
Araújo FR, Ramos CAN, Luíz HL, Péres IAHFS, Oliveira RHM, Souza IIF, et al. Avaliação de um Protocolo de Extração de DNA Genômico a Partir de Sangue Total. Campo Grande: Embrapa MS, 2009. Comunicado Técnico 120. 2009. p. 5.
Barea JA, Pardini MIMC, Gushiken T. Extração de DNA de materiais de arquivo e fontes escassas para utilização em reação de polimerização em cadeia (PCR). Rev Bras Hematol Hemoter. 2004; 26(4): 274-81. [ Links ]
Buchanan FC, Fitzsimmons CJ, Van Kessel AG, Thue TD, Winkelman-Sim DC, Schmutz SM. Association of a missense mutation in the bovine leptin gene with carcass fat content and leptin mRNA levels. Genet Sel Evol. 2002; 34(1): 105-16. [ Links ]
Caldart ET, Chiappetta CM, Lopes EF, Ravazzolo A. Análise comparativa de métodos de extração de DNA genômico de células do sangue e do leite de pequenos ruminantes. Acta Sci Vet. 2011; 39(1), 945. [ Links ]
Canola PA, Oliveira R, Baldani CD, Machado RZ. Estudo Comparativo entre Técnicas de Extração de DNA e Realização da Reação em Cadeia da Polimerase (PCR) para o Diagnóstico de Theileria equi e Babesia caballi. ARS Veterinaria. 2007; 23(3): 165-71. [ Links ]
Crispim BA, Silva DBS, Banari AL, Seno LO, Grisolia AB. Discriminação alélica em ovinos naturalizados do Pantanal Sul-Matogrossense por meio de marcadores microssatélites. J Selva Andina Res Soc. 2012; 3: 3-13. [ Links ]
Dias-Salman AK, Mussolini-Laureano MM. Protocolos para extração de DNA genômico de amostras de pêlo de bovinos. Porto Velho. 2006. Circular técnica 87. p. 6.
Lee JH, Park Y, Choi JR, Lee EK, Kim HS. Comparisons of three automated systems for genomic DNA extraction in a clinical diagnostic laboratory. Yonsei Med J. 2010; 51(1): 104-10. [ Links ]
Magajevski FS, Gírio RJS. Avaliação da Sensibilidade da PCR frente a quatro Técnicas para Extração de DNA de Leptospira interrogans Sorovar Pomona em Sêmen Bovino Experimentalmente Contaminado. Ars Vet. 2008; 24(1): 29-33. [ Links ]
Marengoni NG, Machado MRF, Gasparino E. Extração de DNA genômico em tecidos sólidos de peixes teleósteos. Semin Ciênc Agrár. 2006; 27(1): 99-106. [ Links ]
Moore DD, Dowhan D. Preparation and analysis of DNA. In Current Protocols in Molecular Biology. 1995. p. 2–11. Edited by FM. Ausubel R, Brent RE, Kingston DD, Moore JG, Seidman J, Smith A, Struhl K. New York: Wiley.
Olerup O, Zetterquist H. HLA-DR typing by PCR amplification with sequencespecific primers (PCR-SSCP) in 2 hours: An alternative to serological DR typing in clinical practice including donor-recipient matching in cadaveric transplantation. Tissue Antigens. 1992; 39: 225-35. [ Links ]
Posnett ES, Fehrsen J, De Waal DT, Ambrosio RE. Detection of Babesia equi in infected horses and carrier animals using a DNA probe. Vet Parasitol. 1991; 39(1-2): 19-32. [ Links ]
Oliveira MCS, Regitano LCA, Roese AD, Anthonisen DG, Patrocínio E, Parma MM, et al. Fundamentos teórico-práticos e protocolos de extração e de amplificação de DNA por meio de reação em cadeia da polimerase. São Carlos: Embrapa Pecuária Sudeste; 2007. p. 43.
Promega. Technical Manual: Wizard®Genomic DNA Purification Kit. 2014. [Access: 08 jul 2016]. Available at:<https://www.promega.com.br/resources/protocols/technical-manuals/0/wizard-genomic-dna-purification-kit-protocol/> [ Links ].
R Development Core Team. R: A language and environment for statistical computing. R Foundation for Statistical Computing. Vienna, Austria. 2012. [ Links ]
Regitano LCA. Extração de DNA para aplicação em reação em cadeia da polimerase (PCR). In: Regitano LCA, Coutinho LL eds. Biologia molecular aplicada à produção animal. Brasília: Embrapa Informação Tecnológica. 2001. p. 180-86.
Sambrook J, Fritsch EF, Maniatis T. Molecular Cloning. A Laboratory Manual. 2ª ed. Cold Spring Harbor: Cold Spring Harbor Laboratory Press; 1989.
Silva LE, Santos DBS, Crispim BA, Vaini JO, Grisolia AB, Seno LO. Variação de concentração de proteinase K em protocolos de extração de DNA de bovino. Arch Vet Sci. 2013; 18(2): 15-9. [ Links ]
______________











 uBio
uBio