Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Científica Ciencia Médica
versión impresa ISSN 2077-3323
Rev Cient Cienc Méd vol.20 no.2 Cochabamba 2017
Artículo Original
METFORMINA EN EL TRATAMIENTO DEL SÍNDROME DE OVARIOS POLIQUÍSTICOS. UN ENSAYO CLÍNICO ALEATORIZADO.
METFORMIN IN THE POLYCYSTIC OVARIAN SYNDROME TREATMENT. A RANDOMIZED CLINICAL TRIAL.
Dra. Eonice Lopez Bascope1-2-4-a; Dr. Yercin Mamani Ortiz1-3-b-c-d; Dr. Gabriel RubénLamas Llanos1-b; Dr. Marlom Herrera Apaza1-b; Dra. Lizbeth Lazo2-a-c.
1 Facultad de Medicina, Universidad Mayor de San Simon, Cochabamba-Bolivia.
2 Seguro Social Universitario (SSU - UMSS);
3 Instituto de Investigaciones Biomédicas e Investigación Social (IIBISMED UMSS),
4 Hospital de Capinota-Cochabamba.
a Ginecóloga Obstetra.
b Médico Cirujano.
c Docente Investigador IIBISMED
d Doctorando en Salud Pública Umea University - Suecia.
Correspondencia a: Nombre: Yercin Mamani Ortiz
Correo electrónico: yercin2003@hotmail.com Telf. y celular: 70373111
Procedencia y arbitraje: no comisionado, sometido a arbitraje externo.
Recibido para publicación: 12 de noviembre 2017
Aceptado para publicación: 19 de diciembre 2017
Citar como: Rev Cient Cienc Med 2017;20(2): 45-52.
RESUMEN
Introducción: El Síndrome de Ovario Poliquístico, es la causa más frecuente de infertilidad anovulatoria; caracterizado por irregularidades menstruales, signos de exceso de andrógenos, obesidad y resistencia a la insulina.
Objetivo: Evaluar la inclusión de los sensibilizadores de insulina como la metformina en el tratamiento para Síndrome de ovario poliquístico, asociada con anticonceptivos orales combinados, versus la monoterapia con anticonceptivos orales combinados
Materiales y métodos: Se realizó un ensayo clínico aleatorizado con 60 mujeres de ≥18 años, divididas en 2 grupos homogéneos de 30 pacientes: uno recibió monoterapia con anticonceptivos orales combinados y otro recibió tratamiento combinado de anticonceptivos más metformina. El tratamiento se realizó durante 3 ciclos de 3 meses. La equivalencia terapéutica fue comparada mediante la "prueba T de Student" para muestras independientes. Se utilizó la regresión logística bivariada y regresión logística multimonial para la obtención del Odds Ratio crudos y ajustados.
Resultados: El tiempo promedio de remisión de la clínica, fue menor en la terapia combinada con 3,07±0,21 meses para la oligomenorrea, 3,07±0,21 meses para el acné, y 7,52±0,42 meses para el hirsutísimo; la diferencia entre las medias de remisión clínica fue estadísticamente significativa para la oligomenorrea (p=0,02) y el acné (p=0,001). La media del tiempo de remisión por ecografía fue menor en el grupo que recibió terapia combinada (6,7±0,23 meses), siendo esta diferencia estadísticamente significativa (p=<0,001).
Conclusión: El tratamiento combinado del Síndrome de ovario poliquístico con Anticonceptivos orales combinados + Metformina (500mg/día), favorece a una remisión ecográfica más corta, así como el de los síntomas asociados, y una menor tasa de recurrencia a los 3 meses.
Palabras clave: Ensayo Controlado Aleatorizado, Síndrome de Ovario Poliquístico, Metformina.
ABSTRACT
Background: Polycystic ovary syndrome is the most frequent cause of anovulatory infertility, characterized by menstrual irregularities, signs of androgen excess, obesityand insulin resistance.
Objective: To evaluate the inclusion of sensitizers as metformin, in the treatment of Polycystic ovary syndrome, combined with combined oral contraceptives, versus monotherapy with combined oral contraceptives
Materials and methods: A randomized clinical trial was conducted with 60 women aged ≥18 years, divided into 2 homogeneous groups of 30 patients: one received monotherapy with combined oral contraceptives and another received combined treatment of the contraceptives with Metformin. The treatment was performed during 3 cycles of 3 months each. The therapeutic equivalence was compared using the Student's T test for independent samples. Bivariate logistic regression and multimonial logistic regression were used to obtain crude and adjusted Odds Ratio.
Results: Average time of remission of the clinic sintoms was lower in the combined therapy, with 3,07 ± 0,21 months for Oligomenorrhea, 3,07 ± 0,21 months for acne, and 7,52 ± 0,42 months for hirsutism; the difference between the means of clinical remission was statistically significant for oligomenorrhea (p = 0,02) and acne (p = 0,001). The mean time of remission by ultrasound was lower in the group receiving combination therapy (6,7 ± 0,23 months), this difference being statistically significant (p = <0,001).
Conclusion: Combined treatment of Polycystic ovary syndrome with combined oral contraceptives + Metformin (500mg/day), favors a shorter ultrasound remission, as well as the associated symptoms, and a lower rate of recurrence at 3 months.
Keywords: Randomized Controlled Trial, Polycystic Ovary Syndrome, Metformin.
INTRODUCCIÓN
El Síndrome de Ovario Poliquístico (SOP), es una de las patologías endocrinas más frecuentes en mujeres en edad reproductiva de 18 a 45 años, con una prevalencia que varía entre 5 a 10% entre los diferentes estudios1-4. El cual se caracteriza por la presencia de oligo-anovulacion, hiperandrogenismo clínico o laboratorial y ovarios poliquísticos en la ultrasonografía; según el Panel de Consenso de Rotterdam-Holanda en 20032,3,5,6, es necesario dos de tres criterios para el diagnóstico, con o sin asociación de las otras manifestaciones clínicas encontradas como: irregularidades menstruales, signos de exceso de andrógenos (testosterona [T] libre o índice de T libre elevados); obesidad y resistencia a la insulina1. Sin embargo, la Androgen Excess Society Guidelines en 2006, incluye que es necesario demostrar: hiperandrogenismo clínico o laboratorial y oligo-anovulacion u ovarios poliquísticos; ambos criterios deben estar presentes para el diagnóstico7.
El SOP, tiene diversas consecuencias en la salud de la mujer; uno de los más importantes son los problemas reproductivos1; siendo considerada la causa más frecuente de infertilidad anovulatoria, 90 a 95% de mujeres que no pueden concebir presentan el síndrome de ovarios poliquísticos8,9; otros problemas se relacionan con el metabolismo, donde la mayor parte de los pacientes presenta dislipidemia con aumento de triglicéridos, disminución de lipoproteínas de alta densidad4,10; además de la resistencia a la insulina en un 50 a 80 % de las pacientes10; puede existir consecuencias psicológicas11, por las manifestaciones de hiperandrogenismo6, que pueden llevar a la paciente a un cuadro de depresión y ansiedad3 o a un desorden de bipolaridad12.
El inadecuado control o ausencia de tratamiento puede traer problemas a largo plazo, como enfermedades cardiovasculares13, hiperlipidemia14, obesidad15, problemas con el embarazo 1 y cáncer de endometrio, la mayoría de ellas relacionada con las alteraciones metabólicas que produce la resistencia a la insulina, que se presenta en la mayor cantidad de pacientes2,4,6,9,11,14.
La resistencia a la insulina, juega un rol fundamental en la fisiopatología del SOP4, estimulando la producción de andrógenos a nivel ovárico y suprarrenal, disminuyendo la proteína fijadora de esteroides sexuales y estimulando la secreción de hormona luteinizante, incrementado de esta forma la producción de andrógenos16; por lo que el uso de sensibilizantes a la insulina, como la metformina, demostró mejorar varios aspectos clínicos en diferentes grados, mostrando también efectos benéficos con los problemas reproductivos17,18.
Es por ello que más allá del tratamiento convencional con anticonceptivos orales, el presente estudio pretende evaluar la inclusión en el tratamiento del SOP, de los sensibilizadores de insulina como la metformina, asociada con anticonceptivos orales combinados (ACO), versus la monoterapia con ACO.
MATERIALES Y MÉTODOS
Se realizó un ensayo clínico aleatorizado no probabilístico, longitudinal-prospectivo; de verificación de equivalencia terapéutica entre la monoterapia con ACO versus la terapia combinada con Metformina + ACO, en pacientes con SOP, que acuden al servicio de ginecología del Seguro Social Universitario de la Universidad Mayor de San Simón (SSU-UMSS) en la ciudad de Cochabamba-Bolivia; durante el periodo comprendido entre enero 2015 a enero 2016.
La población de estudio estuvo conformada por todas las pacientes que acudieron al servicio de consulta externa de ginecología y recibieron un diagnóstico clínico de SOP (CIE-10: E-28.2)19 incluyendo la presencia de uno o más de los siguientes síntomas: obesidad, hirsutismo, acné, acantosis nigricans, oligomenorrea, dismenorrea y/o amenorrea6. El SOP fue confirmado por ultrasonografía en el Servicio de Imagenología del SSU-UMSS en base a los criterios de Rotterdam: Por lo menos un ovario que tenga: 1) 12 o más folículos (2-9 mm de diámetro) o 2) volumen ovárico mayor de 10 ml6.
Fueron elegibles para el estudio 80 pacientes, seleccionadas mediante un muestreo aleatorio no probabilístico y de asignación proporcional para ambos grupos; 10 de las cuales no cumplieron con los criterios de inclusión y 10 no aceptaron participar en el estudio; contándose con una muestra de 60 pacientes. Todas ellas, llegaron por primera vez al servicio y cumplieron los criterios de selección: a) pacientes con diagnóstico confirmado de SOP por ecografía; b) edad de 18 a 49 años de edad (basado en la frecuencia de casos este grupo etario6; c) aceptación de su participación en el estudio y el seguimiento posterior a los 9 meses de haber iniciado el tratamiento; d) control ultrasonográfico al 3er y 6to mes en caso de no remisión. Fueron excluidas del estudio, aquellas pacientes con: diabetes mellitus; antecedentes de ooforectomía unilateral, pacientes con insuficiencia venosa periférica, cardiopatía, en periodo de lactancia o con embarazo en curso.
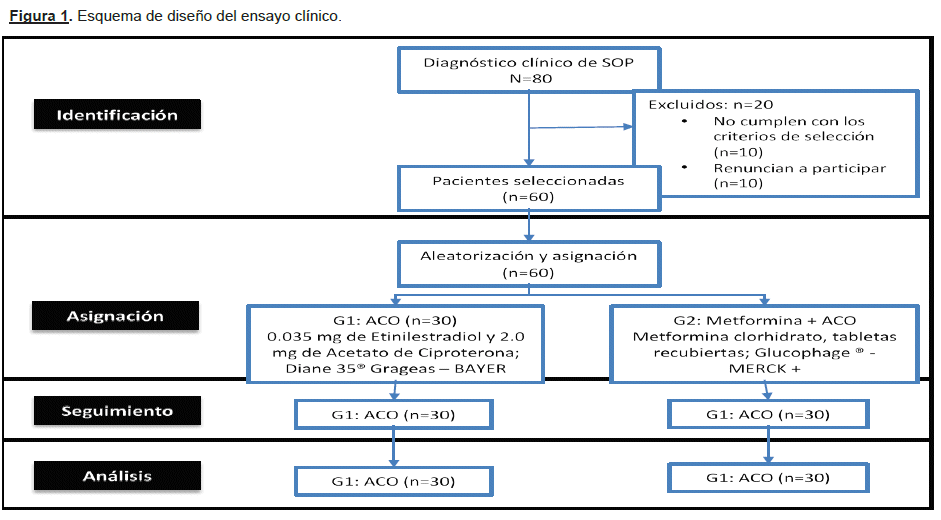
La muestra fue dividida en 2 grupos homogéneos de 30 pacientes por grupo: grupo de ensayo 1 (GE-1): monoterapia ACO (21 grageas por ciclo que contienen: 0,035 mg de etinilestradiol y 2,0 mg de acetato de ciproterona; Diane 35® Grageas - BAYER); Grupo de ensayo 2 (GE-2): metformina 500mg/día más ACO (metformina clorhidrato, tabletas recubiertas; Glucophage ® -MERCK). La asignación de los sujetos de estudio en cada grupo, fue realizada utilizando el método de aleatorización restrictiva o equilibrada, asegurándonos de que el número de sujetos de cada grupo del ensayo sea el mismo, para facilitar el análisis de los resultados20; calculándose con este tamaño muestral el poder del estudio (power=0,0912), el error Alfa (<x=0,051) y beta ((3=0,95) mediante el software PASS 2008®, conforme el modelo propuesto para pruebas secuenciales en grupos homogéneos, descrito por O'Brien (1979) ; respetando el tamaño muestral mínimo para ensayos clínicos de la Declaración CONSORT (acrónimo de CONsolidated Standards Of Reporting Trials), actualizada el 201021. (Ver Figura 1)
El tratamiento para ambos grupos de estudio se realizó durante 3 ciclos, cada uno de 3 meses, a la finalización de cada ciclo se realizó la verificación de cumplimiento del esquema de tratamiento con cada una de las pacientes en la consulta externa del servicio de ginecología, siendo este un requisito para la continuación dentro del estudio o en su defecto su alejamiento.
Los datos recolectados, se ingresaron en una matriz generada con Microsoft Excel® versión 2010. Para el análisis de los datos se usó el programa STATA/MP v-14.0®; así como para presentar e interpretar la información de los resultados para las variables de estudio, utilizando métodos de estadística descriptiva y pruebas paramétricas para la asociación entre variables, así como la significancia estadística.
La normalidad de las variables cuantitativas, fue verificada para cada grupo, mediante la prueba de Sktest (skewness/kurtosis test for normality; Test de asimetría/kurtosis para normalidad) con un valor de p= >(α=0,05)22; corroboradas por la prueba de Levene, de igualdad de varianza, entre ambos grupos para la comparación de medias. Los cálculos de medias aritméticas para las variables cuantitativas se acompañan de Desviaciones Estándar (DE) así como el Intervalo de Confianza al 95% (95% IC). La verificación de la equivalencia terapéutica fue comparada mediante la prueba de T de Student para muestras independientes con los datos grupales.
Se realizó también un análisis con Chi cuadrado (X2) para la evaluación de la asociación estadística entre cada uno de los efectos colaterales y la pertenencia al grupo de estudio de referencia (MET-ACO). Se utilizó la regresión logística bivariada para el cálculo de Odds Ratio (OR) crudos para cada uno de estos efectos colaterales por subgrupo de estudio y la regresión logística multimonial para la obtención del OR ajustado para explicar el efecto del tratamiento propuesto sobre los efectos colaterales.
Para evaluar la edad como una variable de confusión (confundente) en la remisión del cuadro, así como de la sintomatología asociada, se utilizó la correlación de Pearson, además de una desagregación de proporciones por grupo etario entre las que remitieron su sintomatología por encima de los 6 meses como parámetro de control.
Limitaciones del estudio:
Cabe resaltar que el presente estudio cuenta con diversas limitaciones en relación a la recolección de la información y a la inclusión de variables de estudio, debido a que para el mismo se utilizaron las evaluaciones estipuladas en los protocolos de atención institucionales para esta patología, sin considerar otras variables laboratoriales (perfil hormonal, lipídico y glicémico) que pudieran complementar el análisis de los resultados; los mismos que tienen un costo elevado en nuestro medio y no podía correr por cuenta del equipo de investigación ni de las participantes; utilizando el criterio clínico y ecográfico como herramientas de inclusión, seguimiento y control de las pacientes que participaron del estudio.
Consideraciones Éticas
El presente trabajo contó con la aprobación del comité de investigación del Seguro Social Universitario, ante la ausencia de un comité de ética institucional. Todos los pacientes mayores de edad y hábiles por derecho, firmaron el consentimiento informado, dentro de lo estipulado en la Declaración de Helsinki, actualizada en la Asamblea General de la Asociación Médica Mundial, en Seúl-Corea-2008. Se mantuvo el principio de confidencialidad tomando en cuenta la identificación personal a través del número de la historia clínica y se aseguró el seguimiento posterior de las pacientes que no remitieron su sintomatología hasta los 9 meses que duró el estudio, con un manejo multidisciplinario, apoyados por otras unidades del hospital hasta su remisión.
RESULTADOS
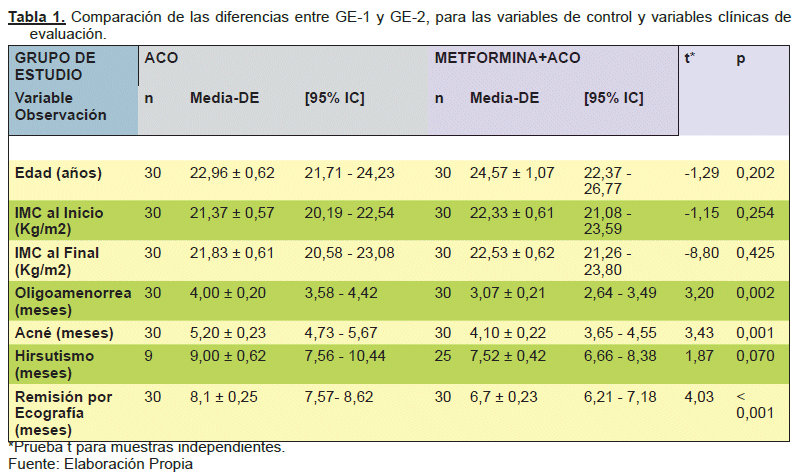
Luego de analizados los datos, observamos que el 50% de las pacientes fueron estudiantes (n=30) y 50% fueron trabajadoras universitarias aseguradas (n=30) (entre docentes y administrativas), de las cuales la distribución de las estudiantes fue mayor en el grupo de la Monoterapia con ACO, y por el contrario el grupo de trabajadoras universitarias aseguradas estuvo en mayor proporción incluida en el tratamiento combinado de ACO+Metformina; sin embargo, la edad media de ambos grupos fue similar; con un 22,96±0,62 años en el grupo de la monoterapia; y de 24,57±1,07 años en el grupo de la terapia combinada; y si bien existe una diferencia, esta no es estadísticamente significativa (p=0,202). De la misma manera, el Índice de Masa Corporal (IMC) al inicio y al final del estudio, no tienen una diferencia significativa entre ambos grupos (p=>0,05), asegurándose de esta manera que son 2 poblaciones equiparables y comparables en relación a estas variables de estudio. (Ver Tabla N°1)
Con relación a los principales criterios clínicos diagnósticos del síndrome de ovario poliquístico el 100% de las pacientes presentaron oligomenorrea y acné; ambos de manejos farmacológicos y solamente 34 pacientes presentaron hirsutismo que representa un 55,6%. El tiempo promedio de remisión de la clínica, fue menor en la terapia combinada con 3,07±0,21 meses para la oligomenorrea; 3,07±0,21 meses para el acné y 7,52±0,42 meses para el hirsutismo; la diferencia entre las medias de remisión clínica fue significativa para la oligomenorrea (p=0,02) y el acné (p=0,001), pero no así para el hirsutismo (p=0,070). (Ver Tabla N° 1)
La media del tiempo de remisión por ecografía fue menor en el grupo que recibió terapia combinada (6,7±0,23 meses) en relación con el que recibió monoterapia con ACO, en la que fue mayor (8,10 ±0,25 meses), siendo esta diferencia estadísticamente significativa (p=< 0,001). (Ver Tabla N° 1)
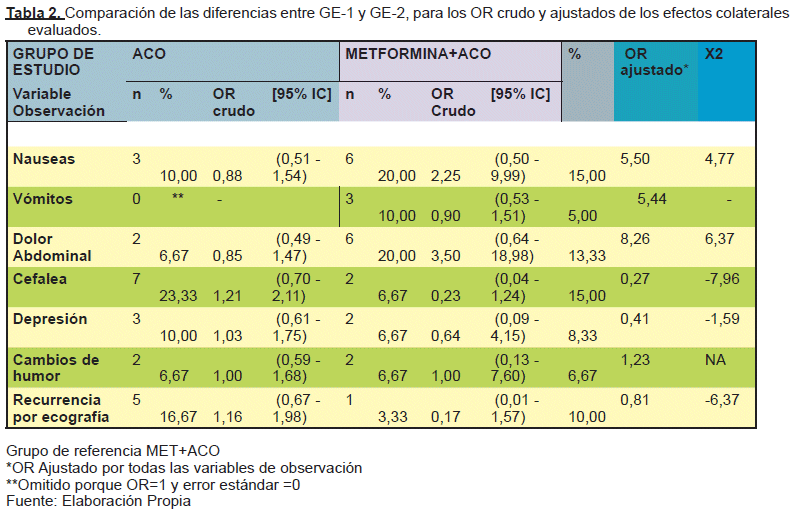
Los efectos colaterales informados por las pacientes durante el periodo de tratamiento, fue variado en ambos grupos siendo mayor las náuseas (20%, n=6), el dolor abdominal (20%, n=6) y los vómitos (10%, n=3) en el grupo que recibió la terapia combinada entre ACO+Metformina. Por el contrario, el grupo que recibió monoterapia presentó una mayor frecuencia de casos de cefalea (23,33%, n=7), náuseas y depresión (10%, n=3). En ambos grupos, fue similar la proporción de presentación de los cambios de humor como efecto adverso al tratamiento recibido (6,67%, n=2). (Ver Tabla N° 2)
Se realizó el cálculo de OR crudo mediante regresión logística binaria, para analizar el riesgo de padecer estos efectos colaterales por la pertenencia a un grupo de estudio específico fue comprobada para la cefalea y el cambio de humor en el grupo que recibió solo ACO, así como las náuseas y dolor abdominal en el grupo que recibió terapia combinada (OR crudo=>1). El OR ajustado para todos los efectos adversos muestra niveles de riesgo para las náuseas, vómitos, dolor abdominal y los cambios de humor; considerando el grupo que recibió terapia combinada como referencia para el análisis (OR ajustado=>1), corroboradas por la prueba de Chi-2 (X2) para la asociación estadística entre las pertenencia a un grupo específico de estudio y la presencia o ausencia del efecto colateral (X2=±1), observando el efecto protector de la terapia combinada frente a la cefalea (X2= -7,96) y la depresión (X2= -1,59). (Ver Tabla N° 2)
Así mismo observamos que la recurrencia ecográfica del SOP al tercer mes luego de haber concluido el esquema de tratamiento, fue sustancialmente menor en el tratamiento combinado (3,33%, n=1) en relación a la monoterapia donde la recurrencia alcanzó el 17%, n=5), el riesgo de recurrencia solo fue válida en el grupo de ACO (OR crudo=1,16) y no así para el grupo que recibió el tratamiento combinado; donde tanto el OR crudo como el OR ajustado fueron inferiores a 1, considerándose un efecto protector, corroborada por la asociación negativa por la prueba de Chi-2 (X2=-6,37). (Ver Tabla N°2)
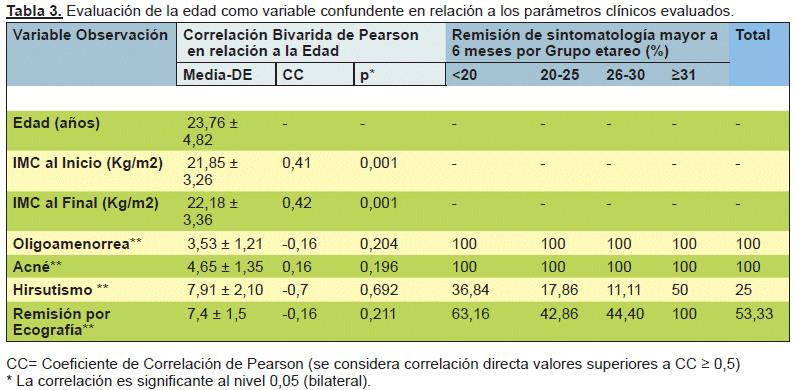
Otro hallazgo llamativo que se debe reportar, es que la ganancia de peso en ambos grupos fue similar, con una media de 0,56±0,20 kg en el grupo de la monoterapia, frente a los 0,20±0,13 Kg de la terapia combinada; sin embargo, este factor no representa un factor confundente de los hallazgos reportados, al igual que la edad; por lo que se realizó un análisis de correlación bivariada de Pearson, en el que no se observa una correlación directa (CC Pearson ≥ 0,5) entre ninguna de las variables y la edad. Así mismo, se desagregó el porcentaje de remisión de la sintomatología por encima de los 6 meses para cada uno de los grupos etarios; donde tampoco se observa una relación lineal ascendente entre ninguno de los síntomas evaluados y la edad. (Ver Tabla N° 3)
DISCUSIÓN
Los hallazgos del presente estudio son muy particulares por el tipo de población estudiada, mujeres jóvenes en edad fértil del Seguro Social Universitario. Es por ello que es importante resaltar que en el estudio participaron grupos proporcionales de estudiantes, así como trabajadoras universitarias, evaluándose la homogeneidad de ambos grupos que son equiparables y/o comparables.
Siguiendo el planteamiento del estudio, observamos claramente que el tiempo de remisión por ecografía es mucho menor en el tratamiento combinado con ACO + Metformina, en algunos casos con hasta 3 meses de diferencia en relación a la media del grupo que recibió monoterapia, similar a lo reportado por D. Cibula et al (2004) que en un ensayo clínico realizado con 28 mujeres con SOP23, observaron una remisión a los 6 meses, mayor en el grupo que recibió metformina a dosis de 1 500 mg/dia, en comparación con el ACO (250 μg de norgestimato y 35 μg de etinilestradiol); siendo la concentración de metformina utilizada en nuestro estudio mucho menor al del estudio de referencia; en este mismo estudio se reporta un efecto positivo de la terapia combinada en relación a la glucosa alterada en ayunas, la resistencia a la insulina, así como la testosterona libre, sin embargo observaron que en ambos grupos de estudio los niveles del perfil lipídico se elevaron. Estos parámetros no fueron evaluados en nuestro estudio por las limitaciones económicas; sin embargo, serán considerados como base para un estudio posterior23.
Al igual que la anterior, la clínica remitió marcadamente en menos tiempo en el grupo que recibió la terapia combinada, en todos los parámetros evaluados (oligomenorrea, acné, hirsutismo), estos hallazgos son contrarios a los hallazgos reportados por Iwata et al (2015) comparó 3 grupos: el grupo 1 recibió ACO (etinilestradiol 35 μg, ciproterona 2mg), el grupo 2 recibió metformina (850mg/12h) y el grupo 3 ACO+Metformina , reportando una mayor reducción del acné y el hirsutismo (escala de Ferriman -Gallwey Ferriman) a los 6 meses de seguimiento en el grupo que recibió solo ACO. Este aspecto es muy importante, considerando que las pacientes acuden en primer lugar por estos signos clínicos y no así por una valoración específica del SOP, por lo que la aceptación del tratamiento es mayor, por el hecho de la observancia de la remisión de los síntomas y signos característicos de la patología.
Los efectos adversos durante el tratamiento, si bien fueron en una proporción menor al 23% en todos los casos, fue mayor en algunos síntomas, como las náuseas, vómitos y el dolor abdominal en el grupo del tratamiento combinado; estos síntomas deben ser mejor estudiados para mejorar la aceptación de este tratamiento en un próximo estudio; estos parámetros clínicos no son evaluados en los estudios de referencia, siendo los parámetros laboratoriales más evaluados, es así que Iwata et al (2015), reportan un incremento en los niveles de hormona luteinizante en el grupo que recibió terapia combinada23.
Sin embargo, se resalta que además de una rápida remisión por ecografía; la recurrencia por ecografía, también fue sustancialmente menor, presentándose en apenas el 3% de casos en comparación al de la terapia combinada, ello favorece a la recomendación del uso de este tratamiento en las pacientes atendidas por SOP, apoyadas por los hallazgos D. Cibula et al., que reportan una regulación del perfil hormonal (testosterona, H. luteinizante) así como el perfil glicémico y/o insulina; mismos que deberán ser considerados en estudios posteriores, como parte de la asociación del SOP al síndrome metabólico23.
Un hallazgo casual, pero no menos importante, es el de la ganancia de peso, medido por incremento en el IMC, donde observamos que ambos grupos presentaron una elevación mínima en promedio, siendo relativamente inferior en el grupo que recibió tratamiento combinado. Este aspecto es muy importante, pues este factor es el que en muchos casos genera el abandono del tratamiento por tratarse de una población joven que cuida bastante el peso corporal por los cánones de belleza inmersos en nuestra población.
CONCLUSIÓN
En base a la evidencia del presente trabajo; podemos concluir que el tratamiento combinado del SOP con ACO + Metformina (500mg/día), favorece a una remisión ecográfica más corta, así como el de los síntomas asociados (oligomenorrea, acné e hirsutismo), con una tasa de recurrencia a los 3 meses inferior en comparación al grupo de estudio que recibió monoterapia con ACO.
RECOMENDACIONES
En base a los hallazgos del presente estudio, se sugiere actualizar y modificar los protocolos de atención vigentes para el SOP en nuestro medio y considerar la evaluación del síndrome metabólico en pacientes con SOP y viceversa; así como la inclusión de la metformina en los protocolos de manejo terapéutico.
AGRADECIMIENTOS:
Nuestro equipo de investigación agradece al Seguro Social Universitario de la Universidad Mayor de San Simón, por el apoyo logístico brindado para el presente estudio.
Conflictos de intereses: Los autores declaramos no tener ningún conflicto de intereses con la institución donde se realizó el trabajo de investigación.
REFERENCIAS
1. Pacheco J. Manejo del síndrome de ovario poliquístico en la mujer infértil. Notas recientes sobre el Consenso de Thessaloniki; Rev Per Ginecol Obstet; 2008; 54(2). Disponible en: http://www.spog.org.pe/web/revista/index.php/RPGO/article/view/1103/pdf_121. [ Links ]
2. Merino P, Schulin-Zeuthen C, Codner E. Diagnóstico del síndrome de ovario poliquístico: nuevos fenotipos, nuevas incógnitas;Rev méd Chile;2009; 137(8):1071-80 Disponible en: http://www.scielo.cl/scielo.php?pid=S0034-98872009000800012&script=sci_arttext&tlng=en. [ Links ]
3. Sir PT, Preisler RJ, Magendzo NA. Síndrome de ovario poliquístico. diagnóstico y manejo;Rev Med Clin Condes;2013; 24(5): 818-26 Disponible en: http://www.sciencedirect.com/science/article/pii/S0716864013702293. [ Links ]
4. Borbón Cordero MF, Robles Quirós F. Síndrome de Ovario Poliquistico. Rev Clin Esc Med; 2016; 6(1):134-7. Disponible en: http://new.medigraphic.com/cgi-bin/resumen.cgi?IDARTICULO=63866. [ Links ]
5. Capella D, Aedo S, Irribarra C. Consensos existentes para el diagnóstico del Síndrome de Ovario Poliquístico;Rev Obstet Ginecol;2014;14(1):39-44. Disponible en: https://goo.gl/HpMZzG [ Links ]
6. Aparcana R, Pacheco J. Síndrome de ovario poliquístico y el Consenso de Rótterdam. Rev Per Ginecol Obstet;2004;50(1):45-60. Disponible en: http://spog.org.pe/web/revista/index.php/RPGO/article/view/440/408. [ Links ]
7. Azziz R, Carmina E, Dewailly D, Diamanti-Kandarakis E, Escobar-Morreale HF, Futterweit W, et al. The Androgen Excess and PCOS Society criteria for the polycystic ovary syndrome: the complete task force report. Fertility and sterility;2009; 91(2):456-88.Disponible en: http://www.sciencedirect.com/science/article/pii/S0015028208013927. [ Links ]
8. Rojas P, Medina D, Torres L. Infertilidad;MediSur;2011; 9(4):66-77.Disponible en: http://www.redalyc.org/pdf/1800/180022368012.pdf. [ Links ]
9. Vázquez JC, Calero JL, Carías JP, Monteagudo G. Correspondencia clínica, hormonal y ecográfica en el diagnóstico del síndrome de ovarios poliquísticos;Rev Cubana Endocrinol; 2016;27(1):4-17. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1561-29532016000100002. [ Links ]
10. Roa M, Arata-Bellabarba G, Valeri L, Velázquez-Maldonado E. Relación entre el cociente triglicéridos/cHDL, índices de resistencia a la insulina y factores de riesgo cardiometabólico en mujeres con síndrome del ovario poliquístico;Endocrinología y Nutrición; 2009;56(2):59-65.Disponible en: http://www.sciencedirect.com/science/article/pii/S1575092209705534. [ Links ]
11. Gómez-Acosta CA, Vinaccia S, Quiceno JM. El síndrome de ovario poliquístico: aspectos psicológicos;Rev chil obstet ginecol;2015;80(4):341-7. Disponible en: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0717-75262015000400010&nrm=iso. [ Links ]
12. Rodríguez M, Gempeler J, Pérez V, Ribero O. Polycystic ovarian syndrome and its potential association with bipolar disorder in patients with eating disorder; Revista Mexicana de Trastornos Alimentarios;2017;8(2):142-50. Disponible en: http://www.sciencedirect.com/science/article/pii/S2007152317300113. [ Links ]
13. García VM. Estudio del riesgo cardiovascular en pacientes con Síndrome de Ovario Poliquístico (SOP) [Tesis Doctoral].Creación de grupos de riesgo;2015. Disponible en: http://roderic.uv.es/bitstream/handle/10550/47056/tesis%20final.pdf?sequence=1&isAllowed=y.
14. Jiménez M, Iturrieta G, Aguilera S, Cárcamo R, Galvez N, Valdés G. Características clínicas y metabólicas de síndrome de ovario poliquístico en la ciudad de Temuco;Rev chil endocrinol diabetes;2014;7(3):85-88.Disponible en: http://revistasoched.cl/3_2014/2-Jimenez.pdf. [ Links ]
15. Gutiérrez C, Villavicencio A, Lozano C-A, Lozano-Hernández R. Tensión arterial y masa corporal en mujeres infértiles con síndrome de ovario poliquístico y su relación con el perfil hormonal;Rev Obstet Ginecol Venez; 2014;74(3):170-6. Disponible en: http://www.scielo.org.ve/scielo.php?pid=S0048-77322014000300005&script=sci_arttext. [ Links ]
16. Rodríguez J, Puig M. Relación entre la insulinorresistencia y el síndrome de ovario poliquístico y sus comorbilidades metabólicas;Rev Cubana Med Gen Integr; 2013;30(4). Disponible en: http://www.medigraphic.com/pdfs/revcubmedgenint/cmi-2015/cmi154j.pdf. [ Links ]
17. Thessaloniki-ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Consensus on infertility treatment related to polycystic ovary syndrome. Fertility and Sterility;2008;89(3):505-22.Disponible en: http://www.sciencedirect.com/science/article/pii/S0015028207036618. [ Links ]
18. Tominaga LV, Lechuga AV, Pella R, Sierra J, Núñez L, Cuadros R. Mejores tasas de éxito de FIV/ICSI con el uso de metformina en mujeres con ovario poliquístico;Rev Per Ginecol Obstet;2015;56(4):289-93.Disponible en: http://www.spog.org.pe/web/revista/index.php/RPGO/article/view/213. [ Links ]
19. Sáez C, Rocha A, Torres M, Urra-Canales A, Muñoz J. Epidemiología del síndrome de ovario poliquístico en Chillán-Chile;Rev ANACEM;2016;10(1). Disponible en: http://www.revistaanacem.cl/wp-content/uploads/2016/12/3.-EPUB2016101.16-TC-012.pdf. [ Links ]
20. Piaggio G, Elbourne DR, Pocock SJ, Evans SJ, Altman DG, Group C. Reporting of noninferiority and equivalence randomized trials: extension of the CONSORT 2010 statement;JAMA;2012;308(24):2594-604.Disponible en: https://www.ncbi.nlm.nih.gov/pubmed/23268518 [ Links ]
21. Cobos-Carbo A, Augustovski F. Declaración CONSORT 2010: actualización de la lista de comprobación para informar ensayos clínicos aleatorizados de grupos paralelos;Med clín (Barc);2011;137(5):213-15.Disponible en: http://www.consort-statement.org/Media/Default/Downloads/Translations/Spanish_es/Spanish%20CONSORT%20Statement.pdf [ Links ]
22. Ghasemi A, Zahediasl S. Normality tests for statistical analysis: a guide for non-statisticians;Int Journal Endocrinol Metab;2012;10(2):486-89.Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3693611/. [ Links ]
23. Iwata MC, Porquere L, Sorpreso ICE, Baracat EC, Soares Júnior JM. Association of oral contraceptive and metformin did not improve insulin resistance in women with polycystic ovary syndrome;Rev Assoc Med Bras;2015;61(3):215-19.Disponible en: http://www.scielo.br/scielo.php?pid=S0104-42302015000300215&script=sci_arttext. [ Links ]