Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista Científica Ciencia Médica
versión impresa ISSN 2077-3323
Rev Cient Cienc Méd vol.18 no.2 Cochabamba 2015
ARTÍCULO ORIGINAL
Expresión del ki-67, p53, p16 y bcl-2 en Ameloblastomas
Expression of ki-67, p53, p16 and bcl-2 in Ameloblastomas
Fleischmacher Abrahamz Noelia1; Rivera Helen2
1Odontólogo. Postgrado de Cirugía Bucal. Universidad Central de Venezuela. Facultad de Odontología
2 Patólogo Bucomaxilo facial. Instituto de Investigaciones Odontológicas "Raúl Vicentelli". Universidad Central de Venezuela. Facultad de Odontología.
Correspondencia a: Fleischmacher Abrahamz Noelia
fleischmacher@hotmail.com
Procedencia y arbitraje: no comisionado, sometido a arbitraje externo.
Recibido para publicación: 14 de Mayo del 2015
Aceptado para publicación: 01 de Junio del 2015
Citar como: Rev Cient Cienc Med 2015;18(2): 18-23
Abreviaturas utilizadas en este artículo:
AB = Ameloblastoma
OMS = Organización Mundial de la Salud
AS = Ameloblastoma sólido
AU = Ameloblastoma uniquístico
AD = Ameloblastoma Desmoplásico
AP = Ameloblastoma Periférico
IREPO = Instituto de Referencia de Patología Oral
TOQQ = Tumor Odontogénico Queratoquístico
TOA = Tumor Odontogénico Adenomatoide
RESUMEN
El objetivo de la presente investigación fue determinar la expresión de Ki-67, p53, p 16 y bcl-2 en Ameloblastoma Sólido y Uniquístico. El presente estudio fue retrospectivo de tipo clínico-patológico, experimental y correlacional. Se realizó análisis clínico-patológico de las variables: género, grupos de edad, diagnóstico histopatológico y localización anatómica y análisis inmunohistoquímico siguiendo protocolo estandarizado utilizando los marcadores Ki-67, p16, p53 y bcl-2 en el Laboratorio de Histopatología Bucal "Dr. Pedro Tinoco" de la Facultad de Odontología de la Universidad Central de Venezuela durante el período 2008-2013. De las biopsias bucomaxilofaciales se tomaron como muestra 34 casos diagnosticados histopatológicamente como Ameloblastoma Uniquístico (16 casos), Ameloblastoma Sólido (9 casos), y 9 casos como control con el diagnóstico de Tumor Odontogénico Queratoquístico. Se realizó análisis estadístico para correlación de variables a través de la prueba Kruskall-Wallis empleando Software estadístico SPSS®Versión N° 20 para sistema MAC OSX con un nivel de significancia del 99% (p<0,01). Se observó predominio del género masculino entre la segunda y tercera década de vida. Localización anatómica más frecuente en sector posterior mandibular, diagnóstico histopatológico más frecuente ameloblastoma uniquístico. El análisis inmunohistoquímico reveló al marcador Ki-67 como la más expresada, seguida por p53, bcl-2 y p16 indicando transformación neoplásica y proliferación asociado a tasa de recidiva Los marcadores utilizados son de utilidad para evaluar comportamiento biológico para sugerir tratamiento quirúrgico adecuado en cada caso.
Palabras clave: Ameloblastoma, Inmunohistoquímica, Pronóstico
ABSTRACT
The objective of this research was to determine the expression of Ki-67, p53, p16 and bcl-2 Solid and unicystic Ameloblastoma.This study was retrospective clinicopathological, experimental and correlational. Clinico-pathological analysis of the variables were: gender, age, anatomical site and histopathological diagnosis and immunohistochemical analysis using standardized protocol following the Ki-67, p16, p53 and bcl-2 markers in the Laboratory of Oral Histopathology "Dr. Pedro Tinoco "of the Faculty of Dentistry, Central University ofVenezuela during the period 2008-2013.The maxillofacial biopsies were sampled 34 cases diagnosed histopathologically as Ameloblastoma unicystic (16 cases), Ameloblastoma Solid (9 cases), and 9 cases as control diagnosis Odontogenic Tumor Queratoquístico statistical analysis for correlation of variables was performed through the Kruskal-Wallis test using SPSS statistical software version No. 20 MAC OSX system with a significance level of 99% (p <0.01).often males between the second and third decade of life was observed. Most frequent anatomical location in mandibular posterior, more frequent histopathological diagnosis unicystic ameloblastoma. Immunohistochemical analysis revealed the marcador Ki-67 as the expressed, followed by p53, bcl-2 and p16 indicating neoplastic transformation and proliferation associated with recurrence rate markers used are useful for assessing biological behavior to suggest appropriate surgical treatment in each case.
Keywords: Ameloblastoma, Immunohistochemistry, Prognosis
INTRODUCCIÓN
El ameloblastoma (AB) es un tumor benigno de epitelio odontogénico maduro, con estroma fibroso sin ectomesénquima odontogénico1 y constituye uno de los tumores odontogénicos más frecuentes1. Su presentación más común es en mandíbula en región posterior en pacientes del sexo masculino entre la tercera y cuarta década de la vida2. Según la clasificación histológica de los tumores odontogénicos propuesta por la Organización Mundial de la Salud (OMS)1 el AB ha sido clasificado en cuatro entidades distintas, reconociéndose el ameloblastoma sólido (AS), uniquístico (AU), desmoplásico (AD) y periférico (AP)1.
La conducta del AB es variable, hasta la fecha en nuestro país, no disponemos de resultados de estudios inmunohistoquímicos en relación al AB en términos de predicción de comportamiento biológico.
En la actualidad se han venido realizando técnicas moleculares, las cuales pretenden identificar expresión genética, diferenciación y transformación maligna; ayudándonos a relacionar pronóstico y manejo quirúrgico de los mismos.
Los marcadores pronóstico son moléculas que se expresan durante las distintas fases del ciclo celular, lo que podría indicar la proliferación activa de la célula o el potencial de transformación oncogénica3. Esta expresión molecular puede ser identificada por medio de técnicas de inmuno-histoquímica. La utilidad diagnóstica de esta técnica radica en que por medio de esta podemos identificar diferenciación y proliferación celular mediante marcadores tumorales específicos3.
El objetivo general de la investigación fue determinar la expresión de ki-67, p53, p16 y bcl-2 en AS y AU que orientan a la relación entre el pronóstico y el manejo quirúrgico de los mismos a través de la correlación de la expresión de los marcadores tumorales con la localización anatómica, diagnóstico histopatológico, género y grupos de edad, tomando como grupos control para el análisis inmunohistoquímico muestras de Tumor Odontogénico Queratoquístico.
En el Instituto de Referencia de Patología Oral (IREPO), de la Facultad de Odontología de la Universidad de Chile se realizó un estudio cuyo objetivo fue comparar el recuento de inmuno-tinción de p53 y Ki-67 en Tumor Odontogénico Queratoquístico (TOQQ) y en AS. En ambos tumores la expresión de p53 fue mayor respecto a la de Ki-67, con una diferencia estadísticamente significativa3.
En el Laboratorio de Patología del Hospital de Emergencia del Condado de Craiova estudiaron la expresión de p53, bcl-2 y Ki-67 en células epiteliales tumorales en AB. La inmunoexpresión de p53 y Bcl-2 se identificó en más del 50% de las células marcadas4.
MATERIALES Y MÉTODOS
Se realizó un estudio retrospectivo de tipo clínico-patológico, experimental y correlacional, que consistió en analizar la expresión de los oncogenes y marcadores de proliferación en AS y AU de los maxilares. Fue realizada en las instalaciones del Laboratorio de Histopatología Bucal "Dr. Pedro Tinoco", adscrita al Instituto de Investigaciones Odontológicas "Raúl Vicentelli" de la Facultad de Odontología de la Universidad Central de Venezuela durante el período 2008-2013.
De un total de 17 224 biopsias bucomaxilofaciales, se seleccionó una muestra que consistió en 34 casos con el diagnóstico histopatológico de AU (16 casos), AS (9 casos) y Tumor Odontogénico Queratoquístico (TOQQ) (9 casos) como casos control ya que ambos son considerados neoplasias benignas odontogénicas, las que difieren notoriamente en su pronóstico y plan de tratamiento.
Se consideraron como criterios de inclusión a las biopsias bucomaxilofaciales con el diagnóstico histopatológico de AU y AS que aceptaron firmar el consentimiento informado. Se excluyeron pacientes con otras patologías de los maxilares.
La investigación fue evaluada y aprobada por el Comité de Bioética de la Facultad de Odontología de la Universidad Central de Venezuela, contando con el respaldo de un consentimiento informado de los participantes, se consideró aspectos bioéticos para la toma de muestra, obtención de láminas y bloques a ser usados en la investigación.
Una vez seleccionados los casos a estudiar, se reclasificaron histológicamente de acuerdo a la clasificación de la OMS (2005)1.
Desde el punto de vista clínico-patológico se cuantificaron los datos correspondientes a las variables: género, grupo etario, diagnóstico histopatológico y localización anatómica.
En cuanto al análisis clínico-patológico no fueron tomados en cuenta los casos de Tumor Odontogénico Queratoquístico, ya que, los mismos, se utilizaron como casos control en el análisis inmunohistoquímico.
En cuanto al análisis inmunohistoquímico de la muestra estudiada se evaluaron el Ameloblastoma en sus variantes Sólida y Uniquística y el Tumor Odontogénico Queratoquístico (TOQQ) como casos controles; siendo ambos tumores epiteliales y de comportamiento clínico agresivo, considerados neoplasias benignas odontogénicas, las que difieren notoriamente en su pronóstico y plan de tratamiento.
Se realizaron cortes a partir de 3μm de los bloques en parafina correspondientes a cada caso a estudiar y de los controles adecuados para cada anticuerpo. Se utilizaron láminas silanizadas y se realizó la técnica inmunohistoquímica siguiendo protocolo estandarizado.
Los anticuerpos primarios utilizados para detectar los antígenos fueron Ki-67 (clon SP6; Biocare®, USA) dilución 1:200; p53 (clon DO-7; Dako®, Cytomation, USA) dilución 1:100; p16 (clon INK4; Biogenexx®, USA) dilución 1:100; bcl2 (clon 124; Dako®, Cytomation, USA) dilución 1:50. El sistema de detección fue Starr Trekk Universal HRP Detection System (Biocare®, USA) a un pH de 6,0. La solución recuperadora fue Solución Buffer Citrato al 0,05% y pH 6,0 (Tween20®, USA), como revelador Diaminobenzidina (DAB) cromógeno estable (Biocare®, USA) y se utilizaron láminas silanizadas (Dako®, Cytomation, USA).
Para los cortes de inmunohistoquímica, se examinaron los patrones de expresión de los diferentes marcadores en los tejidos, utilizando una escala semicuantitativa de 0 a 3 cruces (+) para marcaje positivo y "sin expresión" o negativo (-) para tejidos no marcados.
Se evaluó la localización de la inmunoreacción del anticuerpo a nivel celular, determinando si se encontraba en: Membrana Citoplasmática, Núcleo o Citoplasma. Para la inmunoreacción positiva del gen p16 también se evaluó si se encontraba: Localizada con patrón débil localizado o difuso con patrón fuerte.
Una vez registrados los datos en un instrumento de recolección de información, se organizaron, procesaron y tabularon las variables en estudio, realizando los diferentes cruces de categorías de variables.
Desde el punto de vista descriptivo, la información recolectada durante el proceso experimental se ordenó en forma de cuadros de frecuencia para cada variable, se relacionó a su vez con otras variables estudiadas para su análisis y discusión. Utilizando parámetros estadísticos descriptivos: Media, Desviación Típica y porcentajes para medir los resultados de las diferentes variables.
Desde el punto de vista inferencial, se empleó la Prueba de Kruskall-Wallis (k) para medir el grado de asociación y variabilidad de los diferentes AB en relación a las variables clínicas, histopatológicas e inmunohisto químicas y la Prueba de Odds ratios para evaluar las correlaciones entre las variables clínicas, histopatológicas e inmuno-histoquímicas, con un Nivel de Significancia del 99% (p<0,01) a través del Software estadístico SPSS® en español Versión N° 20 para sistema MAC OSX.
RESULTADOS
La distribución de acuerdo al diagnóstico histopatológico presento para AU 64% de los casos diagnosticados mientras que el AS presentó un 36% de los mismos.
El género masculino en ambos tipos de AB representa un 60% de los casos, en el femenino un 40%.
El rango de edad fue de 10 a 69 años, con un promedio de 32 años y desviación de ±16 años. El grupo de edad con mayor frecuencia fue el comprendido entre 20 a 29 años con 32%, seguido por el grupo de 30 a 39 años con 24%. El grupo de 10 a 19 años con 20%, el grupo de 40 a 49 años y 60 a 69 años 12% respectivamente. El AS y AU se presentaron en mandíbula en un 71% y en maxilar en un 29%. El AS presentó 4 localizaciones anteriores y 6 localizaciones posteriores; mientras que el AU presentó 3 localizaciones anteriores y 15 posteriores
En la presente investigación se observó inmunopositividad en AS para ki-67 con 88,9%, p53 con 88,9% y bcl-2 con 77,8%; para p16 el resultado estadísticamente significativo (p<0,01) fue para los casos control con el 100%. (Grafico 1)
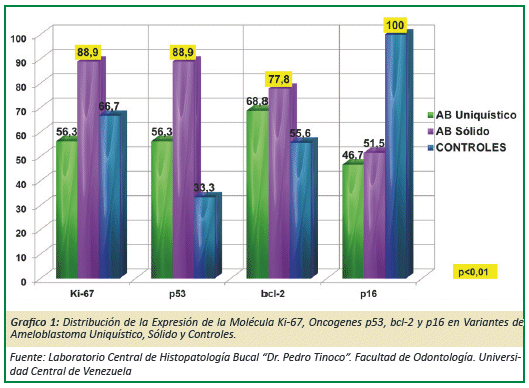
La expresión de los marcadores fue el siguiente: 11 casos de AU para bcl-2 en citoplasma; en AS 8 casos para ki-67 y p53 en núcleo respectivamente y 7 casos para bcl-2 en citoplasma, para los casos controles fueron para ki-67 con 6 casos en núcleo y bcl-2 con 5 casos en citoplasma. (Grafico 2)
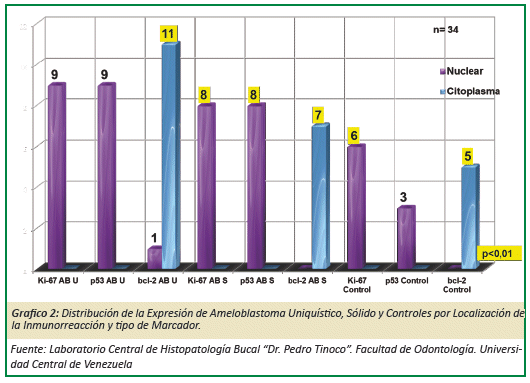
El nivel de expresión de estos marcadores mostró para p53 en AU 9 casos, ki-67 en AS en 5 casos y en casos controles con 6 casos. (Grafico 3)
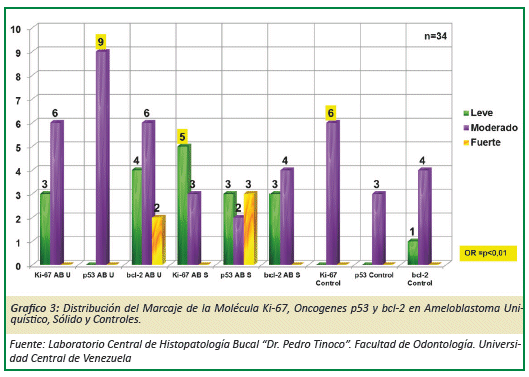
DISCUSIÓN
La distribución de los AB acorde al diagnóstico histopatológico se comenta en un estudio realizado en el Laboratorio de Patología Oral de la Universidad del Pacífico, en San Francisco, donde se estudiaron 1 088 tumores odontogénicos reportó una prevalencia del 54% de AS y un 46% en AU5 resultados que contrastan con los encontrados en el estudio donde el AU representa el mayor porcentaje con un 64%.
La distribución de los AB de acuerdo al género, en el Hospital Universitario Docente de la Universidad de Lagos, Nigeria6 se evidenció mayor prevalencia en el género masculino concordando con nuestros resultados.
La distribución de AS y AU por grupos de edad, en general la literatura reporta que la mayor incidencia ocurre en la cuarta década de la vida con un promedio de 33 años7. En un estudio realizado en el Departamento de Patología Oral de la Pontificia Universidad Católica de Minas Gerais, Brasil el rango de edad fue de 12 a 76 años, con un promedio de 36 años8 similar a lo reportado en la presente investigación.
La distribución de AS y AU de acuerdo a localización anatómica en el estudio de López Alvarenga y col.8 realizado en el Departamento de Patología Oral de la Pontificia Universidad Católica de Minas Gerais-Brasil, evidenció que en mandíbula el sitio de mayor predilección fue la región del cuerpo y ángulo (45,8%) seguida del ángulo y rama (37,5%) y en menor frecuencia la zona anterior (12,5%). En el estudio realizado en el Departamento de Cirugía Plástica y Reconstructiva de la Facultad de Medicina, de la Universidad Dokuz Eylul, Turquía9; refieren que en la localización mandibular se ven afectadas con mayor frecuencia la región premolar, molar y la rama ascendente de la mandíbula lo que coincide con los resultados obtenidos en la investigación.
Actualmente se considera que la transformación neoplásica es una acumulación de mutaciones en una gran región del genoma4. Entre los marcadores más destacados, asociados a actividad neoplásica, encontramos p53 y Ki-679. Por otro lado el oncogén p16 como factor de restricción en el punto de control G1/S y la proteína bcl-2 relacionada con la regulación de apoptosis siendo estos marcadores útiles para predecir el comportamiento de esta lesión, considerando que los tumores odontogénicos son neoplasias benignas pero infiltrantes9, cabe preguntarse si los mecanismos de crecimiento e infiltración son semejantes a los de neoplasias malignas.
Muchos estudios han utilizado el inmunomarcaje de p53 como marcador indirecto de mutación, sin embargo, no se ha demostrado una estricta relación entre la expresión inmuno-histoquímica y mutación del gen9. Por otra parte, la molécula de proliferación Ki-67 ha demostrado también ser un buen marcador para detectar la tasa de recidiva en lesiones tumorales10,11 se ha correlacionado con estadios TNM más avanzado y metástasis en cáncer12.
En la Facultad de Odontología de la Pontificia Universidad Javeriana se realizó un estudio comparativo en el cual se evaluó el índice de inmunoexpresión de Ki-67, mediante conteo celular en 10 casos de AU y en 10 casos de AS, obteniendo como resultado en los diez casos de AU negatividad para la inmunotinción con Ki-67, mientras que en los diez casos de AS se observó positividad en un promedio de 3,7%; ninguno se ubicó por encima del 10% de expresión13 contrario a los resultados obtenidos en esta investigación.
Por otra parte en cuanto al proto-oncogen bcl-2 se realizó un estudio en el Departamento de Patología Oral y Maxilofacial de las escuelas de Odontología de Isfahan y Yazd en Iran, donde examinaron la expresión de bcl-2 y Ki-67 entre AS y Tumor Odontogénico Adenomatoide (TOA) El índice de marcaje para ambos de acuerdo con la tinción celular fueron para Ki-67 en AS y Tumor Odontogénico Adenomatoide (TOA) eran 4% y 1% respectivamente, y de bcl-2 en AS y Tumor Odontogénico Adenomatoide (TOA) fueron 63% y 26% respectivamente, evidenciando que el mayor porcentaje de estos dos marcadores en AS en comparación con el Tumor Odontogénico Adenomatoide, confirma el comportamiento clínicamente agresivo del AS a diferencia del Tumor Odontogénico Adenomatoide14.
La oncoproteína p16 inhibe la transición de G1/S del ciclo celular y por tanto detiene la proliferación celular, en condiciones normales no regula el ciclo celular e inhibe la apoptosis. En el Centro de Investigación Multidisciplinario para Enfermedades Orales, en la Universidad de Donau-Austria, se realizó un estudio que reportó una relación estadísticamente significativa entre la expresión de p16 y la presencia de VPH en un grupo de carcinomas de cabeza y cuello15; de estos datos se podría especular que la expresión del p16, en especial para el TOQQ en este trabajo pudiese tener relación con una etiología de origen viral.
Se realizó un estudio en el Servicio de Cirugía Oral y Maxilofacial, del Hospital de Emergencia del Condado, en Craiova-Rumania para determinar la inmuno expresión de p16 y Ki67 en 19 AB16. La inmunorreacción del p16 estaba presente en el 90,9% de los casos contrario a lo reflejado en nuestro estudio. La inmunorreacción Ki-67 se envidenció en todos los casos16. La evaluación de marcadores como p16 y Ki67 pueden ser útiles para distinguir diferentes tipos de AB en términos de comportamiento clínico agresivo16,17.
Finalmente, y dado que estos marcadores han sido asociados con una función específica, posibles diferencias en su inmunodetección permitirían contribuir a establecer si el comportamiento clínico tanto del TOQQ como de Ameloblastoma Sólido y Uniquístico está mayormente determinado por la proliferación celular (Ki-67) (p16) o por la inhibición de la apoptosis (p53) (bcl-2), información que podría utilizarse para mejorar la comprensión de su comportamiento biológico18. Esto se puede traducir en el futuro en mejores y más específicos y efectivos tratamientos, lo cual impactaría positivamente en la calidad de vida de los sujetos que los presentan.
Como resultado de la presente investigación se sugiere que el AS debe ser tratado mediante resección quirúrgica con márgenes de seguridad, debido la evidencia de alta proliferación celular (Ki-67) e inhibición de la apoptosis (p53)(bcl-2), aunado a un bajo porcentaje de p16 responsable de detener la proliferación celular; lo que sugiere alto potencial de crecimiento.
En cuanto al AU los resultados obtenidos en este estudio reflejan expresión de marcaje medio para proliferación celular (Ki-67) e inhibición de la apoptosis (p53)(bcl-2); aunque los valores para p16 demuestran también una expresión de marcaje medio, lo que orienta que el procedimiento a seguir es el tratamiento conservador como enucleación y curetaje, sin embargo, en casos de AB donde la clínica muestre un curso más agresivo, o en el caso de AU intramurales deben ser considerados como AS requiriendo un tratamiento radical.
El tratamiento que deben recibir los AB a menudo es un tema de controversia entre los especialistas. Para tomar una decisión adecuada, debemos considerar los siguientes factores: tipo histológico, localización anatómica, proximidad a estructuras nobles, dimensiones del tumor, edad, condiciones físicas y expectativas del paciente.
AGRADECIMIENTOS: A la Sra. Adrianna Smitter. Histotecnólogo, por la preparación del material analizado.
REFERENCIAS
1. Barnes L, Eveson J, Reichart P, Sidranski D. World healt Organization Classification of Tumours Pathology & Genetics Head and Neck Tumors. IARC Press. Lyon 2005:284-308.
2. Sapp JP, Eversole LR, Wysocki GP. Patología Oral y Maxilofacial Contemporánea. 2nd Ed. Madrid, España:Elsevier; 2006:128-134 [ Links ]
3. Maturana A, Aitken J, Reyes M, Rojas-Alcayaga G. Expresión inmunohistoquímica de ki-67 y p53 en tumor odontogénico queratoquístico en comparación con ameloblastoma multiquístico. Rev. Clin. Periodoncia Implantol. Rehabil. Oral 2014; 7(1):12-16. [ Links ]
4. Florescu A, Simionescu C, Ciurea R, Pitru A. p53, bcl-2 and ki-67 immunoexpression in follicular solid ameloblastomas. Rom J Morphol Embryol 2012; 53(1):105-109 [ Links ]
5. Buchner A, Merrel PW, Carpenter WM. Relative frequency of central odontogenic tumors: a study of 1.088 cases from Northern California and comparision to studies from other parts of the world. J Oral Maxillofac Surg 2006; 64:1343-52 [ Links ]
6. Ladeinde A, Ajayo O, Ogunlewe M, Adeyemo W, Arotiba G, Bamgbose B, Akinwande J. Odontogenic tumors: A review of 319 cases in a Nigerian teaching hospital. OOOO 2005; 99:191-95 [ Links ]
7. Sapp JP, Eversole LR, Wysocki GP. Patología Oral y Maxilofacial Contemporánea. 2nd. Madrid, España:Elsevier; 2006:128-134 [ Links ]
8. López R, Jaeger F, Gomes JH, Leal RM. Ameloblastoma: un estudio retrospectivo de 48 casos. Rev Esp Cir Oral Maxilofac 2013; 148:11-16 [ Links ]
9. Vayvada H, Mola F, Menderes A, Yilmaz M. Surgical management of ameloblastoma in the mandible: Segmental mandibulectomy and immediate reconstruction with free fibula or deep circumflex iliac artery flap. J Oral Maxillofac Surg. 2006; 64:1532-9. [ Links ]
10. Migaldi M, Sartori G, Rossi G, Cittadini A, Sgambato A. Tumor cell proliferation and microsatellite alterations in human ameloblastoma. Oral Oncol 2008; 44(1):50-60 [ Links ]
11. Kuroyanagi N, Sakuma H, Miyabe S, Machida J, Kaetsu A, Yokoi M et al. Prognostic factors for keratocystic odontogenic tumor (Odontogenic keratocyst): Analysis of clinico-pathologic and immunohistochemical findings in cysts treated by enucleation. J Oral Pathol Med 2009; 38(4):386-392 [ Links ]
12. Lothaire P, de Azambuja E, Dequanter D, Lalami Y, Sotiriou C, Andry G, Castro G Jr, Awada A. Molecular markers of head and neck squamous cell carcinoma: Promising signs in need of prospective evaluation. Head Neck 2006; 28(3):256-269 [ Links ]
13. Ochoa LS, Martínez EM, Bustillo JA. Estudio comparativo de la expresión inmunohistoquímica del Ki-67 en los ameloblastomas uniquístico y sólido. Univ Odontol 2009; 28(61):67-73 [ Links ]
14. Sayed MR, Sayed HT, Ali TH, Ehsan TH, Arezu K. A comparative immunohistochemical study of Ki-67 and Bcl-2 expression in solid ameloblastoma and adenomatoid odontogenic tumor. Dent Res J 2012; 9(2):192–197
15. König F, Krekeler G, Hönig J, Cordon-Cardon C, Fischer G, et al. Relation between Human Papillomavirus positivity and p16 expression in head and neck Carcinomas. A tissue Microarray study. Anticancer Research 2007; 27:283-288. [ Links ]
16. Olimid DA, Florescu AM, Cernea D, Georgescu CC, Margaritescu C, Simionescu CE, Stepan AE. The evaluation of p16 and Ki67 immunoexpression in ameloblastomas. Rom J Morphol Embryol 2014; 55(2):363-7. [ Links ]
17. Gadbail A, Patil R, Chaudhary M. Co-expression of Ki-67 and p53 protein in ameloblastoma and keratocystic odontogenic tumor. Acta Odontológica Scandinavica 2012; 70(6):529-535 [ Links ]
18. Simon E, Merkx M, Vuhahula E, Ngassapa D, Stoelinga PJ. A 4 year prospective study on epidemiology and clinicopathological presentation of odontogenic tumors in Tanzania. OOOO 2005; 99:598-602 [ Links ]














