Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Científica Ciencia Médica
versión impresa ISSN 1817-7433versión On-line ISSN 2220-2234
Rev Cient Cienc Méd v.12 n.2 Cochabamba 2009
ENTREVISTA
ESTATINAS — UNA ENTREVISTA CON EL DR. ELVIN MOLLINEDO
Gustavo A. Baumann-Pinto
Dr. Luis Elvin Mollinedo Perez
Médico Cirujano, Universidad Mayor de San Andrés (UMSA). La Paz-Bolivia.
Especialidad: Infectología (Universidad de Chile).
Master en Ciencias Médicas con Mención en Microbiología (Universidad de Chile).
M.B.A. (Master Of Business Administration) Escuela Europea de Negocios, Titulación Europea.
Especialista en Medicina Tropical y del Viajero - Gorgas Course In Clinical Tropical Medicine.
Universidad de Alabama Birmigam. Instituto de Medicina Tropical Alexander Von Humbolt-U. Cayetano Heredia.
Especialista en Enfermedades Entéricas Cin Enfasis en Colera. Universidad Ver Sheva - Israel.
Docente Investigador, Jefe de Unidad de Genética Molecular y Microbiología. En el Instituto de Genética de la Facultad de Medicina - UMSA
Editor: Podría comenzar con una breve descripción sobre las dislipidemias y sus riesgos.
Dr. E. Mollinedo: Bajo el concepto de Dislipidemias se incluye a un grupo de patologías caracterizadas por alteraciones en la concentración de lípidos sanguíneos en niveles que involucran un riesgo para la salud: comprenden situaciones clínicas en las que existen concentraciones anormales de colesterol total (cT), colesterol de alta densidad (c-HDL), colesterol de baja densidad (c-LDL) y también de los triglicéridos (TG).
Hasta hace algunos años, se manejaba el concepto de Hiperlipidemias o Hiperlipemia, pero el mismo fue quedando en desuso, puesto que lo que verdaderamente ocurre es un incremento del cT, cLDL y los TG, con descenso del cHDL. De este modo un "Perfil Lipidíco" dislipidemico, se constituye en un factor de riesgo mayor y modificable de enfermedad cardiovascular, en especial coronaria.
Es bueno destacar que los niveles muy altos de TG se asocian también al desarrollo de pancreatitis aguda.
Los niveles de colesterol sanguíneo están determinados fundamentalmente por dos factores principales: las características genéticas del individuo (producción de colesterol endógeno), como por factores adquiridos (dieta, balance calórico, actividad física), es decir el aporte del llamado colesterol exógeno.
El colesterol que es transportado en el organismo en forma de lipoproteínas de baja densidad (c-LDL) está directamente correlacionado con el riesgo de enfermedad coronaria. El colesterol que forma parte de lipoproteínas de alta densidad (c-HDL) está inversamente correlacionado con el riesgo coronario.
En un examen de laboratorio de rutina de "Perfil Lipídico" también se determinan las lipoproteínas de muy baja densidad (VLDL), las mismas son las que contienen la mayoría de los TG del suero y algunas de sus formas son igualmente aterogénicas.
La dislipidemia comprendida de esta manera es la principal causa de aterosclerosis, en la actualidad se conoce muy precisamente el mecanismo de aterogénesis, estando constituido el mismo en términos generales por el atrapamiento de c-LDL oxidadas por parte de los macrófagos en la matriz subendotelial, iniciándose de este modo un proceso inflamatorio que involucra también a las células musculares lisas. El progreso de la placa aterosclerótica lleva a la oclusión del lumen arterial.
Innumerables estudios han demostrado contundentemente que con la reducción de los niveles de c-LDL se producen beneficios tanto en la morbilidad como en la mortalidad cardiovascular. Sobre dicha base el blanco fundamental del tratamiento es la reducción de esta partícula, y el grado de intensidad terapéutica será en función del riesgo global del sujeto. De esta forma la terapia hipolipemiante serán más agresivas en pacientes que ya han desarrollado enfermedad aterosclerótica (prevención secundaria) y menos agresivas en pacientes que aun no desarrollaron patología cardiovascular (prevención primaria).
Editor: ¿Cuáles son los objetivos actuales de la terapia hipolipemiante basándose en las guías internacionales vigentes?
Dr. E. Mollinedo: En el mundo entero los lineamentos que más se aceptan son los que elabora el Panel de Expertos en el Tratamiento de las Dislipidemias del Adulto (Adult Treatment Panel: ATP), del Programa Nacional Americano para Educación sobre el Colesterol (National Colesterol Education Program: NCEP), que desarrolló hasta el momento actual tres guías, denominadas ATP I, ATP II y ATP III.
Las Guías del ATP I (1988) enfatizaron el tratamiento exclusivamente en búsqueda de la reducción del c-LDL, lo que se lograba mediante resinas de intercambio y ácido nicotínico.
En las Guías ATP II (1993) el riesgo del paciente orienta la terapéutica; el objetivo del c-LDL para los pacientes coronarios se establece en <100 mg/dL y se incluye a las estatinas como "drogas mayores".
Las Guías ATP III (2001) establecen el nivel óptimo de c-LDL en < 100 mg/dL; el grupo de pacientes en alto riesgo, con objetivo primario de c-LDL < 100 mg/dL incluye a los pacientes con equivalentes coronarios, prestándose por otro lado mayor atención al c-HDL y los niveles del colesterol No-HDL que se establecen como un objetivo secundario de la terapéutica.
En ATP III (2001) las metas de c-LDL a lograr se establecen según el riesgo del paciente:

Editor: ¿Cuáles son los niveles "meta" de reducción de colesterol LDL, dentro de los actuales conceptos terapéuticos?
Dr. E. Mollinedo: En el año 2004 se realiza una actualización a la Guía ATP III, introduciéndose las siguientes recomendaciones: obtener un perfil lipoproteico en ayunas en todos los adultos de 20 años o mayores (repetir cada 5 años); establecer la presencia de coronariopatía, de equivalentes de riesgo coronario y de factores de riesgo para el desarrollo de coronariopatía; a pacientes con riesgo intermedio estimar el Riesgo Framingham; establecer la presencia de síndrome metabólico; considerar factores de riesgo emergentes, como la Proteína C Reactiva de Alta Sensibilidad o Ultrasensible (us-PCR).
Se clasifica al perfil lipoproteico como sigue:
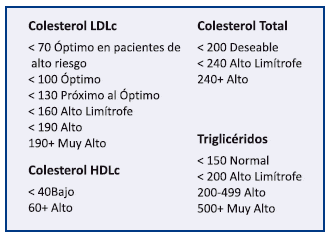
Indicaciones terapéuticas basadas en el LDLc y la estratificación del riesgo:

De esta manera, la actualización 2004 del ATP III 2001 incluyo las siguientes modificaciones:
1. LDLc óptimo en pacientes de riesgo muy alto < 70 mg/dL.
2. Se define riesgo muy alto a los pacientes coronarios con: múltiples factores de riesgo (diabetes); factores de riesgo mal controlados (tabaquismo); síndrome metabólico; síndrome coronario agudo.
3. Se definen los objetivos LDL estándar para el riesgo muy alto, a alto y moderadamente alto. Igualados o superados los mismos iniciar terapia farmacológica.
4. Se definen objetivos opcionales para el Riesgo Muy Alto y Moderadamente Alto.
Editor: A propósito de su comentario. ¿Qué es la proteína C reactiva ultrasensible? y ¿Qué relación guarda con el control, evaluación y correlación del riesgo cardiovascular y regresión de la placa ateromatosa?
Dr. E. Mollinedo: La proteína C reactiva (PCR) es una sustancia que se produce en el hígado y se secreta al torrente sanguíneo. Su concentración aumenta en presencia de inflamación. La determinación de PCR se ha usado durante muchos años como indicador de presencia de infección bacteriana o vírica así como para controlar los cambios en la inflamación asociados a muchas enfermedades inflamatorias y autoinmunes.
Hace algunos años, varios estudios revelaron que la PCR puede ser también un indicador de enfermedad cardiovascular en población aparentemente sana. Sin embargo, la concentración de PCR en sangre es normalmente tan baja que se requiere una técnica especialmente sensible para medirla. Esta prueba se llama PCR ultra sensible o PCR-us.
La historia de la relación entre enfermedad cardiovascular e inflamación tiene uno de sus comienzos en el análisis del Multiple Risk Factor Intervention Trial, en el que se encuentra una asociación de la proteína C reactiva (PCR) con el infarto de miocardio con un odds ratio (OR) de 4,3 que persistía a pesar del ajuste por tabaquismo y otros factores de riesgo clásicos (Am J Epidemiol 1996; 144: 537-547); así como también en el Cardiovascular Health Study and the Rural Health Promotion Project, en el que se sugería una asociación más estrecha de riesgo de infarto con la PCR para mujeres (OR: 4,50) que para los hombres (OR: 1,75) (VascBiol 1997; 17: 1121-1127). Poco después en un subanálisis del Physicians' Health Study se comprobó su papel predictor en la enfermedad cardiovascular (N Engl J Med 1997; 336: 973-979).
La determinación cuantificación en sangre de la Proteína C-Reactiva Ultrasensible (PCR-us), en ingles: High-Sensitivity C-Reactive Protein (hs-CRP) en la actualidad tiene un papel clave en la evaluación del riesgo vascular, en la práctica clínica, muchos médicos cuantifican ya de rutina la PCR-us, como un biomarcador inflamatorio asociado con un riesgo notablemente incrementado de infarto de miocardio, stroke, enfermedad arterial periférica, y muerte cardíaca súbita. Este marcador es considerado muy sensible, incluso en individuos al parecer sanos y con los niveles bajos de c-LDL.
Hasta ahora, más de una docena de estudios en gran escala han demostrado que incluir en los pacientes la cuantificación de PCR-us, constituye una excelente herramienta de predicción independiente de futuros eventos cardiovasculares, y que la evaluación de la PCR-us añade valiosa información pronóstica sobre el riesgo cardiovascular individual, sean cuales sean los niveles de c-LDL, destacándose que los criterios son aplicables a todos los grupos de riesgo establecidos en el Score de Framingham, por otro lado la PCR-us es un marcador útil en todos los estadios del Síndrome Metabólico. Por estudios previos se conoce que la PCR-us predice también el riesgo de eventos coronarios recurrentes y tiene un alto valor pronóstico en isquemia coronaria aguda así como en el seguimiento posterior a las intervenciones quirúrgicas sobre las coronarias.
En el Estudio de Salud de la Mujer en EEUU (Women's Health Study), en la cual se incorporaron mujeres aparentemente sanas, con niveles bajos de c-LDL, pero con niveles altos de PCR-us, se evidenció que estas pacientes tienen un riesgo absoluto más alto de desarrollar futuros eventos vasculares que aquellas pacientes con altos niveles de c-LDL, pero que tienen niveles bajos de PCR-us. Sin embargo en las actuales guías, los pacientes con c-LDL < 130 mg/dL no son considerados candidatos para la terapia con estatinas, en el marco de los criterios corriente en prevención primaria.
Por otro lado, tanto estudios experimentales como clínicos han demostrado que las estatinas tienen evidentes efectos antiinflamatorios directos, y ahora esta claramente establecido que el tratamiento con estatinas disminuyen los niveles de PCR-us.
Es por todo esto que, actualmente se considera que la pesquisa de PCR-us debería ser incorporada como un método que permita mejorar la decisión de optar por una terapia con estatinas, particularmente en aquellos pacientes con niveles normales o bajos de c-LDL, pero con niveles altos de PCR-us.
En noviembre de 2008 Ridker P, Danielson E y un grupo de investigadores de varios países, publicaron en el New England Journal of Medicine (N Engl J Med 2008;359:2195-2207) las conclusiones del ensayo JÚPITER (Justification for the Use of Statins in Prevention: an Intervention Trial Evaluating Rosuvastatin) cuya hipótesis es de que pacientes con niveles relativamente altos de PCR ultrasensibles pero sin hiperlipemia podrían beneficiarse con el tratamiento con estatinas.
Este estudio randomizado, controlado con placebo y doble ciego, incluyó a 17 802 pacientes aparentemente sanos con PCR > 2 mg/L y LDL-colesterol < 130 mg/dl, sin otras enfermedades o factores de riesgo graves. Se les administró 20 mg de Rosuvastatina diarios, realizándose visitas de seguimiento periódicas y se midió como desenlace principal el desarrollo de un evento cardiovascular mayor (IAM no fatal, stroke no fatal, angina inestable con requerimiento de internación, revascularización arterial o muerte confirmada de causas cardiovasculares). El tiempo de seguimiento estipulado era de 5 años pero se vio interrumpido a los 1.9 años por el comité evaluador independiente debido a una reducción significativa de los eventos primarios en el grupo tratado con la droga.
Como resultado de este ensayo clínico, los autores observaron en el grupo tratado con Rosuvas-tatina una reducción del LDL-colesterol del 50% y de PCR ultrasensible del 37 % a los 12 meses respecto al grupo placebo.
En cuanto a los desenlaces, el número de eventos cardiovasculares en el grupo tratado fue significativamente menor que en el grupo placebo (Riesgo Relativo: 0.56), tanto analizándolos en conjunto como individualmente. Según las estimaciones obtenidas el número de pacientes que deberían ser tratados con Rosuvastatina por 2 años para prevenir un desenlace primario es 95 y por 4 años es 31.
Los efectos adversos registrados mostraron, en su mayoría, igual frecuencia en ambos grupos. En base a estos contundentes hallazgos, actualmente se plantea la terapia con Rosuvastatina como una nueva herramienta preventiva en pacientes con PCR-us ligeramente elevada como único marcador de riesgo, vale decir uso de estatinas incluso en pacientes con c-LDL normal y sin otros factores de riesgo cardiovascular.
Editor: ¿Cómo sido la evolución de las es-tatinas desde sus comienzos de los años 80'?
Dr. E. Mollinedo: El desarrollo de las estatinas es una de las manifestaciones que mejor define la moderna farmacología. De partida se definió exactamente la diana terapéutica donde se deseaba actuar para bloquear la síntesis de colesterol en el hígado: la HMG-CoA reductasa, enzima involucrada en la síntesis del colesterol. Conocida la misma se inició la búsqueda de sustancias que cumplieran los requisitos exigidos para el bloqueo del receptor hasta que se lograron encontrar las primeras moléculas que se fueron perfeccionando hasta conseguir las actuales estatinas.
Históricamente, mevastatina fue la primera estatina aislada a partir de hongos, pero su eficacia para inhibir la HMG-CoA reductasa estaba limitada por su toxicidad y fue pronto retirada del mercado. Posteriormente, en 1979, Hoffman y col. aislaron la lovastatina. Se obtuvieron de los hongos Penicillium citrinum y Aspergillus terreus respectivamente. La pravastatina es un metabolito fúngico, aislado de cultivos de Nocardia autotrophica, mientras que la fluvastatina fue la primera estatina totalmente sintética. A partir de este momento se sintetizaron la simvastatina, a partir de un producto de la fermentación del Aspergillus terreus y todas las demás, manteniéndose la investigación en esta línea en el momento actual.
Hasta el 2008, las estatinas reconocidas por la FDAyla EUDRA son: Atorvastatina; Cerivastatina, retirada del mercado en el 2001 por el laboratorio fabricante (Bayer) debido a su asociación con mayor frecuencia de graves efectos adversos; Fluvastatina; Lovastatina; Pitavastatina; Pravastatina; Simvastatina; Rosuvastatina.
La mejoría de las propiedades farmacológicas de las estatinas podría lograrse con la creación de productos con mayor efecto sobre las lipo-proteínas aterogénicas sin que se comprometa el perfil de seguridad asociado con esta clase de fármacos. Desde el punto de vista farmacológico, una estatina "óptima" debería tener una inhibición enzimática máxima; debería poseer una distribución preferencial en el hígado y actuar en ese nivel más que en la periferia y debería tener características farmacocinéticas óptimas, incluso duración de acción y máxima regulación sobre los receptores hepáticos de LDL. Por otra parte, la posibilidad de inducir interacciones farmacológicas debería ser mínima.
La rosuvastatina es una nueva estatina que se produce desde 1998. Los datos farmacológicos sugieren que el fármaco reúne casi todos (si no todos) los requisitos comentados con anterioridad.
Editor: Pero, ¿en qué grado responden los niveles de HDL a estas estatinas?
Dr. E. Mollinedo: Para mejorar el riesgo CV en pacientes con bajos niveles de HDL-c existen varias opciones terapéuticas, que incluyen modificaciones del estilo de vida y agentes con acción sobre los lípidos. No obstante, como fuera demostrado para la terapia de reemplazo hormonal, no todas las drogas que elevan el c-HDL pueden reducir el riesgo de ECV. Los fibratos y el ácido nicotínico son efectivos para elevar el c-HDL pero sólo tienen efectos modestos sobre los niveles de c-LDL. Las estatinas son consideradas la terapia de primera línea para el tratamiento de la dislipidemia por su eficacia para reducir el LDL-c. Además, pueden aumentar el c-HDL, pero este efecto depende de la dosis y podría estar relacionado con el aumento de producción de apo AI. En general, las estatinas con mayor eficacia para reducir el c-LDL y los niveles de partículas de LDL parecen ser las más efectivas para modificar el perfil de c-HDL. Sin embargo, las dosis elevadas de atorvastatina suelen ser menos efectivas que las dosis bajas para aumentar los niveles de c-HDL, posiblemente por incremento del catabolismo de apo AI.
El estudio STELLAR -que comparó rosuvastatina, atorvastatina, simvastatina y pravastatina-demostró categóricamente que la mayor eficacia para reducir el LDL-c y aumentar el HDL-c se da con rosuvastatina, en comparación con las otras estatinas.
Editor: ¿Cuál es el potencial de las estatinas para reducir del volumen de la placa de ateroma ya establecida?
Dr. E. Mollinedo: Cuando se piensa en regresión debe tenerse en cuenta que hay muchos factores que son vitales para la modificación de la lesión. No se trata solamente de un acumulo de lípidos. La placa madura, cubierta por la delgada cápsula fibrosa que previene la trombosis, puede llegar a producir una obstrucción por la actividad inflamatoria intensa que está ocurriendo en su interior.
De manera que los lípidos y la inflamación, la placa, la madurez de la lesión, el grosor de la cápsula, la actividad inflamatoria que ocurra en la lesión, las células y componentes humorales allí presentes, todos tienen su importante papel en la erosión, ruptura, estabilización o regresión de la placa.
Un objetivo largamente buscado y que ha sido difícil demostrar reducción en la placa, principalmente porque la metodología de evaluación que se utilizaba descansaba en la angiografía coronaria, con las limitaciones ya conocidas y resultantes del fenómeno de Glagov, que hace a la "luminografía" (la explicación de lo que hace la angiografía) un método insuficiente e incompleto.
Dados los antecedentes del estudio REVERSAL, en el que la máxima dosis de la más efectiva estatina hasta el momento, la atorvastatina, había podido detener la progresión de la lesión aunque no demostró regresión, cabía preguntarse si la más reciente estatina, rosuvastatina, con su mayor efectividad para la reducción de c-LDL y para la modificación de c-HDL, podría mostrar reducción. Nissen, el mismo autor de los estudios CAMELOT y REVERSAL, llevó a cabo el estudio ASTEROID (JAMA 2006; 295:1556-1565.) en el que se evaluó con la misma metodología estandarizada (IVUS = IntraVascular UltraSound) de REVERSAL, los cambios ocurridos en la placa en pacientes con enfermedad coronaria que recibían la máxima dosis de rosuvastatina.
Los Resultados en desenlaces primarios, en el cambio percentual en el volumen de ateroma, la reducción promedio fue -0.98% (3.15%) y la mediana -0.79% (intervalos de confianza de 97.5% - 1.21 a - 0.53), con valor de p < 0.001 en relación con la línea basal. Para el segundo parámetro de eficacia primaria, cambio en el volumen de ateroma en el subsegmentos de 10mm con mayor enfermedad, el cambio promedio fue -6.1 (10.1) mm3 y el cambio mediano-5.6 mm3 (IC 97.5% - 6.8 a - 4.0 mm3), para una reducción mediana de 9.1%.
En el Estudio METEOR, en el que se evalúo la detención de la progresión de lesiones en pacientes con enfermedad clínicamente aparente, así como la regresión de la placa son claramente factibles, tal como se demostró en estudios anteriores, en particular el estudio ASTEROID y metanálisis previos, que han mostrado que se pueden lograr regresión. Sin embargo, la medicina debe tener metas más ambiciosas que hacer corrección de la enfermedad clínicamente aparente. Debe buscarse la prevención primordial y cuando esta falla, la detección temprana y la intervención efectiva en las etapas iniciales se convierten en la primera prioridad.
La intervención con estatinas ha demostrado claramente tener impacto en lípidos y en desenlaces. Aunque hay niveles variables de costo-efectividad, es claramente superior cuando se las utiliza en poblaciones de riesgo intermedio o alto.
Para evaluar la utilidad de una intervención en una población de aparente bajo riesgo pero con lesiones incipientes, medidas por un aumento del espesor de la íntima media (IMT) de la arteria carótida, se planeó el estudio METEOR. Una justificación para esta intervención está en el hecho de que entre 10% y 15% de los pacientes que se admiten con infartos agudos (Khot) están libres de factores de riesgo tradicionales y han sido clasificados como de riesgo bajo. El IMT ha demostrado serpredictor de enfermedad cardiovascular, y tener buena correlación con otras mediciones, así como tener buena relación con la incidencia de eventos futuros.
En los resultados en (IMT), la terapia con rosuvastatina logró detener la progresión de la aterosclerosis, medida por IMT, en el período de dos años. En tanto que con placebo hubo un aumento de 0.0131 mm/año (IC95% 0.0087 a 0.0174), en el grupo de rosuvastatina hubo un cambio de -0.0014 (reducción) (IC95% -0.0041 a 0.0014). El resultado muestra clara diferencia estadísticamente significativa entre los dos grupos (p < 0.001). Como conclusión del estudio, se logra detener la progresión de las lesiones carotídeas, determinadas por IMT, en pacientes de bajo riesgo con lesiones incipientes.
Editor: ¿Cuál es el perfil de seguridad?
Dr. E. Mollinedo: En los miles de pacientes incorporados a los mega-ensayos clínicos que evaluaron la eficacia y seguridad de las estatinas, el porcentaje de pacientes que suspendieron el tratamiento por efectos adversos fue similar entre los tratados con estatinas o placebo. La rabdomiólisis, el efecto adverso de mayor gravedad por su potencial letalidad, se describió en sólo un paciente tratado con simvastatina en el estudio 4S.
El sistema de la citocromo P450 (CYP) es el principal responsable del metabolismo hepático de las estatinas. Lovastatina, atorvastatina y cerivastatina son metabolizadas de preferencia por la isoenzima CYP3A4. En el metabolismo de la cerivastatina está involucrado además CYP2C8. Simvastatina es metabolizada tanto por CYP3A4 como CYP3A5. Fluvastatina tiene mayor afinidad por el CYP2C9, mientras que la pravastatina es metabolizada por diferentes enzimas, atribuyéndose un papel secundario a CYP3A4.
El efecto tóxico muscular de las estatinas es dosis/concentración plasmática dependiente, como se demuestra cuando aumenta la incidencia de este efecto adverso al asociar estatinas con inhibidores del sistema microsomal hepático citocromo P450. Entre los fármacos que inhiben la isoenzima CYP3A4 se encuentran ketoconazol, itraconazol, ciclosporina, eritromicina, claritromicina, verapamil y diltiazem.
Las estatinas hidrofóbicas (lovastatina, simvastatina) tendrían mayor facilidad para atravesar membranas biológicas que las estatinas hidrofílicas (pravastatina, fluvastatina). Esta propiedad podría significar diferencias en la capacidad para producir miotoxicidad; sin embargo, no existen estudios concluyentes que muestren diferencias significativas en la incidencia de esta reacción adversa entre estos 4 medicamentos.
El mecanismo fisiopatológico del daño muscular es desconocido. Se postula que la reducción del colesterol intracelular resulta en una menor concentración de colesterol en la membrana, que puede llevar a una disminución de la fluidez de ésta. Otros plantean que la miotoxicidad por estatinas estaría relacionada con la elevación del calcio intracelular inducida por estos fármacos.
Los derivados del ácido fíbrico (gemfibrozilo, clofibrato) -fármacos eficaces en las dislipidemias que cursan con hipertrigliceridemia-pueden desarrollar miotoxicidad como efecto adverso, riesgo que se potencia al asociarlo con estatinas. Entre las advertencias para la prescripción de estatinas se describe esta interacción, pero la asociación de ambos tipos de fármacos no se ha considerado una contraindicación absoluta, dado que excepcionalmente se emplean en dislipidemias mixtas severas.
Casos de rabdomiólisis con insuficiencia renal secundaria y en algunos pocos casos fatales, se han asociado con mayor frecuencia al uso de cerivastatina que a otras estatinas. En la mayoría de los casos la cerivastatina se utilizó simultáneamente con gemfibrozilo; sin embargo, una proporción de pacientes no recibían este fibrato. En mayo de 2001, el Sistema Español de Farmacovigilancia comunicó 34 casos de rabdomiólisis asociados a cerivastatina, cifra claramente superior a la registrada con otras estatinas. El 65% de los pacientes estaban en tratamiento concomitante con gemfibrozilo. En Estados Unidos, la FDA recibió información de 31 muertes debidas a rabdomiolisis severa asociada al uso de cerivastatina, 12 de los cuales recibían gemfibrozilo simultáneamente. Hasta enero de 2001, el Sistema Australiano de Farmacovigilancia había recibido 95 comunicaciones de efectos adversos por cerivastatina, de las cuales 17 (18%) correspondían a rabdomiólisis. Este porcentaje era notoriamente superior al comunicado con otras estatinas (0,3%-1,2%). La aparición de este daño muscular iba más allá de la asociación a gemfibrozilo, lo que se habría solucionado al poner énfasis en la contraindicación formal de la asociación de ambos hipolipemian-tes. Laboratorios Bayer debe haber considerado todos estos antecedentes para tomar la decisión de suspender la comercialización del medicamento cerivastatina a nivel mundial.
En resumen, la rabdomiólisis es un efecto de clase de estos medicamentos, tiene una baja incidencia, pero es el efecto adverso más grave descrito para las estatinas. Es dosis-dependiente, favorecido por interacciones con fármacos que inhiben su metabolismo o comparten la miotoxicidad.
Las estatinas son el pilar del tratamiento de las dislipidemias y mejoran el pronóstico de la enfermedad vascular ateroesclerótica. El balance riesgo-beneficio favorece ampliamente a estos medicamentos, pero debemos estar atentos cuando el paciente nos comunique debilidad muscular o mialgias, que pueden ser la manifestación inicial de la miotoxicidad.
Editor: ¿Cómo evaluaría el apego a estos regímenes terapéuticos y su aplicación en nuestro medio?
Dr. E. Mollinedo: Sabemos que terapias efectivas para enfermedades crónicas requieren una adherencia diaria a la medicación durante prolongados períodos de tiempo. Los tratamientos complejos en base a múltiples fármacos pueden representar una barrera para tal apego.
El envejecimiento de la población y el predominio de enfermedades crónicas tales como dislipidemia, hipertensión, diabetes e insuficiencia cardíaca, ha originado que muchos pacientes estarán bajo múltiples regímenes de medicamento. Por ejemplo, los pacientes con diabetes requieren agentes hipoglicemiantes, antihipertensivos, hipercolesterolémicos, y terapia antitrombótica diarias, que hoy conocemos como "polifarmacia".
Las estatinas administradas una vez al día permite a los pacientes continuar la terapia indefinidamente, sin embargo, varias fuentes de información han demostrado que muchos pacientes tienen una adherencia diaria sub-óptima e índices bajos de persistencia a largo plazo. La carga de medicación con otras medicinas concurrentemente prescritas es el catalizador de la falta de adherencia y persistencia al uso de estatinas. Diversos estudios han demostrado que para una persona, la adherencia y persistencia en el tiempo declinan con el aumento de las dosis diarias prescritas y por la aparición de efectos adversos.
Los médicos por ningún motivo deberían disuadirse a iniciar una terapia con estatinas por temor a incrementar la complejidad médica del régimen, sino por el contrario deberían estar atentos a la falta de persistencia de la terapia, particularmente en pacientes jóvenes y sanos, ya que el tratamiento con estatinas no condonara un "sentirse mejor" en los pacientes, que es habitualmente lo que buscan los mismos.
En la actualidad, a la luz de los múltiples estudios realizados, sabemos que las estatinas son fármacos muy seguros y eficaces para el logro de objetivos médicos, por lo cual la mayor responsabilidad en la persistencia en los tratamientos a las estatinas el día de hoy recae en la responsabilidad del médico para explicar y sensibilizar a su paciente de los beneficios que obtendrá con el tratamiento y también de los riesgos que implicaran para la salud del paciente el no tomar las estatinas o el suspenderlas inconsultamente.














