Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz vol.26 no.1 La Paz 2020
ACTUALIZACIÓN
LEISHMANIASIS EN BOLIVIA
LEISHMANIASIS IN BOLIVIA
Zoraida Mollinedo1 & Sergio Mollinedo2
1. Docente Universidad Autónoma del Beni. Guayaramerin-Beni, Bolivia
2. Ex Jefe del Laboratorio Nacional de Parasitología, Entomología y Medicina Tropical, INLASA.
Correspondencia: Juan Sergio Mollinedo Pérez
Email: jsergiomollinedo@gmail.com
Teléfono celular: X-591-71537553
RESUMEN
Se presenta una revisión de las tres últimas décadas sobre la leishmaniasis en Bolivia; entre 1983 a 2015 se registraron 54540 casos de Leishmaniasis Cutánea Americana (LCA): Leishmaniasis Cutánea (LC): 46406; Leishmaniasis Mucocutánea (LMC): 8100; Leishmaniasis Cutáneo Difusa (LCD): 5; y Leishmaniasis Visceral (LV): 56. La mayoría de los enfermos provenían de la cuenca del río Amazonas (97.9%) y los restantes de la cuenca del Río de la Plata. La cantidad de casos nativos y el número de municipios con focos naturales de transmisión aumentaron de 80 municipios el año 2000, 91 el 2007 a 95 el 2014; incrementando de cinco a siete los departamentos endémicos. Las características clínico epidemiológicas son similares con Argentina, Perú y Brasil en las zonas de frontera; los municipios bolivianos con Perú y Brasil tienen mayores prevalencias. De las 121 especies de Phlebotominae registradas, siete especies están incriminadas en la transmisión de seis especies de Leishmania que circulan en el país en un nuevo escenario con casos autóctonos más dispersos en tiempo y espacio, con múltiples patrones culturales en por lo menos 15 eco-regiones entre 170 a 2700 m. La sub notificación de casos y la falta de medicamentos se ha profundizado en la última década y el diagnóstico es básico en una precaria red de laboratorios que no ha implementado aun el diagnóstico de LV por pruebas rápidas.
Palabras clave: Leishmaniasis, Enfermedades desatendidas, Enfermedades emergentes, Bolivia.
ABSTRACT
A review of last three decades on leishmaniasis in Bolivia is presented. Between 1983 and 2015, it has been reported 54540 cases of American Cutaneous Leishmaniasis (ACL), 46406 cases of Cutaneous Leishmaniasis (CL), 8100 Mucocutaneous Leishmaniasis (MCL), 5 Diffuse Cutaneous Leishmaniasis (DCL), and 56 Visceral Leishmaniasis (VL). Most of the patients came from the Amazon river basin (97.9%) while the rest from Rio de la Plata's basin. Native cases and municipalities with natural transmission sources have increased from 80 municipalities in 2000 to 91 on 2007 and 95 on 2014; increasing from five to seven endemic states. Clinical epidemiological characteristics are similar in Argentina, Perú and Brasil in the border areas; and Bolivian municipalities with Perú and Brasil have higher prevalence. Seven of 121 registered Phlebotominae species are incriminated in the transmission of six Leishmania types circulating the country in a new scenario with autochthonous cases more dispersed in time and space, with multiple cultural patterns in at least 15 eco-regions that varyfrom 170 to 2700 meters. The under-reporting of cases and the lack of medication has deepened over this last decade; diagnosis is rudimentary in a precarious network of laboratories that has not implemented diagnosis of LV by rapid tests yet.
Key words: Leishmaniasis, Neglected diseases, Emergent diseases, Bolivia.
INTRODUCCIÓN
Bolivia, tiene una población de 10027274 habitantes,1 distribuidos en 9 departamentos (primer nivel sub nacional); es conocido como "País del Altiplano", sin embargo más del 60% de su territorio son zonas tropicales o sub tropicales.
Las tendencias económicas en Bolivia han cambiado a lo largo del tiempo provocando flujos migratorios interregionales de personas susceptibles y socialmente vulnerables a zonas geográficas donde existe el riesgo de transmisión de la leishmaniasis. De actividades mineras extractivas en la zona andina (hasta década del 1980), se ha cambiado a la agroindustria en los valles y Amazonía (década del 1990 adelante), y la explotación de hidrocarburos (a partir del año 2000), los migrantes se han visto obligados a trasladar su cultura a paisajes completamente nuevos y reestructurar sus hábitos de trabajo, su concepción de la familia, comunidad y país. Las estrategias de adaptación conllevan altos costos emocionales y cognitivos, que podrían interrumpir la red de contención social, además de la falta de inmunidad y el estado nutricional deficiente e inadecuado, lo que aumenta la susceptibilidad a las enfermedades.2
MATERIAL Y MÉTODOS
La fuente para este artículo se sustenta en la revisión de los expedientes clínicos de los casos y la información obtenida por los autores durante más de tres décadas en diferentes instituciones relacionadas con los procesos de investigación sobre la leishmaniasis en Bolivia.
a) En 1982, se creó la Unidad de Parasitología y Medicina Tropical (UPAMET) en el Instituto Boliviano de Biología de Altura de Bolivia (IBBA) con la participación del Ministerio de Salud, Universidad mayor de San Andrés y la Cooperación Francesa (Instituto Pasteur, ORSTOM); los casos de sospecha de leishmaniasis del Hospital General (Dermatología) y servicios de salud provinciales comenzaron a estudiarse, mientras se realizaban investigaciones activas en áreas de colonización de los departamentos de La Paz (Yungas y Alto Beni) y Beni, y misiones especiales a los departamentos de Cochabamba (Chapare) y Pando (ríos Orthon y Madre de Dios). Cada paciente tenía un archivo clínico ad hoc de leishmaniasis, frotis, cultivos de parásitos, serología y resultados de diagnósticos IDR. Algunos casos especiales requirieron procedimientos adicionales como la inoculación en hámster, el aislamiento de cultivos y la caracterización por electroforesis de isoenzimas y anticuerpos monoclonales.3-4
b) En el Laboratorio Nacional de Parasitología y Entomología (LNPE) del Instituto Nacional de Laboratorios de Salud (INLASA), realizando una investigación activa y pasiva en los departamentos de La Paz, Tarija, Beni, Pando, Chuquisaca (SM. datos no publicados). Los protocolos desarrollados en el UPAMET se implementaron solo en parte debido a la falta de infraestructura, reactivos y recursos humanos capacitados.
c) En 2006, como responsable (SM) del Programa Nacional para el Control de la Leishmaniasis (PNCL); estandarizó, sistematizo y socializo la información; los informes de IBBA desde 1982 se tomaron como informes oficiales de prevalencia, aunque el sistema era consciente de que la información no tenía en cuenta los informes de otras instituciones, como CENETROP.5-10 Investigaciones y documentos no publicados que hasta la actualidad son emitidos (Reuniones nacionales del PNCL; informes de SEDES, Epidemiología, Ministerio de Salud, tesis universitarias, documentos presentados a reuniones, congresos, etc.). A partir del 2006, el informe de leishmaniasis se convirtió en obligatorio en cada jurisdicción para los Servicios Departamentales de Salud (SEDES), con el fin de superar el sub registro que aún es una importante preocupación; se editó una Guía Operativa,11 y se desarrolló y comenzó a implementar un Control de Plan de Cinco Años.12
d) De 1982 al 2005, un equipo boliviano-francés (IBBA e INLASA), e investigadores del Institut de Recherche pour de Developpement (IRD), llevó a cabo investigaciones entomológicas en la zona tropical de los departamentos de La Paz (Yungas, Alto Beni), Beni, Cochabamba, Pando y Tarija, en estaciones de captura de bosques a 2000 m, 1400 m, 900 my 250 msnm).2-3-4-13
e) Del 2011 al 2019, ZM realizó actividades de promoción y prevención de enfermedades desatendidas, incluida la leishmaniasis, implementando investigaciones operativas en los departamentos de Pando y Beni.
RESULTADOS
Leishmaniasis Visceral (LV):
Migone,14 reporto el primer caso conocido de Leishmaniasis Visceral (LV) en América en 1913, posteriormente comenzaron a reportarse casos de la enfermedad principalmente en Brasil y ocasionales en otros países; en Bolivia hasta antes de 1950, se tiene referencia confusa de casos ocurridos en la frontera con Brasil y Paraguay.15-16
En el año 1982, Leishmania infantum fue identificada en un perro de 'Yungas', departamento La Paz, (900 a 1650 msnm).17 El mismo año describimos en el 'Hospital del niño', lo que conocemos como el "primer caso autóctono de leishmaniasis visceral en Bolivia", varón de dos años, con sintomatología típica, del cual aislamos y tipificamos el parásito.18 Otras investigaciones en el área encontraron el vector Lutzomyia longipalpis;19 simultáneamente también se registraron perros, que fueron incriminados como reservorios domésticos de L. infantum por serología, autopsias y cultivos de órganos en el hígado. bazo y médula ósea).20
De 1939 al 2018, se reportaron 56 casos de VL en Bolivia,21-22 generalmente en niños.23-24-25 Los pocos casos reportados son inconsistentes con las investigaciones que muestran una gran exposición en el ambiente peri domestico a densidades altas de Lutzomyia longipalpis;13-19-26 presencia habitual de perros infectados20 y la detección de infecciones sub clínicas con pruebas serológicas (ELISA-rK39); en 15 de 123 niños (14.4%) en la provincia Caranavi, departamento de La Paz27 y cinco (0,7%), provincia A. Arce, departamento de Tarija.21-28-29 Solo se detectan los casos típicos sintomáticos, mientras que las poblaciones dispersas lejos de las ciudades no son tan visibles en el sistema de vigilancia de la salud boliviana, por lo que es imposible estimar su verdadera prevalencia.
Leishmaniasis Cutánea Americana (LCA)
Son las formas clínicas predominantes con diversas expresiones clínicas, que van desde tipos leves de leishmaniasis cutánea (LC) hasta leishmaniasis mucocutánea (LMC), con una tasa de 85/15. La primera evidencia de la LCA en el territorio que ahora se denomina Bolivia, fue hecha por Fray Rodrigo Loayza (1586), quien describe una "enfermedad que se come las narices de los indios en los Yungas";30 más tarde, M. Antonio Vaca Diez en 1876,31 relata un viaje que describe la epidemiología, características clínicas, tratamientos y evolución de la enfermedad. Sagarnaga,32 en 1903, describió varios casos durante la Guerra de Acre; mientras que Nazario Pardo Valle (1906),33 circunscribió LC a los márgenes habitados de los ríos de cinco departamentos (La Paz, Beni, Pando, Santa Cruz y Cochabamba). Posteriormente los informes fueron presentados esporádicamente: Veintemillas (1928);34 Desjeux (1974);35 Desjeux et al (1974);36 Walton y Chinel (1979).37-38
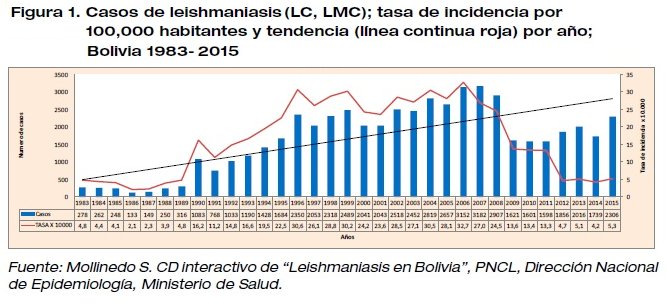
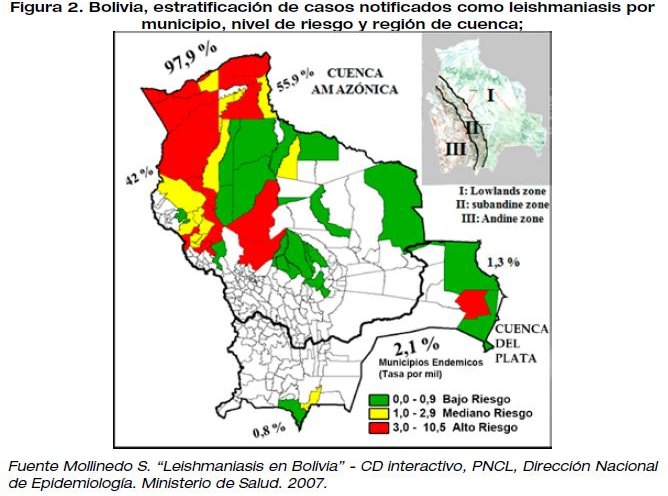
De 1982 a 1993, participamos en el diagnóstico con algún tipo de leishmaniasis de 2076 pacientes en el UPAMET; 1922 pacientes fueron diagnosticados en el LNPE entre 1998 al 2006; en conjunto con el SEDES Tarija registramos 1250 pacientes entre 1997 a 2018,28 y en conjunto con SEDES Pando registramos 6.614 casos de LCA de 1996 al 2018.39 Para el 2016 se comenzó a socializar los gráficos de la Tendencia secular de casos de Leishmaniasis en todas sus formas, por año y tasa de incidencia por 100.000 habitantes, (FIGURA 1) y el mapa de Bolivia estratificado de casos notificados como leishmaniasis por municipio, nivel de riesgo y cuencas hidrográficas. (FIGURA 2).
Leishmaniasis Cutáneo Difusa (LCD)
Denominada también Leishmaniasis cutáneo anérgica; Convit y Lapenta describieron en Venezuela el primer caso en América (1945), los enfermos tenían presencia de lesiones nodulares diseminadas, sin ulceración, ricas en formas amastigotas y la intradermorreacción de Montenegro era negativa.
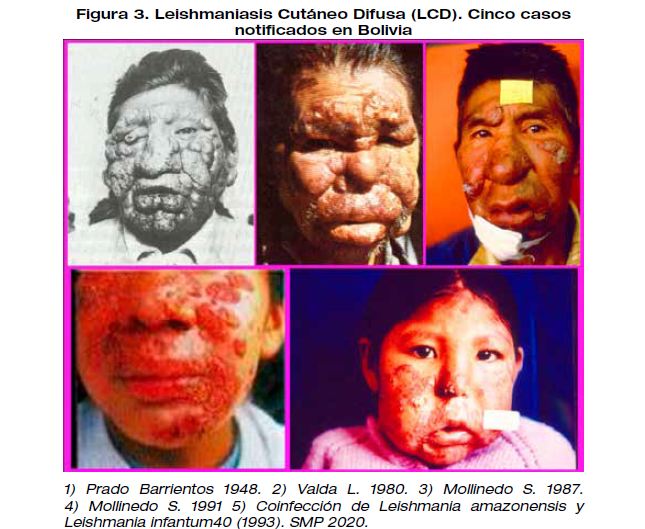
En Bolivia se han registrado cinco casos: 1) 1) varón, 42 años, procedencia Irupana (Provincia Sur Yungas), comerciante, con seis años de evolución, reportado por Prado Barrientos en 1948. 2) Varón, 68 años, procedencia Coroico (Provincia Nor Yungas), labrador, con cinco años de evolución, reportado por Valda L. en 1980. 3) Varón, 45 años, procedencia Coroico (Provincia Nor Yungas), lavandero, con 33 años de evolución, estudiado por Mollinedo S. en 1987. 4) Mujer, de 28 años, procedencia Chulumani (Provincia Sur Yungas), agricultora, con cuatro años de evolución, estudiada por Mollinedo S. en 1991 5) Mujer, de 5 años, procedencia Carrasco (Provincia Caranavi), evolución de dos años, los estudios concluyeron que se trataba de una Coinfección de Leishmania amazonensis y Leishmania infantum (1993).40
F. Prado-Barrientos el año 1948;; Un segundo caso fue descrito por Valda L. (1980); dos otros fueron estudiadas por el autor 1987,1991 (datos no publicados) y en 1993 se encontró un caso de co-infección.40 (FIGURA 3).
Datos de vigilancia
Los informes de casos en los departamentos endémicos no tenían un registro nacional hasta el año 1982. Tarija, el sexto departamento endemo epidémico, notificó 1250 casos (1987-2018), el brote inicial en Bermejo que se está extendiendo en dirección noreste abarcando otros cuatro municipios (Padcaya, Carapari, Entre Ríos y Yacuiba).28 El PNCL añadió a Chuquisaca como el séptimo departamento endémico en base al reporte de casos humanos, aunque los estudios de sustento científico aun están en curso. El diagnóstico en la mayoría de los casos se realiza mediante detección pasiva, por lo que el sesgo de información es inevitable debido a poblaciones muy dispersas en algunas áreas inaccesibles y agentes insuficientemente capacitados.
Una compañía de exploración petrolera con actividad intensiva en el bosque primario amazónico (departamentos de La Paz y Beni, (1983-1984) reporto 185 casos de LCA en un año, 52.8% de la fuerza laboral.41-42 Un otro proyecto de colonización (Proyecto Río Colorado, Departamento de Beni, UMSA) informó el 50% de la incidencia de LC en 38 colonos en el período de un año (1984-1985). Mientras que 85 colonos del río Undumo (1996-1997) y 63 colonos del río Madidi (1997-1998) mostraron una incidencia de LC de 47,05% y 49,2% respectivamente (SM, datos no publicados).
La principal especie de parásito involucrado en el desarrollo de la LCA en Bolivia fue Leishmania (Viannia) braziliensis, con diferentes patrones epidemiológicos en diferentes regiones debido a factores como medio ambiente, actividad y exposición humana y biodiversidad entomológica.13-43-44
TENDENCIA
La tendencia de los casos de LCA creció de 278 a 3.153 del año 1983 al 2007 respectivamente;11-25 en ese año se informaron en 91 municipios de un total de 327 (27.8%), de los cuales al menos 61 municipios tuvieron casos autóctonos (19% del total), con una población en riesgo de alrededor de 1180000 personas, por lo que la tasa de incidencia promedio de leishmaniasis en Bolivia aumentó de 4,8 a 27.0 por 100000 habitantes por año.11-25 (Figura 1). Para el año 2007, cuando se registró la mayor incidencia en el país, la región de la cuenca del Amazonas reportó el 97.9% de los casos (42% en la zona sub tropical y 55.9% en la selva tropical). El 2.1% restante de los casos se notificó en la cuenca del Río de la Plata (0.8% en la zona sub tropical y 1.3% en las planicies tropicales);25 (Figura 2) los nuevos municipios informantes están ubicados en zonas muy poco habitadas y lejanas por lo que su notificación es irregular;11-25 en el mismo año, tres departamentos informaron el 87% de los casos: La Paz: 1753 (55%); Beni 574 (18%) y Pando 416 casos (13%).
En el año 2000, el PNCL reportó 2043 casos con LCA en 80 municipios (50 municipios con transmisión autóctona), luego, en 2001, los municipios se estratificaron según la incidencia por 1000 habitantes, 24 como alto riesgo (tasa de 3.0 a 10.5 x 1000 habitantes); 13 con riesgo medio (tasa de 1,0 a 2,9 x 1000 habitantes) y 24 municipios con riesgo bajo (tasa de 0 a 0,9 x 1000 habitantes), además de los casos de inmigrantes de 30 municipios no endémicos registrados en la región andina.11 Durante el 'año pico' de 2007, se notificaron 3182 casos de LCA en 91 municipios.25 La incidencia más alta de transmisión a nivel de municipio se informó en el departamento de Pando en los municipios de Santos Mercado fronterizo con Brasil (27.7 por 1000 habitantes) y la frontera de Filadelfia con Perú (18.9 por 1000 habitantes) y en el departamento de La Paz en Chulumani (22.0 por 1000 habitantes).11-25
La leishmaniasis afecta principalmente a poblaciones vulnerables de bajos ingresos; El 55% de los 2076 pacientes estudiados entre 1982 y 1993 fueron migrantes itinerantes o definitivos de la región andina no expuesta; Luna V y cols.45 estudiaron 2909 pacientes (2001 al 2006), 90.8% eran indígenas (77.6% aymaras, 21.8%, Quechuas, 0.6% mosetenes) mientras que los casos restantes se distribuyen como 7.2% mestizos, 1.6% blancos 0.4% negros. La mayoría de los casos (75,4%) estaban relacionados con el comercio o el cultivo de la coca (Erythroxylon coca).
La prevalencia promedio de LMC en los últimos 30 años es del 7%, generalmente por metástasis de la primo infección cutánea y tratamiento insuficiente o no adecuado.11-24 La proporción inicial por sexo hombre/mujer fue de 4/1 en los años 80, (migrantes pioneros varones a la zona tropical); cambiando a 2/1 en 2007 (rol laboral cada vez más importante de la mujer).11-24-28-39
La tasa de LCA en niños menores de 5 años de edad es del 8%, lo que sugiere una transmisión peridoméstica. En el foco de las Yungas (colonización antigua), el 65% de los pacientes tiene LCA antes de los 10 años de residencia, principalmente con úlceras en la cara y en ambos sexos; se propuso que este patrón se produce debido al cambio en los hábitos de las especies de vectores, y a las densidades o incluso al cambio de las especies de vectores principales en las áreas peridomésticas y domésticas.13-21-29-46-47 Sin embargo, el grupo de edad con mayor incidencia de LCA fue el económicamente activo, relacionado con actividad laboral en los bosques. De un total de 27,724 casos reportados entre 1997 y 2007, el grupo de 15-49 años reportó el 67% de los casos, con solo 403 (1.3%) menores de un año.25
TEMPORALIDAD
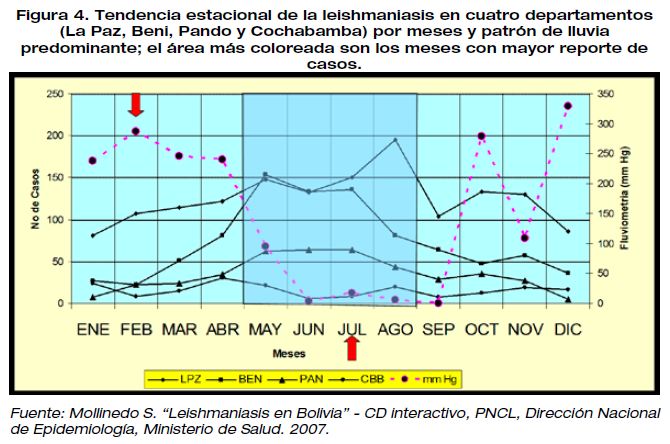
Las notificaciones mensuales en los focos en los departamentos de La Paz, Beni, Pando y Cochabamba en el año 2006, señalan un mayor número de casos entre los meses de mayo a agosto, después de la temporada de lluvias.11-25-46-47 Las observaciones repetidas durante más de 30 años, nos permiten suponer que en el foco de las Yungas (zona sub tropical) el patrón de transmisión (contacto-vector-reservorio humano) se agrupa entre enero a marzo (temporada de lluvias), período en que las casas son invadidas por grandes roedores (reservorios potenciales) en busca de refugio y alimento, época que coincide con la densidad pico del vector Pintomyia nuneztovari anglesi. Por otro lado, en relación con las actividades de exposición laboral, en Alto Beni y la región de la Amazonia, la infección se produciría en el momento de la tala y el corte del bosque (chaqueo) en la estación seca de julio a septiembre.11-13-46-47 (Figura 4).
ESPECIES DE LEISHMANIA
Se han descrito seis especies de Leishmania asociadas con enfermedades humanas en Bolivia: Leishmania (V.) braziliensis;2-7-10-41-43-48-49-50 Leishmania (L) infantum;18-24 Leishmania (L.) amazonensis;51-52 Leishmania (V.) lainsoni;53 Leishmania (V.) guyanensis;54-55 una variante local de L. (Leishmania) mexicana.56
No hay estudios de prevalencia disponibles para cada una de las especies de parásitos; la mayoría de los casos de LMC se reportan en la región subtropical, con una alta prevalencia de Leishmania (V.) braziliensis. La variante de L. (L.) mexicana fue reportada por primera vez en el año 2.017, requiriendo una investigación adicional.
FLEBOTOMINAE
Su investigación en Bolivia puede dividirse en tres periodos: a) estudios pioneros: Jorge Velasco (1973), en los Yungas del Departamento de La Paz4 y los trabajos por el equipo del Centro Nacional de Enfermedades Tropicales (CENETROP) en el Departamento de Santa Cruz5-7. b) de 1982 a 1993 el equipo del IBBA y de 1998 al 2006 en el INLASA, que en conjunto con la Cooperación Francesa (Institut de Recherche pour le Developpement), realizamos investigaciones en las zonas selváticas, peri domiciliares y domiciliares en las zonas tropicales de los Departamentos de La Paz, Beni, Pando, Santa Cruz y Tarija.4-13 c) Desde 2005 a la actualidad, Centro Universitario de Medicina Tropical (CUMETROP), Facultad de Medicina, Universidad San Simón, con investigaciones en los Departamentos de Cochabamba y Tarija.
Para el año 2016, se tenían registradas 121 especies de flebótomos en Bolivia;39 los mapas actuales de distribución de flebótomos son incompletos, tanto a nivel local como nacional; la diversidad de ecosistemas desde la zona sub tropical a la amazónica (170 a 2700 m), muestran una fauna diversa de Phlebotominae, con diferente distribución y densidades según la altitud. Se incriminaron siete especies como vectores de parásitos de Leishmania: Lutzomyia longipalpis;19 Psychodopygus yucumensis;57 Psy. llanosmartinsi;57 Psy. carrerai carrerai;58 Pyntomyia nunestovari anglesi;59-60-61-62 Nyssomyia neivai;29-63 Ny. shawi;54 sin embargo investigadores de países vecinos en zona de frontera, han señalado otras especies comprobadas o sospechosas de su rol vectorial.
El humano es menos atractivo que los animales para Lu. longipalpis, vector de L. infantum;13-19 las otras seis especies son altamente antropofílicas, con un mayor riesgo en lugares donde sus densidades son altas; Psy. yucumensis, Psychodopygus llanosmartinsi y Psy. carrerai carrerai están estrechamente relacionadas con el bosque primario. En el área de focos de Yungas Py. nuneztovari anglesi y en el foco Isiboro Secure Ny. shawi son dominantes en entornos domésticos y peri domesticos.46-59-60-61-62-63 Otras posibles especies de vectores posibles son Psy. ayrozai y Bichromomyia flaviscutellata que se había encontrado en áreas endémicas y tiene una fuerte antropofilia.13 Los poblaciones bolivianas dan nombres comunes a las Lutzomyias: Quechicho, Champari, Ya te vi, Plumilla, Roco roco.
La adaptación de algunas especies de flebotominas a ambientes periurbanos y el consecuente cambio en sus hábitos, permite la instalación de ciclos peri domésticos eventuales por "vectores permisivos" que podrían involucrar a más de una especie de leishmania simpátrica. En este sentido, las especies predominantes de Py. nunestovari anglesi en las Yungas (valles interandinos del departamento de La Paz) se encontraron infectadas con Le. (V.) braziliensis y Le. (L.) amazonensis;51-52 Se observó un escenario similar con Ny. shawi, la especie más importante en el peri domicilio en el área de Isiboro Secure (departamento de Cochabamba), donde se encontró que estaba infectada con: Leishmania (V.) braziliensis y Leishmania (V.) guyanensis.55 En la zona del Amazónica (Pando, Beni y norte de La Paz), se tenía registradas 20 especies;13 diferentes autores han reportado a Ny. whitmani y Trichophoromyia auraensis como las especies más frecuentes en la región amazónica occidental, trinacional (Brasil, Perú y Bolivia), seguidas de Ps. davisi, Ps. carrerai, Ny. antunesi y Ps. llanosmartinsi.39
En Tarija, se han notificado cuatro especies, Ny. neivai 64 y Mg. migonei, han sido incriminadas como vectores de L. (V) braziliensis, y se encontraron naturalmente infectadas en Argentina, junto a Ev. cortelezzii, Psathromyia bigeniculata, Psa. punctigeniculata, Micropygomyia quinquefer. Nyssomyia neivai es la más abundante en bosques secundarios y ambientes peri-domésticos asociados con casos humanos.28
Respecto a LV, el principal vector de LV, Lutzomyia longipalpis, otras especies de flebótomos próximas a Lu. longipalpis como Lu. cruzi o menos relacionadas, pero adaptadas a los ambientes con modificación antrópica como Migonemyia migonei, pueden actuar como el/los vector(es) de L. infantum en áreas de LV en las que no existe Lu. longipalpis o en escenarios con presencia simpátrica de ambas especies.22 Hasta 2016, se habían descrito cuatro regiones con la presencia de dos morfo tipos de Lu. longipalpis: fenotipo 1S en el foco del departamento de La Paz; fenotipo 2S hallado en la Provincia Germán Busch del departamento de Santa Cruz y en dos zonas andinas entre 1.800 y 2.700 m, en la localidades de Uyuni del departamento de Chuquisaca y Toro-Toro del departamento de Potosí; En 2017, se registró la presencia de Lu. longipalpis en Assis, estado del Acre, frontera trinacional Brasil, Bolivia y Perú, y el 2018 se encontraron ejemplares en Yacuiba, provincia Gran Chaco del departamento de Tarija; estas dos últimas descripciones están acompañadas con la presencia de casos de LV humanos, lo que nos hace presumir la dispersión de Lu. longipalpis fenotipo 1S en esas dos regiones, siendo necesario mayores estudios.21-22
RESERVORIOS
El perro (Canis lupus familiaris) se considera la principal fuente de infección de Leishmania infantum en el centro de atención de los Yungas de La Paz; sin embargo, en relación con Leishmania (V.) braziliensis, el perro sería más una víctima similar al humano que un reservorio, y tiene un papel marginal en el ciclo de estos parásitos.13-20 Otras infecciones naturales por Leishmania han sido reportadas principalmente en marsupiales, roedores, carnívoros y edentados; habiendo sido aislada L. (V.) braziliensis y L. (L.) amazonensis de Conepatus chinga rex;51 L. (L.) amazonensis de Akodon sp.; Oligoryzomys spp.; Sciuris vulgaris y Orizomys capito;51-65 y Leishmania (L) infantum del Coendu prehensilis.66
Actualmente. el ciclo de transmisión en muchos focos es solo parcialmente conocido, principalmente sobre reservorios silvestres. En los focos de bosque primario (áreas de colonización o incursión humana reciente, el humano tiene contacto directo con vectores que se alimentan de animales silvestres; en focos secundarios (áreas de colonización más antigua) el humano está infectado por vectores adaptados a ambientes antrópicos (cultivos, bosque residual), con animales domésticos y sinantrópicos silvestres, y tan cerca de las áreas donde duermen que los vectores podrían entrar en las casas para alimentarse de los seres humanos.13-28-39 Es necesario mayores estudios para determinar el papel que juegan estas especies en el ciclo de transmisión de especies de Leishmania.
DIAGNÓSTICO
La población en riesgo está dispersa en regiones con dificultades de acceso y con una cobertura insuficiente de los centros de salud. La mayoría de los pacientes demandan atención en el sistema de salud con lesiones ya avanzadas y después de haber recurrido a primero a familiares (tratamientos empíricos), luego a la comunidad (experiencia de antiguos enfermos) y finalmente a curanderos (medicina tradicional), al no solucionar su problema de salud opta por trasladarse a un centro de salud (tarda entre uno a cinco días en llegar); las barreras de accesibilidad resultaron en una gran peregrinación entre la atención de salud pública para el diagnóstico y tratamiento de pacientes con leishmaniasis.67
Los pacientes generalmente viajan por carretera o por ríos durante dos o tres días para ser atendidos en centros de salud y entre tres y siete días para llegar a centros especializados en ciudades grandes.
En nuestra experiencia en el IBBA (1982 a 1993), estudiamos por encima de 4000 pacientes, en los cuales 2078 diagnosticamos Leishmaniasis, mediante frotis de los bordes de la lesión (3 o más por paciente), con una sensibilidad del 38 al 80%; también se realizó serología en todos los pacientes. en casos especiales (forma, tipo de lesión y origen) se inició el protocolo para aislar el parásito, 103 cultivos (68 positivos), 52 cepas de tipificadas por isoenzimas; obteniendo cuatro pacientes con LV (0,19%); dos con LCD (0.09%); 1366 con LC (65.7%) y 706 con LMC (34.02%). En INLASA (1998 a 2006) estudiamos más de 3000 pacientes, en 1922 de ellos se diagnóstico LCA: 1384 con LC (72%) y 538 con LMC (27,9%) realizando frotis en todos ellos, reacción intradérmica a 26 pacientes, no pudiendo realizar otros exámenes. La consolidación de la red de laboratorios de diagnóstico para la leishmaniasis presenta obstáculos debido a las restricciones de apoyo financiero para la capacitación, pero particularmente debido a la falta de cumplimiento de los protocolos regulatorios y el apoyo financiero para permitir el cumplimiento de esta regulación; la referencia y contra referencia de las muestras dentro de la red de Laboratorios prácticamente no existe y aun no se ha implementado el diagnóstico de LV por pruebas rápidas en los Niveles I y II del Sistema Nacional de Salud.68-69-70 Los laboratorios de las grandes ciudades realizan pruebas de Biología molecular, en protocolos de investigación. 50-71-72-73
TRATAMIENTO
El antimonato de meglumina (comercial y genérico), es el tratamiento de primera línea con que se distribuye de forma gratuita, tiene una tolerancia aceptable y una buena respuesta terapéutica, mediante inyección intramuscular en una dosis de 20 mg SbV / kg / día, en una serie (20 días para LC, 30 días para LMC y LV), realizando una segunda serie (persistencia de la úlcera y frotis positivos), generalmente en forma ambulatoria; La eficacia clínica para LC osciló entre 70% y 90%; en la LV fue de 100%.11-25-28-39-74 La cantidad de medicamentos distribuidos por el PNCL no siempre es suficiente para satisfacer la demanda real, proporcionando menos del 50%; agencias como la iglesia y organizaciones no gubernamentales intentan cubrir el 50% restante (el costo del tratamiento por paciente variaba de US $ 250 a US $ 300), además muchos pacientes recurren a servicios de salud fronterizos en otros países.28-39 Los pacientes con LMC son tratados con Anfotericina B, en los hospitales de II nivel.11-25-74
En el último decenio diversos investigadores han propuesto la reutilización de medicamentos, uso de combinaciones, inmunomoduladores, investigación en vacunas, investigación de plantas y nuevos sistemas de aprovisionamiento. Diferentes protocolos de tratamiento se han implementado: antimoniato de meglumina intralesional;74 Antimoniato de meglumina solo o en combinación a Estibogluconato de sodio;75 Anfotericina B;76 Itraconazol77 y miltefosina; este último producto con resultados alentadores: tan efectiva como Glucantime o Anfotericina B frente a lesiones de LC y LMC, con menor toxicidad y dosificación oral.79-81
De los 36 grupos pueblos originarios, los Tsiman y Tacana (departamento de La Paz, Beni y Pando) y guaraní (departamento de Santa Cruz y Tarija) han contribuido con los conocimientos tradicionales con fitoterapias: Galipea longlifora, Pera beniensis;82-85 y Piper aduncum, Piper leavilimbun; Piper peltatum; Piper rusbyi; Vermonia squamulosa86 de las que se aislaron compuestos con actividad antifúngica y leishmanicida.
PREVENCIÓN Y CONTROL
El PNCL implementó la estrategia de "prevención y control", con recomendaciones básicas para la población a fin de evitar las picaduras de insectos en áreas endémicas, principalmente al amanecer y al atardecer, promoviendo el uso de repelentes de insectos, rejillas anti-insectos en puertas y Ventanas (1989), también otras actividades esporádicas que son financiadas por otros programas (malaria) cuando existe una presión política por los medios de comunicación sobre eventuales brotes. La falta de recursos y evidencias sobre actividades de prevención efectivas no ha permitido su implementación, especialmente en áreas donde Leishmania no coexiste con otras enfermedades. La sub notificación que siempre existió, se ha incrementado en el tiempo hasta llegar según algunos autores a 73,4% debido a la centralización de actividades del PNCL y la inaccesibilidad de los servicios de salud.87
La fumigación residual de los interiores de las casas y de los materiales impregnados con insecticida (mosquiteros, cortinas y ropa de trabajo) ha demostrado que son eficaces para proteger a las personas de infecciones y enfermedades. Se llevó a cabo un ensayo piloto de control con insecticidas (deltametrina) en un foco de LC en una aldea de las Yungas (zona de colonización más antigua), donde hubo evidencia de transmisión intra o peri-doméstica, durante el comienzo de la temporada de lluvias (Enero de 1987). Las paredes de las viviendas domésticas fueron tratadas (área de alojamiento de la casa, perreras, casetas avícolas y montículos), con deltametrina a 0.025 g / m2; como resultado Lu. Longipalpis, el vector local de LV, desapareció de las casas y los refugios para animales durante 9 y 10 meses, respectivamente.26
El control integrado de enfermedades transmitidas por vectores, se propuso repetidamente en Bolivia, desafortunadamente la rotación del personal técnico responsable de los programas y de las autoridades políticas, la propuesta no se consolidó en una acción continua. La "lucha antipalúdica" con el tratamiento intradomiciliario con insecticidas, utilizado de 1956 al 2018, tuvo una cronología de uso de diferentes agentes químicos: Organoclorados (DDT) 1956-1993, Piretroides (Lambdacihalotrina y Deltametrina) 1993-2013; Carbamatos (Bendiocarb) 2014-2018. Estos tratamientos aunados a otras iniciativas permitieron que la endemia por malaria disminuyese de 148 a 19 municipios para el 2018. Muchos de los 129 municipios en los que actualmente ya no se realiza tratamiento residual en paredes con insecticida, tenían en coexistencia malaria y leishmaniasis, por lo que se ha eliminando el beneficio potencial colateral de reducción de diferentes vectores diferentes a los anofelinos; lamentablemente no se registraron ni realizaron los estudios de impacto de estas actividades con respecto a los flebótomos. Así mismo, desde 2015 se realizó la distribución masiva de mosquiteros tratados con insecticida de larga duración (MTILD), solamente en los 19 municipios priorizados de la Amazonía boliviana.39
La efectividad de la ropa de trabajo (overoles) impregnada con insecticidas, se probó en un ensayo controlado en trabajadores en la jungla con una disminución en los casos nuevos de LCA, desafortunadamente los trabajadores por el calor mutilaron los overoles en sus brazos y muslos invalidando el estudio, lo que demuestra que La eficacia teórica muchas veces no se puede reproducir en condiciones de campo.42
DETERMINANTES RELEVANTES
Algunos eventos que contribuyen a los riesgos de transmisión y brotes son causados por los seres humanos (migración, deforestación, urbanización); otros son cambios en la susceptibilidad del huésped humano a la infección (inmunosupresión y desnutrición) y otros se deben a cambios ambientales naturales o eventos climáticos.88
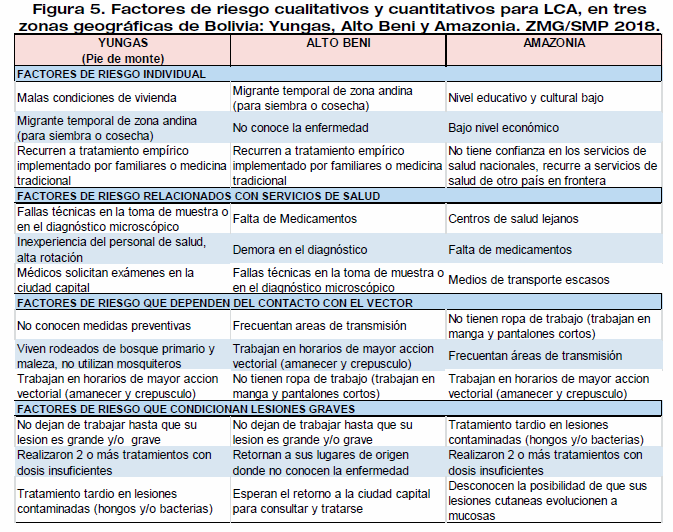
Se realizó un estudio en nativos y migrantes para investigar los factores de riesgo de la aparición de leishmaniasis cutánea (LC) y su forma mucosa (LMC) en 703 sujetos; los factores más significativos fueron: el género, el estado nativo / migratorio, la actividad y la distancia entre el hogar y el bosque; el riesgo es de tres a diez veces mayor en los migrantes que en los nativos (aparentemente debido a los lugares donde se establecieron y la susceptibilidad de los migrantes. Una otra investigación específica en 300 personas: 100 de cada una de las tres zonas geográficas endémicas (Yungas, Alto Beni y Amazonia), donde la densidad de la población aumenta mientras que las condiciones sanitarias están disminuyendo. Los determinantes relevantes identificados fueron discriminados individualmente, relacionándolos con los servicios de salud, moduladores del contacto con el vector y aquellos que causan lesiones graves. (Figura 5).
COMENTARIOS
En Bolivia Como en las otras áreas endémicas del mundo, la propagación, la ruralización y la tendencia a la urbanización de las leishmaniasis tienen una relación aparente con las intervenciones antrópicas sobre el medio ambiente.28-39-88 Las principales actividades de salud son priorizadas para el área andina, donde cada vez habitan menos población boliviana, sin embargo en la cuenca Amazónica cada vez la enfermedades de transmisión vectorial y las zoonosis tienen una mayor prevalencia; los casos notificados de leishmaniasis han estado aumentando al pasar el tiempo debido a la migración, deforestación, cambio climático y el aumento de las actividades dentro de la selva; se han observado la aparición de nuevas áreas endémicas y una tendencia al alza en la notificación de casos hasta 2008; factores logísticos y políticos han contribuido al cambio aparente en la tendencia de los casos y la tasa de incidencia de la enfermedad en el período de 2009 a 2015.
Los entornos urbano-rurales estudiados permiten afirmar que Bolivia es uno de los países latinoamericanos con mayor prevalencia de LCA; para mitigar el riesgo es necesario aumentar la capacidad de los SEDES en diagnóstico (no sólo básico), reserva estratégica de medicamentos, vigilancia activa de casos, muestreos entomológicos regulares y principalmente sensibilizar a la población (trabajadores, empresarios y autoridades) a fin de plantear estrategias participativas de control.
La existencia de numerosos informes de trabajo local y regional que permanece y los niveles intermedios, tesis, reuniones nacionales, informes técnicos de los SEDES, son denominados "información gris", que debería ser considerada por las autoridades, y rescatada para promover su difusión y publicación a mediante la orientación técnica y científica por parte de las agencias de cooperación internacional y las universidades.
El Plan quinquenal12 aprobado con la coparticipación de representantes nacionales de diversas instituciones, tenía como objetivos i. desarrollo de herramientas de Salud Pública para la comunidad y el personal de salud de Nivel I y II.11-25-68-69-70-75 ii. la construcción, mejora estructural, equipamiento y formación de recursos humanos a nivel nacional. iii. el fortalecimiento de los vínculos entre el Ministerio de Salud y las organizaciones de investigación (Universidades). iv. Incremento de las bolsa de financiamiento con la cooperación internacional y nacional (cofinanciamiento por Gobernaciones y municipios) mediante un banco de proyectos de investigación; solo los dos primeros objetivos se consolidaron en forma parcial, debido a un constante rotación de autoridades; quedando como un desafío a replantear y consolidar.
CONTRIBUCIÓN DE LOS AUTORES
Conceptualización: JSM, ZAM.
Datos históricos: JSM.
Análisis formal: JSM, ZAM.
Investigación: JSM, ZAM.
Diseño de tablas, figuras y soporte informático: ZAM
Borrador original: JSM.
Escritura, revisión y edición: ZAM, JSM.
AGRADECIMIENTOS
Los autores agradecen a los técnicos, enfermeros y médicos generales del nivel I, de los SEDES del área endémica; a los profesionales de IBBA e INLASA por su colaboración, a los pacientes que hemos tratado de brindar el mejor servicio posible; a los Lic. Pavel S. y Pavel E. Mollinedo G. por la elaboración de las figuras y al Dr. Oscar Daniel Salomón por la revisión del manuscrito.
CONFLICTO DE INTERESES
Los autores garantizan que no tienen conflicto de intereses respecto a lo que se expresa en este trabajo.
REFERENCIAS
1. INE. Censo de Población y Vivienda. Instituto Nacional de Estadística2012.. Descarga pdf. Bolivia. Acceso Noviembre 2018 Disponible en: https://www.ine.gob.bo/index.php/prensa/publicaciones/.../318-la-paz-censo-2012 [ Links ]
2. Desjeux P, Le Pont F, Mollinedo S, Tibayrenc M. Les Leishmania de Bolivie I. Leishmania braziliensis Vianna, 1.911 dans les departements de La Paz et du Beni. Premiers isolements de souches d'origen humaine. Caracterisationen zymatique.CollInt CNRS/INSER, IMEEE. 1986.p. 401-10. [ Links ]
3. Desjeux P, Le Pont F, Mollinedo S, Tibayrenc M. Relations leishmaniose et altitude. Formes cliniques, données épidemiologiques. Colloque INSERM "Anthropologie et biologie des populations andines". Editions INSERM. Toulouse. France.1976. p.247-256.
4. Mollinedo S. Reporte final Proyecto Chasqui II: Leishmaniasis, Chagas, Malaria, Toxoplasmosis, Enteroparasitosis; Instituto Boliviano de Biología de la Altura; 1994. [ Links ]
5. De Muynck A. CENETROP a joint Belgian-Bolivian medical development project in Santa Cruz, Bolivia. Ann Soc Belg Med Trop 1979; 59: 325-327. [ Links ]
6. De MuynkA, Orellana H, Ribera B, Melgar B, Silva de Lagrava M. Estudio epidemiológico y clínico de la leishmaniasis mucocutanea en Yapacani (Oriente Boliviano). Bol. Inf. CENETROP 1978;N°4:155-167.
7. La Fuente C, Recacoechea M, Tibayrenc M, Urjel R, Darras C, Cardozo L. Leishmaniasis en Bolivia: presencia de dos complejos de Leishmania en los Llanos Orientales del Departamento de Santa Cruz-Bolivia. Bol. Científico Centro Enfermedades Trop. 1986;12:1-15. [ Links ]
8. Recacochea M. Ulceras cutáneas en nuestro medio, especial énfasis en leishmaniasis cutáneo-mucosa. Bol. Inf. CENETROP.1980; 6. Bolivia: 24-30.
9. Urjel R, Recacoechea M, La Fuente C, Orellana H. A simple method for the collection of material from cutaneous and mucocutaneous leishmaniasis lesions. Trans R SocTrop Med Hyg.1983;77: 882-883. [ Links ]
10. Urjel R, Recacoechea M, Desjeux P, Bermudez H, Villaroel G, Balderrama S, Carrasco J, Aguilar O, Dujardin JC, Le Reay D. Leishmaniasis en los Llanos de Bolivia VI; Caracterización preliminar de once aislados de Leishmania. Bol Científico Centro Enfermedades Trop.1987;13: 38-44. [ Links ]
11. Mollinedo S., Monasterios H, Magne M, Vallejos E, Velarde J, Chuquimia G. Leishmaniasis - Guía operativa para el control en Bolivia. Serie de documentos técnico-normativos. Ministerio de Salud y Deportes. La Paz. Bolivia. 2007. [Acceso Noviembre 2018]. Disponible en: https://www.researchgate.net/publication/277311188_Leishmaniasis_-_Guia_Operativa_para_el_Control_en_Bolivia
12. Mollinedo S. "Plan Quinquenal Leishmaniasis 2007-2011". Programa Nacional de Control de las leishmaniasis. Unidad de Epidemiología, Dirección General de Servicios de Salud, Ministerio de Salud y Deportes. La Paz. Bolivia. 2007.
13. Le Pont F, Desjeux P, Torres M, Fournet A, Mouchet J. Leishmanioses et phlebotomes en Bolivie. Institut Francais de Recherche Scientifique pour le Developpement en coopération ORSTOM -INSERM. ORSTOM.1992;Paris. France.
14. Migone LE. Um caso de kalazar a Assuncion (Paraguai). Bulletin de la Société de PathologieExotique. 1913;6:118-20. [ Links ]
15. Arruda W., Da Costa FC, Nahas S, Rosenberg G. Leishmaniose visceral americana: Constataçao de dois casos. Brasil Medico. 1949; 8-9, p. 63-65.
16. Gatti G, Boggino J. Prieto C. Un nouveau foyer de leishmaniose viscerale en Amérique du Sud. Bulletin de la Société de Pathologie Exotique.1939; 32: 602-605. [ Links ]
17. Angles R., Le Pont F, Desjeux P. Visceral canine leishmaniasis in Bolivia. Trans. Roy. Soc. Trop. Med. Hyg. 1982; 76: 704. [ Links ]
18. Desjeux P, Aranda E, Aparicio O, Mollinedo S. Human visceral leishmaniasis in Bolívia: First proven autochthonous case from "Los Yungas". Trans R Soc Trop Med Hyg.1983; 77:1003-1011. [ Links ]
19. Le Pont F, Desjeux P. Leishmaniasis in Bolivia I: Lutzomyia longipalpis (Lutz & Neiva, 1.912) as the vector of visceral leishmaniasis in Los Yungas. Trans R Soc Trop Med Hyg.1985; 79: 227-231. [ Links ]
20. Le Pont F, Mollinedo S, Mouchet J, Desjeux P. Leishmaniose en Bolivie IV. Le chien dans les cycles des Leishmanioses en Bolivie. Mem Inst Oswaldo Cruz.1989; 84: 417-421. [ Links ]
21. Mollinedo JS, Mollinedo ZA, Gironda W, Mollinedo PE, Mollinedo RE, Salomon OD. 2020. Leishmaniasis en Bolivia-XIV Leishmaniasis Visceral-Revisión y estado actual. 55° Congreso da Sociedade Brasileira de Medicina Tropical. Belo Horizonte. Brasil.
22. Mollinedo JS, Mollinedo ZA, Gironda WJ, Mollinedo RE, Mollinedo P, Salomon OD. 2020. Visceral Leishmaniasis in Bolivia, Current Status. In press.
23. Mollinedo S, Muñoz M, Hervas D, Yaksic N, Torres M, Desjeux P. Leishmaniasis visceral y tegumentaria en niños en dos zonas endémicas de Bolivia. Parasitología al Día.1992;16:117-120. [ Links ]
24. Dimier-David L, Inofuentes A, Carrasco M, David C, Vargas F, Revollo S, Dedet JP. A new case of autochthonous visceral leishmaniasis in Bolivia. Ann Soc Belg Med Trop.1991;71: 275-278. [ Links ]
25. Mollinedo S. "CD interactivo de Leishmaniasis en Bolivia", Programa Nacional de Control de la Leishmaniasis, Dirección Nacional de Epidemiología, Ministerio de Salud, Bolivia. Edición USAID; 2007
26. Le Pont F, Padilla JM, Desjeux P, Richard A, Mouchet J. Impact of the spraying of deltamethrin in a focus of leishmaniasis in Bolivia. Ann Soc Belg Med Trop.1989; 69:223-232. [ Links ]
27. Flores MD, Postigo J, Mita N, Cruz I, Alvar J, Bastrenta B. Leishmaniasis visceral sub clínica en 123 individuos de un cantón de la Provincia Caranavi-La Paz. Bolivia. Rev Soc Bol Ped. 2002; 41:80-85. [ Links ]
28. Mollinedo S, Mollinedo Z, Magne M, Gironda WJ, Salomon OD. Leishmaniasis en Bolivia. Revisión y estado actual en Tarija, frontera con Argentina. Biomédica. 2020; 40(Supl. 1):45-61. [ Links ]
29. Mollinedo S. Situación actual de la leishmaniasis en el departamento de Tarija, frontera con la Argentina. Boletín Informativo Epidemiológico. Unidad de Epidemiología. Ministerio de Salud y Deportes Bolivia.2006; N°3:1-4.
30. Balcázar J. M. Epidemiologia Boliviana. 1946;Imprenta López. Buenos Aires. Argentina.
31. Garrett J. La espundia en Bolivia. Observaciones del Dr. Manuel Antonio Vaca Diez (Comentario histórico). Boletín Informativo de CENETROP.1983; 9:1-5. [ Links ]
32. Sagarnaga E. Recuerdos de la Campaña de Acre de 1903. Mis Notas de Viaje. Talleres gráficos la Prensa de J. L. Calderón. 1909;La Paz, Bolivia.
33. Pardo-Valle N. La espundia en territorio boliviano. Revista del Instituto Médico de Sucre 1906;1: 8-11. [ Links ]
34. Veintemillas JE. Mentioned without reference by Balcazar JM. Epidemiologia Boliviana. Imprenta López. Buenos Aires. Argentina. 1946; 250 p.
35. Desjeux P. Leishmaniose cutanéé et cutanéo-muqueuse américaine. Etude de 113 cas observés en Bolivie [These Doctorat Médecine]. Paris. France. 132 p. 1974.
36. Desjeux P., Quilici M, Lapierre J. A propos de 113 cas de leishmaniose cutanée et cutanéo-muqueuse observés en Bolivie. Etude sero-inmunologique de 71 cas. Bull. Soc. Path. Exot. 1974; 67: 387-395. [ Links ]
37. Walton BC, Chinel LV, E. Eguia O. Onset of espundia after many years of occult infection with Leishmania braziliensis. American Journal of Tropical Medecine and Hygiene.1973;22: 696-698.
38. Walton BC, Chinel LV. Racial differences in espundia. Annals of Tropical Medecine and Parasitology.1979;73: 23-29. [ Links ]
39. Mollinedo ZA, Noto J, Mollinedo PE, Gironda WJ, Mollinedo JS, Salomon OD. Leishmaniasis en Bolivia - Revisión y estado actual en Pando, Bolivia - Frontera con Brasil y Perú. 2020. En prensa. [ Links ]
40. Martinez E, Mollinedo S, Torrez M, Muñoz M, Bañuls S, Le Pont F. Co-infection by Leishmania amazonensis and L. infantum/L.chagasi in a case of diffuse cutaneous Leishmaniasis in Bolivia. Trans R SocTropMedHyg.2002;96: 529-532. [ Links ]
41. Desjeux P, Mollinedo S, Le Pont F, Paredes A, Ugarte G. Cutaneous leishmaniasis in Bolivia. A study of 185 human cases from Alto Beni (La Paz department). Isolation and isoenzyme characterization of 26 strains of Leishmania braziliensis braziliensis. Trans R Soc Trop Med Hyg.1987; 81:742-746. [ Links ]
42. Mollinedo S, Desjeux P, Le Pont F. American leishmaniasis. SHELL Intemational Petroleum Maatschappij B.V., Occupational Health and Hygiene Digest. 1985; Beni Bolivia 23:14-16.
43. Bermudez H, Torrico F, Rojas E, Balderrama F, Le Ray D, Guerra H, Arevalo J. Leishmaniasis in the lowlands of Bolivia, prevalence of the disease in two groups of localities with different settlement ages in Carrasco Tropical, Cochabamba. Arch Inst Pasteur Tunis.1993; 70.Francia:443-453.
44. Gomez C, Rodriguez-Morales AJ, Franco-Paredes C. Impact ofClimate Variability in the Occurrence of Leishmaniasis in Bolivia. Am J Trop Med Hyg.2006; 75 (5 Suppl): 42. [ Links ]
45. Luna V, Chuquimia G, Parra R, Palacios J, Neves M, Carvalho-Costa F. Active surveillance of American tegumentary leishmaniasis in endemic areas in rural Bolivia. Revista da Sociedad de Brasileira de Medicina Tropical. 2012;45(1). Brasil: 30-34. [ Links ]
46. Le Pont F, Mouchet J, Desjeux P, Torres-Espejo JM, Richard A. Epidemiology of cutaneous leishmaniasis in Bolivia 2. Transmission patterns. Ann Soc Belg Med Trop.1989;69: 307-312. [ Links ]
47. Torrez M, Le Pont F, Mouchet J, Desjeux P, Richard A. Epidemiologie de la Leishmaniose tegumentaire en Bolivie 1. Description des zones d'etude et frequence de la maladie. Ann Soc Belge Med Trop.1989;69: 297-306. [ Links ]
48. Torrez-Espejo JM, Pratlong F, Le Pont F, Mouchet J, Desjeux P, Rioux JA. Leishmaniasis in Bolivia V. Human strains of Leishmania (V.) braziliensis from the Department of Pando. Mem Inst Oswaldo Cruz.1989; 84: 583. [ Links ]
49. Dimier-David L, David C, Ravisse P, Bustillos R, Revollo S, Lyevre P, Munoz M, Vargas F, Dedet JP. Parasitological diagnosis of mucocutaneous leishmaniasis due to Leishmania b. braziliensis in Bolivia. Rev Soc Bras Med Trop.1991;24:231-234. [ Links ]
50. Revollo S, Dimier-David L, David C, Lyevre P, Camacho C, Dedet JP.. Isoenzyme characterization of Leishmania braziliensis braziliensis isolates obtained from Bolivian and Peruvian patients. Trans R Soc Trop Med Hyg.1992; 86: 388-391. [ Links ]
51. Martinez E, Le Pont F, Torrez M, Telleria J, Vargas F, Muñoz M.A new focus of cutaneous leishmaniasis due to Leishmania amazonesis in a Sub Andean region of Bolivia. Acta Trop.1998; 71: 97-106. [ Links ]
52. Telleria J, Bosseno MF, Tarifa T, Buitrago R, Martinez E, Torrez M. Putative reservoirs of Leishmania amazonensis in a Sub-andean focus of Bolivia identified by kDNA-Polymerase Chain Reaction. Mem Inst Oswaldo Cruz.1999;94: 5-6. [ Links ]
53. Martinez E, Le Pont F, Mollinedo S, Cupolillo E.A first case of cutaneous leishmaniasis due to Leishmania (Viannia) lainsoni in Bolivia. Trans R Soc Trop Med Hyg.2001; 95: 375-377. [ Links ]
54. Garcia L, Kindt A, Quispe-Tintaya KW, Bermudez H, Llanos A, Arevalo J, Bañuls AL, De Doncker S, Le Ray D, Dujardin JC. American tegumentary leishmaniasis: antigene polymorphism, taxonomy and clinical pleomorphism. Infect Genet Evol.2005:5:109-116. [ Links ]
55. Garcia AL, Tellez T, Parrado R, Rojas E, Bermudez H, Dujardin JC. Epidemiological monitoring of American Tegumentary leishmaniasis: molecular characterization of a peridomestic transmission cycle in the Amazonian lowlands in Bolivia. Trans R Soc Trop Med Hyg. 2007;101:1208-1213. [ Links ]
56. Bilbao-Ramos P, Dea-Ayuela MA, Cardenas-Alegría O, Salamanca E, Santalla-Vargas J. A, Benitod C, Flores N, Bolás-Fernández F. Leishmaniasis in the major endemic region of Plurinational State of Bolivia: Species identification, phylogeography and drug susceptibility implications. Acta Tropica.2017; 176. USA: 150-161.
57. Le Pont F, Desjeux P. Leishmaniasis in Bolivia II. The involvement of Psychodopygus yucumensis and Psychodopygus llanosmartinsi in the sylvatic transmission cycle of Leishmania braziliensis braziliensis in the lowland subandean region. Mem Inst Oswaldo Cruz.1981;81: 311-318. [ Links ]
58. Le Pont F, Breniere F, Mouchet J, Desjeux P. Leishmaniose en Bolivie III. Psychodopygus carrerai carrerai (Barretto 1946) nouveau vecteur de Leishmania braziliensis Vianna, 1911 en milieu sylvatique de région sub andine basse. C R Acad Sc Paris.1988; 307. Paris. France: 279-282.
59. Le Pont F, Mouchet J, Desjeux P. Leishmaniasis in Bolivia VI. Observations on Lutzomyia nuneztovari anglesi Le Pont & Desjeux, 1984 the presumed vector of tegumentary leishmaniasis in the Yungas focus. Mem Inst Oswaldo Cruz.1989;84:277-278. [ Links ]
60. Martinez E, Le Pont F, Torrez M, Telleria J, Vargas F, Dujardin JC, Dujardin JP, Lutzomyia nuneztovari anglesi (Le pont & Desjeux, 1984) as a vector of Leishmania amazonensis in a sub-Andean leishmaniasis focus of Bolivia. Am J Trop Med Hyg.1999; 61:846-849. [ Links ]
61. Le Pont F, Mouchet J, Desjeux P. Leishmaniasis in Bolivia VI. Observations on Lutzomyia nuneztovari anglesi Le Pont, F, Desjeux P, 1984 The presumed vector of tegumentary leishmaniasis in the Yungas focus. Mem Inst Oswaldo Cruz.1989; 84: 277-278. [ Links ]
62. Torrez M, López M, Le Pont F, Martínez E, Munoz M, Hervas D, Yaksic N, Arevalo J, Sossa D, Dedet JP, Dujardin JC. Lutzomyia nuneztovari anglesi (Diptera: Psychodidae) as a probable vector of Leishmania braziliensis in the Yungas, Bolivia. Acta Trop.1998;71: 311-316. [ Links ]
63. Marcondes CB, Le PontF, LozoveiAL. Lutzomyia neivai (Pinto, 1926) in Bolivia (Diptera, Psychodidae, Phlebotominae). Mem Inst Oswaldo Cruz.1998;93: 203-204. [ Links ]
64. Bermudez H., Garcia AL, Troncoso F. Leishmaniasis in the lowlands of Bolivia. Entomological studies on sandflies ofthe "Valle del Sacta". Tropical Carrasco ofthe Department of Cochabamba. Arch Inst Pasteur Tunis.1993; 70: 455-463. [ Links ]
65. Kerr SF, Emmons LH, Melby PC, Liu C, Perez LE, Villegas M. Leishmania amazonensis infections in Oryzomys acritus and Oryzomys nitidus from Bolivia. Am J TropMedHyg.2006; 75:1069-1073. [ Links ]
66. Le Pont F, Mouchet J, Desjeux P. Leishmaniasis in Bolivia VII. Infection of sentinel porcupines (Coendou prehensilis, L.) by Leishmania (Le.) chagasi. Mem Inst Oswaldo Cruz.1989;84:575. [ Links ]
67. Eid D, San Sebastian M, Hurtig AK, Goicolea I. Leishmaniasis patients pilgrimage to access health care in rural Bolivia: a qualitative study using human rights to health approach. BMC international Health and Human Rights. 2019 19:2 p:2-9.
68. Mollinedo S. Manual de Diagnóstico de procedimientos de laboratorio para el diagnóstico de las Leishmaniasis. Ministerio de Salud y Deportes. 2006. La Paz. Bolivia.
69. Mollinedo S. 1.. -Las Leishmaniosis - Modulo de Auto aprendizaje para auxiliares de servicios de salud. Serie de Documentos Técnico normativos. Publicación N° 81. Ministerio de Salud. La Paz. Bolivia. 2008. [Acceso Noviembre 2018]. Disponible en: https://www.researchgate.net/.../309282371_Las_Leishmaniosis_-_Modulo_de_Auto_ap...
70. Mollinedo S.. 2.-Técnicas de laboratorio para el diagnóstico de las Leishmaniosis. Módulo de auto aprendizaje para técnicos de laboratorio. Serie de Documentos Técnico normativos. Publicación 82. Ministerio de Salud. La Paz. Bolivia. 2008. [Acceso Noviembre 2018]. Disponible en: https://www.researchgate.net/.../309282490_Las_Leishmaniosis_-_Modulos_de_auto_ap...
71. Bastrenta B., Mita N, Buitrago R, Vargas F, Flores M, Machane M, Yacsik N, Torrez M, Le Pont F, Breniere F. Human mixed infections of Leishmania spp. and Leishmania-Trypanosoma cruzi in a sub Andean Bolivian area: identification by polymerase chain reaction/hybridization and isoenzyme. Mem Inst Oswaldo Cruz. 2003; 98: 255-264. [ Links ]
72. Garcia L, Kindt A, Bermudez H, Llanos-Cuentas A, De Doncker S, Arevalo J, Quispe-Tintaya KW, Dujardin JC. Culture-independent species typing of neotropical Leishmania for clinical validation of a PCR-based assay targeting heat shock protein 70 genes. J Clin Microbiol.2004; 42:2294-2297. [ Links ]
73. Garcia, AL, Parrado R, De Doncker S, Bermudez H, Dujardin JC. American tegumentary leishmaniasis: direct species identification of Leishmania in non-invasive clinical samples. Trans. R. Soc. Trop. Med. Hyg. 2007;101: 368-371. [ Links ]
74. Mollinedo S. Manual práctico de tratamiento de las Leishmaniasis, Unidad de Parasitología y Entomología, Instituto Nacional de Laboratorios de Salud La Paz Bolivia. 2006; [Acceso Noviembre 2018]Disponible en: www.bionica.info/biblioteca/Mollinedo2002.pdf [ Links ]
75. Bermudez H, Rojas E, Garcia L, Desjeux P, Dujardin JC, Boelaert M, Chappuis F. Generic sodium stibogluconate is as safe and effective as branded meglumine antimonate, for the treatment of tegumentary leishmaniasis in Isiboro Secure Park, Bolivia. Ann Trop Med Parasitol.2006; 100: 591-600.
76. Dedet JP, Melogno R, Cardenas F, Valda L, David C, Fernandez V, Torrez ME, Dimier-David L, Lyevre P, Villareal ME. Rural campaign to diagnose and treat mucocutaneous leishmaniasis in Bolivia. Bull World Health Organ.1995; 73: 39-45. [ Links ]
77. Rodriguez LV, Dedet JP, Paredes V, Mendoza C, Cardenas F. A randomized trial of amphotericin B alone or in combination with itraconazole in the treatment of mucocutaneous leishmaniasis. Mem Inst Oswaldo Cruz.1995;90: 525-528. [ Links ]
78. Rojas E, Parrado R, Delgado R, Reithinger R, Garcia AL. Leishmaniasis in Chaparé, Bolivia [letter]. Emerg Infect Dis [serial on the Internet]. 2009; Apr [date cited]. Available at: http://www.cdc.gov/EID/content/15/4/678.htm. DOI: 10.3201/eid1504.081257
79. Soto J, Rea J, Balderrama M, Toledo J, Soto P, Valda L, Berman JD..Efficacy of miltefosine for Bolivian cutaneous leishmaniasis. Am J Trop Med Hyg.2008; 78:210-211. [ Links ]
80. Soto J, Toledo J, Valda L, Balderrama M, Rea I, Parra R, Ardiles J, Soto P, Gómez A, Molleda F, Fuentelsaz C, Anders G, Sindermann H, Engel J, Berman J. Treatment of Bolivian mucosal leishmaniasis with miltefosine. Clin Infect Dis.2007;44:350-356. [ Links ]
81. Soto J, Valda-Rodriquez L, Toledo J, Vera-Navarro L, Luz M, Monasterios-Torrico H, Vega J, Berman J. Comparison of generic to branded pentavalent antimony for treatment of new world cutaneous leishmaniasis. Am J Trop Med Hyg.2004; 71:577-581. [ Links ]
82. Fournet A, Barrios AA, Muñoz V, Hocquemiller R, Roblot F. Cave A. Antileishmanial activity of a tetralone isolated from Ampelocera edentula, a Bolivian plant used as a treatment for cutaneous leishmaniasis. Planta Med.1994;60: 8-12. [ Links ]
83. Fournet A, Barrios AA, Muñoz V, Hocquemiller R, Roblot F, Cavé A. Antiprotozoal activity of quinoline alkaloids isoleted from Galipea longiflora, a Bolivian plant used as a treatment for cutaneous leishmaniasis. Phytotherapy Research.1994;8:174-178.
84. Fournet A, Angelo A, Muñoz V, Roblot F, Hocquemiller R, Cave A. Biological and chemical studies of Perabenensis, a Bolivian plant used in folk medicine as a treatment of cutaneous leishmaniasis. J Ethnopharmacol. 1992;3 7:159-164. [ Links ]
85. Fournet A, Ferreira ME, Rojas A, Torres S, Fuentes S. In vivo efficacy of oral and intralesional administration of 2-substituted quinolines in experimental treatment of new world cutaneous leishmaniasis caused by Leishmania amazonensis. Antimicrobial Agents and Chemotherapy.1996; 40: 2447-2451. [ Links ]
86. Flores EN, Cabrera G, Jiménez IA, Bazzocchi IL, Giménez A. Estudio fotoquímico de 14 especies del género Piper spp. con actividad antifüngica y/o leishmanicida in Vitro. Revista Biofarbo. Bolivia.2000; 8: 9-16.
87. Eid D, Guzman-Rivero M, Rojas E, Goicolea I, HurtigAK, Illanes D, San Sebastian M. Assessment of a Leishmaniasis Reporting System in Tropical Bolivia Using the Capture-Recapture Method. Am. J. trop. Med. Hyg., 98(1), 2018, pp. 134-138.
88. Desjeux P. The increase in risk factors for leishmaniasis worldwide. Trans R Soc Trop Med Hyg, 2001; 95: 239-243. [ Links ]