Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz vol.24 no.2 La Paz 2018
ACTUALIZACIÓN
RESISTENCIA BACTERIANA POR BETA LACTAMASAS DE ESPECTRO EXTENDIDO: UN PROBLEMA CRECIENTE
BACTERIAL RESISTANCE BY EXTENDED SPECTRUM BETA LACTAMASE: A GROWING PROBLEM
Dr. Guillermo Urquizo Ayala, Dra. Jackeline Arce Chuquimia, Dra. Gladys Alanoca Mamani *
* Unidad de Medicina Interna, Hospital de Clínicas Universitario, La Paz- Bolivia
RESUMEN
Las ß-lactamasas de espectro extendido (BLEE) son enzimas que generan resistencia a la mayoría de los b-lactámicos, incluyendo a penicilinas, cefalosporinas de primera, segunda, tercera generación, monobactámicos, excepto a la cefamicina y carbapenémicos. Esta resistencia se vio incrementada por el indiscriminado uso de cefalosporinas para infecciones incluso leves. También cuentan con frecuencia con genes para otros antimicrobianos como ser aminoglucosidos, tetraciclinas y cotrimoxazol. Además, las cepas BLEE (+) son más frecuentemente resistentes a quinolonas que las cepas no productoras de BLEE. La resistencia actual que existe a las betalactamasas de espectro extendido aumenta las tasas de mortalidad, ya que en pacientes con infecciones se inician tratamientos empíricos, que al no tener buena respuesta ocasionan que el cuadro clínico llegue a evolucionar hasta la sepsis. El tratamiento de elección en estos casos es el uso de carbapenémicos, recomendación que se basa principalmente en el resultado de resistencia observada in vitro. Los nuevos carbapenémicos, como ertapenem o doripenem parecen tener una excelente actividad. Se realiza una revisión de los aspectos básicos de la aparición de cepas BLEE y su importancia en el manejo de pacientes con cuadros infecciosos, que son de frecuente presentación en los Hospitales de referencia.
Palabras clave: b - lactamasas, cepas BLEE, resistencia bacteriana.
SUMMARY
The beta-lactamase (ESBL) spread spectrum are enzymes that generate most of the b-lactamic resistance, including penicillin, cephalosporins of first, second, third generation, monobactams, except the cephamycin and carbapenem. This resistance was increased by the indiscriminate use of cephalosporins to even mild infections. Also, frequently have other genes for antimicrobials such as aminoglycosides, tetracycline and co-trimoxazole. In addition, ESBL (+) strains are most frequently resistant to quinolones to non-ESBL producing strains. The current resistance that exists to the extended-spectrum beta lactamase increase mortality rates, in patients with infections begin empirical treatments, which do not have good clinical response to evolve reaches sepsis. The treatment of choice in these cases is the use of carbapenem, recommendation based mainly that relies mainly on the result of resistance observed in vitro. The new carbapenem, ertapenem or doripenem appear to have an excellent activity. He is a review of the basics of the appearance of ESBL and its importance in the management of patients with infectious pictures, which are frequent presentation in referral Hospitals.
Key words: b - lactamases, ESBL strains, bacterial resistance.
INTRODUCCIÓN
Desde el siglo pasado se cuenta con sustancias de origen natural que contribuyen a la muerte bacteriana sin afectar al huésped humano. Estas son los antibióticos(1). Los antibióticos son sustancias químicas producidas por un ser vivo o un derivado sintético, que mata o impide el crecimiento de ciertas clases de microorganismos sensibles, generalmente son fármacos usados en el tratamiento de infecciones por bacterias, de ahí que se les conozca como antibacterianos.
Paul Vuillemin es el contribuyente del pensamiento de que los seres vivos son capaces de producir sustancias que inactivan o directamente matan a otros seres con los cuales convivían, este concepto fue presentado en 1889 como "influencias antibióticas", y fue Selman Waksman, en 1941 planteo la utilización del término "antibiótico" para referirse al grupo creciente de sustancias con propiedades antibacterianas. El primer producto antibacteriano de origen natural fue descubierto por E. de Freudenreich al estudiar la piocianasa, el pigmento liberado por la Pseudomona aeruginosa, la misma que impedía el crecimiento de otras bacterias. Rudolf Emmerich y Oscar Loew en 1889 demostraron que el pigmento no solamente inhibía el crecimiento de bacterias sino también las destruia.(1)
En 1928, Fleming estudiando las variantes cromógenas del Staphylococcus aureus, encontró que en una de las placas de agar que había descartado se había producido la lisis del germen, aparentemente en relación con el crecimiento de un hongo en la adyacencia. Fleming pudo demostrar que el hongo (Penicillium) producía una sustancia capaz de difundir a través del agar y de lisar la bacteria. Llamó a esta sustancia "penicilina".(1)
Desde su descubrimiento y al haber sido denominada la "droga milagrosa", la penicilina se utilizó sin distinción en muchos productos de venta libre, desde pastillas para la garganta, ungüentos nasales y cremas cosméticas; el descontrolado uso favoreció la resistencia creciente contra la penicilina. Es por tal motivo que la resistencia a antimicrobianos se debe a varios factores como ser: el uso indiscriminado, la dosis empleada, el tiempo de uso de un antibiótico y varios estudios muestran la influencia geográfica, dado que mientras mayor sea el número de los destinatarios, mayor será el riesgo de la utilización de concentraciones subterapéuticas. Este uso de antibióticos en concentraciones subterapeuticas, determina un desarrollo de cepas resistentes.
HISTORIA DE LA RESISTENCIA POR BETALACTAMASAS
La resistencia bacteriana fue un descubrimiento dado a conocer por Abraham y Chain en 1940, por medio de cultivos de Escherichia coli observaron la inactivación de soluciones de penicilina y las llamaron penicilinasas ; esta es una betalactamasa, una enzima producida por algunas bacterias, capaces de hidrolizar irreversiblemente el enlace amida del núcleo betalactámico de la penicilina y es responsable de la resistencia de éstas ante la acción de antibióticos betalactámicos como las penicilinas, las cefalosporinas, monobactamicos y carbapenémicos. El grado de resistencia depende de la cantidad de la enzima producida, la aparición de las primeras betalactamasas ocurrió en 1963 donde se aislaron en cepas de E. coli la TEM- 1, posteriormente la SHV-1 y la PSE-1. En 1960 se descubren las primeras penicilinas sintéticas, la meticilinas y ampicilinas, también se desarrolló la primera generación de la familia de las cefalosporinas. Estas fueron más efectivas que las penicilinas porque se infiltraban más rápido en la membrana externa de bacilos Gram negativo. Para 1978 infecciones por Gram negativos aumentan en frecuencia porque existe pérdida de genes productores de porinas como el Omp C que produce disminución en la permeabilidad de la membrana y la aparición de cefalosporinasas. A partir de esa época aparecen la cefamicina, los carbapenemes, las oxyimiocefalosporinas, monobactames, y los inhibidores de betalactamasas como el ácido clavulánico, ácido penicilánico y sulfonas. Para 1978 existía aún un grupo de bacterias resistentes tales como: Enterobacter, Serratia, Citrobacter, Morganella y Burkholderia. Estas especies eran capaces de producir carbapenemasas, por mutaciones estructurales por plásmidos.
En Alemania en 1983 fue descubierta la primera betalactamasa de espectro extendido, la SHV-2. Y siete años más tarde es reportada en Francia, donde posterior a eso comienzan a aislarse betalactamasas derivadas del TEM; la TEM-3 donde se observan nuevas mutaciones, también se encuentran cuatro variantes naturales TEM-4, TEM-8, TEM-15 y TEM-25. La TEM-12 aparece en 1987 con la sustitución de la serina en vez de la arginina en la posición 164, estas cepas eran mucho más resistentes a ceftazidima y aztreonam que las cepas productoras de TEM- 1 y TEM-2.(2,6)
Para 1991 aparecen los primeros derivados de betalactamasaTEM con alta afinidad para el ácido clavulánico, (SHV-6), este fenómeno se describe en sangre de neonatos donde se aísla Escherichia coli resistente, dos betalactamasas de espectro expandido son descritas, la OXA-11 y la OXA-14, aislada de P. aeruginosa, ambas tienen un alto nivel de resistencia a ceftazidima, pero no a aztreonam. También aparecen cepas de P. aeruginosa que producían una betalactamasa con resistencia a ambos antibióticos a la que se le llamó PER-1, éstas fueron reportadas en París y en Turquía. En Estambul también fue reportada en cepas de Salmonella sp. En 1999 se observa en la familia de Enterobacteriaceae, resistencia a múltiples antibióticos, no solo a B-lactamicos sino también a quinolonas, esto se debe a que la bacteria modifica sus proteínas de membrana, mismo mecanismo que predomina en K. pneumoniae.(2)
Las betalactamasas de espectro extendido fueron identificadas primero en K. pneumoniae y ocasionalmente en Enterobacteriaceae, este descubrimiento primero se vio en Francia, seguido de Estados Unidos y finalmente en el resto de Europa. Al principio se observaba esta mutación mediada por plásmidos en infecciones nosocomiales, se creía que los microorganismos productores de BLEE eran exclusivos de infecciones nosocomiales, de paciente que ingresaban con enfermedades debilitantes, tratamiento antimicrobiano de amplio espectro y estancia prolongada, especialmente en las unidades de cuidados intensivos y cirugía, actualmente esta infección se ha visto en paciente ambulatorios.(2,5,6)
Las betalactamasas son enzimas catalíticas que actúan hidrolizando el enlace amídico del anillo betalactámico, formadas por peptidoglucanos con estructura cuaternaria, sintetizado por bacterias y algunos hongos, capaces de defender a las bacterias o utilizadas por la bacteria para sintetizar su pared bacteriana(2). Son más de 190 enzimas de tipo ß-lactamasa, se dividen en clases de acuerdo con su peso molecular, punto isoeléctrico y sitio activo entre otros y constituyen la mayor causa de resistencia bacteriana hacia antibióticos con anillos betalactámicos.
Las ß-lactamasas de espectro extendido (BLEE) generan resistencia a la mayoría de los b-lactámicos, incluyendo a penicilinas, cefalosporinas de primera, segunda, tercera generación, monobactámicos, excepto a la cefamicina y carbapenémicos. Esta resistencia se vio incrementada por el aumento de uso de cefalosporinas. También cuentan con frecuencia con otros genes para otros antimicrobianos como ser aminoglucosidos, tetraciclinas y cotrimoxazol. Además, las cepas BLEE (+) son más frecuentemente resistentes a quinolonas que las cepas no productoras de BLEE, se desconoce la causa (2,6). Las BLEE se identificaron como TEM-12, SHV-2 y CTX-M-9. La resistencia ha sido descrita en microorganismos gramnegativos, principalmente en Klebsiella pneumoniae, Klebsiella oxytoca y Escherichia coli, pero también en los géneros Acinetobacter, Burkholderia, Citrobacter, Enterobacter, Morganella, Proteus, Pseudomonas, Salmonella, Serratia y Shigella (5). El estudio SMART, realizado en 28 paises, que reunió 6156 cultivos de infecciones intraabdominales por bacilos gramnegativos, mostró una prevalencia en el caso de microorganismos productores de BLEE de 17% para K. pneumoniae y 10% para E. coli.(2,6)
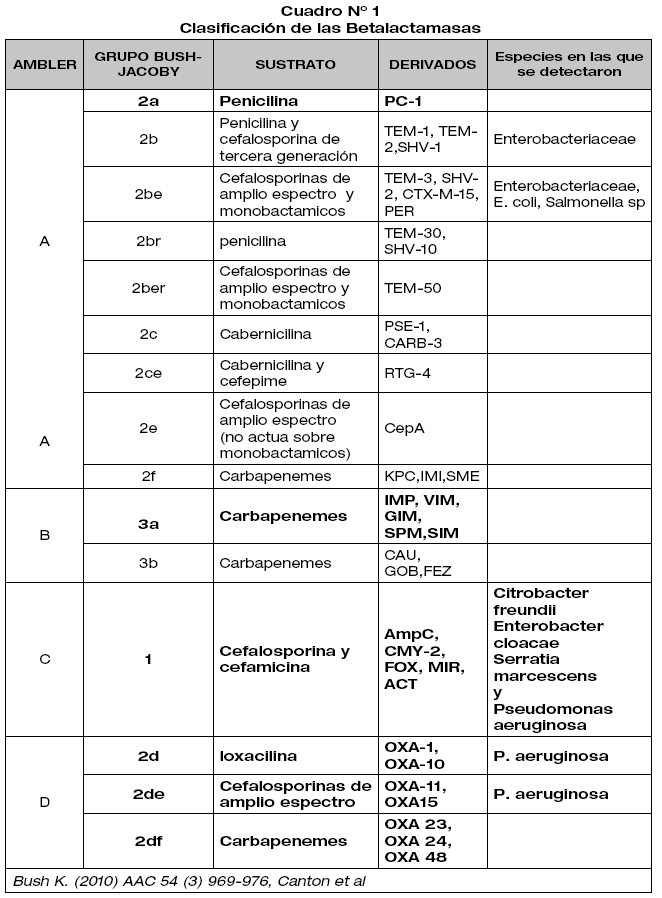
CLASIFICACIÓN DE LAS BETALACTAMASAS Y LAS CEPAS BLEE
Las betalactamasas se clasifican dependiendo de su grupo según la clasificación de Amber, en las de clase A y D principalmente y de estas en la clase A se encuentran los tipos SHV (excepto SHV-1), Enzimas tipo TEM (excepto TEM-1 y TEM-2), Enzimas tipo CTX-M, Enzimas BLEE menores tipo PER, GES, VER; y en ENZIMAS CLASE D, se tiene la tipo OXA de espectro extendido (OXA-11, OXA-13, OXA-15, OXA-18) Con el aporte de Ambier, Jaurin y Grundstrom queda propuesta una clasificación basada en el peso molecular, espectro y grado de homología en secuencias de aminoácidos, postulándose las cuatro clases:
Clase A: Enzimas serma con actividad preferentemente penicilinasas.
Clase B: Metaloenzimas con actividad preferentemente cefalosporinasas.
Clase C: Cefalosporinasas cromosómicas de bacterias Gram negativo.
Clase D: Enzimás serinas que hidrolizan oxaciclina
La clasificación de Bush - Jacoby y Medeiros se basa en los criterios anteriores y nuevos criterios como son: codificación plasmídica o cromosómica; espectro de hidrólisis; espectro de inhibición hacia clavulánico (CA), cloxacilina (CLOX), sulbactam (SUL), aztreonam (AZ), ceftazidima.(2,6)
FACTORES DE RIESGO
Los factores de riesgo para la adquisición de una infección por cepa BLEE, son múltiples. Principalmente se debe al uso empírico de antibióticos de amplio espectro que con frecuencia se emplean más en pacientes gravemente enfermos y que favorecería la selección de cepas resistentes. Ortega et al. apunta como factores predictivos para el aislamiento de E. coli con BLEE la adquisición nosocomial, el sondaje urinario y la terapia previa con betalactámico. Avilés y Betancourt, el 2016, nos muestra los factores de riesgo de presentar cepa BLEE en infecciones urinarias provenientes de la comunidad, describiéndose la enfermedad prostática, infecciones urinarias recurrentes, la edad avanzada, pacientes mayores de 60 años, diabetes mellitus, el uso de catéter vesical, y el uso previo de antimicrobianos, toma el tiempo de uso como promedio los tres meses anteriores al cultivo positivo, como betalactámicos, cefuroxima oral, aminopenicilinas, fluoroquinolonas y cefalosporinas. Existen factores asociados a su aparición, los más relevantes son el antecedente de infección urinaria causada por un microorganismo productor de BLEE, el uso de reciente de antimicrobianos, el antecedente de hospitalización reciente o vivir institucionalizado. La principal utilidad de predecir una infección por BLEE es que la cobertura antimicrobiana inapropiada durante la fase empírica en espera de los cultivos se asocia a mayor mortalidad en pacientes con infecciones graves por BLEE. El estudio de Ortega et al asocia esta mayor mortalidad, la gravedad clínica inicial (shock al diagnóstico) y el tratamiento empírico inadecuado.(3,4)
TRATAMIENTO
La resistencia actual que existe a las betalactamasas de espectro extendido aumenta las tasas de mortalidad, ya que, en pacientes con infecciones, incluso leves, se inician tratamientos empíricos, que al no tener buena respuesta en cuanto al cuadro clínico llega a evolucionar hasta sepsis. En relación con las cepas no productoras de betalactamasas de espectro extendido con microorganismos formadores de estas enzimas existe mayor mortalidad, donde el mayor factor de riesgo es el inicio tardío del antimicrobiano adecuado. Entre los principales cuadros de sepsis por estas bacterias se observan los de foco urinario, ya que las infecciones urinarias al ser tan comunes dan lugar al inicio de terapia empírica, creando a un futuro resistencia principalmente a cefalosporinas y quinolonas.
El tratamiento de elección en estos casos es el uso de carbapenémicos, recomendación que se basa principalmente en el resultado de resistencia observada in vitro. Los nuevos carbapenémicos, como ertapenem o doripenem parecen tener una excelente actividad. Existe un ensayo clínico que evaluó el tratamiento empírico de ceftriaxona en las pielonefritis agudas no complicadas, existiendo malos resultados clínicos y de laboratorio en un tercio de los pacientes. En las infecciones por Bacterias gramnegativas productoras de betalactamasas de espectro extendido las opciones terapéuticas son limitadas, por la resistencia que presentan a las cefalosporinas, penicilinas de amplio espectro y aztreonam, y como se comentaba anteriormente, la resistencia que presentan los plásmidos a otros antibióticos como ser quinolonas y el fenómeno de resistencia cruzada es muy frecuente. Los carbapenemes son los antibióticos más eficaces frente a infecciones por cepas de E. coli y K. pneumonie productoras de BLEE, con dudas respecto a la utilización de cefamicinas como la cefoxitina y las combinaciones de betalactámicos con inhibidores de betalactamasas como piperacilina-tazobactam.(6,7)
En las infecciones urinarias adquiridas en la comunidad con sospecha de cepa BLEE, se puede utilizar antibióticos de amplio espectro en espera de resultados de sensibilidad, tales como cefalosporinas de tercera generación, piperacilina-tazobactam, o carbapenemes. Cuando en los pacientes con pielonefritis aguda que progresan a sepsis grave y shock séptico que requieren tratamiento empírico en una unidad de cuidados intensivos, la administración empírica temprana de carbapenemes puede ser la mejor opción, hasta tener los resultados de susceptibilidad, principalmente en lugares con alta prevalencia de infecciones por bacterias productoras de BLEE.(9)
CONCLUSIONES
El uso indiscriminado de antibióticos de amplio espectro ha ocasionado la aparición de cepas resistentes de bacterias en infecciones diversas, incluso las adquiridas en la comunidad, por lo que es una recomendación fundamental que el tratamiento antimicrobiano sea guiado por protocolos de manejo en cada caso en particular, con dosis y tiempos adecuados de tratamiento; en caso de pacientes referidos a hospitales u hospitalizados con infecciones nosocomiales es necesario el tratamiento guiado por cultivo y antibiograma de manera adecuada y oportuna.
REFERENCIAS
1. Belloso W.H. 103 Historia de los antibióticos, Rev. Hosp. Ital. B.Aires, Vol. 29 Nº 2, diciembre 2009.
2. Abarca G., Herrera M, Betalactamasas: su importancia en la clínica y su detección en el laboratorio, Rev. méd. Hosp. Nac. Niños (Costa Rica) vol.36 n.1-2 San José Jan. 2001
3. Grandas Y, Greco C, Porras M, Trejos-Suárez J. Identificación genotípica de ß-lactamasas de espectro espectro extendido (BLEE) (blaTEM y blaSHV) en Escherichia. coli uropatógena. Rev. Fac. Cienc. Salud UDES. 2016;3(1.S1):15 [ Links ]
4. Yábar MN, Curi-Pesantes B, Torres CA, Calderón-Anyosa R, Riveros M, Ochoa TJ. Multirresistencia y factores asociados a la presencia de betalactamasas de espectro extendido en cepas de Escherichia coli provenientes de urocultivos. Rev Peru Med Exp Salud Publica. 2017;34(4):660-5. doi: 10.17843/rpmesp.2017.344.2922
5. Aviles C. Betancour P. Factores asociados a infecciones urinarias producidas por enterobacterias productoras de ß-lactamasas de espectro extendido: una cohorte prospectiva. Rev Chilena Infectol 2016; 33 (6): 628-634 [ Links ]
6. Hernández JR, et al. Escherichia coli y Klebsiella pneumoniae productores de betalactamasas de espectro extendido en hospitales españoles (Proyecto GEIH-BLEE 2000), Enferm Infecc Microbiol Clin 2003;21(2):77-82
7. E. García-Vázquez, Bacteriemias por Escherichia coli productor de betalactamasas de espectro extendido (BLEE): significación clínica y perspectivas actuales, Rev Esp Quimioter 2011;24(2):57-66 [ Links ]
8. F. Navarro, Detección fenotípica de mecanismos de resistencia en microorganismos gramnegativosEnferm Infecc Microbiol Clin. 2011;29(7):524–534
9. Kang CI, Clinical Practice Guidelines for the Antibiotic Treatment of Communit y-Acquired Urinar y Tract Infections, Infect Chemother 2018;50 (1):67-100, https://doi.org/10.3947/ic.2018.50.1.67 [ Links ]














