Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz v.20 n.2 La Paz 2014
CASO CLÍNICO
EFECTIVIDAD DE LA TERAPIA TRIPLE ANTIRRETROVIRAL EN LACTANTE MENOR CON DIAGNÓSTICO DE SIDA CATEGORIA C
Dr. Arturo Raúl Arévalo B.*, Dr. Pablo Mattos**, Dra. Janeth Gonzales**, Dra. Jeannett De La Fuente Jeria*
* Pediatra hospital Materno Infantil
** Terapista Infantil hospital Materno Infantil
RESUMEN
La falta de medicación antirretroviral durante el embarazo, la no aplicación del protocolo de prevención perinatal del VIH-1 y VIH-2 (PACTG 076) en el momento de la cesárea y la administración de inhibidores de la transcriptasa inversa al recién nacido, es la respuesta más directa a la falta de acciones de protección para los niños (as) que nacen de sus progenitoras que se encuentran viviendo con el virus de la inmunodeficiencia humana (VIH). En el caso de la nena de 4 meses de edad que nace de un vientre donde se encontraba el presente el VIH, presentan una evolución clínica, inmunológica y virológica que progresivamente la va llevando al estado de caquexia, además de presentar procesos infecciosos secundarios a oportunistas, que se complican con una sepsis determinando la necesidad de ventilación asistida. La administración de forma inmediata de los antirretrovirales (ARV) recomendados por el Programa Nacional de Lucha Contra el VIH/SIDA, sin incluso contar con resultados de carga viral materna, tampoco de la pacientita se asocia dos inhibidores nucleótidos de la transcriptasa inversa, con un inhibidor de la transcriptasa inversa no nucleósido, y los antimicóticos y antimicrobianos adecuados, la respuesta clínica, celular es satisfactoria, así ocurrió con la lactante menor que tratamos.
Es cierto que nuestra preferencia es hacer asociaciones con principios químicos de mejor acción sobre este virus, como en nuestro caso ante la evidencia de que la nevirapina nos produjo al quinto día de tratamiento una reacción de alergia (la literatura relata que los casos de esta naturaleza generalmente evolucionan a la muerte), habiéndose además asociado antihistamínicos por vía venosa, y la administración de un inhibidor de la proteasa viral que también es un químico asociado (lopinavir + Ritonavir), habiéndose obtenido una respuesta espectacular, a pesar del fondo de caquexia en que se encontraba la lactante menor de 4 meses de edad.
Todo estos acontecimientos de ver cada día más casos de mujeres embarazadas que se enteran de ser portadoras de este virus cuando sus bebes evolucionan atípicamente y/o se encuentran en situaciones clínicas gravísimas, tendrían un mejor pronóstico si se decidiera considerar al VIH/SIDA como el problema de salud número uno en nuestro país.
Palabras clave: Infección por VIH/SIDA, Déficit inmunológico grave, Inhibidor de proteasa, Inhibidor de la transcriptasa inversa, recuperación clínica.
ABSTRACT
The lack of antiretroviral medication during pregnancy, failure to apply the protocol perinatal HIV-1 and HIV-2 (PACTG 076) at the time of cesarean delivery and administration of inhibitors of reverse transcriptase newborn is the more directly to the lack of protective actions for children (as) that arise from their mothers who are living with human immunodeficiency virus (HIV) response.
In the case of the baby 4 months of age born from a womb where HIV was present, present a clinical, immunological and virological evolution is progressively moving the state of cachexia, besides presenting secondary to opportunistic infectious processes which are complicated by sepsis determining the need for assisted ventilation.
The administration immediately antiretroviral (ARV) recommended by the National Programme for the Fight Against HIV/AIDS, without even having maternal viral load results, either of two nucleotides pacientita reverse transcriptase inhibitors dela associated with an inhibitor of non-nucleoside reverse transcriptase and appropriate antifungal and antimicrobial, clinical, cellular response is satisfactory, so it happened with the lowest infant who try.
It is true that our preference is to make partnerships with chemical principles of best action on this virus, as in our case given the evidence that nevirapine we came on the fifth day of treatment an allergic reaction (literature reports that cases of this nature death usually evolve), having further associated antihistamines intravenously, and administration of a viral protease inhibitor which is also an associated chemical (lopinavir + ritonavir), a dramatic response being obtained, despite the background of cachexia that infants under 4 months of age was.
All these events to see more and more cases of pregnant women who learn to be carriers of this virus when their babies evolve atypically and / or are in very serious clinical situations, would have a better prognosis if it decides to treat HIV/AIDS as the number one health problem in our country.
Keywords: HIV infection/AIDS, inmunologic grave deficit, protease inhibitor, reverse transcriptase inhibitor, clinical recovery
INTRODUCCIÓN
Hablar de la infección por el virus de la inmunodeficiencia humana (VIH) era invariablemente una enfermedad progresiva y mortal donde el médico era un espectador de la historia natural, de la enfermedad, sus acciones en la mayoría de los casos produciendo una deficiencia celular, e humoral, con el consecuente daño clínico y principalmente las infección oportunistas y la activación de diferentes formas e cáncer, hasta antes de la introducción de los antirretrovirales (ARV) de acción mixta, quiere decir de acción en los diferentes puntos blancos que el virus de la inmunodeficiencia humana (VIH) utiliza para poder realizar su acción de contacto, su penetración, invasión y su posterior replicación dentro de la célula que resulta ser su hospedera , que
hoy en día nos muestra sus potentes beneficios en lograr la recuperación de incluso lactantes que viven con el VIH y desarrollan procesos patológicos oportunistas que los llevan a la caquexia, y su descompensación metabólica general, debiendo ser atendidos de forma urgente en la unidad de terapia infantil. Esta experiencia que hemos tenido de forma multidisciplinaria entre los intensivistas de UTIP y nosotros nos permitió mediante el uso asociado de dos antirretrovirales nucleósidos y uno no nucleósido, terapia nutricional específica y apoyo multivitamínico la recuperación clínica, celular y nutricional en 12 días a partir del inicio de esta terapia combinada, si bien al 6to día de evolución la paciente presenta una reacción de hipersensibilidad al a ARV inhibidor de la transcriptasa inversa no nucleósido, que fue retirado de forma inmediata en su protocolo de tratamiento e incorporamos un inhibidor de la integrasa asociado a su prolongador de acción antiretroviral. La respuesta fue espectacular y la lactante menor de 5 meses de edad fue dada de alta en condiciones de recuperación nutricional.
Esta experiencia tiene el objetivo de participar que la asociación de 2 ITIN y un inhibidor de la integrasa permite la recuperación de pacientes clasificados en la categoría C de SIDA y la disponibilidad que brinda el Programa Nacional y Regional de SIDA de medicamentos; la posibilidad de tener niveles de carga viral que pueden ser monitorizados, y la aplicación de la Fórmula de Recuento Total de Linfocitos en menores de 5 años, permite a los médicos adoptar con la mayor rapidez una terapia eficiente. Esta comunicación hace posible tratar eficazmente la infección por el VIH y mejorar la salud y la supervivencia de pacientes que hasta hace pocos años estaba condenada a morir tempranamente.
PRESENTACIÓN DEL CASO CLÍNICO
Se trata de una lactante menor de 4 meses de edad que fue transferida del municipio del Alto, del centro de salud Los Andes, con los diagnósticos de Neumonía muy grave, Desnutrición moderada a severa y tuberculosis en estudio, le realizan terapia combinada con antimicrobianos y antimicóticos por vía parenteral y ante una evolución de dos semanas sin respuesta clínica trasfieren a un hospital de mayor complejidad.
Los datos clínicos aportados por la madre, una adolescente de 18 años, en estado de calle, refiere que estuvo dos semanas con accesos de tos seca paroxística que le producen vómitos alimenticios y rechazo completo al seno materno, además de alzas térmicas no cuantificadas persistentes, deposiciones líquidas frecuentes y abundantes. Entre los resultados de sus exámenes que cuenta se tienen un hemograma con un hematocrito de 40%, hemoglobina 13 g/dL, la fórmula blanca presenta segmentados 48 %, Linfocitos 52 %. Una proteína C reactiva +++, examen general de orina normal y una citología fecal sin eritrocitos. Además de una placa de RX con infiltrado bilateral, horizontalización de arcos costales.
Después de cinco días en dicho centro de salud es trasferida al servicio de Urgencias del hospital Materno Infantil de la Caja Nacional de Salud, y por las condiciones clínicas de la paciente se interna en UTIP con los diagnósticos de PVVS, choque hipovolémico, neumonía atípica versus tuberculosis miliar, desnutrición grave, síndrome de dificultad respiratoria grave, dermatitis del pañal severa. La terapia que se realiza de forma inmediata es pasarla a ventilación mecánica asistida (se le administra fentanilo, midazolan, dopamina), (Ver fig. N° 1). Se plantea a su madre del pronóstico vital reservado.
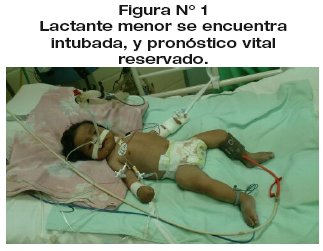
Los terapistas infantiles solicitan la valoración por la especialidad a 24 horas de su internación, acudimos a la interconsulta y después de valorar los antecedentes de madre con Prueba Rápida de VIH reactiva y con diagnóstico de sífilis, con el padre de 24 años de edad con ocupación albañil, con diagnóstico de sífilis, fallecido en accidente automovilístico, y la paciente previamente tratada con antimicrobianos del tipo de las cefalosporinas de tercera generación y antimicóticos del tipo de los imidazoles, con un deterioro del estado nutricional, y procesos infeccioso múltiple (pulmonar y séptico generalizada), catalogamos a la paciente de acuerdo al examen clínico realizado donde se evidencia la presencia de emaciación generalizada con tejido celular sub cutáneo desaparecido, arcos costales prominentes, facies con huesos cigomáticos visibles, palidez universal intensa, presencia de ganglios cervicales, axilares e inguinales múltiples de diámetro variable (mayores a 2 cm), relleno capilar mayor a 5 segundos, se encuentra intubada y sin automatismo respiratorio, mucosa oral con placas blanquecinas abundantes. La auscultación pulmonar revela presencia de estertores crepitantes diseminados, frecuencia cardiaca aumentada, presión arterial en el percentilo 50, hepatoesplemenomegalia, lesiones eritematosas y descamativas en región perianal, neurológico sin respuesta (se encuentra en coma inducido).
Posterior a la extubación la paciente (ver Figura N°2) presenta una crisis convulsiva por lo que se realiza de emergencia una TAC con HSA Fisher III, edema cerebral, hematoma intraparenquimatoso occipital derecho con dos densidades lo que traduce sangrado antiguo. Clínicamente la paciente se encuentra con pupilas isocóricas, midriasis, reflejo fotomotor lento. Nutricionalmente tiene una pérdida de 43% en menos de 30 días para su peso ideal
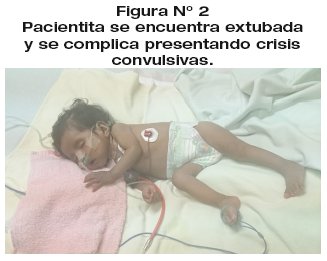
Exámenes complementarios:
Carga Viral (que es reportada posteriormente con 6'309.573 copias de RNA para el VIH-1, recuento de linfocitos CD4+/CD8+, no se procesan por defectos en el aparato. Recuento Total de Linfocitos: 1.789, se interpreta como supresión moderada inmunológica (ver cuadro N° 1) para comparar resultados.

Gasometría arterial con acidosis metabólica descompensada: Hemograma de control con hemoglobina de 11.9 g/dL, leucopenia de 4000 cayados 3%, segmentados 47%, eosinófilos 4%, linfocitos 43 %, monocitos 3 %. Plaquetas en 93.000. Glucemia de 86 mg/dL. Función renal normal, función hepática anormal leve.
TRATAMIENTO
Triasociado antirretroviral: zidovudina (ZDV) 360 mg/SupCm2). 12-12, lamivudina (3TC) 4 mg/kg 12-12, nevirapina (NVP) 150 mg/SupCm2 (dosis de ataque por7 días), al 5to día presenta Rash morbiliforme en miembros superiores, tórax y miembros inferiores por lo que se descontinúa la NVP y se inicia lopinavir/ritonavir 230 mg/SupCm2 12-12, estos ARVs se administran por sonda nasogástrica, también se trata con fluconazol, vancomicina, amikacina, INH y sulfametoxaxol/trimetroprim como profilaxis.
Su aporte nutricional (Requerimiento de calorías y proteínas por grupos etarios en condiciones de ser un niño que vive con el VIH, Guía de Cuidado y Apoyo Nutricional para Personas Viviendo con VIH/Sida) es en base a sus requerimientos energéticos basales a los que se adiciona un 150 % sobre su basal, proteínas y triglicéridos son calculados de acuerdo a la tabla de la OMS para estados caquécticos secundarios al VIH, además se le administra megadosis de multivitaminas por sonda naso gástrica SNG, con buena aceptación. Se realiza impregnación con fenitoina iv, por las crisis convulsivas y posteriormente fenobarbital vo, que es controlado por neurología infantil del hospital Materno Infantil.
La paciente es dada de alta a los 34 días (ver fig. 3) de internación con una recuperación celular y nutricional evidente, recibe su dieta por vía oral y es atendida por la madre, quien se encuentra bajo atención del CDVIR-LP. Se acuerda con la madre que debe asistir al hospital materno Infantil para su control y seguimiento de la paciente, y debe continuar con su apoyo psicológico, además de ser atendida en su centro de salud público que le corresponda.

DISCUSIÓN
Las acciones que el médico debe seguir para lograr repetir experiencias como la informada, y lograr ser actores principales en la disminución la trasmisión perinatal del VIH, no son complejas, sino más bien son fáciles de llevar a cabo y consisten principalmente en la identificación los más temprano posible para saber el estado de la madre en relación a ser portadora del VIH, y lograr que ella se empodere de la necesidad de cuidar a su futuro hijo/a mediante la conveniencia de la realización de la prueba de ELISA (de preferencia la de 4ta generación) en el embarazo; Evaluación del grado de inmunodeficiencia existente, mediante: a) Carga viral inicial; entre 2 y 6 semanas después de iniciar o cambiar TAR, bimensualmente hasta alcanzar cargas indetectables y a la semanas 34-36 planificar la cesárea y b) realizar un CD4+/CD8+ trimestral; Durante el embarazo administrar terapia antirretroviral igual a la mujer no embarazada, basados en los criterios inmunológicos y clínicos; debiendo en lo posible evitar medicamentos con potencial de teratogenicidad, (Efavirenz); La gestante que es una PVVS debe ser tratada con TAR independiente de su carga viral (con uno o más antirretrovirales que atraviesen la barrera placentaria adecuadamente), iniciando idealmente antes de la semana 28 de gestación, porque hay evidencias de ser más efectiva que aquella que se administra desde la semana 36.
En situaciones especiales como la ausencia de control prenatal adecuado o ante una Prueba rápida (+) debe iniciarse TAR lo más pronto posible y efectuar la prueba confirmatoria (Westwern Blot) posteriormente; Los regímenes son triasociados y en combinaciones específicas que mejoran la efectividad de la reducción de la transmisión perinatal.
Desde hace 32 años atrás la mejor vacuna es la información y esta debe consistir en un instrumento de educación a favor de disminuir los factores de riesgo materno como suspender cigarrillo y uso de drogas ilícitas, tratamiento de infecciones del tracto genital, uso de condones femeninos y/o masculinos mientras esté embarazada.
REFERENCIAS
1. Piatak M, Saag MS, Yang LC, Clark SJ, Kappes JC, Luk KC, et al. High levels of HIV-1 in plasma during all stages of infection determined by competitive PCR. Science. 1993;259:1749-54. [ Links ]
2. Pachl C, Todd JA, Kern DG, Sheridan PJ, Fong SJ, Stempien M, et al. Rapid and precise quantification of HIV-1 RNA in plasma using a branched DNA signal amplification assay. J Acquir Immune Defic Syndr Hum Retrovirol. 1995;8:446-54. [ Links ]
3. Kievits T, van Gemen B, van Strijp D, Schukkink R, Dircks M, Adriaanse H, et al. NASBA isothermal enzymatic in vitro nucleic acid amplification optimized for the diagnosis of HIV-1 infection. J Virol Methods. 1991;35:273-86. [ Links ]
4. Saag MS. Use of HIV viral load in clinical practice: back to the future [Editorial]. Ann Intern Med. 1997;126:983-5. [ Links ]
5. Wei X, Ghosh SK, Taylor ME, Johnson VA, Emini EA, Deutsch P, et al. Viral dynamics in human immunodeficiency virus type 1 infection. Nature. 1995;373:117-22. [ Links ]
6. Guidelines for the use of antiretroviral agents in HIV-infected adults and adolescents (January 28, 2000). Retrieved September 2000, from: http://www.hivatis.org/guidelines/adult/text/index/htr. [ Links ]
7. Carpenter CC, Cooper DA, Fischl MA, Gatell JM, Gazzard BG, Hammer SM, et al. Antiretroviral therapy in adults: updated recommendations of the International AIDS Society-USA Panel. JAMA. 2000;283:381-90. [ Links ]
8. Rich JD, Dickinson BP, Spaulding A, Lafazia L, Flanigan TP. Interpretation of indeterminate HIV serology results in an incarcerated population. J Acquir Immune Defic Syndr Hum Retrovirol. 1998;17:376-9. [ Links ]
9. Mylonakis E, Paliou M, Greenough TC, Flanigan TP, Letvin NL, Rich JD. Report of a false-positive HIV test result and the potential use of additional tests in establishing HIV serostatus. Arch Intern Med. 2000;160:2386-8. [ Links ]
10. Mellors JW, Munoz A, Giorgi JV, Margolick JB, Tassoni CJ, Gupta P, et al. Plasma viral load and CD4+ lymphocytes as prognostic markers of HIV-1 infection. Ann Intern Med. 1997;126:946-54. [ Links ]
11. Mellors JW, Rinaldo CR, Gupta P, White RM, Todd JA, Kingsley LA. Prognosis in HIV-1 infection predicted by the quantity of virus in plasma. Science. 1996;272:1167-70 [Published erratum appears in Science 1997;275:14].
12. Sande MA, Volberding P. The medical management of AIDS. 4th ed. Philadelphia: Saunders, 1995:40.
13. Kojima E, Shirasaka T, Anderson B, Chokekijchai S, Sei S, Yarchoan R, et al. Monitoring the activity of antiviral therapy for HIV infection using a polymerase chain reaction method coupled with reverse transcription. AIDS. 1993;7(suppl 2):S101-5. [ Links ]
14. Lin HJ, Myers LE, Yen-Lieberman B, Hollinger FB, Henrard D, Hooper CJ, et al. Multicenter evaluation of quantification methods for plasma human immunodeficiency virus type 1 RNA. J Infect Dis. 1994;170:553-62. [ Links ]
15. Cavert W. In vivo detection and quantitation of HIV in blood and tissues. AIDS. 1998;12(suppl A):S27-34. [ Links ]
16. Lin HJ, Pedneault L, Hollinger FB. Intra-assay performance characteristics of five assays for quantification of human immunodeficiency virus type 1 RNA in plasma. J Clin Microbiol. 1998;36:835-9. [ Links ]
17. Rompalo AM, Astemborksi J, Schoenbaum E, Schuman P, Carpenter C, Holmberg SD, et al. Comparison of clinical manifestations of HIV infection among women by risk group, CD4+ cell count, and HIV-1 plasma viral load. HER Study Group. HIV Epidemiology Research. J Acquir Immune Defic Syndr Hum Retrovirol. 1999;20:448-54. [ Links ]
18. Hughes MD, Johnson VA, Hirsch MS, Bremer JW, Elbeik T, Erice A, et al. Monitoring plasma HIV-1 RNA levels in addition to CD4+ lymphocyte count improves assessment of antiretroviral therapeutic response. ACTG 241 Protocol Virology Substudy Team. Ann Intern Med. 1997 ;126:929-38. [ Links ]
19. O'Brien WA, Hartigan PM, Daar ES, Simberkoff MS, Hamilton JD. Changes in plasma HIV RNA levels and CD4+ lymphocyte counts predict both response to antiretroviral therapy and therapeutic failure. VA Cooperative Study Group on AIDS. Ann Intern Med. 1997;126:939-45. [ Links ]
20. Volberding PA. HIV quantification: clinical applications. Lancet. 1996;347:71-3. [ Links ]
21. Sterling TR, Lyles CM, Vlahov D, Astemborski J, Margolick JB, Quinn TC. Sex differences in longitudinal human immunodeficiency virus type 1 RNA levels among seroconverters. J Infect Dis. 1999;180:666-72. [ Links ]
22. Brambilla D, Reichelderfer PS, Bremer JW, Shapiro DE, Hershow RC, Katzenstein DA, et al. The contribution of assay variation and biological variation to the total variability of plasma HIV-1 RNA measurements. The Women Infant Transmission Study Clinics. Virology Quality Assurance Program. AIDS. 1999;13:2269-79. [ Links ]














