Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz v.19 n.1 La Paz 2013
CASOS CLINICOS
MIASTENIA GRAVIS DEL ADULTO
MYASTHENIA GRAVIS DEL ADULTERY
* Dra. Mónica Molina Monasterios, **Dra. Edna C. Serrano Arancibia.
RECIBIDO: 15/03/2013
ACEPTADO: 03/04/2013
RESUMEN
La miastenia gravis (MG) es una enfermedad neuromuscularautoinmuney crónica caracterizada por grados variables de debilidad de los músculos esqueléticos del cuerpo. La denominación proviene del latín y el griego, y significa literalmente «debilidad muscular grave». Debuta con un cuadro insidioso caracterizado por ptosis palpebral bilateral y disminución de fuerza muscular, que rápidamente se recuperan con el descanso pero que reaparece al reiniciar el ejercicio. Suele iniciarse en los músculos peri oculares. En pocas ocasiones el inicio es agudo.
Palabras clave: Miastenia grave, SUMMARY
Myasthenia gravis (MG) is a chronic autoimmune neuromuscular disease characterized by varying degrees of weakness of the skeletal muscles of the body. The name comes from Latin and Greek, and literally means "grave muscle weakness. " Insidious debut with a picture characterize by bilateral ptosis and decreased muscle strength, which quickly recover with rest but comes back when you restart the exercise. It usually begins in the periocular muscles. Rarely, onset is acute.
Key words: Myasthenia gravis.
Caso clínico 1: Hombre de 38 años de edad sin historia médica previa. Ingresó por instauración gradual de hace 3 meses con debilidad generalizada, adinamia, ptosis palpebral bilateral a predominio derecho. La exploración neurológica destaca discreta ptosis palpebral y diplopía clara en los 4 puntos cardinales.
Los exámenes generales de laboratorio destacaron fosfatasa alcalina elevada, hipertrigliceridemia, calcio 8,4, troponinas (-), CPK (-). Además Anticuerpos antireceptor de Acetil colinestersa positivo, prueba de neostigmina positiva a los 30 min (respuesta favorable de diplopía) prueba de estimulación repetitiva a baja frecuencia positiva con decremento hasta 35% (figura 1).
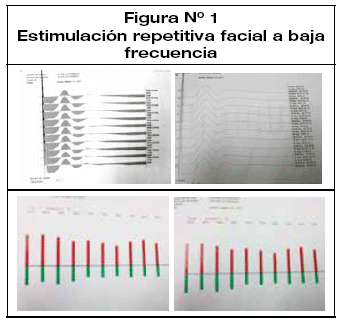

Tomografia de torax: normal (figura 2).
Radiografía de torax: normal (figura 3).
Hormonas tiroideas: normales.
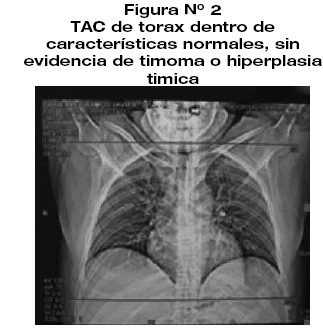
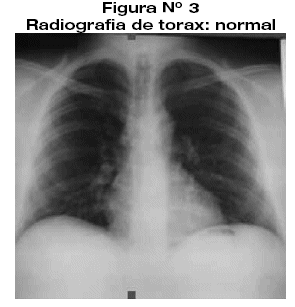
Caso clínico 2: Mujer de 29 años de edad, hipertensa sin tratamiento. Ingresó por cuadro de 1 año de evolución durante su gestación, pero no realizo seguimiento o tratamiento por temor a complicaciones en el embarazo, al encontrarse en el 4to mes de puerperio acude con la persistencia de ptosis palpebral y debilidad de miembros torácicos además de periodos de diplopía. La exploración neurológica destaca ptosis palpebral moderada y fuerza muscular de 4/5 en miembros torácicos diplopía discreta en los 4 puntos cardinales.
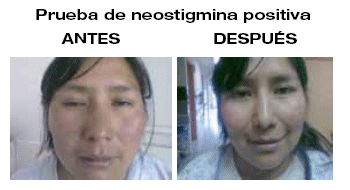
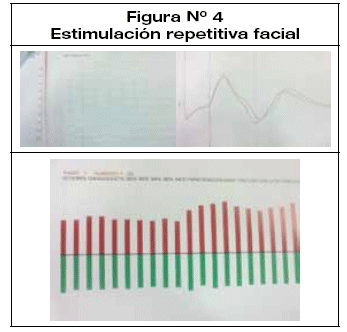
Los exámenes generales de laboratorio destacaron fosfatasa alcalina normal, calcio 8,2 troponinas (-) CPK (-). Además Anticuerpos antireceptor de Acetil colinestersa positivo, prueba de neostigmina positiva a los 10 min (respuesta favorable de ptosis, fuerza muscular proximal) (figura 4), prueba de estimulación repetitiva a baja frecuencia positiva con decremento hasta 26% (figura 4-5).
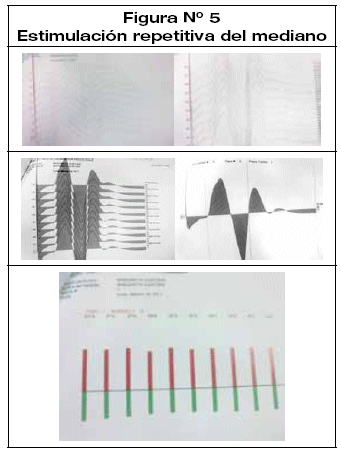
Caso clínico 3: Hombre de 86 años de edad, con habito tabáquico importante, diabético, diagnosticado con bronquitis hace 2 semanas previa su internación realizando tratamiento con Penicilina, aminoglucosidos, además diagnosticado de hernia de hiato en tratamiento con omeprazol, antiácidos a base de magnesio, con automedicación: benzodiacepinas, paracetamol,magnatil, metoclorpramida, ibuprofeno, diclofenaco. Ingresó por cuadro de 1 mes de evolución en forma súbita con debilidad muscular generalizada a predominio de miembros proximales además de ptosis palpebral bilateral, disartria, disfagia exacerbándose por las tardes. La exploración neurológica destaca disartria, agudeza visual disminuida, ptosis palpebral bilateral, disfagia, fuerza muscular de 4/5 en las 4 extremidades.
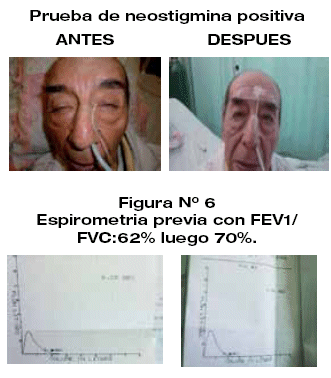
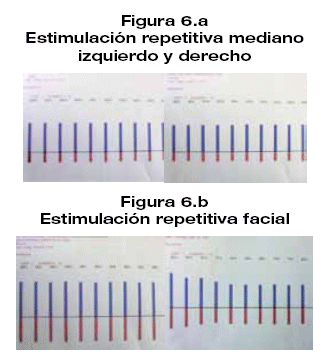
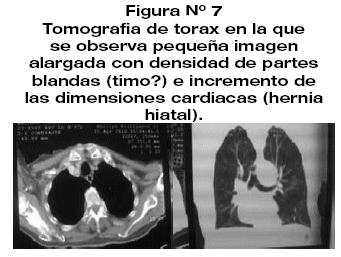
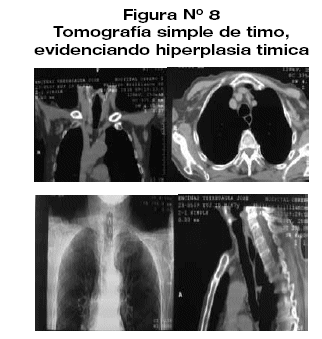
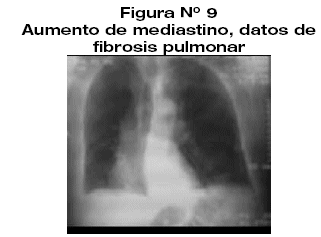
Los exámenes generales de laboratorio destacaron fosfatasa alcalina normal, calcio 7.8 troponinas (-) CPK (-). Gasometría arterial con PO2 35 y sat. O2 65,2%Además Anticuerpos antireceptor de Acetil colinestersa positivo, prueba de neostigmina positiva a los 5 min (respuesta favorable de ptosis, fuerza muscular proximal), espirometria con patrón mixto (figura 6). prueba de estimulación repetitiva a baja frecuencia positiva con decremento hasta 27% (figura 6.a y 6.b). Cuenta con TAC de torax, timo y radiografía de torax (figura 7-8-9).
DISCUSIÓN
Es una entidad rara, que tiene dos picos de incidencia: el primero, entre la segunda y tercera década de la vida y compromete principalmente a las mujeres; y el segundo, entre la sexta y séptima décadas con predominio de los hombres, con una prevalencia de 0,5 a 5 por 100.000 habitantes y una incidencia de 50 a 125 casos por millón, aproximadamente en Estados Unidos 25.000 personas padecen la enfermedad. El 75% de los pacientes cursan con alteraciones tímicas, que bien pueden ser hiperplasias tímicas (85%) y timoma (10-15 %). Con respecto a los anticuerpos contra el receptor de acetilcolina, están elevados en el 85% de los pacientes con la enfermedad. En el grupo restante se encuentran normales (Drachman 1994). La entidad se asocia a otras enfermedades autoinmunes, como el Lupus eritematoso sistémico, la artritis reumatoidea, la anemia perniciosa, la tiroiditis de Hashimoto, la enfermedad de Graves-Basedow y el vitiligo, entre otras (cuadro 1).
En relación a la patogenia, es una enfermedad autoinmune; es decir, se desencadena por una respuesta inmune anómala contra un antígeno exógeno al huésped, generando anticuerpos que agreden un antígeno endógeno que se expresa en diferentes órganos; en el caso particular el receptor de acetilcolina que se localiza en la región pos sináptica de las fibras musculares estríadas. En la Miastenia aún se desconoce cuál es el estímulo antigénico, pero se sabe según los modelos experimentales que tomando el suero de pacientes con la enfermedad, e inoculándolo en animales de laboratorio se produce la patología. Tal vez lo más que se ha llegado a conocer es que en el timo hay unas células mioepiteliales que poseen receptores de acetilcolina en la superficie y el contacto inmunológico con linfocitos T alterados genera a través de plasmocitos la producción de los anticuerpos contra el receptor de acetilcolina, aunque el disparador de ésta respuesta tampoco se conoce.
Hay tres mecanismos mediante los cuales ocurre la entidad:
1. Por una degradación acelerada de los receptores de acetilcolina.
2. Por un bloqueo de los receptores mediado por anticuerpos.
3. Por un daño secundario de la unión neuromuscular (Drachman 1994).
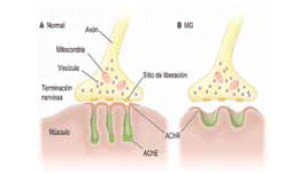
El receptor de acetilcolina consta de cinco subunidades; entre esas dos subunidades alpha a las cuales se une la acetilcolina, abriendo el canal, que es voltaje dependiente y permite el paso de cationes como el Na+ y el K+ despolarizando la membrana pos sináptica y generando potenciales de acción en miniatura que al ser sumados generan un potencial de acción capaz de ser difundido hacia otras fibras musculares, y mediante segundos mensajeros permitir la entrada de calcio a la célula, generando la contracción de miofibrillas, que a su vez se traduce en la contracción muscular. Como es bien sabido al ser dañada por anticuerpos la unión neuromuscular disminuye el número de receptores de acetilcolina y hay una disminución en el número de folias pos sinápticas, lo que altera de alguna forma la contracción muscular produciendo debilidad y fatigabilidad en los pacientes.
Con respecto a la clínica para efecto de manejo y estadificación en grados de funcionabilidad, se estableció una clasificación para la Miastenia Grave.
Clasificación de Osserman (1958) Grado Ia Miastenia Ocular
Grado Ib Miastenia generalizada forma leve
Grado II Miastenia generalizada forma moderada
Grado III Miastenia generalizada forma severa
Grado IV Crisis Miasténica
Los pacientes inicialmente pueden tener diplopía y ptosis palpebral en el caso de la miastenia ocular, también signos de compromiso bulbar, con alteraciones de la voz como disfonía, disfagia y en los casos severos, grados III y IV de la clasificación, compromiso de los músculos respiratorios. (Cuadro N° 2)
Los pacientes generalizada presentan fatiga y debilidad que empeora con la contracción muscular repetitiva y que el paciente lo nota al realizar actividades y que el cuadro empeora a medida que progresa el día, con mayor fatiga en las tardes. La debilidad generalizada se presenta en el 85% de los pacientes con miastenia generalizada (Toro 1994).
El diagnostico definitivo tiene 3 componentes: clínica, electrofisiología e inmunología:
1. Prueba de Tensilón (Toro J 1994)
2. Test de estimulación repetitiva
3. Test de Fibra única
4. Anticuerpos contra el receptor de acetilcolina por RIA.
De acuerdo con la clínica del paciente la severidad de los síntomas, incluyendo los músculos comprometidos por la enfermedad, se dan medicamentos que tratan los síntomas y no cambian el curso de la enfermedad; otros que frenan la respuesta inmunológica y finalmente la timectomía, que cambia el curso de la enfermedad. Se mencionan brevemente algunos de ellos:
1. Para la miastenia ocular el tratamiento de elección lo constituyen los esteroides por vía oral, con un esquema que puede iniciarse con dosis bajas de prednisona.
2. En los casos generalizados la terapia de elección, que es sintomática, la constituyen los inhibidores de la acetilcolinesterasa, (enzima que en la hendidura sináptica degrada rápidamente la acetilcolina presente luego de la contracción muscular). El efecto benéfico de estos productos es incrementar un poco más la vida media de la acetilcolina. El principal medicamento es el Mestinón, su compuesto activo es el bromuro de piridostigmina, disponible en tabletas de 60 mg; tiene un efecto de inicio de acción de 30 minutos, con una duración hasta 6 horas. (Godman y Gilman 1988).
El otro inhibidor de la acetilcolinesterasa es la Neostigmina se encuentra en el mercado en ampollas de 0,5 mg y se usa en casos en los que el paciente tiene contraindicada la vía oral, o en el postoperatorio luego de la timectomía.
Cuando las medicaciones sintomáticas fallan se usan los inmunosupresores que incluyen los esteroides, la azathioprina, la ciclosporina. Los corticoides se usan con cautela en los pacientes con las formas generalizadas, ya que su uso puede desencadenar una crisis miasténica (30% de los pacientes).
Otras terapias que se usan son: la plasmaféresis, que disminuye con los recambios el número de anticuerpos; es un procedimiento invasivo que requiere de un acceso venoso central y requiere que el paciente esté estable hemodinámicamente: su uso principal es para los pacientes que están en crisis miasténica; los pacientes que previamente a la cirugía de timo presentan una capacidad vital menor de 2 lt; los pacientes que tienen cuadros de miastenia generalizada moderada a severa que van a recibir esteroides. Los recambios se hacen en el transcurso de una semana con un volumen total de recambio de 250 cc/kg.
Finalmente la gammaglobulina hiperinmune humana que funciona como un inmunomodulador de la respuesta inmune se usa a una dósis de 0,4 gm/ kg/d, durante 5 días, tiene las mismas indicaciones de la plasmaféresis. Tiene la ventaja de la facilidad en la administración, como limitante el costo, al igual que la plasmaféresis y como efectos secundarios principalmente la cefalea, meningitis aséptica y disfunción renal por necrosis tubular. La cirugía está indicada en los pacientes con timoma y en los que tienen miastenia generalizada con estudios de imágenes positivos para timo. Son mejores los resultados en pacientes menores de 45 años. La timectomía trans external mejora el pronóstico: 35% de los pacientes mejoran y no requieren medicación; en 50% la dosis de medicación que necesita es menor y 15% no responden.
La inmunoglobulina no presenta interacciones medicamentosas conningún fármaco.
CONCLUSIONES
En este artículo se demostró que la miastenia grave es variable ya que se cuentan con 3 diferentes casos, los mismos con diferente clínica pero con relación neurofisiología e inmunológica, destacando factores de que condicionaron la presentación (embarazo) y exacerbación por automedicación.
Actualmente se encuentran completando tratamiento con Mestinon con respuesta favorable y buena tolerancia. Es importante realizar seguimiento de estos paciente ya que como sabemos existe la tendencia a la recidiva y prevenir posibles complicaciones que se podrían deber a inmunodepresión, sin embargo, cuando enfrentamos una patología como esta siempre se debe buscar la posible etiología agotando todas las pruebas clínicas y laboratoriales, para poder enfrentarlas con un tratamiento precoz y efectivo que como en estos casos dejen las menores secuelas posibles.
NOTAS
* Medico Neuróloga - Neurofisiología. Hospital materno Infantil. Caja Nacional de Salud ** Médico Residente IV Neurología. Hospital Materno Infantil. Caja Nacional de Salud. Responsable: Dra. Mónica Molina Monasterios. E-mail: monicmolina@hotmail.com
REFERENCIAS
1. Howard JF. Myasthenia Gravis. A manual forthe health careprovider. Myasthenia Gravis Foundation of America. St. Paul, Minnesota, USA. 1° Ed. 2005. [ Links ]
2. Meriggioli MN. The diagnosis of Myasthenia Gravis. Syllabi of the AAN. 2009. [ Links ]
3. Wolfe GI. Treatment of Myasthenia Gravis. Syllabi of the AAN. 2009. [ Links ]
4. Benatar M, Kaminski H. Tratamiento médico y quirúrgico para la miastenia ocular (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2008 Número 4. xford: Update Software Ltd. Disponible en: http://www.update-software.com. (Traducida de The Cochrane Library, 2008 Issue 3. Chichester, UK: John Wiley & Sons, Ltd.). [ Links ]
5. Bershad EM, Feen ES, Suarez JI. Myasthenia gravis crisis. South Med J. 2008; 101(1): 63-9. [ Links ]
6. Bichuetti DB, Barros TM, Oliveira EM, Annes M, Gabbai AA. Demyelinating disease in patients with myasthenia gravis. Arq Neuropsiquiatr. 2008; 66(1): 5-7. [ Links ]
7. Conti-Fine BM, Milani M, Wang W. CD4+ T cells and cytokines in the pathogenesis of acquired myasthenia gravis. Ann N YAcadSci. 2008; 1132:193-209. [ Links ]
8. Gajdos P, Chevret S, Toyka K. Inmunoglobulina intravenosa para la miastenia gravis (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2008 Número 4 Oxford: Update Software Ltd. Disponible en: http://www.updatesoftware. com. (Traducida de The Cochrane Library, 2008 Issue 3. Chichester, UK: John Wiley & Sons, Ltd.). [ Links ]
9. Grob D, Brunner N, Namba T, Pagala M. Lifetime course of myasthenia gravis. Muscle Nerve. 2008; 37(2): 141-9. [ Links ]
10. Hart IK, Sathasivam S, Sharshar T Agentes inmunosupresores para la miastenia gravis (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2008 Número 4. Oxford: Update Software Ltd. Disponible en: http://www.updatesoftware. com. (Traducida de The Cochrane Library, 2008 Issue 3. Chichester, UK: John Wiley & Sons, Ltd.). [ Links ]
11. Juel VC, Massey JM. Myasthenia gravis. Orphanet J Rare Dis. 2007; 2: 44. [ Links ]
12. Luchanok U, Kaminski HJ. Ocular myasthenia: diagnostic and treatment recommendations and the evidence base. Curr Opin Neurol. 2008; 21(1):8-15. [ Links ]
13. Mahadeva B, Phillips LH 2nd, Juel VC. Autoimmune disorders of neuromuscular transmission. Semin Neurol. 2008; 28(2): 212-27. [ Links ]
14. Pul R, Stangel M. Using immunoglobulins in muscular disease treatment. Expert Opin Biol Ther. 2008; 8(8): 1143-50. [ Links ]
15. Raica M, Cimpean AM, Ribatti D. Myasthenia gravis and the thymus gland. A historical review. Clin Exp Med. 2008; 8(2): 61-4. [ Links ]
16. Schneider-Gold C, Gajdos P, Toyka KV, Hohlfeld RR. Corticosteroides para la miastenia grave (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2008 Número 4. Oxford: Update Software Ltd. Disponible en: http://www.updatesoftware. com. (Traducida de The Cochrane Library, 2008 Issue 3. Chichester, UK: John Wiley & Sons, Ltd.). [ Links ]
17. Sathasivam S. Steroids and immunosuppressant drugs in myasthenia gravis. Nat Clin Pract Neurol. 2008; 4(6): 317-27. [ Links ]
18. Zinman L et al. IVimmunoglobulin in patients with myasthenia gravis: a randomized controlled trial. Neurology. 2007; 68(11): 837-41. [ Links ]