Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz v.17 n.1 La Paz 2011
EDUCACIÓN MÉDICA CONTÍNUA
REVISIONES SISTEMÁTICAS (2)
Dr. Raúl Arturo Arévalo Barea*, Dr. Gonzalo Ortuño**, Univ. Dory Esther Arévalo Salazar***
* Diplomado Medicina Basada Evidencias, Revisiones Sistemáticas, Metodología de la Investigación, Elaboración de Guías Clínicas. Centro Latinoamericano de Perinatología. Uruguay-OPS.
** Coordinador Carrera de Fisioterapia - Universidad Central
*** Estudiante Carrera de Medicina - Universidad Mayor de San Andrés
Las revisiones sistemáticas (RS) logran establecer cuándo los efectos de la atención clínica son consistentes y cuándo pueden aplicarse los resultados de las investigaciones a los diferentes grupos de población.
Las RS se estructuran en base a métodos explícitos y sistemáticos donde se limitan los sesgos (errores sistemáticos), y reducen los resultados encontrados por azar, haciendo así que el resultado sea más consistente sobre los cuales se pueden sacar conclusiones y tomar decisiones (Atman 1992). Los metanálisis al usar métodos estadísticos para resumir los resultados de estudios independientes entre sí pueden proporcionar estimaciones más precisas sobre los efectos de la atención clínica en comparación de aquellos resultados derivados de las investigaciones individuales incluidas en una RS.
Otra característica importante es que las RS se basan en revisiones de las investigaciones clínicas controladas con distribución aleatorias (Randomised Controlled Trials) porque tienen mayores posibilidades de dar informaciones más fiables.
Cuando se inicia la elaboración de una RS se debe empezar por la preparación de un Protocolo que debe estar organizado en secciones que sigan los pasos que se requieren para la preparación y actualización de las RS:
Formulación del problema.
Localización y selección de los estudios.
Evaluación de la calidad de los estudios.
Obtención de los datos.
Análisis y presentación de los resultados.
Interpretación de los resultados.
Mejora y actualización de las revisiones.
FORMATO DE UNA REVISIÓN SISTEMÁTICA (BASADA EN LA REVISIÓN DE COCHRANE)
Las condiciones básicas para la elaboración de las revisiones sistemáticas que han sido desarrollas por los Grupos de Revisores Cochrane, Grupo Asesor del Programa Review Manager (RevMan), han generado un software que es usado para la preparación de las RS de Cochrane. Este software RevMan brinda la ayuda necesaria a los revisores para que puedan elaborar las revisiones mediante el formato adecuado y a preparar los archivos necesarios para trasladar las revisiones por medios electrónicos a la Base de Datos Cochrane de Revisiones Sistemáticas.
El formato de las revisiones sistemáticas posee varios objetivos. Colabora a quienes las consultan a encontrar de forma rápida los resultados de las investigaciones y a evaluar su validez, la aplicabilidad de sus resultados, y sus implicaciones. El formato es útil para su publicación electrónica y su actualización, y dispone de informes cuando se hace consultas informativas o mediante una impresión.
El formato adquiere la característica de ser lo suficientemente flexible como para adaptarse a diferentes tipos de revisiones, incluidas las que hacen una única comparación y aquellas que plantean comparaciones múltiples, o a las revisiones preparadas por grupos de ensayo multicéntrico que usan datos de pacientes individuales.
Es muy importante conocer que la Base de Datos Cochrane de Revisiones Sistemáticas, se halla bien definido y es de estructura fija, y que además se encuentran descritos en el Manual Cochrane.
CARÁTULA
Título
Revisores
Detalles de citación
Fuentes de apoyo y direcciones de contactos
Qué contenido es nuevo
TEXTO DE LA REVISIÓN:
Sinopsis (preparada en colaboración con centros de expertos).
Resumen en formato estructurado:
El texto de la revisión, debe constar de una introducción la misma que considere los antecedentes y objetivos.
Los materiales deben considerar los criterios de selección de los estudios (tipos de estudios, tipos de participantes, tipos de intervenciones, tipos de medidas de resultados) y la estrategia de búsqueda.
En relación a la metodología y los resultados deben realizar una descripción de los estudios, con calidad metodológica y deben alcanzar los resultados principales, y llegar a las conclusiones de los revisores.
Estrategias de búsqueda para la identificación de los estudios
Métodos de revisión
Descripción de los estudios
Calidad metodológica
Resultados
Discusión
Conclusión de los revisores
Implicaciones para la práctica
Implicaciones para la investigación
Agradecimientos
CONFLICTOS DE INTERÉS: Las revisiones deben estar libres de cualquier sesgo real o potencial, causado por la recepción de cualquier beneficio en efectivo o en especies, cualquier patrocinio derivado. Los revisores deben informar de cualquier conflicto de intereses capaz de influir en su juicio, incluye conflictos personales, académicos, políticos, de tipo económico o de cualquier índole.
REFERENCIAS:
Referencias de los estudios
Estudios incluidos
Estudios excluidos
Estudios pendientes de evaluación
Estudios en curso
Otras referencias
Referencias adicionales
Otras versiones publicadas de esta revisión
CUADROS Y FIGURAS:
Los Cuadros y figuras serán estándar que muestren las características de los estudios incluidos , la especificación de las intervenciones que se compararon, los resultados de los estudios incluidos y la lista de los estudios que fueron excluidos.
También se deben considerar los cuadros adicionales de la teoría al ejemplo:
PLANTEAMIENTO DE UN PROBLEMA:
La práctica clínica y quirúrgica habitual en los procesos de las vías respiratorias inferiores infecciosas (IVRI) incluye la administración suplementaria de oxígeno. Al no conocerse la efectividad de la oxigenoterapia y de los diferentes métodos para administrar el oxígeno, se plantean varios cuestionamientos, entre los que son de relevancia establecer la efectividad de la oxigenoterapia, el fracaso del tratamiento (fracaso para alcanzar una PaO2 > 60 mmHg), de la seguridad que los métodos que se emplean son eficientes:
ANTECEDENTES
1. MÁSCARA FACIAL: es una máscara plástica conectada a una fuente de oxígeno, adaptada por encima de la nariz y la boca del paciente, que tiene perforaciones de lado a lado, que permiten la entrada de aire de la habitación cuando se coloca sobre la cara del niño. Es necesario usar velocidades de flujo generalmente altas para evitar el riesgo de acumulación de dióxido de carbono. Con este método la concentración de oxígeno varía de acuerdo con la velocidad del flujo respiratorio del neonato y del flujo de oxígeno en el sistema (Frey 2003). Interfiere con la alimentación para la que debe quitarse. Muchos neonatos no permiten mantener la máscara.
2. CAJA PARA LA CABEZA O CAMPANA: Caja plástica o tienda: colocada en torno a la cabeza del neonato (Myers 2002). Necesita velocidades de flujo altas (más de 5 l/min) para evitar respirar de nuevo el dióxido de carbono (Frey 2003). Es el único método que permite medir con precisión el FiO2. Limitan la movilidad y la alimentación del paciente. No aumenta el riesgo de distensión gástrica o de obstrucción de las vías respiratorias.
3. CATÉTER NASOFARÍNGEO: Tubos blandos con varios orificios distales que se insertan en la nariz hasta una profundidad igual a la distancia entre el lado del orificio nasal hasta el frente del oído (Frey 2003; Myers 2002). Se usa con velocidades de flujo bajas. Es necesario usar humidificadores para evitar que se sequen las secreciones faríngeas. Se puede bloquear con mucus, lo que puede causar obstrucción de las vías respiratorias. Hay riesgo de distensión gástrica si se desplaza el catéter. Según la OMS se recomienda un catéter nasofaríngeo 8F.
4. CATÉTER NASAL: Un tubo delgado, flexible colocado en la nariz con la punta en la cavidad nasal (Frey 2003), hasta una profundidad equivalente a la distancia entre el lado del orificio nasal hasta el margen interno de la ceja. Tiene las mismas desventajas que el catéter nasofaríngeo.
5. CÁNULA NASAL O TENEDOR NASAL: Consta de dos cánulas blandas que surgen de la tubería de administración de oxígeno, diseñadas para permanecer justo en los orificios nasales. El FiO2 varía con el flujo inspiratorio de los pacientes, el flujo de gas de la cánula, la relación entre la cánula y el diámetro nasal y el peso corporal del paciente. Debido a esto, el FiO2 que llega a las vías respiratorias del paciente, no es fácil de determinar. Puede bloquearse con secreciones, pero no hay riesgo de que se produzca distensión gástrica (Frey 2003; Myers 2002).
PRESIÓN POSITIVA CONTINUA EN LAS VÍAS RESPIRATORIAS (PPCVR) NASAL: La PPCVR es aplicar presión positiva continua en las vías respiratorias. La PPCVR nasal es un tratamiento que suministra aire algo presurizado durante todo el ciclo respiratorio. Se administra a través de una máscara que se coloca y se asegura sobre la nariz o la nariz y la boca de la persona. También puede administrarse a través de un tenedor binasal corto. La presión positiva ligera se usa para aumentar la cantidad de aire inhalado sin aumentar el trabajo respiratorio.
Otro aspecto que es muy importante conocer o tener referencias valederas son las complicaciones que pueden ocurrir entre las que se saben tenemos: neumoencéfalo informado por Fremckner 1990 en una niña de ocho meses de recién nacida con diagnóstico de neumonía estafilocócica grave. El oxígeno se suministró a través de un catéter nasofaríngeo introducido 5 a 7 cm desde el orificio nasal. Se observó exoftalmos 24 horas después de la inserción del catéter. Las tomografías computadorizadas mostraron un neumocéfalo pronunciado con 2 cm de aire subdural en la región frontal. Se determinó que el catéter había perforado el hueso del cráneo y se había ubicado dentro del cráneo. Campos 1994 informa de un neumocéfalo y exoftalmos grave en el lado derecho, desarrollados en un niño de 11 meses de vida mientras recibía oxígeno por un catéter nasofaríngeo como parte del tratamiento de una neumonía bacteriana y sinusitis. El catéter se insertó en el orificio nasal derecho y suministraba oxígeno a 2 l/min. El evento adverso ocurrió ocho días después de la inserción del catéter. La tomografía computadorizada reveló aire en la cavidad orbitaria y un neumocéfalo moderado en la región frontal y temporal derecha.
Estas descripciones pueden ser consideradas como poco casuales, pero el hecho está en que si se presentaron, y si las dudas se acrecientan es necesario esclarecerlas, por lo que para poder ser más específicos hemos de editar la revisión sistemática sobre este tema.
Nota. Por el espacio que utiliza, 77 fojas vemos por conveniente citar lo más relevante de los aspectos base de una RS, además nos será de utilidad para tener un formato modelo.
LA BIBLIOTECA COCHRANE PLUS
2011 Número 1 ISSN 1745-9990
Oxigenoterapia para las infecciones de las vías respiratorias inferiores en niños de entre tres meses y 15 años de edad
Maria Ximena Rojas, Claudia Granados Rugeles, Laura Patricia Charry-Anzola
(Revision Cochrane traducida). En: Biblioteca Cochrane Plus 2009 Número 2. Oxford: Update Software Ltd. Disponible en: http://www.update-software.com. (Traducida de The Cochrane Library, 2009 Issue 1 Art no. CD005975. Chichester, UK: John Wiley & Sons, Ltd.)
Resumen
Antecedentes
La práctica habitual en las infecciones de las vías respiratorias inferiores (IVRI) incluye la administración complementaria de oxígeno. No se conoce la efectividad de la oxigenoterapia y de los diferentes métodos de administrar el oxígeno. Esta revisión contribuye al uso racional del oxígeno en el tratamiento de las IVRI.
Objetivos
Determinar en el tratamiento de las IVRI: la efectividad de la oxigenoterapia y de los métodos para administrar el oxígeno; la seguridad de estos métodos; y las indicaciones de la oxigenoterapia.
Estrategia de búsqueda
Se realizó búsquedas en el Registro Cochrane Central de Ensayos Controlados The Cochrane Library 2008, número 2; MEDLINE (enero 1966 hasta marzo 2008); EMBASE (1990 hasta diciembre 2007); y en LILACS (enero 1982 hasta marzo 2008).
Criterios de selección
Los ensayos controlados aleatorios (ECAs) que compararon la administración de oxígeno versus ninguna oxigenoterapia o los métodos de administración de oxígeno en las IVRI hipoxémicas en niños (tres meses a 15 años de edad). Determinar las indicaciones de la oxigenoterapia, los estudios observacionales estaban incluidos.
Obtención y análisis de los datos
Se evaluaron 551 títulos. No se encontraron estudios que compararon usar oxígeno versus no usarlo. Cumplieron los requisitos de la revisión cuatro ECAs que compararon los métodos de administración y 12 estudios observacionales que evaluaron la exactitud de los signos clínicos que indicaban la hipoxemia. Se realizó un metanálisis de los ECAs que compararon los métodos de administración de oxígeno.
Resultados principales
Tres estudios evaluaron la efectividad de las cánulas nasales [tenedores nasales (TN)] versus los catéteres nasofaríngeos (CNF). El efecto de la estimación agrupada no mostró diferencias (OR 0,96; IC del 95%: 0,48 a 1,93) del fracaso del tratamiento (número de niños que no alcanzaron la adecuada SaO2). Un estudio comparó la efectividad del TN versus el catéter nasal (CN). No se encontraron diferencias del fracaso del tratamiento (el número medio de episodios de desaturación por niño: grupo con CN 2,75; DE ± 2,18 episodios por niño; grupo con TN 3; DE ± 2,5 episodios por niño, p = 0,64). Otro estudio comparó la máscara facial (MF) y la caja para la cabeza (CC) versus el CNF. El uso de la MF mostró un menor riesgo de fracaso del tratamiento (fracaso para alcanzar una PaO2 > 60 mmHg) que el CNF (OR 0,20; IC del 95%: 0,55 a 0,88). Así como el uso de la CC en comparación con el CNF (OR 0,40; IC del 95%: 0,13 a 1,12).
Los estudios que evaluaron la exactitud de los signos y los síntomas que indicaban hipoxemia mostraron que la cianosis, el quejido expiratorio, la dificultad para la alimentación y el estado de alerta mental son los más específicos para predecir la hipoxemia, y sus resultados fueron consistentes entre los estudios.
Conclusiones de los autores
Parece que la efectividad y la seguridad del TN y del CNF son similares cuando se usan en pacientes con IVRI. No hay ningún signo o síntoma clínico que identifique con exactitud la hipoxemia. Se necesitan estudios que identifiquen cuál es el método de administración de oxígeno más efectivo y seguro.
Resumen en términos sencillos
La oxigenoterapia se usa como tratamiento complementario en el tratamiento de las infecciones de las vías respiratorias inferiores en los niños
Los objetivos principales de esta revisión fueron determinar la efectividad y seguridad de los sistemas no invasivos de administración de oxígeno en la recuperación de los niños con infecciones de las vías respiratorias inferiores (IVRI). Otros objetivos fueron determinar las indicaciones de la oxigenoterapia, describir los criterios clínicos para concluir la oxigenoterapia, determinar las indicaciones para continuar la oxigenoterapia después del alta y estimar los costos asociados con cada método de administración de oxígeno.
Para responder estas preguntas se realizó una búsqueda amplia de ensayos controlados aleatorios (ECAs) de la oxigenoterapia en el tratamiento de las IVRI en los niños. No se encontraron ensayos que compararan usar oxígeno con no uso de oxígeno. Sólo cuatro ECAs y una revisión sistemática cumplieron todos los criterios de elegibilidad.
Las pruebas encontradas indican que Las cánulas nasales (tenedores nasales) pueden ser más efectivos que los catéteres nasofaríngeos y nasales para administrar oxígeno a los pacientes pediátricos con IVRI, en particular porque el tenedor nasal tiene pocos efectos secundarios y ningún evento adverso grave. Sin embargo, los intervalos de confianza (IC) del 95% obtenidos en el análisis general del riesgo del fracaso del tratamiento y del riesgo de eventos adversos, mostraron ausencia de precisión en ambos casos. No hay suficientes pruebas para determinar cuál de los métodos no invasivos disponibles de administración se debe usar en el tratamiento de la hipoxemia en los niños con IVRI.
No se encontró ningún signo clínico, modelo o sistema de puntuación que identifique con exactitud a los niños hipoxémicos.
Como los recursos varían entre los contextos, se debe considerar la eficacia, la tolerabilidad y la seguridad de los pacientes, el coste y la disponibilidad, cuando se elige el mejor método no invasivo de administración de oxígeno para el tratamiento de los niños con IVRI hipoxémico. Es necesario realizar estudios dirigidos a identificar el método no invasivo de administración de oxígeno más efectivo y seguro para ayudar a los profesionales de la salud a tomar las mejores decisiones. Las investigaciones adicionales deben considerar la eficacia, la tolerabilidad, la seguridad y los costes de los métodos estudiados.
Antecedentes
Descripción de la condición
Las infecciones agudas de las vías respiratorias inferiores (IVRI) se encuentran entre las principales causas de morbilidad y mortalidad en los niños menores de cinco años de edad en los países de bajos ingresos (Benguigui 1999). Se estima que 4,3 millones de niños menores de cinco años de edad mueren cada año de IVRI agudas. En Colombia, las IVRI agudas son la afección más frecuente en los consultorios de pacientes ambulatorios. Es la causa más frecuente de hospitalización en los niños menores de cinco años de edad y la segunda causa más frecuente de mortalidad en este grupo etario después de la diarrea.
En los países con bajos ingresos está limitado el uso suplementario de oxígeno, y sólo unos pocos centros de asistencia sanitaria son capaces de proporcionarlo, por lo que frecuentemente los niños son referidos a los hospitales con acceso a este recurso. Puede ser muy difícil a las familias obtener acceso a estos hospitales, por carecer de recursos económicos, por la necesidad de romper rutinas y por tener que viajar largas distancias. Como resultado, algunos padres no pueden aceptar las referencias y dejan los niños sin el tratamiento completo.
Descripción de la intervención
Hay múltiples guías y protocolos que recomiendan la oxigenoterapia como un componente importante del tratamiento de las IVRI agudas graves (Arango 1999; Shann1993;WHO1993). La Organización Mundial de la Salud (OMS) ha formulado recomendaciones sobre las IVRI agudas en los niños menores de cinco años de edad, que se incluyeron en el WHO/UNICEF Integrated Management of Childhood Illness (IMCI) programme (Programa Integrado para la atención a las enfermedades prevalentes de la infancia de la OMS/UNICEF) (WHO 2000). En esta estrategia sencilla se recomienda a los profesionales de la atención sanitaria tratar a los niños con tos y frecuencia respiratoria normal (tos o resfrío) sin antibióticos y sin hospitalización. Recomiendan diagnosticar una neumonía en los niños con respiración rápida, sin tiraje torácico, los que deben recibir tratamiento ambulatorio con antibióticos. La OMS diagnostica neumonía grave en los niños con neumonía y tiraje torácico y recomienda la hospitalización y el tratamiento con los antibióticos apropiados. Se recomienda administrar oxígeno a los niños con neumonía grave y cianosis o incapacidad para alimentarse ("enfermedad muy grave" o "neumonía muy grave") (Berman 1991).
Los suplementos de oxígeno son de la mayor importancia en presencia de hipoxemia y su valor varía de acuerdo con la altura (Lozano 2001; Reuland 1991).
No existe una guía específica sobre el método de administración de oxígeno en las IVRI agudas. Varios estudios y guías han descrito diferentes velocidades de flujo según la edad y el peso de los pacientes, y las concentraciones dependen de los métodos usados (Kumar 1997; Muhe 2001; Myers 2002; WHO 1993). Hay varios métodos no invasivos para usar en las IVRI sin complicaciones, como:
Máscara facial; Caja para la cabeza o campana; Catéter nasofaríngeo; Catéter nasal; Tenedor nasal o cánula nasal; Presión positiva continua en las vías respiratorias (PPCVR) nasal:
De qué manera podría funcionar la intervención
La OMS recomienda en general el uso de los catéteres nasofaríngeos y de la cánula nasal (tenedor nasal) como métodos seguros y eficientes de administración de oxígeno (WHO 1993). Los pacientes más gravemente enfermos pueden requerir métodos invasivos como la presión positiva continua (PPCVR) y la ventilación mecánica.
Por qué es importante realizar esta revisión
Los niños menores de cinco años de edad también pueden ser afectados por la bronquiolitis o la neumonía viral (sin infección bacteriana activa). En ciertos contextos clínicos los médicos quizás puedan establecer estos diagnósticos y puede ser apropiado no usar antibioticoterapia (Lozano 1994). En el caso de la bronquiolitis, el único tratamiento aceptado en todo el mundo es la oxigenoterapia, cuando es necesario. En algunos lugares la administración de oxígeno en niños con infecciones respiratorias es un procedimiento habitual, por lo que se propone determinar su eficacia, riesgo y repercusión.
Además, se conoce poco de los datos experimentales acerca de los efectos de los suplementos de oxígeno y la repercusión de los diferentes métodos no invasivos de administración de oxígeno en los niños con IVRI agudas. Esta revisión sistemática de la bibliografía evaluó el efecto de los sistemas no invasivos de administración de oxígeno en la recuperación de los niños sobre la mejoría de la oximetría de pulsos y de los signos de dificultad respiratoria, la duración de la estancia hospitalaria, las tasas de mortalidad y las necesidades de la ventilación. Esta revisión apoya el uso racional del oxígeno médico en el tratamiento de las IVRI en los países de bajos ingresos, donde la atención apropiada está limitada por la falta de recursos.
Objetivos:
Objetivos primarios
Determinar la efectividad de la oxigenoterapia en el tratamiento de las IVRI graves en los niños. Determinar la efectividad y la seguridad de los diferentes métodos de administración de oxígeno en el tratamiento de las IVRI agudas graves en los niños dado por: la frecuencia del fracaso del tratamiento o del deterioro clínico que ocurre con cada método; el tipo y la frecuencia de efectos secundarios con cada método; el tipo y la frecuencia de eventos adversos graves informados con cada método; la velocidad de flujo requerido para lograr la saturación adecuada de oxígeno; la necesidad de usar ventilación mecánica con cada método.
Objetivos secundarios
Determinar las indicaciones de la oxigenoterapia en los niños con IVRI (es decir, describir los valores de saturación de oxígeno o los signos clínicos que pueden indicar el uso de oxigenoterapia).
Describir los factores (tipo de enfermedad subyacente, gravedad de la hipoxemia en la presentación etc.) que influyen en la duración de la oxigenoterapia con cada método de administración de oxígeno.
Describir los criterios clínicos para finalizar la oxigenoterapia.
Determinar las indicaciones para continuar la oxigenoterapia después del alta.
Estimar los costes asociados con cada método de administración de oxígeno.
Métodos:
Criterios para la valoración de los estudios para esta revisión
Tipos de estudios:
Ensayos controlados aleatorios (ECAs) o cuasi aleatorios que compararon:
1. usar oxigenoterapia versus no usarla; o
2. diferentes métodos de administración de oxígeno para el tratamiento en las IVRI graves o hipoxémicas agudas en los niños (entre tres meses a 15 años de edad).
Se excluyeron los estudios realizados en poblaciones específicas con otros problemas respiratorios (como enfermedades pulmonares crónicas, asma, displasia broncopulmonar, hipertensión pulmonar, neumonía complicada) y los estudios realizados en poblaciones específicas de pacientes con otras enfermedades subyacentes (como inmunodeficiencias, trastornos metabólicos, enfermedades neurológicas que afectaban la función pulmonar, o problemas cardíacos).
El protocolo de esta revisión informó que sólo se iban a considerar los ECAs o ensayos cuasialeatorios para la inclusión. Sin embargo, para responder a los objetivos secundarios relacionados con las indicaciones de la oxigenoterapia en los niños con IVRI, se incluyeron estudios observacionales (estudios de cohorte de alta calidad).
Tipos de participantes
Los niños de entre tres meses y 15 años de edad con diagnóstico de IVRI grave como neumonía o bronquiolitis. Se decidió buscar los estudios que incluían los niños con hasta 15 años de edad porque los niños mayores también presentan IVRI y los resultados de esta revisión podían aplicarse a esta población. La IVRI se define como la presencia de tos con o sin fiebre, signos de dificultad respiratoria (tiraje subcostal, respiración rápida, uso de los músculos respiratorios accesorios, cianosis, flúter nasal) o bronquiolitis, definida como el primer episodio de sibilancias en niños menores de tres años de edad, con o sin diagnóstico radiológico de neumonía/bronquiolitis, con o sin saturación baja de oxígeno sanguíneo.
Tipos de intervenciones
1. Usar oxigenoterapia versus no usarla.
2. La administración de oxígeno mediante cualquiera de los siguientes métodos no invasivos de administración:
Mascara facial: Una máscara plástica colocada por encima de la nariz y la boca del paciente conectada a una fuente de oxígeno, con perforaciones laterales que permiten la entrada del aire de la habitación.
Caja para la cabeza o campana: Caja plástica o tienda colocada alrededor de la cabeza del neonato.
Catéter nasofaríngeo: Tubos blandos con varios orificios distales que se insertan en la nariz hasta una profundidad igual a la distancia entre el lado del orificio nasal hasta el frente del oído.
Catéter nasal: Un tubo delgado, flexible, pasado a través de la nariz y con su punta en la cavidad nasal, a una profundidad igual a la distancia entre el lado del orificio nasal y el margen interno de la ceja.
Tenedor nasal o cánula nasal: Consiste en dos cánulas blandas conectadas a una fuente de oxígeno, diseñadas para permanecer justo en los orificios nasales.
Presión positiva contínua en las vías respiratorias (PPCVR) nasal: Un tratamiento de las vías respiratorias que emplea presión positiva ligera durante la inhalación para aumentar el volumen de aire inspirado. Se suministra a través de una máscara que se coloca y se asegura por encima de la nariz del niño. También puede administrarse a través de un tenedor binasal corto.
Tipos de medida de resultado
Métodos de búsqueda para la identificación de los estudios
Búsquedas electrónicas:
Se realizaron búsquedas en el Registro Cochrane Central de Ensayos Controlados (Cochrane Central Register of Controlled Trials, CENTRAL)...
MEDLINE (OVID) (ej. 1. exp Oxygen Inhalation Therapy/ , 2. oxygen therapy. mp., 3. oxygen administration.mp., 4. oxygen delivery.mp., etc.
Los siguientes términos se agregaron a la estrategia original para buscar los estudios observacionales que informaban sobre signos clínicos que podían indicar el uso de la oxigenoterapia:
1. exp anoxemia/, 2. anoxemia/blood., 3. anoxemia/diagnosis, 4. anoxemia/therapeutic use., etc.
Búsqueda de otros recursos
Obtención y análisis de los datos Selección de los estudios
Los tres revisores (MXR, CG, LCH) exploraron de forma independiente todos los títulos identificados con las búsquedas electrónicas. Después de examinar los resúmenes, se recuperó el texto completo de los estudios potencialmente pertinentes para la inclusión. Dos autores de la revisión examinaron cada artículo (MXR-LCH o CG-LCH). Cuando surgieron desacuerdos el tercer revisor no incluido en la primera evaluación (CG o MXR) examinó el artículo sin conocer la evaluación anterior.
EXTRACCIÓN Y MANEJO DE LOS DATOS
Los tres revisores extrajeron, registraron de forma independiente los siguientes datos, cuando estaban disponibles en el informe del estudio, o por contacto directo con el autor.
Evaluación del riesgo de sesgo en los estudios incluidos
Los tres revisores realizaron de forma independiente una evaluación metodológica de los estudios que cumplieron con los criterios de elegibilidad con el uso de las Users' Guides to the Medical Literature (Guyatt 2002). La evaluación de la calidad de los ECAs incluyó las siguientes medidas de calidad: la asignación al azar y la ocultación de la asignación, la evaluación cegada de los resultados a la asignación de los grupos y el cumplimiento del seguimiento. La evaluación de la calidad de los estudios de diagnóstico (signos clínicos evaluados asociados a hipoxemia) consideró la independencia y cegamiento de la evaluación de la prueba de diagnóstico y sus resultados.
La información se registró en un formulario diseñado con antelación.
Medidas del efecto del tratamiento
Los resultados de los estudios incluidos se presentan en la tabla "Características de los estudios incluidos", describen los estudios incluidos que responden a los objetivos secundarios cuando los ECAs no estaban disponibles. El análisis cuantitativo de los resultados (ECAs) se basó en el principio de intención de tratar (intention-to-treat principle). Cada estudio se analizó individualmente para determinar el riesgo relativo/odds ratio (RR/OR) de los resultados categóricos predeterminados, como el fracaso para lograr la oxigenación adecuada (la medida de resultado principal de esta revisión), ulceración o hemorragia de la nariz, obstrucción nasal, la lucha o el malestar en las 24 primeras horas y la muerte durante el tratamiento (si se informó en los estudios incluidos).
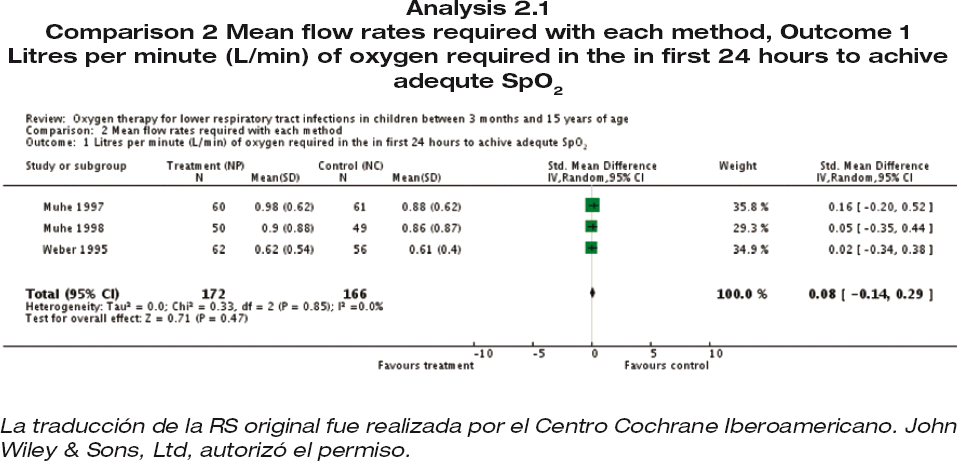
Se usó la diferencia de medias estandarizada (DME) en los resultados continuos como litros por minuto (l/min) del oxígeno requerido en las 24 primeras horas para lograr saturación de oxígeno adecuada medida con el oxímetro (SpO2). Se obtuvo un efecto general de esos resultados principales con el modelo de efectos aleatorios. Debido a la heterogeneidad clínica encontrada (diferencias de las características de la población al inicio, diferentes altitudes, ningún dato estratificado por la edad y gravedad de la IVRI) en la evaluación de estudios observacionales de los signos y los síntomas clínicos asociados con la hipoxemia, no se realizó ningún análisis estadístico para agrupar sus resultados. Se calculó la sensibilidad, especificidad y los cocientes de probabilidad de cada síntoma y signo evaluado en los estudios incluidos.
Resultados
Descripción de los estudios: Aquí se observan las características de los estudios incluidos y excluidos) el por qué
Resultados de la búsqueda
Se exploraron 559 títulos en total; 25 en CENTRAL, 365 en MEDLINE, 135 en EMBASEy34en LILACS. Se examinaron los resúmenes y algunos textos completos (cuando fue necesario) para establecer la elegibilidad. La búsqueda en la base de datos obtuvo 50 estudios potencialmente elegibles; las referencias de los estudios examinados produjeron 33 estudios adicionales potencialmente elegibles; y cuatro estudios se identificaron por la opinión de expertos. De estos estudios, inicialmente se seleccionaron 23 para su inclusión. Los otros artículos se rechazaron por las siguientes razones: eran revisiones narrativas, estudios no aleatorios, incluían neonatos o prematuros, incluían pacientes con otras enfermedades, comparaban estrategias de tratamiento diferentes a la oxigenoterapia o diferentes métodos de administración de oxígeno, eran editoriales o cartas, guía prácticas o población adulta.
Estudios incluidos
El estudio Kumar 1997 (en New Delhi), estudio Muhe 1997 (en Addis Ababa), ensayo Muhe 1998 (en Addis Ababa), otros...
Descripción de los estudios observacionales incluidos para determinar las indicaciones de la oxigenoterapia
Se incluyeron 12 estudios para determinar las indicaciones de la oxigenoterapia en niños con IVRI (es decir, describir los valores de saturación de oxígeno o los signos clínicos que indican el uso de oxigenoterapia)...
Descripción de los informes de casos incluidos los eventos adversos
Se encontraron dos estudios de informe de casos que describían eventos adversos graves relacionados con estos métodos no invasivos de administración de oxígeno en los neonatos entre tres meses y cinco años de edad con IVRI (Campos 1994; Frenckner 1990).
Frenckner (1990) informó un neumocéfalo detectado en una niña de ocho meses de vida con neumonía estafilocócica grave. El oxígeno se suministró a través de un catéter nasofaríngeo introducido 5 a 7 cm desde el orificio nasal. Se observó exoftalmos 24 horas después de la inserción del catéter. Las tomografías computadorizadas mostraron un neumocéfalo pronunciado con 2 cm de aire subdural en la región frontal. Se determinó que el catéter había perforado el hueso del cráneo y se había ubicado dentro del cráneo.
Campos 1994 informó un neumocéfalo y exoftalmos grave en el lado derecho, desarrollados en un niño de 11 meses de vida mientras recibía oxígeno por un catéter nasofaríngeo como parte del tratamiento de una neumonía bacteriana y sinusitis. El catéter se insertó en el orificio nasal derecho y suministraba oxígeno a 2 l/min. El evento adverso ocurrió ocho días después de la inserción del catéter. La tomografía computadorizada reveló aire en la cavidad orbitaria y un neumocéfalo moderado en la región frontal y temporal derecha.
Riesgo de sesgo en los estudios incluidos
Ensayos clínicos aleatorios incluidos de la efectividad de los métodos de administración
Kumar 1997 usó un método cuasialeatorio para asignar los pacientes a los grupos de tratamiento en un diseño cruzado (secuencia predeterminada). No hubo ninguna descripción del orden en el que los niños se asignaron a los diferentes métodos de administración. La evaluación de la medida de resultado principal fue completamente objetiva, aunque se pensó que no fue cegada, usaron el análisis de gases en sangre arterial y un oxímetro de pulsos. No se perdieron pacientes durante el seguimiento. Según la evaluación de la calidad este estudio tiene riesgo de sesgo, porque no se estandarizó la evaluación de la medida de resultado principal y la secuencia de asignación no se describió claramente, y otros...
Estudios observacionales incluidos para determinar las indicaciones para la oxigenoterapia en los niños con IVRI
Se incluyeron 12 estudios observacionales de diagnóstico (Basnet 2006; Duke 2002; Dyke1995; Gutierrez 2001; Laman 2005; Lodha 2004; Lozano 1994; Onyango 1993; Reuland 1991; Smyth 1998; Usen 1999; Weber 1997).
Efectos de las intervenciones
Como ya se declaró, no se encontraron estudios que compararan la administración de oxígeno versus ninguna administración de oxígeno en el tratamiento de la IVRI en niños desde tres meses a 15 años de edad...
Efectividad del tenedor nasal versus el catéter nasofaríngeo en el tratamiento de las IVRI agudas graves en los niños
1. Fracaso del tratamiento
2. Eventos adversos
3. Efectos adversos graves
4. Velocidades de flujo medias requeridas con cada método para lograr SaO2 adecuada
Efectividad de la máscara facial y la caja de la cabeza versus el catéter nasofaríngeo en el tratamiento de las IVRI agudas graves en los niños
Sólo un estudio informó la efectividad comparada de la máscara facial y de la caja de la cabeza con el catéter nasofaríngeo (Kumar 1997)...
Indicaciones para la oxigenoterapia en los niños con IVRI
Para describir los valores de saturación de oxígeno o los signos clínicos que indiquen el uso de la oxigenoterapia se incluyeron 11 estudios realizados con la intención de evaluar la exactitud de cada signo y síntoma presente en el momento del ingreso para indicar la presencia de hipoxemia...
DISCUSIÓN
Efectividad de los métodos no invasivos de administración en el tratamiento de las IVRI agudas graves en los niños
Algunos de los estudios incluidos (Kumar 1997; Muhe 1997; Weber 1995) evaluaron la efectividad del tenedor nasal en comparación con el catéter nasofaríngeo por el fracaso en lograr adecuada SaO2 en las horas que seguían al administración de oxígeno. No hubo diferencias del riesgo de fracaso del tratamiento entre los grupos (tenedor nasal versus catéter nasofaríngeo).
Tampoco hubo diferencias de la frecuencia de episodios de desaturación de oxígeno entre ambos grupos cuando se comparó el tenedor nasal versus el catéter nasal (una versión más corta del catéter nasofaríngeo) (p = 0,64) (Muhe 1998). En relación con los efectos secundarios asociados con cada método, el único efecto adverso que mostró una diferencia significativa entre los grupos fue la obstrucción nasal debida a la producción intensa de mucus y fue más frecuente en el grupo con el catéter nasofaríngeo.
El neumocéfalo es el único evento adverso grave asociado con el catéter nasofaríngeo que se ha informado. En lo que se refiere a la velocidad de flujo medio necesaria para lograr adecuada SaO2, los resultados fueron similares en ambos grupos (catéter nasofaríngeo/ catéter nasal y tenedor nasal) y no se encontraron diferencias significativas.
Los resultados del estudio de Kumar 1997 mostraron que las altas velocidades de flujo usadas en las cajas de la cabeza y en las máscaras faciales son mucho más efectivas para lograr la saturación adecuada de oxígeno que las bajas velocidades de flujo usadas en las cánulas nasales y en los catéteres nasofaríngeos. Sin embargo, las diferencias de la cantidad de oxígeno requerido por esos métodos son significativamente altas (4 l/min versus 1 l/min respectivamente), y esto puede aumentar el coste del tratamiento por día de IVRI en los niños. La administración de oxígeno en muchos hospitales de países de bajos ingresos es limitada y el uso de los sistemas con flujo alto puede contribuir a este problema.
En resumen, las pruebas indican que el tenedor nasal puede ser más efectivo que los catéteres nasofaríngeos y nasales para la administración de oxígeno en los pacientes pediátricos con IVRI, porque el tenedor nasal causa menos efectos secundarios y no se ha asociado con eventos adversos graves. Sin embargo, los resultados obtenidos del riesgo del fracaso del tratamiento y el riesgo de eventos adversos son imprecisos y no permiten confirmar que el tenedor nasal es el método más efectivo y más seguro de administración de oxígeno como otros autores han planteado anteriormente (Muhe 1997; Weber 1995). Por lo tanto, no hay suficientes pruebas para definir cuál de los métodos no invasivos de administración es el mejor para el tratamiento de la hipoxemia en los niños con IVRI.
Ya que los recursos varían entre los contextos, se debe considerar la eficacia, la tolerabilidad y la seguridad de los pacientes, el coste y la disponibilidad, cuando se elige el mejor método no invasivo de administración de oxígeno para el tratamiento de los niños con IVRI hipoxémicas. Para ayudar a los trabajadores de la salud a que tomen la decisión correcta, se necesitan estudios que se dirijan a identificar el método de administración de oxígeno no invasivo más seguro y más efectivo. Las investigaciones futuras deben considerar la eficacia, la tolerabilidad, la seguridad y los costes de los métodos en estudio.
Indicaciones para la oxigenoterapia en los niños con IVRI
Se han realizado varios estudios para tratar de identificar las variables predictivas clínicas de la hipoxemia en los niños con IVRI. Este interés responde a la necesidad de los médicos y los trabajadores de la salud de los países con ingresos bajos y medianos, en los que los recursos de salud y los suministros son limitados, de determinar la presencia de hipoxemia en los neonatos y los niños sin usar un oxímetro o la determinación de gases en sangre arterial. Sin embargo, todos estos esfuerzos han indicado que no hay ningún signo o síntoma particular que indique claramente la presencia de hipoxemia. Esta revisión confirma los resultados anteriores al mostrar la amplia variabilidad de la sensibilidad y la especificidad de cada signo o síntoma encontrado por 12 autores que siguieron métodos similares de medición de los signos clínicos, así como métodos similares de medición de la hipoxemia (todos usaron un oxímetro). Esta amplia variabilidad puede ser debida a las diferencias de las definiciones de hipoxemia usadas entre los estudios realizados en altitudes similares; por ejemplo, Onyango 1993, realizado a 1670 m.s.n.m. definió la hipoxemia como SaO2 < 91%, Dyke 1995 realizado a una altitud similar (1600 m.s.n.m.) definió la hipoxemia como SaO2 < 86%; y Duke 2002 realizado a la misma altitud de Dyke, definió la hipoxemia como SaO2 < 88%. Otro aspecto importante que puede explicar esta variabilidad es la implicación de fijar un punto de corte para las frecuencias respiratorias que indican la taquipnea a cualquier nivel particular, de acuerdo con la edad de los niños. Como Smyth 1998 y Lozano 1994 mostraron, la sensibilidad y la especificidad de este signo cambia según el punto de corte establecido para la frecuencia respiratoria. Debido a este resultado, el uso de "taquipnea" como un indicador para la oxigenoterapia daría lugar a una proporción de los niños tratados con oxígeno innecesariamente y otra proporción que no recibirá oxígeno cuando en realidad lo necesitan.
Aún con estas fuentes de variabilidad, algunos autores han realizado diferentes esfuerzos para mejorar la predicción de la hipoxemia en los niños con IVRI, derivados de las reglas de las variables predictivas clínicas o los modelos predictivos basados en la combinación de los signos y los síntomas clínicos presentes en el momento del ingreso.
Estos modelos tampoco son comparables entre los estudios y su confiabilidad para predecir la hipoxemia todavía es incierta.
Las guías WHO 1993 para la oxigenoterapia en los niños con infecciones respiratorias agudas recomiendan la oxigenoterapia para los neonatos y los niños que presentan cianosis o incapacidad para beber, como casos prioritarios. Según las pruebas presentadas en esta revisión, la cianosis es en verdad uno de los signos más específicos para determinar la presencia de hipoxemia, pero la incapacidad de alimentarse o beber ha mostrado ser muy inespecífico y no sensible en los estudios que lo evaluaron. WHO 1993 también recomienda administrar oxígeno a los niños que presentan tirajes torácicos graves, o con una frecuencia respiratoria mayor o igual a 70 respiraciones/minuto, o a los neonatos menores que resoplan cuando respiran. En esta revisión estos tres signos, cuando se consideraron individualmente, han mostrado ser muy inespecíficos para determinar la presencia de hipoxemia. La sensibilidad y la especificidad de los tirajes torácicos son ampliamente variables en todos los grupos etarios informados (sensibilidad: min 32, máximo 98; especificidad: min 7, máximo 94); la frecuencia respiratoria, como se señaló anteriormente, no es una variable predictiva útil de la hipoxemia, ya que no hay puntos de corte exactos establecidos por los grupos etarios; y el gruñido es específico pero no sensible para determinar la presencia de hipoxemia.
Algunos de los estudios incluidos (Duke 2002; Gutierrez 2001; Smyth 1998; Usen 1999; Weber 1997) evaluaron la precisión de los modelos de regresión que incluyeron todos los criterios recomendados por WHO 1993 (incapacidad para alimentarse, cianosis, frecuencias respiratorias > 70 r/m, o tiraje torácico grave) para predecir la hipoxemia. En general, este modelo mostró alta sensibilidad entre los estudios (62%, 76%, 80,9% y 27% respectivamente) para determinar la presencia de hipoxemia, pero baja especificidad (este resultado se esperaba ya que el agregar signos mejora la sensibilidad y disminuye la especificidad). Según estos resultados, después del algoritmo recomendado por WHO 1993 resultará que se administrará oxígeno a pacientes sin hipoxemia. Duke 2002 por ejemplo, encontró que al usar este modelo sumamente sensible, a casi el 50% de los niños estudiados se les administraría oxígeno sin necesitarlo. De acuerdo con estos resultados, si se usan los criterios de la OMS para administrar el oxígeno puede realizarse un uso inapropiado del oxígeno médico, que es un recurso muy limitado en la mayoría de los establecimientos de salud en los países de bajos ingresos. Al seguir estos criterios también se aumentan los costos del tratamiento médico de las infecciones respiratorias agudas en los neonatos y los niños.
Esta revisión ha indicado que todavía no hay ningún signo clínico, modelo o sistema de puntuación, que identifique con exactitud a los niños hipoxémicos. La medición de la SaO2es todavía una prueba particularmente importante para los médicos para tomar la decisión correcta con respecto a si dar o no suplementos de oxígeno a los neonatos y los niños con IVRI. Como muchos autores han declarado, para mejorar el uso racional del oxígeno médico es necesario invertir los recursos para administrar monitores de saturación de oxígeno a los contextos clínicos y a todos los establecimientos de salud en los países de bajos ingresos. Tener un monitor de saturación de oxígeno en las salas de urgencias puede contribuir no sólo al uso racional del oxígeno médico, sino también a evitar el riesgo de efectos secundarios asociados con el uso del oxígeno en los neonatos y los niños pequeños. A largo plazo, esta inversión puede dar lugar a opciones más efectivas en función de los costes, al disminuir el "derroche" de oxígeno.


Agradecimientos Datos y análisis

Novedades

Antecedentes
Primera publicación del protocolo: Número 2, 2006
Primera publicación de la revisión: Número 1, 2009
Contribuciones de los autores
María Ximena Rojas (MXR) y Claudia Granados (CG) diseñaron la revisión, establecieron los objetivos y criterios para considerar los estudios para el protocolo. MXR se encargó principalmente de escribir el protocolo (60%), y CG la ayudó a escribirlo (40%).
Laura Patricia Charry-Anzola (LCH) estuvo implicada en el desarrollo de la revisión. Realizó la búsqueda manual y en la base de datos y recuperó el texto completo de los artículos.
MXR, CG y LCH participaron activamente en la selección, evaluación y extracción de datos de los artículos para esta revisión. MXR fue responsable principal de la redacción del manuscrito; CG y LCH examinaron y corrigieron el manuscrito.
Declaraciones de interés
Ninguno conocido.
Fuentes de financiación
Recursos internos
Department of Pediatrics, Department of Clinical Epidemiology and Biostatistics. Pontificia Universidad Javeriana, Colombia.
Protected time for review authors. Monetary support to pay for full text articles
Recursos externos
No sources of support supplied
Diferencias entre el protocolo y la revisión
As highlighted in the 'Types of studies' section, during the development of this review we decided to consider observational studies for inclusion to respond the following secondary objective (already considered in the protocol of this review): to determine the indications for oxygen therapy in children with LRTIs (i.e. to describe the oxygen saturation values or clinical signs that would indicate the use of oxygen therapy).
Información de contacto
Authors: Maria Ximena Rojas1, Claudia Granados Rugeles2, Laura Patricia Charry-Anzola1, otros...
Referencias (SÓLO COLOCAMOS COMO EJEMPLOS TRES):
Referencias de los estudios incluidos en esta revisión
Kumar 1997 {published data only}
Kumar RM, Kabra SK, Singh M. Efficacy and acceptability of different modes of oxygen administration in children: implications for a community hospital. Journal of Tropical Pediatrics 1997; 43(1): 47-9. [MEDLINE: ]
Referencias adicionales
Arango 1999
Arango Loboguerrero M. Control of acute respirtatory infections in children between 2 months and 5 years of age: Section IV: Prevention and Control. Chapter18. In: Benguigui, et al. editor(s). Respiratory Infections in Children. IMCI. PAHO. ACTH/AIEPI-1-1, 1999: 343-53.
Tablas (se coloca como ejemplo una sola tabla)
Características de los estudios
Características de los estudios incluidos [ordenados por ID del estudio]
Figuras
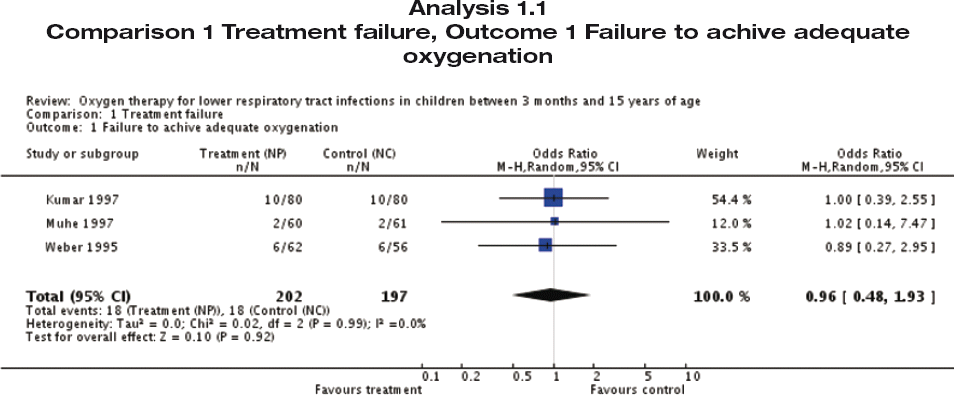
Como interpretar la gráfica del Odds Ratio: Simbolos
♦ (Diamante); Gran tamaño muestral.
■ (Caja tamaño grande); Tamaño muestral mediano.
■ (Caja tamaño pequeño); Tamaño muestral pequeño.
• (Punto); Tamaño muestral muy pequeño.
CONCLUSIONES FINALES: Al terminar este capítulo de revisiones sistemáticas "metanálisis", consideramos haber logrado que los que viven con la intensidad necesaria de lograr cambios a corto y mediano plazo que logren beneficiar aunque sea a un solo paciente son necesarios y esto es lo que hace la diferencia, de estar sometidos al lento pasar del tiempo y no buscar nuevos caminos de logros.
Se encuentran hoy en día libros, revistas, se hacen seminarios, conferencias sobre estos aspectos, pero lo importante es desarrollar de forma comunitaria grupos de trabajo, a los que brindaremos nuestras propias experiencias y conocimientos aprendidos, además de seguir en el camino del permanente aprendizaje.
En el próximo número tendremos la satisfacción de revisar los aspectos de la "ELABORACIÓN DE GUÍAS CLINICAS BASADAS EN LA EVIDENCIA"
"EL HACER ES PARTE DE LA VOLUNTAD DE BRINDAR, EL CRITICAR Y NO HACER, ES PARTE DEL QUE NO MIRA MÁS ALLÁ DE SU MÍNIMO INTERIOR"
REFERENCIAS
1. Chalmers I, Dickersin K, Chalmers TC. Getting to grips with Archie Cochrane's genda. BMJ 1992;305: 786 [ Links ]
2. Mulrow CD. Rationale for systematic reviews. BMJ 1994;309:597-9. [ Links ]
3. Huque MF. Experiences with meta-analysis in NDA submissions. Proc Biopharmaceutical Section Am Statist Assoc 1988;2: 28-33. [ Links ]
4. Egger M, Davey Smith G. Misleading meta-analysis. Lessons from "an effective, safe, simple" intervention that wasn't. BMJ 1995;310:752-4. [ Links ]
5. Eysenck HJ. An exercise in mega-silliness. Am Psychol 1978;33: 517. [ Links ]
6. Easterbrook PJ, Berlin JA, Gopalan R, Matthews DR. Publication bias in clinical research. Lancet 1991;337: 867-72. [ Links ]
7. Gotzsche PC. Reference bias in reports of drug trials. BMJ 1987;295:654-6. [ Links ]
8. Egger M, Zellweger-Zähner T, Schneider M, Junker C,Lengeler C, Antes G. Language bias in randomised controlled trials published in English and German. Lancet 1997;350:326-9. [ Links ]
9. Egger M, Davey Smith G. Meta-analysis: bias in location and selection of studies. BMJ. [ Links ]
10. Light RJ, Pillemer DB.Summing up. The science of reviewing research. Cambridge, MA: Harvard University Press, 1984. [ Links ]
11. Villar J, Piaggio G, Carroli G, Donner A. Factors affecting the comparability of meta-analyses and largest trials results in perinatology. J Clin Epidemiol 1997;50: 997-1002. [ Links ]
12. Galbraith R. A note on graphical presentation of estimated odds ratios from several clinical trials. Stat Med 1988;7: 889-94. [ Links ]














