Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz v.17 n.1 La Paz 2011
ARTÍCULO DE REVISIÓN
MANEJO Y TRATAMIENTO DE LA PANCREATITIS AGUDA EN LA UNIDAD DE CUIDADOS INTENSIVOS
Dr. Oscar Vera Carrasco*
* Especialista en Medicina Crítica y Terapia Intensiva.
Prof. Emérito de la Facultad de Medicina-Universidad Mayor de San Andrés.
Email: oscar4762@yahoo.es
DEFINICIÓN
La pancreatitis aguda (PA) es un proceso inflamatorio agudo del páncreas, desencadenado por la activación inapropiada de las enzimas pancreáticas, con lesión tisular y respuesta inflamatoria local y sistémica. Conlleva en ocasiones compromiso variable de otros tejidos o sistemas orgánicos distantes.
CLASIFICACIÓN
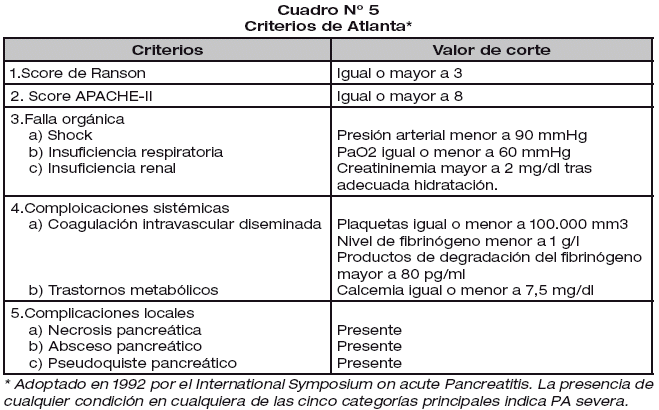
El sistema de clasificación basado en la clínica según el consenso de Atlanta de 1992 es el siguiente:
Pancreatitis aguda leve: es un proceso inflamatorio pancreático agudo en el que, el hallazgo patológico fundamental es el edema intersticial de la glándula, y existe mínima repercusión sistémica.
Pancreatitis aguda grave: es la que se asocia a fallas orgánicas sistémicas o a complicaciones locales como necrosis, pseudoquiste o absceso. Generalmente, es consecuencia de la existencia de necrosis pancreática, aunque ocasionalmente, se pueden presentar evidencias de gravedad en pancreatitis edematosas.
• Necrosis: se manifiesta como zonas localizadas o difusas de tejido pancreático no viable que, generalmente, se asocian a necrosis grasa peripancreática. En la tomografía se aprecian como zonas con menor densidad que la del tejido normal, pero mayor que la densidad líquida, y que no incrementan su densidad con el medio de contraste.
Colecciones líquidas agudas: éstas son de densidad líquida que carecen de pared y se presentan precozmente en el páncreas o cerca de él.
• Pseudoquiste: es la formación de densidad líquida (rica en enzimas digestivas), caracterizada por la existencia de una pared de tejido fibroso o de granulación, que no aparece antes de las cuatro semanas después del inicio de la pancreatitis.
Absceso pancreático: es una colección circunscrita de pus, en el páncreas o su vecindad, que aparece como consecuencia de una pancreatitis aguda y contiene escaso tejido necrótico en su interior.
Pancreatitis aguda severa
La pancreatitis aguda severa (PAS) se caracteriza por la presencia de necrosis parenquimatosa, necrosis de la grasa retroperitoneal, fallo sistémico, un cuadro clínico tormentoso y el desarrollo de complicaciones potencialmente letales. Afecta del 20 al 25% de los pacientes que desarrollan una pancreatitis. Se considera que un paciente es portador de PAS si presenta alguno de los siguientes criterios:
1. Fallo orgánico con uno o más de los siguientes criterios: shock (presión arterial sistólica <90 mm Hg), insuficiencia respiratoria (PaO2 <60 mmHg), insuficiencia renal (creatinina sérica>2mg/dl luego de la hidratación) y sangrado gastrointestinal (> 500 ml en 24 horas).
2. Complicaciones locales tales como necrosis, pseudoquistes o abscesos.
3. Al menos 3 de los criterios de Ranson (ver más adelante).
4. Al menos 8 de los criterios del APACHE II.
Se ha comprobado, que la falla orgánica que se presenta en la primera semana y se resuelve dentro de las 48 horas, no es un indicador de un ataque severo de pancreatitis aguda.
ETIOLOGÍA
1) Litiasis biliar: 40-50% de los casos. Sólo en el 20-30% se encuentra el cálculo enclavado en la papila. El barro biliar y la microlitiasis son factores de riesgo para el desarrollo de PA y probablemente son la causa de la mayoría de las PA idiopáticas.
2) Alcohol: 35% de las PA. Es infrecuente en bebedores ocasionales.
3) Post-CPRE: Hay hiperamilasemia en el 50% de las CPRE y síntomas en el 1-10%.
4) Postquirúrgica: En cirugía mayor cardiaca y abdominal. Alta mortalidad (10-45%).
5) Hipertrigliceridemia: Con trigliceridemia >1000 mg/dl. Mecanismo desconocido.
6) Idiopática: Representa el 10% de los casos.
7) Fármacos: Azatioprina, valproato, estrógenos, metronidazol, pentamidina, sulfonamidas, tetraciclinas, eritromicina, trimetropina, nitrofurantoina, diuréticos de asa, tiazidas, metildopa, mesalamina, sulindac, paracetamol, salicilatos, cimetidina, ranitidina, corticoides, ddI, Lasparginasa, 6-mercaptopurina, procainamida, cocaína, IECA.
8) Infecciones:
- Virus: VIH, CMV, parotiditis, Coxackie, EBV, rubeola, varicela, adenovirus.
- Bacterias: Mycoplasma, Salmonella, Campylobacter, Legionella, Leptospira, TBC.
- Parásitos: Áscaris, Fasciola hepática.
9) Traumatismo abdominal.
10) Metabólica: Hipercalcemia, insuficiencia renal.
11) Obstructiva: Obstrucción de la ampolla de Vater (tumores periampulares, divertículo yuxtacapilar, síndrome del asa aferente, enfermedad de Crohn duodenal), coledococele, páncreas divisum, páncreas anular, tumor pancreático, hipertonía del esfínter de Oddi.
12) Tóxicos: Organofosforados, veneno de escorpión.
13) Vascular: Vasculitis (LES, PAN, PTT), hipotensión, HTA maligna, émbolos de colesterol.
14) Miscelánea: Pancreatitis hereditaria, úlcera duodenal penetrada, hipotermia, transplante de órganos, fibrosis quística, quemaduras, carreras de fondo.
CUADRO CLÍNICO
Dolor abdominal: es el síntoma capital, presente en más del 90% de los enfermos. Habitualmente es de inicio rápido, intenso, constante, ubicado en el hemiabdomen superior, clásicamente irradiado "en faja" o en "cinturón", de difícil control. Irradiación al dorso presentan el 50% de los pacientes.
Vómitos y estado nauseoso: otra síntomatología importante, y presente en el 70-90 % de los pacientes.
La distensión abdominal, el íleo paralítico, la ictericia y el colapso cardiocirculatorio pueden estar también presentes, en especial en aquellos casos más graves.
Los signos físicos varían en su localización, extensión, intensidad y calidad, todo ello en relación con la zona pancreática interesada, la gravedad y naturaleza de los hallazgos patológicos, el estadio del ataque, la presencia, extensión o ausencia de peritonitis, íleo o ascitis, la participación de otros órganos abdominales, etcétera. En el examen físico siempre se deben incluir el peso, la talla, el índice de masa corporal (IMC), la temperatura, la saturación de oxígeno (SaO2), la frecuencia cardiaca, la frecuencia respiratoria y la tensión arterial. Pueden destacarse el signo de Mayo-Robson (dolor a la palpación del ángulo costo lumbar posterior izquierdo) y el signo de Cullen (equímosis periumbilical).
Ejemplo:
- El espasmo de los músculos abdominales.
- Percusión del abdomen (timpanismo o matidez).
- Disminución de los ruidos intestinales.
- Presencia de febrícula.
- Taquicardia.
- Disnea y ortopnea, distensión abdominal, ascitis, derrame pleural, atelectasia pulmonar o condensación, hipovolemia y shock (en formas graves).
- En ocasiones aparecen signos cutáneos y subcutáneos (signo de Grey Turner y signo de Cullen: equimosis periumbilical).
EXÁMENES COMPLEMENTARIOS
Laboratorio:
- Determinaciones enzimáticas: la determinación de amilasemia y amilasuria , elevación de la lipasa (específica).
- Hemograma: Leucocitosis, Hb. y Hcto. generalmente superan las cifras normales, a causa de la hemoconcentración.
- Bilirrubinemia y calcemia (hipocalcemia = gravedad).
- Hiperglucemia y glucosuria (inconstante).
- Incremento de la urea y la creatinina plasmáticas.
- Marcadores de necrosis (Determinación de la proteína C reactiva, la alfa1 antitripsina y la alfa 2 macroglobulina.
- Examen del líquido peritoneal (si se constata presencia de este).
- Coagulograma si el paciente es candidato a procedimientos invasivos (PT, PTT, INR).
1. Amilasa: se eleva a las 2-12 horas de comienzo del dolor y puede normalizarse en 2-5 días. Cifras 3 veces superiores al valor normal sugieren el diagnóstico, pero hay que tener en cuenta que la amilasa se eleva en muchos procesos intra y extraabdominales El grado de hiperamilasemia no se correlaciona con la gravedad del proceso, pero a medida que aumentan las cifras aumenta la sensibilidad y la especificidad. Cifras 5 veces por encima del valor normal son altamente indicativas de PA. Puede ser normal porque su elevación es fugaz y el examen se toma tarde, si existen niveles de triglicéridos muy elevados o si se trata de una P.A. crónica recurrente con insuficiencia pancreática. No es específica.
Puede estar elevada en otros cuadros intraabdominales: colecistitis aguda, coledocolitiasis, úlcera perforada, accidente vascular mesentérico, etc.). La amilasa urinaria elevada es más persistente que la amilasa sérica (7-10 días). Se suele pedir mediciones en orina de 24 hrs. Es más sensible que la amilasa sérica.
2. Lipasa: presenta mayor sensibilidad (S: 94%) y especificidad (E: 96%) que la amilasa total sérica. Se eleva el primer día y los niveles plasmáticos persisten elevados un poco más de tiempo que los de amilasa. Se usa para el diagnóstico de pancreatitis un valor de corte del triple del límite superior del valor normal. Existen aumentos por debajo de 3 veces el valor normal en la insuficiencia renal grave, roturas de aneurisma, nefrolitiasis, obstrucción intestinal, quimio o radioterapia. La determinación simultánea de amilasa y lipasa tiene una S y E > 95%.
3. Otros datos analíticos: Hematocrito (Hcto), leucocitosis con desviación izquierda, hiperglucemia sin cetoacidosis, ↑BUN, ↓PaO2, déficit de bases, ↓Ca, ↓Albúmina, ↑LDH, ↑GOT o GPT, ↑ bilirrubina, ↑fosfatasa alcalina (FA), ↑triglicéridos, Proteína C Reactiva (PCR).
b) ECG: Imprescindible. Sirve para descartar que el dolor sea por cardiopatía isquémica, conocer la situación basal del paciente, y valorar cambios en caso de fallo cardiaco.
Imagenología:
Radiografía simple
Radiografía de abdomen :
- Puede haber presencia de una opacidad prevertebral, colocada trasversalmente sobre L1-L2.
- Ileo segmentario ocasional, es muy raro el neumoperitoneo.
Radiografía de tórax :
- Sobreelevacion del hemidiafragma izquierdo y no siempre derrame pleural o atelectasias basales en el mismo lado. En los casos severos se puede reconocer un infiltrado alveolar difuso que sugiere un síndrome de dificultad respiratoria aguda.
Ecografía abdominal y la endoultrasonografía (EUS).
Tomografía axial computarizada.
Colangio-resonancia.
1. Radiografía tórax: obligada, puede presentar atelectasias, derrame pleural, insuficiencia cardiaca congestiva, SDRA, neumoperitoneo.
2. Radiografía abdomen: Se puede encontrar íleo localizado ("asa centinela") o generalizado, espasmo de un segmento del colon ("signo de la interrupción del colon"), cálculos biliares calcificados, calcificaciones pancreáticas, ascitis. Ayuda en el diagnóstico diferencial con otras enfermedades abdominales: perforación de víscera, isquemia intestinal, oclusión intestinal.
3. Ecografía abdominal: Debe realizarse siempre dentro de las primeras 24h. Se solicita para descartar el origen litiásico de la PA y detectar signos de obstrucción de la vía biliar (de causa litiásica o no). Puede servir en algunos casos para orientar la severidad de la PA.
Si el diagnóstico clínico de presunción de PA no es claro, debe establecerse un árbol de diagnóstico diferencial clínico, para alguno de los cuales es útil la ecografía (colecistitis, isquemia intestinal, apendicitis retrocecal).
4. TAC abdominal: Es el método de imagen más importante para el diagnóstico de la PA y el estudio de su severidad (Cuadro 3). Recordar que es imprescindible la estabilización hemodinámica de los pacientes para su realización y que el "bolo" de contraste intravenoso puede agravar la situación clínica del paciente y/o empeorar otras patologías asociadas (insuficiencia renal, insuficiencia cardíaca). Si la suma de la puntuación obtenida de la evaluación del grado de severidad según cambios morfológicos y del grado de severidad según el área de necrosis es >6 puntos, el paciente es subsidiario de valoración por UCI. Esta indicado en: casos de duda diagnóstica, deterioro clínico, falla orgánica múltiple, sospecha de necrosis pancreática, valoración de complicaciones en casos de pancreatitis grave (se debe realizar a las 48 horas del inicio del cuadro clínico) o persistencia de deterioro.
5. Resonancia magnética de abdomen: se utiliza de manera excepcional, sólo cuando el paciente tenga contraindicación para la realización de TAC.
6. Colangio-resonancia: Se usa en pacientes con pancreatitis biliar y una probabilidad intermedia baja para coledocolitiasis.
DIAGNÓSTICO
El diagnóstico de la pancreatitis aguda se basa en el cuadro clínico, hiperamilasemia y evidencia morfológica de inflamación pancreática. Esta última puede ser demostrada mediante métodos por imágenes (ecografía y/o TAC), cirugía o anatomía patológica.
La obligatoriedad de la presencia de los tres criterios para definir el ataque es especialmente útil para aumentar la especificidad diagnóstica.
DIAGNÓSTICO DIFERENCIAL
Existen procesos abdominales que producen dolor y que pueden cursar con elevación de amilasa (colecistitis aguda, obstrucción del colédoco, perforación del esófago, estómago, intestino delgado o colon, isquemia o infarto intestinal, apendicitis aguda, cuadros ginecológicos agudos como embarazo ectópico roto, salpingitis aguda) y/o lipasa sin existir PA. También existen procesos que producen elevación de enzimas pancreáticas sin producir dolor abdominal, pero puede darse la circunstancia de que un paciente tenga 2 enfermedades al mismo tiempo, las que producen la elevación de la enzima pancreática y el dolor abdominal. Por último, no debemos olvidar nunca, que una angina o un infarto de miocardio de cara diafragmática pueden producir dolor epigástrico similar al de la PA.
De todos los procesos con los que hay que hacer el diagnóstico diferencial, hay que destacar 7 por su severidad y porque en ocasiones presentan gran similitud clínica: Colecistitis aguda, embarazo ectópico (↑β-HCG), perforación de víscera hueca, obstrucción intestinal, isquemia infarto mesentérico, aneurisma disecante de aorta, IAM de cara diafragmática.
EVALUACIÓN DE SEVERIDAD
Existen varias herramientas diagnósticas para evaluar la severidad de la pancreatitis. El diagnóstico adecuado de pancreatitis aguda leve o grave tiene gran implicancia pronóstica y terapéutica. Si bien ningún método aislado ha demostrado suficiente sensibilidad y especificidad, la combinación de criterios objetivos, clínicos y de laboratorio, conjuntamente con la estratificación por TAC de abdomen, constituyen la mejor aproximación actual a la clasificación de la gravedad de la pancreatitis aguda.
En el momento actual, la proteína C reactiva permanece como el mejor marcador bioquímico simple para predecir la severidad de la PA. Debido a que la combinación de scores clínico-fisiológicos con la proteína C reactiva provee buena información a las 48 horas, las investigaciones actuales están focalizadas en la capacidad predectiva de varios marcadores durante las primeras 24 horas de enfermedad. Aún no existe un único marcador que puede utilizarse como predictor óptimo de severidad de enfermedad en la PA. Sin embargo, existen ciertos marcadores que ayudan a mejorar la capacidad predictiva médica. Estos incluyen los que se muestran a continuación, y que se categorizan según el momento de su utilización.
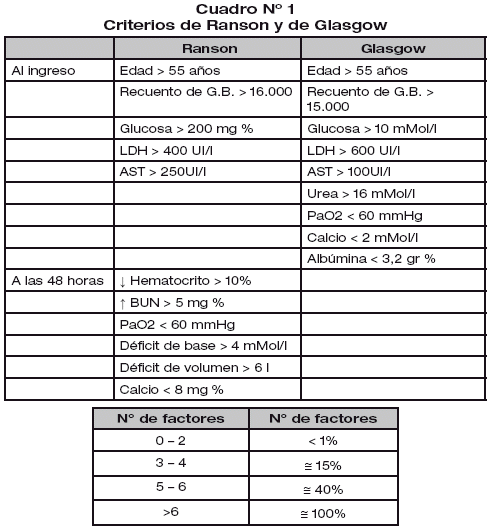
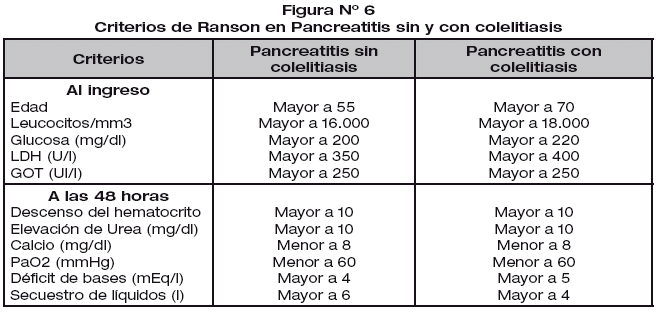
La clasificación clínica es poco confiable y falla en cerca del 50% de los casos. Los criterios de Ranson han demostrado un bajo valor predictivo, y un análisis del valor predictivo individual ha demostrado que los únicos útiles son aquellos que traducen fallas orgánicas (insuficiencia renal o respiratoria y shock) y edad avanzada. Nueve criterios adaptados de Ranson, conocidos como criterios de Glasgow (Cuadro 1) o Score lmrle (Cuadro 2), fueron adoptados desde 1984 como indicadores pronósticos de gravedad, sin embargo su valor predictivo no supera el 70 a 80%.

El Score APACHE II (Acute Physiology and Chronic Health Evaluation) es de uso frecuente en las unidades de cuidados intensivos, y su aplicación al ingreso o dentro de las primeras 48 horas permite diferenciar la pancreatitis aguda leve de la grave. Además, su utilización en cualquier momento de la evolución, es un indicador de gravedad del paciente y del progreso o deterioro de la pancreatitis. Las mediciones que involucran son relativamente simples y se pueden efectuar en la mayoría de los hospitales (Cuadro 4). Aún en ausencia de laboratorio, los criterios de edad y patologías crónicas y, dentro de los criterios fisiológicos agudos, el Glasgow, la temperatura, presión arterial y frecuencias respiratoria y cardíaca, permiten una aproximación a la gravedad.
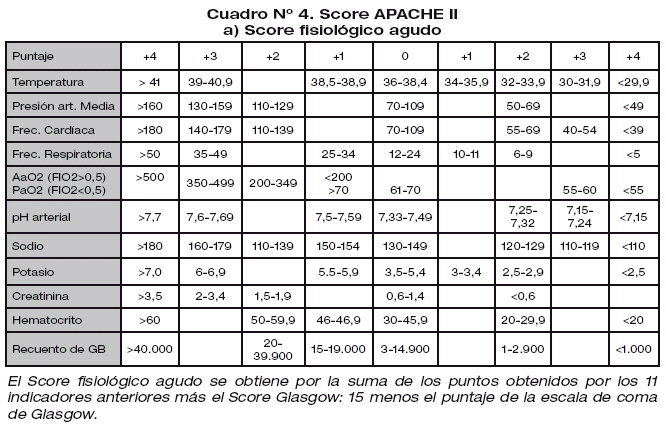
Un score de 9 o más indica pancreatitis grave; sin embargo, con este nivel de corte muchos pacientes que desarrollarán complicaciones quedan excluidos. Un score de 6 permite una sensibilidad de 95% para complicaciones, pero disminuye el valor predictivo a 50%
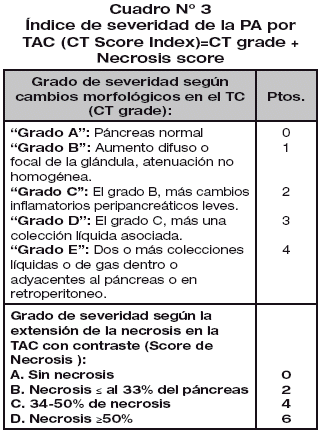
Las indicaciones para la realización urgente de la TAC son:
A. Hallazgos clínicos y bioquímicos no concluyentes y existencia de signos abdominales compatibles con un cuadro abdominal severo: perforación de víscera hueca, oclusión intestinal, isquemia intestinal, aneurisma de aorta abdominal, etc.
B. PA asociada a un fallo de órgano de nueva aparición (shock-TAS <90 mmHg, PaO2< 60mmHg, Cr >2mg/dl, hemorragia digestiva superior a 500 ml/24h).
C. ≥ 3 puntos según los Criterios de Ranson o Glasgow.
D. Impresión clínica de severidad (criterio condicionado por la pericia del médico que evalúa al paciente, pero que se utiliza en guías de consenso para manejo de la PA).
Si no se cumplen los criterios anteriores, no está indicada la realización del TAC abdominal de forma urgente para la estatificación de la gravedad de la PA.
c.5. CPRE: está indicada su realización en las primeras 72 horas de comienzo del dolor en los siguientes casos: a) PA severa de etiología biliar b) Colangitis c) Ictericia d) Dilatación significativa del colédoco. No se realiza en el momento de la atención en Urgencias, sinó con el paciente ya ingresado.
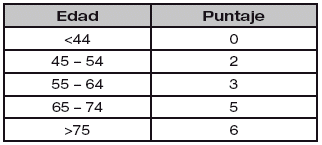
c) Puntaje por patologías crónicas
Por insuficiencias orgánicas graves: cardíaca, respiratoria, renal o hepática, o bien por inmunodeficiencia demostrada. Si existe alguna de estas condiciones, se asignan 5 puntos si se dan en un contexto no quirúrgico o posterior a una intervención de urgencia, y 2 puntos si se presentan en el postoperatorio de una intervención electiva.
a) Puntaje final
Se obtiene por la suma de los puntajes obtenidos en el Score fisiológico agudo, por edad y por patologías crónicas.

COMPLICACIONES
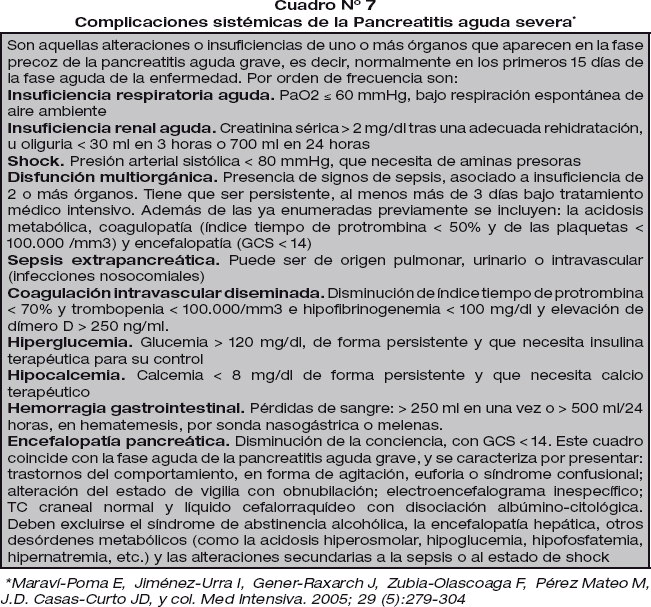
* Complicaciones sistémicas precoces: asociadas a fallo multiorgánico y al síndrome de respuesta inflamatoria sistémica.
- Shock, Insuficiencia respiratoria aguda, Encefalopatía, Insuficiencia renal aguda, complicaciones metabólicas, coagulopatías, síndrome compartimental. Las más severas suelen ser las pulmonares (derrame pleural, síndrome de distrés respiratorio agudo). Cuadro 7.
Complicaciones intermedias: debido a fenómenos locales entre la segunda y quinta semana posterior al ataque agudo.
- Colecciones líquidas agudas
- Necrosis pancreática y/o peripancreática.
- Abscesos y pseudoquistes pancreáticos y sus complicaciones ("fístulas").
Complicaciones tardías:
- Pseudoquistes
- Fístulas gastrointestinales
- Disrupción del conducto pancreático
- Hemorragia local
- Trombosis del sistema venoso
- Ascitis pancreática
- Hemorragia local
TRATAMIENTO
El tratamiento de una PA depende de la etiología y gravedad del cuadro clínico, definido por la extensión de la necrosis y las complicaciones sistémicas. Los tres objetivos más importantes son: 1. Terapia de soporte para prevención de complicaciones, 2. Terapia directa para causas específicas de pancreatitis y 3. Reconocimiento temprano y tratamiento agresivo de complicaciones.
Los pacientes estables diagnosticados de PA con criterios de "gravedad" precoces presentan una alta tasa de complicaciones. Estos pacientes con Pancreatitis aguda grave necesitan una estrecha monitorización (incluyendo PVC, diuresis, frecuencia cardíaca, frecuencia respiratoria, tensión arterial y oxigenación) y un manejo adecuado, por lo que deberán ingresar en áreas hospitalarias donde se garanticen sus necesidades de monitorización y tratamiento. En este contexto, las UCI han contribuido al mejor pronóstico de estos pacientes, donde el abordaje va a ir dirigido fundamentalmente al control del dolor, reposición de la volemia y control hemodinámico, corrección de los electrolitos y del equilibrio acido-básico y a asegurar una adecuada nutrición tras el periodo de ayuno inicial.
1. Terapia de soporte para prevención de complicaciones
Hidratación parenteral: expansión agresiva de volemia, 250-300 ml/hora (preferentemente solución salina isotónica o glucosalina) con aporte de 90-140 mEq/día las primeras 48 horas posterior a la admisión. Monitorización hemodinámica (presión arterial, FC, PVC), SaO2, turgencia de la piel, inspección de mucosas, hematocrito, diuresis, electrolitos séricos y urinario. Objetivo: lograr una PVC 8 a 12 mm Hg, PAM >65 mm Hg, una diuresis de 0,5 ml/kg/ hora y Pvc02 mayor de 70%. Existen trastornos de los electrolitos que precisan su corrección, entre ellos, la hipocalcemia que solo precisa tratamiento si hay afectación neuromuscular (tetania) y la hipomagnesemia.
Se precisa trasfusión de hematíes si el hematocrito (Hcto) está por debajo del 25% y albúmina si esta está por debajo de 2 gr/dl.
• Analgesia: Meperidina 50-100 mg vía intravenosa cada 4 horas, o en perfusión continua, a razón de 0,15-0,7 mg/kg peso/hora (diluir 200 mg en 100 ml de solución salina isotónica, ritmo de 5-25 ml/h). Precaución en ancianos, puede producir cuadro confusional. Puede combinarse con Ketorolaco vía intravenosa 30 mg cada 6-8 horas, o Metamizol 2 g intravenoso lento cada 6-8 horas. NO USAR MORFINA. El Fentanilo se utiliza en pacientes que requieren grandes dosis de Meperidina. La sedación puede utilizarse como coadyuvante de la analgesia fundamentalmente en pacientes que precisen ventilación mecánica o en el tratamiento del síndrome de abstinencia alcohólica.
• Dieta: aunque el ayuno para "reposo pancreático" se utiliza universalmente, continúa siendo que ésta acelera la recuperación en la PA. La sonda nasogástrica sólo está indicada en casos de íleo severa, distensión abdominal o emesis persistente.
La nutrición enteral deberá ser precoz por sonda naso-yeyunal (en las primeras 48-72 horas). Lo ideal es comenzar la administración por vía oral, cuando el paciente tolere, tenga hambre y no haya dolor. Ésta se inicia con 100-300 ml de líquidos claros cada 4 horas, si tolera se progresa a dieta blanda por 3 a 4 días, y luego a sólidos. El contenido calórico se aumenta desde 160 hasta 640 kcal por comida. Se sugiere iniciar el primer día con 250 kcal/día y menos de 5 g de grasa, progresando de tal forma que en el quinto día reciba 1.700 kcal/día y 35-40 g de grasa (otra recomendación es: 24,1 kcal/kg, proteínas 1,43 g/ kg).
La nutrición parenteral total en caso de contraindicación para nutrición enteral.
Oxigenación: mantener la saturación arterial de oxígeno igual o mayor a 90% a fin de de mantener la oxigenación pancreática y prevenir la necrosis. Considerar soporte ventilatorio con asistencia respiratoria mecánica y ventilación protectora del pulmón.
Antibióticoterapia: la administración profiláctica de antibióticos en PA severa en ausencia de infección específica es controversial. En caso de que exista sospecha clínica de infección, se realizará tratamiento empírico, en lo posible previa punción del tejido necrosado bajo TAC y hemocultivos para direccionar el tratamiento ulterior. Si la PCR es superior a 20 mg/dl o existe necrosis peri pancreática extensa detectada en la TAC debe considerarse la administración de tratamiento o profilaxis con un antibiótico activo frente a enterobacterias, enterococo spp. y microorganismo de la flora intestinal (Imipenem 500 mg cada 6 horas I.V.; Meropenem 500 mg cada 8 horas I.V. durante 14 días; Cefalosporinas de 3a. generación o Piperacilina-tazobactam).
2. Terapia directa para causas específicas de pancreatitis
Está orientada a cada entidad nosológica causante del cuadro clínico, por ejemplo terapia hipolipemiante en pancreatitis dislipémicas. En presencia clínica de colangitis u obstrucción biliar, detectada en la ecografía, y en los pacientes en quienes está contraindicada la colecistectomía, debe realizarse colangiopancreatografía retrógrada endoscópica (CPRE) y esfinterotomía urgente dentro de la 24-48 horas. En caso de ausencia de coledocolitiasis no hay evidencia para recomendar esfinterotomía endoscópica.
3. Reconocimiento temprano y tratamiento agresivo de las complicaciones
Realizar de forma urgente una TAC abdominal con contraste para estratificación pronóstica. La aparición de complicaciones locales como necrosis infectada, absceso, hemoperitoneo o pseudoquiste mayor de 6 cm de diámetro, requiere la realización de técnicas de drenaje percutáneo, endoscópico y/o quirúrgico.
Está indicada la necrosectomía cuando se demuestra infección de la necrosis pancreática; puede ser temprana a las 48-72 horas o tardía 12 días después del inicio. Se puede demostrar la infección por gas dentro de la colección pancreática, o por aspiración con aguja fina dirigida por ecografía o TAC. La necrosectomía temprana se asocia con mortalidad del 27-65%, y del 15% después del cierre primario y lavados postoperatorios. Actualmente se prefiere la cirugía tardía, pues en la temprana la mortalidad es 3,4 veces mayor. La necrosectomía deberá ser cuidadosa, intentando preservar el resto de la glándula, con lavado postoperatorio pero no re-laparatomías programadas.
En el absceso pancreático está indicado el drenaje quirúrgico o, cada vez más frecuente, el drenaje percutáneo con técnicas de radiología intervencionista.
El pseudoquiste pancreático representa la evolución de una PA tipo necrohemorrágica sin infección de la necrosis. Muchos se resuelven espontáneamente. Aquellos llamados pseudoquistes verdaderos (con alguna comunicación al sistema excretor pancreático) deben ser drenados ya sea percutáneamente, vía endoscópica o por vía quirúrgica realizándose un drenaje interno al estómago o al yeyuno por medio de un asa desfuncionalizada en "Y de Roux".
Existen algunos procedimientos quirúrgicos que tienen indicaciones limitadas y cuya efectividad ha sido discutida. Sin embargo, en grupos de pacientes estos procedimientos han sido de beneficio. Entre estos se cuentan: el lavado peritoneal precoz: Su utilidad se mostró en la fase precoz de la PA de curso grave, disminuyendo las complicaciones cardiovasculares y respiratorias (Distrés), sin embargo la mortalidad no ha cambiado.
El drenaje del conducto torácico tiene la misma indicación que el lavado peritoneal; también útil en la fase precoz de la P.A.
La cirugía resectiva precoz con pancreatectomía subtotal y necrosectomía es preconizada por algunos autores para modificar la evolución de la PA de curso grave, que debe estar reservada para centros de referencia dada su potencial alta morbilidad. Su indicación ha sido polémica; sin embargo, en aquellos pacientes con las formas más graves de la enfermedad (7 o más criterios de Ranson), pudieran beneficiarse de esta conducta dada su alta mortalidad aún actualmente pese a los avances en el apoyo de UCI, nutricional, etc.
Las indicaciones de cirugía en la pancreatitis aguda son las siguientes: 1) Necrosis pancreática infectada, 2) Absceso pancreático o peripancreático que no responde al tratamiento no quirúrgico mediante TAC-punción en 24-48 horas, 3) Hacer diagnóstico diferencial con otras patologías agudas que, de no ser intervenidas, supondrían la muerte del paciente (perforación de víscera hueca, isquemia mesentérica aguda, etc., y 4) cuando surgen complicaciones derivadas de la cirugía de la pancreatitis o de la evolución de la pancreatitis aguda grave que pueden tener indicación quirúrgica per se (perforación colónica, obstrucción duodenal, hemorragia masiva, etc.).
REFERENCIAS
1. James R.A. Skipworth and Stephen P. Pereira. Acute pancreatitis. Curr Opin Crit Care 2008,14:172-178
2. Banks; Freeman ML. Practice guidelines in acute pancreatitis Am J Gastroenterol. 2006, 101(10):2379-400
3. Forsmark CE, Baillie J, AGA Institute Technical Review on Acute Pancreatitis, Gastroenterology 2007; 132:2022
4. Maravi-Poma E, et al. Recomendaciones de la 7a Conferencia de Consenso de la SEMICYUC. Pancreatitis aguda grave en Medicina Intensiva. Med Intensiva. 2005; 29(5):279-304
5. Hernández-Tejedor A, Chico-Fernández M. Problemas digestivos. Pancreatis aguda grave. En: Chico-Fernández, Sanchez-Izquierdo Riera JA, Toral-Vázquez D. Guía práctica de medicina intensiva. Bogotá-Colombia. Distribuna Editorial Médica, 2007; 323-30 [ Links ]
6. Scores pronósticos y criterios diagnósticos en el paciente crítico. http://booksmedicos.blogspot.com [ Links ]
7. Hani A.,Peláez M., Alvarado J., Solano C., Suárez Y., Torres D., et al. Protocolo de manejo de pancreatitis aguda. Universitas Médica 2007; 48 (1): 8-20
8. Balthazar, EJ. CT. diagnosis and staging of acute pancreatitis. Radiol Clin North Am 1989; 27, 19-37 [ Links ]
9. García Gil D, Mensa J. Pancreatitis aguda. En: García-Gil D, Mensa J. Terapéutica Médica en Urgencias 2008-2009. Buenos Aires-Argentina. Editorial Médica Panamericana,2009; 116-8 [ Links ]
10. Ledesma-Heyer JP, Arias-Amaral J. Pancreatitis aguda. Med Int Mex 2009;25(4):285-94 [ Links ]
11. Martínez J, Llanos O. Evolución y complicaciones de la pancreatitis aguda. Bol. Esc. Med UC. 1992; 21:196-201. [ Links ]
12. Martínez J., Llanos O. Pancreatitis Aguda: tratamiento quirúrgico. Bol.Esc.Med UC. 1992; 21:210-214. [ Links ]
13. Bollen TL, van Santvoor HC, Besselink van Leeuwen MS, Horvath KD, Freeny PC and Gooszen HG, on behalf of the Dutch Acute Pancreatitis Study Group The Atlanta Classification of acute pancreatitis revisited. British Journal of Surgery 2008; 95: 6-21
14. Santhi Swaroop Vege, Sureh T Chari. Treatment of acute pancreatitis. Last literature review for version 17.1: Enero 2009.Uptodate. [ Links ]
Swaroop, VS, Chari, ST, Clain, JE. Severe acute pancreatitis. JAMA 2004, 291:2865.
15. Aranalde GI. Pancreatitis aguda. En: Bartolomesi S, Aranalde G, Keller L. Manual de Medicina Interna: cálculos, scores y abordajes. Buenos Aires-Argentina. Editorial Corpus, 2010; 183-8 [ Links ]














