Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Acta Nova
versión On-line ISSN 1683-0789
RevActaNova. v.9 n.4 Cochabamba mar. 2020
Artículo Científico
Evaluación de la adición de bacterias lipolíticas autóctonas para estimular a escala de laboratorio la biodegradación de efluentes grasos de una industria aceitera
Evaluation of the addition of automatic lipolytic bacteria to stimulate laboratory scale biodegradation of fat effluents of an oil industry
Mendoza Grájeda D.Y.1, Lopez Terrazas M.2, Montaño Suarez A.M.3
1 Laboratorio Académico y de Investigación de Ingeniería Ambiental, Facultad de Ciencias Exactas y Tecnología (FCET),
2 Laboratorio de Investigación de Microbiología Ambiental y Biotecnología (LIMAB), Facultad de Ciencias Agrícolas (FCA), (U.A.G.R.M.). Santa Cruz, Bolivia.
yerymgrajeda04 04 95@gmail.com
Recibido: 4 de febrero 2020
Aceptado: 18 de febrero 2020
Resumen: La presencia de lípidos en la composición de las aguas residuales puede alterar el correcto funcionamiento de los sistemas dispuestos para su tratamiento. En este sentido, el presente trabajo evalúa la eficiencia de 3 bacterias productoras de lipasa, en la reducción de las concentraciones de grasas/aceites presentes en las aguas residuales de la industria aceitera de donde fueron aislados. Por consiguiente, se estudió las condiciones que permitan el mejor desarrollo de la población bacteriana (antagonismo, respiración, pH y sales reguladoras de pH), además de estudiar la incidencia de diferentes concentraciones (V/V) de suspensiones de las bacterias estudiadas (1%, 2,5% y 5%), en conjunto con diferentes concentraciones de Cloruro de calcio (Cl2Ca) (0%, 1%, 2,5% y 5%). Se comprobó que los mejores resultados (34 mg/L - seguimiento propio; 18,5 mg/L - prueba por tercero) son producto del agregado del inóculo bacteriano de concentración 2,5% (V/V) en conjunto con Cl2Ca al 5% (V/V), formado por una combinación entre las bacterias sospechosas de ser: Pseudomona Sp. y Corynebacterium Sp., agregado a una muestra de efluente graso con pH 7 regulado con carbonato de sodio, en 15 días de tratamiento con aireación asistida. Se concluye que las Bacterias estudiadas evidencian un potencial promisorio para su implementación en sistemas de tratamiento de aguas residuales procedentes de la industria aceitera.
Palabras clave: efluentes grasos, tratamiento, lipasas, cloruro de calcio, aireación.
Abstract: The presence of lipids in the composition of wastewater can alter the proper functioning of the systems arranged for treatment In this sense, the present work evaluates the efficiency of 3 lipase producing bacteria, in reducing the fat / oil concentrations present in the wastewater of the oil industry from which they were isolated. Therefore, the conditions that allow the best development of the bacterial population (antagonism, respiration, pH and pH regulating salts) were studied, in addition to studying the incidence of different concentrations (V / V) of suspensions of the bacteria studied (1 %, 2.5% and 5%), together with different concentrations of calcium chloride (Cl2Ca) (0%, 1%, 2.5% and 5%). It was found that the best results (34 mg / L - own follow-up; 18.5 mg / L - test by third party) are the product of the aggregate of the bacterial inoculum of concentration 2.5% (V / V) in conjunction with C12Ca at 5 % (V / V), formed by a combination between the bacteria suspected of being Pseudomona Sp. And Corynebacterium Sp., Added to a sample of fatty effluent with pH 7 regulated with sodium carbonate, in 15 days of treatment with assisted aeration . It is concluded that the Bacteria studied show a promising potential for its implementation in wastewater treatment systems from the oil industry.
Keywords: fatty effluents, treatment, lipases, calcium chloride, aeration.
1 INTRODUCCIÓN
La conservación de recursos naturales ha cobrado gran importancia a nivel mundial, ocasionando en la sociedad la necesidad de buscar soluciones ambientalmente amigables, basadas en la máxima seguridad, el mínimo impacto ambiental y en la medida de lo posible, en la reducción de la generación de derivados, cuyo tratamiento o disposición aumenta los costos de tratamiento. Por lo expuesto, los tratamientos biológicos se han identificado como procesos capaces de cumplir los criterios mencionados, pudiendo reducir las concentraciones de contaminantes generalmente orgánicos, mediante la acción catalizadora de microorganismos.
Sin embargo, las limitaciones de los tratamientos biológicos están relacionadas con la biodegradabilidad del contaminante a tratar y la presencia de compuestos inhibitorios o tóxicos para el cultivo biológico. En este sentido, la presencia de compuestos grasos en la composición de los efluentes presenta estos efectos, dado que la estructura de dichos compuestos dificulta su degradación por microorganismos no adaptados a su presencia, sumado a que favorecen la aparición de zonas anóxicas, debido a que la oxidación de estos compuestos consumen importantes cantidades del oxígeno disuelto presente en los reactores biológicos, además de generar productos altamente tóxicos debido al proceso de peroxidación lipídica. Por otra parte, la presencia de compuestos grasos ocasiona la obstrucción de los conductos que poseen los sistemas de tratamiento y ocasiona la flotación de lodos, dificultando la deshidratación de los mismos por medios mecánicos, debido a sus propiedades tixotrópicas (Teqma, 2019).
En este sentido, se han identificado organismos capaces de aprovechar como sustratos o fuentes de energía para la realización de sus funciones vitales, las grasas y aceites presentes en los efluentes, mediante la generación de lipasa (hidrolasas de éster de glicerol, EC 3.1.1.3), enzimas que catalizan la hidrólisis de los enlaces éster carboxílico presentes en las grasas, liberando ácidos orgánicos y glicerol en el proceso. Es decir, la aplicación de estos organismos en el tratamiento de aguas residuales, aumentaría la eficiencia de la remoción de grasas y aceites en estos sistemas, buscando reducir los problemas operativos mencionados anteriormente (Aceves, A. E. & Castañeda, L.M., 2012) (Leal, Cammarota, Freire & Sant Anna, 2002).
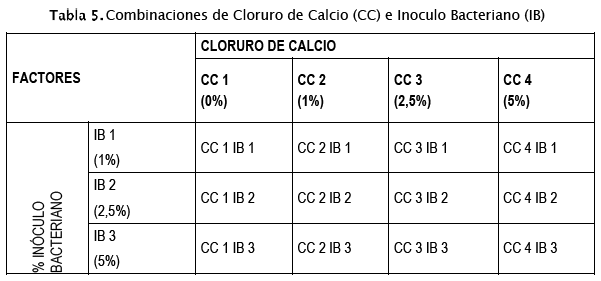
Con base a lo mencionado, se han realizado investigaciones donde se demuestra que la adición de microorganismos productores de lipasa, tienen un efecto positivo en la reducción de las concentraciones de grasas y aceites presentes en aguas residuales, esto en condiciones de pH que rondan la neutralidad (6, 7 y 8) en un rango de temperatura de 30 a 40 °C; además de incidir sobre las concentraciones de DQO y DBO. A su vez, dicha eficiencia puede verse incrementada, ante el agregado de los microorganismos en conjunto con una solución mínima de sales suplementada con cloruro de calcio, siendo la presencia de este ion metálico un estimulante para la producción de la enzima (Wakelin, N.G. & Forster, C.F., 1997) (Mongkolthanaruk, W. & Dharmsthiti, S., 2002) (González, D. et al., 2012) (Bovio, P., 2013) (Huané & Rivera, 2014) (Pazmiño, Y., 2016).
Por tanto, la utilización de microorganismos productores de lipasa capaces de reducir las concentraciones de grasas y aceites, se presenta como una alternativa de tratamiento viable, siempre que se le brinde las condiciones de crecimiento a los microorganismos de interés (Mendoza CLI citado en Huané & Rivera, 2014). En este sentido, la utilización de microorganismos autóctonos, aislados de las mismas aguas residuales donde se implementará el tratamiento enzimático, ofrece mayores ventajas que la utilización de microorganismos ajenos al medio, debido al proceso de adaptación que estos deben realizar, para con las características y condiciones especiales que los efluentes presentan (Alcarraz, M. 2014).
Considerando lo mencionado previamente, el presente trabajo busca evaluar la eficiencia de la adición de tres bacterias productoras de lipasa, en la reducción de las concentraciones de grasas y aceites presentes en las aguas residuales de la industria aceitera de donde fueron aisladas.
2 Materiales y método
2.1 Colección y mantenimiento de microorganismos evaluados
Los microorganismos estudiados en este trabajo fueron 3 bacterias aisladas a partir de muestras de aguas residuales de una industria aceitera, las cuales fueron seleccionadas por poseer actividad lipolítica. El aislamiento de los microorganismos y la identificación, tanto de las bacterias como la actividad lipolítica de las mismas, constituye la realización del trabajo de Grado - Tesis de investigación realizado por Flores, A.L., (2019).
Dada las características de las pruebas de identificación realizadas y la especificidad necesaria para determinar a qué especie pertenecen las bacterias estudiadas, Flores, A.L., (2019) presume que las bacterias de referencia pertenecen a los géneros descritos en la tabla 1.
2.2 Confirmación de actividad lipolítica
Para confirmar de manera cualitativa la actividad lipolítica de las cepas de referencia, se sembraron por duplicado en agar Tributirina, un compuesto oleoso de cadena corta (C4 < 10 átomos de carbono), dividiendo en dos el área de las placas, sembrando por estriado una mitad y formando 3 líneas paralelas en la otra. En placas diferentes, cada bacteria se sembró colocando de manera equidistante 4 discos de papel filtro estéril (diámetro 0,6 cm.) previamente sumergidos en suspensiones bacterianas con una turbidez similar al 0,5 en la escala de McFarland. Se observó el desarrollo de las bacterias y la presencia de halo de lipólisis formado a 35,5 °C en un tiempo de 24 horas.
2.3 Prueba de antagonismo
La evaluación se realizó el fin de observar si las bacterias de referencia tenían la capacidad de poder desarrollarse en un mismo medio, realizando la prueba de inhibición por sensi-discos (Pérez, R., González, T. & Muñoz, J., 2015).
En cajas Petri con agar R2A se realizaron frotis de suspensiones de las bacterias estudiadas, colocando de manera equidistante entre sí, discos de papel filtro sumergidos previamente en la suspensión de cada bacteria estudiada, luego se llevó a incubar durante 24 horas a 35,5 °C.
Se tomó como control el tamaño de las colonias en relación a un blanco, el cual fue sembrado en el mismo medio de cultivo (Agar R2A) sin la realización del frotis; y la presencia de un halo alrededor de la colonia a ser inhibida, lo que indicaría competencia o inhibición entre las bacterias sembradas. La colocación de las bacterias se realizó según lo detallado en la Tabla 2.
Según la codificación (X - Y), "X" representa el inhibidor (bacterias sembrada con el disco estéril) y "Y" representa la bacteria a ser inhibida (sembrada en frotis). Todos los tratamientos contaron con 4 reiteraciones, dando lugar a un total de 24 unidades experimentales, cada tratamiento con su respectivo par de blancos.
2.4 Prueba de respiración bacteriana
Se realizó siembra por extensión en placa, por duplicado de las diluciones 10-2 y 10-3 de las suspensiones de las bacterias de referencia (0,5 en la escala de McFarland), vertiendo 100 μl de las mismas en placas Petri con Agar R2A, para luego cubrir la muestra con una capa de agar R2A, para limitar el libre contacto de oxígeno con los microorganismos de la muestra. Pasadas 24 horas a 35,5 °C se observa el desarrollo del número de unidades formadoras de colonias (UFC), en relación al crecimiento presentado en un blanco, el cual fue sembrado mediante siembra por extensión.
2.5 Selección de compuesto regulador de pH menos agresivo
Esta operación se realizó para observar cómo se comportaban las bacterias de referencia en un medio con un pH neutro, ligeramente ácido y ligeramente básico. Además de evaluar la influencia que 3 reguladores de pH (Bicarbonato de sodio, Carbonato de sodio e Hidróxido de sodio) tendrían sobre el desarrollo de la población bacteriana (Pazmiño, Y., 2016).
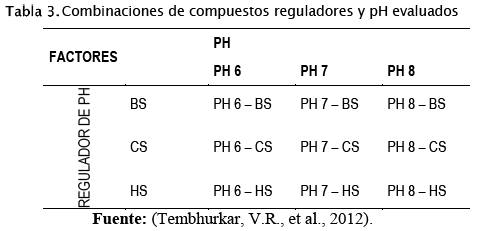
Se realizaron diluciones seriadas hasta la dilución 10-5 de las bacterias de referencia, mismas que fueron sembradas en profundidad en agar R2A, cuyo pH fue regulado a un valor de 5 con ácido clorhídrico (HCl - 0,1 N), para luego elevar este valor según lo descrito en la Tabla 3 con soluciones al 5% de Bicarbonato de sodio (BS), Carbonato de sodio (CS) e Hidróxido de sodio (HS); se llevó a incubación por 24 horas a 35,5 °C, para realizar el conteo de las unidades formadoras de colonias (UFC), pasado el tiempo de incubación.
Cada tratamiento se repitió una vez por cada bacteria, realizando la siembra de las mismas hasta la dilución 10-5 con 2 reiteraciones de cada tratamiento.
2.6 Determinación de las condiciones óptimas para actividad lipolítica
Se estimó la producción de enzimas lipasa mediante la titulación de la muestra con NaOH (0,05 N) en presencia del indicador fenolftaleína, lo que provoca el cambio de un pH neutro o ligeramente acido a uno básico (Tembhurkar, V.R., Kulkarm, M.B. & Peshwe, S.A., 2012).
En 9 ml de caldo Luria Bertani (LB) suplementado con aceite de oliva (1%) como fuente de carbono principal, medio de cultivo previamente esterilizado, se añadió 1 ml de medio mínimo mineral estéril ((KH2PO4 0.6 mg.ml-1; MgSO4 40 μg.ml-1; Na2HPO4 -1.5 mg.ml-1; FeSO4 - 4 μg.ml-1), combinación en la que se agregó los tratamientos señalados en la tabla 4. Para luego incubar las muestras durante 3 días y proceder a neutralizar la actividad enzimática de las mismas, al combinar la muestra incubada con alcohol del 96% en una relación 1:1. Posteriormente se tituló la muestra con NaOH al 0,05 N en presencia de fenolftaleína (0,5%), señalando como punto final de la reacción el viraje de color a rosado de la muestra por más de 30 segundos, midiendo el pH final después de la titulación; como segundo testigo. Todos los tratamientos se realizaron considerando 3 reiteraciones
Después de conocer el volumen de NaOH necesario para neutralizar la muestra, con los valores obtenidos de la misma (volumen y normalidad del NaOH), se procede a calcular la cantidad de enzima producida en cada unidad experimental. Definiendo una unidad de lipasa, como la cantidad de lipasa requerida para liberar una μM de ácido graso por unidad de tiempo (una hora) bajo las condiciones de ensayo.
2.7 Evaluación aplicada de la eficiencia de degradación G/A
Se evaluó si las combinaciones seleccionadas en las fases anteriores en conjunto con la aireación, tienen incidencia sobre las concentraciones de grasas y aceites (G/A) de una muestra de agua residual procedente de la industria aceitera de donde fueron aisladas las bacterias de referencia.

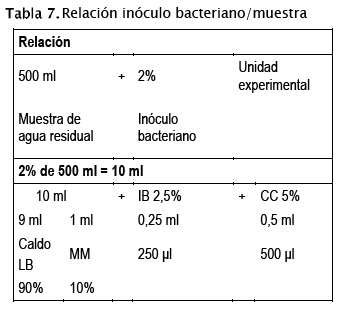
Se preparó el inóculo bacteriano con base a los mejores resultados obtenidos en el punto 2.6., siguiendo la relación descrita en la Tabla 7, incubando el preparado por 24 horas, para luego agregar dicho preparado según lo detallado en la Tabla 8.
Se tomaron en consideración 4 tratamientos, seleccionados en relación al resultado en conjunto de las pruebas mencionadas anteriormente; cada tratamiento contó con 3 duplicados, dando un total de 12 unidades experimentales, cada una con 500 ml de agua residual de industria aceitera, cuyo pH fue regulado a un valor de 7 según los resultados obtenidos en el punto 2.5.; Todas las unidades experimentales se mantuvieron a temperatura ambiente, durante un periodo de incubación de 15 días, con aireación asistida a razón de un caudal de 3 L/min, para realizar la medición de las concentraciones de grasas y aceites mediante destilación por rotavapor, luego del periodo de incubación.
Donde:
C1: Pseudomona Sp. - Corynebacterium Sp. (IB2,5%-CC5%)
C2: Pseudomona Sp. (IB2,5%-CC5%)
2.8 Evaluación de resultados
Para el análisis estadístico de las pruebas: Selección de compuesto regulador de pH menos agresivo y Determinación de las condiciones óptimas para actividad lipolítica se utilizó el diseño de bloques completamente aleatorizados con prueba Duncan para las comparaciones múltiples, luego de confirmar el normal comportamiento de los datos. Para el resto de las pruebas se realizó el análisis de varianza (ANOVA) de un factor, sometiendo los datos de dichas evaluaciones a la prueba estadística de Tukey, considerando una significativa estadística hasta el 5% de probabilidad para todas las pruebas. El análisis se realizó mediante el programa IBM SPSS Statistics 21.
3 Resultados
3.1 Confirmación de actividad lipolítica
La técnica de siembra mediante estrías pudo comprobar que las bacterias estudiadas tienen la capacidad de desarrollarse y crecer en un medio suplementado con un sustrato específico como lo es la Tributirina.
La prueba en sensi-discos señala que las bacterias del género Pseudomona Sp. sembradas en el agar Tributirina, son las que presentan la mayor diferencia de tamaño respecto a sus pares sembrados en agar R2A, siendo las bacterias del genero Bacillus Sp., aquellas cuyos datos presentan un comportamiento anormal, presentando valores negativos lo que indica que en el agar de prueba tubo un mayor crecimiento que su respectivo blanco.
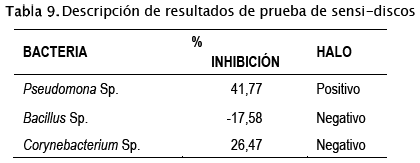
A su vez, la prueba de sensi-discos señaló que la Pseudomona Sp. es la única de las cepas estudiadas con capacidad de hidrolizar la tributirina, dado que esta bacteria fue la única que presento halo de aclaración alrededor de la colonia.
3.2 Prueba de antagonismo
La bacteria del género Corynebaterium Sp. (representada como C) es la bacteria con mayor resistencia al desarrollo de sus pares bacterianos (Pseudomona Sp. y Bacillus Sp.) con las que fue sembrada, en contraste con las bacterias del género Bacillus Sp. (representada como B) la cual es fuertemente inhibida, principalmente por la Pseudomona Sp. (representada como A).
A su vez, se observa que las bacterias de referencia tienen la capacidad de crecer en un mismo medio. Sin embargo, las combinaciones B-A (Bacillus Sp. - Pseudomona Sp.) y C-B (Corynebacterium Sp. - Bacillus Sp.) presentan halos de inhibición, característica no observada en sus contrapartes (A-B y B-C).
El tratamiento con código A-B (Pseudomona Sp. - Bacillus Sp.) resulta ser aquella con un mayor porcentaje de inhibición, comportándose de manera opuesta a su contraparte B-A (Bacillus Sp. Pseudomona Sp.), la cual presenta un porcentaje de inhibición similar a la combinación C-A (Corynebacterium Sp. Pseudomona Sp.).
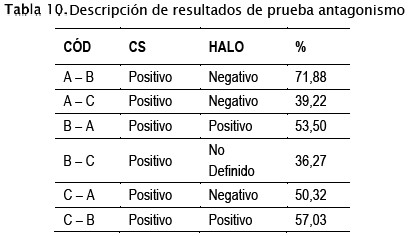
Donde:
COD: Combinación bacteriana
HALO: Halo de inhibición
CS: Crecimiento Simultaneo
%: Porcentaje de Inhibición
3.3 Prueba de respiración bacteriana
Cuantificando el crecimiento de las Unidades Formadoras de Colonias (UFC/ml) nos damos cuenta que las bacterias de referencia (Pseudomonas Sp., Bacillus Sp. y Corynebacterium Sp.) si pueden desarrollarse en un medio con poco oxígeno, aunque la falta de éste, tiene incidencia en el crecimiento de la población bacteriana.
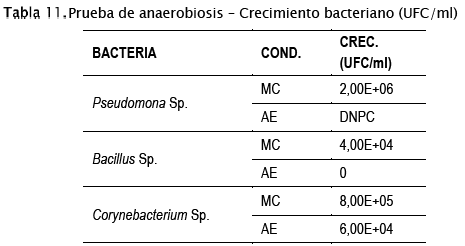
Donde:
COND: Condición
MC: Microaerobia
AE: Aerobia
CREC: Crecimiento bacteriano
En este sentido, el grado de incidencia de la presencia de oxigeno sobre las bacterias de referencia, en relación al blanco sembrado en condiciones normales, se presenta de menor a mayor grado en el siguiente orden:
![]()
3.4 Selección de compuesto regulador de pH menos agresivo
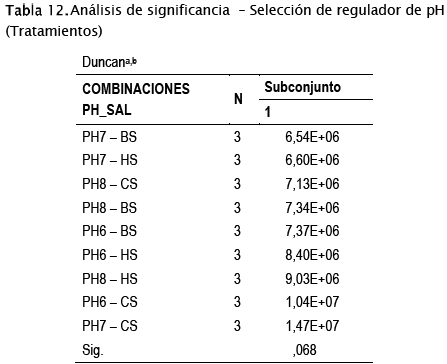
Las varianzas del crecimiento bacteriano considerando solo el efecto de los tratamientos (Tabla 12), son significativamente iguales. Sin embargo, se seleccionó al carbonato de sodio en la combinación PH7CS (pH 7 con carbonato de sodio) como el tratamiento a aplicar en la "Evaluación aplicada de la eficiencia de degradación de G/A", toda vez que dicha combinación presenta el mayor crecimiento bacteriano (UFC/ml) de las bacterias de referencia a un pH neutro, seguido del pH 6.
"Se muestran las medias de los grupos de subconjuntos homogéneos.
Basadas en las medias observadas.
El término de error es la media cuadrática
(Error) = 19862957870370,360."
a. Usa el tamaño muestral de la media armónica = 3,000
b. Alfa = 0,05.
Respecto al crecimiento bacteriano considerando los bloques, la bacteria del género Pseudomona Sp., cuya media es significativamente diferente de sus pares bacterianos, es el microorganismo con mayor crecimiento (2,49E+07 UFC/ml), siendo este mucho mayor que el crecimiento presentado por las bacterias Bacillus Sp. (5,26E+05 UFC/ml) y Corynebacterium Sp. (4,23E+05 UFC/ml) respectivamente, debiendo señalar que las medias de estas últimas no son significativamente diferentes.
3.5 Determinación de las condiciones óptimas para actividad lipolítica
La mayor producción de enzima a nivel de tratamiento proviene de la combinación IB2,5%CC5% (4,291 E-06 μM), seguido de la combinación IB1%CC2,5% (3,953 E-06 μM) y IB5%CC2,5% (3,559 E-06 μM) respectivamente, observando que el porcentaje de inoculo agregado, por sí solo no tiene gran incidencia en la producción de la lipasa, dado que las combinaciones que presentan los valores de producción más altos, presentan concentraciones diferentes, sin mantener la hegemonía de una en particular. Lo que da a entender que la producción de enzima si se ve fomentado por la presencia de iones de calcio en el medio, puesto que se observa que las combinaciones que presentan mayor producción de lipasa, son las que cuentan con mayor porcentaje de cloruro de calcio.
Por otra parte, se hace mención que se consideraron las combinaciones de Pseudomona Sp. - Corynebacterium Sp. y Bacillus Sp. - Corynebacterium Sp., toda vez que dichas combinaciones demostraron poder crecer sin inhibirse.
En este sentido, la mayor producción de enzima se observa en la combinación Pseudomona Sp. - Corynebacterium Sp. (4,901E-06 μM), seguido del bloque formado solo por la Pseudomona Sp. (3,794 E-06 μM), pudiendo afirmar que la bacteria con mayor actividad lipolítica, es la bacteria Pseudomona Sp.
Según lo expuesto previamente, se seleccionó la combinación IB2,5%CC5% (Inóculo bacteriano 2,5% y Cloruro de calcio 5%) como la combinación a ser implementada en la evaluación aplicada del tratamiento enzimático; trabajando a la par con las combinaciones bacterianas mencionadas previamente.
3.6 Evaluación aplicada de la eficiencia de degradación de grasas/aceites
Como se observa en los datos registrados de la evaluación de G/A, los tratamientos que involucran la implementación del consorcio bacteriano Pseudomona Sp. y Corynebacterium Sp. presentan concentraciones de G/A mucho menores que el tratamiento formado únicamente por la Pseudomona Sp.
En este sentido, las unidades experimentales con aireación poseen concentraciones de G/A menores que el blanco, siendo más evidente en el tratamiento P-C-CA, el cual presenta una concentración de 34 mg/l, equivalente a un 21,25% de la concentración inicial (78,75% eficiencia), mucho mayor que la combinación P-CA, la cual muestra una concentración de 124,67 mg/l, equivalente a un 22,08% de eficiencia. Por otro lado, los tratamientos sin aireación presentan concentraciones de G/A mayores al blanco; en el caso del tratamiento P-SA, casi triplica la concentración del blanco, observando una situación similar con el tratamiento P-C-SA.
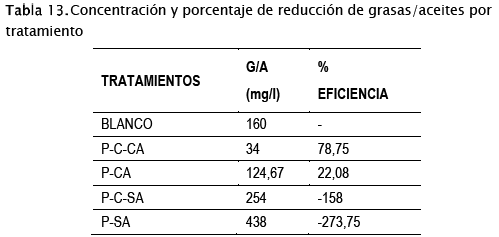
Donde:
BLANCO: Muestra sin tratamiento
P-C-CA: Pseudomona Sp. Corynebacterium Sp. Con Aireación
P-CA: Pseudomona Sp. Con Aireación
P-C-SA: Pseudomona Sp. Corynebacterium Sp. Sin Aireación
P-SA: Pseudomona Sp. Sin Aireación
G/A: Grasas y Aceites
El tratamiento de mayor eficiencia (P-C-CA) fue replicado para ser evaluado por un tercero, el cual fue la "Unidad Técnica de Apoyo a los Laboratorios - UTALAB", laboratorio que indica que las muestras presentadas poseen características señaladas en la tabla 14.
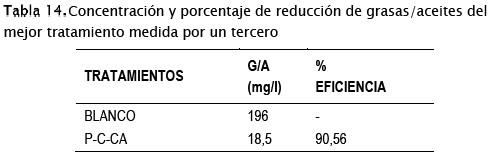
Donde:
BLANCO: Muestra sin tratamiento
P-C-CA: Pseudomona Sp. Corynebacterium Sp. Con Aireación
G/A: Grasas y Aceites
4 Discusión de resultados
4.1 Confirmación de actividad lipolítica
En lo referente a la formación de halos de degradación como prueba de la hidrólisis de tributirina (Tabla 10), el presente estudio no concuerda con lo afirmado por: Lizano, O., (2012); Antúnes, M.(2015); Alcarraz, M., (2014); Rodas, M. & Botello, S., (2016); Otalora, et al., (2000) y Pedroza, et al.,(2017), autores que señalan que pese a la tributirina no ser un medio o suplemento específico para la prueba de hidrólisis por parte de las lipasas, esta es capaz de degradarla formando halos de degradación junto a las colonias formadas, resultado no visto en la realización de las pruebas del presente estudio, salvo el caso de la Pseudomona Sp., lo que incita a intuir que las enzimas (Lipasa) producidas por estas bacterias presentan en cierto porcentaje, afinidad por los sustratos oleicos de cadena corta como la Tributirina.
Por otro lado, la presencia negativa de halos en la siembra de las bacterias del género Bacillus Sp. y Corynebacterium Sp., no significa que éstas no poseen actividad lipolítica, siendo esta una prueba no excluyente.
En lo que se refiere a la incidencia del medio en el tamaño de las colonias, se nota que en todos los casos, el porcentaje de inhibición no excede el 50% (Tabla 9); siendo la Pseudomona Sp. (41,77%) las bacterias cuyo crecimiento se vio mayor reducido, seguido del Corynebacterium Sp. (26,47%) y el Bacillus Sp. (-17,58%), quien presenta un valor negativo, bajo el entendido que en el Agar Tributirina estas presentaron un crecimiento mayor que en el agar R2A, pudiéndose entender que el sustrato oleico (Tributirina) estimula el crecimiento de las colonias de esta bacteria en particular, resultado que guarda relación con lo revisado en literatura (Pazmiño, 2016) (Rodas, M. & Botello, S., 2016) (Pedroza, et al., 2017).
4.2 Prueba de antagonismo
Si bien la técnica utilizada en este trabajo (Detección de inhibición por sensi-discos) es realizada comúnmente en ensayos inmunológicos, para determinar el efecto antagónico entre dos especies microbianas; debido a que se logra visualizar en un medio sólido la actividad productora de metabolitos tóxicos de una cepa antagónica hacia la que es sensible, esta técnica representa ser la adecuada para poder evaluar esta actividad (Pérez, R., González, T. & Muñoz, J., 2015).
Con base a lo expuesto, se observó que las bacterias de referencia pueden desarrollarse juntas, sin embargo, las combinaciones B-A y C-B, llegarían a competir por el alimento existiendo diferencia de tamaño entre las colonias evaluadas y sus respectivos blancos.
Respecto a las combinaciones A-B y B-C, no se observa la formación de halo, pero el porcentaje de inhibición del tamaño de la colonia formada por la primera combinación (A-B) es mayor al 70%, lo que indica una alta competitividad entre las bacterias; al contrario de la segunda combinación (B-C), la cual presenta la menor diferencia de tamaños entre las colonias evaluadas y sus respectivos blancos. Respecto a las combinaciones A-C y C-A, estas no presentan la formación de halo y el porcentaje de inhibición se mantiene al margen del 50% en el caso de la segunda combinación (C-A); por su parte la primera combinación (A-C) presenta el segundo porcentaje de inhibición más bajo (39,22%).
Según lo descrito anteriormente, se seleccionó para la ejecución de las pruebas de "Determinación de las condiciones óptimas para actividad lipolítica" a las combinaciones que representan a las bacterias Pseudomona Sp. en conjunto con Corynebacterium Sp. (A-C y C-A) y Bacillus Sp. en conjunto con Corynebacterium Sp. (B-C y C-B), en vista de que en la primera combinación no se observa la formación de halo de inhibición, además de presentar un crecimiento bacteriano al margen del 50% en relación al blanco, en el caso de la composición C-A; y la segunda combinación, debido a que el porcentaje de inhibición de la composición C-B se mantiene al 57% pese a observar la presencia de un halo de inhibición, además de que la composición B-C es la que posee el menor porcentaje de inhibición.
Respecto a la composición de los consorcios bacterianos, autores como Otalora, et al., (2000) y González, D. et al. (2012), muestran en sus trabajos inóculos formados por bacterias del genero Pseudomonas Sp. y Bacillus Sp. señalando que dichas combinaciones presentan eficiencias de degradación de G/A muy aceptables. Sin embargo, los resultados de la prueba de antagonismo realizados en este trabajo no viabilizan la formación de un inóculo bacteriano formado por estas bacterias, debido a que la bacteria Pseudomona Sp. del presente estudio resulta agresiva al crecimiento de la bacteria Bacillus Sp.
4.3 Prueba de respiración bacteriana
De las pruebas de respiración microaerobia, se concluyendo que las bacterias del género Pseudomonas Sp., son las más resistentes a la falta de oxígeno en relación a sus pares bacterianos. Presentando una resistencia mayor a la presentada por el Bacillus Sp. y el Corynebacterium Sp., microorganismos que según literatura deberían poseer mayor resistencia que la Pseudomona Sp. a la falta de oxígeno.
4.4 Selección de compuesto regulador de pH menos agresivo
Respecto a la preparación del agar R2A, los valores de pH inicial del medio, el volumen de ácido clorhídrico (HCl) y el pH del medio posterior a la titulación con ácido, los pH de prueba (6,7 y 8) también presentan un comportamiento normal.
Con base a las pruebas realizadas, se señala al bicarbonato de sodio como una sal agresiva sobre el crecimiento de las bacterias de referencia, resultado opuesto a lo observado por Pazmiño, Y., (2016), autor que indica que esta sal es el compuesto menos agresivo para el desarrollo de las bacterias lipolíticas, en relación al carbonato de sodio, compuesto que si inhibió el crecimiento de las bacterias lipolíticas evaluadas por este autor.
Respecto a la influencia del hidróxido de sodio, el efecto de este compuesto a un pH 8 (PH8HS) es el menor comparado con los crecimientos dados en los tratamientos PH8CS y PH8BS, lo que puede deberse al volumen de compuesto utilizado al momento de regular el pH del medio donde se efectuó la siembra, puesto que dicho volumen fue de 0,56 ml mientras que en los tratamientos PH8CS y PH8BS, fue de 1,71 ml y 9,06 ml respectivamente, pudiendo notar que a pesar de lo afirmado por Pazmiño, Y., (2016), el bicarbonato de sodio en volúmenes altos inhibe el crecimiento de las bacterias lipolíticas en un grado mayor que los otros reguladores evaluados, a pesar de su agresividad (hidróxido de sodio).
4.5 Determinación de las condiciones óptimas para actividad lipolítica
Respecto a la concentración de inoculo bacteriano, esta no presenta algún patrón de significancia sobre la producción de lipasa, ya que los tratamientos de mayor producción no abarcan una sola de las concentraciones evaluadas (1%, 2,5% y 5%).
Las pruebas de producción de enzima, demuestran que la presencia del ion calcio (Ca+2), estimula la producción de lipasa, toda vez que los tratamientos IB5%CC0%, IB1%CCO% y IB2,5%CC0%, donde no se añadió cloruro de calcio presentan los porcentajes de producción más bajos (32,6%, 39,5% y 44,2% respectivamente) en comparación a los tratamientos donde se añadió la sal en cuestión, conociendo que el tratamiento IB2,5%CC5% (4,3 E-06) es la combinación más eficiente..
En referencia a los resultados observados, autores como Syed, M.N., et al., (2010), Khan, M. & Jithesh, K., (2012), Zouaoui y Bouziane (2012), Matsumae, H. & Shibatani, T., (2017), indican que la actividad enzimática de la lipasa aumenta en presencia de iones de calcio. Por lo dicho, Rasmey, et al., (2017) menciona que el efecto de iones metálicos sobre la actividad de la enzima, puede deberse a un cambio en la solubilidad y el comportamiento de los ácidos grasos ionizados en las interfaces, o el cambio en la propiedades catalíticas de la propia enzima.
Valorando las consideraciones anteriores es que Mongkolthanaruk, W. & Dharmsthiti, S., (2002), lograron mejorar el rendimiento de su inoculo bacteriano (Pseudomonas aeruginosa LP 602, Bacillus sp. B 304 y Acinetobacter calcoaceticus LP 009), reduciendo así el tiempo de tratamiento de sus muestras de aguas residuales ricas en lípidos a 12 días bajo condiciones aerobias, con solo incrementar la composición de algunas sales minerales en una mezcla a la que llamó solución basal de sales.
Otro factor importante a considerar en la producción de enzimas, es la cantidad de inóculo necesaria para lograr una producción óptima, de modo que ésta no se vea afectada por factores presentes en el medio, tales como: concentraciones elevadas de compuestos lipídicos (saturan sitio activo de la enzima) o la presencia de metales pesados o detergentes bacterianos (inhiben o eliminan tanto a la enzima como a los microorganismos productores).
Dando lectura a Huané & Rivera (2014), determinaron que en relación a la concentración o cantidad de inóculo que se emplea, se tiene resultados similares para la actividad de la enzima; declarando que dicho suceso puede deberse al rápido consumo de los nutrientes por parte de un inoculo de mayor concentración bacteriana, lo que acelera la llegada de la fase de muerte bacteriana y por consiguiente la disminución de la actividad enzimática, al contrario de un inoculo de baja concentración, el cual mantiene un crecimiento bacteriano por un periodo de tiempo más largo.
4.6 Evaluación aplicada de la eficiencia de degradación de grasas/aceites
De las lecturas de pH realizadas a las muestras después del periodo de tratamiento, se observa que las combinaciones formadas por el consorcio Pseudomona Sp. Corynebacterium Sp. (P-C-AI y P-C-AN) presentan un aumento en el pH desde el neutro hasta 8 ±03, independientemente de que se hubiera añadido aireación a la muestra, manteniéndose constante el pH de los tratamientos que solo trabajan con la bacteria Pseudomona Sp. (P-AI y P-AN); por lo que se deduce que las muestras donde se agregaron los consorcios (P-C-AI y P-C-AN) presentan mayor concentración de ácidos grasos en relación a los tratamientos donde solo trabaja la Pseudomona Sp.
Respecto a los tratamientos que sufren un aumento de las concentraciones de G/A, Otalora, et al., (2000), autor que evaluó la eficiencia de un consorcio conformado por 6 cepas bacterianas, observó resultados positivos a 8 y 15 días de tratamiento, mientras que al día 30 observó un incremento en las concentraciones de G/A.
En este sentido, se puede atribuir este efecto a la síntesis de triglicéridos a partir de la materia orgánica o ácidos grasos por parte de la lipasa, una vez que los microorganismos degradan las G/A libres que se encuentran en el medio; esto gracias a la capacidad de la enzima de poder catalizar reacciones de transesterificación, reacción de sintetiza triglicéridos a partir de ácidos grasos o materia orgánica.
Por otro lado, González, D. et al. (2012), demostró que la utilización de un consorcio bacteriano fue efectivo en eliminar el 90 % del volumen de residuos grasos y olores desagradables de trampas de grasa; eficiencias cercana a las obtenidas por el tratamiento P-C-CA (78,75% de degradación), el cual presenta una concentración de grasas/aceites de 34 mg/l sin presentar olores desagradables.
Por tanto, basado en González, D. et al. (2012), se reafirma la idea de que la aireación favorece la degradación de las grasas y aceites en la muestras de agua, a la par que facilita la eliminación de malos olores, mismos que fueron advertidos en los tratamientos sin aireación.
Considerando la competitividad entre bacterias, por el sustrato o los recursos necesarios para la realización de sus funciones vitales, Fadile, A., et al., (2011), observó que microorganismos adaptados a las condiciones de las aguas residuales permitieron una tasa de reducción de 84.28% y 93.3% de las concentraciones de DQO y G/A respectivamente, contra eficiencias de 51.88% y 66.6%, obtenidas por un consorcio no adaptado; revelando la importancia de trabajar con un consorcio bacteriano adaptado, puesto que su implementación en las aguas residuales procedentes de restaurantes dio resultados satisfactorios, registrando una eliminación del 83,3% de la DQO y del 81% de las grasas/aceites.
5 Conclusión
La investigación logró determinar que la implementación de bacterias autóctonas, como lo son las bacterias de referencia del presente estudio (Pseudomona Sp Bacillus Sp. Corynebacterium Sp), como tratamiento en la degradación de G/A, presenta eficiencias positivas sobre la degradación de estos compuestos presentes en las unidades experimentales evaluadas. Demostrando que la bacteria que posee mayor actividad enzimática (lipolítica) es la P. aeruginosa, seguida del B. coagulans y el C. aquaticum.
Por lo descrito, las pruebas realizadas en el presente trabajo concluyen lo siguiente:
Se evidenció que las bacterias de referencia se desarrollan mejor a un pH de 7, siendo el carbonato de sodio el regulador de pH menos agresivo al crecimiento bacteriano, toda vez que la P. aeruginosa es la bacteria que presenta mayor resistencia a dicho compuesto, seguido del B. coagulans y el C. aquaticum; respecto a la incidencia de la falta de oxígeno sobre el desarrollo de la población bacteriana, este factor incide en mayor porcentaje sobre el B. coagulans (99,71%), seguido del C. aquaticum (98,43%) y la P. aeruginosa (66,67%). Por su parte, el agar tributirina incide en cierto porcentaje en el crecimiento de las bacterias estudiadas, a excepción del B. coagulans cuyo crecimiento se ve favorecido por la presencia del sustrato tributirina; y la prueba de antagonismo señala que la formación de un consorcio bacteriano solo es posible ante la combinación de P. aeruginosa en conjunto con C. aquaticum y B. coagulans en conjunto con el C. aquaticum, debido a que la P. aeruginosa inhibe el crecimiento del Bacillus.
La actividad enzimática que muestran las bacterias de referencia y las combinaciones de estas (P. aeruginosa - C. aquaticum y B. coagulans - C. aquaticum), se ve estimulada ante la presencia de iones de calcio (Ca2+), observando que la combinación IB2,5%CC5% es el tratamiento que favorece en mayor medida la producción de enzima por parte del consorcio P. aeruginosa -C. aquaticum (4,901E-06 μM) y la de la bacteria P. aeruginosa (3,794E-06 μM), siendo estas las combinaciones con mayor actividad enzimática, tras 72 horas de incubación.
El consorcio P. aeruginosa - C. aquaticum en conjunto con el tratamiento IB2,5%CC5%, demostró ser la combinación de mayor rendimiento respecto a la degradación de las grasas/aceites, disminuyendo la presencia de estos compuestos de una concentración de 160 mg/l a 34 mg/l tras 15 días de tratamiento en condiciones aerobias; resultado que exhibe gran diferencia respecto a la eficiencia presentada por la bacteria P. aeruginosa (124,67 mg/1) implementada en las mismas condiciones.
6 Recomendaciones
Diseñar un sistema de tratamiento adecuado a las necesidades de las bacterias estudiadas.
Evaluar la eficiencia de las bacterias de referencia probando cambiar las concentraciones y/o composición del medio mineral utilizado en este trabajo.
Evaluar la implementación conjunta de las combinaciones propuestas en este trabajo, con sales de cobre en el tratamiento de efluentes grasos, toda vez que se observa que esta sal no reacciona con compuestos lipídicos favoreciendo la precipitación de la materia suspendida o disuelta en el agua.
Referencias Bibliográficas
[1] Aceves, A. E. & Castañeda, L.M., (2012). Producción biotecnológica de lipasas microbianas, una alternativa sostenible para la utilización de residuos agroindustriales. Revista de la Facultad De Química Farmacéutica - Vitae, 19(3), 244-247. [ Links ]
[2] Alcarraz, M. (2014). Evaluación de la actividad proteolítica y lipolítica de cepas para el tratamiento de efluentes de curtiembre. Revista de la Facultad de Ingeniería Industrial. 17(1), 65-70. [ Links ]
[3] Antúnes, M. (2015). Contribución al estudio del sistema de Lipasas de Trichoderma harzianum (Memoria presentada para optar al grado de Doctor en Microbiología y Genética), Universidad de Salamanca, España. [ Links ]
[4] Bovio, P. (2013). Efecto del agregado de suplementos enzimáticos en la comunidad microbiana de reactores metanogénicos de tratamiento de efluentes de industria láctea (Tesis de Grado de la Licenciatura en Bioquímica). Universidad de la Republica, Uruguay. [ Links ]
[5] Fadile, A., Zahra, F., Hassani, Aissam, H., Merzouki, M. & Benlemlih, M. (2011). Aerobic treatment of lipid-rich wastewater by a bacterial consortium, African Journal of Microbiology Research, 5(30), 5333-5342, Doi: 10.5897/AJMR11.700. [ Links ]
[6] Flores, A.L. (2019). Aislamiento e identificación de microorganismos con actividad lipolítica en aguas residuales de una industria aceitera (Tesis de Grado para optar al título de Ingeniera Ambiental). Universidad Autónoma Gabriel René Moreno (U.A.G.R.M.), Santa cruz – Bolivia.
[7] González, D., Amaíz, L., Medina, L., Vargas, R., Izzeddin, N. & Valbuena, O. (2012). Biodegradación de residuo graso industrial empleando bacterias endógenas. Revista Latinoamericana de Biotecnología Ambiental y Algal, 3(2), 105-118. [ Links ]
[8] Huané, J. & Rivera, R. (2014). Evaluación de la adición de un inóculo para estimular a escala de laboratorio la biodegradación de efluentes grasos (Tesis para optar al título profesional de Químico Farmacéutico). Universidad Nacional Mayor de San Marcos, Perú. [ Links ]
[9] Khan, M. & Jithesh, K., (2012). Expresión y purificación de la lipasa estable a los disolventes orgánicos de la biblioteca metagenómica del suelo. World J Microbiol Biotechnology, 28(6), 2417–2424,DOI: doi.org/10.1007/s11274-012-1051-0
[10] Leal, Cammarota, Freire & Sant Anna Jr. (2002). Enzimas hidrolíticas como coajuvantes en el tratamiento anaeróbico de las aguas residuales de leche. Revista Brasileña de Ingeniería Química, 19(2), 1678-4383.
[11] Lizano, O. (2012). Caracterización Bioquímica de la actividad lipolítica de Pseudomonas Atlántica aislada de la Bahía de Paracas. (Tesis para optar al título profesional de Químico Farmacéutico). Universidad Nacional Mayor de San Marcos, Perú. [ Links ]
[12] Matsumae, H. & Shibatani, T., (2017). Purificación y caracterización de la lipasa de Serratia marcescens Sr41 8000 responsable de la hidrólisis asimétrica de los ésteres del ácido 3-fenilglicídico. Revista de Fermentación y Bioingeniería – El SEVIER, 77(2), 152-158. DOI: doi.org/10.1016/0922-338X(94)90315-8.
[13] Mongkolthanaruk, W. & Dharmsthiti, S. (2002). Biodegradación de aguas residuales ricas en lípidos por un consorcio bacteriano mixto. Revista de Tecnología Bioambiental – EL SEVIER, 50(2), 101-105.
[14] Otalora, M.F., Peña, J. L., Martínez, M. M. & Varela, A. (2000). Evaluación de la capacidad degradadora de aceite por bacterias lipolíticas en el lodo residual de la extracción de aceite de palma. Palmas, 21(1), 248-292. [ Links ]
[15] Pazmiño, Y. (2016). Evaluación de la eficiencia de las bacterias lipolíticas de rumen de vaca para la degradación de aguas residuales con grasas y aceites (Trabajo de titulación para optar al grado académico de Ingeniera en Biotecnología Ambiental). Escuela Superior Politécnica de Chimborazo, Ecuador. [ Links ]
[16] Pedroza, C.J., Romero, M. & Orduíz, S. (2017). Actividad lipolítica de Microorganismos aislados de aguas Residuales contaminadas con grasas, Revista de Biotecnología en el Sector Agropecuario y Agroindustrial, 15(1), 36-44. Doi: dx.doi.org/10.18684/BSAA(15)36-44. [ Links ]
[17] Pérez, R., González, T. & Muñoz, J. (2015). Antagonismo microbiano asociado a cepas bacterianas provenientes de jitomate (Lycopersicum esculentum Mill) y maíz (Zea Mays). Revista Iberoamericana de Ciencias, 1(3), 54-60. [ Links ]
[18] Rasmey, A.H., Aboseidah, A., Gaber, S. & Mahran, F. (2017). Characterization and optimization of lipase activity produced by Pseudomonas monteilli 2403-KY120354 isolated from ground beef. African Journal of Biotechnology, 16(2), 96-105. Doi: 10.5897/AJB2016.15820, [ Links ]
[19] Rodas, M. & Botello, S. (2016). Actividad hidrolítica de aislados bacterianos con potencial aplicación en el tratamiento de efluentes de frigorífico. Revista colombiana de ciencia animal, 8(1), 37-43. [ Links ]
[20] Syed, M.N., Iqbal, S., Bano, S., Khan, A.B., Ali-ul-Qader, & Azhar, A., (2010). Purification and characterization of 60 kD lipase linked with chaperonin from Pseudomonas aeruginosa BN-1. African Journal of Biotechnology, 9(45), 7724-7732. DOI: 10.5897/AJB10.369.
[21] Tembhurkar, V.R., Kulkarni, M.B. & Peshwe, S.A. (2012). Optimization of Lipase Production by Pseudomonas spp. in submerged batch process in shake flask culture. Science Research Reporter, 2(1), 46-50. [ Links ]
[22] Teqma – Tecnologías y equipos para el medio ambiente (febrero, 2019). La importancia de la separación de aceites y grasas en el tratamiento del agua residual urbana. Recuperado de https://www.iagua.es/noticias/teqma/importancia-separacion-aceites-y-grasas-tratamiento-agua-residual-urbana
[23] Wakelin, N.G. & Forster, C.F. (1997). Investigación sobre la eliminación microbiana de grasas, aceites y grasas. Revista de Tecnología Bioambiental – EL SEVIER, 59(1), 37-43.
[24] Zouaoui, B. & Bouziane, A., (2012). Production, optimization and characterization of the lipase from Pseudomonas aeruginosa. Romanian Biotechnological Letters, 17(2), 7187- 7193. [ Links ]