Cuadernos Hospital de Clínicas
versión impresa ISSN 1562-6776
Cuad. - Hosp. Clín. vol.60 no.Especial La Paz 2019
CASOS CLÍNICOS
Aplasia pura de serie roja adquirida y enfermedad renal crónica en
terapia de sustitución renal tipo hemodiálisis
Acquired pure aplasia of red cells and chronic kidney disease in renal
replacement therapy type hemodialysis
Guzmán-Mendoza M1, Flores-A. M2
1 Profesora de pre y postgrado de la Facultad de Medicina de la Universidad Mayor de San Andrés. Especialista
en Hematología. Hospital de Clínicas Universitario
2 Especialista en Medicina Interna. Hospital Municipal Cotahuma.
Autor para correspondencia: Dra. Monica Guzmán Mendoza. Dirección: Av. Saavedra, Nro. 2245, zona Miraflores.
La Paz-Bolivia. Teléfono: (591) 76204452. E-mail: mguzman43@yahoo.com
Resumen
La aplasia pura de serie roja (APSR) adquirida es un trastorno hematopoyético poco frecuente caracterizado por anemia normocítica y normocrómica, reticulocitopenia y ausencia de precursores eritroides en la médula ósea, frecuencia que ha ido incrementando en pacientes con enfermedad renal crónica. Presentamos el caso de un varón de 38 años de edad, con hipertensión arterial sistèmica, en terapia hemodialítica. En su evolución cursa con anemia aguda, tras protocolo de estudio se objetivó una aplasia pura de células eritroides por anticuerpos anti eritropoyetina, el paciente recibió bolos de ciclofosfamida, quimioprofilaxis, terapia dialitica, se suspendió la eritropoyetina, presentando buena evolución, efectuándose posteriormente el trasplante renal.
Palabras clave. Aplasia pura de serie roja, enfermedad renal crónica, hemodiálisis, eritropoyetina, anemia.
Abstract
Acquired pure red cells aplasia (PRCA) is a rare hematopoietic disorder characterized by normocytic and normochromic anemia, reticulocytopenia and absence of erythroid precursors in bone marrow, frequency that has been increasing in patients with chronic kidney disease. We present the case of a 38-year-old man with systemic hypertension in hemodialysis therapy. During the course of the disease, acute anemia was observed. After a study protocol, pure erythroid cell aplasia was detected by anti-erythropoietin antibodies, the patient received boluses of cyclophosphamide, chemoprophylaxis, dialysis therapy, erythropoietin was suspended, with favorable evolution. Subsequently, the kidney transplant.
Keywords. Pure aplasia of red cells, chronic kidney disease, hemodialysis, erythropoietin, anemia.
INTRODUCCIÓN
La anemia, que resulta principalmente de la disminución de la producción de eritropoyetina (EPO) por el riñón, es una complicación común y debilitante de la enfermedad renal crónica (ERC). La eritropoyetina recombinante humana (rHuEFO) se constituye en tratamiento a largo plazo de estos pacientes para mantener valores óptimos de hemoglobina (Hb) y para minimizar el requerimiento de soporte transfusional.1 La APSR adquirida es una complicación rara de la terapia con eritropoyetina debida al desarrollo de anticuerpos anti-eritropoyetina (anti-EPOabs).
Esta complicación se ha descrito con más frecuencia en países europeos, principalmente Reino Unido, España, Francia y Canadá2. Presentamos a un paciente con enfermedad renal crónica en programa de hemodiálisis que desarrolló APSR adquirida.
CASO CLÍNICO
Varón de 38 años de edad, residente de La Paz, con antecedente de hipertensión arterial desde sus 33 años, tratado con enalapril, abandona terapia cinco meses previos a la consulta, ingresa al servicio de nefrología del Hospital de Clínicas Universitario de La Paz por cuadro clínico de cuatro meses caracterizado por dolor lumbar persistente, opresivo, no irradiado. Al examen físico de ingreso destacó franca palidez mucocutánea, signos vitales: PA 120/70mmHg, FR36/min, FC 88/min, T° 36°C. Edema bípalpebral bilateral. Pulmonar: murmullo vesicular disminuido subescapular izquierdo. Ruidos cardíacos rítmicos, intensidad incrementada. Abdomen con ausencia de visceromegalias. Edema en miembros inferiores simétrico, blando, blanco. En la analítica de ingreso: Hb 9.7g%, Ht 30%, normocítica, normocrómica, GB 7100/ mm3, linfocitos 23%, segmentados 72%, plaquetas 360000/mm3, creatinina 8.9mg%, urea 163.4mg%, BUN 76.3mg%, colesterol total 224mg%, HDLc 52mg%, LDL 139mg%, triglicéridos 227mg%, glícemia 99mg%, calcemia 7.5mg%, fosfatemia 6mg%; examen de orina con proteinuria, glucosuria, hematuria, cilindros granulosos 0-1 /cm; proteinuria de 24H en 1.9g/1900mL; ecografía renal: RD 106x47mm, R1 89x49mm, bordes irregulares, ambos con parénquíma de ecogenicidad incrementada, pirámides hípoecoicas. Tras su evaluación se define ingreso a hemodiálisis por catéter doble lumen, se continúa terapia con amlodipino 10mg/d, rosuvastatína 10mg/d, carbonato de calcio 500mg c/12h, erítropoyetina recombínante humana alfa subcutánea 4000UI 2 dosis/sem, complejo B 1 comp/d, ácido fólico 5mg/d; dado de alta a los 11 días, posteriormente evaluado en el programa de trasplante renal. Luego de seis meses se registra declinación progresiva de las cifras de Hb y Ht, llegando a valores de 2.2g% y 9% respectivamente, por lo cual se le transfunden dos paquetes globulares, evoluciona con dolor abdominal, astenia, adinamia y se decide su internación en nefrología, se descarta sangrado visceral o cutáneo. Recibió además cargas de hierro, sin mayores cambios en su evolución, por lo que se le administró dos unidades de glóbulos rojos lavados con filtro leucocitario. Valorado por hematología, se solicitó frotis sanguíneo que mostró datos parciales de hemolisis, Ht 15%, Hb 4.8g%, leucopenia con diferencial normal, hiperplaquetosis), T Coombs directo (resultado positivo ++), reticulocitos (resultado 1%), se plantea anemia hemolítica inmunomediada se inició dexametasona 4mg c/8h, 3 dosis, presentó mejoría clínica, se modificó a prednisona 50mg/d, eritropoyetina alfa 10 000UI SC 2 dosis/sem, último control Hb 8g%, Ht 24%, dado de alta a las 5 semanas. Luego de un mes, reinternado por nueva caída de cifras de Hb (3.5g%) y Ht (11 %), se le realiza PAMO que mostró celularidad normal y <5% de eritroblastos; IgG e IgM para Parvovirus no reactivo; perfil inmunológico negativo; hierro sérico 271ug/dL, ferritina 4264ng/mL, capacidad total de fijación de hierro de 369ug/dL. Tras junta médica se define aplasia pura de células eritroides por anticuerpos anti eritropoyetina, por lo que se decide: suspensión de eritropoyetina, bolos de ciclofosfamida, quimioprofilaxis (INH, aciclovir, cotrimoxazol), prednisona, transfusión de una unidad de glóbulos rojos lavados. La evolución fue favorable, dado de alta a las 3 semanas. Posterior a cinco meses se efectivizó trasplante renal de donante vivo.

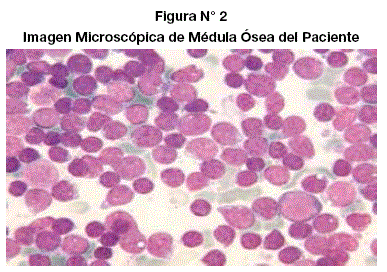
DISCUSIÓN
La APSR se describió por primera vez por Kaznelson en 1922. Puede ser primaria (congènita o anemia de Diamond Blackfan) o adquirida. Es un trastorno raro que se caracteriza principalmente por anemia normocítica normocrómica, reticulocitopenia y una ausencia casi completa de precursores de glóbulos rojos en la médula ósea, pero granulopoyesis y megacariopoyesis esencialmente normales.3
La APSR adquirida puede aparecer como una enfermedad primaria sin ninguna otra enfermedad (APSR idiopàtica) o secundaria a timoma, enfermedades hematológicas malignas, infección viral o bacteriana, enfermedades autoinmunes, embarazo, enfermedad neoplásica, hematopoyética incompatible con grupo sanguíneo ABO Trasplante de células madre y exposición a diversos fármacos o productos químicos, y asociado a anticuerpos antí-erítropoyetina.4
La APSR adquirida en pacientes tratados con rHuEPO, un agente estimulante de la eritropoyesis (AEE), fue descrita primero en 1990, diez años después de su uso como agente terapéutico. Su incidencia se estima en 0.02-0.03 por 10 000 paciente/año1, y se presenta principalmente en pacientes con enfermedad renal quienes reciben eritropoyetina a largo plazo, para mantener niveles óptimos de hemoglobina, minimizar los requisitos de transfusión, y propiciar el trasplante. Según el Ministerio de Salud de BoTívía este bíofármaco está Indicado cuando el valor de hemoglobina (Hb) se encuentra por debajo de 10g/dL5, por lo que el paciente recibió esta terapia desde sus primeras sesiones de hemodiálisis.
En nuestro paciente, se consideraron los siguientes criterios diagnósticos para APSR adquirida secundaria a anti-EPOabs: 1) caída en recuento de glóbulos rojos en aproximadamente 1%, 2) recuento de reticulocitos por debajo o igual a 1%, 3) falta de alteración sustancial en leucocitos y plaquetas, 4) celularídad normal de médula ósea, menos de 1 % de eritroblastos (hasta 5%), 5) células mieloides y megacariocitos normales. Además, cumplía con el antecedente de terapia con eritropoyetina durante al menos tres semanas y requerimiento de al menos una unidad de paquete globular/semana para mantener el nivel de Hb estable. No contamos con RIPA (Radio Inmuno Precipitation Assay) para anti-EPOabs en el país. Se realizó previamente el diagnóstico diferencial de esta entidad6, con resultados negativos.
Bennett CL et al informaron de 1998 a 2004 que casi 200 personas tratadas con epoetina alfa con enfermedad renal crónica desarrollaron anticuerpos contra la epoetina, lo que dio como resultado una APSR. Llegaron a la conclusión de que entre los pacientes con enfermedad renal crónica con APSR asociada a la epoetina, la discontinuación de la epoetina y la terapia inmunosupresora o el trasplante renal son necesarios para la recuperación hematológica.7 Es así que en el presente caso se suspendió EPO y se inicióterapia inmunosupresora, con corticoides y ciclofosfamida, con buena evolución. El cese de la terapia con eritropoyetina sola sin terapia inmunosupresora no revierte la APSR.9
Por otro lado, se ha señalado que una serie de factores fisiopatológicos potenciales, que incluyen la concentración de Hb, otros efectos del tratamiento con AEE, el aumento de la presión arterial y la hiporrespuesta a la AEE, pueden influir en el riesgo cardiovascular durante el tratamiento con AEE en pacientes con ERC.S Por lo que el manejo con los pacientes debe contemplar a cardiología, como fue en el presente caso.
Se han planteado EPO biosimilares, la Epoetin theta es un análogo de epoetin beta, que fue aprobado como creador por la Agencia Europea de Medicina en 2009. Recientemente, también se ha informado un caso de APSR con esta molécula. Los datos de un ensayo clínico que administró epoetin zeta por vía subcutánea a 230 pacientes con ERG no informaron casos de Ac-antíepoétína o APSR.113
Se indica que posterior a la negativización de Ac-antiEPO si es necesario se debe reiniciar la terapia rHuEPO. Un reporte de caso describe a un paciente de hemodiálisis con APSR asociada a Eprex® cuyos anticuerpos de EPO se volvieron índetectables después de la terapia con corticosteroides y que posteriormente respondieron a una recarga con darbepoetin.11
Con un aumento en Ta administración de rHuEPO, especialmente para el tratamiento de la anemia en pacientes con ERC, y en años recientes en pacientes con diversas enfermedades malignas, así como anemia debida a infección por VIH, el número de casos de APSR debido a anticuerpos contra rHuEPO, está aumentando rápidamente.12 Según los datos proporcionados por el laboratorio productor de EPO alfa, a fecha de 31 de diciembre de 2002, el número de casos de APSR asociada al tratamiento con EPO alfa era de 224, con un incremento de la tasa de nuevos casos. Hasta ahora, como factores inmunogénicos se han descrito: seroalbúmina humana en la formulación preparada, la administración subcutánea, y problemas con el almacenaje y la manipulación.13
Por otro lado, otro fenómeno sorprendente que se ha observado regularmente en pacientes con ERC y APSR es un aumento marcado y rápido de la saturación de transferrina, hierro sérico y los niveles de ferritina13, datos que son congruentes con el caso clínico del paciente, incrementándose el hierro sérico en un 1.8 veces y la ferritina en un 11.7 veces.
Por lo tanto, se concluye que debe realizarse una pesquisa intencionada de esta entidad en pacientes con enfermedad renal crónica y anemia, cuya evolución cumpla los criterios antes señalados, evaluándolos de forma multldisciptínaria.
REFERENCIAS
1. Senanayake HMS, Thirumavalavan K, Gunasekara MN, Ratnamalala V. Acquired pure red cell aplasia due to anti-erythropoietin antibodies in a patient with end stage chronic kidney disease. Ceylon Medical Journal 2013;58:86-88. [ Links ]
2. Bennett CL, Luminari S, Nissenson AR, Tallman MS, Klinge SA, Kim B et al. Pure Red-Cell Aplasia and Epoetin Therapy. N Engl J Med 2004;351:1403-8. [ Links ]
3. L.-C. Lim. Acquired red cell aplasia in association with the use of recombinant erythropoietin in chronic renal failure. Hematology 2005; 10(3): 255-259. [ Links ]
4. Rong Fu, Tian Zhang, Bingnan Liu, Jia Song, Guojin Wang, Lijuan Li. The clinical characteristics and therapy response of patients with acquired pure red cell aplasia. Hematology 2018; 23: 639-645. [ Links ]
5. Ministerio de salud y deportes. Programa nacional de salud renal. Normas de hemodiálisis. Bolivia. 2011:55-57. [ Links ]
6. Polanco-Flores NA, Soto-Abraham MV, Izaguirre-Ávila R, Rodríguez-Castellanos FE. Aplasia pura de serie roja adquirida en trasplantado renal: Infección por parvovirus B19 frente a timoma. NefroPlus 2013;5(1):19-24. [ Links ]
7. Bennett CL, Cournoyer D, Carson KR, Rossert J, Luminar! S, Evens AM et al. Long-term outcome of individuals with pure red cell aplasia and antierythropoietin antibodies in patients treated with recombinant epoetin: a follow-up report from the Research on Adverse Drug Events and Reports (RADAR) Project. Blood 2005; 106(10):3343-7. [ Links ]
8. Lammerich A, Balcke P, Bias P, Mangold S, Wiesholzer M. Cardiovascular Morbidity and Pure Red Cell Aplasia Associated With Epoetin Theta Therapy in Patients With Chronic Kidney Disease: A Prospective, Noninterventional, Multicenter Cohort Study. Clin Ther 2016;38(2):276-287. [ Links ]
9. Macdougall 1C, Roger SD, De Francisco A, Goldsmith DJ, Schellekens H, Ebbers H et al. Antibody-mediated pure red cells aplasia in chronic kidney disease patients receiving erythropoiesis-stimulating agents: new insights. Kidney Int 2012 ;81 (8) :727-732. [ Links ]
10. Vincenzo Panichi, Guido Ricchiuti, Alessia Scatena, Lucia Del Vecchio, Francesco Locatelli. Pure red cell aplasia induced by epoetin zeta. Clin Kidney J 2016; 9(4):599-602 [ Links ]
11. June M. McKoy, Robin E. Stonecash, Denis Cournoyer, Jerome Rossert, Allen R. Nissenson, Dennis W. Raisch et al. Epoetin-associated pure red cell aplasia: past, present, and future considerations. Transfusion 2008; 48(8): 1754-1762. [ Links ]
12. Djaldetti M, Blay A, Bergman M, Salman H, Bessler H. Pure red cell aplasiaa rare disease with multiple causes. Biomedicine & Pharmacotherapy 57 (2003) 326-332. [ Links ]
13. Peces R. Aplasia pura de células rojas y anticuerpos anti-eritropoyetina: surgen nuevas evidencias pero persisten las dudas. Nefrología 2003; 23(4):295-297. [ Links ]












 uBio
uBio 

