Cuadernos Hospital de Clínicas
versión impresa ISSN 1562-6776
Cuad. - Hosp. Clín. vol.57 no.1 La Paz 2016
ACTUALIZACIÓN
Fármacos vasoactivos e inotrópicos en el tratamiento del shock séptico
Vasoactive and inotropical drugs in the treatment of septic shock
Ac. Dr. Oscar Vera Carrasco
Profesor Emérito de la Facultad de Medicina-Universidad Mayor de San Andrés Especialista en Medicina Crítica y Terapia Intensiva
INTRODUCCIÓN
El shock séptico o septicémico se define como la hipotensión inducida por sepsis que persiste a pesar de la reanimación adecuada con fluidos, acompañada de alteraciones de la perfusión o disfunción de órganos. O la necesidad de fármacos vasoactivos para corregir la presión arterial. Es un tipo de shock distributivo, con reducción de las resistencias vasculares sistémicas y generalmente aumento del gasto cardíaco.
La sepsis se define como la presencia (posible o documentada) de una infección junto con manifestaciones sistémicas de infección. El shock asociado a sepsis severa como su expresión más grave, operativamente requiere la presencia de un Síndrome de respuesta inflamatoria sistémica (SIRS) de origen infeccioso más criterios de hipoperfusión e hipotensión persistente (presión arterial sistólica < 90 mmHg o presión arterial media (PAM) < 70 mmHg, o caída > 40 mmHg de la presión arterial sistólica desde la basal) que no revierte con la administración de fluidos (2 L de cristaloides en 1 hora) y por lo tanto, requiere el empleo de fármacos vasopresoras para su corrección.
La sepsis grave (sepsis sumada a disfunción orgánica inducida por sepsis o hipoperfusión tisular) además de lo anterior, presenta las siguientes alteraciones: Lactato por encima de los límites máximos normales de laboratorio; Diuresis < 0,5 ml/kg/h durante más de 2 h a pesar de una reanimación adecuada con fluidos; Lesión pulmonar aguda con PaO2/FIO2< 250 con ausencia de neumonía como foco de infección; Lesión pulmonar aguada con PaO2/FIO2< 200 por neumonía como foco de infección; Creatinina > 2,0 mg/dL (176,8 umol/L); Bilirrubina > 2 mg/ dL (34,2 umol/L); Recuento de plaquetas < 100 000 uL, y Coagulopatía (razón internacional normalizada > 1.5)
En 1992 el American College of Chest Physicians (ACCP) y la Society of Critical Care Medicine (SCCM) celebraron una Conferencia de Consenso en la que se establecieron las definiciones en un intento de acabar con la terminología confusa que existía en el contexto de los pacientes sépticos. Se introdujo el término "Síndrome de respuesta inflamatoria sistémica" (SRIS) definido como la respuesta generalizada del organismo ante determinados estímulos, cuya presencia puede deberse etiología infecciosa o no infecciosa, en la que aparecen dos o más de los siguientes hallazgos clínicos: a) Temperatura mayor de 38°C o menor de 36°C; b) Frecuencia cardiaca mayor de 90 latidos por minuto; c) Hiperventilación con frecuencia respiratoria > 20 respiraciones por minuto o PaCO2 < 32 mmHg. y d) Alteración del recuento de leucocitos con más de 12.000 o menos de 4.000/mm3, o más del 10% de cayados.
La sepsis severa y shock séptico lideran la causa de muerte en Terapia Intensiva. El Shock distributivo séptico es el estado de shock más frecuente, y obedece a infecciones diseminadas y tiene un alto índice en mortalidad en las unidades de cuidados intensivos. Tiene dos fases: la fase hiperdinámica y la hipodinámica. La fase hiperdinámica se caracteriza por presentar fiebre, piel enrojecida, petequias, taquicardia, taquipnea, vasodilatación, presión arterial normal, agitación y ansiedad; mientras que la hipodinámica se manifiesta con piel fría, pálida, disminución de la T/A y el gasto cardiaco, temperatura inferior a lo normal, vasoconstricción, oliguria, acidosis metabólica, somnolencia y coma.
Resumiendo, existen muchas clasificaciones, según los últimos consensos que al respecto han surgido y muchas definiciones, sepsis, septicemia, sepsis grave, shock séptico, variando en la presencia de más o menos datos clínicos y de laboratorio sobre todo, por lo que representa una mayor dificultad la diferenciación, por lo que a efectos prácticos y a quienes va dirigido este artículo se pretende ser prácticos.
VASOPRESORES
Son agentes de segunda línea en el tratamiento de la sepsis grave y el shock séptico. Están indicados en pacientes que no responden a la expansión de volumen (normalización de la PVC sin conseguir una TAM por encima de 65 mmHg) o que desarrollan edema pulmonar no cardiogénico. Si el paciente requiere vasopresores, colocar un catéter arterial tan pronto como sea posible.
Cuando con una reposición apropiada de fluidos, no se consigue restaurar una adecuada presión arterial y perfusión orgánica, se debería comenzar la terapia con vasopresores, la cual también puede ser requerida cuando estamos realizando la reposición de fluidos, hasta que se corrija la hipovolemia. Para que sus efectos sean adecuados deben corregirse ciertos factores que pueden interferir, tales como la acidosis.
Se requiere tratamiento con vasopresores para prolongar la vida y mantener la perfusión frente a hipotensión potencialmente mortal, aun cuando no se haya resuelto la hipovolemia. Por debajo de un umbral PAM, se puede perder la autorregulación en lechos vasculares críticos y la perfusión puede tornarse linealmente dependiente de la presión. Por consiguiente, algunos pacientes pueden necesitar tratamiento con vasopresores para lograr una presión de perfusión mínima y mantener un flujo adecuado. Se recomienda que el tratamiento con vasopresores busque como objetivo inicial una PAM de 65 mm Hg.
Cabe tener en cuenta que la definición unánime de hipotensión inducida por sepsis para el uso de PAM en el diagnóstico de sepsis grave es diferente (PAM < 70 mm Hg) del objetivo basado en evidencia de 65mm Hg utilizado en la recomendación de la Campaña para sobrevivir a la sepsis 2012. En cualquier caso, la PAM óptima debe individualizarse ya que puede ser más alta en pacientes con aterosclerosis o hipertensión previa que en pacientes jóvenes sin comorbilidad cardiovascular.
Los vasopresores son una clase heterogénea de fármacos con efectos hemodinámicos potentes e inmediatos. Los vasopresores pueden clasificarse según sus acciones adrenérgicas y no adrenérgicas.
La utilización de diferentes vasopresores se describió en un estudio amplio de cohortes multicéntrico europeo en UCI (Sakr 2006). El vasopresor utilizado con mayor frecuencia fue la norepinefrina (80%), seguido de la dopamina (35%) y la epinefrina (23%) solas o en combinación. La combinación de norepinefrina, dopamina y epinefrina se usó sólo en el 2% de los pacientes con shock. En este informe no se incluyó la vasopresina, ni la terlipresina. Actualmente, la elección de los vasopresores parece basarse principalmente en las preferencias de los médicos (Leone 2005).
Norepinefrina (NE)
La Norepinefrina: aumenta la PA por vasoconstricción con poco cambio de la frecuencia cardíaca y menor incremento de volúmen de bombeo. Es más potente que la dopamina y más efectiva en restaurar la presión arterial, además produce menos taquicardia, y posible incremento de la sobrevida. Sus acciones difieren parcialmente de las de la adrenalina, porque su espectro de activación de los adrenorreceptores es algo distinto. A las dosis habituales (2 - 20 mcg/ min por vía intravenosa) carece de actividad beta 2, mantiene la actividad beta 1 cardíaca y es un potente activador alfa 1. En consecuencia, produce intensa vasoconstricción en la piel, las mucosas y el área esplácnica, incluida la circulación renal, tanto de arteriolas como de vénulas. Al no provocar vasodilatación alfa 2, aumentan la resistencia periférica y la presión diastólica.
La acción cardíaca también es intensa y similar a la de la adrenalina: aumentan la frecuencia cardíaca, la contractilidad, el volumen minuto y la presión sistólica; pero la hipertensión producida provoca con frecuencia bradicardia refleja y el aumento de la poscarga puede ejercer un efecto negativo sobre el gasto cardíaco. Disminuye el flujo sanguíneo en los diversos órganos por vasoconstricción, lo que facilita el metabolismo anaerobio y la producción de metabolitos ácidos. El flujo renal puede verse afectado si la vasoconstricción es intensa o si el sujeto se encuentra en un estado inicial de hipotensión, lo que hace disminuir la filtración glomerular.
Las acciones metabólicas son similares a las de la adrenalina, como la hiperglucemia, pero aparecen a dosis elevadas. Por vía intradérmica produce sudoración. Tampoco atraviesa bien la Barrera hematoencefálica (BHE), por lo que apenas genera acciones centrales.
Aunque no existe una evidencia definitiva de la superioridad de un agente sobre otro, se recomienda la utilización de noradrenalina (NA) sobre la dopamina. Dosis de NA: 0,04 mcg/ kg/min: 8 mg de NA en 250 ml de suero salino fisiológico (0,9%), comenzando a un ritmo de 5 ml/h, con incrementos de 5 ml/h cada 5-10 minutos en función de objetivos hemodinámicos. Es recomendable administrar la NA a través de un catéter venoso central para evitar los efectos adversos de su extravasación al utilizarla por vía periférica.
Hernández y colaboradores, estudiaron una población de pacientes con Shock séptico, y encontraron que los requerimientos de noradrenalina podían identificar enfermos con alto riesgo de fallecer. En base a esta información, procedieron a estratificar la intensidad del Shock séptico como sigue:
- Shock séptico leve: requerimiento máximo de NE < 0,10 ng/kg/min luego de una adecuada reanimación (5% mortalidad).
- Shock séptico moderado: requerimiento máximo de NE entre 0,11 y 0,29 ng/kg/min (22% mortalidad).
- Shock séptico severo: requerimiento máximo de NE > 0,3 ng/kg/min (73% mortalidad).
Dopamina
Las acciones de la dopamina son complejas porque activa con baja afinidad a los receptores alfa y beta 1 adrenérgicos, con escaso o nulo efecto sobre beta 2, a la vez que activa sus receptores dopaminérgicos. Además, la estimulación de receptores D2 presinápticos puede originar una inhibición indirecta de la actividad simpática. La Dopamina aumenta la PA y el gasto cardíaco por aumento del volúmen de bombeo y de frecuencia cardíaca. Puede ser útil en pacientes con función sistólica comprometida.
Su efecto es dosis dependiente, inotrópico y vasopresor. A dosis de 1-3 mcg/kg/min: estímulo receptores dopaminérgicos renales, aumento flujo renal y de diuresis. Nunca esta velocidad de infusión en sepsis. A dosis de 4-10 mcg/kg/min: efecto beta, inotrópico y cronotrópico. Y a dosis de 10-20 mcg/kg/min: efecto vasoconstrictor, alfa. Por encima de 20 mcg/Kg/min sin ventajas respecto a noradrenalina.
A dosis bajas (0,5 mcg/kg/min), la dopamina provoca vasodilatación renal, mesentérica, cerebral y coronaria sin modificaciones en los lechos vasculares musculoesqueléticos. En el túbulo renal inhibe la reabsorción de Na+ y aumenta la diuresis. Estos efectos son mediados por la estimulación directa de receptores D1. A estas dosis, inhibe la liberación de noradrenalina en las terminaciones simpáticas y puede ocasionar hipotensión y bradicardia como consecuencia de la actividad sobre receptores D2, siendo este efecto ampliamente estudiado con fines terapéuticos, para controlar la hipertensión arterial o para aliviar la insuficiencia cardíaca congestiva.
A dosis más elevadas (2-4 mcg/kg/min), la dopamina aumenta la contractilidad y frecuencia cardíacas mediante el estímulo de receptores beta 1 adrenérgicos. Esta taquicardia puede quedar oculta por los efectos bradicardizantes mediados a través del estímulo sobre receptores D2.
A dosis algo más elevadas (4-5 mcg/kg/min), la dopamina puede provocar vasoconstricción por estímulo de alfa adrenorreceptores, y, en estados de shock, son necesarias dosis aún superiores para conseguir estos mismos efectos (alrededor de 20 mcg/kg/min).
Se sugiere el uso de la dopamina como agente vasopresor alternativo a norepinefrina solo en pacientes sumamente seleccionados (por ej., pacientes con riesgo bajo de taquiarritmias y bradicardia absoluta o relativa).
La dopamina puede ser útil particularmente en pacientes con función sistólica deteriorada pero causa más taquicardia y puede ser más arritmogénica que la norepinefrina. También puede influenciar la respuesta endocrina a través del eje hipotálamo hipofiso y tener efectos inmunodepresores. Sin embargo, la información proveniente de aleatorizados que compararon norepinefrina con dopamina no apoya el uso rutinario de dopamina en el manejo de choque septicémico.
Las dosis bajas de dopamina no deberían ser utilizadas para protección renal como parte del tratamiento de la sepsis. Un metaanálisis comparando bajas dosis de dopamina y placebo en pacientes críticos, no demostró mejora de los parámetros (niveles de creatinina, necesidad de terapias de reemplazamiento, gasto urinario y tiempo para la recuperación de la función renal) o máximas de vasopresores convencionales. La dosis renal no es predecible, sus efectos dependen de la actividad de la renina, puede producir desensibilización de receptores e isquemia de la medula renal. La diuresis que produce no es beneficiosa. Puede también producir un deterioro en la circulación esplácnica, alteraciones endocrinas, de la de la inmunidad y depresión del centro respiratorio.
Adrenalina
Es un estimulante muy potente de los receptores alfa y beta. Tanto el corazón como los vasos poseen abundantes alfa y beta adrenorreceptores. En general, los beta suelen ser más sensibles que los alfa, por lo que responden a dosis menores de fármaco, de ahí que las concentraciones pequeñas, como las que se consiguen en inyección subcutánea, produzcan acciones predominantemente beta, mientras que, en inyección intravenosa rápida, provocan también intensas acciones alfa.
En el corazón, la adrenalina incrementa la frecuencia cardíaca sinusal, la velocidad de conducción y la fuerza de contracción (acción beta 1); la sístole es más corta, y la contracción y la relajación del miocardio son más rápidas. La taquicardia sinusal se debe al aumento de la pendiente de despolarización de la fase 4 aumenta también la velocidad de despolarización de la fase O y acorta la duración del potencial de acción y el período refractario. La conducción aurículo-ventricular es más rápida. Este conjunto de efectos contribuye a incrementar el volumen minuto y la presión arterial sistólica y, de forma simultánea, aumenta el consumo de del miocardio. A dosis altas, aumenta el automatismo en el tejido de conducción por la despolarización espontánea de células no sinusales en el sistema de excitación y conducción, facilitando la aparición de extrasístoles y otras arritmias cardíacas (acción beta1).
Produce vasodilatación de las arteriolas del área muscular, de las coronarias y de otros territorios (acción beta 2); como consecuencia, aumenta el flujo sanguíneo y reduce la presión diastólica que; por mecanismo reflejo, origina taquicardia. Este efecto es el que predomina a dosis bajas de adrenalina (0,01-0,1mcg/kg/min por vía intravenosa). Sinembargo,adosisaltas (superiores a 0 ,1 mcg/kg/min por vía intravenosa) activa los receptores alfa 1 y alfa 2, y de las arteriolas de la piel, las mucosas y el área esplácnica, incluida la circulación renal; en consecuencia, eleva la presión arterial, preferentemente la diastólica.
También provoca constricción en los vasos venosos, la cual facilita el retomo venoso y la repleción ventricular durante la diástole. Como a la dosis necesaria para producir activación alfa (vascular) se produce intensa estimulación beta (cardíaca y vascular), pero las consecuencias de la vasoconstricción predominan sobre las de la dilatación, se apreciará un aumento de la resistencia periférica total con elevación de la presión arterial sistólica en mayor grado que la de la diastólica, un aumento de la presión diferencial y taquicardia. Si la hipertensión arterial es intensa, puede originar bradicardia refleja, a la que se pueden sumarextrasístoles. La activación excesiva y prolongada del miocardio resulta peligrosa, tanto por el incremento inadecuado del consumo de O2 como por las micro lesiones que pueden aparecer en los vasos y en las miofibrillas. En síntesis, la adrenalina por sus acciones alfa y beta, aumenta PAM, el IC y tono vascular periférico; aumenta la oferta O2 y consumo; incrementa el lactato y disminuye el flujo regional esplácnico.
En los pacientes que desarrollan un Shock séptico severo hipodinámico se sugiere un ensayo terapéutico con adrenalina por un lapso de 6 horas. La adición de adrenalina tiene como objetivo alcanzar un IC > 3,0 L/min/m2. La adrenalina se titula desde 0,1 hasta 0,5 mcg/kg/min.
Recientemente, el estudio CATS no encontró diferencias en términos de eficacia o seguridad entre la administración de adrenalina versus la combinación nordrenalina/dobutamina en pacientes con Shock séptico. Sin embargo, es importante considerar que este estudio no tuvo el poder estadístico suficiente como para establecer en forma categórica la seguridad de la administración de adrenalina como vasoactivo de primera línea en pacientes con Shock séptico. Es por ello que en nuestro grupo la empleamos con un criterio más bien restrictivo (pero no tardío), en los pacientes más graves con depresión miocárdica y controlando en forma constante la evolución de los parámetros de perfusión. La infusión de adrenalina, en algunos casos, puede ocasionar un deterioro de la perfusión sistémica a pesar de un mejoramiento en los objetivos hemodinámicos. Si se detecta esta situación (evidenciada por alteración de los marcadores de perfusión tisular), se deberá disminuir progresivamente la dosis con ajustes adicionales de NA.
INOTRÓPICOS
Los pacientes con sepsis severa pueden tener GC, normales o incrementados. Por lo tanto, se recomienda instaurar tratamientos con inótropicos/ vasopresores combinados. Cuando monitoriza el gasto cardiaco, se pueden utilizar un Vasopresor y/o Dobutamina, según los resultado del monitoreo.
Dobutamina
Es una catecolamina sintética que estimula a los receptores alfa, beta 1 y beta 2, aunque con predominante efecto beta 1, por lo que mejora el GC. Se caracteriza por estimular la actividad cardíaca; teóricamente, incrementa tanto la contractilidad como la frecuencia cardíaca. La dobutamina tiene mayor actividad inotrópica que cronotrópica. El hecho de que, además, presente cierta acción beta 2 vasodilatadora, determina una reducción de la poscarga que también beneficia a la actividad hemodinámica del corazón.
Estimula preferentemente los receptores beta 1, y, en menor grado, los receptores y beta 2 y alfa 1 adrenérgicos cardíacos. La dobutamina presenta una vida mediade unos 2-4 min, por lo que se administra por vía i. v. A las dosis habituales, aumenta la contractilidad y el volumen minuto cardíacos, y disminuye la presión telediastólica ventricular, pero apenas modifica la frecuencia cardíaca o el flujo sanguíneo renal. Este menor efecto taquicardizante podna atribuirse a que la estimulación alfa 1 adrenérgica aumenta la contractilidad, pero no la frecuencia cardíaca. A dosis altas, la estimulación de los receptores beta 2 produce vasodilatadón coronaria y de la musculatura esquelética, y la de los receptores alfa 1 adrenérgicos, vasoconstricción esplácnica y renal; estas acciones contrapuestas explican por qué la presión arterial no se altera o disminuye.
La dobutamina es un potente agente (3 adrenérgico. Efecto cronotrópico variable; ojo con hipotensión y reposición inadecuada de volumen, porque se puede aumentar la hipotensión. Puede incrementar el IC entre un 25 al 50%, sin incrementos de la presión arterial. El incremento de la perfusión esplácnica se debe al incremento del gasto cardiaco. Se recomienda iniciar con una dosis de 2,5 mcg/Kg./min. Hasta dosis máxima de 20 mcg/Kg./min., presencia de hipotensión arterial o FC superior a 120 latidos/min. La combinación de dosis bajas de dopamina con dosis más altas de dobutamina permite obtener una respuesta inotrópica superior a la obtenida en monoterapia.
La dobutamina es el inotrópico de primera elección para pacientes con gasto cardíaco bajo medido o presunto en presencia de presión de llenado ventricular izquierdo (o evaluación clínica de reanimación con fluidos adecuada) y PAM adecuada. Los pacientes septicémicos que continúan hipotensivos después de la reanimación con fluidos pueden tener gastos cardíacos bajos, normales o elevados. Por consiguiente, el tratamiento con una combinación de inotrópico/ vasopresor, como norepinefrina o epinefrina, se recomienda si no se midió el gasto cardíaco. Cuando existe la posibilidad de monitorear el gasto cardíaco además de la presión arterial, un vasopresor, como norepinefrina, puede utilizarse por separado para lograr el objetivo de niveles específicos de PAM y gasto cardíaco.
En pacientes con bajo gasto, tras una adecuada resucitación con fluidos, la dobutamina puede ser usada para incrementar el gasto cardíaco. Si se usa en presencia de baja presión arterial, debe asociarse a terapia vasopresora. No se recomienda una estrategia para aumentar el índice cardíaco hasta niveles supranormales. Dos estudios clínicos prospectivos54, incluyendo pacientes críticos, no consiguieron demostrar beneficio del aumento del transporte de oxígeno a niveles supranormales por el uso de dobutamina.
En el shock séptico se debe administrar o incorporar: 1. Un tratamiento de prueba con perfusión de dobutamina de hasta 20 mcg/ kg/min al vasopresor (si se usa) en presencia de: (a) disfunción miocárdica, como lo indican las presiones cardíacas de llenado elevadas y bajo gasto cardíaco, o (b) signos continuos de hipoperfusión, a pesar de lograr un volumen intravascular adecuado y PAM adecuada. 2. No recomendamos el uso de una estrategia para aumentar el índice cardíaco a los niveles mucho más altos que los predeterminados.
Los grandes ensayos clínicos prospectivos, que incluyeron pacientes de UCI en estado crítico que padecieron sepsis grave, fracasaron en demostrar beneficios en el aumento de la administración de oxígeno a los objetivos supranormales mediante el uso de dobutamina. Estos estudios no se enfocaron específicamente en pacientes con sepsis graves ni se centraron en las primeras 6 horas de reanimación. Si la evidencia de hipoperfusión tisular persiste a pesar del volumen intravascular adecuado y PAM adecuada, una alternativa viable (diferente a la reversión del traumatismo subyacente) sería incorporar un tratamiento con inotrópicos.
NORADRENALINA
De elección en shock séptico. Potente vasopresor alfa-adrenérgico, también beta-adrenérgico, inotrópico y cronotrópico positivo. Dosis inicial de 0.5 mcg/kg/min e ir ajustando en función de respuesta.
INFUSION: ampollas 1 mg/ml con 10 ml. Diluir 6 viales (60 mg) en 250cc suero glucosado al 5% (extraer 60ml) empezando a 0.5 microgr/kg/min e ir aumentando en función de respuesta.
DOPAMINA
Inotrópico y vasopresor.
- 1-3 mcg/kg/min: estímulo receptores dopaminérgicos renales, aumento flujo renal y de diuresis. Nunca esta velocidad de infusión en sepsis.
- 4-10 mcg/kg/min: efecto beta, inotrópico y cronotrópico.
INFUSION:ampollas de 200 mg con 5 ml, preparar 1 gr. en 500 SG al 5% (480 ml). Comienzo de acción a los 5 minutos. Recomendable realizar la titulación de dosis de mantenimiento en mcg/kg/ min.
DOBUTAMINA
Agonista beta-adrenérgico en dosis de 5-20 mcg/ kg/min. Potente inotrópico, produce aumento del gasto cardíaco. Efecto cronotrópico variable; ojo con hipotensión y reposición inadecuada de volumen, porque se puede aumentar la hipotensión.
INFUSION: ampollas de 250 mg y 20 ml, diluir un gramo en 500 ml de suero glucosado al 5% (desechar 80 ml). Vida media de 2,5 minutos. Empezar a 5 mcg/kg/min e ir aumentando en función de respuesta.
Colofón
El shock asociado a sepsis severa como su expresión más grave, es una entidad catastrófica asociada a una elevada morbimortalidad. Su diagnóstico precoz y tratamiento agresivo en forma protocolizada puede mejorar el resultado. Durante la fase inicial de la reanimación se pueden emplear cristaloides y/o coloides para expandir el espacio intravascular buscando una PVC 8 a 12 mmHg.
En caso de hipotensión refractaria a la administración de fluidos, se recomienda el inicio de noradrenalina en dosis ascendentes hasta obtener una PAM de 65 a 75 mmHg. El objetivo inicial es alcanzar una meta hidráulica (PAM 65 a 75 mmHg y PVC 8 a 12 mmHg); sin embargo, el objetivo final y el verdaderamente relevante, consiste en la normalización de los parámetros hemodinámicos de perfusión tisular: lactacidemia < 4 mmol/L y SvcO2 > 70% (meta metabólica).
La terapia precoz (dentro de las primeras 6 horas de diagnosticada) intenta ajustar o adaptar la función cardiaca al nuevo estado de agresión (sepsis). Esta modalidad de tratamiento pretende mejorar la precarga, la poscarga y la contractilidad cardiaca para obtener un equilibrio adecuado entre la oferta y la demanda de oxígeno, lo que puede salvar las vidas, mejorar el pronóstico e incrementar las posibilidades de supervivencia. Bajas dosis de dopamina no tienen efecto nefroprotector, por lo que su empleo con esta finalidad es inapropiado. Todos los pacientes que requieren vasopresores deberían de tener canalizada una arteria para control de la presión arterial.
REFERENCIAS
1. Rivers E, Nguyen B, Havstad S, Ressler J, Muzzini A, Knoblich B, etal. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med. 2001; 345(19): 1368-77. [ Links ]
2. Surviving Sepsis Campaign 2008. Crit Care Med 2008 Vol. 36, No. 1 [ Links ]
3. Ministerio de sanidad, servicios sociales e igualdad de España. Protocolos Clínico Terapéuticos en Urgencias Extrahospitalarias. Instituto Nacional de Gestión Sanitaria.Madrid 2013 [ Links ]
4. Rodrigo Casanova MP, J. M. García Peña JM, Rodríguez V, Ortega M, Aguilera Celorrio L. Sepsis grave y shock séptico. Rev. Esp. Anestesiol. Reanim. 2007; 54: 484-498 [ Links ]
5. Dellinger RP; Levy MM; Rhodes A; Annane D; Gerlach H; Opal SM et al. y el Comité de recomendaciones de la campaña para sobrevivir a la sepsis, que incluye el subgrupo de pediatría. Campaña para sobrevivir a la sepsis: recomendaciones internacionales para el tratamiento de sepsis grave y choque septicémico, 2012. Febrero de 2013 Volumen 41 Número 2. www.ccmjournal.org [ Links ]
6. Dellinger RP, LevyMM, Carlet, JM, etal: Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: 2008 [published correction appears in Crit Care Med 2008; 36: 1394 -1396]. Crit Care Med 2008; 36:296-327. [ Links ]
7. Hernández G, Bruhn A, Romero C, Larrondo FJ, De la Fuente R, Castillo L. Management of septic shock with a norepinephrine-based hemodynamic algorithm. Resuscitation 2005; 66:63-9. [ Links ]
8. García-Sevilla JLAyMeanaesusJJ. Transmisión catecolaminérgica. Fármacos agonistas catecolaminérgicos. En: Flórez. Farmacologia Humana. Sexta edición. Barcelona, España. Elsevir Mason 2014 [ Links ]
9. Regnier B, Rapin M, Gory G, et al: Haemodynamic effects of dopamine in septic shock. Intensive Care Med 1977; 3:47-53 [ Links ]
10. Annne D, Vignon P, Renault A, Bollaert PE, Charpentier C, Martin C et al. Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: a randomized trial. Lancet 2007; 370: 676-84. [ Links ]
11. Dellinger RP, Levy MM, Carlet JM, Bion J, Parker MM, Jaeschke R et al. Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: 2008. Crit Care Med 2008; 36: 296-327 [ Links ]
12. Gattinoni L, Brazzi L, Pelosi P, et al: A trial of goal-oriented hemodynamic therapy in critically ill patients. Svo2 Collaborative Group. N Engl J Med 1995; 333:1025-1032 [ Links ]
13. Hayes MA, Timmins AC, Yau EH, et al: Elevation of systemic oxygen delivery in the treatment of critically ill patients. N Engl J Med 1994; 330:1717-1722 [ Links ]
14. Vera-Carrasco O. SHOCK: Enfoque diagnóstico y terapéutico en el adulto. Cuad. - Hosp. Clín. v.52 n.2 La Pazjul. 2007 [ Links ]
15. Rodríguez A, BonafontX, Ricart P, Morillas J. Shock séptico: nuevas medidas de tratamiento (vasopresores, esteroides y otras medidas asociadas). En Torradabella P, editor. Sepsis, sepsis grave y shock séptico. Barcelona: Edika Med. 2005:85-96. [ Links ]
16. De la Torre Prados, María Victoria et al. SEPSIS grave : proceso asistencial Integrado/[Sevilla]: Consejería de Salud, 2010. [ Links ]
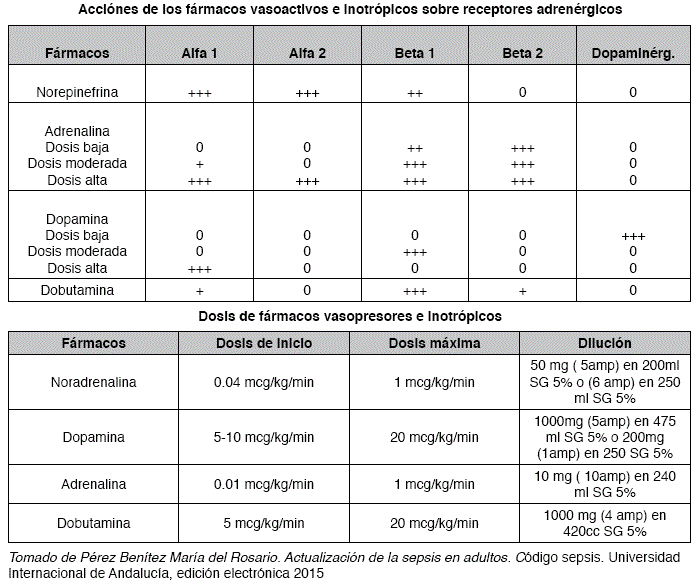
17. Pérez Benítez María del Rosario. Actualización de la sepsis en adultos. código sepsis. Universidad Internacional de Andalucía, edición electrónica 2015 [ Links ]












 uBio
uBio 

