Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Cuadernos Hospital de Clínicas
versión impresa ISSN 1562-6776
Cuad. - Hosp. Clín. vol.54 no.2 La Paz 2009
CASO CLÍNICO
Malaria y embarazo: un caso importado de África
Malaria and pregnancy: an imported case from Africa
Pamela Durán1, & Eddy Martínez2,3
1. Instituto Nacional de Laboratorios de Salud (INLASA), La Paz, Bolivia;
2. Unidad de Parasitología, Medicina Tropical y Medio Ambiente, Instituto de Investigación en Salud y Desarrollo (IINSAD), Facultad de Medicina, Universidad Mayor de San Andrés, La Paz, Bolivia;
3. Cátedra de Parasitología, Facultad de Medicina, Universidad Mayor de San Andrés, La Paz, Bolivia.
Correspondencia: Pamela Durán, duran_pame@yahoo.es
Cómo citar este artículo: Durán P, Martínez E. Malaria y embarazo: Parasitemia recurrente en un caso importado. Cuad Hosp Clín. 2009;54:122-126
PALABRAS CLAVE: Malaria y embarazo, Plasmodium falciparum, artesunato, mefloquina, recrudescencia, parasitemia recurrente, malaria importada.
KEYWORDS: Malaria and pregnancy, Plasmodium falciparum, artesunate, mefloquine, recrudescence, recurrent parasitaemia, imported malaria.
INTRODUCCIÓN
La malaria es un importante problema de salud en el mundo y es la principal causa de enfermedad y muerte en muchas zonas tropicales y subtropicales, principalmente en África subsahariana donde las infecciones por Plasmodium falciparum son las más frecuentes, situación particularmente importante, porque esta especie puede provocar malaria grave e incluso la muerte. Según la Organización Mundial de la Salud se presentan entre 350 a 500 millones de casos por año, la gran mayoría en África subsahariana, donde se registran el 60% de los casos del mundo, el 75% de los casos por P. falciparum y más del 80% de las defunciones.1 Se calculan más de 1 millón de muertes anuales, de las cuales aproximadamente el 95% ocurren en niños africanos, siendo este el sector más vulnerable, en las zonas de alta transmisión los adultos suelen presentar un grado de inmunidad parcial conocida como estado "semiinmune", siendo por lo tanto frecuentes las infecciones asintomáticas o subclínicas. Las personas que no viven ni nacieron en zonas endémicas, suelen ser más susceptibles a la enfermedad y presentar complicaciones si el tratamiento no es oportuno.2
Las mujeres embarazadas por su condición fisiológica son un grupo de alto riesgo, pues la malaria durante el embarazo causa enfermedad sintomática aguda más severa que en ausencia del embarazo y puede tener graves consecuencias tanto para la madre como para el feto,2-4 todas las especies de Plasmodium pueden causar malaria durante el embarazo, pero P. falciparum que es la responsable de la mayoría de los casos, está asociado a las formas más severas y aproximadamente todos los años 25 millones de mujeres embarazadas están en riesgo de infección por esta especie.1,3 La malaria durante el embarazo puede ser causa de enfermedad y muerte materna principalmente en primigestas y multigestas (más de 5 embarazos), los efectos que produce la malaria y que determinan la gravedad para la mujer embarazada están asociados a la anemia, la hipoglucemia y la tendencia a hacer edema agudo de pulmón, además el embarazo favorece las recidivas y las recrudescencias parasitarias, la mayoría de las infecciones por P. falciparum se asocian a la presencia de parásitos en la placenta que parece ser un sitio preferencial para el secuestro y desarrollo de parásitos, esto obstaculizaría el intercambio de nutrientes y oxigeno entre la madre y el feto lo que conlleva al retardo del crecimiento intrauterino (RCIU) y como consecuencia los neonatos son pequeños para la edad gestacional (bajo peso al nacer). La malaria durante el embarazo, puede por lo tanto provocar aborto, prematuridad, retardo del crecimiento intrauterino, muerte fetal, muerte neonatal y muerte materna. Asimismo, pueden nacer niños infectados (malaria congénita).2-7
Siendo la malaria particularmente grave si afecta a las mujeres embarazadas, es muy importante extremar esfuerzos para la utilización de estrategias efectivas para la prevención de la infección en este grupo vulnerable. Cuando las estrategias de prevención no fueron aplicadas o no fueron efectivas y ocurre infección durante el embarazo, es prioritario el diagnóstico precoz y el tratamiento oportuno, para evitar las consecuencias en la madre, el feto y/o el recién nacido. El tratamiento recomendado por la OMS para la malaria durante el primer trimestre de embarazo es el sulfato de quinina 10 mg/Kg peso cada ocho horas durante 7 días y Clindamicina 10 mg/Kg peso cada 12 horas a partir del tercer día de tratamiento por 5 días. Pasado el primer trimestre de embarazo se puede administrar tratamiento combinado con derivados de la artemisinina como ser Artemeter/Lumefantrine (A/L), Artesunato/ Amodiaquina (AS/AQ), Artesunato/ Mefloquina (AS/ MQ) y Artesunato/ Sulfadoxina-Pirimetamina (AS/SP); está completamente proscrita la primaquina durante el embarazo por la alta posibilidad de muerte fetal.1,2,7-11
PRESENTACIÓN DE CASO
Antecedentes clínicos y epidemiológicos
Presentamos el caso de una mujer boliviana natural de Santa Cruz de la Sierra, Bolivia, de 28 años de edad, que permaneció durante 13 meses en la República Democrática de Congo (África central), específicamente en Kindu, donde estuvo como voluntaria de las Fuerza de Paz (Cascos Azules). La paciente retornó a Bolivia conjuntamente con el resto de voluntarios en fecha 13 de enero de 2005. Como norma, el Laboratorio de Referencia en Malaria del Instituto Nacional de Laboratorios de Salud (INLASA), en coordinación con el Programa Nacional de Malaria, realiza exámenes de sangre periférica (gota gruesa y extendido sanguíneo) a todos los repatriados para la identificación de casos importados de malaria. No se identificó parasitemia en el examen realizado a la paciente en fecha 14 de enero 2005. Una semana después de su retorno (21 de enero de 2005), la paciente acude al Laboratorio, para el control rutinario de la parasitemia a todo el contingente; en esa oportunidad, la paciente refería fiebre, cefalea y malestar general, síntomas que se presentaron desde el día anterior.
Antecedentes importantes
En esa oportunidad, la paciente mencionó que cursaba con una gestación próxima a las 12 semanas confirmada con una prueba de embarazo y ecografía. La paciente refirió, que realizó quimioprofilaxis durante los 7 primeros meses de su estadía, en base a mefloquina 250 mg/semana, no continuando con el mismo los restantes 6 meses. No sufrió ningún episodio de malaria durante su estadía en la R. D. de Congo, ni antes de su viaje, tampoco refiere antecedentes de malaria o exposición en zonas endémicas de Bolivia.
Diagnóstico de laboratorio y tratamiento del primer episodio
Se obtuvo sangre periférica por punción capilar en el pulpejo del dedo anular con la que se realizó extendido sanguíneo (frotis) y gota gruesa; se esperó que sequen y se deshemoglobinizó la gota gruesa con agua corriente. Posteriormente, se fijaron ambas con alcohol 96° y se colorearon con solución Giemsa 1:10 durante 45 min.2 Mediante microscopía se identificaron trofozoitos de Plasmodium falciparum tanto en la gota gruesa, como en el extendido sanguíneo. En la gota gruesa, se determinó una densidad parasitaria de 27.970 parásitos por microlitro de sangre. Fueron también positivas para P. falciparum, las pruebas rápidas que detectan la enzima deshidrogenasa láctica del parásito (pLDH): ICT ORCHID, ICT HUMAN, ICT BIORAPID y la prueba ICTAMRAD que detecta la Proteína II Rica en Histidina (HPRII)2 (Tabla 1).
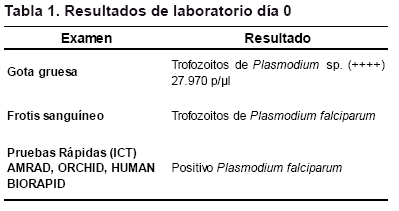
No se administró la terapia combinada con clindamicina y sulfato de quinina (de acuerdo a las normas de tratamiento para el primer trimestre de gestación),2 por no tener disponible la clindamicina.
Con el consentimiento de la paciente, el mismo día se inició monoterapia con artesunato 4mg/Kg peso por tres días. No se realizó la terapia combinada con mefloquina porque está droga está más contraindicada que los derivados de la artemisinina en el primer trimestre de embarazo4,7,8,10,11
Siguiendo el protocolo, se realizaron los controles correspondientes. Los controles de los días 2, 3 y 7 no mostraron parasitemia (Tabla 2).

El día 11 la paciente acudió al laboratorio por presentar malestar general, entonces se detectaron trofozoitos de P. falciparum (parasitemia recurrente), densidad parasitaria 72 parásitos por microlitro. Se administró nuevamente tratamiento con artesunato 4mg/Kg peso por tres días. En los controles de los días 3, 6 y 8 no se detectó parasitemia. Pero sí se presentó parasitemia recurrente en el control del día 14 (Tabla 3).
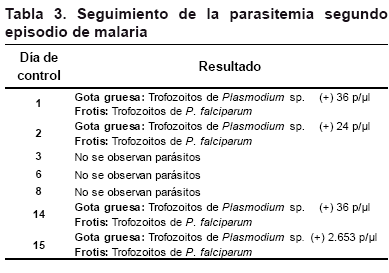
Confirmada la parasitemia recurrente el día 15 del segundo episodio de malaria, se administró el tratamiento combinado con Artesunato 4mg/ Kg peso por tres días y Mefloquina 12,5mg/Kg peso por dos días,2 se realizaron controles de la parasitemia los días 1, 2 y 7 después de iniciado el nuevo tratamiento. No se evidenció parasitemia en estos controles. No se realizaron más controles porque la paciente tuvo que retornar a su lugar de residencia en la ciudad de Santa Cruz de la Sierra. Nos comunicamos por teléfono con la paciente y refirió no haber presentado ninguna manifestación clínica compatible con malaria. El embarazo llegó a término sin ninguna complicación, por referencia de la paciente el parto fue eutócico y el recién nacido no tenía ningún problema de salud (afirmación del médico tratante).
DISCUSIÓN
Es conocido que en la monoterapia con artesunato o derivados de la malaria por P. falciparum es muy probable la parasitemia recurrente.17-20 En este caso, se utilizó esta monoterapia porque la paciente cursaba con un embarazo de menos de 12 semanas. En general, la OMS recomienda el tratamiento con sulfato de quinina más clindamicina en el primer trimestre, porque se conoce la toxicidad de la mefloquina y no hay evidencia plena de la seguridad del uso del artesunato,7,8,10 porque estudios sobre roedores y primates han mostrado embriotoxicidad.12-14 También se eligió el artesunato, además de su probable mayor seguridad, por el hecho de que existen varias evidencias de resistencia a la mefloquina en África.15,16 El tratamiento logró el aclaramiento rápido, pero temporal de la parasitemia en 2 oportunidades y como era probable, en ambos casos se presentó parasitemia recurrente tardía,17,18,19 los días 11 y 14. Un estudio realizado en Gabón, África sobre 50 niños entre 4 y 15 años de ambos sexos, utilizando el mismo esquema, monoterapia con artesunato 4mg/Kg peso día por 3 días mostró de manera similar un rápido aclaramiento de la parasitemia (≤72 h, ![]() 34 h), desaparición de la fiebre entre las 22 a 26 h, pero con recurrencias tardías, siendo la tasa de cura de 92% al día 14 y 62% al día 28, mostrando alta tasa de falla terapeútica tardía con este esquema.20 Los esquemas utilizados de más días (5 a 7) mostraron también recurrencias pero con menos frecuencia.17,18 Sin embargo, este manejo permitió ganar tiempo y que la paciente alcance el segundo trimestre de gestación, momento a partir del cual está recomendada la terapia combinada de artesunato más mefloquina, la que fue eficaz y determinó cura parasitológica (aclaramiento de la parasitemia) y cura clínica. La paciente tuvo que trasladarse a la ciudad de Santa Cruz donde vivía, por lo que se realizó el control por consulta telefónica, indagando si presentó nuevamente manifestaciones clínicas compatibles con malaria y principalmente indagando manifestaciones clínicas o secuelas de la infección malárica en el recién nacido. Por referencia de la madre, el embarazo llegó a término con el nacimiento de una niña con peso adecuado para la edad gestacional.
34 h), desaparición de la fiebre entre las 22 a 26 h, pero con recurrencias tardías, siendo la tasa de cura de 92% al día 14 y 62% al día 28, mostrando alta tasa de falla terapeútica tardía con este esquema.20 Los esquemas utilizados de más días (5 a 7) mostraron también recurrencias pero con menos frecuencia.17,18 Sin embargo, este manejo permitió ganar tiempo y que la paciente alcance el segundo trimestre de gestación, momento a partir del cual está recomendada la terapia combinada de artesunato más mefloquina, la que fue eficaz y determinó cura parasitológica (aclaramiento de la parasitemia) y cura clínica. La paciente tuvo que trasladarse a la ciudad de Santa Cruz donde vivía, por lo que se realizó el control por consulta telefónica, indagando si presentó nuevamente manifestaciones clínicas compatibles con malaria y principalmente indagando manifestaciones clínicas o secuelas de la infección malárica en el recién nacido. Por referencia de la madre, el embarazo llegó a término con el nacimiento de una niña con peso adecuado para la edad gestacional.
La evolución favorable de la gestación y el nacimiento de una niña saludable son una situación satisfactoria, porque es por demás conocido que la malaria por P. falciparum, es particularmente grave durante el embarazo, tanto para la madre como para el producto, siendo en el mundo tropical, sobre todo en África, la principal causa de mortalidad materna y fetal, también está asociada a parto inmaduro o parto prematuro, retardo del crecimiento intrauterino y malaria congénita. La monoterapia con artesunato a pesar de que determinó un efecto solamente parcial sobre la parasitemia, fue probablemente la causa más importante para que no se hayan producido las temidas complicaciones de la malaria durante el embarazo. Adicionalmente, el tratamiento combinado fue felizmente efectivo, ya que existía el temor de resistencia al tratamiento, porque la infección se debía a una cepa importada de África central, esta es una de las zona geográficas donde circulan con frecuencia cepas de P. falciparum mutiresistentes a los antimaláricos.1 El año 2007, un estudio muestra fallas terapéuticas asociadas a la monoterapia con artesunato y sugiere una probable resistencia a este producto coincidiendo con otros autores en la necesidad de la terapia combinada.19 Nosten et al, en un estudio con una importante cantidad de mujeres embarazadas que recibieron tratamiento con mefloquina, encontró que esta condición no estuvo asociada con aborto, bajo peso al nacer, retraso neurológico o malformación congénitas; sin embargo, los resultados sugieren que el tratamiento con mefloquina durante el embarazo podría estar asociado con un riesgo mayor de mortinatos,15 a pesar de que esto no está comprobado, se constituyó en otra de las razones para no haber administrado inicialmente este producto. La paciente no hizo un cuadro complicado de malaria a diferencia de varios otros casos del mismo contingente que presentaron malaria grave (5 casos) uno de ellos fatal (datos no publicados).
No se administró la mefloquina en los primeros tratamientos porque se coordinó con la paciente esta situación, previa información de que no existe evidencia suficiente de la seguridad de uso de este medicamento en el primer trimestre del embarazo y que más bien, la OMS recomienda no usarlo en esta edad gestacional y más aún existen evidencias de efectos colaterales conocidos que contraponen su uso y sugieren buscar otras alternativas terapéuticas. La OMS recomienda que en la malaria no complicada, el tratamiento combinado basado en artemisinina debe usarse en el segundo y tercer trimestres, pero sólo debe usarse en el primer trimestre si es el único tratamiento eficaz disponible.7
Entre otra cosas, este caso pone una vez más en evidencia (coincidente con las normas), que existe una permanente necesidad de realizar exámenes de laboratorio de manera obligatoria y sistemática a todos los viajeros que retornan al país luego de haber permanecido en zonas de alta transmisión para evitar la importación de cepas de parásitos eventualmente multiresistentes a los antimaláricos.16,21
Como norma, los miembros de fuerzas de paz que cumplen misiones en zonas donde circulan cepas de P. falciparum resistentes a los antimaláricos, deben hacer quimioprofilaxis con mefloquina. En este caso, la paciente realizó (como corresponde) la quimioprofilaxis durante los primeros 7 meses de permanencia la cual dejó posteriormente (como también corresponde), ya que esta forma de profilaxis está recomendaba para permanencias cortas de alrededor de 90 días, que se puede extender hasta 6 meses.11 En permanencias de más tiempo se tienen que extremar esfuerzos para aplicar otras medidas de profilaxis.
REFERENCIAS
1. Roll Back Malaria, World Health Organization, UNICEF. World Malaria Report 2005. Geneva, 2005. [ Links ]
2. Martínez E, Durán P. Manual de Diagnóstico y Tratamiento de la Malaria en Bolivia. La Paz, Bolivia, 2009.
3. Desai M, ter Kuile FO, Nosten F, McGready R, Asamoa K, Brabin B, Newman RD. Epidemiology and burden of malaria in pregnancy. Lancet Infect Dis. 2007;7:93-104. [ Links ]
4. Menendez C. Malaria during pregnancy. Curr Mol Med. 2006;6:269-273 [ Links ]
5. Greenwood B, Alonso P, ter Kuile FO, Hill J, Steketee RW. Malaria in pregnancy: priorities for research. Lancet Infect Dis. 2007;7:169-174. [ Links ]
6. Ramal C, Pinedo P. Malaria en gestantes entre marzo del 2002 y julio del 2003: experiencia en el Hospital Regional de Loreto, Perú. Acta Med Per. 2008;25(4):220-223. [ Links ]
7. World Health Organization. Assessment of the safety of artemisinin compounds in pregnancy. Report of two informal consultations convened by WHO in 2006. Geneva, World Health Organization, 2007 (WHO/CDS/ MAL/2003.1094. WHO/GMP/TDR/Artemisinin/07.1.). [ Links ]
8. Nosten F, McGready R, d'Alessandro U, Bonell A, Verhoeff F, Menendez C, Mutabingwa T, Brabin B: Antimalarial drugs in pregnancy: A review. Current Drug Safety. 2006;1:1-15. [ Links ]
9. Coll O, Menendez C, Botet F, Dayal R, Carbonell-Estrany X, Weisman LE, et al. Treatment and prevention of malaria in pregnancy and newborn. J Perinat Med. 2008;36:15-29. [ Links ]
10. Ward SA, Sevene EJ, Hastings IM, Nosten F, McGready R. Antimalarial drugs and pregnancy: safety, pharmacokinetics, and pharmacovigilance. Lancet Infect Dis. 2007; 7:136-144. [ Links ]
11. WHO Guidelines for the treatment of malaria. WHO/ HTM/MAL/2006.1108. WHO, 2006.
12. Clark RL, White TEK, Clode SA, Gaunt I, Winstanley P, Ward SA. Developmental toxicity of artesunate and an artesunate combination in the rat and rabbit. Birth Defects Res (Part B). 2004; 71:380-394. [ Links ]
13. Longo M, Zanoncelli S, Manera D, Brughera M, Colombo P, Lansen J, et al. Effects of the antimalarial drug dihydroartemisinin (DHA) on rat embryos in vitro. Reprod Toxicol. 2006;21:83-93.
14. White TEK, Clark RL. Sensitive periods for developmental toxicity of orally administered artesunate in the rat. Birth Defects Res (Part B). 2008;83:407-417. [ Links ]
15. Nosten F, Vincenti M, Simpson J, Yei P, Lay Thwai K, de Vries A, et al. The Effects of Mefloquine Treatment in Pregnancy. Clinical Infectious Diseases. 1999;28:808-815. [ Links ]
16. WHO. Containment of Malaria Multi-Drug Resistance on the Cambodia-Thailand Border. Report of an Informal Consultation Phnom Penh, 29-30 January 2007. Geneva, WHO, 2007. SEA-MAL-246 [ Links ]
17. Schwarz NG, Oyakhirome S, Pötschke M, Gläser B, Klouwenberg PK, Altun H, et al. 5-day nonobserved artesunate monotherapy for treating uncomplicated falciparum malaria in young Gabonese children. Am J Trop Med Hyg. 2005;73(4):705-709 [ Links ]
18. Hassan Alin M, Ashton M, Kihamia CM, Mtey GJB, Björkman A. Clinical efficacy and pharmacokinetics of artemisinin monotherapy and in combination with mefloquine in patients with falciparum malaria. Br J Clin Pharmacol. 1996;41:587-592. [ Links ]
19. Umar RA, Jiya NM, Hassan SW, Abdullahi K, Ahmed JM, Nata'ala U. Apparent Drug Failure Following Artesunate Treatment of Plasmodium falciparum in Sokoto, Nigeria: Three Case Reports. Trends in Medical Research. 2007;2(2):113-116. [ Links ]
20. Borrmann S, Adegnika AA, Missinou MA, Binder RK, Issifou S, Schindler A, et al. Short-course Artesunate Treatment of Uncomplicated Plasmodium falciparum Malaria in Gabon. Antimicrobial Agents and Chemotherapy. 2003;47(3):901 -904.
21. Trape JF. The public health impact of chloroquine resistance in Africa. Am J Trop Med Hyg. 2001 ;64:12-17. [ Links ]












 uBio
uBio 

