Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Ecología en Bolivia
Print version ISSN 1605-2528On-line version ISSN 2075-5023
Ecología en Bolivia vol.54 no.2 La Paz Sept. 2019
Artículo
Lista actualizada y comentada de los mamíferos de Bolivia
Updated and annotated checklist of mammals from Bolivia
Luis F. Aguirre1,2*, Teresa Tarifa3,4*, Robert B. Wallace5, Nuria Bernal H.5, Lizette Siles6,7, Enzo Aliaga-Rossel8 & Jorge Salazar-Bravo 9,4
1Centro de Biodiversidad y Genética, Facultad de Ciencias y Tecnología, Universidad Mayor de San Simón, Casilla 538, Cochabamba, Bolivia.
2Fundación Programa para la Conservación de los Murciélagos de Bolivia, Cochabamba, Bolivia.
3Orma J. Smith Museum of Natural History, The College of Idaho, 2112 Cleveland Blvd, Caldwell, Idaho, 83605-4432, USA.
4Colección Boliviana de Fauna, Calle 27 Cota Cota, Campus Universitario, La Paz, Bolivia.
5Wildlife Conservation Society, Programa Bolivia, calle Gabino Villanueva 340, Calacoto, La Paz, Bolivia.
6Museo de Historia Natural Alcides d'Orbigny, Av. Potosí 1458, Cochabamba, Bolivia.
7Departamento de Biología, Universidad de La Serena. Raúl Bitrán 1305, La Serena, Chile.
8Instituto de Ecología, Universidad Mayor de San Andrés, Calle 27 Cota Cota, Campus Universitario, La Paz, Bolivia.
9Department of Biological Sciences, Texas Tech University, PO Box 43131, 79409 Lubbock, Texas, USA.
*Autores de correspondencia (primera autoría compartida): laguirre@fcyt.umss.edu.bo, teresa_tarifa@yahoo.com
Recibido: 04.08.19, Aceptado: 02.10.19.
Resumen
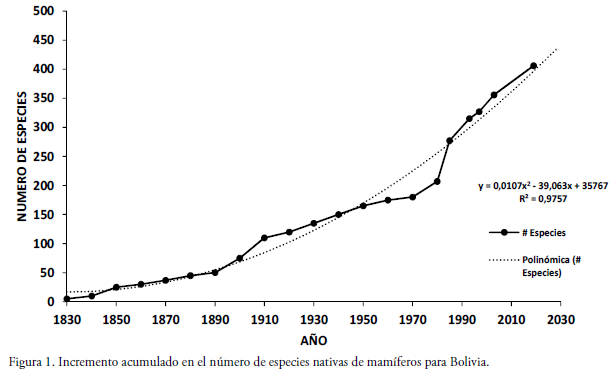
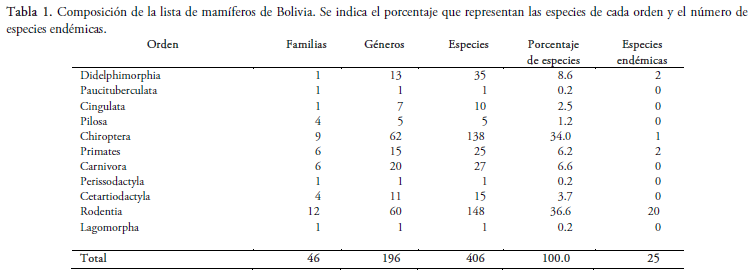
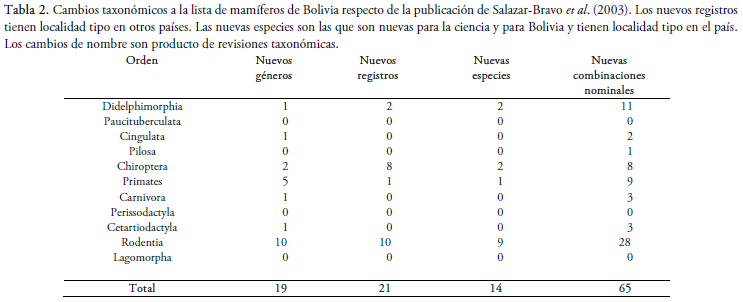
Presentamos la actualización más completa, a la fecha, de la lista de mamíferos de Bolivia. Incorporamos y describimos cambios taxonómicos recientes y nuevos registros para el país efectuados desde la última lista publicada en 2003. Para la elaboración de la lista se revisaron publicaciones científicas recientes y se consideró que las nuevas adiciones y los cambios taxonómicos incluidos cuenten con algún tipo de evidencia verificable. A la fecha la lista de mamíferos para Bolivia incluye 406 especies nativas, pertenecientes a 11 órdenes, 46 familias y 196 géneros, lo que representa un incremento de 51 especies con respecto a la lista de 2003. Entre aquellas adicionadas, 14 fueron nuevas para la ciencia y tienen localidad tipo en Bolivia. Los órdenes más diversos fueron Rodentia (148 especies), Chiroptera (138), Didelphimorphia (35) y Carnívora (27); un total de 25 especies son endémicas para Bolivia. Se listan además 14 especies de mamíferos introducidos. Se prevé que se adicionen nuevos registros y cambios taxonómicos a esta lista como resultado de inventarios biológicos actualmente en ejecución, reidentificación de especímenes depositados en colecciones de mamíferos nacionales y extranjeras, y revisiones taxonómicas futuras.
Palabras clave: Anotaciones taxonómicas, Especies nativas, Especies introducidas, Mamíferos, Taxonomía.
Abstract
We present an update to the list of mammals known to occur in Bolivia. We incorporate and describe recent taxonomic changes and new records for the country made since the last list published in 2003. New records and taxonomic changes were considered only if they had verifiable evidence. To date, the list of mammals for the country includes 406 native species, belonging to 11 orders, 46 families and 196 genera, representing an increase of 51 species over the 2003 list. Among those added, 14 were new to science and have type localities in Bolivia. The most diverse orders were Rodentia (148 species), Chiroptera (138), Didelphimorphia (35) and Carnivora (27); a total of 25 species are endemic to Bolivia. In addition, 14 species of introduced mammals are listed. Additional records and taxonomic changes are expected as a result of biological inventories currently in execution, re-identification of specimens deposited in national and foreign mammal collections, and future taxonomic revisions.
Key words: Introduced species, Mammals, Native species, Taxonomic annotations, Taxonomy.
Este trabajo está dedicado a la memoria de Boris Ríos-Uzeda, Mario Baudoin Weeksy Wendy Townsend. Excelencia, compromiso e infatigable esfuerzo por el conocimiento y la conservación de la biodiversidad de Bolivia, es el legado que nos dejan y la luz que ilumina el camino de los que los seguimos. Queridos amigos, los llevamos en el corazón.
Introducción
Bolivia se encuentra entre los países más biodiversos del número de ecorregiones (Salazar-Bravo et al. 2002, Tarifa & planeta (Ibisch 2001). Esta elevada diversidad se debe a su Aguirre 2009). A pesar de que la biodiversidad es uno de los ubicación geográfica, su variada topografía y un gran patrimonios más importantes de la humanidad, se está perdiendo a tasas alarmantes (Ceballos et al. 2015). Con el fin de protegerla, los estados miembros firmantes del Convenio sobre la Diversidad Biológica (CDB) de las Naciones Unidas (ONU), entre ellos Bolivia, requieren identificar y monitorear la diversidad biológica, incluyendo desde los componentes estructurales hasta funcionales (Green et al. 2009).
La diversidad biológica es dinámica, evoluciona y cambia continuamente en respuesta a las fluctuaciones bióticas y abióticas y por esto, es necesario registrar y monitorear su estado en el tiempo y el espacio (Issac et al. 2004). Al momento de proponer estrategias claves de conservación, las listas de especies, actualizadas y taxonómicamente bien justificadas, informan la formulación de políticas adecuadas de manejo y protección de las especies (Daugherty et al. 1990, Hazevoet 1996, Brito 2004). Con 6399 especies vivientes documentadas, los mamíferos son uno de los grupos más carismáticos y representativos a nivel mundial (Burgin et al. 2018). El conocimiento sobre la diversidad de los mamíferos se ha incrementado notablemente en un período de 13 años (de 2005 al 2018); por ejemplo, Burgin et al. (2018) calcularon un incremento de 1058 especies vivientes (incluyendo 88 nuevos géneros y 14 familias recién reconocidas), siendo el Neotrópico la región con el mayor número de especies de mamíferos en el mundo. Estos avances sobre el conocimiento taxonómico también abarcaron a las especies de mamíferos en Bolivia. Por esto, es ineludible trabajar en la actualización taxonómica de la lista de los mamíferos presentes en el país.
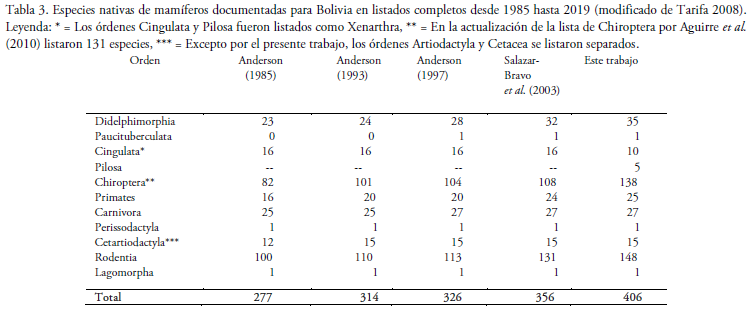
La última lista de mamíferos presentes en Bolivia data de hace 16 años (Salazar-Bravo et al. 2003). En este lapso se realizaron algunos esfuerzos para actualizar la lista de mamíferos para Bolivia. Una de las instancias más importantes fue la evaluación del estado de conservación de las especies de mamíferos para el Libro Rojo de la Fauna Silvestre de los Vertebrados de Bolivia, donde se consideraron un total de 389 especies de mamíferos (Tarifa & Aguirre 2009), lo que significó un incremento de 33 especies con respecto a la lista de Salazar-Bravo et al. (2003). Esta actualización constituyó la base para el Plan de Acción para los Mamíferos Amenazados de Bolivia (Ministerio de Medio Ambiente y Agua 2014) y para un análisis sobre prioridades de conservación de los mamíferos de Bolivia (Peñaranda & Simonetti 2015 y 2016, Tellería & Yapu-Alcázar 2016). Así mismo, se realizaron actualizaciones de algunos taxones, por ejemplo, los murciélagos (Aguirre et al. 2010) y los mamíferos medianos y grandes (Wallace et al. 2010, 2013a). No obstante, a la fecha, no se cuenta con una lista actualizada de las especies de mamíferos de Bolivia que refleje los avances y cambios taxonómicos que se han dado en los últimos 16 años. Por ello, y dada la importancia de contar con esta información, abordamos este trabajo con los siguientes objetivos: 1) generar una lista actualizada de las especies nativas de mamíferos presentes en Bolivia, 2) proporcionar anotaciones taxonómicas sobre los cambios en la lista de mamíferos nativos del país, y 3) actualizar la lista de las especies introducidas (domesticadas y/o asilvestradas) de mamíferos presentes en Bolivia.
Métodos
El ordenamiento taxonómico sigue la lista de Salazar-Bravo et al. (2003) complementada con los cambios producidos en la taxonomía de varios de los grupos de mamíferos. Para el orden Chiroptera se usó también la lista de Aguirre et al. (2010) y, con excepción de los órdenes Didelphimorphia, Rodentia y la familia Felidae, se consultaron los capítulos en el libro sobre mamíferos medianos y grandes de Bolivia editado por Wallace et al. (2010). Para realizar la actualización taxonómica revisamos publicaciones científicas y artículos recientes disponibles en revistas nacionales e internacionales. Las adiciones de nuevos registros de especies se consideraron únicamente si contaban con registros fidedignos (por ejemplo, especímenes depositados en colecciones científicas y/o fotografías inequívocas) y evitamos considerar especies registradas únicamente mediante observaciones. Las numerosas fuentes revisadas están mencionadas en las anotaciones taxonómicas en este trabajo. No se incluyeron las especies de presencia hipotética o probable en el país, aunque algunas se mencionan en las anotaciones taxonómicas. Tampoco se incluyen los subgéneros. Dada la relevancia taxonómica por la complejidad en la riqueza sistemática de los roedores y murciélagos, se incluyeron a las tribus dentro de este análisis, pero no así para el resto de los mamíferos. Las especies endémicas para el país se resaltan con negrillas en la lista de especies nativas de mamíferos. En una lista separada se presentan los mamíferos introducidos en el país con base en Rico et al. (2015).
Resultados
En Bolivia, al momento de finalizado este trabajo, se tenían registradas 406 especies de mamíferos, incluidos en 11 órdenes, 46 familias y 196 géneros. Del total de especies, 25 son endémicas de Bolivia. A continuación, se presenta los siguientes resultados: 1) La lista actualizada de especies de mamíferos de Bolivia, resaltando en negritas las especies endémicas; 2) las anotaciones taxonómicas en que se expone con detalle los cambios realizados con referencia a la lista de Salazar-Bravo et al. (2003) y para los murciélagos con respecto a la lista de Aguirre et al. (2010); 3) la lista de especies introducidas presentes en Bolivia.
Especies nativas
COHORTE Marsupialia Illiger, 1811
ORDEN DIDELPHIMORPHIA Gill, 1872
FAMILIA Didelphidae Gray, 1821
SUBFAMILIA Caluromyinae Reig et al., 1987
GÉNERO Caluromys J. A. Allen, 1900
Caluromys lanatus (Olfers, 1818)
Caluromys philander (Linnaeus, 1758)
SUBFAMILIA Didelphinae Gray, 1821
TRIBU Didelphini Gray, 1821
GÉNERO Chironectes Illiger, 1811
Chironectes minimus (Zimmermann, 1780)
GÉNERO Didelphis Linnaeus, 1758
Didelphis albiventris Lund, 1840
Didelphis marsupialis Linnaeus, 1758
Didelphis pernigra J. A. Allen, 1900
GÉNERO Lutreolina Thomas, 1910
Lutreolina crassicaudata (Desmarest, 1804)
Lutreolina massoia Martínez-Lanfranco, Flores, Jayat y D’Elía, 2014
GÉNERO Philander Brisson, 1762
Philander canus (Osgood, 1913)
TRIBU Metachirini Hershkovitz, 1992
GÉNERO Metachirus Burmeister, 1854
Metachirus myosuros (Temminck, 1824)
TRIBU Marmosini Reig, 1981
GÉNERO Marmosa Gray, 1821
SUBGÉNERO Marmosa Gray, 1821
Marmosa (Marmosa) macrotarsus (Wagner, 1842)
SUBGÉNERO Micoureus Lesson, 1842
Marmosa (Micoureus) constantiae (Thomas, 1904)
Marmosa (Micoureus) rapposa (Thomas, 1899)
Marmosa (Micoureus) rutteri Thomas, 1924
SUBGÉNERO Stegomarmosa Pine, 1972
Marmosa (Stegomarmosa) lepida (Thomas, 1888)
GÉNERO Monodelphis Burnett, 1830
SUBGÉNERO Mygalodelphys Pavan y Voss, 2016
Monodelphis kunsi Pine, 1975
Monodelphis osgoodi Doutt, 1938
Monodelphis peruviana (Osgood, 1913)
SUBGÉNERO Pyrodelphys Pavan y Voss, 2016
Monodelphis emiliae (Thomas, 1912)
SUBGÉNERO Monodelphis Burnett, 1830
Monodelphis domestica (Wagner, 1842)
Monodelphis glirina (Wagner, 1842)
Monodelphis sanctaerosae Voss, Pine y Solari 2012
TRIBU Thylamyini Hershkovitz, 1992
GÉNERO Cryptonanus Voss, Lunde y Jansa, 2005
Cryptonanus unduaviensis (Tate, 1931)
GÉNERO Gracilinanus Gardner y Creighton, 1989
Gracilinanus aceramarcae (Tate, 1931)
Gracilinanus peruanus (Tate, 1931)
GÉNERO Marmosops Matschie, 1916
SUBGÉNERO Sciophanes Díaz-Nieto, Jansa y Voss, 2016
Marmosops bishopi (Pine, 1981)
SUBGÉNERO Marmosops Matschie, 1916
Marmosops creightoni Voss, Tarifa y Yensen, 2004
Marmosops cf. impavidus
Marmosops noctivagus (Tschudi, 1845)
Marmosops ocellatus (Tate, 1931)
GÉNERO Thylamys Gray, 1843
SUBGÉNERO Thylamys Gray, 1843
Thylamys pallidior (Thomas, 1902)
Thylamys pusillus (Desmarest, 1804)
Thylamys sponsorius (Thomas, 1921)
Thylamys venustus (Thomas, 1902)
SUBFAMILIA Glironiinae Voss y Jansa, 2009
GÉNERO Glironia Thomas, 1912
Glironia venusta Thomas, 1912
ORDEN PAUCITUBERCULATA Ameghino, 1894
FAMILIA Caenolestidae Trouessart, 1898
GÉNERO Lestoros Oehser, 1934
Lestoros inca (Thomas, 1917)
COHORTE Placentalia Owen 1837
ORDEN CINGULATA Illiger, 1811
FAMILIA Dasypodidae Gray, 1821
SUBFAMILIA Dasypodinae Gray, 1821
GÉNERO Dasypus Linnaeus, 1758
Dasypus beniensis Lönnberg, 1942
Dasypus novemcinctus Linnaeus, 1758
Dasypus septemcinctus Linnaeus, 1758
FAMILIA Chlamyphoridae Bonaparte, 1850
SUBFAMILIA Euphractinae Winge, 1923
GÉNERO Chaetophractus Fitzinger, 1871
Chaetophractus vellerosus (Gray, 1865)
Chaetophractus villosus (Desmarest, 1804)
GÉNERO Euphractus Wagler, 1830
Euphractus sexcinctus (Linnaeus, 1758)
SUBFAMILIA Chlamyphorinae Bonaparte, 1850
GÉNERO Calyptophractus Fitzinger, 1871
Calyptophractus retusus (Burmeister, 1863)
SUBFAMILIA Tolypeutinae Gray, 1865
GÉNERO Cabassous McMurtrie, 1831
Cabassous unicinctus (Linnaeus, 1758)
GÉNERO Priodontes F. Cuvier, 1825
Priodontes maximus (Kerr, 1792)
GÉNERO Tolypeutes Illiger, 1811
Tolypeutes matacus (Desmarest, 1804)
ORDEN PILOSA Flower, 1883
FAMILIA Bradypodidae Gray, 1821
GÉNERO Bradypus Linnaeus, 1758
Bradypus variegatus Schinz, 1825
FAMILIA Cyclopedidae Pocock, 1924
GÉNERO Cyclopes Gray, 1821
Cyclopes catellus Thomas, 1928
FAMILIA Megalonychidae P. Gervais, 1855
GÉNERO Choloepus Illiger, 1811
Choloepus hoffmanni W. Peters, 1858
FAMILIA Myrmecophagidae Gray, 1825
GÉNERO Myrmecophaga Linnaeus, 1758
Myrmecophaga tridactyla Linnaeus, 1758
GÉNERO Tamandua Gray, 1825
Tamandua tetradactyla (Linnaeus, 1758)
ORDEN CHIROPTERA Blumenbach, 1779
FAMILIA Emballonuridae Gervais, 1855
SUBFAMILIA Emballonurinae Gervais, 1855
GÉNERO Cormura Peters, 1867
Cormura brevirostris (Wagner, 1843)
GÉNERO Cyttarops Thomas, 1913
Cyttarops alecto Thomas, 1913
GÉNERO Diclidurus Wied-Neuwied, 1820
Diclidurus albus Wied-Neuwied, 1820
GÉNERO Peropteryx Peters, 1867
Peropteryx kappleri Peters, 1867
Peropteryx macrotis (Wagner, 1843)
GÉNERO Rhynchonycteris Peters, 1867
Rhynchonycteris naso (Wied-Neuwied, 1820)
GÉNERO Saccopteryx Illiger, 1811
Saccopteryx bilineata (Temminck, 1838)
Saccopteryx canescens Thomas, 1901
Saccopteryx leptura (Schreber, 1774)
FAMILIA Phyllostomidae Gray, 1825
SUBFAMILIA Carolliinae Miller, 1924
GÉNERO Carollia Gray, 1838
Carollia benkeithi Solari y Baker, 2006
Carollia brevicauda (Schinz, 1821)
Carollia manu Pacheco, Solari y Velazco, 2004
Carollia perspicillata (Linnaeus, 1758)
SUBFAMILIA Desmodontinae Wagner, 1840
TRIBU Desmodontini Wagner, 1840
GÉNERO Desmodus Wied-Neuwied, 1826
Desmodus rotundus (É. Geoffroy, 1810)
GÉNERO Diaemus Miller, 1906
Diaemus youngi (Jentink, 1893)
TRIBU Diphyllini Baker, Solari, Cirranello y Simmons, 2016
GÉNERO Diphylla Spix, 1823
Diphylla ecaudata Spix, 1823
SUBFAMILIA Glossophaginae Bonaparte, 1845
TRIBU Choeronycterini Solmsen, 1998
GÉNERO Anoura Gray, 1838
Anoura aequatoris (Lönnberg 1921)
Anoura caudifer (É. Geoffroy, 1818)
Anoura cultrata Handley, 1960
Anoura fistulata Muchhala, Mena y Albuja, 2005
Anoura geoffroyi Gray, 1838
Anoura peruana (Tschudi, 1844)
GÉNERO Choeroniscus Tschudi, 1844
Choeroniscus minor (Peters, 1868)
GÉNERO Lichonycteris Thomas, 1895
Lichonycteris degener Miller, 1931
TRIBU Glossophagini Bonaparte, 1845
GÉNERO Glossophaga É. Geoffroy, 1818
Glossophaga soricina (Pallas, 1766)
SUBFAMILIA Glyphonycterinae Baker, Solari, Cirranello y Simmons, 2016
GÉNERO Glyphonycteris Thomas, 1896
Glyphonycteris behnii (Peters, 1865)
Glyphonycteris daviesi (Hill, 1964)
GÉNERO Trinycteris Sanborn, 1949
Trinycteris nicefori (Sanborn, 1949)
SUBFAMILIA Lonchophyllinae Griffiths, 1982
TRIBU Hsunycterini Parlos, Timm, Swier, Zeballos y Baker, 2014
GÉNERO Hsunycteris Parlos, Timm, Swier, Zeballos y Baker, 2014
Hsunycteris pattoni (Woodman y Timm, 2006)
Hsunycteris thomasi (J. A. Allen, 1904)
TRIBU Lonchophyllini Griffiths, 1982
GÉNERO Lionycteris Thomas, 1913
Lionycteris spurrelli Thomas, 1913
GÉNERO Lonchophylla Thomas, 1903
Lonchophylla dekeyseri Taddei, Vizotto y Sazima 1983
SUBFAMILIA Lonchorhininae Gray, 1806
GÉNERO Lonchorhina Tomes, 1863
Lonchorhina aurita Tomes, 1863
SUBFAMILIA Micronycterinae Van Den Bussche, 1992
GÉNERO Lampronycteris Sanborn, 1949
Lampronycteris brachyotis (Dobson, 1879)
GÉNERO Micronycteris Gray, 1866
Micronycteris hirsuta (Peters, 1869)
Micronycteris megalotis (Gray, 1842)
Micronycteris microtis Miller, 1898
Micronycteris minuta (Gervais, 1856)
Micronycteris yatesi Siles y Brooks, 2013
SUBFAMILIA Phyllostominae Gray, 1825
TRIBU Macrophyllini Gray, 1866
GÉNERO Macrophyllum Gray, 1838
Macrophyllum macrophyllum (Schinz, 1821)
GÉNERO Trachops Gray, 1847
Trachops cirrhosus (Spix, 1823)
TRIBU Phyllostomini Gray, 1825
GÉNERO Gardnerycteris Hurtado y Pacheco, 2014
Gardnerycteris crenulatum (É. Geoffroy, 1803)
GÉNERO Lophostoma d’Orbigny, 1836
Lophostoma brasiliense Peters, 1867
Lophostoma carrikeri (J. A. Allen, 1910)
Lophostoma silvicolum d’Orbigny, 1836
GÉNERO Phylloderma Peters, 1865
Phylloderma stenops Peters, 1865
GÉNERO Phyllostomus Lacépède, 1799
Phyllostomus discolor Wagner, 1843
Phyllostomus elongatus (É. Geoffroy, 1810)
Phyllostomus hastatus (Pallas, 1767)
GÉNERO Tonatia Gray, 1827
Tonatia bidens (Spix, 1823)
Tonatia saurophila Koopman y Williams, 1951
TRIBU Vampyrini Bonaparte, 1838
GÉNERO Chrotopterus Peters, 1865
Chrotopterus auritus (Peters, 1856)
GÉNERO Vampyrum Rafinesque, 1815
Vampyrum spectrum (Linnaeus, 1758)
SUBFAMILIA Rhinophyllinae Baker, Solari, Cirranello y Simmons, 2016
GÉNERO Rhinophylla Peters, 1865
Rhinophylla pumilio Peters, 1865
SUBFAMILIA Stenodermatinae Gervais, 1856
TRIBU Stenodermatini Gervais, 1856
GÉNERO Artibeus Leach, 1821
Artibeus anderseni Osgood, 1916
Artibeus concolor Peters, 1865
Artibeus glaucus Thomas, 1893
Artibeus gnomus Handley, 1987
Artibeus lituratus (Olfers, 1818)
Artibeus obscurus (Schinz, 1821)
Artibeus planirostris (Spix, 1823)
GÉNERO Chiroderma Peters, 1860
Chiroderma salvini Dobson, 1878
Chiroderma trinitatum Goodwin, 1958
Chiroderma villosum Peters, 1860
GÉNERO Enchisthenes K. Andersen, 1906
Enchisthenes hartii (Thomas, 1892)
GÉNERO Mesophylla Thomas 1901
Mesophylla macconnelli Thomas, 1901
GÉNERO Platyrrhinus Saussure, 1860
Platyrrhinus albericoi Velazco, 2005
Platyrrhinus brachycephalus (Rouk y Carter, 1972)
Platyrrhinus incarum (Thomas, 1912)
Platyrrhinus infuscus (Peters, 1880)
Platyrrhinus lineatus (É. Geoffroy, 1810)
Platyrrhinus masu Velazco, 2005
Platyrrhinus umbratus (Lyon, 1902)
GÉNERO Pygoderma Peters, 1863
Pygoderma bilabiatum (Wagner, 1843)
GÉNERO Sphaeronycteris Peters, 1882
Sphaeronycteris toxophyllum Peters, 1882
GÉNERO Uroderma Peters, 1865
Uroderma bilobatum Peters, 1866
Uroderma magnirostrum Davis, 1968
GÉNERO Vampyressa Thomas, 1900
Vampyressa thyone Thomas, 1909
GÉNERO Vampyriscus Thomas, 1900
Vampyriscus bidens (Dobson, 1878)
GÉNERO Vampyrodes Thomas, 1900
Vampyrodes caraccioli (Thomas, 1889)
TRIBU Sturnirini Miller, 1907
GÉNERO Sturnira Gray, 1842
Sturnira erythromos (Tschudi, 1844)
Sturnira giannae Velazco y Patterson, 2019
Sturnira lilium (É. Geoffroy, 1810)
Sturnira magna de la Torre, 1966
Sturnira oporaphilum (Tschudi, 1844)
Sturnira sorianoi Sánchez-Hernández, Romero-Almaraz y Schnell, 2005
Sturnira tildae de la Torre, 1959
FAMILIA Mormoopidae Saussure, 1860
GÉNERO Pteronotus Gray, 1838
Pteronotus gymnonotus (J. A. Wagner, 1843)
Pteronotus personatus (J. A. Wagner, 1843)
Pteronotus rubiginosus (J. A. Wagner, 1843)
FAMILIA Noctilionidae Gray, 1821
GÉNERO Noctilio Linnaeus, 1766
Noctilio albiventris Desmarest, 1818
Noctilio leporinus (Linnaeus, 1758)
FAMILIA Furipteridae Gray, 1866
GÉNERO Furipterus Bonaparte, 1837
Furipterus horrens (F. Cuvier, 1828)
FAMILIA Thyropteridae Miller, 1907
GÉNERO Thyroptera Spix, 1823
Thyroptera discifera (Lichtenstein y Peters, 1854)
Thyroptera tricolor Spix, 1823
FAMILIA Natalidae Gray, 1866
GÉNERO Natalus Gray, 1838
Natalus macrourus (Gervais, 1856)
FAMILIA Molossidae Gervais, 1856
SUBFAMILIA Molossinae Gervais, 1856
GÉNERO Cynomops Thomas, 1920
Cynomops abrasus (Temminck, 1827)
Cynomops planirostris (Peters, 1866)
GÉNERO Eumops Miller, 1906
Eumops auripendulus (Shaw, 1800)
Eumops chimaera Gregorin, Martins Moras, Acosta, Lobao Vasconcellos, Poma, Rodrigues dos Santos y Paca, 2016
Eumops glaucinus (Wagner, 1843)
Eumops hansae Sanborn, 1932
Eumops patagonicus Thomas, 1924
Eumops perotis (Schinz, 1821)
Eumops trumbulli (Thomas, 1901)
GÉNERO Molossops Peters, 1866
Molossops temminckii (Burmeister, 1854)
GÉNERO Molossus É. Geoffroy, 1805
Molossus currentium Thomas, 1901
Molossus molossus (Pallas, 1766)
Molossus pretiosus Miller, 1902
Molossus rufus É. Geoffroy, 1805
GÉNERO Neoplatymops Peterson, 1965
Neoplatymops mattogrossensis (Vieira, 1942)
GÉNERO Nyctinomops Miller, 1902
Nyctinomops aurispinosus (Peale, 1848)
Nyctinomops laticaudatus (É. Geoffroy, 1805)
Nyctinomops macrotis (Gray, 1840)
GÉNERO Promops Gervais, 1856
Promops centralis Thomas, 1915
Promops nasutus (Spix, 1823)
GÉNERO Tadarida Rafinesque, 1814
Tadarida brasiliensis (I. Geoffroy, 1824)
FAMILIA Vespertilionidae Gray, 1821
SUBFAMILIA Myotinae Tate, 1942
GÉNERO Myotis Kaup, 1829
Myotis albescens (É. Geoffroy, 1806)
Myotis dinellii Thomas, 1902
Myotis keaysi J. A. Allen, 1914
Myotis midastactus Moratelli y Wilson 2014
Myotis nigricans (Schinz, 1821)
Myotis oxyotus (Peters, 1867)
Myotis riparius Handley, 1960
SUBFAMILIA Vespertilioninae Gray, 1821
TRIBU Eptesicini Volleth y Heller, 1994
GÉNERO Eptesicus Rafinesque, 1820
Eptesicus andinus J. A. Allen, 1914
Eptesicus brasiliensis (Desmarest, 1819)
Eptesicus chiriquinus Thomas, 1920
Eptesicus diminutus Osgood, 1915
Eptesicus furinalis (d'Orbigny, 1847)
TRIBU Lasiurini Tate, 1942
GÉNERO Lasiurus Gray, 1831
Lasiurus blossevillii (Lesson & Garnot, 1826)
Lasiurus ega (Gervais, 1856)
Lasiurus villosissimus É. Geoffroy, 1806
TRIBU Nycticeiini Gervais, 1855
GÉNERO Rhogeessa H. Allen, 1866
Rhogeessa io Thomas, 1903
TRIBU Vespertilionini Gray, 1821
GÉNERO Histiotus Gervais, 1856
Histiotus diaphanopterus Feijó, Da Rocha y Althoff, 2015
Histiotus laephotis Thomas, 1916
Histiotus macrotus (Poeppig, 1835)
Histiotus montanus (Philippi y Landbeck, 1861)
Histiotus velatus (I. Geoffroy, 1824)
ORDEN PRIMATES Linnaeus, 1758
FAMILIA Aotidae Elliot, 1913
GÉNERO Aotus Illiger, 1811
Aotus azarae (Humboldt, 1811)
Aotus nigriceps (Dollman, 1909)
FAMILIA Atelidae Gray, 1825
GÉNERO Alouatta Lacépède, 1799
Alouatta caraya (Humboldt, 1812)
Alouatta sara Elliot, 1910
GÉNERO Ateles É. Geoffroy, 1806
Ateles chamek (Humboldt, 1812)
GÉNERO Lagothrix É. Geoffroy, 1812
Lagothrix lagotricha Pucheran, 1857
FAMILIA Callitrichidae Gray, 1821
GÉNERO Callimico Miranda Ribeiro, 1922
Callimico goeldii (Thomas, 1904)
GÉNERO Cebuella Gray, 1866
Cebuella pygmaea (Spix 1823)
GÉNERO Mico Lesson, 1840
Mico melanurus (É. Geoffroy, 1812)
GÉNERO Leontocebus Wagner, 1840
Leontocebus weddelli (Deville, 1849)
GÉNERO Saguinus Hoffmannsegg, 1807
Saguinus imperator (Goeldi, 1907)
Saguinus labiatus (É. Geoffroy, 1812)
FAMILIA Cebidae Bonaparte, 1831
GÉNERO Cebus Erxleben, 1777
Cebus unicolor Spix, 1823
GÉNERO Saimiri Voigt, 1831
Saimiri boliviensis (I. Geoffroy y de Blainville, 1834)
GÉNERO Sapajus Kerr, 1792
Sapajus apella (Linnaeus, 1758)
Sapajus cay (Illiger, 1815)
Sapajus macrocephalus (Spix, 1823)
FAMILIA Hominidae Gray, 1825
GÉNERO Homo Linnaeus, 1758
Homo sapiens Linnaeus, 1758
FAMILIA Pitheciidae Mivart, 1865
GÉNERO Pithecia Desmarest, 1804
Pithecia irrorata Gray, 1843
GÉNERO Plecturocebus Byrne, Rylands, Carneiro, Lynch Alfaro, Bertuol, da Silva, Messias, Groves, Mittermeier, Farias, Hrbek, Schneider, Sampaio y Boubli, 2016
Plecturocebus aureipalatii (Wallace, Gómez, Felton y Felton, 2006)
Plecturocebus donacophilus (d'Orbigny, 1836)
Plecturocebus modestus (Lönnberg, 1939)
Plecturocebus olallae (Lönnberg, 1939)
Plecturocebus pallescens (Thomas, 1907)
Plecturocebus toppini (Thomas, 1914)
ORDEN CARNIVORA Bowdich, 1821
FAMILIA Canidae Fischer von Waldheim, 1817
GÉNERO Atelocynus Cabrera, 1940
Atelocynus microtis (Sclater, 1883)
GÉNERO Cerdocyon Smith, 1839
Cerdocyon thous (Linnaeus, 1766)
GÉNERO Chrysocyon Smith, 1839
Chrysocyon brachyurus (Illiger, 1815)
GÉNERO Lycalopex Burmeister, 1854
Lycalopex culpaeus (Molina, 1782)
Lycalopex gymnocercus (Fischer, 1814)
GÉNERO Speothos Lund, 1839
Speothos venaticus (Lund, 1842)
FAMILIA Felidae Fischer von Waldheim, 1817
GÉNERO Leopardus Gray, 1842
Leopardus colocola (Molina, 1782)
Leopardus geoffroyi (d'Orbigny y Gervais, 1844)
Leopardus jacobita (Cornalia, 1865)
Leopardus pardalis (Linnaeus, 1758)
Leopardus tigrinus (Schreber, 1775)
Leopardus wiedii (Schinz, 1821)
GÉNERO Panthera Oken, 1816
Panthera onca (Linnaeus, 1758)
GÉNERO Puma Jardine, 1834
Puma concolor (Linnaeus, 1771)
GÉNERO Herpailurus Severtzov, 1858
Herpailurus yagouaroundi (É. Geoffroy, 1803)
FAMILIA Mephitidae Bonaparte, 1845
GÉNERO Conepatus Gray, 1837
Conepatus chinga (Molina, 1782)
FAMILIA Mustelidae Fischer von Waldheim, 1817
GÉNERO Eira Hamilton Smith, 1842
Eira barbara (Linnaeus, 1758)
GÉNERO Galictis Bell, 1826
Galictis cuja (Molina, 1782)
Galictis vittata (Schreber, 1776)
GÉNERO Lontra Gray, 1843
Lontra longicaudis (Olfers, 1818)
GÉNERO Mustela Linnaeus, 1758
Mustela frenata (Lichtenstein, 1831)
GÉNERO Pteronura Gray, 1837
Pteronura brasiliensis (Gmelin, 1788)
FAMILIA Procyonidae Gray, 1825
GÉNERO Bassaricyon J. A. Allen, 1876
Bassaricyon alleni Thomas, 1880
GÉNERO Nasua Storr, 1780
Nasua nasua (Linnaeus, 1766)
GÉNERO Potos É. Geoffroy y Cuvier, 1795
Potos flavus (Schreber, 1774)
GÉNERO Procyon Storr, 1780
Procyon cancrivorous (Cuvier, 1798)
FAMILIA Ursidae Fischer von Waldheim, 1817
GÉNERO Tremarctos Gervais, 1855
Tremarctos ornatus (Cuvier, 1825)
ORDEN PERISSODACTYLA Owen, 1848
FAMILIA Tapiridae Gray, 1821
GÉNERO Tapirus Brisson, 1762
Tapirus terrestris (Linnaeus, 1758)
ORDEN CETARTIODACTYLA Montgelard, Catzeflis y Douzery, 1997
SUBORDEN Suina Gray, 1868
FAMILIA Tayassuidae Palmer, 1897
GÉNERO Parachoerus Rusconi, 1930
Parachoerus wagneri (Rusconi, 1930)
GÉNERO Pecari
Pecari tajacu (Linnaeus, 1758)
GÉNERO Tayassu Fischer von Waldheim, 1814
Tayassu pecari (Link, 1795)
SUBORDEN Tylopoda Illiger, 1811
FAMILIA Camelidae Gray, 1821
GÉNERO Lama G. Cuvier, 1800
Lama glama (Linnaeus, 1758)
Lama guanicoe (Müller, 1776)
GÉNERO Vicugna Lesson, 1842
Vicugna pacos (Linnaeus, 1758)
Vicugna vicugna (Molina, 1782)
SUBORDEN Ruminantia Scopoli, 1777
FAMILIA Cervidae Goldfuss, 1820
GÉNERO Blastocerus Wagner, 1844
Blastocerus dichotomus (Illiger, 1815)
GÉNERO Hippocamelus Leuckart, 1816
Hippocamelus antisensis (d'Orbigny, 1834)
GÉNERO Mazama Rafinesque, 1817
Mazama americana (Erxleben, 1777)
Mazama chunyi (Hershkovitz, 1959)
Mazama gouazoubira (G. Fischer, 1814)
GÉNERO Odocoileus Rafinesque, 1832
Odocoileus virginianus (Zimmermann, 1780)
GÉNERO Ozotoceros Ameghino, 1891
Ozotoceros bezoarticus (Linnaeus, 1758)
SUBORDEN Whippomorpha Waddell, Okada y Hasegawa, 1999
INFRAORDEN Cetacea Brisson, 1762
FAMILIA Iniidae Gray, 1846
GÉNERO Inia d'Orbigny, 1834
Inia boliviensis (d'Orbigny, 1834)
ORDEN RODENTIA Bowdich, 1821
SUBORDEN Sciuromorpha Brandt, 1855
FAMILIA Sciuridae G. Fischer, 1817
SUBFAMILIA Sciurinae G. Fischer, 1817
GÉNERO Hadrosciurus J. A. Allen, 1915
Hadrosciurus spadiceus (Olfers, 1818)
GÉNERO Microsciurus J. A. Allen, 1895
Microsciurus flaviventer (Gray, 1867)
GÉNERO Notosciurus J. A. Allen, 1914
Notosciurus pucheranii (Fitzinger, 1867)
SUBORDEN Myomorpha Brants, 1855
FAMILIA Cricetidae G. Fischer, 1817
SUBFAMILIA Sigmodontinae Wagner, 1843
Sigmodontinae incertae sedis
GÉNERO Chinchillula Thomas, 1898
Chinchillula sahamae Thomas, 1898
TRIBU Abrotrichini D'Elia, Pardiñas, Teta y Patton, 2007
GÉNERO Abrothrix Waterhouse, 1837
Abrothrix andina (Philippi, 1858)
Abrothrix jelskii (Thomas, 1894)
TRIBU Akodontini Cockerell & Printz in Cockerell et al., 1914
GÉNERO Akodon Meyen, 1833
Akodon aerosus Thomas, 1913
Akodon albiventer Thomas, 1897
Akodon boliviensis Meyen, 1833
Akodon budini (Thomas, 1918)
Akodon caenosus Thomas, 1918
Akodon dayi Osgood, 1916
Akodon fumeus Thomas, 1902
Akodon kofordi Myers y Patton, 1989
Akodon lutescens J. A. Allen, 1901
Akodon mimus (Thomas, 1901)
Akodon pervalens Thomas, 1925
Akodon siberiae Myers y Patton, 1989
Akodon simulator Thomas, 1916
Akodon subfuscus Osgood, 1944
Akodon toba Thomas, 1921
Akodon varius Thomas, 1902
GÉNERO Juscelinomys Moojen, 1965
Juscelinomys huanchacae Emmons, 1999
GÉNERO Kunsia Hershkovitz, 1966
Kunsia tomentosus (Lichtenstein, 1830)
GÉNERO Lenoxus Thomas, 1909
Lenoxus apicalis (J. A. Allen, 1900)
GÉNERO Necromys Ameghino, 1889
Necromys amoenus (Thomas, 1900)
Necromys lactens (Thomas, 1918)
Necromys lasiurus (Lund, 1840)
GÉNERO Oxymycterus Waterhouse, 1837
Oxymycterus hiska Hinojosa, Anderson y Patton, 1987
Oxymycterus hucucha Hinojosa, Anderson y Patton, 1987
Oxymycterus inca Thomas, 1900
Oxymycterus juliacae J. A. Allen, 1900
Oxymycterus nigrifrons Osgood, 1944
Oxymycterus paramensis Thomas, 1902
TRIBU Andinomyini Salazar-Bravo, Pardiñas, Zeballos & Teta, 2016
GÉNERO Andinomys Thomas, 1902
Andinomys edax Thomas, 1902
GÉNERO Punomys Osgood, 1943
Punomys kofordi Pacheco y Patton, 1995
TRIBU Euneomyini Pardiñas, Teta & Salazar-Bravo, 2015
GÉNERO Neotomys Thomas, 1894
Neotomys ebriosus Thomas, 1894
TRIBU Ichthyomyini Cockerell & Printz in Cockerell et al., 1914
GÉNERO Chibchanomys Voss, 1988
Chibchanomys sp.
TRIBU Oryzomyini Vorontsov, 1959
GÉNERO Cerradomys Weksler, Percequillo y Voss, 2006
Cerradomys maracajuensis (Langguth y Bonvicino, 2002)
Cerradomys scotti (Langguth y Bonvicino, 2002)
GÉNERO Euryoryzomys Weksler, Percequillo y Voss, 2006
Euryoryzomys legatus (Thomas, 1925)
Euryoryzomys nitidus (Thomas, 1884)
GÉNERO Holochilus Brandt, 1835
Holochilus chacarius Thomas, 1906
Holochilus sciureus Wagner, 1842
GÉNERO Hylaeamys Weksler, Percequillo y Voss, 2006
Hylaeamys acritus (Emmons y Patton, 2005)
Hylaeamys perenensis (J. A. Allen, 1901)
Hylaeamys yunganus (Thomas, 1902)
GÉNERO Microryzomys Thomas, 1917
Microryzomys minutus (Tomes, 1860)
GÉNERO Neacomys Thomas, 1900
Neacomys amoenus Thomas, 1903
Neacomys vargasllosai Hurtado y Pacheco, 2017
GÉNERO Nectomys Peters, 1861
Nectomys apicalis Peters, 1861
Nectomys sp.
GÉNERO Nephelomys Weksler, Percequillo y Voss, 2006
Nephelomys keaysi (J. A. Allen, 1900)
Nephelomys levipes (Thomas, 1902)
GÉNERO Oecomys Thomas, 1906
Oecomys bicolor (Tomes, 1860)
Oecomys cleberi Locks, 1981
Oecomys mamorae (Thomas, 1906)
Oecomys phaeotis (Thomas, 1901)
Oecomys roberti (Thomas, 1904)
Oecomys sydandersoni Carleton, Emmons y Musser, 2009
Oecomys trinitatis (J. A. Allen y Chapman, 1893)
Oecomys sp.
GÉNERO Oligoryzomys Bangs, 1900
Oligoryzomys andinus (Osgood, 1914)
Oligoryzomys brendae Massoia, 1998
Oligoryzomys chacoensis (Myers y Carleton, 1981)
Oligoryzomys destructor (Tschudi, 1844)
Oligoryzomys occidentalis Contreras y Rosi, 1980
Oligoryzomys pachecoi Hurtado y D'Elía, 2018
GÉNERO Pseudoryzomys Hershkovitz, 1962
Pseudoryzomys simplex (Winge, 1887)
TRIBU Phyllotini Vorontsov, 1959
GÉNERO Andalgalomys Williams y Mares, 1978
Andalgalomys pearsoni (Myers, 1977)
GÉNERO Auliscomys Osgood, 1915
Auliscomys boliviensis (Waterhouse, 1846)
Auliscomys pictus (Thomas, 1884)
Auliscomys sublimis (Thomas, 1900)
GÉNERO Calomys Waterhouse, 1837
Calomys boliviae (Thomas, 1901)
Calomys callosus (Rengger, 1830)
Calomys laucha (G. Fisher, 1814)
Calomys lepidus (Thomas, 1884)
Calomys musculinus (Thomas, 1913)
Calomys tener (Winge, 1887)
GÉNERO Eligmodontia F. Cuvier, 1837
Eligmodontia hirtipes (Thomas, 1902)
GÉNERO Galenomys Thomas, 1916
Galenomys garleppii (Thomas, 1898)
GÉNERO Graomys Thomas, 1916
Graomys chacoensis (J. A. Allen, 1901)
Graomys domorum (Thomas, 1902)
GÉNERO Phyllotis Waterhouse, 1837
Phyllotis caprinus Pearson, 1958
Phyllotis osilae J. A. Allen, 1901
Phyllotis tucumanus (Thomas, 1912)
Phyllotis xanthopygus (Waterhouse, 1837)
GÉNERO Tapecomys Anderson y Yates, 2000
Tapecomys primus Anderson y Yates, 2000
Tapecomys wolffsohni (Thomas, 1902)
TRIBU Thomasomyini Steadman & Ray, 1982
GÉNERO Rhagomys Thomas, 1886
Rhagomys longilingua Luna y Patterson, 2003
GÉNERO Rhipidomys Tschudi, 1845
Rhipidomys austrinus Thomas, 1921
Rhipidomys gardneri Patton, da Silva y Malcolm, 2000
Rhipidomys leucodactylus (Tschudi, 1845)
GÉNERO Thomasomys Coues, 1884
Thomasomys andersoni Salazar-Bravo y Yates, 2007
Thomasomys aureus (Tomes, 1860)
Thomasomys australis Anthony, 1925
Thomasomys daphne Thomas, 1917
Thomasomys ladewi Anthony, 1926
Thomasomys oreas Anthony, 1926
SUBORDEN Hystricomorpha Brandt, 1855
FAMILIA Caviidae G. Fischer, 1817
SUBFAMILIA Caviinae G. Fischer, 1817
GÉNERO Cavia Pallas, 1766
Cavia aperea Erxleben, 1777
Cavia tschudii Fitzinger, 1867
GÉNERO Galea Meyen, 1833
Galea comes Thomas, 1919
Galea leucoblephara Burmeister, 1861
Galea musteloides Meyen, 1833
GÉNERO Microcavia H. Gervais y Ameghino, 1880
Microcavia niata (Thomas, 1898)
SUBFAMILIA Dolichotinae Pocock, 1922
GÉNERO Dolichotis Desmarest, 1819
Dolichotis salinicola Burmeister, 1876
SUBFAMILIA Hydrochoerinae Gray, 1825
GÉNERO Hydrochoerus Brisson, 1762
Hydrochoerus hydrochaeris (Linnaeus, 1766)
FAMILIA Cuniculidae G. S. Miller y Gidley, 1918
GÉNERO Cuniculus Brisson, 1762
Cuniculus paca (Linnaeus, 1766)
Cuniculus taczanowskii (Stolzmann, 1885)
FAMILIA Dasyproctidae Bonaparte, 1838
GÉNERO Dasyprocta Illiger, 1811
Dasyprocta azarae Lichtenstein, 1823
Dasyprocta variegata Tschudi, 1845
GÉNERO Myoprocta Thomas, 1903
Myoprocta pratti Pocock, 1913
FAMILIA Chinchillidae Bennett, 1833
SUBFAMILIA Chinchillinae Bennett, 1833
GÉNERO Chinchilla Bennett, 1829
Chinchilla chinchilla (Lichtenstein, 1830)
GÉNERO Lagidium Meyen, 1833
Lagidium viscacia (G. I. Molina, 1782)
SUBFAMILIA Lagostominae Wiegmann, 1835
GÉNERO Lagostomus Brookes, 1829
Lagostomus maximus (Desmarest, 1817)
FAMILIA Dinomyidae Alston, 1876
GÉNERO Dinomys Peters, 1873
Dinomys branickii Peters, 1873
FAMILIA Erethizontidae Bonaparte, 1845
GÉNERO Coendou Lacépède, 1799
Coendou bicolor (Tschudi, 1844)
Coendou prehensilis (Linnaeus, 1758)
Coendou rufescens (Gray, 1865)
FAMILIA Abrocomidae Miller and Gidley, 1918
GÉNERO Abrocoma Waterhouse, 1837
Abrocoma boliviensis Glanz y Anderson, 1990
Abrocoma cinerea Thomas, 1919
FAMILIA Ctenomyidae Lesson, 1842
GÉNERO Ctenomys Blainville, 1826
Ctenomys andersoni Gardner, Salazar-Bravo y Cook, 2014
Ctenomys boliviensis Waterhouse, 1848
Ctenomys conoveri Osgood, 1946
Ctenomys erikacuellarae Gardner, Salazar-Bravo y Cook, 2014
Ctenomys frater Thomas, 1902
Ctenomys leucodon Waterhouse, 1848
Ctenomys lessaii Gardner, Salazar-Bravo y Cook, 2014
Ctenomys lewisi Thomas, 1926
Ctenomys nattereri Wagner, 1848
Ctenomys opimus Wagner, 1848
Ctenomys steinbachi Thomas, 1907
Ctenomys yatesi Gardner, Salazar-Bravo y Cook, 2014
FAMILIA Echimyidae Gray, 1825
SUBFAMILIA Dactylominae Tate, 1935
GÉNERO Dactylomys I. Geoffroy St.-Hilaire, 1838
Dactylomys boliviensis Anthony, 1920
Dactylomys dactylinus (Desmarest, 1817)
Dactylomys peruanus J. A. Allen, 1900
SUBFAMILIA Echimyinae Gray, 1825
GÉNERO Isothrix Wagner, 1845
Isothrix bistriata Wagner, 1845
GÉNERO Makalata Husson, 1978
Makalata didelphoides (Desmarest, 1817)
SUBFAMILIA Eumysopinae Rusconi, 1935
GÉNERO Mesomys Wagner, 1845
Mesomys hispidus (Desmarest, 1817)
GÉNERO Proechimys J. A. Allen, 1899
Proechimys brevicauda (Günther, 1876)
Proechimys gardneri da Silva, 1998
Proechimys longicaudatus (Rengger, 1830)
Proechimys pattoni da Silva, 1998
Proechimys simonsi Thomas, 1900
Proechimys steerei Goldman, 1911
GÉNERO Thrichomys Trouessart, 1880
Thrichomys pachyurus Wagner, 1845
SUBFAMILIA Myocastorinae Ameghino 1902
GÉNERO Myocastor Kerr, 1792
Myocastor coypus (Molina, 1782)
FAMILIA Octodontidae Waterhouse, 1839
GÉNERO Octodontomys Palmer, 1903
Octodontomys gliroides (Gervais y d'Orbigny, 1844)
ORDEN LAGOMORPHA Brandt, 1855
FAMILIA Leporidae Fischer, 1817
GÉNERO Sylvilagus Gray, 1867
Sylvilagus brasiliensis Linnaeus, 1758
Anotaciones taxonómicas
DIDELPHIMORPHIA
El orden Didelphimorphia fue revisado ampliamente en su clasificación por Voss & Jansa (2009) quienes propusieron cambios importantes a nivel de subfamilias y tribus. En la lista de Salazar-Bravo et al. (2003) sólo se reconocían dos subfamilias: Caluromyinae y Didelphinae, mientras que en esta revisión reconocemos adicionalmente a Glironiinae siguiendo la taxonomía de Voss & Jansa (2009; ver la justificación más adelante). Por otra parte, la compilación de este orden por Gardner (2007) incluyó tres tribus en la subfamilia Didelphinae: Didelphini, Metachirini y Monodelphini, en tanto que la revisión de Voss & Jansa (2009) adicionó dos tribus nuevas (Marmosini y Thylamyini), y eliminó una (Monodelphini), por lo que a la fecha se reconocen cuatro tribus. El género Monodelphis se incluye ahora junto con Marmosa dentro de la tribu Marmosini.
Lutreolina Un análisis filogenético empleando caracteres moleculares y morfológicos por Martínez-Lanfranco et al. (2014) demostró la existencia de una especie no reconocida hasta ese momento y que se describió como Lutreolina massoia. Esta nueva especie es endémica del bosque montano boliviano-tucumano y tiene registros conocidos para los departamentos bolivianos de Tarija y Chuquisaca y las provincias argentinas de Jujuy, Salta y Tucumán. Los límites del rango de distribución de esta nueva especie no están completamente definidos. Especímenes de L. crassicaudata provenientes de las sabanas de los departamentos del Beni, La Paz (Pampas del Heath) y del sur de Perú corresponden a especímenes con medidas más grandes que las conocidas para L. massoia, y aunque se asignaron de manera provisional a la subespecie L. crassicaudata crassicaudata, es necesario evaluar su identidad taxonómica.
Philander El género fue recientemente revisado por Voss et al. (2018) usando técnicas moleculares y morfométricas. Estos autores reconocieron ocho especies distribuidas en bosques tropicales y subtropicales del Neotrópico, desde el sur de México hasta el norte de Argentina. Según estos autores, Philander opossum (Linnaeus, 1758), la especie incluida en la lista de Salazar-Bravo et al. (2003), está restringida al noreste de Sudamérica, mientras que P. canus corresponde a las poblaciones presentes en Bolivia.
Metachirus La taxonomía del género Metachirus ha cambiado radicalmente en los últimos años; por mucho tiempo fue considerado monotípico con Metachirus nudícaudatus (E. Geoffroy, 1803) abarcando un amplio rango de distribución desde el sur de México hasta el norte de Argentina. Con base en análisis morfológicos y morfométricos, Vieira (2006) confirmó patrones de variación genética encontrada en otros estudios y propuso el reconocimiento como especies plenas para varios taxones previamente reconocidos como subespecies. Voss y colaboradores (2019) aumentaron el número de caracteres e incluyeron secuencias del citocromo- b; estos autores restringieron M. nudicaudatus al noreste de la Amazonia, concluyendo que la especie de Metachirus presente en Bolivia es M. myosuros. Sin embargo, recientes inventarios biológicos por parte de Wildüfe Conservation Society (WCS) en el Parque Nacional y Área Natural de Manejo Integrado Madidi registraron especímenes de Metachirus con tallas corporales menores (entre 25 y 30%) y diferencias significativas en caracteres craneales a los descritos para M. myosuros por Voss et al. (2019); estos resultados sugieren que en Bolivia existe más de una especie de Metachirus (N. Bernal datos no publicados).
Marmosa El género fue revisado por Gutiérrez et al. (2010), Rossi et al. (2010) y Voss et al. (2014). En esta última revisión se reconocieron cinco subgéneros, de los cuales tres están presentes en Bolivia: Marmosa, Micoureus y Stegomarmosa. La especie M. (Marmosa) macrotarsus es el taxón reconocido para Bolivia, toda vez que fue elevada al rango de especie y atendiendo a una definición más restringida (al este de la Amazonia y el bosque Atlántico) de Marmosa murina (Linnaeus, 1758), que fue la especie incluida en la lista de Salazar-Bravo et al. (2003).
En la lista de Salazar-Bravo et al. (2003), Micoureus Gardner y Creighton, 2008 fue considerado un género separado de Marmosa, en tanto que en la presente lista se considera como un subgénero de Marmosa siguiendo a Voss et al. (2004), Voss & Jansa (2009) y Gutiérrez et al. (2010). Se reconocieron tres especies para Bolivia: M. (Micoureus) constantiae, M. (Micoureus) demerarae (Thomas, 1905) y M. (Micoureus) regina (Thomas, 1898) (Voss et al. 2004, Voss & Jansa 2009, Gutiérrez et al. 2010). En una revisión taxonómica reciente del subgénero Micoureus por De Lima Silva et al. (2019) se reconoció como especie plena a M. (Micoureus) budini Thomas, 1920, anteriormente considerada una subespecie de M. constantiae (Anderson 1997, Salazar-Bravo et al. 2003). Se aplicó este nombre a las poblaciones bolivianas de la región central, este y sur, abarcando localidades en los departamentos de Cochabamba, Santa Cruz, Chuquisaca y Tarija. Para poblaciones del norte y noreste de Bolivia (departamentos de Pando y Santa Cruz) se utilizó el nombre de M. (Micoureus) constantiae. Es importante señalar que en la revisión realizada por De Lima Silva et al. (2019) no incluyó especímenes del departamento de La Paz.
La validez de M. (Micoureus) budini para poblaciones bolivianas no fue aceptada por Voss et al. (2019), quienes asignaron el nombre M. (Micoureus) rapposa para las poblaciones de elevaciones medias en los bosques nublados andinos desde el departamento de Junín en Perú a través de los Yungas de Bolivia hacia el noreste de Argentina, y también para las poblaciones de tierras bajas del Cerrado, desde el este de Bolivia a través del centro de Brasil hacia el este de Paraguay. En este trabajo seguimos la propuesta de Voss et al. (2019).
De Lima Silva et al. (2019) indicaron la presencia de M. regina (Thomas, 1898) para Bolivia. Sin embargo, Voss et al. (2019) consideraron que ese nombre no es atribuible paralas poblaciones de Micoureus en la Amazonia, siendo el nombre apropiado el de M. (Micoureus) rutteri. Finalmente, tanto De Lima Silva et al. (2019) como Voss et al. (2019) restringieron a .M. (Micoureus) demerarae (Thomas, 1905) para localidades desde el centro-este de Brasil hacia el norte de Sudamérica, por lo que esta especie, como se la conoce ahora, no está presente en Bolivia. Las especies en el subgénero Micoureus están actualmente en revisión y por ello, el arreglo taxonómico propuesto podría cambiar (R. Voss 2019, com. pers.). Finalmente, el subgénero Stegomarmosa comprende una sola especie en Bolivia: M. (Stegomarmosa) lepida.
Monodelphis El género ha sido revisado por Solari (2007), Pavan et al. (2014) y Pavan & Voss (2016). Pavan & Voss (2016) proponen cinco subgéneros que constituyen grupos monofiléticos con características morfológicas diagnósticas bien definidas; bajo este esquema taxonómico, en Bolivia están presentes tres subgéneros: Monodelphis, Mygalodelphys y Pyrodelphys. En Bolivia, el subgénero Monodelphis comprende tres especies: M. (Monodelphis) domestica, M. (Monodelphis) glirina y M. (Monodelphis) sanctarosae. Esta última fue descrita como nueva para la ciencia por Voss et al. (2012). El holotipo proviene de Santa Rosa de la Roca, departamento de Santa Cruz y difiere claramente de otras especies del grupo en tamaño, caracteres morfológicos cualitativos y secuencias del citocromo-¿ (Voss et al. 2012). Desde el 2012, M. sanctarosae no ha sido reportada para otras localidades dentro o fuera de Bolivia, por lo que a la fecha es considerada como una especie endémica de la región de la Chiquitanía, al este del departamento de Santa Cruz.
Dentro del subgénero Mygalodelphys se encuentran tres especies: M. (Mygalodelphys) kunsi, M. (Mygalodelphys) osgoodi y M. (Mygalodelphys) peruviana. S alazar-Bravo et al. (2003) listaron a Monodelphis peruviana como sinónimo de Monodelphis adusta, pero de acuerdo con la revisión de Solari (2007), M. adusta tiene una distribución restringida al norte de Sudamérica y por ello adoptamos el nombre sugerido por Solari (2007) para la especie presente en Bolivia. Finalmente, en el subgénero Pyrodelphys está comprendida una sola especie: M. (Pyrodelphys) emiliae.
Gracilinanus El género fue revisado por Voss et al. (2005) donde también se describió un nuevo género, Cryptonanus. Estos dos géneros presentan características morfológicas diagnósticas distintas y los análisis filogenéticos mostraron que son cercanos, pero no son taxones hermanos. En el nuevo género Cryptonanus se encuentra C. unduaviensis (listada como parte del género Gracilinanus en Salazar-Bravo et al. 2003). Si bien hay mención reciente de Cryptonanus chacoensis para Bolivia (e.g., Gardner 2007, de la Sancha & D'Elía 2015), no existen al momento especímenes confirmados de esta especie en el país.
Dentro del género Gracilinanus están presentes en Bolivia dos especies: G aceramarcae y G peruanus. Esta última fue listada como G. agilis (Burmeister, 1854) en Salazar-Bravo et al. (2003). No obstante, Semedo et al. (2015) en una revisión sobre la taxonomía y relaciones filogenéticas de Marmosa agilis peruana Tate, 1931, propuso, con base en datos morfológicos y moleculares, la validez de M. peruana como especie plena bajo el nombre Gracilinanus peruanus. El rango de distribución de esta especie abarca desde el centro de Perú, por el centro de Bolivia hasta el oeste de Brasil, en los estados de Rondónia y el noroeste de Mato Grosso. La taxonomía y distribución del género Gracilinanus es poco conocida y por ello existen vacíos en su distribución que requieren ser resueltos (Semedo et al. 2015).
Marmosops La taxonomía y distribución de las especies del género Marmosops en Bolivia fue revisada por Voss et al. (2004), en tanto que, Díaz-Nieto & Voss (2016) y Díaz-Nieto et al. (2016) revisaron el género completo en todo su rango de distribución. La revisión de Voss et al. (2004) adicionó tres especies de Marmosops a la lista de Salazar-Bravo et al. (2003), incluyendo una nueva especie para la ciencia y endémica de Bolivia: Marmosops creightoni. El holotipo proviene del valle de Zongo, en el departamento de La Paz (Voss et al. 2004). Las otras dos especies fueron: Marmosops "impavidus" y Marmosops noctivagus. Consideramos Marmosops dorothea de la lista de Salazar-Bravo et al. (2003) como sinónimo de Marmosops noctivagus (Voss et al. 2004, Voss & Jansa 2009, Díaz-Nieto et al. 2016). Así mismo, están presentes en Bolivia, Marmosops ocellatus y Marmosops bishopi (Voss et al. 2004, Voss & Jansa 2009, Díaz-Nieto et al. 2016), que ya fueron incluidas en Salazar-Bravo et al. (2003).
Las revisiones de Díaz-Nieto & Voss (2016) y Díaz-Nieto et al. (2016) reconocieron dos subgéneros: Sciophanes y Marmosops. En el nuevo subgénero Sciophanes se incluye a M. (Sciophanes) bishopi, mientras que en el subgénero Marmosops se incluye a cuatro especies: M. (Marmosops) creightoni, M. (Marmosops) "impavidus", M. (Marmosops) noctivagus y M. (Marmosops) ocellatus (Díaz-Nieto et al. 2016, Díaz-Nieto & Voss 2016). La forma nominal "impavidus"'no está claramente identificada como miembro del subgénero Marmosops (Díaz-Nieto et al. 2016), pero conservadoramente, la mantenemos en la presente lista hasta que se aclare su estatus.
Thylamys El género ha sido revisado por Giarla et al. (2010), Giarla et al. (2014) y Palma et al. (2014). Con base en marcadores moleculares, análisis filogenético y métodos morfológicos Giarla et al. (2010) reconocieron dos subgéneros: Xerodelphys y Thylamys. En Bolivia no están presentes especies en el subgénero Xerodelphys, en tanto que en el subgénero Thylamys están comprendidas cuatro de las siete especies reconocidas a la fecha: T. (Thylamys)pallidior, T. (Thylamys) pusillus, T. (Thylamys) sponsorius y T (Thylamys) venustus. En la presente lista adicionamos una nueva especie para Bolivia, Thylamys sponsorius, especie del grupo venustus distribuida al sur de Bolivia y Argentina (Giarla et al. 2010, Giarla et al. 2014, Palma et al. 2014). Así mismo, hemos adoptado la nomenclatura propuesta por Giarla et al. (2010) y Palma et al. (2014) para dos especies previamente listadas en Salazar-Bravo et al. (2003) como Thylamyspusilla (ahora T. pusillus) y Thylamys venusta (ahora T. venustus). En la revisión de Giarla et al. (2010), Thylamys macrura (ahora T. macrurus) listada en Salazar-Bravo et al. (2003), ha sido restringida al este de Paraguay y Mato Grosso do Sul (Brasil), y por esto queda excluida de la presente lista para Bolivia.
Glironia - El género fue incluido en Salazar-Bravo et al. (2003) en la subfamilia Caluromyinae, siguiendo la clasificación de Anderson (1997). El género Glironia fue también considerado como parte de la subfamilia Caluromyinae en la compilación de Gardner (2007). Sin embargo, en el presente listado aceptamos la propuesta de Voss & Jansa (2009) que incluyen a Glironia como parte de la nueva subfamilia Glironiinae dentro de la familia Didelphidae.
CINGULATA
Los órdenes Cingulata y Pilosa fueron citados como subórdenes en el orden Xenarthra (Cope, 1889) en Salazar-Bravo et al. (2003) siguiendo a Delsuc et al. (2001). Sin embargo, en la compilación de Gardner (2007), siguiendo la propuesta por McKenna & Bell (1997), Xenarthra constituye un magnaorden que comprende dos órdenes con especies vivientes: Cingulata y Pilosa. El orden Cingulata, según los análisis filogenéticos de Gibb et al. (2015) incluye a dos familias: Dasypodidae y Chlamyphorydae, y además tiene soporte monofilético para las cuatro subfamilias Dasypodinae, Euphractinae, Chlamyphorinae, y Tolypeutinae; en tanto que el orden Pilosa comprende cuatro familias: Myrmecophagidae, Cyclopedidae, Bradypodidae y Megalonychidae.
Dasypodidae
Chaetophractus Estudios taxonómicos recientes, con base en análisis genéticos y morfológicos, han sugerido que Chaetophractus nationi es un sinónimo de C. vellerosus (Abba et al. 2015, Poljak et al. 2018). En este trabajo adoptamos esta taxonomía, pero recalcamos la necesidad de conducir estudios adicionales que pongan a prueba esta hipótesis.
Calyptophractus Recientes análisis filogenéticos por Delsuc et al. (2012) sugieren que las dos especies de pichiciegos, Chlamyphorus truncatus y Ch. retusus, pertenecen a géneros distintos, posición que aceptamos en esta revisión. Por tanto, la especie Chlamyphorus retusus listada en Salazar-Bravo et al. (2003) pertenece al género Calyptophractus.
Dasypus Revisiones taxonómicas por Feijó & Cordeiro-Estrela (2016) y Feijó et al. (2018) sugirieron que Dasypus kappleri es en realidad un complejo de tres especies, cada una con distribuciones separadas. Estos autores restringen Dasypus kappleri al noreste de Sudamérica, siendo la especie presente en Bolivia Dasypus beniensis, la cual reemplaza en la presente lista a D. kappleri listada en Salazar-Bravo et al. (2003).
PILOSA
Si bien el trabajo de Preslee et al. (2019) recientemente ha mostrado que existiría parafilia de Megalonichidae, situando a Choloepus dentro de la familia Mylodontidae, Delsuc et al. (2019) manteienen a los perezosos de dos dedos dentro de la familia Megalonichidae y esta es la clasificación que mantenemos en esta lista.
Cyclopes Miranda et al. (2017) revisaron la confusa taxonomía del género Cyclopes. Luego de un análisis integral de datos morfológicos, morfométricos y moleculares sugirieron que lo que era considerado una sola especie, en realidad incluía siete especies diferentes a lo largo de su distribución. En Bolivia, a la fecha, sólo una especie está confirmada, C. catellus, que reemplaza a C. dydactylus catellus listada en Salazar-Bravo et al. (2003).
CHIROPTERA
Desde la publicación de Salazar-Bravo et al. (2003), la lista de especies de murciélagos presentes en Bolivia fue actualizada por Aguirre et al. (2010). Desde entonces, se han reportado nuevas adiciones y cambios taxonómicos a nivel de varias subfamilias, tribus, géneros y especies.
Emballonuridae
Para la taxonomía superior seguimos la clasificación de Lim et al. (2007) que incluye a todos los géneros del Neotrópico en la subfamilia Emballonurinae, tribu Diclidurini.
Phyllostomidae
La familia Phyllostomidae es la segunda en diversidad entre los Chiroptera (Baker et al. 2016). Para la taxonomía superior, seguimos la revisión de la familia Phyllostomidae por Baker et al. (2016) y Cirranello et al. (2016), quienes con base en genética y morfología propusieron la organización taxonómica de esta familia en 11 subfamilias, 12 tribus y 9 subtribus. Las nuevas subfamilias que se encuentran presentes en Bolivia son: Micronycterinae (Lampronycteris y Micronycteris), Lonchorhininae (Lonchorhind), Glyphonycterinae (Glyphonycteris y Trinycteris) y Rhinophyllinae (Rhinophylla). Las tres primeras pertenecían previamente a la subfamilia Phyllostominae y la última a la subfamilia CaroUiinae. Se definieron tribus en las siguientes subfamilias: dos en Desmodontinae (Desmodontini y Diphyllini), tres en Glossophaginae (dos en Bolivia, Choeronycterini y Glossophagini), dos en Lonchophyllinae (Hsunycterini y Lonchophyllini), tres en Phyllostominae (Macrophyllini, Phyllostomini y Vampyrini) y dos en Stenodermatinae (Stenodermatini y Sturnirini). En el presente trabajo no incluimos el nivel taxonómico de subtribus.
Anoura El registro de Anoura fistulata por Mantilla-Meluk et al. (2014) en la localidad de Azero, Chuquisaca fue invalidado por Calderón-Acevedo & Muchhala (2018), quienes revisaron el espécimen y determinaron que en realidad pertenece a A. caudifer. Sin embargo, dos especímenes fueron colectados recientemente en el Parque Nacional y Área Natural de Manejo Integrado Madidi, en localidades más cercanas al registro en Perú (Siles & Wallace, en prep.), por lo que revalidamos la presencia de esta especie en Bolivia.
Lonchophylla El género Lonchophylla fue revisado por Parios et al. (2014), quienes al mismo tiempo describieron un nuevo género (Hsunycteris) para las especies previamente conocidas para Bolivia como L. pattoni y L. thomasi. En la revisión y análisis filogenético de la tribu Lonchophyllini, Woodman y Timm (2006) asignaron dos especímenes colectados en la meseta de Huanchaca a L. dekeyseri, la que a la fecha es la única especie en el género Lonchophyla conocida en Bolivia. Moratelli & Dias (2015) argüyeron que estos especímenes son bastante diferentes de individuos en otras poblaciones de la especie y sugirieron una re-examinación de los mismos. Incluimos a L. dekeyseri en esta lista hasta que se realice dicha revisión.
Hsunycteris El estudio por Parios et al. (2014) sugirió la inclusión de cuatro géneros en la subfamilia Lonchophyllinae: Lonchophylla sensu stricto, Lionycteris, Xeronycteris y Platalina. La lista por Aguirre et al. (2010) incluyó a Lonchophylla thomasi, la que está en la presente lista como Hsunycteris thomasi. Velazco et al. (2017) describieron una nueva especie de Hsunycteris para el Perú y mencionaron entre los ejemplares analizados para la comparación, la presencia de Hsunycteris pattoni proveniente de los departamentos de Beni (1.5 km río abajo Costa Marques) y Santa Cruz (Meseta de Huanchaca, Parque Nacional Noel Kemppf Mercado, especie que adicionamos a la lista para Bolivia.
Gardnerycteris Con base en una revisión filogenética, Hurtado-Miranda & Pacheco (2014) analizaron morfológicamente el género Mimon, encontrando que el mismo es polifilético y lo separaron en dos géneros: Mimon y Gardnerycteris. Este último está presente en Bolivia con una especie (Gardnerycteris crenulatum) la que fue listada por Aguirre et al. (2010) en el género Mimon.
Micronycteris En una revisión del género Micronycteris, Siles et al. (2013) describieron una nueva especie para la ciencia: M. yatesi, que se encuentra en las ecorregiones de los Yungas, Cerrado y Bosques Secos Interandinos, constituyéndose en el primer murciélago endémico para Bolivia. Uno de los paratipos en la descripción de M. yatesi fue la base del registro de Micronycteris sanborni en Bolivia (Brooks et al. 2001), por lo que esa especie no está presente en el país. Adicionalmente, retiramos de esta lista a M. schmidtorum, porque el registro se basó en un espécimen que no se encuentra depositado en una colección científica (Terán 2010), y porque en la revisión genética y morfológica de los especímenes del género por Siles et al. (2013) se concluyó que, a la fecha, esta especie no se encuentra registrada en Bolivia.
Tonatia Paca et al. (2012) reportaron tres ejemplares de Tonatia bidens provenientes del bosque ribereño, el chaparral de Abayoy y del Bosque Seco Chiquitano del departamento de Santa Cruz. Su presencia en Bolivia significa una ampliación de su distribución de casi 240 km al sur respecto del registro más próximo en Brasil.
Artibeus - Baker et al. (2016) y Cirranello et al. (2016) definieron al género Dermanura como un subgénero de Artibeus, por lo que en la presente lista las especies anteriormente incluidas en el género Dermanura se consideran en el género Artibeus: Artibeus (Dermanura) anderseni,A (Dermanura) glaucus y A. (Dermanura) gnomus. El resto de las especies pertenecen al subgénero Artibeus.
Platyrrhinus Velazco et al. (2018), mediante una aproximación integrando morfometría y modelación de nicho y genética, confirmaron que P. nigellus es un sinónimo subjetivo de P. umbratus, por lo que esta última especie es la que está presente en Bolivia, mientras que P. incluye en la lista de especies para el país.
Sturnira Una revisión filogenética del género Sturnira por Velazco & Patterson (2013) sugirió que 5. lilium consistía en un complejo de siete especies y limitaron la distribución de S. lilium al Escudo Brasilero (Le., bosque Atlántico, Cerrado, Caatinga y Chaco). Por lo tanto, S. lilium sensu stricto quedó restringido a la región sureste de Bolivia, en el Chaco y Chiquitanía. Recientemente Velazco & Patterson (2019) describieron una nueva especie como Sturnira giannae, perteneciente anteriormente al complejo de especies 5. lilium. Esta nueva especie se distribuye en la región amazónica del norte de Bolivia, en los departamentos del Beni y Pando. Estas especies se consideran alopátricas (Velazco & Patterson 2019), por ello se necesita evaluar las poblaciones de regiones intermedias (norte de Santa Cruz, Beni, La Paz, Cochabamba, Chuquisaca y Tarija). Ambas especies pueden ser discriminadas con base en caracteres morfológicos, lo cual facilita la revisión de los especímenes de Bolivia para determinar su distribución, tarea que está pendiente.
Natalidae
Natalus El género Natalus para Sudamérica, y Bolivia en particular, ha recibido mucha atención dando como resultado cambios de nombre. Salazar-Bravo et al. (2003) listaron a Natalus stramineus como la especie presente en Bolivia. Trabajos posteriores restringieron la distribución de esa especie a Centroamérica y el norte de Sudamérica, y elevaron de subespecie a especie a las poblaciones de esta parte de la región como Natalus espiritosantensis (Tejedor 2006, Aguirre et al. 2010). Sin embargo, Garbino & Tejedor (2013) demostraron que N. espiritosantensis no era el nombre más antiguo disponible para la especie al sur del Amazonas, debiendo ser considerado el nombre de N. macrourus como el válido. Estamos de acuerdo con este cambio y lo incluimos en la presente lista.
Molossidae
Eumops En una evaluación del género Eumops, Gregorin et al. (2016) realizaron un análisis filogenético basado en caracteres morfológicos y datos del gen mitocondrial citocromo-b, producto de ello describieron una nueva especie: Eumops chimaera, con ejemplares provenientes de Bolivia, de la Tierra Comunitaria de Origen Turubo Este, en el departamento de Santa Cruz. Esta especie representa una adición a la lista para Bolivia.
Vespertilionidae
Eptesicus Poma Urey et al. (2019) reportaron dos especies del género Eptesicus para Bolivia: E. brasiliensis y E. diminutus. El registro de E. brasiliensis está apoyado por un espécimen colectado en 1984 por S. Anderson en Comarapa (departamento de Santa Cruz), que fue publicado anteriormente como E. andinus (Anderson 1997) y posteriormente como E. chiriquinus (Davis & Gardner 2008). Este cambio no afecta al registro de E. chiriquinus, con base en especímenes colectados en los departamentos de Chuquisaca y Potosí (Siles 2007). Eptesicus diminutus cuenta con dos ejemplares de referencia provenientes del departamento de Santa Cruz (Poma Urey et al. 2019).
Histiotus Hoofer & Van Den Bussche (2003) concluyeron que genéticamente Histiotus es un subgénero de Eptesicus, pero seguimos a Handley & Gardner (2008) en considerarlo un género separado. Acosta & Venegas (2006) reportaron por primera vez a Histiotus macrotus para el país, en base a dos especímenes colectados en el departamento de Santa Cruz. Uno de esos registros aún es válido, pero el otro fue reidentificado por Feijó et al. (2015) como H. diaphanopterus, una especie recientemente descrita. Otros registros de H. diaphanopterus para Bolivia provienen del Cerrado de Pampagrande (Santa Cruz) y de Vallegrande (Fernandes Semedo et al. 2016).
Lasiurus La tribu Lasiurini fue revisada, con base en datos genéticos, por Baird et al. (2015, 2017) quienes propusieron dividir Lasiurus en tres géneros (Aeorestes, Dasypterus y Lasiurus). Dasypterus Peters, 1870 fue considerado un género separado en las listas de Salazar-Bravo et al. (2003) y Aguirre et al. (2010), pero ha sido considerado un subgénero de Lasiurus por Simmons (2005), Gardner & Handley (2007), entre otros. La división de Lasiurus fue rechazada por Ziegler et al. (2016) debido a que la monofilia del género no es cuestionada en ningún estudio y porque este cambio violaría uno de los principios fundamentales de la nomenclatura zoológica que implica el mantener la estabilidad, siempre que sea posible. Posteriormente, este cambio también fue rechazado por Simmons & Cirranello (2019), por lo que en la presente lista mantenemos al género Lasiurus como el único válido. Por otro lado, Baird et al. (2015) elevaron la subespecie L. cinereus villosissimus, distribuida en Sudamérica, a rango de especie y restringieron L. cinereus a Norteamérica. Este cambio también fue adoptado por Simmons y Cirranello (2019) y es el que seguimos en la presente lista, por ello L. cinereus es reemplazado por L. villosissimus.
Myotis Sustentados en caracteres morfológicos y diferencias en el color del pelaje, Moratelli & Wilson (2014) describieron a Myotis midastactus con base en especímenes provenientes de las sabanas de Bolivia de los departamentos de Beni y Santa Cruz. Posteriormente ampliaron su distribución a Paraguay (Moratelli et al. 2015), por lo que dejó de ser una especie endémica para Bolivia. Myotis simus está confinada exclusivamente al centro-norte de la cuenca del Amazonas en el Brasil.
PRIMATES
Desde la lista de Salazar-Bravo et al. (2003) se han dado varios cambios en la taxonomía de los primates, que exponemos a continuación. Siguiendo a Anderson (1997), incluimos en la presente lista al hombre (Homo sapiens).
Callitrichidae
Callithrix Tras el reconocimiento de tres géneros de titíes, aquellos presentes en la selva Atlántica del Brasil permanecieron en el género Callithrix y los amazónicos se ubicaron en el género Mico, de esta manera Callithrix melanura listada en Salazar-Bravo et al. (2003) es ahora Mico melanurus. Así mismo, se propuso que los titíes pigmeos merecían mantenerse en su propio género (Cebuella), a pesar de su parentesco con los otros dos géneros de titíes, por lo que Callithrix pygmaea listada en Salazar-Bravo et al. (2003) se lista en el presente trabajo como Cebuella pygmaea (de la Torre & Rylands 2008).
Saguinus La taxonomía reciente reconoce múltiples géneros de primates tamarinos amazónicos, con el género Saguinus dividido en dos: Leontocebus y Saguinus (Rylands et al. 2016). Siguiendo esta disposición, y el reconocimiento de especies adicionales (Rylands & Mittermeier 2013), Saguinus fuscicollis weddelli cambió a Leontocebus weddelli weddelli. Finalmente, Porcel et al. (2010) y Wallace et al. (2010, 2013a) no reconocieron la presencia de Saguinus melanoleucus crandalli en el departamento de Pando, porque la referencia original de esta especie en el país (Emmons 2002), se basó en la observación de un individuo pequeño entre un grupo de Leontocebus weddelli weddelli. En la presente lista optamos por esta posición y eliminamos esta especie de la lista para Bolivia.
Cebidae
Cebus Siguiendo los recientes cambios taxonómicos para los pequeños monos capuchinos sin copete por Boubli et al. (2012) y Lynch Alfaro et al. (2012), la especie Cebus albifrons listada para Bolivia en Salazar-Bravo et al. (2003) cambió a Cebus unicolor.
Sapajus Los monos capuchinos robustos y copetudos han sido separados recientemente del género Cebus y se los ha colocado en un nuevo género, Sapajus (Boubli et al. 2012, Lynch Alfaro et al. 2012). Sapajus libidinosus sigue siendo una especie válida, pero se encuentra en el Cerrado del oeste de Brasil (Rylands & Kierulff 2015). Por lo tanto, podría estar presente en el este de Bolivia, pero aún no hay un registro confirmado. El Grupo de Especialistas en Primates Neotropicales de la UICN propuso la presencia de tres especies de Sapajus en Bolivia: Sapajus apella, en la mayoría de las tierras bajas bolivianas (Rylands et al. 2015a); Sapajus cay, en el sur del Chaco (Rimoli et al. 2018); y Sapajus macrocephalus en el departamento de Pando, al norte del río Madre de Dios (Rylands et al. 2015b). Esta posición es la adoptada en esta lista.
Pitheciidae
Pithecia La taxonomía de las especies en el género Pithecia han sido recientemente revisadas por Marsh (2014) y Serrano-Villavicencío et al. (2019). En este reporte y atendiendo al detallado trabajo de estos últimos autores reconocemos a Pithecia irrorata Gray, 1843 como la única especie del género en Bolivia.
Plecturocebus Desde la lista de Salazar-Bravo et al. (2003) se han producido cambios notables en la taxonomía del género Callicebus. Usando análisis moleculares, morfológicos y biogeográficos, Byrne et al. (2016) propusieron la división de este género en tres géneros (dos de ellos nuevos): Callicebus, para los monos tití del bosque atlántico; Cheracebus, para las especies del norte amazónico; y Plecturocebus, para las especies del sur de la Amazonia, incluyendo todas las especies bolivianas. Así mismo, el número de especies reconocidas aumentó de 28 (Van Roosmalen et al. 2002) a 34 (Byrne et al. 2016). Para Bolivia, la revisión de Byrne et al. (2016) confirmó la presencia de cuatro especies del grupo donacophilus que fueron listados en Salazar-Bravo et al. (2003) y en Martínez & Wallace (2010): P. donacophilus, P. modestus, P. olallae y P. pallescens. Por otro lado, se han producido cambios importantes para los dos miembros del anteriormente reconocido grupo cupreus (Van Roosmalen et al. 2002): P. cupreus y P. dubius; ambas especies mencionadas en la lista de Salazar-Bravo et al. (2003). Van Roosmalen et al. (2002) clarificaron que P. cupreus está distribuido exclusivamente en un área cerca del río Solimoes en Brasil y la frontera con Perú. Por otro lado, Byrne et al. (2016) consideraron P. dubius como un sinónimo de P. caligatus. Sin embargo, la evidencia más reciente sugiere que los monos tití en los bosques al norte del río Madre de Dios son Plecturocebus toppini (Wallace et al. 2013b, Vermeer & Tello-Alvarado, 2015) y es así como lo reportamos en la presente lista, adicionando una nueva especie de mono tití para el país.
Así mismo, una nueva especie de mono tití fue descrita para Bolivia en 2006 como Callicebus aureipalatii, ahora referido como P. aureipalatii. La localidad tipo está ubicada en el Campamento Roco Roco, río Hondo, al norte del departamento de La Paz, en el Parque Nacional y Área Natural de Manejo Integrado Madidi (Wallace et al. 2006).
Atelidae
Alouatta Wallace & Rumiz (2010) llevaron a cabo un examen fotográfico de especímenes identificados como Alouatta guariba beniensis depositados en el Museo Real de Historia Natural en Estocolmo y descartaron la presencia de una población aislada de dicha especie en el departamento de Beni y reidentificaron estos especímenes como A. carayá o A. sara o híbridos de los mismos. Seguimos el criterio de Wallace & Rumiz (2010) y eliminamos A. guariba beniensis de la lista para Bolivia; por consiguiente, solo las dos especies del género reconocidas por Salazar-Bravo et al. (2003), es decir A. carayá y A. sara son incluidas en este reporte.
Lagothrix La especie listada para Bolivia en Salazar-Bravo et al. (2003) fue Lagothrix cana tschudii. Posteriores revisiones taxonómicas del género (Ruíz-García et al. 2014, Di Fiore et al. 2015, Ruiz-García et al. 2019) reconocieron sólo dos especies: L. flavicauda y L. lagotricha, ésta última con cuatro subespecies. El más reciente análisis filogenético de Lagothrix por Ruiz-García et al. (2019), en el que se incluyen muestras del sur de Perú y norte de Bolivia, provee evidencia de que tschudii debería ser reconocida como una quinta subespecie de L. lagothricha, siendo en consecuencia la forma boliviana de los bosques montanos del norte del departamento de La Paz: L. lagothricha tschudii.
CARNÍVORA
Con algunas excepciones (ver Felidae), la taxonomía del orden Carnívora se ha mantenido relativamente estable desde la lista de Salazar-Bravo et al. (2003). La taxonomía de la familia Felidae se ha modificado en gran parte debido al empleo de técnicas moleculares en análisis filogenéticos.
Felidae
Herpailurus Uno de los cambios taxonómicos controversiales en la familia Felidae fue la inclusión del yaguarundí en el género Puma, propuesto por Johnson et al. (2006) y apoyado por Zhou et al. (2017) en un estudio utilizando mitogenomas. En contraste, existe evidencia que el yaguarundí y el puma no son especies hermanas (p.e., Agnarsson et al. 2010 con base en sequencias de citocromo-b), lo que puede refutar que ambas especies pertenezcan al mismo género. Utilizando técnicas de secuenciación de ADN ancestral, Barnes et al. (2005) incluyeron en su estudio al guepardo americano (Miracinonyx), una forma fósil del Pleistoceno al Reciente de Norteamérica, el cual resulta ser el género hermano de Puma. Considerando que yaguarundis y pumas muestran patrones ecológicos y morfológicos distintos, y que es posible que Miracionyx haya sido un género hermano de Puma, en esta lista, aceptamos la propuesta conservadora de Kitchener et al. (2017) e incluimos al yaguarundí en el género Herpailurus, lo cual difiere de la lista de Salazar-Bravo et al. (2003). Finalmente, el yaguarundí presenta fuertes variaciones cromáticas a lo largo de su distribución, lo que llevó a que se consideren entre cinco y ocho subespecies válidas. Sin embargo, un estudio molecular del rango total de su distribución concluyó que el yaguarundí es una especie monotípica (Ruiz-García & Pinedo-Castro, 2013). Esta posición fue seguida por Kitchener et al. (2017) y es la misma que seguimos en la presente lista.
Leopardus En las últimas dos décadas, el género Leopardus fue subdividido en cuatro géneros o subgéneros (Leopardus, Oncifelis, Lynchailurus y Oreailurus). No obstante, análisis filogenéticos y revisiones recientes han sugerido la existencia de un sólo género, Leopardus Gray, 1842 (Johnson et al., 2006; Kitchener et al., 2017). El género Oncifelis, con tres especies, fue citado en Salazar-Bravo et al. (2003) y es considerado ahora como parte del género Leopardus.
La reciente compilación de Kitchener et al. (2017) corrige el nombre Leopardus colocólo a Leopardus colocóla siguiendo la forma original del nombre atribuido a Molina (1782), criterio que seguimos en este trabajo. La taxonomía de L. colocóla continúa siendo controversial, aunque se han realizado trabajos usando técnicas moleculares como los de Cossíos et al. (2009) y Ruiz-García et al. (2013), que indican la existencia de una sola especie, pero con al menos dos ciados, distinguiendo en su rango de distribución las poblaciones del norte y el sur (Cossíos et al. 2009). Con base en los estudios de Cossíos et al. (2009) y Ruiz-García et al. (2013), Kitchener et al. (2017) reconocieron un total de siete subespecies y no descartaron que algunas de ellas puedan ser reconocidas a nivel de especie cuando haya más información disponible. Kitchener et al. (2017) listaron una sola subespecie para Bolivia: Leopardus colocóla, budini (Pocock, 1941), la que fue incluida en Salazar-Bravo et al. (2003) como Oncifelis pajeros ssp. No obstante, basados en un registro fotográfico, se documentó la presencia en el país de Leopardus colocóla, braccatus [=Leopardus colocólo braccatus] en el departamento del Beni (Díaz Luque et al., 2012).
La taxonomía de Leopardus tigrinus no está resuelta completamente y se ha propuesto que esta especie en realidad constituye un complejo de especies. Las diferencias morfológicas en el pelaje están respaldadas por diferencias moleculares y se ha detectado además hibridización con otras especies del género Leopardus (Ruiz-García et al., 2018). La subespecie listada al momento para Bolivia es Leopardus tigrinus tigrinus (Schreber, 1775). La especie fue incluida en Salazar-Bravo et al. (2003) como Oncifelis tigrina.
PERISSODACTYLA
El tapir o anta de tierras bajas (Tapirus terrestris) es la única especie presente en Bolivia. En 2013, se describió una nueva especie de tapir para la Amazonia, Tapirus kabomani (Cozzuol et al. 2013). Esta especie se considera significativamente más pequeña en tamaño y peso, T. terrestris puede pesar hasta 320 kg, en tanto que T. kabomani pesa alrededor de 110 kg. Por el momento no hay evidencia convincente de que esta forma esté presente en Bolivia, y, en cualquier caso, Voss et al. (2014) han cuestionado la validez de esta forma como una nueva especie, argumentando que la evidencia presentada no se encuentra apoyada de manera adecuada en información genética, morfológica y etnográfica.
CETARTIODACTYLA
Desde la década de los 60s, datos paleontológicos y morfológicos habían sugerido una relación cercana entre Cetácea y Artiodactyla (Van Valen 1966, 1968). Esta hipótesis recibió confirmación con la incorporación de estudios moleculares en los que se encontró que los hippopotami son los parientes más cercanos de Cetácea (Montgelard et al. 1997). Gingerich et al. (2001) reportaron fósiles de cetáceos con huesos de tobillos y tarsos que son diagnósticos de Artiodactyla, lo que respaldó los resultados moleculares. En consecuencia, varios estudios proveen sólida evidencia sobre el parentesco cercano entre Cetácea y los Hippopotamidae de los Artiodactyla (Naylor & Adams 2001, Boisserie et al. 2005, 2010, Orliac et al. 2010, Zhou et al. 2011). Estos resultados hacen a Artiodactyla parafilético con respecto a Cetácea. Con el objetivo de tener un ciado monofilético y que refleje su contenido, se ha usado el nombre Cetartiodactyla (Montgelard et al. 1997). En este contexto "artiodáctilos" significa "no-cetáceos cetartiodáctilos" (Gingerich et al. 2017). Por otra parte, si se favorece la prioridad ordinal de los nombres, se podría continuar con el uso del orden Artiodactyla, pero incluyendo a Cetácea como parte de este orden. En este trabajo optamos por el uso del nombre de orden Cetartiodactyla.
Camelidae
Vicugna La taxonomía de los camélidos domésticos sigue en controversia, pero desde la lista de Salazar-Bravo et al. (2003), con base en estudios arqueozoológicos y moleculares Kadwell et al. (2001), Wheeler (2003, 2005) y Marín et al. (2007) sugirieron que la alpaca pertenece ahora al mismo género que la vicuña, siendo ahora: Vicugna pacos. En tanto, que la llama (Lama glamd) y el guanaco (Lama guanicoe) no han cambiado de género. Este cambio ya fue reconocido en el capítulo de Villalba et al. (2010) en el libro de mamíferos medianos y grandes de Bolivia.
Cervidae
Mazama- Gutiérrez et al. (2017) revisaron la taxonomía del género Mazama en su trabajo sobre los cérvidos de las Américas. Uno de los resultados más notables fue que en los análisis moleculares, Mazama americana se reveló como un grupo polifilético, compuesto de dos ciados denominados grupo 1 y grupo 2. En el grupo 1 están incluidas las poblaciones de M. americana de Bolivia. Otro resultado importante de ese trabajo fue que M. americana y M. gouazoubira no se recuperaron como taxones emparentados, y para resolver ese problema M. gouazoubira tendría que pasar a otro género, siendo un nombre disponible para ese ciado el de Nanelaphus (Fitzinger, 1873). La resolución de la taxonomía de Mazama spp. está aún pendiente, por ello, conservadoramente, dejamos en la lista para Bolivia las tres especies del género Mazama que fueron listadas en Salazar-Bravo et al. (2003).
Odocoileus Gutiérrez et al. (2017), en la misma revisión taxonómica anteriormente mencionada, recuperaron en los análisis moleculares al género Odocoileus como no monofilético. De igual manera, no consideraron a Odocoileus peruvianus como una especie separada, más bien como una subespecie O. virginianus peruvianus, y es así como la incluimos en la presente lista.
Parachoerus La sistemática de la familia Tayassuidae ha sido recientemente revisada por Dutra et al. (2017) usando un análisis filogenético en base a datos morfológicos y moleculares. El género Catagonus es polifilético, y por ello se revalidaron dos géneros: Brasiliochoerus y Parachoerus, y se describió uno adicional, Protherohyus. El género Catagonus descrito por Ameghino en 1904 solo contiene a especies extintas. Parachoerus fue descrito originalmente por Rusconi en 1930 como un subgénero y fue posteriormente elevado a nivel de género, incluyéndose en el mismo a la especie viviente Parachoerus wagneri (Rusconi, 1930). Los miembros vivientes de esta familia pertenecen a una sola subfamilia, Tayassuinae, y a una sola tribu, Tayassuini. Pécari tajacu y Tayassu pécari tienen una distribución amplia en Sudamérica, en tanto que Parachoerus wagneri es endémico del Chaco seco en el oeste de Paraguay, sureste de Bolivia y norte de Argentina.
Iniidae
Inia El delfín de río boliviano, localmente llamado "bufeo", es el único cetáceo en el país. Presenta una distribución restringida a los ríos de la cuenca superior del Madeira. La taxonomía del delfín de río todavía está en discusión (Aliaga-Rossel 2010). Algunos investigadores consideran la forma boliviana de Inia como una subespecie (Iniageoffrensis boliviensis), a pesar de los numerosos estudios moleculares publicados que indican que la especie boliviana es válida (Ruiz-García 2009, Gravena et al. 2014). A la fecha se está preparando para el Sistema Integrado de Información Taxonómica (ITIS) una nueva explicación con base en todos los estudios genéticos existentes con el fin de aclarar el estado de I boliviensis como especie independiente (W. Gravena 2018, com. pers.).
RODENTIA
La taxonomía del orden Rodentia en Sudamérica sufrió recientemente un proceso de reestructuración y remozamiento (Patton et al. 2015). Para el orden Rodentia, en la presente lista de mamíferos bolivianos, seguimos mayormente las propuestas taxonómicas expuestas en este libro, complementadas con numerosas referencias posteriores.
Sciuridae
La taxonomía de las especies de ardillas sudamericanas fue revisada de manera regional y comprensiva hace más de un siglo en la monografía de J.A. Alien (1915). Desde entonces, algunos géneros de ardillas sudamericanas fueron incluidas en revisiones taxonómicas recientes, como Villalobos & Cervantes-Reza (2007) y Pečnerová & Martínková (2012). No obstante, la contribución de De Vivo & Carmignotto (2015) constituye la compilación taxonómica más reciente. En ese trabajo se sugieren cambios notables en la taxonomía de las ardillas sudamericanas, especialmente en las del género Sciurus, que comprende especies presentes en Bolivia. Aún con el avance que significa el trabajo de estos colegas brasileños, existen todavía varios temas referidos a los límites Ínter- e intraespecíficos, así como aspectos de las relaciones filogenéticas y diversificación de la familia Sciuridae en la región Neotropical que quedan por dilucidarse. Compilaciones recientes como las de Thorington et al. (2012) o Kropowski et al. (2016) presentan información detallada sobre la biología de las ardillas sudamericanas, pero no intentan resolver preguntas pendientes sobre su sistemática y la taxonomía, por lo que consideramos que las propuestas taxonómicas de De Vivo & Carmignotto (2015) son las más actualizadas y son las que optamos por seguir en la presente lista.
De Vivo & Carmignotto (2015) para la familia Sciuridae en Sudamérica reconocen 19 especies organizadas en siete géneros, tres de los cuales tienen registros en Bolivia. El género Microsciurus permanece sin cambios respecto de la lista de Salazar-Bravo at al. (2003), en tanto que el género Sciurus es actualmente considerado sinónimo subjetivo de Hadrosciurus y Notosciurus.
Hadrosciurus El género Hadrosciurus comprende el concepto de Sciurus spadiceus en Salazar-Bravo et al. (2003). En Bolivia están presentes tres de las cuatro subespecies que comprende el género. Las subespecies tentativamente reconocidas para Bolivia son: H. spadiceus castus (Thomas, 1903), presente en una única localidad en el departamento de La Paz; H. spadiceus spadiceus (Olfers, 1818), distribuida al oeste del departamento de Santa Cruz; y H. spadiceus tricolor (Tschudi, 1845), asignada para el centro de Bolivia. Las subespecies de Hadrosciurus en Bolivia tienen límites de distribución cercanos, pero presentan características distintivas en la coloración del pelaje que permite su asignación a una de las subespecies. No obstante, es necesario mencionar que los especímenes bolivianos asignados a H. spadiceus tricolor difieren de los especímenes de esta misma subespecie en otros países (De Vivo & Carmignotto 2015).
Notosciurus En el género Notosciurus están incluidas, como Notosciurus pucheranii, las poblaciones originalmente incluidas como especies Sciurus ignitus (con dos subespecies reconocidas) y Sciurus argentinius, y listadas como tal en Salazar-Bravo et al. (2003). De las cuatro subespecies reconocidas por De Vivo & Carmignotto (2015), tres están presentes en Bolivia: N. pucheranii argentinius (Thomas, 1921), en el extremo sur de Bolivia; N. pucheranii boliviensis (Osgood, 1921), distribuida desde el sur de Perú al centro de Bolivia; y N. pucheranii ignitus (Gray, 1867), que ocurre al este de los Andes, en la cuenca Amazónica.
Las ardillas del centro de Bolivia (departamentos de Cochabamba, Chuquisaca, partes de Tarija y Santa Cruz) están notoriamente ausentes en las colecciones que revisaron De Vivo & Carmignotto (2015). Es muy posible que formas de estas regiones representen taxones nuevos para la ciencia y que por el momento se descarten como errores en las identificaciones; caso en punto es el espécimen de Sciurus argentinius listado en Salazar-Bravo et al. (2003), en base a un espécimen colectado en la cuenca del río Urucuti en el centro del departamento de Chuquisaca (Emmons 1997). Este espécimen se considera ahora como un representante de N pucheranii argentinius, pero fue calificado por De Vivo & Carmignotto (2015) como una anomalía o una identificación errada con base en el número de pares de mamas indicado por Emmons (1997).
Cricetidae
Siguiendo a Musser & Carleton (1993), Salazar-Bravo et al. (2003) incluyeron a todos los roedores del continente en la familia Muridae. En este trabajo, atendiendo a los criterios de Musser & Carleton (2005), se separan a las ratas y ratones nativos de Sudamérica de aquellos que fueron introducidos desde el Viejo Mundo en dos familias diferentes: Cricetidae y Muridae, respectivamente. Las ratas y ratones de la familia Muridae están presentes en Bolivia únicamente como especies introducidas (ver más adelante). Los ratones de Sudamérica de la familia Cricetidae están comprendidos en tres subfamilias: Neotominae, Tylominae y Sigmodontinae, siendo ésta última la única que está presente en Bolivia. Los roedores sigmodontinos comprenden una amplia diversidad de especies mayormente endémicas del continente sudamericano (Patton 2015a).
Los géneros comprendidos en la subfamilia Sigmodontinae han sido agrupados en tribus que han variado en número y contenido dependiendo de los criterios adoptados por los diferentes autores. En la compilación más reciente de la subfamilia, Pardiñas et al. (2017) reconocieron para Sudamérica nueve tribus que consideran con un contenido genérico relativamente estable, y 12 géneros con afiliaciones filogenéticas poco claras agrupados como Sigmodontinae incertae sedis, cuatro de los cuales están presentes en Bolivia. Pardiñas et al. (2015) y Salazar-Bravo et al. (2016) describieron dos nuevas tribus: Euneomyini y Andinomyini, respectivamente, reconociéndose ahora en el país un total de ocho tribus de las 11 actualmente consideradas para la subfamilia Sigmodontinae. En este trabajo seguimos el criterio de Cazzaniga, Cañón y Pardiñas (2019) sobre la disponibilidad, autoría y fecha de publicación de los nombres tribales en los roedores sigmodontinos.
Tribu Abrotrichini
Con base en datos morfológicos y moleculares, D'Elía et al. (2007) describieron una nueva tribu, Abrotrichini, en la que agruparon cinco géneros, siendo Abrothrix (incluyendo Chroeomys) el único con registros confiables en Bolivia. El género Abrothrix (incluyendo Chroeomys) fueron agrupados anteriormente en el denominado "Andean clade" y así fue incluido en la lista de Salazar-Bravo et al. (2003). Más recientemente, usando numerosos caracteres morfológicos y marcadores moleculares mitocondriales y nucleares, Teta et al. (2017) dividieron a esta tribu en dos nuevas subtribus y asignaron al género Abrothrix cuatro subgéneros como resultado de su amplia variación morfológica. Dos de los subgéneros de Abrothrix están presentes en Bolivia: Angelomys y Chroeomys, tal como se explica a continuación.
Abrothrix El género Abrothrix en Bolivia comprende dos especies: Abrothrix (Angelomys) andina y Abrothrix (Chroeomys) jelskii, estas especies fueron listada en Salazar-Bravo et al. (2003) como Abrothrix andinus y Chroeomys jelskii, respectivamente. Para Chroeomys jelskii Salazar-Bravo et al. (2003) listaron adicionalmente cuatro subespecies. El género Chroeomys fue sugerido como un sinónimo subjetivo de Abrothrix con base en la interpretación taxonómica de filogenias moleculares y la poca variación morfológica entre sus especies constituyentes (D'Elía 2003); esta interpretación se reafirmó en la revisión de Patterson et al. (2015). Otros autores han propuesto un estatus subgenérico para Chroeomys (Teta et al. 2016) criterio que seguimos en la presente lista.
Tribu Akodontini
Esta tribu es la segunda más diversa en número de géneros y especies entre los Sigmodontinae, con un total de 83 especies y con un amplio rango de distribución en el continente (D'Elía & Pardiñas 2015b; Pardiñas et al. 2017). El contenido de esta tribu permaneció más o menos estable entre mediados de los 70s y mediados de los 90s, cuando la aplicación de técnicas moleculares a los estudios filogenéticos resultó en cambios radicales en la composición de la tribu, por ejemplo, en la escisión de cinco géneros para formar la tribu Abrotrichini (ver arriba). Akodontini incluye actualmente 16 géneros vivientes (D'Elía & Pardiñas 2015b; Pardiñas et al. 2017), seis de los cuales están presentes en Bolivia: Akodon, Juscelinomys, Kunsia, Lenoxus, Necromys y Oxymycterus.
Akodon El género Akodon es uno de los más diversos, con un total de 35 especies reconocidas (Pardiñas et al. 2017). En comparación con la lista presentada por Salazar-Bravo et al. (2003) el cambio mayor en la presente lista proviene de la revisión del grupo de especies de Akodon boliviensis para el noroeste de Argentina elaborada por Jayat et al. (2010). En ese trabajo Akodon lutescens caenosus fue reconocida como una especie plena, Akodon caenosus, que constituye el miembro más pequeño dentro del grupo Akodon boliviensis.
Es importante mencionar que aún existe incertidumbre sobre el estatus taxonómico de algunas especies del género que permanecen pobremente conocidas, entre ellas Akodon pervalens y Akodon dayi, hasta ahora endémicas para Bolivia (Pardiñas et al. 2017). Anderson (1997) ya mencionó la importancia de revisar los especímenes de Bolivia identificados como A. pervalens, trabajo que aún está pendiente. En esta lista mantenemos ambas especies hasta que se hagan las revisiones pertinentes.
Juscelinomys Previamente se consideraron dos especies de este género para el país: Juscelinomys huanchacae y / guaporensis (Emmons 1999, Salazar-Bravo et al. 2003, Emmons et al. 2006). Posteriormente, Emmons & Patton (2012) notaron la falta de consistencia en caracteres diagnósticos para segregar especímenes de Juscelinomys de Bolivia en dos especies, por lo que optaron en reconocer una sola especie como válida: / huanchacae. Juscelinomys huanchacae es considerada una especie endémica para Bolivia.
Kunsia Salazar-Bravo et al. (2003) listaron para Bolivia la subespecie Kunsia tomentosus tomentosus, una de las dos subespecies anteriormente reconocidas. No obstante, Pardiñas et al. (2009) sugirieron que las diferencias, previamente aceptadas, entre las dos subespecies estaban basadas en variación individual o de edad, proponiendo en consecuencia que Kunsia tomentosus es una especie monotípica, un criterio que seguimos en la presente lista.
Lenoxus Este género tiene una distribución muy restringida en Bolivia y Perú. Salazar-Bravo et al. (2003) incluyeron para la lista de mamíferos bolivianos la subespecie Lenoxus apicalis boliviae. La revisión de Patton (2015) no reconoce diferenciación subespecifica, criterio que seguimos en el presente trabajo.
Necromys Aunque aún persiste la discusión sobre la consistencia de la sinonimia de Necromys Ameghino, 1889 y Bolomys Thomas, 1916 (Gurgel-Filho et al. 2015, Jayat et al. 2016a), en la presente lista optamos por el uso del nombre genérico Necromys con base en los argumentos expuestos por D'Elía et al. (2008), Pardiñas et al. (2015c) y Jayat et al. (2016a). Por consiguiente, incluimos a las especies anteriormente comprendidas en el género Bolomys en la lista de Salazar-Bravo et al. (2003) dentro del género Necromys. El género Necromys requiere aún de una revisión comprensiva que trate los problemas de nomenclatura y delimitación de especies (D'Elía et al. 2008). En base al análisis genético por D'Elía et al. (2008) adicionamos Necromys lenguarum a las tres especies anteriormente listadas para Bolivia en Salazar-Bravo et al. (2003), aunque se ha argumentado que Necromys lenguarum debería ser tratado como sinónimo de Necromys lasiurus (Pardiñas et al. 2015c, 2017), un criterio que seguimos en la presente lista.
Oxymycterus En la revisión reciente de género Oxymycterus, Oliveira & Goncalves (2015) consolidaron como especie plena a Oxymycterus nigrifrons. Esta especie fue listada en Salazar-Bravo et al. (2003) como O. nigrifrons ssp. 1. En la presente lista incluimos a la especie indicada como O. nigrifrons, junto con otras cinco especies ya listadas anteriormente.
Tribu Andinomyini
Con base en datos moleculares, cariotipos y caracteres morfológicos, Salazar-Bravo et al. (2016) describieron la tribu Andinomyini para agrupar los géneros Andinomys y Punomys, ambos presentes en Bolivia. El género Andinomys fue listado en Salazar-Bravo et al. (2003) como incertae seáis, en tanto que Punomys constituye un nuevo registro para el país (ver abajo).
Andinomys La lista de Salazar-Bravo et al. (2003) reconoció la presencia de la subespecie A. edax edax para Bolivia. La misma subespecie fue mencionada para el sur de Bolivia y el extremo norte de Argentina en la compilación del género en Salazar-Bravo & Jayat (2015). No obstante, recientemente Jayat et al. (2017) no encontraron evidencia para dar soporte a la validez de las dos subespecies anteriormente aceptadas y concluyeron que Andinomys edax es monotípica.
Punomys Punomys kofordi constituye una adición a las especies de mamíferos de Bolivia. El primer registro está basado en un único espécimen colectado en 1987 en el departamento de La Paz (Salazar-Bravo et al. 2011). El registro de Punomys en Bolivia extendió el rango de distribución conocido del género en 240 km SE desde la localidad más próxima en Perú (Salazar-Bravo et al. 2011). Actualmente existen otros registros en el departamento de La Paz (J. Salazar-Bravo, datos no publicados).
Tribu Euneomyini
Con base en un análisis filogenético con marcadores moleculares y apoyado por caracteres morfológicos substantivos, Pardiñas et al. (2015a) describieron una nueva tribu, Euneomyini, para agrupar a tres géneros mayormente andinos (Neotomys, Irenomys y Euneomys), de los cuales sólo Neotomys tiene registros en Bolivia. El género Neotomys fue incluido como Sigmodontinae incertae sedis en la lista de Salazar-Bravo et al. (2003) y en la revisión de Ortiz & Jayat (2015).
Tribu Oryzomyini
La tribu Oryzomyini es la más diversa entre los roedores sigmodontinos sudamericanos, con 141 especies organizados en 29 géneros (Pardiñas et al. 2017). La tribu Oryzomyini está representada en Bolivia por 11 géneros: Cerradomys, Euryoryzomys, Holochilus, Hylaeamys, Microryzomys, Neacomys, Nectomys, Nephelomys, Oecomys, Oligoryzomys y Pseudoryzomys. El esfuerzo más notable entre los estudios taxonómicos de los géneros en esta tribu corresponde a la extensa redefinición del género Oryzomys con base en análisis filogenéticos (Weksler 2006, Weksler et al. 2006, Weksler & Percequillo 2011). Con la finalidad de contar con una clasificación monofilética del género, Weksler et al. (2006) describieron 10 nuevos géneros, de los cuales cuatro están presentes en Bolivia: Cerradomys, Euryoryzomys, Hylaeamys y Nephelomys.
Cerradomys El género Cerradomys, anteriormente entendido como el grupo Oryzomys subflavus, comprende ocho especies, pero se considera que existen aún otras formas no descritas (Bonvicino et al. 2014, Percequillo 2015a). Dos especies están presentes en Bolivia: Cerradomys maracajuensis, listada anteriormente como Oryzomys subflavus (Salazar-Bravo et al. 2003) y Cerradomys scotti, que constituye un nuevo registro para el país. La primera mención de C. scotti corresponde a un espécimen proveniente del Parque Nacional Noel Kempff Mercado en el departamento de Santa Cruz (Emmons et al. 2006). Por otra parte, Brooks et al. (2004) describieron una nueva especie para Bolivia: Oryzomys andersoni, miembro del grupo O. subflavus, con base en un espécimen proveniente de la localidad Pozo Mario, Estancia Las Conchas en el departamento de Santa Cruz, la cual posteriormente fue considerada como un sinónimo júnior de C. scotti (Emmons et al. 2006, Weksler et al. 2006).
Euryoryzomys Actualmente, el género Euryoryzomys incluye seis especies que presentan una variación morfológica, de cariotipo y molecular que podría indicar una diversidad mayor de formas en el género (Percequillo 2015b). Las dos especies presentes en Bolivia, E. legatus y E. nitidus, fueron listadas en Salazar-Bravo et al. (2003) como parte del género Oryzomys.
Holochilus Salazar-Bravo et al. (2003) consideraron que sólo una especie del género Holochilus estaba presente en Bolivia: Holochilus sciureus. Sin embargo, con base en especímenes presentes en las colecciones del Museo de Historia Natural Noel Kempff Mercado de Santa Cruz y del Museo Argentino de Ciencias Naturales Bernardino Rivadavia, Pardiñas & Teta (2011) confirmaron la presencia de H chacarius para el este de Bolivia. Adicionalmente, estos autores sugirieron que los límites de distribución de estas dos especies en Bolivia no están bien definidos y es posible encontrarlos en simpatría en la región oriental. Dos trabajos de interés sobre la sistemática del género, uno basado en morfología y citogenética (Goncalves et al. 2015) y, el otro, en un muestreo bastante amplio de caracteres moleculares (D'Elía et al. 2015) confirmaron la presencia de H. sciureus y H. chacarius en Bolivia, criterio que se sigue en la presente lista.
Hylaeamys Las seis especies que se reconocen en el género Hylaeamys pertenecieron al complejo Oryzomys capito u Oryzomys megacephalus (Percequillo 2015c). En el género Hylaeamys están comprendidas las formas H. perenensis y H. yunganus anteriormente listadas en Salazar-Bravo et al. (2003) como parte del género Oryzomys. Por otra parte, Emmons & Patton (2005) describieron una nueva especie para la ciencia perteneciente al complejo O. megacephalus. La nueva especie Oryzomys acritus tiene como localidad tipo El Refugio Huanchaca en el Parque Noel Kempff Mercado al noreste del departamento de Santa Cruz. Posteriormente, en la revisión del género Oryzomys por Weksler et al. (2006) Oryzomys acritus fue incluida en el género Hylaeamys. Hylaeamys acritus es considerada una especie endémica para el país.
Neacomys La sistemática del género Neacomys se modificó profundamente en la última década (Weksler & Bonvicino 2015a, Hurtado & Pacheco 2017, Sanchez-Vendizú et al. 2018). Originalmente se consideró para Bolivia una sola especie, Neacomys spinosus (Thomas, 1882) (Salazar-Bravo et al. 2003, Weksler & Bonvicino 2015a). No obstante, la revisión de N. spinosus por Hurtado & Pacheco (2017) restringió la distribución de esta especie a los bosques montanos nublados del norte del Perú y propuso el reconocimiento como especie plena de Neacomys amoenus para las poblaciones que habitan en el Cerrado al oeste de Brasil y el noreste del departamento de Santa Cruz en Bolivia, entre los 200 y 900 m de altura. Al mismo tiempo, estos autores describieron una nueva especie para la ciencia (Neacomys vargasllosai) que incluye especímenes colectados en Bolivia y que está distribuida en los bosques montanos nublados desde el sur del Perú hacia el centro de Bolivia hasta el límite oeste del departamento de Santa Cruz.
Nectomys La compilación de información del género Nectomys de Bonvicino & Weksler (2015) no hace referencia a especímenes provenientes de Bolivia, pero propone que la especie presente en Bolivia sería Nectomys apicalis, misma que fue incluida en Salazar-Bravo et al. (2003). La posterior revisión del género por Chiquito (2015), propuso la existencia de una especie aún no descrita de Nectomys para Bolivia, denominada "Nectomys sp. A Mamoré-Beni", distribuida en el noroeste del país en la vertiente oriental de los Andes. Incluimos esta especie como Nectomys sp. en la presente lista.
Nephelomys En el género Nephelomys se reconocen provisionalmente 13 especies, pero hay evidencia de que la diversidad taxonómica en el género necesita ser evaluada comprensivamente (Percequillo 2015d). En este género están comprendidas las formas N. keaysi y N. levipes, previamente incluidas como parte del género Oryzomys en Salazar-Bravo et al. (2003).
Oecomys El género Oecomys es uno de los más diversos en la tribu Oryzomyini, con 17 especies reconocidas al momento para Sudamérica (Carleton & Musser 2015, Pardiñas et al. 2016b, Suárez-Villota et al. 2017). Con base en análisis moleculares, citogenéticos y morfológicos, Suárez-Villota et al. (2017) revisaron la sistemática de Oecomys usando mayormente muestras de Brasil y reconocieron 15 linajes distintos, siendo seis de ellos un complejo de especies con al menos ocho nuevos taxones. Estos resultados muestran la complejidad de este género, por lo que su taxonomía alfa y los límites de las especies permanecen sin resolverse. Los análisis de Suárez-Villota et al. (2017) revelaron la presencia de un taxón no descrito para Bolivia, denominado Oecomys sp. 3 proveniente del departamento del Beni; esta forma se reconoció anteriormente como Oecomyssp. por Pardiñas et al. (2016b).
Salazar-Bravo et al. (2003) listaron cinco especies de Oecomys para Bolivia. A la presente lista se adicionan tres especies, dos constituyen nuevos registros y una es una nueva especie para la ciencia. Los dos registros son: Oecomys phaeotis, conocida de una localidad en el departamento de Cochabamba (Carleton & Musser 2015) y O. cleberi, registrada en una localidad sobre el río Biata en el Departamento del Beni (Pardiñas et al. 2016b). El registro de O. cleberi en Bolivia extiende el rango de distribución en más de 700 km desde la localidad conocida más cercana en Brasil. La nueva especie, O. sydandersoni tiene como localidad tipo El Refugio Huanchaca al este del departamento de Santa Cruz. Esta especie se conoce de tres localidades de los departamentos de Santa Cruz y Beni, y constituye una especie endémica para el país (Carleton et al. 2009).
Algunos de los registros asociados con Oecomys bicolor en la lista de Salazar-Bravo et al. (2003) provenientes de bosques montanos arriba de 1200m están ahora asociados con Oecomys phaeotis. En cuanto a O. trinitatis, la misma fue inicialmente listada como O. cf. trinitatus en Salazar-Bravo et al. (2003), citando como fuente la identificación tentativa en Emmons (1998) para especímenes provenientes del Parque Nacional Noel Kempff Mercado, en el departamento de Santa Cruz. Posteriormente, el registro de O. trinitatus para Bolivia fue confirmado por Emmons et al. (2006) y por Carleton & Musser (2015).
Oligoryzomys El género Oligoryzomys tiene una taxonomía compleja e inestable debido a la presencia de especies morfológicamente crípticas. La filogenia de varias especies del grupo y los límites entre especies han sido tratado en trabajos recientes, aunque aún no existe una revisión del género que sea inclusiva (e.g., Palma et al. 2010, Teta et al. 2013, González-Ittig et al. 2014, Weksler & Bonvicino 2015b, Da Cruz & Weksler 2018, Hurtado & D'Elía 2018a, Rivera et al. 2018). Dos intentos recientes de generar hipótesis sobre los límites entre especies utiliando marcadores moleculares (Da Cruz & Weksler 2018; Hurtado & D'Elía 2019), encontraron que varias de las especies estudiadas incluían dos o más unidades evolutivas independientes, lo que indica que la resolución de la taxonomía de este género está aún en proceso y queda mucho por ser dilucidado.
Rivera et al. (2018) evaluaron el complejo de especies crípticas incluidas como parte de la especie nominal Oligoryzomys flavescens, en la que estaba incluida Oligoryzomys sp. B, listada en Salazar-Bravo et al. (2003). Los análisis filogenéticos del marcador mitocondrial utilizado apoyado por sutiles diferencias morfológicas sugieren a estos autores que la subespecie Oligoryzomys flavescens occidentalis, debería ser reconocida como una especie válida, Oligoryzomys occidentalis. En este trabajo concordamos preliminarmente con esta propuesta, pero resaltamos el hecho de que ninguno de los marcadores nucleares utilizados por Rivera et al. (2018) resuelven al taxón "ciado oeste" como monofiletico. Por el momento, Oligoryzomys occidentalis reemplaza a Oligoryzomys sp. B en la lista de Salazar-Bravo et al. (2003)
Teta et al. (2013) revisaron el estado taxonómico de Oligoryzomys brendae, considerado anteriormente como parte de Oligoryzomys destructor. Las poblaciones de Argentina y del sur de Bolivia están ahora asignadas a O. brendae, en tanto que la especie O. destructor está asignada a las poblaciones del norte de Bolivia presentes en los bosques montanos nublados (Hurtado & D'Elía 2018a). La reciente revisión de Hurtado & D'Elía (2018a) sobre la taxonomía de O. destructor, propuso el reconocimiento de dos subespecies, siendo O. d. destructor la subespecie presente en Bolivia. No obstante, el límite de distribución de dicha subespecie en Bolivia no está determinado.
Por otra parte, Hurtado & D'Elía (2018b) describieron una especie nueva de Oligoryzomys para la ciencia y endémica para los Yungas del centro de Bolivia. Los especímenes fueron anteriormente identificados como O. destructor. La nueva especie Oligoryzomys pachecoi se encuentra en los bosques montanos nublados del centro de Bolivia, en los departamentos de Cochabamba, Chuquisaca y Tarija, entre los 1280 y 1960 m de altitud, con la localidad tipo en Tinkusiri, en el departamento de Cochabamba. Esta forma había sido identificada anteriormente como una posible nueva especie por Paresque (2010), una referencia que Hurtado & D'Elía (2018b) utilizaron, pero no citaron.
Tribu Phyllotini
La tribu Phyllotini es uno de los principales componentes de la subfamilia Sigmodontinae, siendo la cuarta en número de especies, con un total de 59 especies reconocidas para Sudamérica (Pardiñas et al. 2017). En la última clasificación formal de Sigmodontinae se incluyeron 11 géneros en la tribu Phyllotini, de los que ocho están presentes en Bolivia: Andalgalomys, Auliscomys, Calomys, Eligmodontia, Galenomys, Graomys, Phyllotis y Tapecomys (Pardiñas et al. 2017).
Calomys En contraste con la lista de Salazar-Bravo et al. (2003), en esta revisión seguimos el criterio de Salazar-Bravo (2015), quien sinonimizó Calomys fecundus bajo C. boliviae, atendiendo a los resultados de análisis filogenéticos desarrollados por Dragoo et al. (2003), entre otros.
Eligmodontia Lanzone & Ojeda (2005) y Mares et al. (2008) han mostrado que el epíteto específico correcto para la especie de Eligmodontia del altiplano boliviano es Eligmodontia hirtipes y no E. puerulus como se listó en Salazar-Bravo et al. (2003). Se considera, además, que la especie es monotípica.
Graomys En la lista de Salazar-Bravo et al. (2003) se siguió el criterio de Anderson (1997) en reconocer a la forma grande y gris del Chaco como Graomys griseoflavus. Estudios morfométricos, cromosómicos y genéticos han demostrado que el concepto de G. griseoflavus incluye al menos dos especies: G. chacoensis y G. griseoflavus, siendo la primera válida para las poblaciones bolivianas (Braun & Patton 2015) y la segunda está en el Chaco argentino, asociada al Monte y la Patagonia (Pardiñas et al. 2018).
Phyllotis La taxonomía y los límites entre las especies del género Phyllotis han evolucionado mucho desde la lista de Salazar-Bravo et al. (2003), no sólo en Bolivia, sino en la mayor parte de la distribución del género (Steppan & Ramírez 2015). Recientemente, y con base en filogenias moleculares, se reconoció a Phyllotis tucumanus como una nueva especie para el país (Jayat et al. 2016b). Por otra parte, en el trabajo de Jayat et al. (2016b) se reconocieron cuatro grupos monofiléticos dentro de un concepto amplio de P. tucumanus, de los cuales la forma 4 es la que está presente en el país, mientras que las tres formas restantes están restringidas a la Argentina.
Tapecomys En la lista de Salazar-Bravo et al. (2003) se incluyó a la forma wolffsohni dentro del género Phyllotis. Sin embargo, Steppan et al. (2007) demostraron que esta especie debería estar incluida en el género Tapecomys, un criterio con el que concordamos en esta lista.
Tribu Thomasomyini
Rhagomys El género Rhagomys fue incorporado a la lista de mamíferos bolivianos por Villalpando et al. (2006), apenas tres años después de ser descrita como nueva para la ciencia y para Perú por Luna & Patterson (2003). Rhagomys es un sigmodontino muy poco conocido pero su posición filogenética dentro de la tribu Thomasomyini parece estar bien solventada por análisis moleculares (Percequillo et al. 2004, D'ElíaíT al. 2006).
Rhipidomys En la última revisión del género Rhipidomys de Tribe (2015), se reconoció para Bolivia la especie Rhipidomys gardneri con base en un espécimen proveniente de Chijchipani, en la región de Ñor Yungas, en el departamento de La Paz. Salazar-Bravo et al. (2003) listaron esta especie como Rhipidomys sp. 1.
Thomasomys El género Thomasomys es posiblemente uno de los menos conocidos en el continente sudamericano, en parte debido a una alta diversidad de especies, con AA especies reconocidas en la compilación de Pacheco (2015). A la fecha, seis especies están reportadas como presentes en Bolivia. La especie Thomasomys taczanowskii (Thomas, 1882), anteriormente listada para Bolivia en Salazar-Bravo et al. (2003), fue removida de la lista actual dado que ahora está limitada a Ecuador y norte de Perú. Otras diferencias notables con respecto a la lista de Salazar-Bravo et al. (2003), incluyen el reconocimiento de Thomasomys australis como una especie distinta de T. daphne (Pacheco 2015) y la descripción de una nueva especie para la ciencia como Thomasomys andersoni. El espécimen tipo de T andersoni proviene de la localidad de la planta hidroeléctrica de Corani en el departamento de Cochabamba (Salazar-Bravo & Yates 2007). De las seis especies reconocidas a la fecha para el país, tres son consideradas endémicas: T. andersoni, T. australis y T. ladewi.
Caviidae
Caviinae
La subfamilia Caviinae incluye a tres géneros recientes: Cavia, Galea y Microcavia, y varios más en el registro fósil. Con una amplia distribución geográfica y ecológica en Sudamérica, los miembros de la subfamilia Caviinae están presente en el registro fósil desde el Mioceno tardío (Madozzo-Jaén & Pérez 2017). La compilación por Dunnum (2015) es la más actualizada y es la autoridad en la que nos basamos en esta sección.
Cavia Dos especies de cuyes silvestres se conocen en Bolivia. El epíteto específico para las poblaciones silvestres en los llanos y las zonas intervenidas de menos de 1.500 m de altitud es Cavia aperea, lo que contrasta con la taxonomía usada en Salazar-Bravo et al. (2003).
Galea En este trabajo concordamos con Dunnum (2015) en restringir el nombre Galea musteloides para las formas del altiplano y valles interandinos del centro del país. Basados en filogenias moleculares, la forma G comes se reconoce para poblaciones del sur de Bolivia (antes reconocidas como G. musteloides) y G leucoblephara para las formas distribuida en el sureste del país y antes asignadas a G spixii (Dunnum & Salazar-Bravo 2010).
Hydrochoerinae
En la lista de Salazar-Bravo et al. (2003), la capibara o carpincho se incluyó como parte de su propia familia Hydrochaeridae siguiendo la nomenclatura en Anderson (1993). La pertenencia de la capibara a una familia distinta, o su inclusión dentro de la familia Caviidae, tiene una larga historia que no trataremos en este trabajo. No obstante, atendiendo a resultados de análisis filogenéticos recientes se trata aquí como miembro de la familia Caviidae (e.g., Upham & Patterson 2012, 2015, Dunnum 2015).
Hydrochoerus El nombre genérico de la capibara presenta también inconsistencias históricas que son tratadas en detalle por Moreira et al. (2013). El nombre Hydrochaeris Brünnich, 1772 fue usado en Anderson (1993) y en Salazar-Bravo et al. (2003). En esta lista seguimos las aclaraciones expuestas en Moreira et al. (2013), citando los criterios de la Comisión Internacional de Nomenclatura Zoológica (ICZN por su sigla en inglés), que reconocen la validez del género Hydrochoerus Brisson, 1762 y así mismo reconoce el nombre de la especie hydrochaeris Linnaeus, 1766, siendo el nombre binomial Hydrochoerus hydrochaeris (Linnaeus, 1766).
Cuniculidae
Cuniculus Incluimos a C. taczanowskii con base en un espécimen proveniente del campamento San Juanito en el Área Natural de Manejo Integrado Apolobamba en el departamento de La Paz (Ríos-Uzeda et al. 2004).
Dasyproctidae
wocta - Salazar-Bravo et al. (2003), siguiendo a Anderson (1997), reconocieron sólo una especie para Bolivia: Dasyprocta punctata Gray, 1842 con tres subespecies. La compilación de Patton & Emmons (2015) restringió D. punctata al norte de Sudamérica y Centroamérica. Siguiendo el criterio presentado por estos autores, en este trabajo reconocemos para Bolivia dos especies: Dasyprocta azarae, distribuida al sur del río Beni y Dasyprocta variegata, en el extremo norte del país. Patton & Emmons (2015) no validaron subespecies para ninguna de las dos especies presentes en Bolivia, sin embargo, estos autores indicaron la necesidad de revisar críticamente los límites de distribución de ambas especies en el norte de Bolivia y la reexaminación de especímenes bolivianos provenientes del Chaco y el Cerrado.
La necesidad de una revisión integral fue apoyada por el trabajo de Teta & Lucero (2016), quienes hicieron un análisis morfológico cualitativo y cuantitativo de especímenes de Argentina, Paraguay y Bolivia y concluyeron que el concepto actual de D. azarae no es aplicable en ese rango de distribución, siendo necesaria una redefinición integral de los límites de las especies. Hasta que esto se concrete, en la presente lista reconocemos para Bolivia las dos especies mencionadas: D. azarae y D. variegata.
Myoprocta Myoprocta pratti fue incluida en la lista de Salazar-Bravo et al. (2003) citando avistamientos de animales vivos en localidades del departamento de Pando. Miserendino & Azurduy (2005) documentaron el primer espécimen para el país constituido por una piel curtida rescatada de un cazador en la localidad de Luz de América, Reserva Nacional de Vida Silvestre Amazónica Manuripi en el departamento de Pando. Una reciente publicación por Teta (2018) sobre el género Myoprocta, analizó la variabilidad morfológica cuantitativa del cráneo a lo largo de su rango de distribución. En este trabajo el autor discute la importancia de caracteres morfométricos en la separación de las dos especies de Myoprocta actualmente reconocidas y confirma que las poblaciones bolivianas corresponden a M. pratti, aunque sugiere que aún se necesita bastante trabajo taxonómico en el grupo.
Chinchillidae
Chinchilla Salazar-Bravo et al. (2003) incluyeron en la lista de los mamíferos bolivianos a Chinchilla brevicaudata Waterhouse, 1848 siguiendo la propuesta de Woods (1993). La compilación reciente de Spotorno & Patton (2015) incluye las poblaciones bolivianas de chinchilla dentro de la especie Chinchilla chinchilla, especie listada en Anderson (1997) y propuesta que aceptamos en este trabajo. Spotorno & Patton (2015) consideran a C. chinchilla monotípica, adoptando la recomendación de Anderson (1997). Es importante mencionar que la presencia de la chinchilla en Bolivia estaba basada en registros históricos (Tarifa 2009, Copa Alvaro et al. 2014). Después de casi ocho décadas, recientemente se han documentado varios grupos de individuos en la Reserva de Fauna Andina Eduardo Avaroa en el departamento de Potosí (Delgado et al. 2018a, 2018b, Elíseo Delgado, com. pers.).
Erethizontidae
Coendou - El género Coendou contiene 13 especies vivientes (Voss 2015). Salazar-Bravo et al. (2003) listaron para el país dos especies de amplia distribución geográfica en Sudamérica: Coendou bicolor y C. prehensilis. En la presente lista adicionamos el registro de C. rufescens con base en la reidentificación de Voss (2011) de un espécimen identificado como C. bicolor proveniente de la localidad de Incachaca en el departamento de Cochabamba. Posteriormente, Acosta et al. (2018) sumaron el registro de dos especímenes adicionales provenientes de las localidades de El Sunchal, en el departamento de Cochabamba, y Torrecillas, en la región de La Siberia, en el departamento de Santa Cruz.
Adicionalmente, Acosta et al. (2018) citaron un registro fotográfico de un individuo de puerco espín, publicado originalmente en el periódico nacional Los Tiempos e identificado por los autores como C. rufescens proveniente de la localidad de Pojo en el departamento de Cochabamba. Los registros publicados por Acosta et al. (2018) adquieren una importancia adicional al documentar la ampliación del rango de distribución de C. rufescens en el país, debido a la sugerencia de Voss (2011) sobre que el registro aislado de esta especie en Cochabamba, Bolivia, podría deberse al transporte intencional de esta especie por los Incas (Voss 2011,2015).
Ctenomyidae
En los últimos años se ha logrado una mejor comprensión sobre la distribución y la diversidad de las especies del género Ctenomys en Bolivia, incluyendo la descripción y la designación de sinonimias de varias formas. Como consecuencia, la lista que incluimos en este trabajo difiere en varios aspectos a la presentada en Salazar-Bravo et al. (2003).
Ctenomys Entre los roedores sudamericanos, el género Ctenomys es el más diverso en número de especies, con 63 especies reconocidas en la compilación de Bidau (2015), a las que se adicionan cuatro nuevas especies descritas para Bolivia (Gardner et al. 2014), reconociéndose a la fecha un total de 67 especies en el género. En la lista de Salazar-Bravo et al. (2003) se consideró el registro de 10 especies de Ctenomys en Bolivia, incluyendo a Ctenomys goodfellowi como una especie plena. Sin embargo, análisis filogenéticos moleculares y la caracterización cromosómica y génica (alozimas) demostró que C. goodfellowi es en realidad un sinónimo subjetivo de C. boliviensis (Gardner et al. 2014). La especie C. minutus listada en Salazar-Bravo et al. (2003), siguiendo a Anderson (1997), ha sido removida de la lista de Bolivia dado que esta especie, que ya tenía una asignación tentativa para el país, está actualmente restringida para el sur de Brasil (Bidau 2015). Los tres especímenes asignados por Anderson (1997) a C. minutus, corresponden ahora a la nueva especie C. yatesi descrita por Gardner et al. (2014).
Con base a especímenes de una localidad en Vallegrande en el departamento de Santa Cruz, Azurduy Ferreira (2005) describió una nueva especie de Ctenomys para Bolivia, con el nombre Ctenomys mariafareüi. La descripción de esa especie fue publicada en la revista digital Kempffiana. Al tiempo de su publicación no cumplió con los requerimientos del Código Internacional de Nomenclatura Zoológica, por lo que constituye un nomen nudum (Bidau 2015). Los especímenes asignados por Azurduy Ferreira (2005) corresponden a la nueva especie Ctenomys erikacuellarae descrita por Gardner et al. (2014).
Las cuatro nuevas especies para la ciencia descritas por Gardner et al. (2014) son las siguientes: Ctenomys erikacuellarae, C. yatesi, C. andersoni y C. lessai, reconociéndose ahora un total de 12 especies presentes en Bolivia. El género Ctenomys es el que tiene el mayor número de especies endémicas para el país con las siguientes siete especies: C. andersoni, C. boliviensis, C. erikacuellarae, C. lessai, C. lewisi, C. steinbachi y C. yatesi.
Echimyidae
La familia Echimyidae es una de las más diversas y ocupa una amplia gama de hábitats en el Neo trópico. La familia está pobremente representada en Bolivia, pues de los 23 géneros reconocidos, apenas seis tienen registros confiables en el país (Emmons et al. 2015, Emmons & Fabre 2018).
Proechimys El género Proechimys ha sufrido cambios desde la lista de Salazar-Bravo et al. (2003). Con base en la reciente compilación de Patton & Leite (2015) se incluyen solamente cinco especies para Bolivia, ya que Proechimys hilda fue considerada por estos autores como sinónimo de P. steeri. Recientemente, y con base en caracteres morfológicos, cromosómicos, y moleculares, se reportó una nueva especie para el país: P. pattoni, documentada con dos especímenes colectados en 1986 y provenientes de la localidad de río Madre de Dios, cerca de Santa Rosa, en el departamento de Pando (Sánchez-Vendizú et al. 2018).
Thrichomys Para el género Thrichomys, Pessóa et al. (2015) reconocen cuatro especies nominales válidas, aunque sugieren que el número podría incrementarse, dadas las incongruencias encontradas en los análisis morfométricos, citogenéticos y moleculares, que sustentan la existencia de al menos cinco especies reconocibles, algunas aún por describir. En Bolivia, una sola especie está presente: T. pachyurus, listada anteriormente como T. apereoides en Salazar-Bravo et al. (2003). Esta última especie (T. apereoides) está ahora restringida al este de Brasil (Pessóa et al. 2015).
Especies introducidas
Los mamíferos introducidos o exóticos son especies no nativas de un área geográfica e incluyen formas domésticas (por ejemplo, el ganado) y asilvestrado (por ejemplo, perros, cerdos, cabras) en zonas rurales y en áreas protegidas del país (Aguirre et al. 1996, Aliaga-Rossel & Painter 2010, Aliaga-Rossel et al. 2012, Rico et al. 2015) por lo que es importante considerarlas en este trabajo. Las especies de mamíferos introducidos en Bolivia son un total de 14 especies, pertenecientes a cinco órdenes, siete familias y 12 géneros. La lista se presenta a continuación:
ORDEN CARNÍVORA Bowdich, 1821
FAMILIA Canidae Fischer von Waldheim, 1817
GÉNERO Canis Linnaeus, 1758
Canis lupus familiaris Linnaeus, 1758
FAMILIA Felidae Fischer von Waldheim, 1817
GÉNERO Felis Linnaeus, 1758 Felís catus Linnaeus, 1758
ORDEN PERISSODACTYLA Owen, 1848
SUBORDEN Hippomorpha Wood, 1937
FAMILIA Equidae Gray, 1821
GÉNERO Equus Linnaeus, 1758
Equusferus caballus Linnaeus, 1758
Equus asinus Linnaeus, 1758
ORDEN CETARTIODACTYLA Montgelard, Catzeflis y Douzery, 1997
SUBORDEN Suina Gray, 1868
FAMILIA Suidae Gray, 1821
GÉNERO Sus Linnaeus, 1758
Sus scrofa Linnaeus, 1758
FAMILIA Bovidae Gray, 1821
GÉNERO Bos Linnaeus, 1758
Bos taurus Linnaeus, 1758
GÉNERO Bubalus Smith, 1827
Bubalus bubalis (Linnaeus, 1758)
GÉNERO Capra Linnaeus, 1758
Capra hírcus (Linnaeus, 1758)
GÉNERO Ovis Linnaeus, 1758
Ovis arles Linnaeus, 1758
ORDEN RODENTIA Bowdich, 1821
FAMILIA Muridae Illiger, 1811
GÉNERO Mus Linnaeus, 1758
Mus musculus Linnaeus, 1758
GÉNERO Rattus Fischer, 1803
Rattus norvegícus (Berkenhout, 1769)
Rattus rattus (Linnaeus, 1758)
ORDEN LAGOMORPHA Brandt, 1855
FAMILIA Leporidae Fischer, 1817
GÉNERO Lepus Linnaeus, 1758
Lepus europaeus Pallas, 1778
GÉNERO Oryctolagus Lilljeborg, 1866
Oryctolagus cunículus (Linnaeus, 1758)
Discusión
En los últimos 16 años, desde la publicación de Salazar-Bravo et al. (2003), la lista de especies de mamíferos presentes en Bolivia se ha incrementado de 356 a 406 especies nativas (incluyendo al hombre que no fue listado anteriormente), lo que constituye un incremento de 50 especies. Esto representa la adición de aproximadamente 3.2 especies nuevas anualmente. Si comparamos este incremento promedio de especies anuales con las listas más recientes para Colombia (Solari et al. 2013, Ramírez-Chaves et al. 2016) y Argentina (Teta et al. 2018), el incremento de Bolivia fue inferior al de Colombia, que registró en un período de 16 años, una adición promedio de 5.5 especies al año, pero fue superior al de Argentina, que tuvo, en un período de 12 años, un incremento promedio de 1.9 especies. En un contexto histórico, el número de especies conocidas para Bolivia se ha incrementado homogéneamente, excepto entre 1980 y 1985 cuando la lista pasó de 207 a 277 especies (14 especies anualmente). En las décadas previas y en las subsiguientes, incluyendo los últimos 16 años, la tasa de incremento ha estado en el rango de 5 a 3 especies al año (Fig. 1).
Las 406 especies de mamíferos nativos listados en este trabajo corresponden a 11 órdenes, 46 familias y 196 géneros (Tabla 1). A éstas se suman 14 especies de mamíferos introducidos (incluyendo especies domésticas), representados en cinco órdenes, siete familias y 12 géneros. Los tres órdenes con el mayor número de especies son Rodentia con 148 especies (36.6 % del total), Chiroptera con 138 especies (34.0 % del total) y Didelphimorphia con 35 especies (8.8% del total). Estos tres órdenes suman en conjunto 321 especies (79.1% del total de especies de mamíferos). Los otros órdenes presentados en orden descendiente por número de especies son: Carnívora (27), Primates (25), Cetartiodactyla (15), Cingulata (10), Pilosa (5) y con una sola especie Paucituberculata, Perissodactyla y Lagomorpha.
Los taxones jerárquicos superiores se mantuvieron más o menos estables con respecto a la lista de Salazar-Bravo et al. (2003). A nivel de orden se destacan la inclusión de Cingulata y Pilosa como órdenes separados, siguiendo la taxonomía de Gardner (2007b) y la inclusión de los órdenes Artiodactyla y Cetácea bajo Cetartiodactyla, dado que estudios moleculares han mostrado una relación filogenética entre estos dos órdenes (e.g., Montgelard et al. 1997, Gingerich et al. 2017; ver mayores detalles en las anotaciones taxonómicas). A nivel de familia un cambio notable es la inclusión de la capibara o carpincho (Hydrochoerus hydrochaeris) como miembro de la familia Caviidae, en vez de en su propia familia Hydrochaeridae, atendiendo a resultados de análisis filogenéticos (e.g., Upham & Patterson 2012, 2015; ver mayores detalles en las anotaciones taxonómicas). La familia Phyllostomidae tuvo grandes cambios en las revisiones de Baker et al. (2016) y Cirranello et al. (2016); a nivel de subfamilias, de las 11 actuales, cuatro fueron validadas o redefinidas y se describieron dos. A nivel de subfamilia, en el orden Didelphimorphia se adoptó la propuesta de Voss & Jansa (2009), quienes constituyeron la subfamilia Glironiinae dentro de la familia Didelphidae en la que está incluida el género Glironia que fue anteriormente listado en la subfamilia Caluromyinae.
A nivel de los taxones jerárquicos menores se han producido numerosos cambios desde la lista de mamíferos de Salazar-Bravo et al. (2003) y la actualización de la lista de murciélagos de Aguirre et al. (2010). Se han adicionado a la lista un total de 19 nuevos géneros, 21 nuevos registros de especies con localidad tipo en otros países, 14 nuevas especies para la ciencia con localidad tipo en el país y 65 cambios de nombre con base en revisiones taxonómicas (Tabla 2; ver anotaciones taxonómicas). El orden Rodentia es el que ha tenido mayores cambios, seguido por los órdenes Didelphimorphia, Chiroptera y Primates. En cuanto a las nuevas especies para la ciencia, el orden Rodentia tiene nueve nuevas especies (Hylaeamys acritus, Nectomys sp., Oecomys sydandersoni, Oligoryzomys pachecoi, Thomasomys andersoni, Ctenomys andersoni, Ctenomys erikacuellarae, Ctenomys lessaii y Ctenomys yatesi); seguido por Chiroptera y Didelphimorphia con dos especies cada uno (Micronycteris yatesi, Myotis midastactus, Marmosops creightoni, Monodelphis sanctarosae, respectivamente); y finalmente Primates con una especie (lecturocebus aureipalatii). Cinco de estas especies provienen del departamento de Santa Cruz, tres del departamento de Cochabamba, dos del departamento de La Paz, dos del departamento de Chuquisaca y una del departamento del Beni.
Un análisis de especies conocidas para Bolivia en comparación con las listas de especies en países limítrofes (en particular Brasil y Perú) muestra que el grupo menos representado, comparativamente, es el de los equímidos. En particular, los equímidos arborícolas como Pattonomys, Echimys, y varios cursoriales o semi-fosoriales como Clyomys y Carterodon. Aquellas investigaciones que están trabajando en áreas limítrofes requerirán métodos no convencionales para registrar especímenes de estos géneros.
En el presente trabajo registramos un total de 25 especies endémicas para Bolivia. El orden Rodentia es el que tiene el mayor número de especies, con un total de 20 especies, incluyendo dos especies aún no descritas (Tabla 1). El género Ctenomys es el que tiene el mayor endemismo, con un total de seis especies. A la fecha sólo se conoce el estado de conservación de nueve de las 25 especies endémicas a nivel nacional (Tarifa & Aguirre 2009, T. Tarifa datos no publicados) y lo mismo ocurre a nivel mundial (IUCN 2019); el resto de las especies no ha sido evaluado o se considera con datos insuficientes, principalmente porque no se conocen los aspectos más importantes de su historia natural (Le., área de ocupación, abundancia, tendencia poblacional). Estos aspectos deben ser evaluados por los investigadores en Bolivia y asegurar que estas especies se incluyan en planes de conservación nacionales.
El incremento sucesivo en el número de especies desde la primera lista publicada por Anderson en 1985, en la que reportaba un total de 277 especies, a la presente lista, con 406 especies (Tabla 3), es una muestra de lo mucho que se ha avanzado en el conocimiento de la diversidad de los mamíferos en Bolivia. No obstante, aún queda mucho por hacer en el conocimiento de los mamíferos en el país. Se espera que producto de esfuerzos de inventario de la biodiversidad que se han dado recientemente (e.g., Identidad Madidi) y la revisión taxonómica de diferentes taxones de mamíferos, se describan nuevas especies para la ciencia y por tanto se incremente el registro de nuevas especies para el país (Salazar-Bravo datos no publicados, Bernal, Siles y Wallace datos no publicados). Para esta tarea, las colecciones científicas de historia natural continuarán jugando un rol muy importante, ya que los especímenes de referencia constituyen la evidencia más sólida e indispensable en la taxonomía.
La diversidad biológica de Bolivia constituye un campo fértil de estudio para los biólogos y una responsabilidad para que las acciones de conservación aseguren su presencia en el país para las generaciones futuras. Dos de los mayores desafíos identificados al momento son: 1) la necesidad permanente de formación profesional en sistemática y taxonomía y 2) la disponibilidad de claves de identificación actualizadas que faciliten los trabajos de inventarios y ecología. Los listados taxonómicos constituyen la base fundamental sobre la que se asientan las decisiones legales que ayuden a establecer las medidas de conservación, ejemplos de ello son las evaluaciones sobre el riesgo de extinción de las especies (Le., libros rojos), y las decisiones de donde establecer áreas prioritarias para la conservación (e.g., Aguirre et al. 2016). Un pobre entendimiento de la taxonomía de las especies representa una limitante para las acciones de conservación (Vogel Ely et al. 2017) resultando en la pérdida de la biodiversidad por falta de políticas que normen el impacto de las actividades humanas sobre las especies y los ecosistemas de los que éstas dependen.
Agradecimientos
Los autores agradecen a Robert S. Voss por sus generosos comentarios a la lista de marsupiales y a Eric Yensen por la revisión del texto sobre Cetartiodactyla y el resumen en inglés. Las siguientes personas proveyeron referencias y/o información: Agustín Abba, Elisandra Chiquito, Guillermo D'Elía, Noé de la Sancha, Luán Gabriel De Lima Silva, Jon Dunnum, Isabel Galarza, Rita Gomes Rocha, Pablo Jayat, Isabel Moya, Adriana Rico, Joseph A. Cook, Sofía Marques Silva, Ulyses Par diñas, Bruce Patterson, Silvia Pavan, Sergio Solari, Cleusa Vogel Ely, Alexandra M. R. Bezerra, Robert S. Voss, Eric Yensen y José Luis Poma Urey. Finalmente, las siguientes instituciones fueron fundamentales para la producción de este trabajo: Centro de Biodiversidad y Genética (FCyT, UMSS), Orma J. Smith Museum of Natural History (The College of Idaho, USA), Colección Boliviana de Fauna, Fundación Gordon y Betty Moore, Instituto de Ecología y Carrera de Biología (Universidad Mayor de San Andrés), Museo de Historia Natural "Alcides d'Orbigny", Museum of Southwestern Biology (University of New México, USA), Programa para la Conservación de los Murciélagos de Bolivia, Whitley Fund for Nature y Wildlife Conservation Society. Especial agradecimiento a Ulyses Pardiñas y Sergio Solari quienes revisaron el manuscrito y aportaron a mejorar el mismo.
Referencias
Abba, A.M., G.H. Cassini, G. Valverde, M-F. Tilak, S.F. Vizcaíno, M. Superina & F. Delsuc. 2015. Systematics of hairy armadillos and the taxonomic status of the Andean hairy armadillo (Chaetophractus nationi). Journal of Mammalogy 96: 673–689.
Acosta, L.H. & C. Venegas. 2006. Algunas consideraciones taxonómicas de Histiotus laephotis e H. macrotus, en Bolivia. Kempffiana 2:109–115.
Acosta, L.H., J.L. Poma Urey & H. Azurduy. 2018. Nuevos registros del puerco espín cola corta (Coendou rufescens Gray 1865) en bosques nublados de Bolivia. Kempffiana 14: 22–31.
Agnarsson, I., M. Kuntner & L.J. May–Collado. 2010. Dogs, cats, and kin: A molecular species-level phylogeny of Carnivora. Molecular Phylogenetics and Evolution 54:726–745.
Aguirre, L.F., C.J. Mamani S., K. Barboza-Márquez & H. Mantilla-Meluk. 2010. Lista actualizada de los murciélagos de Bolivia. Revista Boliviana de Ecología y Conservación Ambiental 27: 1–7.
Aguirre, L.F., W. Hanagarth & R.J. de Urioste. 1996. Mamíferos del Refugio de Vida Silvestre Espíritu, Dpto. Beni, Bolivia. Ecología en Bolivia 28:29–44.
Aguirre, L. F., R. A. Medellín, B. Rodríguez-Herrera. 2016. From threat to opportunity, strategies for bat conservation in the Neotropics. pp. 140-153. En: A. A. Aguirre & R. Sukumar, Tropical Conservation. Perspectives on Local and Global Priorities. Oxford University Press, Nueva York.
Aliaga-Rossel, E. 2010. Conservation of the river dolphin (Inia boliviensis) in Bolivia. pp. 55–70. En: Ruíz-Garcia, M. & J. Shostell (eds.) Biology, Evolution and Conservation of the River Dolphins in South America and Asia: Unknown Dolphins in Danger. Nova Science Publishers, Inc., Nueva York.
Aliaga-Rossel, E. & L. Painter. 2010. Tayassuidae y Suidae. pp. 573–596. En: Wallace, R.B., H. Gómez, Z.R. Porcel & D.I. Rumiz (eds.) Distribución, Ecología y Conservación de los Mamíferos Medianos y Grandes de Bolivia. Centro de Ecología Difusión Simón I. Patiño, Santa Cruz.
Aliaga-Rossel, E., B. Ríos-Uzeda & H. Ticona. 2012. Amenazas de perros domésticos en la conservación del cóndor, el zorro y el puma en las tierras altas de Bolivia. Revista Latinoamericana de Conservación 2-3: 78–81.
Allen, J.A. 1915. Review of the South American Sciuridae. Bulletin of the American Museum of Natural History 34: 147–309.
Anderson, S. 1985. Lista preliminar de mamiferos bolivianos. Cuadernos de la Academia Nacional de Ciencias de Bolivia 65: 5-16. [ Links ]
Anderson, S. 1993. Los mamiferos bolivianos: notas de distribuci6n y claves de identificaci6n. Publicación Especial del Instituto de Ecología (Colección Boliviana de Fauna), La Paz. 159 p.
Anderson, S. 1997. Mammals of Bolivia, taxonomy and distribution. Bulletin of the American Museum of Natural History 231: 1–652.
Azurduy Ferreira, H. 2005. Descripción de una nueva especie de Ctenomys (Rodentia, Ctenomyidae) de los Valles Interandinos de Bolivia. Kempffiana 1: 70–74.
Baird, A.B., J.K. Braun, M.A. Mares, J.C. Morales, J.C. Patton, C.Q. Tran & J.W. Bickham. 2015. Molecular systematic revision of tree bats (Lasiurini): doubling the native mammals of the Hawaiian Islands. Journal of Mammalogy 96: 1255–1274.
Baird, A.B., J.K. Braun, M.D. Engstrom, A.C. Holbert, M.G. Huerta, B.K. Lim, M.A. Mares, J.C. Patton & J.W. Bickham. 2017. Nuclear and mtDNA phylogenetic analyses clarify the evolutionary history of two species of native Hawaiian bats and the taxonomy of Lasiurini (Mammalia: Chiroptera). PLoS ONE 12(10): e0186085.
Baker, R.J., S. Solari, A. Cirranello & N.B. Simmons. 2016. Higher level classification of phyllostomid bats with a summary of DNA synapomorphies. Acta Chiropterologica 18: 1-38.
Barnett, R., I. Barnes, M.J. Phillips, L.D. Martin, C.R. Harington, J.A. Leonard & A. Cooper. 2005. Evolution of the extinct Sabretooths and the American cheetah-like cat. Current Biology 15(15): R589–R590.
Bidau, C.J. 2015. Family Ctenomyidae Lesson, 1842. pp. 818–877. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Boisserie, H.-R., F. Lihoreau, M. Brunet & F.C. Howell. 2005. The position of Hippopotamidae within Cetartiodactyla. Proceedings of the National Academy of Sciences of the United States of America 102: 1537–1541.
Boisserie, J.-R., F. Lihoreau, M. Orliac, R.E. Fisher, E.M. Weston & S. Ducrocq. 2010. Morphology and phylogenetic relationships of the earliest known hippopotamids (Cetartiodactyla, Hippopotamidae, Kenyapotaminae). Zoological Journal of the Linnean Society 158: 325–366.
Bonvicino, C.R., F. Casado & M. Weksler. 2014. A new species of Cerradomys (Mammalia: Rodentia: Cricetidae) from Central Brazil, with remarks on the taxonomy of the genus. Zoologia (Curitiba) 31: 525-–540.
Bonvicino, C.R. & M. Weksler. 2015. Genus Nectomys Peters, 1861. pp. 369–377. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Boubli, J.P., A.B. Rylands, I.P. Farias, M.E. Alfaro & J. Lynch Alfaro. 2012. Cebus phylogenetic relationships: A preliminary reassessment of the diversity of the untufted capuchin monkeys. American Journal of Primatology 74: 381–393.
Braun, J.K. & J.L. Patton. 2015. Genus Graomys Thomas, 1916. pp. 523–531. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Brito, D. 2004. Lack of adequate taxonomic knowledge may hinder endemic mammal conservation in the Brazilian Atlantic Forest. Biodiversity and Conservation 13: 2135–2144.
Brooks, D.M., T. Tarifa, J.M. Rojas, R.J. Vargas & H. Aranibar. 2001. A preliminary assessment of the mammalian fauna of the eastern Bolivian panhandle. Mammalia 65: 509–520.
Brooks, D.M., R.J. Baker, R.J. Vargas M., T. Tarifa, H. Aranibar & J.M. Rojas. 2004. A new species of Oryzomys (Rodentia: Muridae) from an isolated pocket of Cerrado in Eastern Bolivia. Occasional Papers Museum of Texas Tech University 241: 1–11.
Burgin, C.J., J. Colella, P.L. Kahn & N.S. Upham. 2018. How many species of mammals are there? Journal of Mammalogy 99: 1–14.
Byrne, H., A.B. Rylands, J.C. Carneiro, J.W. Lynch Alfaro, F. Bertuol, M.N.F. da Silva, M. Messias, C.P. Groves, R.A. Mittermeier, I. Farias, T. Hrbek, H. Schneider, I. Sampaio & J.P. Boubli. 2016. Phylogenetic relationships of the New World titi monkeys (Callicebus): first appraisal of taxonomy based on molecular evidence. Frontiers in Zoology 13:10.
Calderón-Acevedo, C.A. & N.C. Muchhala. 2018. Identification and diagnosis of Anoura fistulata with remarks on its presumed presence in Bolivia. Journal of Mammalogy 99: 131–137.
Carleton, M.D., L.H. Emmons & G.G. Musser. 2009. A new species of the rodent genus Oecomys (Cricetidae: Sigmodontinae: Oryzomyini) from eastern Bolivia, with emended definitions of O. concolor (Wagner) and O. mamorae (Thomas). American Museum Novitates 3661: 1–32.
Carleton M.D. & G.G. Musser. 2015. Genus Oecomys Thomas, 1906. pp. 393–416. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Cazzaniga, N.J., C. Cañon & U. Pardiñas. 2019. The availability, authorships and dates of tribal names in the Sigmodontinae (Rodentia, Cricetidae) current classification. Bionomina 15: 37-50.
Ceballos, G., P.R. Ehrlich, A.D. Barnosky, A. García, R.M. Pringle & T.M. Palmer. 2015. Accelerated modern human–induced species losses: Entering the sixth mass extinction. Science Advances 1: e1400253.
Chiquito, E.A. 2015. Sistemática do género Nectomys Peters, 1861 (Cricetidae: Sigmodontinae). Tese (Doutorado). Escola Superior de Agricultura "Luiz de Queiroz" Centro de Energia Nuclear na Agricultura, Piracicaba. [ Links ]
Cirranello, A., N.B. Simmons, S. Solari & R.J. Baker. 2016. Morphological diagnoses of higher-level phyllostomid taxa (Chiroptera: Phyllostomidae). Acta Chiropterologica 18: 39–71.
Copa Alvaro, M.E., G.S. Mendieta & A.L. Deane. 2014. Distribución potencial de la chinchilla de cola corta (Chinchilla chinchilla, Rodentia) en el sudoeste de Bolivia. Ecología en Bolivia 49: 65–76.
Cossíos, D., M. Lucherini, M. Ruíz-García &B. Angers. 2009. Influence of ancient glacial periods on the Andean fauna: The case of the Pampas Cat (Leopardus colocolo). BMC Evolutionary Biology 9: 1–12.
Cozzuol, M., C.L. Clozato, E.C. Holanda, F.H.G. Rodrigues, S. Nienow, B. de Thoisy, R.A.F. Redondo & F.R. Santos. 2013. A new species of tapir from the Amazon. Journal of Mammalogy 94: 1331–1345.
D’Elía, G. 2003. Phylogenetics of Sigmodontinae (Rodentia, Muroidea, Cricetidae), with special reference to the akodont group, and with additional comments on historical biogeography. Cladistics 19: 307–323.
D’Elía, G.L. Luna, E.M. Gonzalez & B.D. Patterson. 2006. On the Sigmodontinae radiation (Rodentia, Cricetidae): An appraisal of the phylogenetic position of Rhagomys. Molecular Phylogenetics and Evolution 38: 558–564.
D’Elía, G., U.F.J. Pardiñas, P. Teta & J.L. Patton. 2007. Definition and diagnosis of a new tribe of sigmodontine rodents (Cricetidae: Sigmodontinae), and a revised classification of the subfamily. Gayana 71: 187–194.
D’Elía, G., U.F.J. Pardiñas, J. Pablo Jayat & J. Salazar-Bravo. 2008. Systematics of Necromys (Rodentia, Cricetidae, Sigmodontinae): Species limits and groups, with comments on historical biogeography. Journal of Mammalogy 89: 778–790.
D’Elía, G. & U.F.J. Pardiñas. 2015a. Subfamily Sigmodontinae Wagner, 1843. pp. 63–73. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
D’Elía, G. & U.F.J. Pardiñas. 2015b. Tribe Akodontini Vorontsov 1959. pp. 140–144. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
D’Elía, G., J.D. Hanson, M.R. Mauldin, P. Teta & U.F.J. Pardiñas. 2015. Molecular systematics of South American marsh rats of the genus Holochilus (Muroidea, Cricetidae, Sigmodontinae). Journal of Mammalogy 96: 1081–1094.
Da Cruz, M.O.R. & M. Weksler. 2018. Impact of tree priors in species delimitation and phylogenetics of the genus Oligoryzomys (Rodentia: Cricetidae). Molecular Phylogenetics and Evolution 119: 1–12.
Daugherty, C.H., A. Cree, J.M. Hay & M.B. Thompson. 1990. Neglected taxonomy and continuing extinctions of tuatara (Sphenodon). Nature 347: 177–179.
Davis, W.B. & A.L. Gardner. 2008. Genus Eptesicus. pp. 440-449. En: Gardner, A.L. (ed.). Mammals of South America: Marsupials, Xenarthrans, Shrews and Bats. University of Chicago Press.
de la Torre, S & A.B. Rylands. 2008. Cebuella pygmaea. The IUCN Red List of Threatened Species 2008: e.T41535A10493764. http://dx.doi.org/10.2305/IUCN.UK.2008.RLTS.T41535A10493764.en.
De Lima Silva, L.G., D.C. Ferreira & R. Vieira Rossi. 2019. Species diversity of Marmosa subgenus Micoureus (Didelphimorphia, Didelphidae) and taxonomic evaluation of the white-bellied woolly mouse opossum Marmosa constantiae. Zoological Journal of the Linnean Society XX: 1-38.
De Vivo, M. & A.P. Carmignotto. 2015. Family Sciuridae G. Fischer, 1817. pp. 1–48. En: Patton, J.L., U.F.J. Pardiñas &G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Delgado, E., L.F. Pacheco, J. Salazar-Bravo & O. Rocha. 2018a. Rediscovery of the chinchilla in Bolivia. Oryx 52: 13–15.
Delgado, E., L.F. Pacheco, J. Salazar-Bravo & O. Rocha. 2018b. La chinchilla de cola corta (Chinchilla chinchilla) en Bolivia: comentarios sobre localidades reportadas y bases para su conservación. Ecología en Bolivia 53: 31–38.
Delsuc, F., F.M. Catzeflis, M.J. Stanhope & E.J.P. Douzery. 2001. The evolution of armadillos, anteaters and sloths depicted by nuclear and mitochondrial phylogenies: implications for the status of the enigmatic fossil Eurotamandua. Proceedings of the Royal Society Biological Sciences Series B 268: 1605-1615.
Delsuc, F., M. Superina, M.K. Tilak, E.J. Douzery & A. Hassanin. 2012. Molecular phylogenetics unveils the ancient evolutionary origins of the enigmatic fairy armadillos. Molecular Phylogenetics and Evolution 62: 673–680.
Delsuc, F., M. Kuch, G. C. Gibb, E. Karpinski, D. Hackenberger, P. Szpak, J. G. Martínez, J. I. Mead, H. G. McDonald, R. D.E. MacPhee, G. Billet, L. Hautier, & H. N. Poinar. 2019. Ancient Mitogenomes Reveal the Evolutionary History and Biogeography of Sloths. Current Biology 29, 2031–2042.
Di Fiore, A., P.B. Chaves, F.M. Cornejo, C.A. Schmitt, L. Cortés-Ortiz, V. Fagundes, C. Roos & V. Pacheco. 2015. The rise and fall of a genus: Complete mtDNA genomes shed light on the phylogenetic position of yellow-tailed woolly monkeys, Lagothrix flavicauda, and on the evolutionary history of the family Atelidae (Primates: Platyrrhini). Molecular Phylogenetics and Evolution 82: 495–510.
Díaz Luque, J.A., V. Beraud, P.J. Torres, F.P. Kacoliris, G. Daniele, R.B. Wallace & I. Berkunsky. 2012. First record of Pantanal cat, Leopardus colocolo braccatus, in Bolivia. Mastozoología Neotropical 19: 299–301.
Díaz-Nieto, J.F. & R.S. Voss. 2016. A revision of the didelphid marsupial genus Marmosops, Part 1. Species of the subgenus Sciophanes. Bulletin of the American Museum of Natural History 402: 1–70.
Díaz-Nieto, J.F., S.A. Jansa & R.S. Voss. 2016. DNA sequencing reveals unexpected recent diversity and an ancient dichotomy in the American marsupial genus Marmosops (Didelphidae: Thylamyini). Zoological Journal of the Linnean Society 176: 914–940.
Duarte, J.M.B., S. Gonzalez & J. Maldonado. 2008. The surprising evolutionary history of South American deer. Molecular Phylogenetics and Evolution 49: 17–22.
Dunnum, J.L. & J. Salazar-Bravo. 2010. Phylogeny, evolution, and systematics of the Galea musteloides complex (Rodentia: Caviidae). Journal of Mammalogy 91: 243–259.
Dunnum, J.L. 2015. Family Caviidae G. Fischer, 1817. pp. 690-726. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Dragoo, J.W., J. Salazar-Bravo, L.J. Layne & T.L. Yates. 2003. Relationships within the Calomys callosus species group based on amplified fragment length polymorphims. Biochemical Systematics and Ecology 31: 703–713.
Dutra, R.P., D.M. Casali, R.V. Missagia, G.M. Gasparini, F.A. Perini & M.A. Cozzuol. 2017. Phylogenetic systematics of peccaries (Tayassuidae: Artiodactyla) and a classification of South American tayassuids. Journal of Mammalian Evolution 24: 345–358.
Emmons, L. 1997. Mammals of the Rio Urucuti basin, south central Chuquisaca, Bolivia. pp. 30-33, App. 4-5. En: Schulenberg, T.S. & K. Awbrey (eds.) A rapid assessment of the humid forest of south central Chuquisaca, Bolivia. Conservation International, RAP Working Papers 8, Washington, D.C.
Emmons, L.H. 1998. Mammal species of Parque Nacional Noel Kempff Mercado. pp. 341–347. App. 3. En: Killeen, T.J. & T. S. Schulenberg (eds.) A Biological Assessment of Parque Nacional Noel Kempff Mercado, Bolivia. RAP Working Paper 10, Conservation International, Washington, D.C.
Emmons, L.H. 1999. Two new species of Juscelinomys (Rodentia: Muridae) from Bolivia. American Museum Novitates 3280: 1–15.
Emmons, L.H. 2002. Mammal fauna of northestern Pando, Bolivia, 1992. pp. 79-82, App. 5. En: Montambault, J.R. (ed.) Informes de las Evaluaciones Biológicas Pampa del Heath, Perú, Alto Madidi, Bolivia y Pando, Bolivia. RAP Bulletin of Biological Assessment 24, Conservation International, Washington, D.C.
Emmons, L.H. & J.L. Patton. 2005. A new species of Oryzomys (Rodentia: Muridae) from eastern Bolivia. American Museum Novitates 3478: 1–26.
Emmons, L.H., V. Chávez, N. Rocha, B. Phillips, I. Phillips, L.F. del Aguila & M.J. Swarner. 2006. The non-flying mammals of Noel Kempff Mercado National Park (Bolivia). Revista Boliviana de Ecología y Conservación Ambiental 19: 23–46.
Emmons, L.H. & J.L. Patton. 2012. Taxonomic revision of Bolivian Juscelinomys (Rodentia, Cricetidae) with notes on morphology and ecology. Mammalia 76: 285–294.
Emmons, L.H., Y.L.R. Leite & J.L. Patton. 2015. Family Echimyidae Gray, 1825. pp. 877–880. En: Patton, J. L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Emmons L.H. & P.H. Fabre. 2018. A review of Pattonomys/Toromys clade (Rodentia: Echimyidae), with descriptions of a new Toromys species and a new genus. American Museum Novitates 3894: 1–52.
Feijó A., P.A. Rocha & S.L. Althoff. 2015. New species of Histiotus (Chiroptera: Vespertilionidae) from northeastern Brazil. Zootaxa 4048: 412–427.
Feijó A. & P. Cordeiro-Estrela. 2016. Taxonomic revision of the Dasypus kappleri complex, with revalidations of Dasypus pastasae (Thomas, 1901) and Dasypus beniensis Lönnberg, 1942 (Cingulata, Dasypodidae). Zootaxa 4170(2):271–297.
Feijó A., B.D. Patterson & P. Cordeiro-Estrela.2018. Taxonomic revision of the long-nosed armadillos, Genus Dasypus Linnaeus, 1758 (Mammalia, Cingulata). PLoS ONE 13(4): e0195084. https://doi.org/10.1371/journal.pone.0195084
Fernandes Semedo, T.B &A. Feijó. 2016. Filling the gap: first record of the transparent winged big-eared bat Histiotus diaphanopterus (Chiroptera: Vespertilionidae) in southwestern Brazil. Mammalia 81: 323–327.
Garbino, G.S.T. & A. Tejedor. 2013. Natalus macrourus (Gervais, 1856) (Chiroptera: Natalidae) is a senior synonym of Natalus espiritosantensis (Ruschi, 1951). Mammalia 77: 237–240.
Gardner, A.L. (ed.) 2007[2008]. Mammals of South America, Volume 1 Marsupials, xenarthrans, shrews, and bats. The University of Chicago Press, Chicago and London. 669 p.
Gardner, A. L. 2007. Tribe Monodelphini Hershkovitz, 1992. Pp. 39-43. En: A. L. Gardner (ed.) Mammals of South America, Volume 1 Marsupials, Xenarthrans, Shrews, and Bats. The University of Chicago Press, Chicago y Londres.
Gardner, A. L. & M. Dagosto. 2007. Tribe Metachirini Reig, Kirsch, and Marshall, 1985. Pp. 35-39. En: A. L. Gardner (ed.) Mammals of South America, Volume 1 Marsupials, Xenarthrans, Shrews, and Bats. The University of Chicago Press, Chicago and London.
Gardner, A.L. & C.O. Handley, Jr. 2007. Genus Lasiurus Gray, 1831. Pp. 457–468. En: Gardner, A.L. (ed.) Mammals of South America, Volume 1 Marsupials, Xenarthrans, Shrews, and Bats. The University of Chicago Press, Chicago and London.
Gardner, S.L., J. Salazar-Bravo & J.A. Cook. 2014. New species of Ctenomys Blainville 1826 (Rodentia: Ctenomyidae) from the lowlands and central valleys of Bolivia. Special Publications Museum of Texas Tech University 62: 1–34.
Giarla, T.C., R.S. Voss & S.A. Jansa. 2010. Species limits and phylogenetic relationships in the didelphid marsupial genus Thylamys based on mitochondrial DNA sequences and morphology. Bulletin of the American Museum of Natural History 346: 1–67.
Giarla, T.C., R.S. Voss & S.A. Jansa. 2014. Hidden diversity in the Andes: Comparison of species delimitation methods in montane marsupials. Molecular Phylogenetics and Evolution 70: 137–151.
Gibb, G.C., F. L. Condamine, M. Kuch, J. Enk, N. Moraes-Barros, M. Superina, H. N. Poinar & F. Delsuc. 2015. Shotgun mitogenomics provides a reference phylogenetic framework and timescale for living Xenarthrans. Molelcular Biology and Evolution 33:621–642.
Gingerich, P.D., M.U. Haq, I.S. Zalmout, K.I. Hussain & M.S. Malkani. 2001. Origin of whales from early artiodactyls: hands and feet of Eocene Protocetidae from Pakistan. Science 293: 2239–2242.
Gingerich, P.D., K. Heissig, R.M. Bebej & W. von Koenigswald. 2017. Astragali of Pakicetidae and other early-to-middle Eocene archaeocetes (Mammalia, Cetacea) of Pakistan: locomotion and habitat in the initial stages of whale evolution. Palaeontologische Zeitschrift 91: 601–627.
Gonçalves, P.R., P. Teta & C.R. Bonvicino. 2015. Genus Holochilus Brandt, 1835. pp. 325–335. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
González-Ittig, R.E., P.C. Rivera, S.C. Levis, G.E. Calderón & C.N. Gardenal. 2014. The molecular phylogenetics of the genus Oligoryzomys (Rodentia: Cricetidae) clarifies rodent host-hantavirus associations. Zoological Journal of the Linnean Society 171: 457–474.
Gravena, W., I.P. Farias, M. Da-Silva, V. Da-Silva & T. Hrbek. 2014. Looking to the past and the future: were the Madeira River rapids a geographical barrier to the boto (Cetacea: Iniidae)? Conservation Genetics 15: 619–629.
Gregorin, R., L.M. Moras, L.H. Acosta, K.L. Vasconcellos, J.L. Poma, F. Rodrigues dos Santos & R.C. Paca. 2016. A new species of Eumops (Chiroptera: Molossidae) from southeastern Brazil and Bolivia. Mammalian Biology 81: 235–246.
Gurgel-Filho, N.M., A. Feijó & A. Langguth. 2015. Pequenos mamíferos do Ceará (Marsupiais, morcegos e roedores sigmodontíneos) com discussão taxonômica de algunas espécies. Revista Nordestina de Biologia 23: 3–150.
Gutiérrez, E., S.A. Jansa & R.S. Voss. 2010. Molecular systematics of mouse opossums (Didelphidae: Marmosa): Assessing species limits using mitochondrial DNA sequences, with comments on phylogenetic relationships and biogeography. American Museum Novitates 3692: 1–22.
Gutiérrez, E.E., K.M. Helgen, M.M. McDonough, F. Bauer, M.T.R. Hawkins, L.A. Escobedo-Morales, B.D. Patterson & J.E. Maldonado. 2017. A gene-tree test of the traditional taxonomy of American deer: the importance of voucher specimens, geographic data, and dense sampling. ZooKeys 697: 87–131.
Hazevoet, C.J. 1996. Conservation and species lists: taxonomic neglect promotes the extinction of endemic birds, as exemplified by taxa from eastern Atlantic islands. Bird Conservation International 6:181–196.
Handley Jr., C.O. & A.L. Gardner. (2008) Genus Histiotus. pp. 450-457. En: Gardner, A.L. (ed.). Mammals of South America: Marsupials, Xenarthrans, Shrews and Bats. University of Chicago Press, Chicago.
Hoofer, S.R. & R.A. Van Den Bussche. 2003. Molecular phylogenetics of the chiropteran family Vespertilionidae. Acta Chiropterologica 5:1–63.
Hurtado, N. & V. Pacheco. 2017. Revision of Neacomys spinosus (Thomas, 1882) (Rodentia: Cricetidae) with emphasis on Peruvian populations and the description of a new species. Zootaxa 4242: 401–440.
Hurtado, N. & G. D’Elía. 2018a. Taxonomy of the long-tailed mouse Oligoryzomys destructor (Sigmodontinae: Oryzomyini) with the designation of neotypes for Hesperomys destructor Tschudi, 1844 and Hesperomys melanostoma Tschudi, 1844. Journal of Zoological Systematics and Evolutionary Research 57: 1–18.
Hurtado, N. & G. D’Elía. 2018b. A new species of long-tailed mouse, genus Oligoryzomys Bangs, 1900 (Rodentia: Cricetidae), from the Bolivian Yungas. Zootaxa 4500: 341–362.
Hurtado, N, & G. D’Elía. 2019. An assessment of species limits of the South American mouse genus Oligoryzomys (Rodentia, Cricetidae) using unilocus delimitation methods. Zoologica Scripta 48: 557– 570.
Hurtado-Miranda, N.E. & V. Pacheco-Torres. 2014. Análisis filogenético del género Mimon Gray, 1847 (Mammalia, Chiroptera, Phyllostomidae) con la descripción de un nuevo género. Therya 5: 751–791.
Ibisch, P.L. 2001. Bolivia is a megadiversity country and a developing country. pp 213–241. En: Barthlott, W., M. Winiger&N. Biedinger (eds.) Biodiversity. Springer, Berlin, Heidelberg.
Isaac, N.J.B., J. Mallet & G.M. Mace. 2004. Taxonomic inflation: its influence on macroecology and conservation. TRENDS in Ecology and Evolution 19: 464–469.
IUCN 2019. The IUCN Red List of Threatened Species. Version 2019-1. http://www.iucnredlist.org. [ Links ]
Jayat, J.P., P.E. Ortiz, J. Salazar-Bravo, U.F.J. Pardiñas & G. D’Elía. 2010. The Akodon boliviensis species group (Rodentia: Cricetidae: Sigmodontinae) in Argentina: species limits and distribution, with the description of a new entity. Zootaxa 2409: 1–61.
Jayat, J.P., G. D’Elía, P.E. Ortiz & P. Teta. 2016a. A new species of the rodent genus Necromys Ameghino (Cricetidae: Sigmodontinae: Akodontini) from the Chaco Serrano grasslands of northwestern Argentina. Journal of Mammalogy 97: 1321–1335.
Jayat, J.P., P.E. Ortiz, F.R. González & G. D’Elía. 2016b. Taxonomy of the Phyllotis osilae species group in Argentina; the status of the “Rata de los nogales” (Phyllotis nogalaris Thomas, 1921; Rodentia: Cricetidae). Zootaxa 4083: 397–417.
Jayat, J.P., G. D’Elía, R. Torres, S.E. Pacheco, P.E. Ortiz, J. Salazar-Bravo & B.D. Patterson. 2017. Integration of morphological, ecological, and genetic evidence suggests that the genus Andinomys (Rodentia, Cricetidae) is monospecific. Journal of Mammalogy 98: 1060–1077.
Johnson, W.E., E. Eizirik, J. Pecon-Slattery, W.J. Murphy, A. Antunes, E. Teeling & S.J. O’Brien. 2006. The Late Miocene radiation of modern Felidae: a genetic
assessment. Science 311: 73–77.
Kadwell, M., M. Fernández, H.F. Stanley, R. Baldi, J.C. Wheeler, R. Rosadio & M.W. Bruford. 2001. Genetic analysis reveals the wild ancestors of the llama and the alpaca. Proceedings of the Royal Society, London B - Biological Sciences 268: 2575–2584.
Kitchener, A.C., Ch. Breitenmoser-Würsten, E. Eizirik, A. Gentry, L. Werdelin, A. Wilting, N. Yamaguchi, A.V. Abramov, P. Christiansen, C. Driscoll, J.W. Duckworth, W. Johnson, S.-J. Luo, E. Meijaard, P.J. O’Donoghue. K. Sanderson, M. Seymour, C. Bruford, M. Groves, K. Hoffmann, Z. Nowell, S. Timmons & S. Tobe. 2017. A revised taxonomy of the Felidae. The final report of the Cat Classification Task Force of the IUCN/ SSC Cat Specialist Group. Cat News Special Issue 11: 1–80.
Lanzone, C. & R.A. Ojeda. 2005. Citotaxonomía y distribución del género Eligmodontia (Rodentia, Cricetidae, Sigmodontinae). Mastozoología Neotropical 12: 73–77.
Lim, B.K., M.D. Engstrom, J.W. Bickham & J.C. Patton. 2007. Molecular phylogeny of New World sheath-tailed bats (Emballonuridae: Diclidurini) based on loci from the four genetic transmission systems in mammals. Biological Journal of the Linnean Society 93: 189–209.
Luna, L. & B.D. Patterson. 2003. A remarkable new mouse (Muridae: Sigmodontinae) from southeastern Peru: with comments on the affinities of Rhagomys rufescens (Thomas, 1886). Fieldiana, Zoology 101: 1–24.
Lynch Alfaro, J.W., A.J. De Sousa E Silva Jr. & A.B. Rylands. 2012. How different are robust and gracile capuchin monkeys? An argument for the use of Sapajus and Cebus. American Journal of Primatology 74: 273-286.
Madozzo-Jaén, M.C. & M.E. Pérez. 2017. The most ancient caviine rodent (Hystricognathi, Cavioidea) comes from the late Miocene of Northwest Argentina (South America). Historical Biology 29: 376–383.
Mantilla-Meluk, H., L. Siles & L.F. Aguirre. 2014. Geographic and ecological amplitude in the nectarivorous bat Anoura fistulata (Pyhllostomidae: Glossophaginae). Caldasia 36: 373–388.
Mares, M.A., J.K. Braun, B.S. Coyner & R.A. Van Den Bussche. 2008. Phylogenetic and biogeographic relationships of gerbil mice Eligmodontia (Rodentia, Cricetidae) in South America, with a description of a new species. Zootaxa 1753: 1–33.
Marín, J.C., B. Zapata, B.A. González, C. Bonacic, J.C. Wheeler, C. Casey, M.W. Bruford, R.E. Palma, E. Poulin, M.A. Alliende & A.E. Spotorno. 2007. Sistemática, taxonomía y domesticación de alpacas y llamas: nueva evidencia cromosómica y molecular. Revista Chilena de Historia Natural 80: 121–140.
Marsh, L.K. 2014. A taxonomic revision of the saki monkeys, Pithecia Desmarest, 1804. Neotropical Primates 21: 1–165.
Martínez, J. & R.B. Wallace. 2010. Pitheciidae. pp. 305–330. En: Wallace, R.B., H. Gómez, Z.R. Porcel & D.I. Rumiz (eds.) Distribución, Ecología y Conservación de los Mamíferos Medianos y Grandes de Bolivia. Centro de Ecología Difusión Simón I. Patiño, Santa Cruz.
Martínez-Lanfranco, J.A., D. Flores, J.P. Jayat & G. D’Elía. 2014. A new species of lutrine opossum, genus Lutreolina Thomas (Didelphidae), from the South American Yungas. Journal of Mammalogy 95: 225–240.
Mazák, J.H. 2012. Retraction for Christiansen and Mazák. A primitive Late Pliocene cheetah, and evolution of the cheetah lineage. Proceedings of the National Academy of Sciences of the United States of America 109: 15072–15072.
McKenna, M.C. & S. K. Bell. 1997. Classification of Mammals Above Species Level. Columbia University Press, Nueva York.
Ministerio de Medio Ambiente y Agua. 2014. Plan de Acción para la conservación de mamíferos amenazados. PGD impresiones, La Paz. 102 p. [ Links ]
Miranda, F., D.M. Casali, F.A. Perini, F.A. Machado & F.R. Santos. 2017. Taxonomic review of the genus Cyclopes Gray, 1821 (Xenarthra: Pilosa), with the revalidation and description of new species. Zoological Journal of the Linnean Society 183: 687–721.
Miserendino, R.S. & H. Azurduy. 2005. Nota sobre el primer espécimen de Myoprocta pratti (Rodentia, Dasyproctidae) para Bolivia. Kempffiana 1: 55–57.
Montgelard, C., F.M. Catzeflis & E. Douzery. 1997. Phylogenetic relationships of artiodactyls and cetaceans as deduced from the comparison of cytochrome b and 12s rRNA mitochondrial sequences. Molecular Biology and Evolution 14: 550–559.
Moratelli, R. & D.E. Wilson. 2014. A new species of Myotis (Chiroptera, Vespertilionidae) from Bolivia. Journal of Mammalogy 95: 17–25.
Moratelli, R. & D. Dias. 2015. A new species of nectar-feeding bat, genus Lonchophylla, from the Caatinga of Brazil (Chiroptera, Phyllostomidae). ZooKeys 514: 73–91.
Moratelli, R., L. Idárraga & D.E. Wilson. 2015. Range extension of Myotis midastactus (Chiroptera, Vespertilionidae) to Paraguay. Biodiversity Data Journal 3: e5708 doi: 10.3897/BDJ.3.e5708.
Moreira, J.R., M.R. Alvarez, T. Tarifa, V. Pacheco, A. Taber, D.G. Tirira, E.A. Herrera, K.M.P.M.F. Ferraz, J. Aldana-Dominguez & D.W. Macdonald. 2013. Taxonomy, natural history and distribution of the capybara. pp. 3–37. En: Moreira, J.R., K.M.P.M.B. Ferraz, E.A. Herrera & D. W. Macdonald (eds.) Capybara Biology, Use and Conservation of an Exceptional Neotropical Species. Springer, Nueva York.
Musser, G.G. & M.D. Carleton. 1993. Family Muridae. pp. 501–756. En: Wilson, D.E. & D.M. Reeder (eds.) Mammal Species of the World. 2nd edition. Smithsonian Institution Press, Washington, DC.
Musser, G.G. & M.D. Carleton. 2005. Superfamily Muroidea. pp. 894–1531. En: Wilson, D.E. & D.M. Reeder (eds.) Mammal Species of the World. 3rd edition. The Johns Hopkins University Press, Baltimore.
Naylor, G.J.P. & D.C. Adams. 2001. Are the fossil data really at odds with the molecular data? Morphological evidence for Cetartiodactyla phylogeny reexamined. Systematic Biology 50: 444–453.
Oliveira de, J.A. & P.R. Gonçalves. 2015. Genus Oxymycterus Waterhouse, 1837. pp. 247–268. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Orliac, M., J.-R. Boisserie, L. MacLatchy, F. Lihoreau & D. Pilbeam. 2010. Early Miocene hippopotamids (Cetartiodactyla) constrain the phylogenetic and spatiotemporal settings of hippopotamid origin. Proceedings of the National Academy of Sciences of the United States of America 107: 11871–11876.
Ortiz, P.E. & J.P. Jayat. 2015. Genus Neotomys Thomas, 1894. pp. 99–101. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Paca, R.C., L.H. Acosta & F.S. Aguanta. 2012. Primer registro de Tonatia bidens (Spix, 1823) (Chiroptera: Phyllostomidae), en Bolivia. Chiroptera Neotropical 18: 1063–1066.
Pacheco, V. 2015. Genus Thomasomys Coues, 1884. pp. 617–682. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Palma, R.E., E. Rodríguez-Serrano, E. Rivera-Milla, C.E. Hernandez, J. Salazar-Bravo, M.I. Carma, S. Belmar-Lucero, P. Gutierrez-Tapia, H. Zeballos & T.L. Yates. 2010. Phylogenetic relationships of the pygmy rice rats of the genus Oligoryzomys Bangs, 1900 (Rodentia: Sigmodontinae). Zoological Journal of the Linnean Society 160: 551–566.
Palma, R.E., D. Boric-Bargetto, J.P. Jayat, D.A. Flores, H. Zeballos, V. Pacheco, R.A. Cancino, F.D. Alfaro, E. Rodriguez-Serrano & U.F.J. Pardiñas. 2014. Molecular phylogenetics of mouse oposums: new findings on the phylogeny of Thylamys (Didelphimorphia, Didelphidae). Zoologica Scripta 43: 217–234.
Pardiñas, U.F.J., G. D’Elía & P. Teta. 2009. Una introducción a los mayores sigmodontinos vivientes: revisión de Kunsia Hershkovitz, 1966 y descripción de un nuevo género (Rodentia: Cricetidae). Arquivos do Museu Nacional, Rio de Janeiro 66: 509–594.
Pardiñas, U.F.J. & P. Teta. 2011. Fossil history of the marsh rats of the genus Holochilus and Lundomys (Cricetidae, Sigmodontinae) in southern South America. Estudios Geológicos 67: 111–129.
Pardiñas, U.F.J., P. Teta & J. Salazar-Bravo. 2015a. A new tribe of Sigmodontinae rodents (Cricetidae). Mastozoología Neotropical 22: 171–186.
Pardiñas, U.F.J., P. Teta, D. Alvarado-Serrano, L. Geise, J.P. Jayat, P.E. Ortiz, P.R. Gonçalves & G. D’Elía. 2015b. Genus Akodon Meyen, 1833. pp. 144–204. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Pardiñas, U.F.J., P. Teta, P.E. Ortiz, J.P. Jayat & J. Salazar-Bravo. 2015c. Genus Necromys Ameghino, 1889. pp. 232–247. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Pardiñas, U.F.J., L. Geise, K. Ventura & G. Lessa. 2016a. A new genus for Habrothrix angustidens and Akodon serrensis (Rodentia, Cricetidae): Again paleontology meets neontology in the legacy of Lund. Mastozoologia Neotropical 23: 93–115.
Pardiñas, U.F.J., P. Teta, J. Salazar-Bravo, P. Myers & C.A. Galliari. 2016b. A new species of arboreal rat, genus Oecomys (Rodentia, Cricetidae) from Chaco. Journal of Mammalogy 97: 1177–1196.
Pardiñas, U.F.J., P. Myers, L. León-Paniagua, N. Ordóñez-Garza, J.A. Cook, B. Kryštufek, R. Haslauer, R.D. Bradley, G.I. Shenbrot & J.L. Patton. 2017. Family Cricetidae (true hamsters, voles, lemmings and New World rats and mice). pp. 204–279. En: Wilson, D.E., T.E. Lacher, Jr. & R.A. Mittermeier (eds.) Handbook of the Mammals of the World. Volume 7. Rodents II. Lynx Edicions, Barcelona.
Pardiñas, U. F. J., Simoes Libardi, G. & Galliari, C. A. 2018. Localidades típicas de cricétidos en tierras incógnitas: Jesematathla y Waikthlatingmayalwa en el Chaco paraguayo. Mastozoología Neotropical 25: 491-498. [ Links ]
Paresque, R. 2010. Diversificação das espécies do gênero Oligoryzomys Bangs, 1900 (Rodentia, Cricetidae) na região neotropical. Tesis de doctorado en biología/genética, Universidade de São Paulo, São Paulo.
Parlos, J.A., R.M. Timm, V.J. Swier, H. Zeballos & R.J. Baker. 2014. Evaluation of paraphyletic assemblages within Lonchophyllinae, with description of a new tribe and genus. Occasional Papers, Museum of Texas Tech University 320: 1–23.
Patterson, B.D., M.F. Smith & P. Teta. 2015. Genus Abrothrix Waterhouse, 1837. pp. 109–127. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Patton, J.L. 2015a. Suborden Myomorpha Brants, 1855. pp. 58–60. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Patton, J.L. 2015b. Genus Lenoxus Thomas, 1909. pp. 231–232. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía, (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Patton, J.L. & L.H. Emmons. 2015. Family Dasyproctidae Bonaparte, 1838. pp. 733–762. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Patton, J.L. & R.N. Leite. 2015. Genus Proechimys J. A. Allen, 1899. pp. 950–989. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía, (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.). 2015. Mammals of South America, volume 2 Rodents. The University of Chicago Press, Chicago.
Pavan, S.E., S.A. Jansa & R.S. Voss. 2014. Molecular phylogeny of short-tailed opossums (Didelphidae: Monodelphis): Taxonomic implications and tests of evolutionary hypotheses. Molecular Phylogenetics and Evolution 79: 199–214.
Pavan, S.E. & R.S. Voss. 2016. A revised subgeneric classification of Short-tailed opossums (Didelphidae: Monodelphis). American Museum Novitates 3868: 1–44.
Pečnerová, P. & N. Martínková. 2012. Evolutionary history of tree squirrels (Rodentia, Sciurini) based on multilocus phylogeny reconstruction. Zoologica Scripta 41: 211–219.
Peñaranda, D.A. & J.A. Simonetti. 2015. Predicting and setting conservation priorities for Bolivian mammals based on biological correlates of the risk of decline. Conservation Biology 29: 834-843.
Peñaranda, D. & J. Simonetti. 2016. The informative nature of unexpected results: reply to Tellería and Yapu‐Alcázar. Conservation Biology 30: 907–909.
Pessôa, L.M., W.C. Tavares, A.C.A. Neves & A.L.G. da Silva. 2015. Genus Thrichomys E.-L. Trouesssart, 1880. pp. 989–999. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Percequillo, A.R., P.R. Goncalves & J.A. de Oliveira. 2004. The rediscovery of Rhagomys rufescens (Thomas, 1886), with a morphological redescription and comments on its systematic relationships based on morphological and molecular (cytochrome b) characters. Mammalian Biology 69: 238–257.
Percequillo, A.R. 2015a. Genus Cerradomys Weksler, Percequilloand Voss, 2006. pp. 300–308. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Percequillo, A.R. 2015b. Genus Euryoryzomys Weksler, Percequillo and Voss, 2006. pp. 312–321. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Percequillo, A.R. 2015c. Genus Hylaeamys Weksler, Percequillo and Voss, 2006. pp. 335–346. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Percequillo, A.R. 2015d. Genus Nephelomys Weksler, Percequillo and Voss, 2006. pp. 377–390. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Poljak. S., A.M. Ferreiro, M.B. Chiappero, J. Sánchez, M. Gabrielli & M.S. Lizarralde. 2018. Phylogeography of screaming hairy armadillo Chaetophractus vellerosus: Successive disjunctions and extinctions due to cyclical climatic changes in southern South America. PLoS ONE 13: e0190944. https://doi.org/10.1371/journal.pone.0190944
Poma Urey, J.L., L.H. Acosta & M.R. Ingala. 2019. Dos especies de Eptesicus Rafinesque, 1820 (Chiroptera, Vespertilionidae) registradas por primera vez en Bolivia. Ecología en Bolivia 54: 155-161.
Porcel, Z.R., H. López-Strauss, J. Martínez & R.B. Wallace. 2010. Callitrichidae. pp. 235–262. En: Wallace, R.B., H. Gómez, Z.R. Porcel & D.I. Rumiz (eds.) Distribución, Ecología y Conservación de los Mamíferos Medianos y Grandes de Bolivia. Centro de Ecología Difusión Simón I. Patiño, Santa Cruz.
Presslee, P., G. J. Slater, F. Pujos, A. M. Forasiepi, R. Fischer, K. Molloy, M. Mackie, J. V. Olsen, A. Kramarz, M. Taglioretti, F. Scaglia, M. Lezcano, J. L. Lanata, J. Southon, R. Feranec, J. Bloch, A. Hajduk, F. M. Martin, R. Salas Gismondi, M. Reguero, C de Muizon, A Greenwood, B. T. Chait, K. Penkman, M. Collins & R. D. E. MacPhee. 2019. Palaeoproteomics resolves sloth relationships. Nature Ecolog y & Evolution 3: 1121–1130.
Rico, A., Aliaga-Rossel E. & A. Palabral. 2015. Especies exóticas e invasoras del valle de La Paz. pp. 757–786. En Moya, M.I., R.I. Meneses & J. Sarmiento (eds.) Historia Natural de un Valle en los Andes: La Paz. Museo de Historia Natural, La Paz.
Rimoli, J., G. Ludwig, J. Lynch Alfaro, F. Melo, J. Mollinedo & M. dos Santos M. 2018. Sapajus cay. The IUCN Red List of Threatened Species. http://dx.doi.org/10.2305/IUCN.UK.2015-1.RLTS.T42696A70613732.en.
Ríos-Uzeda, B., R.B. Wallace & J. Vargas. 2004. La jayupa de la altura (Cuniculus taczanowskii, Rodentia, Cuniculidae), un nuevo registro de mamíferos para la fauna de Bolivia. Mastozoología Neotropical 11: 109–114.
Rivera, P.C., R.E. González-Ittig, A.R. Barcia, L.I. Trimarchi, S. Levis, G.E. Calderón & C.N. Gardenal. 2018. Molecular phylogenetics and environmental niche modeling reveal a cryptic species in the Oligoryzomys flavescens complex (Rodentia, Cricetidae). Journal of Mammalogy 99: 363–376.
Rossi, R.V., R.S. Voss & D.P. Lunde. 2010. A revision of the didelphid marsupial genus Marmosa. Part 1. The species in Tate’s ‘mexicana’ and ‘mitis’ sections and other closely related forms. Bulletin of the American Museum of Natural History 334:1–83.
Rossi, R.V. & J.M.B. Duarte. 2016. Mazama nemorivaga. The IUCN Red List of Threatened Species 2016: e.T136708A22158407. http://dx.doi.org/10.2305/IUCN.UK.2016-1.RLTS.T136708A22158407.en.
Ruiz-García, M. 2009. Changes in the demographic trends of pink river dolphins (Inia) at the microgeographical level in Peruvian and Bolivian rivers and within the Upper Amazon: Microsatellites and mtDNA analyses and insights into Inia’s origin. Nova Science Publishers, Inc., Nueva York.
Ruiz-García, M. & M. Pinedo-Castro. 2013. Population genetics and phylogeographic analyses of the yaguarundi (Puma yagouaroundi) by means of three mitochondrial markers: The first molecular population study of this species. pp. 245–288. En: Ruíz-García, M. & J.M. Shostell (eds.) Molecular Population Genetics, Evolutionary Biology and Biological Conservation on Neotropical Carnivores. Nova Science Publishers, Inc., Nueva York.
Ruiz-García, M., D. Cossíos, M. Lucherini, J. Yánez, M. Pinedo-Castro &B. Angers. 2013. Population genetics and spatial structure in two Andean cats (the Pampas Cat, Leopardus pajeros and the Andean Mountain Cat, L. jacobita) by means of nuclear and mitochondrial markers and some notes on skull biometrics. Pp 187-244. En: Ruíz-García, M. & J.M. Shostell (eds.) Molecular Population Genetics, Evolutionary Biology and Biological Conservation on Neotropical Carnivores. Nova Science Publishers, Inc., Nueva York.
Ruiz-García, M., M. Pinedo-Castro & J.M. Shostell. 2014. How many genera and species of woolly monkeys (Atelidae, Platyrrhine, Primates) are there? The first molecular analysis of Lagothrix flavicauda, an endemic Peruvian primate species. Molecular Phylogenetics and Evolution 79: 179–198.
Ruiz-García, M., M. Pinedo-Castro & J.M. Sholtell. 2018. Small spotted bodies with multiple specific mitochondrial DNAs: Existence of diverse and differentiated tigrina lineages or species (Leopardus spp: Felidae, Mammalia) throughout Latin America. Mitochondrial DNA Part A 29: 993–1014.
Ruiz-García, M., A. Albino, M. Pinedo-Castro, H. Zeballos, A. Bello, N. Leguizamon & J.M. Shostell. 2019. First molecular phylogenetic analysis of the Lagothrix taxon living in southern Peru and northern Bolivia: Lagothrix lagothricha tschudii (Atelidae, Primates), a new subspecies. Folia Primatologica. https://doi.org/10.1159/000497251
Rusconi, C. 1930. Las especies fósiles argentinas de pecaríes (Tayassuidae) y sus relaciones con las del Brasil y Norte America. Anales del Museo Nacional de Historia Natural "Bernardino Rivadavia" 36: 121–241.
Rylands, A.B. & R.A. Mittermeier. 2013. Family Callitrichidae (marmosets and tamarins). pp. 262–346. En: Mittermeier, R.A., A.B. Rylands & D.E. Wilson (eds.) Handbook of the mammals of the world. Primates, Vol. 3. Lynx Edicions, Barcelona.
Rylands, A.B. & M.C.M. Kierulff. 2015. Sapajus libidinosus. The IUCN Red List of Threatened Species 2015: e.T136346A70613080. http://dx.doi.org/10.2305/IUCN.UK.2015-1.RLTS.T136346A70613080.en.
Rylands, A.B., J-P., Boubli, R.A. Mittermeier, R.B. Wallace & N. Ceballos-Mago. 2015a. Sapajus apella. The IUCN Red List of Threatened Species 2015: e.T39949A70610943.
Rylands, A.B., J-P., Boubli, R.A. Mittermeier, P. Stevenson, E. Palacios & S. de la Torre S. 2015b. Sapajus macrocephalus. The IUCN Red List of Threatened Species 2015: e.T42696A70613732.
Rylands, A.B., E.W. Heymann, J. Lynch Alfaro, J.C. Buckner, C. Roos, C. Matauschek, J.P. Boubli, R. Sampaio & R.A. Mittermeier. 2016. Taxonomic review of the New World tamarins (Primates: Callitrichidae). Zoological Journal of the Linnean Society 1–26.
Salazar–Bravo, J., T.L. Yates, & M. Zalles. 2002. Los Mamíferos de Bolivia. Pp. 65-113, In: G. Ceballos and J. Simmoneti (eds.) Diversidad y Conservación de los Mamiferos de Latino America. CONABIO-UNAM. Mexico, D.F.
Salazar-Bravo, J., T. Tarifa, L.F. Aguirre, E. Yensen & T.L. Yates. 2003. Revised Checklist of Bolivian mammals. Occasional Papers, Museum of Texas Tech University 220: 1–27.
Salazar-Bravo, J. & T.L. Yates. 2007. A new species of Thomasomys (Cricetidae: Sigmodontinae) from Central Bolivia. pp. 747–774. En: Kelt, D.A., E. Lessa, J. Salazar-Bravo & J.L. Patton (eds.) The Quintessential Naturalist: Honoring the Life and Legacy of Oliver P. Pearson. University of California Publication in Zoology 134.
Salazar-Bravo, J., J. Miralles-Salazar, A. Rico-Cernohorska & J. Vargas. 2011. First record of Punomys (Rodentia: Sigmodontinae) in Bolivia. Mastozoología Neotropical 18: 143–146.
Salazar-Bravo, J. 2015. Genus Calomys Waterhouse, 1837. pp. 481–507. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Salazar-Bravo, J. & J.P. Jayat. 2015. Genus Andinomys Thomas, 1902. pp. 75–77. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Salazar-Bravo, J., U.F.J. Pardiñas, H. Zeballos & P. Teta. 2016. Description of a new tribe of sigmodontine rodents (Cricetidae: Sigmodontinae) with an updated summary of valid tribes and their generic contents. Occasional Papers, Museum of Texas Tech University 338: 1–23.
Sánchez-Vendizú, P., J.A. Cook, J. Wood & J. Salazar-Bravo. 2018. First record of Proechimys pattoni da Silva, 1998 (Rodentia, Echimyidae) in northwestern Bolivia. Check List 14: 1115–1121.
Sánchez-Vendizú, P., V. Pacheco, & D. Vivas-Ruiz. 2018. An introduction to the systematics of small-bodied Neacomys (Rodentia, Cricetidae) from Peru with descriptions of two new species. American Museum Novitates 3913: 1-39.
Segura, V., F. Prevosti y G. Cassini. 2013. Cranial ontogeny in the Puma lineage, Puma concolor, Herpailurus yagouaroundi, and Acinonyx jubatus (Carnivora: Felidae): A three-dimensional geometric morphometric approach. Zoological Journal of the Linnean Sociaty 169: 235–250.
Semedo, T. B. F., M. V. Brandão, A. P. Carmignotto, M. Da Silva Nunes, I. Pires Farias, M. N. Ferreira Da Silva & R. V. Rossi. 2015. Taxonomic status and phylogenetic relationships of Marmosa agilis peruana Tate, 1931 (Didelphimorphia: Didelphidae), with comments on the morphological variation of Gracilinanus from centralwestern Brazil. Zoological Journal of the Linnean Society 173: 190-216.
Serrano-Villavicencio, J., C. Hurtado, R. Vendramel, & F. Oliveira do Nascimento. 2019. Reconsidering the taxonomy of the Pithecia irrorata species group (Primates: Pitheciidae). Journal of Mammalogy 100: 130–141.
Siles, L. 2007. Noteworthy records of Eptesicus chiriquinus and Eptesicus andinus (Vespertilionidae) from Bolivia. Bat Research News 48(2): 31-33. [ Links ]
Siles, L. & R.B. Wallace. En prep. New country records of bats (Chiroptera) for Bolivia in the Madidi National Park.
Siles, L., D.A. Brooks, H. Aranibar, T. Tarifa, J. Vargas, J.M. Rojas & R.J. Baker. 2013. A new species of Micronycteris (Chiroptera: Phyllostomidae) from Bolivia. Journal of Mammalogy 94: 881–896.
Simmons, N.B. 2005. Order Chiroptera. pp. 312–529. En: Wilson, D.E. & D.M. Reeder (eds.) Mammal Species of the World. 2nd edition. Smithsonian Institution Press, Washington, DC.
Simmons, N.B. & A.L. Cirranello. 2019. Bat Species of the World: A taxonomic and geographic database. www.batnames.org. Descargado el 22 de julio de 2019.
Solari, S. 2007. New species of Monodelphis (Didelphimorphia: Didelphidae) from Peru, with notes on M. adusta (Thomas, 1897). Journal of Mammalogy 88: 319–329.
Solari, S. & V. Martínez-Arias. 2014. Cambios recientes en la sistemática y taxonomía de murciélagos Neotropicales (Mammalia: Chiroptera). Therya 5: 167–196.
Smith, M.F. & J.L. Patton. 1999. Phylogenetic relationships and the radiation of Sigmodontine rodents in South America: Evidence from cytochrome b. Journal of Mammalian Evolution 6: 89–128.
Spotorno, A.E. & J.L. Patton. 2015. Superfamily Chinchilloidea Bennett, 1833. pp. 762–783. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Suárez-Villota, E.Y., A.P. Carmignotto, M.V. Brandão, A.R. Percequillo & M.J. de J. Silva. 2017. Systematics of the genus Oecomys (Sigmodontinae: Oryzomyini): molecular phylogenetic, cytogenetic and morphological approaches reveal cryptic species. Zoological Journal of the Linnean Society 184: 1–29.
Steppan, S.J. & O. Ramírez. 2015. Genus Phyllotis Waterhouse, 1837. pp. 535–555. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Steppan, S.J., O. Ramirez, J. Banbury, D. Huchon, V. Pacheco, L. Walker & A.O. Spotorno. 2007. A molecular reappraisal of the systematics of the leaf-eared mice Phyllotis and their relatives. pp. 799–826. En: Kelt, D.A., E. Lessa, J. Salazar-Bravo & J.L. Patton (eds.) The quintessential naturalist: honoring the life and legacy of Oliver P. Pearson. University of California Publication in Zoology 134.
Tarifa, T. 2008. La mastozoología en Bolivia: Una historia de pioneros bolivianos y padres extranjeros. Mastozoología Neotropical 15(2): 223-239. [ Links ]
Tarifa, T. 2009. Chinchilla chinchilla. Pp. 457-459. En: Libro Rojo de la Fauna Silvestre de los Vertebrados de Bolivia. Ministerio de Medio Ambiente y Agua. La Paz.
Tarifa, T. & L. F. Aguirre. 2009. Mamíferos. Pp. 419-571. En: Libro Rojo de la Fauna Silvestre de los Vertebrados de Bolivia. Ministerio de Medio Ambiente y Agua. La Paz.
Tejedor, A. 2006. The type locality of Natalus stramineus (Chiroptera: Natalidae): implications for the taxonomy and biogeography of the genus Natalus. Acta Chiropterologica 8: 361–380.
Tellería, L. & M. Yapu-Alcázar. 2016. Conservation priorities for Bolivian mammals: response to Peñaranda and Simonetti. Conservation Biology 30: 905-906.
Teta, P. 2018. Geographic variation in quantitative skull traits in the genus Myoprocta Thomas, 1903 (Rodentia, Dasyproctidae) and its taxonomic implication. Mammalia 83: 212-218. [ Links ]
Teta, P., J.P. Jayat, P.E. Ortiz & G. D’Elía. 2013. The taxonomic status of Oligoryzomys brendae Massoia, 1998 (Rodentia, Cricetidae), with comments on the availability of this name. Zootaxa 3641: 433–447.
Teta, P. & S.O. Lucero. 2016. ¿Cuántas especies del género Dasyprocta (Rodentia, Dasyproctidae) hay en la Argentina? Mastozoología Neotropical 23: 193–199.
Teta, P., C. Cañón, B.D. Patterson & U.F.J. Pardiñas. 2016. Phylogeny of the tribe Abrotrichini (Cricetidae, Sigmodontinae): integrating morphological and molecular evidence into a new classification. Cladistics 33: 153–182.
Terán, M. 2010. Nuevos registros de murciélagos (Chiroptera: Phyllostomidae: Phyllostominae) para el departamento de La Paz, Bolivia. Revista Boliviana de Ecología y Conservación Ambiental. 27: 85–91.
Thorington Jr., R.W., J.L. Koprowski, M.A. Steele & J.F. Whatton. 2012. Squirrels of the World. The Johns Hopkins University Press, Baltimore.
Tribe, C.J. 2015. Genus Rhipidomys Tschudi, 1845. pp. 583–617. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Upham, N.S. & B.D. Patterson. 2012. Diversification and biogeography of the Neotropical caviomorph lineage Octodontoidea (Rodentia: Hystricognathi). Molecular Phylogenetics and Evolution 63: 417–429.
Upham, N.S. & B.D. Patterson. 2015. Phylogeny and evolution of caviomorph rodents: a complete timetree for living genera. pp. 63–120. En: Vassallo, A.I. & D. Antenucci (eds.) Biology of Caviomorph Rodents: Diversity and Evolution. Sociedad Argentina para el Estudio de los Mamíferos (SAREM), Buenos Aires.
Van Roosmalen, M.G.M., T. Van Roosmalen & R. Mittermeier. 2002. A taxonomic review of titi monkeys, genus Callicebus Thomas, 1903, with the description of two new species, Callicebus bernhardi and Callicebus stephennaski from Amazonia. Neotropical Primates 10 (suppl.): 1-52.
Van Valen, L. 1966. Deltatheridia, a new order of mammals. Bulletin of the American Museum of Natural History 132: 1–126.
Van Valen, L. 1968. Monophyly or diphyly in the origin of whales. Evolution 22: 37-41. [ Links ]
Velazco, P.M. & B.D. Patterson. 2013. Diversification of the yellow-shouldered bats, genus Sturnira (Chiroptera, Phyllostomidae), in the New World tropics. Molecular Phylogenetics and Evolution 68: 683–698.
Velazco, P.M., J.A., Soto-Centeno, D.W. Fleck, R.S. Voss & N.B. Simmons. 2017. A new species of nectar-feeding bat of the genus Hsunycteris (Phyllostomidae: Lonchophyllinae) from northeastern Peru. American Museum Novitates 3881: 1–26.
Velazco, P.M., L. Guevara & J. Molinari. 2018. Systematics of the broad-nosed bats, Platyrrhinus umbratus (Lyon, 1902) and P. nigellus (Gardner and Carter, 1972) (Chiroptera: Phyllostomidae), based on genetic, morphometric, and ecological niche analyses. Neotropical Biodiversity 4: 118–132.
Velazco, P.M. & B.D. Patterson. 2019. Small mammals of the Mayo River Basin in northern Peru, with the description of a new species of Sturnira (Chiroptera, Phyllostomidae). Bulletin of the American Museum of Natural History 429:1–67.
Vermeer, J. & J.C. Tello-Alvarado. 2015. The distribution and taxonomy of titi monkeys (Callicebus) in Central and Southern Peru, with the description of a new species. Primate Conservation 29: 9–29. https://doi.org/10.1896/052.029.0102
Vieira, C. L. G. C. 2006. Sistemática do jupati Metachirus Burmeister, 1854 (Mammalia: Didelphimorphia). Tesis de maestria. Centro de Ciéncias Humanas e Naturais, Universidade Federal Do Espírito Santo, Espírito Santo. 103 p.
Villalba, M.L., E. Cuéllar & T. Tarifa. 2010. Camelidae. pp 597–628. En: Wallace, R.B., H. Gómez, Z.R. Porcel & D.I. Rumiz (eds.) Distribución, Ecología y Conservación de los Mamíferos Medianos y Grandes de Bolivia. Centro de Ecología Difusión Simón I. Patiño, Santa Cruz.
Villalobos, F. & F. Cervantes-Reza. 2007. Phylogenetic relationship of Mesoamerican species of the genus Sciurus (Rodentia: Sciuridae). Zootaxa 1525: 31–40.
Villalpando, G., J. Vargas & J. Salazar-Bravo. 2006. First record of Rhagomys (Mammalia: Sigmodontinae) in Bolivia. Mastozoologia Neotropical 13: 143–149.
Vogel Ely, C., S. A. de L. Bordignon, R. Trevisan & I. I. Boldrini. 2017. Implications of poor taxonomy in conservation. Journal of Nature Conservation 36: 10-13.
Voss, R.S., T. Tarifa & E. Yensen. 2004. An introduction to Marmosops (Marsupialia: Didelphidae), with the description of a new species from Bolivia and notes on the taxonomy and distribution of other Bolivian forms. American Museum Novitates 3466: 1–40.
Voss, R.S., D.P. Lunde & S.A. Jansa. 2005. On the contents of Gracilinanus, with the description of a previously unrecognized clade of small didelphid marsupials. American Museum Novitates 3482: 1–34.
Voss, R.S. & S.A. Jansa. 2009. Phylogenetic relationships and classification of Didelphid marsupials, an extant radiation of New World Metatherian Mammals. Bulletin of the American Museum of Natural History 322: 1–177.
Voss, R.S. 2011. Revisionary notes on Neotropical porcupines (Rodentia: Erethizontidae) 3. An annotated checklist of the species of Coendou Lacépède, 1799. American Museum Novitates 3720: 1–36.
Voss, R.S., R.H. Pine & S. Solari. 2012. A new species of the didelphid marsupial genus Monodelphis from Eastern Bolivia. American Museum Novitates 3740: 1–14.
Voss, R.S., E.E. Gutiérrez, S. Solari, R.V. Rossi & S.A. Jansa. 2014. Phylogenetic relationships of mouse opossums (Didelphidae, Marmosa) with a revised subgeneric classification and notes on sympatric diversity. American Museum Novitates 3817: 1–27.
Voss, R.S., K.M. Helgen & S.A. Jansa. 2014. Extraordinary claims require extraordinary evidence: a comment on Cozzuol et al. (2013). Journal of Mammalogy 95:893–898.
Voss, R.S. 2015. Family Erethizontidae Bonaparte, 1845. pp. 786–805. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Voss, R.S., J.F. Díaz-Nieto & S.A. Jansa. 2018. A revision of Philander (Marsupialia: Didelphidae), Part 1: P. quica, P. canus, and a new species from Amazonia. American Museum Novitates 3891: 1–70.
Voss, R. S., D. W. Fleck & S. A. Jansa. 2019. Mammalian diversity and Matses ethnomammalogy in Amazonian Peru Part 3: Marsupials (Didelphimorphia). Bulletin of the American Museum of Natural History 432: 1-87.
Wallace, R.B., H. Gomez, A. Felton & A. Felton. 2006. On a new species of titi monkey, genus Callicebus Thomas, from western Bolivia (Primates, Cebidae) with preliminary notes on distribution and abundance. Primate Conservation 20: 29–39.
Wallace, R.B. & D. I. Rumiz. 2010. Atelidae. pp. 331-366. En: Wallace, R.B., H. Gómez, Z.R. Porcel & D. I. Rumiz (eds.) Distribución, Ecología y Conservación de los Mamíferos Medianos y Grandes de Bolivia. Centro de Ecología Difusión Simón I. Patiño, Santa Cruz.
Wallace, R.B., H. Gómez, Z.R. Porcel & D.I. Rumiz (Eds.). 2010. Distribución, Ecología y Conservación de los Mamíferos Medianos y Grandes de Bolivia. Centro de Ecología Difusión Simón I. Patiño, Santa Cruz. 906 p.
Wallace, R.B., H. Lopez-Strauss, N. Mercado & Z.R. Porcel. 2013a. Base de Datos sobre la Distribución de los Mamíferos Medianos y Grandes de Bolivia. DVD Interactivo. Wildlife Conservation Society, La Paz, Bolivia.
Wallace, R.B., J. Martinez, H. Lopez-Strauss, J. Barreta, A. Reinaga & L. Lopez. 2013b. Conservation challenges facing two threatened endemic titi monkeys (Callicebus modestus & C. olallae) in a naturally fragmented Bolivian forest. pp. 493-501. En: Marsh, L.K. (ed.) Primate in Fragments: Complexity and Resilience. Developments in Primatology: Progress and Prospects. Springer Science+Business Media, Nueva York.
Weksler, M. 2006. Phylogenetic relatioships of oryzomyine rodents (Muridae: Sigmodontinae): separate and combined analyses of morphological and molecular data. Bulletin of the American Museum of Natural History 296: 1–149.
Weksler, M., A.R. Percequillo & R.S. Voss. 2006. Ten new genera of Oryzomyine rodents (Cricetidae: Sigmodontinae). American Museum Novitates 3537: 1–29.
Weksler, M. & A.R. Percequillo. 2011. Key to the genera of the tribe Oryzomyini (Rodentia: Cricetidae: Sigmodontinae). Mastozoologia Neotropical 18: 281–292.
Weksler, M. & C.R. Bonvicino. 2015. Genus Neacomys Thomas, 1900. pp. 361–369. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Weksler, M. & C.R. Bonvicino. 2015. Genus Oligoryzomys Bangs, 1900. pp. 417–437. En: Patton, J.L., U.F.J. Pardiñas & G. D’Elía (eds.) Mammals of South America, Volume 2 Rodents. The University of Chicago Press, Chicago.
Wheeler, J.C. 2003. Evolution and origin of the domestic camelids. International Lama Registry (ILR) Report8. [ Links ]
Wheeler, J.C. 2005. El debate sobre el origen de la alpaca. Revista de la Academia Peruana de Ciencias Veterinarias 5 & 6: 40-43. [ Links ]
Woods, C.A. 1993. Suborder Hystricognathi. pp. 771–806. En: Wilson, D.E. & D.M. Reeder (eds.) Mammal Species of the World. 2nd edition. Smithsonian Institution Press, Washington, DC.
Woodman, N. & R. Timm. 2006. Characters and phylogenetic relationships of nectar-feeding bats, with descriptions of new Lonchophylla from western South America (Mammalia: Chiroptera: Phyllostomidae: Lonchophyllini). Proceedings of the Biological Society of Washington 119: 437-476.
Ziegler A.C, F.G. Howarth & N.B. Simmons. 2016. A second endemic land mammal for the Hawaiian Islands: a new genus and species of fossil bat (Chiroptera: Vespertilionidae). American Museum Novitates 3854: 1–52.
Zhou, X., S. Xu, Y. Yang, K. Zhou & G. Yang. 2011. Phylogenomic analyses and improved resolution of Cetartiodactyla. Molecular Phylogenetics and Evolution 61: 255–264.
Zhou, Y., S.-R. Wang & J.-Z. Ma. 2017. Comprehensive species set revealing the phylogeny and biogeography of Feliformia (Mammalia, Carnivora) based on mitochondrial DNA. PLoS ONE 12: e0174902.