Services on Demand
Journal
Article
Indicators
Related links
Share
Ecología en Bolivia
Print version ISSN 1605-2528On-line version ISSN 2075-5023
Ecología en Bolivia vol.47 no.2 La Paz Sept. 2012
Artículo
Ensamble de hormigas en relación a cobertura vegetal en una zona periurbana de La Paz (Bolivia)
Ant assemblage in relation to vegetal cover in a periurban area of La Paz (Bolivia)
A. Bruno Miranda1,3, Kazuya Naoki2 & Miguel Limachi3
1Carrera de Biología, Universidad Mayor de San Andrés, C/ 27 Cota Cota, La Paz, Bolivia
Email: abrunomirandac@gmail.com Autor de correspondencia
2Centro de Análisis Espacial, Instituto de Ecología, Universidad Mayor de San Andrés, Casilla 10077 - Correo Central, La Paz, Bolivia
3Colección Boliviana de Fauna - Museo Nacional de Historia Natural, C/ 26 Cota Cota, La Paz, Bolivia
Resumen
Las hormigas son frecuentemente utilizadas como bioindicadores de la integridad ecosistémica debido a su sensibilidad a cambios antrópicos del medio ambiente, especialmente a cobertura vegetal, uso de tierra y contaminación. El objetivo de este estudio fue relacionar el ensamble de hormigas a características de diferentes tipos de vegetación en una zona periurbana de la ciudad de La Paz, Bolivia. Los ensambles de hormigas fueron estudiados a través de trampas de caída ubicados en 30 sitios. La vegetación de cada sitio fue cuantificada por medio de línea de intercepción según sus características fisonómicas y estructurales. Durante el estudio se registraron 14 morfoespecies de hormigas pertenecientes a cuatro subfamilias: Dolichoderinae, Formicinae, Myrmicinae y Ponerinae. Según ordenación por NMDS, el ensamble de hormigas se conformó en tres grupos asociados con el tipo de vegetación: Arboleda, pajonal y prado. Esta asociación fue parcialmente explicada por la selección de algunas morfoespecies de hormigas para las características de vegetación. Los resultados de este estudio apoyan la influencia de la vegetación sobre el ensamble de hormigas y sugieren la potencialidad de uso de hormigas como bioindicadores en zonas urbanas.
Palabras clave: Área periurbana, Bioindicación, Ensamble, Formación vegetal, Hormigas.
Abstract
Ants are frequently used as bioindicators of ecosystem integrity due to its sensibility to anthropic changes of environment, especially to canopy cover, land use, and contamination. The objective of this study was to relate the ant assemblage to the characteristics of different vegetation types in a periurban area of La Paz city. Ant assemblages were studied by means of pitfall traps in 30 sites. Vegetation at each site was quantified by interception lines according to their physiognomic and structural characteristics. During the study we registered 14 morphospecies belonging to four subfamilies: Dolichoderinae, Formicinae, Myrmicinae y Ponerinae. By NMDS ordination, ant assemblage conformed in three groups associated with vegetation type: Grove, grassland and meadow. This association was partially explained by the ant morphospecies' selection of vegetation characteristics. This study's results confirm the influence of vegetation on ant assemblage and suggest the potential use of ants as bioindicators in urban areas.
Key words: Ants, Assemblage, Bioindication, Periurban area, Vegetal cover.
Introducción
Las hormigas son consideradas como indicadores eficaces de la integridad ecosistémica debido a sus características biológicas y buen conocimiento taxonómico del grupo (Fernández 1996, Folgarait 1998, Andersen & Majer 2004, Majer et al. 2007). En varios países, las hormigas han sido utilizadas como indicadores en programas de monitoreo y evaluación de cambios en el ecosistema (Ribas et al. 2012), impacto ambiental (Andersen et al. 2004), manejo en reservas naturales y áreas protegidas (Toro & Ortega 2006, Mitrovich et al. 2010), sistemas agroforestales y uso de tierra (Armbrecht et al. 2005, Rivera & Armbrecht 2005) y pastoreo y quema (Andersen 1991a, Ratchford et al. 2005).
La urbanización, como otro tipo de impacto a sistemas naturales, provoca una constante transformación de los patrones y procesos ecológicos (Vitousek et al. 1997, Faeth et al. 2005), creándose un mosaico de ambientes con diferentes grados de perturbación y de estrés ambiental para los organismos. La urbanización puede además ocasionar la pérdida de hábitats afectando la composición y riqueza de especies (McIntyre 2000, Philpott et al. 2010). Por otro lado, algunas especies pueden tomar ventaja de los ambientes perturbados e incrementar su abundancia (McKinney 2002, Yamaguchi 2005), causando una reducción de diversidad por interacciones competitivas (Andersen 1992). De esta manera, la reducción de diversidad en zonas urbanas o periurbanas se encontrará relacionada en parte a la disminución de la heterogeneidad estructural de la matriz (p.e. tipo de vegetación) (McIntyre 2000), reducción de la variedad natural de recursos disponibles (McKinney 2006) y alteración de la composición natural de especies en los hábitats.
Varios estudios han centrado su atención en las diferencias en riqueza, composición o grupos funcionales de hormigas en hábitats periurbanos y urbanos (Vepsäläinen et al. 2008); así como el rol y beneficios que pueden cumplir estos organismos en la manutención o restauración de funciones ecosistémicas (Niemelä 1999, Burger et al. 2003, Sandfor et al. 2008). En Suramérica se consta el incremento y presencia de hormigas nativas y/o exóticas en zonas urbanas o periurbanas (Pacheco do Nascimento 2005, Chacón de Ulloa et al. 2006), las cuales estarían influenciadas por las características ambientales de cada región. Algunas especies podrían explotar remanentes de vegetación natural, aisladas y pequeñas distribuidas en zonas urbanas, ser capaces de tolerar un alto grado de perturbación y por tanto reflejar la heterogeneidad de hábitat y uso de suelo (McIntyre et al. 2001). Por otro lado, una alta diversidad en vegetación y/o estructura vegetativa compleja podría incrementar la riqueza en especies de estos y otros invertebrados (McIntyre et al. 2001). Todos estos aspectos brindan pautas de interpretación ecológica de comunidades, que con estrategias de manejo y monitoreo apropiadas permitirían mantener los procesos ecológicos vinculados a la biodiversidad (Niemelä 1999, Burger et al. 2003).
Estudios relacionados al monitoreo y bioindicación en zonas periurbanas o urbanas en la ciudad de La Paz (Bolivia) se han enfocado principalmente a comunidades de aves y líquenes (Garitano-Zabala & Gismondi 2003, Villegas 2005, Canseco et al. 2006, Campos 2010) y hasta la fecha no se ha realizado algún estudio relacionado con hormigas. Se ha constatado que ensambles de invertebrados podrían indicar el efecto de urbanización a escalas espaciales más pequeñas respecto a grupos de vertebrados (Clark & Samways 1997). El entendimiento de estos patrones de hormigas en relación a la variabilidad en composición vegetal o fisonomía de hábitats permitirán la aplicación de estos organismos a otros niveles espaciales como bioindicadores en áreas urbanas como la ciudad de La Paz y ayudará a formular herramientas, propuestas de manejo y establecer políticas ambientales estratégicas y de monitoreo para mantener o mejorar la diversidad de fauna asociada a la vegetación. Debido a esto, este estudio pregunta si ¿existen ensambles de hormigas asociados a diferentes tipos de hábitat en una zona periurbana de la ciudad de La Paz? y si ¿la distribución espacial de cada especie estará relacionada con a la cobertura vegetal a micro-escala existente en la zona?
Área de estudio
El estudio se realizó en los predios de la Universidad Mayor de San Andrés (Campus Universitario de Cota Cota), La Paz, Bolivia (16º32'S, 68º03'O, 3.450 m). El área constituye un mosaico de diferentes formaciones vegetales exóticas, algunos manchones con flora y vegetación nativa de valles secos y algunos elementos de pre-puna y puna, áreas de lagunas naturales y cuerpos de agua temporales (Vargas 1985, Zeballos 2000). Debido a la perturbación diferencial del sitio, la vegetación fue delimitada según sus características fisonómicas en: (a) Pajonal, áreas con predominancia de gramíneas (Stipa ichu, S. mucronata, Eragrostis sp.) y algunas plantas como Viguieraprocumbens; (b) Humedal, sectores anegados con vegetación higrófita y/o hidrofítica; (c) Matorral, predominancia de arbustos, sufrútices o algunas cactáceas dispersas (Pluchea sp., Baccharis spp., V. procumbens, Opuntia sp., otras especies de cactos); (d) Arboleda, de eucalipto (Eucalyptus globulus) o de pino (Pinus radiata); y (e) Prado, con presencia y predominancia de Pennisetum clandestinum y otras herbáceas.
Métodos
Los datos fueron obtenidos del 14-23 de abril de 2010. Se establecieron 30 áreas circulares de muestreo (15 m de radio, 709 m2 de superficie), distante al menos 50 m entre sí, de manera estratificada para cada formación vegetal previamente definida. Debido a que no se conoce área de territorio, distancia de forrajeo y otras características biológicas para las diferentes morfoespecies de hormigas (Beckers et al. 1989, Tschinkel et al. 1995), se asumió aleatoriedad en la distribución en los nidos (Levings & Traniello 1981) y que las áreas de muestreo fueron lo suficientemente alejadas y estadísticamente independientes. Para obtener la composición de hormigas se instaló una trampa de caída en el centro de cada área de muestreo durante seis días. Cada trampa consistió en un vaso de 750 ml con alcohol al 70%. Se realizó la separación e identificación de morfoespecies utilizando la clave taxonómica de Palacios & Fernández (1996). Las muestras de referencia fueron depositadas en la Colección Boliviana de Fauna.
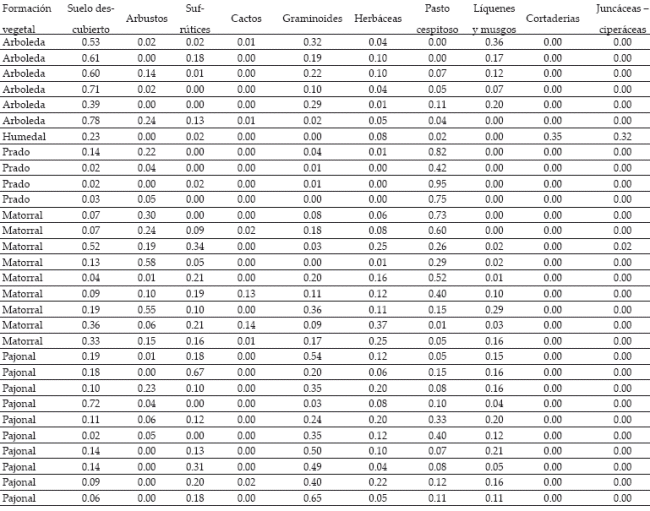
Para cuantificar cobertura vegetal como variable ambiental que explica la presencia de especies de hormigas, se establecieron dos líneas diametrales de 30 m con orientación NE-SO y NO-SE en cada área de muestreo. Se cuantificó el porcentaje absoluto de cada forma de vida vegetal a lo largo de estas líneas por medio del método de línea de intercepción (Matteucci & Colma 1982, López 1996). Para las formas vegetales se siguieronlas clasificaciones propuestas en Matteucci & Colma (1982) y Kent & Coker (1992): árboles, arbustos, sufrútices, y cactáceas mayores a 0.7 m de altura, gramíneas, herbáceas no graminoides mayores a 0.2 m de altura, pasto cespitoso menor a 0.2 m de altura, criptógamas (líquenes y musgos) y suelo descubierto.
Análisis de datos
El ensamble de hormigas para cada punto de muestreo fue analizado por ordenación de mínima distorsión espacial (NMDS) con índice de similitud de Jaccard y 100 permutaciones. La interpretación de resultados fue complementada con el análisis de correspondencia canónica (CCA) y 100 permutaciones, utilizando la característica de cobertura vegetal como matriz secundaria. Al realizar el CCA se consideraron seis juegos de datos como matriz principal con la combinación de tres datos de hormigas: (1) presencia-ausencia, (2) abundancia categorizada (transformación de número de individuos a diferentes categorías: 1 ind.= 1,2-5 ind.= 2,6-20 ind.= 3,20-50 ind. = 4 y >50 ind. = 5) (Andersen 1991b) y (3) abundancia transformada logarítmicamente, en dos listas de hormigas (a) incluyendo el total de las 14 especies de hormigas registradas y (b) 11 especies, excluyendo las especies capturadas en una sola trampa de caída. Ordenación para comunidad de hormigas fue realizada con el paquete Vegan del programa R versión 2.11.1 (R Development Core Team 2011).
Resultados
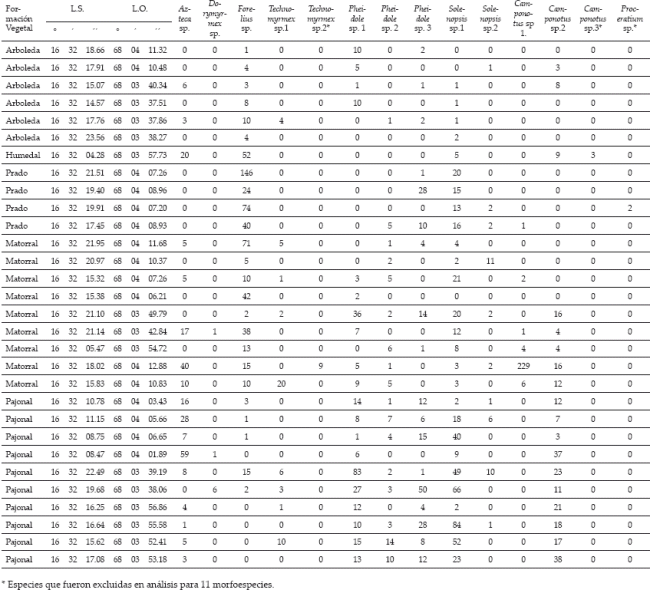
Se registraron 14 morfoespecies de hormigas (ocho géneros, cuatro subfamilias) durante este estudio (Tabla 1).
| Tabla 1. | Hormigas registradas en el campus universitario de Cota Cota (La Paz. Bolivia). Se indican los promedios de números de individuos capturados por muestra en cada formación vegetal. Los números en paréntesis indican el número de muestras por formación vegetal. |
 | |
El ensamble de hormigas muestreadas para arboleda, prado y pajonal se encontraron más similares en composición por análisis con NMDS (Fig. 1).
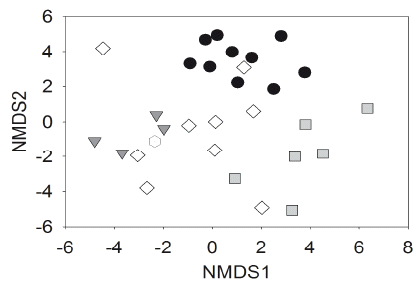 | |
| Figura 1. Ordenación de ensamblaje de hormigas de Cota Cota (La Paz, Bolivia) por ordenación de mínimo distorsión espacial (NMDS) con similitud de Jaccard. Valor de estrés = 17.30. Los símbolos indican el tipo de la formación vegetal: Arboleda | |
Según CCA, los primeros dos ejes explicaron entre el 26 y 51% de la variación total (Tabla 2); diferente transformación de los datos e inclusión/ exclusión de especies raras no afectaronfuertemente los resultados del análisis. La mayoría de los seis juegos de datos mostraron que las variables ambientales: suelo descubierto, cactos, graminoides y herbáceas, afectaron a la distribución de hormigas (Fig. 2, tabla 2). La presencia de las especies de hormigas estuvo relacionada a cierta proporción de cobertura vegetal para las zonas de muestreo: Forelius sp. con pasto cespitoso; Azteca sp. con cactáceas, herbáceas y suelo descubierto; Pheidole spp., Camponotus sp. 2., Solenopsis sp. 1, Dorymyrmex sp. y Technomyrmex sp. 1 con sufrútices, gramíneas y criptógamas (Fig. 2).
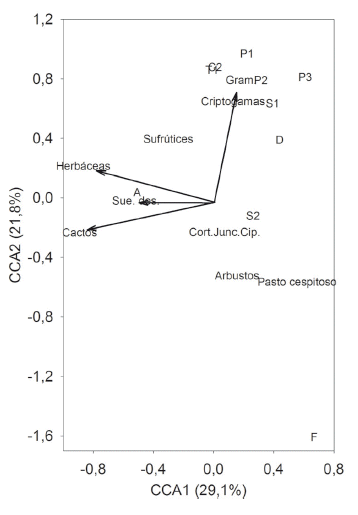 | |
| Figura 2. Asociación de especies de hormigas y características de la vegetación por análisis de correspondencia canónica (CCA) en campus universitario de Cota Cota a partir de resultados de presencia - ausencia para once especies. A = Azteca sp., D = Dorymyrmex sp., F = Forelius sp., T1 = Technomyrmex sp. 1, P1 = Pheidole sp. 1, P2 = Pheidole sp. 2, P3 = Pheidole sp. 3, S1 = Solenopsis sp. 1, S2 = Solenopsis sp. 2, Camponotus sp. 1 (x =-2.8466, y = -0.4961), C2 = Camponotus sp. 2. | |
| Tabla 2. | Distancia euclidiana de los primeros dos ejes (longitud de flecha) de variables ambientales del Análisis de Correspondencia Canónica (CCA); considerando presencia - ausencia, abundancia categorizada, y transformación a log10 para 14 y 11 especies de hormigas para cada análisis. Significanda: *** = <0.001, ** = <0.01, * = <0.05, • = <0.1. |
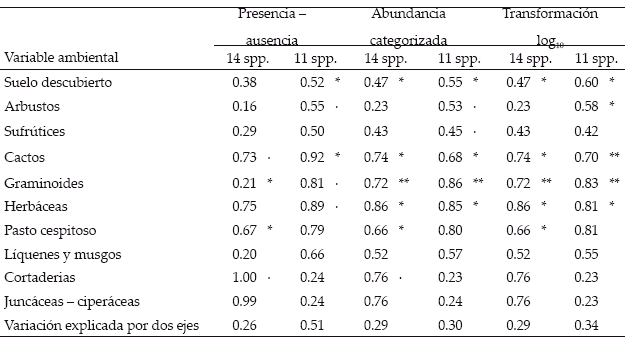 | |
Discusión
Nuestros resultados sugieren que los ensamblajes de hormigas están relacionados a las características fisionómicas de vegetación de la zona periurbana y esta relación es parcialmente explicada por la asociación de algunas especies con las variables en cobertura vegetal presentes en estos hábitats (Fig. 1).
Varios estudios han confirmado la relación entre heterogeneidad en vegetación y variación de la composición de comunidades de hormigas a diferentes escalas espaciales (Bestelmeyer & Wiens 1996, Pik et al. 2002, Hill et al. 2008). Esta asociación puede deberse a la variedad de recursos disponibles para la alimentación y sitios para el anidamiento (Armbrecht et al. 2004, Friedrich & Philpott 2009, Blütghen & Feldhaar 2010), productividad del ambiente (Kaspari et al. 1999) o condiciones micro-ambientales creadas por la cobertura vegetal (Kaspari & Wieser 2000, Maes et al. 2003). De esta manera, el entendimiento de estos patrones de hormigas podría ser mejor explicada por su respuesta a las condiciones ambientales y vínculo de sus características biológicas.
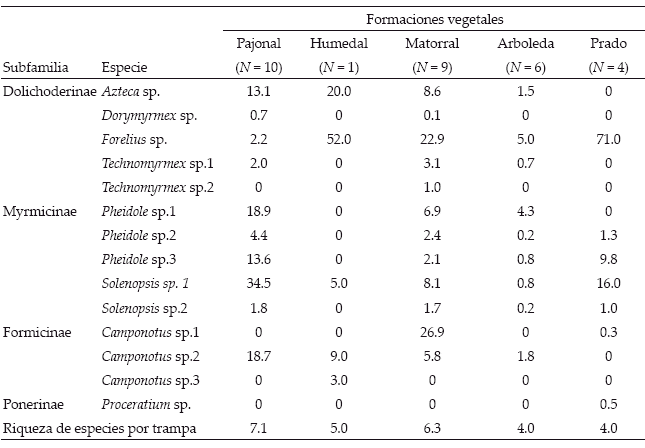
Camponotus sp. 2, Solenopsis sp. 1, Azteca sp. y Forelius sp. fueron hallados en casi todos los hábitats (Tabla 1); la presencia de otras morfoespecies, en algunos casos exclusiva, constata otros procesos que influyen sobre el ensamble. Los valores de riqueza para pajonal y matorral respecto a los de prado y arboleda demostrarían las condiciones bajo las que éstas se mantienen. Pajonal y matorral presentan parches con sucesión vegetal natural; sin embargo este último es el que se halló con mayor grado de perturbación y diferenciación de ensambles para toda el área de muestreo (Fig. 1, tabla 1). En cambio, para prado y arboleda las condiciones de modificación parecen hallarse constantes en el tiempo, pero reducirían la riqueza en morfoespecies. Para arboleda la cobertura vegetal de eucaliptos o pinos sobre la superficie podría estar causando reducción en la actividad de forrajeo por efecto que tienen sobre la dinámica biológica del suelo (Souto et al. 2001) o limitando condiciones térmicas para el desarrollo de larvas de hormigas (Maes et al. 2003). De esta forma, se argumenta que el ensamble en una matriz de vegetación estaría influenciada por la intensidad y frecuencia de perturbación que potencia o limita la distribución de hormigas en un área (Yamaguchi 2004). Adicionalmente se sugiere tomar en cuenta la importancia de la ubicación geográfica de la zona, la presencia de vegetación nativa en la zona y la conectividad con hábitats más naturales para el mantenimiento de la riqueza en ensambles de hormigas.
Koya (1983) señala algunas características morfológicas, biológicas y ecológicas de especies de hormigas presentes en la localidad de Huaraco, La Paz (Puna semiárida, Belpaire de Morales 1994), descripciones que son similares a las observadas en las morfoespecies de este estudio. El autor destaca el consumo de semillas de gramíneas, hojas de plantas y restos de insectos, la correspondencia en tamaño de ítems alimenticio encontrados en nido y tamaño corporal individuos de cada especie, la aleatoriedad de la distribución de nidos y/o de acuerdo a las características del terreno, la ubicación de éstos bajo rocas, plantas o sobre el sustrato no compactado, el comportamiento transporte de larvas a cámaras de la superficie del nido para aprovechamiento térmico durante días soleados y decremento de actividad de forrajeo desde abril a septiembre (época seca). La relación de Solenopsis sp. 1, Pheidole spp., Camponotus sp. 2, además de Technomyrmex sp. 1 y Dorymyrmex sp. hacia sectores con gramíneas pareció estar relacionado efectivamente a la disponibilidad de recursos conforme a las características oportunistas o generalistas de estos géneros (Silvestre et al. 2003, Pitts et al. 2005, Pirk et al. 2009) (Fig. 2). En cuanto a Solenopsis sp. 2, Technomyrmex sp. 2 y Proceratium sp., como organismos crípticos y pequeños, posiblemente presenten requerimientos especiales de hábitat con actividad hipogea o forrajeadoras en detritos vegetales (Andersen 2000, Silvestre et al. 2003). Para Camponotus sp. 1, Camponotus sp. 3, Solenopsis sp. 2y Technomyrmex sp. 2 puede que su presencia no esté definida satisfactoriamente por variables de vegetación; número de individuos capturados en algunos casos no fue el apropiado para su uso en análisis, por lo que se sugiere el uso de técnicas complementarias de muestreo para constatar otras variables que estén determinando su distribución. Otras especies parecen responder directamente a sectores con modificación en vegetación, como Forelius sp., que parece estar asociada al pasto cespitoso, al igual que Proceratium sp. encontrada solamente en este sector. Forelius sp. se encuentra en la mayoría de las viviendas de la ciudad de La Paz (obs. pers.), por lo que se sugiere su adaptabilidad hacia zonas altamente perturbadas. Azteca sp. parece estar relacionada a ambientes más xéricos y expuestos, con escasa cobertura vegetal; no se conoce información biológica de esta especie, pero se sugiere aprovechamiento inicial de esta especie en zonas perturbadas e influencia negativa a mayor perturbación. Se observa que la presencia de algunas especies del complejo Solenopsis saevissima en su distribución natural pueden hallarse relacionadas a la modificación de hábitat de áreas urbanas al igual que especies de Pheidole y algunas de Camponotus en América (Chacón de Ulloa 2003, Oliveira & Campos-Farinha 2005) o podrían persistir bajo determinada calidad de estrés ambiental. La presencia de algunas especies en diferentes formaciones de vegetación y relación con sus características vegetativas constata indirectamente procesos subyacentes expresados en el cambio de ensambles de hormigas por perturbación humana en el hábitat; en otros casos parece que variables de otro tipo son relevantes a las especies de hormigas. Se observa la potencialidad de uso de estas hormigas en la toma de decisiones y políticas sobre conservación o manutención de hábitats relacionadas a la vegetación (p.e. en zonas rurales, periurbanas y/o urbanas).
Este estudio está limitado en su área geográfica y tiempo de duración. Esfuerzo de trampeo para algunas formaciones vegetales no fue suficiente, por esto se sugiere que en un futuro se realicen muestreos con cebo en transectos o grillas, búsqueda manual exhaustiva, uso de trampas hipogeas y otras técnicas apropiadas para obtener un panorama más completo en diversidad y evaluar la influencia de la disposición de parches y de la vegetación adyacente. Consideramos además que la ejecución de estudios locales en biología para cada especie de hormiga: tamaño de individuos y biomasa de colonia (Tschinkel et al. 1995), gremio y territorialidad (Adams 2003, Pearce - Duvet et al. 2011), densidad y distribución de colonias (Cushman et al. 1988) e interacciones interespecíficas, como patrones de uso de espacio, dominancia, y segregación de recursos (Parr & Gibb 2010), brindarían pautas para un mayor entendimiento de comunidades de hormigas a nivel local. Además, debido a que la vegetación no es la única variable que determina la distribución de las especies, la consideración de otros factores microambientales, como la temperatura o humedad (Kaspari 1993), características físicas del suelo, entre otros, podrá elucidar los procesos que determinan el ensamble de comunidades de hormigas en zonas periurbanas y urbanas (Andersen 2000, Albretch & Gotelli 2001, Armbrecht et al. 2004).
Conclusiones
Ensamble de hormigas se halla relacionado a las características fisionómicas del hábitat. Se sugiere que la correspondencia de presencia de especies de hormigas es a variables de vegetación en el hábitat. Aún así, mayores estudios sobre la biología de las especies de hormigas en el valle de La Paz son necesarios para la respuesta de estos organismos a cambios en el ambiente, además, de investigación relacionada al de uso de hormigas como indicadoras de perturbación de hábitat en zonas urbanas para programas de monitoreo, mantenimiento y/o restauración de ecosistemas.
Agradecimientos
Agradecemos al apoyo constante de James Aparicio por el préstamo de material de laboratorio y espacio de trabajo en el Área de Herpetología de la Colección Boliviana de Fauna. Esther Valenzuela quien apoyó el acceso a sectores del Jardín Botánico La Paz y áreas del campus Universitario de Cota Cota. Ramiro P. López y Emilia García colaboraron en los métodos para cuantificar la vegetación e identificación de plantas. A Luis Pacheco y revisores anónimos de Ecología en Bolivia cuyas observaciones y sugerencias contribuyeron enormemente a la versión final del manuscrito.
Referencias
Adams, E. S. 2003. Experimental analysis of territory size in a population of the fire ant Solenopsis invicta. Behavioral Ecology 14: 48-53. [ Links ]
Albretch, M. & N. J. Gotelli. 2001. Spatial and temporal niche partitioning in grassland ants. Oecologia 126:134-141.
Andersen, A. N. 1991a. Responses of ground-foraging ant communities to three experimental fire regimes in a savanna forest of tropical Australia. Biotropica 23: 575-585. [ Links ]
Andersen, A. N. 1991b. Sampling communities of ground-foraging ants: pitfall catches compared with quadrat counts in an Australian tropical savanna. Australian Journal of Entomology 16: 273-279. [ Links ]
Andersen, A. N. 1992. Regulations of momentary diversity vy dominant species in exceptionally rich ant communities of the Australian seasonal tropics. American Naturalist 140: 401-420. [ Links ]
Andersen, A. N. 2000. Global ecology of rainforest ants. pp. 25-33. En: Agosti, D., J. Majer, L. Alonso & T. Schultz (eds.). Ants. Standard Methods for Measuring and Monitoring Biodiversity. Smithsonian Institution Press, Washington DC. [ Links ]
Andersen, A. N., A. Fisher, B. D. Hoffman, J. L. Read & R. Richards. 2004. Use of terrestrial invertebrates for biodiversity monitoring in Australian rangelands, with particular reference to ants. Austral Ecology 29: 87-92.
Andersen, A. N. & J. D. Majer. 2004. Ants show the way down under: invertebrates as bioindicators in land management. Frontiers on Ecological Environment 2: 291-298.
Armbrecht, I., I. Perfecto & J. Vandermeer. 2004. Enigmatic biodiversity correlations: ants diversity responds to diverse resources. Science 204: 284-286.
Armbrecht, I., L. Rivera & I. Perfecto. 2005. Reduced diversity and complexity in the leaf-litter ant assemblage of Colombian coffee plantations. Conservation Biology 19: 897-907.
Beckers, R., S. Goss, J. L. Deneubourg & J. M. Pasteels. 1989. Colony size, communication and ant foraging strategy. Psyche 96: 239-256.
Belpaire de Morales, C. (ed.) 1994. Huaraco, comunidad de la puna. Ártes Gráficas Latina, La Paz. 261 p.
Bestelmeyer, B. T. & J. A. Wiens. 1996. The effects of land use on the structure of ground-foraging ant communities in the Argentine Chaco. Ecological Applications 6:1225-1240.
Blütghen, N. & H. Feldhaar. 2010. Food and shelter: how resources influence ant ecology. pp. 115-136. En: Lach, L., C. L. Parr & K. L. Abbott (eds.). Ecology of Ants. Oxford University Press, Nueva York. [ Links ]
Burger, J. C., R. A. Redak, E. B. Allen, J. T. Rotenberry & M. F. Allen. 2003. Restoring arthropod communities in coastal sage scrub. Conservation Biology 17:460-467.
Campos, J. 2010. Desarrollo de un índice biológico de integridad basado en comunidades de aves nativas en zonas urbanas y periurbanas de la ciudad de La Paz - Bolivia. Tesis de licenciatura en biología, Universidad Mayor de San Andrés, La Paz. 71 p. [ Links ]
Canseco, Á., R. Anze & M. Franken. 2006. Comunidades de líquenes: indicadores de la calidad del aire en la ciudad de La Paz, Bolivia. Acta Nova 3: 286-307.
Clark, T. E. & M. J. Samways. 1997. Sampling arthropod diversity for urban ecological landscaping in a species-rich southern hemisphere botanic garden. Journal of Insect Conservation 1: 221-234.
Cushman, J. H., G. D. Martinsen & A. I. Mazeroll. 1988. Density and size dependent spacing ant nests: evidence for intraspecific competition. Oecologia 77: 522-525.
Chacón de Ulloa, P. 2003. Hormigas urbanas, pp. 351-359. En: Fernández, F. (ed.). Introducción a las Hormigas de la Región Tropical. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Bogotá. [ Links ]
Chacón de Ulloa, P., G. I. Jaramillo & M. M. Lozano. 2006. Hormigas urbanas en el departamento del valle del Cauca, Colombia. Revista Académica Colombiana en Ciencias 30: 435-441.
Faeth, S. H., P. S. Warren, E. Shochat & W. A. Marussich. 2005. Trophic dynamics in urban communities. BioScience 55: 399-407.
Fernández, F. E. 1996. Introducción al estudio de las hormigas. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Santa fé de Bogotá. 398 p. [ Links ]
Folgarait, P. J. 1998. Ant biodiversity and its relationship to ecosystem functioning: a review. Biodiversity and Conservation 7:1221-1244. [ Links ]
Friedrich, R. & S. Philpott. 2009. Nest-site limitation and nesting resources of ants (Hymenoptera: Formicidae) in urban green spaces. Environmental Entomology 38: 600-607.
Garitano-Zabala, Á. & P. Gismondi. 2003. Variación de la riqueza y diversidad de la ornitofauna en áreas verdes urbanas de las ciudades de La Paz y El Alto (Bolivia). Ecología en Bolivia 38: 65-78.
Hill, J., K. S. Summerville & R. Brown. 2008. Habitat associations of ant species (Hymenoptera: Formicidae) in a heterogeneous Mississippi landscape. Environmental Entomology 37:453-463.
Kaspari, M. 1993. Body size and microclimate use in Neotropical granivorous ants. Oecologia 96: 500-507. [ Links ]
Kaspari, M., S. O'Donell & J. R. Kercher. 1999. Energy, density, and constraints to species richness: ant assemblages along a productivity gradient. American Naturalist 155: 280-293.
Kaspari, M. & M. Wieser. 2000. Ant activity along moisture gradients in a Neotropical forest. Biotropica 32: 703-711.
Kent, M. & P. Coker. 1992. Vegetation description and analysis. John Wiley and Sons, Ontario. 363 p.
Koya, F. 1983. Algunos aspectos ecológicos de los formícidos de la puna seca semiárida del altiplano boliviano. Tesis de licenciatura en biología, Universidad Mayor de San Andrés, La Paz. 116 p. [ Links ]
Levings, S. C. & J. F. A. Traniello. 1981. Territoriality, nest dispersion and community structure in ants. Psyche 88: 265-321.
López, R. 1996. Patrones de diversidad vegetal en el valle de La Paz.. Tesis de licenciatura en biología, Universidad Mayor de San Andrés, La Paz. 112 p. [ Links ]
Maes, D., H. Van Dyck, W. Vanreusel & J. Cortens. 2003. Ant communities (Hymenoptera: Formicidae) of Flemish (north Belgium) wet heathlands, a declining habitat in Europe. European Journal of Entomology 100: 545-555.
Majer, J., G. Orabi & L. Bisevac. 2007. Ants (Hymenoptera: Formicidae) pass the bioindicator scorecard. Myrmecologycal News 10: 69-76.
Matteucd, S. & A. Colma. 1982. Metodología para el estudio de la vegetación. Secretaria General de la Organización de los Estados Americanos Programa Regional de Desarrollo Científico y Tecnológico, Washington DC. 168 p.
McIntyre, N. E. 2000. Ecology of urban arthropods: a review and a call to action. Ecology and Population Biology 93: 825-835. [ Links ]
McIntyre, N. E., J. Rango, W. F. Fagan & S. H. Faeth. 2001. Ground arthropod community structure in a heterogeneous urban environment. Landscape and Urban Planning 52: 257-274.
McKinney, M.L. 2002.Urbanization, biodiversity, and conservation. BioScience 52: 2002. [ Links ]
McKinney, M. L. 2006. Urbanization as a major cause of biotic homogenization. Biological Conservation 127: 247-260. [ Links ]
Mitrovich, M. J., T. Matsuda, K. H. Pease & R. Fisher. 2010. Ants as a measure of effectivenes s of habitat conservation planning in Southern California. Conservation Biology 24:1239-1248.
Niemelä, J. 1999. Ecology and urban planning. Biodiversity and Conservation 8: 119-131. [ Links ]
Oliveira, M. F. & A. E. C. Campos-Farinha. 2005. Formigas urbanas do município de Maringá, PR, e su as implicações. Arquivos do Instituto Biologico 72: 33-39.
Pacheco do Nascimento, R. 2005. Conservation of invertebrates in urban areas: a study of case with ants in the Brazilian Cerrado. Tesis de maestría, Federal de Uberländ University, Uberländia. 61 p. [ Links ]
Palacios, E. & F. Fernández. 1996. Clave para las subfamilias y géneros. pp. 233-260. En: Andrade,G., G. Amat & F. Fernández (eds.). Introducción al Estudio de las Hormigas. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Santa fé de Bogotá. [ Links ]
Parr, C. L. & H. Gibb. 2010. Competition and the role of dominant ants. pp. 77-96. En: Lach, L., C. L. Parr & K. L. Abbott (eds.). Ecology of Ants. Oxford University Press, Nueva York. [ Links ]
Pearce - Duvet, J., C. Elemans & D. H. Feener. 2011. Walking the line: search behavior and foraging succes in ant species. Behavioral Ecology: 1-9.
Philpott, S., I. Perfecto, I. Armbrecht & C. L. Parr. 2010. Ant diversity and function in disturbed and changing habitats. pp. 137-158. En: Lach, L., C. L. Parr & K. L. Abbott (eds.). Ecology of Ants. Oxford University Press, Nueva York. [ Links ]
Pik, A., J. M. Dangerfield, R. Bramble, C. Angus & D. Nipperess. 2002. The use of invertebrates to detect small-scale habitat heterogeneity and its application to restoration practices. Environmental Monitoring and Assessment 75:179-199.
Pirk, G. I., F. di Pasquo & J. Lopez de Casanave. 2009. Diet of two sympatric Pheidole spp. ants in the central Monte desert: implications for seed-granivore interactions. Insectes Sociaux 56: 277-283.
Pitts, J., J. Mc Hugh & R. Kenneth. 2005. Cladistic analysis of the fire ants of the Solenopsis saevissima species-group (Hymenoptera: Formicidae). Zoologica Scripta 34: 493-505.
R Development Core Team. 2011. R: a language and environment for statistical computing. R Foundation for Statistical Computing. Vienna, Austria. URL: http://www.R-project.org [ Links ]
Ratchford, J. S., S. E. Wittman, E. S. Jules, A. M. Ellison, N. J. Gotelli & N. J. Sanders. 2005. The effects of fire, local environment and time on ant assemblages in fens and forests. Diversity and Distributions 11: 487-497.
Ribas, C. R., R. B. F. Campos, F. A. Schmidt & R. R. C. Solar. 2012. Ants as indicators in Brazil: a review with suggestions to improve the use of ants in environmental monitoring programs.Psyche 2012:23 p.
Rivera, L. & I. Armbrecht. 2005. Diversidad de tres gremios de hormigas en cafetales de sombra, de sol y bosques de Risalda. Revista Colombiana de Entomología 31: 89-96.
Sandfor, M. P., P. N. Manley & D. D. Murphy. 2008. Effects of urban development on ant communities: implications for ecosystem services and management. Conservation Biology 23:131-141.
Silvestre, R., C. R. F. Brandäo & R. R. da Silva. 2003. Grupos funcionales de hormigas: el caso de los gremios del Cerrado. pp. 113-148. En: Fernández, F. (ed.). Introducción a las Hormigas de la Región Tropical. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Bogotá. [ Links ]
Souto, X. C., J. C. Bolaño, L. Gonzélez & M. J. Reigosa. 2001. Allelopathic effects of tree species on some soil microbial populations and herbaceous plants. Biologia Plantarum 44: 269-275.
Toro, E. & O. E. Ortega. 2006. Composición y diversidad de hormigas (Hymenoptera: Formicidae) en algunas áreas protegidas del valle de Aburrá. Revista Colombiana de Entomología 32: 214-220.
Tschinkel, W. R., E. S. Adams & T. Macom. 1995. Territory area and colony size in the fire ant, Solenopsis invicta. Journal of Animal Ecology 64: 473-480.
Vargas, E. 1985. Estudio de la flora y vegetación de la Cuenca del río Jillusaya (Prov. Murillo - La Paz) como base para un futuro manejo. Tesis de licenciatura en biología, Universidad Mayor de San Andrés, La Paz. 97 p. [ Links ]
Vepsäläinen, K., H. Ikonen & M. Koivula. 2008. The structure of ant assemblages in an urban area of Helsinki, southern Finl and. Annales Zoologici Fennici 45:109-127.
Villegas, M. 2005. Relación entre variable ambientales de urbanización y las comunidades de aves nativas en la ciudad de La Paz: bases para programas de monitoreo. Tesis de licenciatura en biología, Universidad Mayor de San Andrés, La Paz. 57 p. [ Links ]
Vitousek, P. M., H. A. Mooney, J. Lubchenco & J. Melillo. 1997. Human domination of earth's ecosystems. Science 277:294-299.
Yamaguchi, T. 2004. Influence of urbanization on ant distribution in parks of Tokio and Chiba City, Japan. I. Analysis of ant species richness. Ecological Research 19: 209-216. [ Links ]
Yamaguchi, T. 2005. Influence of urbanization on ant distribution in parks of Tokyo and Chiba city, Japan II. Analysis of species. Entomological Science 8:17-25.
Zeballos, M. 2000. Estudio de los cambios en la composición florística, cobertura vegetal y fenología a lo largo de un ciclo anual en el parea permanente de Cota Cota -La Paz. Tesis de licenciatura en biología, Universidad Mayor de San Andrés, La Paz. 133 p. [ Links ]
Artículo recibido en: Abril de 2012.
Manejado por: Diana Silva
Aceptado en: Julio de 2012.
Anexo 1: Coordenadas geográficas de puntos de muestreo en latitud y longitud ±10 m y número de hormigas encontradas en treinta trampas de caída.
Anexo 2: Composición vegetal por forma de vida expresada en proporción absoluta para cada punto de muestreo.












 uBio
uBio